Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Revista de Ciências Agrárias
versão impressa ISSN 0871-018X
Rev. de Ciências Agrárias vol.42 no.4 Lisboa dez. 2019
https://doi.org/10.19084/rca.18099
ARTIGO
Características biométricas e fisiológicas de sementes de Echium plantagineumL. em diferentes épocas de colheita
Biometric characteristics and physiological seeds of Echium plantagineum L. in different times of harvesting
Rodrigo Roso1,*, Ubirajara Russi Nunes1, Caren Alessandra Müller1, Juçara Terezinha Paranhos2, Joner Silveira Dalcin1, Tiéle Stuker Fernandes1 e César Tiago Forte1
1 Departamento de Fitotecnia, Universidade Federal de Santa Maria, Santa Maria, Brasil
2 Departamento de Biologia, Universidade Federal de Santa Maria, Santa Maria, Brasil
(*E-mail: rodrigoroso@yahoo.com.br)
RESUMO
O objetivo deste trabalho consistiu em avaliar as características biométricas e fisiológicas de diásporos (carcerulídeo: fruto concrescido com a semente) de Echium plantagineum colhidas em diferentes épocas, e a influência do armazenamento dos diásporos na germinação e viabilidade das sementes. Utilizou-se um fatorial 5 x 2 para avaliar as épocas de colheita dos frutos (03/out, 18/out, 01/nov, 15/nov e 01/dez) e tratamento de quebra da dormência (presença ou ausência). Os diásporos foram submetidos a avaliação da qualidade fisiológica, através de testes de germinação, índice de velocidade de germinação e viabilidade das sementes após cada colheita e depois do armazenamento durante seis meses, bem como a caracterização biométrica dos mesmos. Os frutos produzidos no início do período reprodutivo apresentam maiores dimensões e maior massa, ocorrendo dormência das sementes antes da dispersão do fruto. Ocorre variação na germinação das sementes de E. plantagineumno decorrer das épocas de colheita dos frutos, podendo estar relacionada com fatores genéticos e ambientais. A dormência das sementes é quebrada com o armazenamento durante seis meses e a imersão em nitrato de potássio (0,2%) durante 12-h e ácido giberélico (500 mg L-1) durante 48-h.
Palavras-chave: ácido giberélico, diásporo, flor-roxa, nitrato de potássio, viabilidade.
ABSTRACT
The objective of this work was to evaluate the biometric and physiological characteristics of diaspores (carcerulide: seeded seed fruit) of Echium plantagineum harvested at different times, and the influence of diaspores storage on seed germination and viability. A 5 x 2 factorial was used to evaluate fruit harvesting times (03/Oct, 18/Oct, 01/Nov, 15/Nov and 01/Dec) and dormancy break treatment (presence or absence). The diaspores were submitted to physiological quality evaluation through tests of germination, germination speed index and seed viability after each harvested and after storage for six months, as well as their biometric characterization. The fruits produced at the beginning of the reproductive period present have larger dimensions and larger mass, occurring seeds dormancy before fruit dispersal. There is variation in the germination of E. plantagineum seeds during the fruit harvesting periods, which may be related to genetic and environmental factors. Seed dormancy is broken with storage for six months and immersion in potassium nitrate (0.2%) for 12-h and gibberellic acid (500 mg L-1) for 48-h.
Keywords: gibberellic acid, diaspores, purple-flower, potassium nitrate, viability.
INTRODUÇÃO
O sucesso da introdução de espécies caracterizadas como plantas daninhas em novos ambientes envolve a capacidade de dispersão das sementes a longas distâncias, seguida pela rápida multiplicação e expansão no território (Mahmood et al., 2016), mantendo crescimento populacional positivo, adaptando-se às condições de heterogeneidade ambiental (Araldi et al., 2013). Dentre os fatores que influenciam a sobrevivência e adaptação às condições adversas destaca-se a eficiência reprodutiva, na qual a maioria das plantas daninhas presentes nos ambientes agrícolas possui reprodução sexuada, pela formação e disseminação de sementes (Araldi et al., 2013).
Naquele contexto se insere a espécie Echium plantagineumL. (syn. Echium lycopsisL.) que pertence à família Boraginaceae, popularmente conhecida como flor‑roxa, soagem, chupa-mel, língua-de-vaca ou soagem-viperina. É uma espécie herbácea, anual ou vivaz (hemicriptófito), nativa da região do Mediterrâneo, considerada uma planta daninha importante na Austrália, África do Sul, Canadá e na América do Sul (Weston et al., 2012), Portugal (Vasconcelos et al., 2004), estando presente na Região Sul do Brasil, causando prejuízos em culturas agrícolas e pastagens, nestas devido à sua toxicidade para os animais resultante da presença de alcalóides pirrolizidinas (equimina, equimidina) (Vasconcelos et al., 2004). Devido ao rápido crescimento, adaptação às variações de temperatura e fotoperíodo, alta capacidade de competição, sistema radicular agressivo e profundo com rápido crescimento, elevada produção de área foliar e sementes, dormência e vários fluxos de emergência durante o ano, é considerada uma planta daninha problemática (Piggin, 1976; Forcella et al., 1986; Konarzewski et al., 2012).
Echium plantagineumpossui inflorescências escorpioides, apresentando flores com ovário súpero, bicarpelar, gamocarpelar e tetralocular (formação de uma parede secundária no ovário), com um óvulo por lóculo e gineceu ginobásico, que na maturação do fruto, se separam ficando unidos pela base do estilete (Souza e Lorenzi, 2012). Este tipo de gineceu forma frutos denominados carcerulídeos (fruto seco indeiscente e unisseminado), cuja semente permanece unida ao fruto (mericarpo), sendo a unidade de disseminação e propagação (Moreira e Bragança, 2010). Na inflorescência, a maturação dos frutos assim como a dispersão, ocorre de forma irregular, da base para o ápice, possuindo a presença de frutos maduros e flores na mesma inflorescência.
A produção de semente em E. plantagineumpode-se estender por um período considerável, por apresentar floração indeterminada, ocorrendo exposição a variações ambientais durante o estádio reprodutivo, como disponibilidade hídrica, temperatura, fotoperíodo e nutrientes (Piggin, 1976). Nessa espécie, e na maioria das plantas daninhas, as primeiras flores emitidas produzem sementes o mais rápido possível sendo dispersas mais cedo (Konarzewski et al., 2012; Taghizadeh et al., 2012). O tempo de desenvolvimento das sementes e as condições ambientais durante a maturação na planta-mãe podem influenciar nos atributos físicos e fisiológicos da semente, como tamanho, grau de dormência e quantidade de reservas, afetando a velocidade de germinação e o sucesso da próxima geração (El-Keblawy e Al-Rawai, 2006). Dessa forma, uma mesma planta pode produzir sementes com diferentes tamanhos, massa e grau de dormência no mesmo ciclo produtivo ou inflorescência.
O tamanho das sementes está relacionado com a profundidade à qual são capazes de germinar e emergir (Araldi et al., 2013). De forma geral, sementes maiores possuem capacidade de emergir em maiores profundidades, ao contrário de sementes pequenas que apresentam menor quantidade de reservas, e a emergência restringe-se aos primeiros milímetros de solo. Nalgumas Brassicaceae ocorre algo semelhante, por exemplo em Raphanus raphanistrumL. (Taghizadeh et al., 2012).
Nas plantas daninhas, a dormência das sementes pode apresentar diferentes períodos, tendo como causa diferentes mecanismos, que variam de acordo com a espécie e depende de estímulos ambientais durante o processo de maturação das sementes, assim como aqueles predominantes após a libertação da planta mãe (Vivian et al., 2008; Ali et al., 2012). Existem dois tipos de dormência, a primária que é característica de uma semente madura, que possui tegumento permeável à água, sendo induzida pelo ácido abscísico (ABA) durante a fase de maturação enquanto ainda está presente na planta mãe, e que permanece após a dispersão (Finch-Savage e Leubner-Metzger, 2006). E a secundária que é imposta pelo tegumento impermeável, ou quando as condições ambientais não são favoráveis para a germinação (Salvador et al., 2007). Na dormência primária a planta libera as sementes já dormentes ao solo. Nesse caso, envolve o balanço entre substâncias inibidoras e promotoras de germinação, como as hormonas ABA e ácido giberélico (GA) (Bewley e Black, 1994). Para a quebra da dormência vários métodos podem ser utilizados, entre os quais se destaca o tratamento das sementes com compostos azotados (KNO3), hormonas (ácido giberélico), presença ou ausência de luz e temperatura (Salvador et al., 2007), e a duração e condições de armazenamento das sementes, que podem atuar eliminando substâncias inibidoras da germinação presente nas sementes (Pereira et al.,2011).
O conhecimento de formas de sobrevivência e adaptação das plantas daninhas a novos ambientes é importante para o estabelecimento de estratégias de gestão eficientes. Características como massa, dimensões das sementes e variações do grau de dormência, estão relacionadas com o sucesso reprodutivo, viabilidade e persistência da espécie num sistema agrícola (Konarzewski et al., 2012). Face ao exposto, o presente trabalho teve como objetivo avaliar as características biométricas e fisiológicas de frutos de E. plantagineumcolhidos em diferentes épocas, e a influência do período de armazenamento na germinação e viabilidade das sementes.
MATERIAL E MÉTODOS
Os frutos de E. plantagineum foram colhidos manualmente, nos meses de outubro a dezembro de 2015, numa parcela agrícola localizada no município de Restinga Seca, RS (29° 51' 29" S e 53° 31' 41" O e altitude 72 m), com histórico de infestação por essa planta daninha (± 20 plantas m-2). A área da colheita caracteriza-se pelo cultivo de soja (Glycine max (L.) Merrill) no verão e azevém (Lolium multiflorumL.) no inverno.
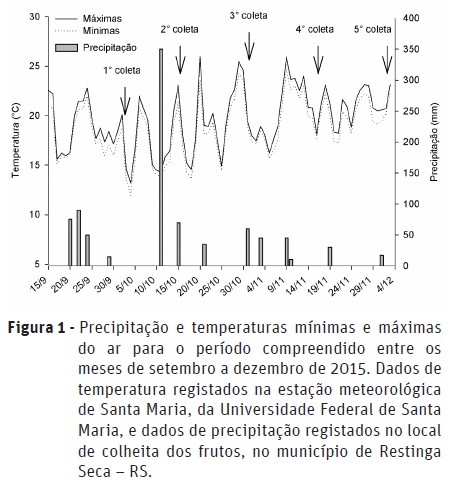
Os dados de temperaturas mínimas e máximas do ar foram registados na estação meteorológica automática, e os dados de precipitação foram medidos no local do ensaio (Figura 1).
Foram realizadas cinco colheitas de frutos, que se iniciaram 15 dias após o início da antese (DAIA), ou seja, quando mais de 50% das plantas se apresentavam nesse estádio. As colheitas foram realizadas em 03/outubro, 18/outubro, 01/novembro, 15/novembro e 01/dezembro de 2015. Em cada data, colheram-se em plantas previamente marcadas, apenas os frutos que apresentavam coloração escura e se desprendiam facilmente da planta mãe, possuindo aparentemente maturidade fisiológica. Os mesmos passaram por um processo de limpeza manual, secos à sombra durante cinco dias e armazenados em sacos de papel Kraft em condição de laboratório (± 25 °C), até a realização dos ensaios.
Após cada colheita, os frutos passaram pela caracterização biométrica, sendo avaliado o comprimento, a largura e a espessura, com auxílio de um paquímetro digital, em quatro repetições de 20 diásporos por época de colheita. Determinou-se também o grau de umidade e a massa de mil sementes conforme as Regras para Análise de Sementes (Brasil, 2009).
Para avaliar a qualidade fisiológica inicial, um lote de frutos foi de imediato submetido a testes de germinação das sementes após cada colheita, e outro lote foi armazenado durante seis meses, para estudos da quebra da dormência das sementes. Os ensaios foram organizados de forma fatorial 5 x 2, no qual o primeiro fator corresponde às épocas de colheita dos frutos, e o segundo à realização ou não da quebra da dormência das sementes. Para isto, os diásporos (carcerulídeo: fruto concrescido com a semente) foram imersos numa solução de nitrato de potássio (0,2%) por 12-h, lavados em água corrente por 10 min, e submetidos a imersão em solução de ácido giberélico (500 mg L-1) por mais 48-h, sendo lavados novamente (Roso et al., 2017).
Utilizou-se, para todos os ensaios de laboratório, o delineamento experimental inteiramente casualizado (DIC), com quatro repetições de 50 diásporos. Os ensaios foram realizados em câmara de germinação do tipo Biochemical Oxigen Demand (B.O.D.) com fotoperíodo de 24-h e temperatura de 20 °C (Roso et al., 2017). Os testes foram conduzidos em caixa de acrílico transparente do tipo gerbox (11,0 x 11,0 x 3,5 cm), sob três folhas de papel germiteste umedecidas com água destilada em quantidade equivalente a 2,5 x a massa do papel seco (Brasil, 2009). A umidade do substrato foi monitorada diariamente, visando mantê-la adequada para a germinação.
As variáveis analisadas foram germinação aos sete e 14 DAS (dias após a sementeira) e índice de velocidade de germinação (IVG) durante 14 dias, considerando germinada quando ocorresse a protusão da raiz primária (≥ 2 mm) conforme Bewley e Black (1994). A porcentagem de germinação foi calculada pala equação G (%) = (N/A) x 100, onde, N = número de sementes germinadas e A = número total de sementes postas para germinar. Já o IVG foi calculado pela equação IVG = ((G1/N1) + (G2/N2) + (Gn/Nn)), onde, G = número de sementes germinadas em cada contagem e N= número de dias da sementeira a cada contagem (Maguire, 1962). Também foi avaliado o comprimento da raiz primária, parte aérea, total e massa seca das plântulas aos 14 (DAS) de acordo com Nakagawa (1999).
No final dos ensaios foi avaliada a viabilidade das sementes que não germinaram através do teste de tetrazólio. Para isso, os diásporos foram seccionados de forma longitudinal ao embrião e colocados em solução aquosa de 2,3,5 trifenil cloreto de tetrazólio (0,1%) a 35 °C, por quatro horas, no escuro (Brasil, 2009). Após o tratamento, foram lavados em água, e as sementes identificadas como dormentes ou mortas pela interpretação da coloração rósea homogénea do endosperma.
Os dados foram submetidos à análise de variância pelo teste F (p<0,05) através do programa SISVAR (Ferreira, 2011). Os fatores foram comparados pelo teste de Scott-Knott a 5% de probabilidade. Para as variáveis em porcentagem, os dados foram transformados por arco-seno √%/100.
RESULTADOS E DISCUSSÃO
Houve diferenças significativas (p<0,05) para as características biométricas dos frutos e massa de mil sementes de E. plantagineum, os quais foram influenciados pelas épocas de colheita. Observou-se, de maneira geral, que as variáveis comprimento, largura, espessura, e massa de mil sementes apresentaram decréscimo nos valores no decorrer das épocas de colheita dos frutos. Na primeira colheita, realizada em 03 de outubro, os parâmetros comprimento, largura e massa de mil diásporos, apresentaram valores significativamente superiores aos das outras épocas de colheita. Já a espessura de frutos foi significativamente superior na segunda época de colheita, 18 de outubro, com 1,53 mm. Na última colheita (01 de dezembro) observaram-se os menores parâmetros de comprimento, largura e espessura, e massa de mil diásporos (Quadro 1). Isso pode ter ocorrido pelo fato desta espécie possuir floração indeterminada, de rácemos escorpioides, ocorrendo sequencialmente a formação, maturação e dispersão dos frutos da base em direção ao ápice do rácemo, durando esse processo aproximadamente 15 dias para cada fruto. De acordo com Taghizadeh et al. (2012), neste tipo de desenvolvimento e crescimento vegetal pode ocorrer maior direcionamento dos fotoassimilados produzidos para os primeiros frutos formados, havendo competição pelos recursos dentro do rácemo, apresentando o crescimento dos frutos restringido em direção ao ápice. A variação nas dimensões dos frutos e/ou sementes em cada espécie representa uma estratégia de adaptação às necessidades exigidas para a dispersão e emergência das plântulas, justificando o polimorfismo da dimensão das sementes, privilegiando na estratégia de maior sucesso as dimensões em vez da quantidade das mesmas (Araldi et al., 2013). Resultados obtidos por Konarzewski et al. (2012) avaliando populações de E. plantagineum em diferentes regiões da Austrália, indicam que em ambientes frios e úmidos ocorre a produção de frutos menores, quando comparado a ambientes quentes e secos, ocorrendo atuação do ambiente árido sobre a pressão de seleção de populações com sementes maiores como forma de adaptação. Neste trabalho verificou-se aumento de aproximadamente 5 °C na temperatura média entre a primeira (03 de outubro) e a última colheita (01 de dezembro), e decréscimo na precipitação (Figura 1), podendo estes fatores climáticos ter influenciado na variação das dimensões e massa dos frutos ao longo das épocas de colheita.
Os resultados de germinação aos sete a 14 DAS, índice de velocidade de germinação, comprimento de parte aérea, raiz, comprimento total de plântulas, massa seca e sementes dormentes realizados após as colheitas dos frutos estão apresentados nos Quadros 2 e 3. De maneira geral houve diferenças significativas (p < 0,05) para todas as variáveis em função das épocas de colheita dos frutos, com exceção no comprimento da parte aérea e sementes dormentes, as quais não apresentaram diferenças significativas. Em todas as colheitas, as sementes que não foram submetidas a quebra da dormência não apresentaram germinação. Nos tratamentos em que foi efetuada quebra de dormência, observou-se que a colheita realizada no dia 18 de outubro se destacou na germinação aos sete DAS, com 15%. Para as variáveis IVG e germinação aos 14 DAS as colheitas de 03 e 18 de outubro e 15 de novembro apresentaram as maiores características, com IVG de 1,7, 1,9 e 1,6 e germinação de 25, 24 e 25%, respectivamente (Quadro 2). O comprimento de raiz (RA) e comprimento total de plântulas (CT) nas colheitas de 03 e 18 de outubro mostraram os maiores valores, com 2,3 e 1,9 cm para RA e 5,0 e 5,3 cm para CT, respectivamente. Já para massa seca, a colheita de 01 de dezembro mostrou-se inferior, diferindo significativamente das outras colheitas.
Ao avaliar a viabilidade das sementes pelo teste de tetrazólio, não se observaram diferenças significativas entre as colheitas. No entanto, quando as sementes não foram submetidas a quebra da dormência obtiveram-se maiores porcentuais de sementes dormentes viáveis, quando comparado as com as sementes submetidas a quebra de dormência.
Esses resultados evidenciam que as sementes de E. plantagineumapresentam dormência, com diferentes intensidades, dependendo da época em que são formadas, com germinação variando entre 13 e 25%. Mesmo após a quebra da dormência ocorreu baixa germinação e alta porcentagem de sementes dormentes viáveis, em todas as épocas de colheita. A variação da germinação entre as épocas de colheita dos frutos está relacionada com a intensidade da dormência, na qual pode ter sido induzida por fatores ambientais, como umidade e temperatura, durante o desenvolvimento das sementes (Wu e Owen, 2015).
Resultados semelhantes foram relatados por El-Keblawy e Al-Rawai (2006) ao trabalhar com Prosopis juliflora(Sw.) DC. (Fabaceaea), os quais encontraram variação da germinação em função de diferentes datas de colheita, atribuindo aos fatores ambientais durante a formação das sementes e aos recursos disponibilizados pela planta mãe, no qual sementes formadas no início do período reprodutivo tem maior disponibilidade de recursos, podendo apresentar menor intensidade de dormência. O mesmo tipo de comportamento foi observado em espécies como Lamium amplexicaule L. (Lamiaceae), Stellaria media(L.) Vill. (Caryophyllaceae), Capsella bursa-pastoris (L.) Medik. (Brassicaceae), Thlaspi arvense L. (Brassicaceae) (Hill et al., 2014) e Amaranthus tuberculatus(Moq.) Sauer. (Amaranthaceae) (Wu e Owen, 2015) também apresentaram diferentes intensidades de dormência em função do período e das condições ambientais durante a formação e maturação das sementes. A diferença na intensidade da dormência em função do período em que são produzidas caracteriza uma estratégia evolutiva das plantas daninhas, distribuindo a germinação ao longo do tempo, visando maximizar a probabilidade de sobrevivência das plântulas (Menezes et al.,2013).
Após o armazenamento durante seis meses as sementes foram submetidas novamente a avaliação da qualidade fisiológica, no qual a análise da variância, através do teste F, revelou que houve efeito significativo dos fatores épocas de colheita e quebra da dormência, e da interação entre eles para todas as variáveis (p< 0,05). Verificou-se que os diásporas colhidos a 18 de outubro e 01 de dezembro apresentaram valores significativamente superior aos das outras datas para as variáveis germinação aos sete e 14 DAS e IVG, independente de tratamento para quebra da dormência (Quadro 4).
No entanto, observou-se que as sementes submetidas à quebra da dormência apresentaram os maiores valores das variáveis estudadas em todas as épocas de colheita, quando comparado às sementes sem tratamento para quebra da dormência. Nas colheitas de 18 de outubro e 1 de dezembro, as sementes apresentaram 88 e 94% de germinação aos 14 DAS quando submetidas ao tratamento de quebra da dormência e 45 e 41% sem tratamento, respectivamente. Nessas mesmas épocas de colheita observaram-se maiores valores de germinação aos sete DAS, com 86 e 94% para sementes que passaram por tratamento de quebra e 42 e 40% sem tratamento, respectivamente. Para IVG verificaram-se valores de 16,3 e 16,8 com tratamento de quebra da dormência e 10,1 e 10,4 sem tratamento, respectivamente. Os resultados de sementes dormentes viáveis indicam que nas colheitas de 15 de outubro e 1 de dezembro houve menor porcentagem destas após a quebra da dormência, com 8 e 3%, respectivamente. No entanto, quando não foi realizado o tratamento de quebra da dormência os valorem ficaram próximos a 40% (Quadro 4).
Esses resultados evidenciam que o armazenamento juntamente com a imersão das sementes em nitrato de potássio e ácido giberélico foram eficientes na quebra da dormência, ocorrendo variação entre as épocas de colheita que pode estar relacionada à intensidade da dormência.
Os resultados do Quadro 5 para comprimento da parte aérea, raiz, comprimento total e massa seca de plântulas após seis meses de armazenamento dos frutos apresentaram maior variabilidade entre as épocas de colheita e a quebra da dormência. Isso pode ter ocorrido por se tratar de uma planta daninha que apresenta diferentes intensidades de dormência em função do período em que são formadas.
Os resultados desse trabalho corroboram com os encontrados por Piggin (1976), que ao trabalhar com sementes de E. plantagineum, verificou que sementes recém colhidas apresentavam dormência, sendo esta quebrada após permanecer um período armazenada em condição de laboratório ou enterradas no solo. Várias outras espécies de plantas daninhas possuem quebra de dormência com o armazenamento, como por exemplo A. tuberculatus no qual foram atribuídas as causas da dormência a fatores genéticos e ambientais durante a formação das sementes (Wu e Owen, 2015). De acordo com alguns autores, (El-Keblawy e Al-Rawai, 2006; Vivian et al., 2008), durante o armazenamento ocorrem alterações físicas e químicas nas sementes, que alteram a permeabilidade do tegumento, o equilíbrio entre substâncias promotoras e inibidoras da germinação e proporciona maturação fisiológica do embrião.
Em síntese, ficou evidente que as plantas de E. plantagineumproduzem frutos com diferentes tamanhos, massa e intensidade de dormência das sementes ao longo do período de produção e maturação, como estratégia de adaptação e sobrevivência ao ambiente, possibilitando a formação de um banco de semente no solo e a distribuição da germinação ao longo do ano.
CONCLUSÕES
Echium plantagineum produziu frutos com maior tamanho e massa no início do período reprodutivo, ocorrendo dormência das sementes quando os frutos ainda estão ligados à planta mãe.
As sementes de E. plantagineum apresentaram variações de germinação em função das épocas de colheita dos frutos, podendo estar relacionada a fatores genéticos e ambientais.
O armazenamento dos frutos durante seis meses e a imersão em nitrato de potássio e ácido giberélico foram eficientes na quebra da dormência e promoção da germinação das sementes de E. plantagineum.
Referências Bibliográficas
Ali, H. H.; Tanveer, A. & Nadeem M.A. (2012) - Evolution of some seed dormancy breaking methods on germination of Rhynchosia capitata (Roth DC). Weed Science Research, vol. 18, n. 1, p. 423-432. [ Links ]
Araldi, R.; Velini, E.D.; Gomes, G.L.G.C.; Carbonari, C.A.; Alves, E. & Trindade, M.L.B. (2013) - Variação do tamanho de sementes de plantas daninhas e sua influência nos padrões de emergência das plântulas. Planta Daninha, vol. 31, n. 1, p. 117-126. http://dx.doi.org/10.1590/S0100-83582013000100013 [ Links ]
Bewley, J.D. & Black, M. (1994) - Seeds: physiology of development and germination.2ª ed. New York: Plenum Press, 445p. [ Links ]
Brasil (2009) - Regras para análise de sementes.Ministério da Agricultura, Pecuária e Abastecimento. Secretaria de Defesa Agropecuária. Brasília: MAPA/ACS, 395p.
El-Keblawy, A. & Al-Rawai, A. (2006) - Effects of seed maturation time and dry storage on light and temperature requirements during germination in invasive Prosopis juliflora. Flora, vol. 201, n. 2, p. 135-143. http://dx.doi.org/10.1016/j.flora.2005.04.009 [ Links ]
Ferreira, D.F. (2011) - Sisvar: a computer statistical analysis system. Ciência e Agrotecnologia, vol. 35, n. 6, p. 1039-1042. http://dx.doi.org/10.1590/S1413-70542011000600001 [ Links ]
Finch-Savage, W.E. & Leubner-Metzger, G.L. (2006) - Seed dormancy and the control of germination. New Phytologist, vol. 171, n. 3, p. 501-523. https://doi.org/10.1111/j.1469-8137.2006.01787.x [ Links ]
Forcella, F.; Wood, J.T. & Dillon, S.P. (1986) - Characteristics distinguishing invasive weeds within Echium (Bugloss). Weed Research, vol. 26, n. 5, p. 351-364. https://doi.org/10.1111/j.1365-3180.1986.tb00718.x [ Links ]
Hill, E.C.; Renner, K.A. & Sprague C.L. (2014) - Henbit (Lamium amplexicaule), common chickweed (Stellaria media), shepherds-purse (Capsella bursa-pastoris), and field pennycress (Thlaspi arvense): fecundity, seed dispersal, dormancy, and emergence. Weed Science, vol. 62, n. 1, p. 97-106. https://doi.org/10.1614/WS-D-13-00074.1 [ Links ]
Konarzewski, T.K.; Murray, B.R. & Godfree R.C. (2012) - Rapid development of adaptive, climate-driven clinal variation in seed mass in the invasive annual forb Echium plantagineum L. PloS One, vol. 7, n. 12, art. e49000. https://doi.org/10.1371/journal.pone.0049000 [ Links ]
Maguire, J.D. (1962) - Speed of germination-aid in selection and evaluation for seedling emergence and vigor. Crop Science,vol. 2, n. 2, p. 176-177. http://dx.doi.org/10.2135/cropsci1962.0011183X000200020033x [ Links ]
Mahmood A.H.; Florentine, S. K.; Chauhan, B. S.; Mclaren, D. A.; Palmer, G. C. & Wright, W. (2016) - Influence of various environmental factors on seed germination and seedling emergence of a noxious environmental weed: green galenia (Galenia pubescens). Weed Science, vol. 64, n. 3, p. 486-494. https://doi.org/10.1614/WS-D-15-00184.1 [ Links ]
Menezes, B.R. da S.; Lopes, H.M.; Pereira, M.B. Moreira, L.B.; Rodrigues, D.L. & Silva, E.R. da. (2013) - Avaliação da germinação e dormência de sementes de arroz vermelho e branco. Revista de Ciências Agroveterinárias, vol. 12, n. 2, p. 129-140. [ Links ]
Moreira, H.J. da C. & Bragança, H.A.B.N. (2010) - Manual de identificação de plantas infestantes – Cultivos de verão. Campinas: FMC, 650 p. [ Links ]
Nakagawa, J. (1999) - Testes de vigor baseados na avaliação das plântulas. In: Krzyzanowski, F.C.; Vieira, R.D. & França-Neto, J.B. (Eds.) - Vigor de sementes: conceitos e testes.Londrina: ABRATES, cap. 2, 85 p. [ Links ]
Pereira, W.V.S.; Vieira, L.M.; Ribeiro, L.M.; Mercante-Simões, M.O. & Oliveira, T.G.S. (2011) - Armazenamento de sementes de maracujazeiros. Pesquisa Agropecuária Tropical, vol. 41, n. 2, p. 273-278. http://dx.doi.org/10.5216/pat.v41i2.8815 [ Links ]
Piggin, C.M. (1976) - Factors affecting seed germination of Echium plantagineumL. and Trifolium subterraneumL. Weed Research, vol. 6, n. 5, p. 337-344. https://doi.org/10.1111/j.1365-3180.1976.tb00423.x [ Links ]
Roso, R.; Nunes, U.R.; Paranhos, J.T.; Müller, C.A.; Fernandes, T.S. & Ludwig, E.J. (2017) - Germination of Echium plantagineum L. seeds submitted to dormancy overcoming and variations in temperature, light and depth of sowing. Journal of Seed Science, vol. 39, n. 3, p. 262-271. http://dx.doi.org/10.1590/2317-1545v39n3174115 [ Links ]
Salvador, F.L.; Victoria Filho, R.; Alves, A.S.R.; Simoni, F. & San Martin, H.A.M. (2007) - Efeito da luz e da quebra de dormência na germinação de sementes de espécies de plantas daninhas. Planta Daninha,vol. 25, n. 2, p. 303-308. http://dx.doi.org/10.1590/S0100-83582007000200009 [ Links ]
Souza, V.C. & Lorenzi, H. (2012) - Botânica sistemática: guia ilustrado para identificação das famílias de fanerógamas nativas e exóticas do Brasil, baseado em APG II. Nova Odessa: Instituto Plantarum, 2ª ed., 704 p. [ Links ]
Taghizadeh, M.S.; Nicolas, M.E. & Cousens, R.D. (2012) - Effects of relative emergence time and water deficit on the timing of fruit dispersal in Raphanus raphanistrumL. Crop and Pasture Science, vol. 63, n. 10, p. 1018-1025. https://doi.org/10.1071/CP12246 [ Links ]
Vasconcelos, T.; Monteiro, A.; Torres, M.O.; Sá, G. & Forte, P. (2014) - Infestantes de Pastagens. Plantas tóxicas e Agressivas. In: Monteiro, A. (Coord.) - Série Didáctica Herbologia 6 ISAPress, Lisboa. 104 p. ISBN: 978-972-8669-58-4 h [ Links ]
Vivian, R.; Silva, A.A.; Gimenes, Jr.M.; Fagan, E.B.; Ruiz, S.T. & Labonia, V. (2008) - Dormência em sementes de plantas daninhas como mecanismo de sobrevivência – breve revisão. Planta Daninha, vol. 26, n. 3, p. 695-706. http://dx.doi.org/10.1590/S0100-83582008000300026 [ Links ]
Weston, L.A.; Weston, P.A. & Mccully, M. (2012) - Production of bioactive napthoquinones by roots of patersons curse (Echium plantagineum) – implications for invasion success? Weed Science Research, vol. 18, n. especial, p. 677-686. [ Links ]
Wu, C. & Owen, M.D.K. (2015) - When is the best time to emerge-II: seed mass, maturation, and afterripening of common waterhemp (Amaranthus tuberculatus) natural cohorts. Weed Science, vol. 63, n. 4, p. 846-854. https://doi.org/10.1614/WS-D-15-00017.1 [ Links ]
Recebido/received: 2019.06.18
Aceite/accepted: 2019.09.18