Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Revista de Gestão Costeira Integrada
versão On-line ISSN 1646-8872
RGCI vol.14 no.3 Lisboa set. 2014
https://doi.org/10.5894/rgci493
ARTIGO / ARTICLE
Diversidade e distribuição dos Crustacea Brachyura dos manguezais dos rios Ariquindá e Mamucabas, litoral sul de Pernambuco, Brasil*
Diversity and distribution of the Crustacea Brachyura from the mangroves of Ariquindá and Mamucabas Rivers, South Coast of Pernambuco, Brazil
Marina de Sá Leitão Câmara de Araújo@, 1, 2; Deusinete de Oliveira Tenório2; Daniela da Silva Castiglioni3, 4
@Corresponding author: <mslc.araujo@gmail.com>
1Universidade de Pernambuco (UPE), Faculdade de Ciências, Educação e Tecnologia de Garanhuns (FACETEG), Departamento de Ciências Exatas e Naturais, Campus Garanhuns, Rua Capitão Pedro Rodrigues, 105, São José, Garanhuns – PE, CEP: 55.294-902. email: Araújo <mslc.araujo@gmail.com>
2Universidade Federal de Pernambuco (UFPE), Museu de Oceanografia Professor Petrônio Alves Coelho, Departamento de Oceanografia (DOCEAN), Av. Arquitetura, s/n, Cidade Universitária, Recife – PE, CEP 50.740-550. e-mail: Tenório <dotmar@globo.com>
3Universidade Federal de Santa Maria (UFSM), Centro Superior de Educação Norte do RS (CESNORS), Departamento de Zootecnia e Ciências Biológicas, Av. Independência, 3751, Vista Alegre, Palmeira das Missões – RS, CEP 98.300-000. e-mail: Castiglioni <danielacastiglioni@yahoo.com.br>
4Universidade Federal de Santa Maria (UFSM), Centro de Ciências Naturais e Exatas, Programa de Pós-Graduação em Biodiversidade Animal, Prédio 17, sala 1140-D, Cidade Universitária, Camobi, km 9. Santa Maria, RS, Brasil.
ABSTRACT
O objetivo deste trabalho foi conhecer a diversidade e alguns aspectos ecológicos dos caranguejos (Decapoda, Brachyura) nos estuários dos Rios Ariquindá e Mamucabas (PE), através da caracterização da estrutura de suas comunidades, com base na composição e diversidade desses crustáceos. As espécies foram amostradas mensalmente entre abril/2008 e março/2009. Foram coletados 8.394 exemplares, sendo 4.501 no manguezal do Rio Ariquindá (25 espécies e 14 gêneros) e 3.893 no manguezal do Rio Mamucabas (21 espécies e 12 gêneros). A maior frequência de espécies nesses manguezais foi dos representantes da Superfamília Ocypodoidea, em especial Uca spp. Comparando os dois estuários, nota-se que cinco espécies (Acantholobulus bermudensis, Austinixa leptodactyla, Callinectes exasperatus, Hexapanopeus caribbaeus e Uca maracoani) foram amostradas apenas no Rio Ariquindá, enquanto uma delas (Armases rubripes) foi encontrada apenas no Rio Mamucabas. A diversidade foi considerada média, de acordo com os índices ecológicos, com valores dentro do esperado para manguezais. Entretanto, nota-se que a diversidade foi menor no manguezal do Rio Mamucabas, resultado que pode estar relacionado aos impactos ambientais que esse estuário vem sofrendo nos últimos anos (represamento, desmatamento, deposição de resíduos sólidos e especulação imobiliária). O presente estudo, associado às medidas de proteção propostas, é de notável importância para a gestão dos crustáceos como recursos pesqueiros costeiros, especialmente se considerarmos que os crustáceos participam da teia trófica de diversos animais, entre eles o homem. A manutenção da diversidade de caranguejos em manguezais é considerada importante para a saúde dos ecossistemas costeiros.
Palavras-chave: Caranguejos, Ecologia, Estuário, Inventário Faunístico, Mangue.
RESUMO
It is important to study the diversity of a given area to comprehend the processes that rule the community and/or ecosystem. Several researches in tropical mangroves revealed that among the most abundant representatives, stand out the Crustacea Brachyura. The Brachyuran fauna of the littoral of Pernambuco (PE), Brazil, is well known, but the studies are mainly species lists. Thus, more detailed studies on the ecology of these communities are required, applying ecological indexes and multivariate analysis. The aim of this study was to know the biodiversity and some ecological aspects of crabs (Decapoda, Brachyura) found in the mangroves of Ariquindá and Mamucabas Rivers (PE), through the characterization of the structure of the community based on the composition and diversity of these crustaceans. For that, two hypothesis were proposed: H1 – The diversity of Brachyura is median for both mangroves, but it is higher at the Ariquindá River, due to its better state of conservation; and H2 – There are no dominant or very frequent species, indicating an environmental equilibrium in the communities. The species were monthly sampled from April 2008 to March 2009. A total of 8,394 individuals were sampled, being 4,501 in the mangrove of the Ariquindá River (25 species and 14 genera) and 3,893 in the mangrove of the Mamucabas River (21 species and 12 genera). The highest frequency of species in both mangroves is found in the Superfamily Ocypodoidea, especially Uca spp. Comparing both estuaries, it can be noticed that five species (Acantholobulus bermudensis, Austinixa leptodactyla, Callinectes exasperatus, Hexapanopeus caribbaeus and Uca maracoani) were sampled only at the Ariquindá River, while one of them (Armases rubripes) was found only at the Mamucabas River. The diversity was considered medium according to the ecologic index for both mangroves, and it is the expected for mangroves of Northeastern Brazil. However, it could be noticed that the diversity was lower at Mamucabas River, a result that might be related to the environmental impacts that this estuary has receiving in the last years (damming, deforestation, deposition of waste and housing occupation), which corroborates H1. The diversity was not high due to the dominance of one species, Uca thayeri, with 1,411 individuals at Ariquindá River and 1,300 at Mamucabas River, refuting H2. Besides, nine species were registered for the first time to the region of Tamandaré: Acantholobulus bermudensis, Armases rubripes, Austinixa leptodactyla, Hexapanopeus angustifrons, H. caribbaeus, Panopeus occidentalis, Sesarma curacaoense, Uca cumulanta and Uca victoriana. In the present study, it was possible to observe how the number of species of Brachyura behaves in the Brazilian coast. The highest number of species of crabs is observed in previous studies performed at mangroves of Pernambuco, with a tendency to decrease towards the South. The number of species recorded in the present study is expected for the Northeast region. In the Southern limit of the distribution of mangroves in South America (State of Santa Catarina), due to the colder climate, the development of mangroves is smaller, so as the diversity of crustaceans. With this, it is confirmed the greatest Brachyuran diversity in tropical areas, more stable ecosystems, such as the mangroves of Pernambuco. This study, coupled with the proposed protection measures, is of notable importance for the management of crustaceans as coastal fishery resources, especially considering that the crustaceans participate in the trophic web of various animals, including man. Maintaining the diversity of crabs in mangroves is considered important to the health of coastal ecosystems.
Keywords: Crabs, Ecology, Estuary, Faunal inventory, Mangrove.
1. Introdução
Segundo Bertini et al. (2004), reunir informações sobre a composição de espécies de uma determinada região é a base para compreender os processos que afetam o equilíbrio de suas comunidades ou de seus ecossistemas. Além disso, a identificação a prioridas espécies é de fundamental importância para interpretar eventos a posteriori, sejam eles naturais ou antrópicos,que possam afetar a assembléia formada por tais espécies. Muitos estudos têm feito levantamentos da megafauna dos manguezais, ecossistemas de transição entre o ambiente marinho e terrestre (Schaeffer-Novelli, 1995), destacando-se os moluscos, os crustáceos e os peixes.
Os crustáceos são importantes componentes nos manguezais e em outros ambientes. Nesse contexto, destacam-se trabalhos realizados sobre a diversidade de Decapoda no litoral brasileiro (p. ex, Coelho, 1965/66; Coelho & Ramos, 1972; Boschi, 2000; Bertini et al.,2004), que, dentre algumas generalizações, permitem afirmar a maior diversidade desse grupo em zonas tropicais e subtropicais do grupo nas zonas temperadas e polares.
De entre os Crustacea Decapoda, a Infraordem Brachyura, que engloba os caranguejos verdadeiros, é um grupo altamente representativo (Melo, 1996), sendo encontrado em quase todos os ecossistemas marinhos e terrestres. Segundo Ng et al. (2008), os caranguejos são encontrados desde fossas submarinas com mais de 6.000 m de profundidade, até montanhas com mais de 2.000 m de altura. Quanto à abundância, ganham destaque em habitats estuarinos, incluindo os manguezais, onde a salinidade e a temperatura variam dramaticamente ao longo dos ciclos de maré. A estimativa que tem sido mais aceita estipula 6.793 espécies e subespécies válidas de Brachyura (Ng et al., 2008).
Os caranguejos constituem um grupo bastante estudado, mas não se pode afirmar que o conhecimento sobre eles esteja completo ou que tenha alcançado um patamar o qual não se possa ultrapassar. Ng et al. (2008) destacaram a importância em se realizar mais estudos sobre a diversidade de Brachyura, e afirmaram que, mesmo em regiões costeiras tropicais, existem muitos ambientes pouco estudados, como rios e manguezais. Apesar de a fauna de crustáceos Brachyura nos manguezais ser bem diversificada e conhecida no litoral pernambucano, esses estudos se constituem basicamente em listagens de espécies (Coelho, 1965/66; Coelho & Coelho-Santos, 1990; Coelho & Ramos-Porto, 1995; Coelho-Filho & Coelho, 1997; Coelho-Santos & Coelho, 2001; Almeida et al., 2006). Dessa forma, ainda faltam estudos mais detalhados sobre a ecologia dessas comunidades, aplicando-se índices ecológicos e análises multivariadas.
Nesse contexto, esse trabalho tem por objetivo conhecer e comparar a diversidade e alguns aspectos ecológicos dos caranguejos (Crustacea, Decapoda, Brachyura) dos manguezais dos Rios Ariquindá e Mamucabas, litoral sul do estado de Pernambuco, através da composição específica e dos índices ecológicos. Tais dados serão importantes para fornecer subsídio técnico-científico para futuros planos de gestão e manejo de crustáceos na zona costeira pernambucana. No presente estudo, foram formuladas as seguintes hipóteses (H):
H1 – A diversidade de Brachyura em ambos os manguezais é média, porém maior no manguezal do Rio Ariquindá devido ao seu melhor estado de conservação; e
H2 – Não existem espécies dominantes ou muito frequentes, demonstrando haver um equilíbrio na comunidade.
2. Descrição da área de estudo
Para a realização do presente estudo, foram escolhidas duas áreas de manguezal com diferentes graus de impactos antrópicos no litoral Sul de Pernambuco: os manguezais dos Rios Ariquindá, considerado no presente trabalho não impactado; e Mamucabas, considerado no presente trabalho pouco impactado, ambos localizados no Município de Tamandaré (Figura 1). Apesar de os dois rios serem considerados não poluídos (IBAMA, 1989; Grego et al., 2009), durante as amostragens de Brachyura, foram constatados impactos de origem antrópica no Rio Mamucabas, como desmatamentos, avanço da construção civil em direção ao manguezal (também documentada por Santos et al., 2001, Araújo et al., 2012 a, b), deposição de lixo, além do impacto causado pelo represamento quando este rio passa pela Reserva de Saltinho.
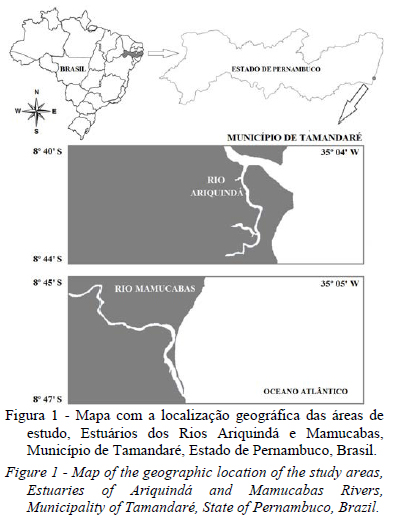
2.1. Manguezal do Rio Ariquindá
O Rio Ariquindá (Figura 1), afluente do Rio Formoso, recebe águas dos rios União, Porto do Tijolo, Porto Alegre e Cabrobó. Considerado de pequeno porte, tem 10 km de extensão e uma profundidade média de 6 m (Grego et al., 2009), sendo propício à navegação. Seu estuário é caracterizado por micromarés, com aplitudes de 1,5 m (Calder & Maÿal, 1998). Estudos indicam que esse estuário não sofre fortes impactos antrópicos, estando isento de poluição orgânica (Grego et al., 2009), mas, com a construção da ponte sobre esse rio, processos erosivos passaram a ser observados.
Os quatro pontos de amostragem no manguezal do Rio Ariquindá podem ser descritos como:
Ponto 1: Local de transição entre o manguezal e o ambiente terrestre, localizado a aproximadamente 400 m da margem do rio. Composto por gramíneas, seguido de Talipariti tiliaceum(L.) Fryxell (Malvaceae) e poucos exemplares de Laguncularia racemosa(L.) C.F. Gaertn. (Combretaceae). Substrato areno-lamoso;
Ponto 2:Ambiente localizado aproximadamente a 200 m da margem do rio, no interior do manguezal, sendo composto por muita vegetação, predominantemente por L. racemosa, seguida de Rhizophora mangle L. (Rhizophoraceae) e poucos exemplares de Avicennia schaueriana Stapf & Leechman ex Moldenke (Acanthaceae). Substrato lamoso;
Ponto 3: Ambiente localizado na margem do rio e composto predominantemente por R.mangle. Substrato lamoso;
Ponto 4: Ambiente localizado a aproximadamente 5 m da margem do rio.Composto por um banco de lama próximo ao rio e com muita vegetação (R. mangle e alguns exemplares de L. Racemosa). Substrato lamoso-arenoso.
2.3. Manguezal do Rio Mamucabas
Outro sistema estuarino que se destaca no litoral sul de Pernambuco é o Complexo Ambiental Ilhetas-Mamucabas (Figura 1), formado pelos rios homônimos. O percurso final desses rios ocorre paralelamente ao litoral e é ladeado por manguezais separados do mar adjacente por um estreito cordão arenoso (CPRH, 1999). Eles fluem em separado e se encontram em uma boca comum chamada Ponta das Ilhetas ou Boca da Barra (Maida & Ferreira, 1997). A nascente do Rio Mamucabas fica a 15 km da baía de Tamandaré, a oeste da Reserva Biológica de Saltinho, e, ao ali entrar, é represado para formar reservatório que abastece o Município de Tamandaré (CPRH, 2001). A distância máxima entre as suas margens é de 31 m. É um rio bastante raso e bem menor que o Rio Ilhetas, impossibilitando a navegação. Foi considerado pelo IBAMA (1989) como um dos rios de águas mais saudáveis do estado de Pernambuco. Entretanto, decorridas mais de duas décadas, foram observados impactos em algumas áreas do manguezal, como desmatamentos, deposição de resíduos sólidos (lixo) e ocupação imobiliária irregular (Santos et al., 2001; Araújo et al., 2012 a, b).
Os quatro pontos de amostragem no manguezal do Rio Mamucabas podem ser descritos como:
Ponto 1: Ambiente de transição entre o manguezal e o ambiente terrestre, localizado a cerca de 200 m da margem do rio, sendo composto predominantemente por gramíneas, seguido de T. tiliaceum e alguns exemplares de R. mangle.Substrato argiloso;
Ponto 2: Ambiente localizado aproximadamente a 100 m da margem do rio no interior do manguezal. Vegetação composta predominantemente por L. racemosa, seguida de R. mangle e poucos exemplares de A. schaueriana. Substrato lamoso;
Ponto 3: Ambiente localizado na margem do rio e composto predominantemente por R. manglee substrato estritamente lamoso;
Ponto 4: Ambiente composto por um banco de algas no interior do manguezal, distante 250 m do rio. Vegetação composta por T. tiliaceum e alguns exemplares de L. racemosa. Substrato lamoso-arenoso.
3. Materiais e Métodos
3.1. Procedimentos de coleta
O calendário de coletas mensais foi elaborado seguindo previsões da tábua de marés da Diretoria de Hidrografia e Navegação (DHN) para o Porto do Recife, em período de lua cheia. O trabalho de campo estendeu-se por um período de um ano, de abril/2008 a março/2009.
Nos quatro pontos estabelecidos em cada estuário, foram realizadas coletas manuais por dois coletores, com um esforço amostral de 30 minutos/ponto, durante o período de maré baixa. A área explorada em cada ponto era de aproximadamente 20 m². Procurou-se abranger todos os microhabitats dos estuários, tais como: tocas escavadas na areia e lama; folhas e troncos em processo de decomposição; raízes e troncos das árvores do mangue; sob e sobre pedras; e em bancos de algas, mexilhões e ostras. Foram utilizadas pás de
jardim para auxiliar na escavação da lama e na remoção de alguns exemplares, que foram levados ao laboratório para processamento.
Em laboratório, os espécimes foram lavados e fixados em álcool 70%, bem como as espécies identificadas por bibliografia especializada (Melo, 1996). Para verificar a sistemática e a validade taxonômica dos nomes científicos, foi consultado o artigo de Ng et al. (2008), além de acessados bancos de dados online, como o World Register of Marine Species (WORMS) e o Integrated Taxonomic Information System (ITIS). Alguns exemplares foram incorporados às coleções científicas do Museu de Oceanografia “Petrônio Alves Coelho” (MO/UFPE) e do Centro Acadêmico de Vitória (CAV/UFPE).
3.2. Análise dos dados
Com base nos resultados das identificações, foram realizadas, para cada estuário, análises quantitativas, ecológicas e multivariadas.
Nas análises quantitativas, foram avaliadas:
1) Abundância total (AT), relacionada ao número absoluto de indivíduos por espécie; 2) Abundância relativa (AR), referente ao percentual relativo de cada espécie, pela fórmula AR = n 100/N (onde n = número de indivíduos por espécie; e N = total de indivíduos na amostra), e classificação das espécies como: dominante (AR≥ 70%); abundante (40 £AR< 70%); pouco abundante (10 <AR< 40%); e rara (AR£ 10%); 3) Frequência de ocorrência (FR) de cada espécie, em porcentagem, obtida pela fórmula: FR = a 100/A (onde a = número de amostras contendo a espécie; e A = total de amostras), com classificação: muito frequente (FR ≥ 70%); frequente (40 £FR< 70%) pouco frequente (10 <FR< 40%); e esporádica (FR£ 10%).Nas análises ecológicas, foram avaliados quatro índices, para cada um dos quais foram estimados os valores mínimos, máximos e médios (± desvio padrão), com possibilidade de agrupamento dos pontos de coleta por estuário caso os valores de diversidade não difiram significativamente entre os pontos pelo teste de Kruskal-Wallis (p> 0,05) (Zar, 1996). Os índices ecológicos avaliados foram:
1) Diversidade de Shannon (H’), que trata da variedade de espécies de organismos vivos em determinada comunidade, habitat ou região (Shannon, 1948), sendo calculada pela seguinte fórmula: H’=- Σ pi log2 pi , com pi = n/N (onde n = número de indivíduos de cada espécie; e N= número total de indivíduos), com os resultados obtidos enquadrados na classificação: muito alta(H´ > 4 bits.ind-1); alta (3 < H’ ≤ 4 bits.ind-1); média (2 < H’ £ 3 bits.ind-1); baixa (1 < H’ £ 2 bits.ind-1); e muito baixa (H’≤ 1 bits.ind-1);
2) Equitabilidade de Pielou (J’), referente à distribuição de indivíduos entre as espécies registradas, sendo proporcional à diversidade, exceto se houver co-dominância de espécie (Pielou, 1969), sendo calculada pela fórmula J’ = H’/log(S) (onde H'= índice de Shannon; e S = número total de espécies). Esse índice varia de 0 a 1, sendo considerados equitativos valores superiores a 0,5;
3) Riqueza de Margalef (D), que trata da abundância numérica em determinada área geográfica, região ou comunidade (Margalef, 1958), sendo calculada a partir da seguinte fórmula D = (S–1)/log(N) (onde S = número de espécies; e N = número de indivíduos por amostra), obedecendo a classificação: baixa diversidade (D <2) e alta diversidade (D > 5);
4) Dominância de Simpson (1-ƛ), que trata da probabilidade de dois indivíduos escolhidos ao acaso na comunidade pertencerem à mesma espécie, variando de 0 a 1 (Simpson, 1949), sendo calculada a partir da fórmula 1-ƛ = 1-Σpi² com pi = n/N, evidenciando maior dominância e menor diversidade quando seus valores forem mais próximos da unidade (Simpson, 1949).
Os dados obtidos também foram submetidos a análises multivariadas, que, devido ao grande número de zeros nas amostras, tiveram que ser previamente log-transformados (logn+1, onde n é o número de exemplares por espécie). Os dados obtidos foram submetidos a uma análise de similaridade, gerando uma matriz triangular, tendo sido eleito o coeficiente de Bray-Curtis como o índice de similaridade ideal para tais dados de abundância. Com base nessa matriz, as afinidades entre as estações de coleta foram estabelecidas por uma análise de ordenação multi-dimensional não-métrica (NMDS). Para testar a ordenação, o coeficiente de estresse de Kruskal foi empregado (estresse mínimo de 0,01). Em seguida, uma análise de percentuais de similaridade (SIMPER) foi empregada para indicar quais espécies mais contribuíram para a similaridade dentro de cada ponto de coleta, bem como para a dissimilaridade entre eles. Por fim, as afinidades entre as espécies foram avaliadas por análise hierárquica de Cluster (Clarke, 1993).
4. Resultados
4.1. Diversidade no manguezal do Rio Ariquindá
4.1.1 Sinopse taxonômica
Um total de 4.501 exemplares de Crustacea Brachyura foi coletado no manguezal do Rio Ariquindá, estando distribuídos em 25 espécies, 14 gêneros e 7 famílias. Dentre esses, a Superfamília Ocypodoidea foi a mais representativa, com 9 espécies, destacando-se as pertencentes aos gênero Uca Leach, 1.814, seguida das Superfamílias Grapsoidea e Xanthoidea, que contribuíram com 7 e 6 espécies do total encontrado no manguezal, respectivamente. As demais espécies pertenciam às Superfamílias Portunoidea (2 espécies) e Pinnotheroidea (1 espécie). A sinopse taxonômica das espécies identificadas encontra-se no Anexo I [Informação Suplementar / Supplementary Information]1.
4.1.2. Análises quantitativas
Quanto à abundância total (AT), Uca thayerise destacou, com 1.411 exemplares. Já em relação à abundância relativa (AR), a maioria das espécies pôde ser considerada rara, com exceção de Sesarma rectum, Uca leptodactylae U. thayeri, consideradas pouco abundantes. Por fim, no tocante à frequência relativa (FR), a maioria das espécies foi considerada esporádica ou pouco frequente, com exceção de Uca burgersi, U. cumulanta, U. leptodactyla e U. Thayeri, consideradas frequentes. As espécies amostradas neste manguezal, bem como sua AT, AR e FR, estão apresentadas no Anexo II [Informação Suplementar / Supplementary Information]1.
Na figura 2, nota-se que as espécies apresentaram diferentes valores de abundância, de acordo com os pontos de coleta, apresentando distintos padrões de distribuição espacial. Algumas espécies apresentaram maior abundância em algumas estações, a saber: Ponto 1 (Armases angustipes, Eurytium limosum, Goniopsis cruentata, Sesarma rectum, Uca burgersi, U. leptodactylae U. rapax); Ponto 2 (S. curacaoensis, U. thayerie Ucides cordatus); Ponto 3 (Acantholobulus bermudensis, Aratus pisonii, Austinixa leptodactyla, Callinectes danae, C. exasperatus, Ocypode quadrata, Pachygrapsus gracilis, P. transversuse Panopeus lacustris); e Ponto 4 (Hexapanopeus angustrifrons, H. caribbaeus, P. occidentalis, Sesarma curacaoensis, U. cumulanta, U. leptodactyla, U. maracoanie U. Victoriana).
4.1.3. Índices ecológicos
No Rio Ariquindá (PE), a diversidade de Shannon (H' = 1,76 ± 0,16 bits.ind-1) e a riqueza de Margalef baixa (D = 1,12 ± 0,12) foram considerados baixos, ao contrário da equitabilidade de Pielou (J' = 0,74 ± 0,06) e a dominância de Simpson(1 - ƛ = 0,63 ± 0,04), considerados altos.
No geral, a diversidade de espécies pode ser considerada média, com pequena oscilação ao longo dos meses do ano. Entretanto, observam-se diferenças espaciais, sendo mais diversos os pontos 1 e 3 (Anexo III [Informação Suplementar / Supplementary Information]1), indicando um padrão de distribuição espacial distinto entre as diferentes áreas de um mesmo manguezal.
4.1.4. Análises multivariadas
Segundo o NMDS (Figura 3), três grupos foram formados, de acordo com os pontos de coleta: pontos 2 e 4 (região marginal do manguezal), com substrato lamoso; e pontos 1 e 3 (região interna do manguezal), cada um deles com vegetação distinta, formando dois grupos. O índice de Bray-Curtis revelou que Uca thayerifoi responsável pela similaridade dentro dos pontos 2 e 4, que apresentaram entre si a menor dissimilaridade (44,5%), o que pode explicar o seu agrupamento. Os pontos que mais diferiram entre si foram o 1 e o 3 (dissimilaridade = 98,4%), por causa das espécies S. rectum, A. angustipese U. burgersi, e 3 e 4 (dissimilaridade = 94,6%), por causa das espécies U. thayeri, U. leptodactyla, U. cumulantae A. pisonii.
A análise de cluster com as principais espécies revelou a formação de três grupos de acordo com os seus valores de abundância (Figura 4). O grupo A foi formado por espécies com maior abundância (com destaque às espécie do gênero Uca), seguidas por aquelas do grupo B, de abundância intermediária (E. limosum, S. curacaoense, G. cruentata e U. Maracoani), e do grupo C, de menor abundância (destaque para os Panopeidae).
4.2. Diversidade no manguezal do Rio Mamucabas
4.2.1 Sinopse taxonômica
Um total de 3.893 braquiúros foi coletado no manguezal do Rio Mamucabas, representados por 21 espécies e distribuídas em 12 gêneros e 06 famílias. Uma dessas espécies, o sesarmídeo Armases rubripes(Rathbun, 1897), foi encontrada somente nesse manguezal. Por outro lado, 05 espécies (Acantholobulusbermudensis, Austinixa leptodactyla, Callinectes exasperatus, Hexapanopeus caribbaeuseUca maracoani) ocorreram apenas no Rio Ariquindá. Assim, vinte espécies foram comuns para ambos os manguezais.
De entre os Brachyura do manguezal do Rio Mamucabas, a Superfamília Ocypodoidea foi a mais representativa (8 espécies), destacando-se as pertencentes aos gênero Uca, seguida das Superfamílias Grapsoidea e Xanthoidea, com 08 e 04 espécies, respectivamente. A Superfamília Portunoidea esteve representada por uma única espécie. A sinopse taxonômica das espécies identificadas encontra-se no Anexo IV [Informação Suplementar / Supplementary Information em http://www.aprh.pt/rgci/rgci-493_Araujo_SuplMat.
4.2.2. Análises quantitativas
Quantoàabundânciatotal(AT),Uca thayerise destacou no manguezal do Rio Mamucabas, com 1.300 exemplares. Já em relação à abundância relativa (AR), a maioriadas espécies foi considerada rara, com exceção de Uca leptodactyla, U. thayerie U. victoriana,consideradas pouco abundantes. No caso da frequência relativa (FR), muitas espécies foram consideradas esporádicas ou pouco frequentes, com exceção de Armases angustipes, Eurytium limosum, Uca burgersi, U. leptodactyla, U. rapax e U. thayeri (espécies frequentes), e U. victoriana (espécie frequente). As espécies amostradas neste manguezal, bem como sua AR e FR, estão apresentadas no Anexo V [Informação Suplementar / Supplementary Information]1.
Os valores de abundância para as espécies diferiram bastante entre os pontos de coleta (Figura 5), a saber:
Ponto 1 (Armases angustipes, A. rubripes, Goniopsis cruentata, Pachygrapsus gracilis, Sesarma Curaçaoensis, Uca cumulantae U. rapax);
Ponto 2 (Eurytium limosum, Panopeus lacustris, S. curacaoensis, U. leptodactyla, U. thayeri, U. victorianae Ucides cordatus);
Ponto 3 (Aratus pisonii, Callinectes danae, Hexapanopeus angustrifrons, Ocypode quadrata, Pachygrapsus gracilis, P. transversus, Panopeus lacustrise P. occidentalis); e
Ponto 4 (S. curacaoensis, S. rectum, U. burgersi, U. leptodactylae U. Victoriana).
4.2.3. Índices ecológicos
De modo similar ao ocorrido no manguezal anterior, o do Rio Mamucabas apresentou baixos valores de diversidade de Shannon (H' = 1,80 ± 0,21 bits.ind-1) e de riqueza de Margalef (D = 1,19 ± 0,14), ao contrário do verificado para a equitabilidade de Pielou (J' = 0,71 ± 0,11) e dominância de Simpson (1 - ƛ = 0,63 ± 0,08), cujos valores foram altos.
De modo geral, a diversidade de espécies pode ser considerada média para este manguezal. Também pode ser observado que os índices não variaram notoriamente ao longo do ano, exibindo apenas pequenas oscilações. Entretanto, observam-se diferenças espaciais, com maiores valores médios para os pontos 1 e 4 (Anexo VI [Informação Suplementar / Supplementary Information]1), indicando, mais uma vez, um padrão de distribuição espacial distinto em diferentes áreas de um mesmo manguezal.
4.2.4. Análises multivariadas
Na Figura 6, é perceptível um menor agrupamento entre os pontos, que apresentaram uma maior dispersão de valores para a NMDS. Um maior agrupamento de pontos de coleta ocorreu para 1, 2 e 4, enquanto o ponto 3 ficou mais disperso (menor similaridade). O índice de similaridade de Bray-Curtis revelou que as espécies Aratus pisoniie Eurytium limosumforam as mais abundantes no ponto 3, enquanto os demais pontos foram dominados por espécies do gênero Uca, o que pode explicar o resultado observado. Esse ponto também apresentou a maior dissimilaridade com os demais pontos, sendo que os mais divergentes foram o 1 e o 3 (dissimilaridade = 78,1%), por causa das espécies A. angustipes, U. burgersi, U. leptodactylae U. victoriana, enquanto os mais similares foram o 1 e o 4 (dissimilaridade = 46,8%), por causa das espécies U. thayeri, U. victoriana, U. burgersie U. leptodactyla.
A análise de cluster, envolvendo as principais espécies do manguezal do Rio Mamucabas, revelou que, com a linha de corte posicionada a 25%, havia a formação de um grupo principal formado por espécies com maior abundância, com destaque àquelas do gênero Uca, e as demais não formando grupos evidentes (Figura 7).
4. Discussão
Os crustáceos da Infraordem Brachyura representam um grupo altamente diverso e bem sucedido. No presente trabalho, um total de 26 espécies foi amostrado. Destas, 09 espécies (34,6%) são registros novos para o Município de Tamandaré (PE), quando considerada a listagem de espécies publicada por Coelho & Ramos-Porto (1995) para a região, a saber: Acantho-lobulus bermudensis, Armases rubripes, Austinixa leptodactyla, Hexapanopeus angustifrons, H. caribbaeus, Panopeus occidentalis, Sesarma curacaoense, Uca cumulantae Uca victoriana. Pelo exposto, fica clara a importância dos levantamentos de diversidade.
É sabido que o número de espécies tende a variar em função da latitude. De acordo com Boschi (2000), a maioria das espécies de Brachyura é encontrada em regiões tropicais e subtropicais, ocorrendo decréscimo na diversidade com o aumento latitudinal. Esse padrão pode ser atribuído à estabilidade dos ecossistemas, que, na história evolutiva da Terra, contribui à existência de uma maior riqueza de espécies em regiões tropicais (Margalef, 1963).
Na Figura 8, pode-se observar como o número de espécies de Brachyura se comporta no litoral brasileiro. De entre todas as espécies registradas para a costa brasileira, o maior número de espécies de caranguejos (36) é observado nos manguezais do Rio Paripe, PE (Coelho-Santos & Coelho, 2001), com tendência adiminuir em direção ao sul do país. O número de espécies registrado no presente estudo está dentro do esperado para a região Nordeste. No estado de Santa Catarina, limite austral da distribuição dos manguezais na América do Sul (28ºS, segundo Schaeffer-Novelli, 1999), devido ao clima mais frio, o desenvolvimento dos manguezais é menor (Schaeffer-Novelli, 1999), o mesmo ocorrendo com a diversidade de crustáceos. Em zonas temperadas, a partir dos 25ºS, os manguezais geralmente são substituídos pelos marismas. No entanto, algumas regiões, como no Saco da Fazenda (SC), os manguezais e marismas coexistem, sendo observada a menor riqueza de caranguejos (5 espécies, segundo Branco et al.,2011). Com isso, confirma-se a maior diversidade de Brachyura em áreas tropicais, ecossistemas mais estáveis, como os estuários pernambucanos.
Apesar da proximidade geográfica dos manguezais onde os caranguejos foram amostrados no presente trabalho, houve uma diferença na composição específica entre eles, com cinco espécies encontradas exclusivamente nos manguezais do Rio Ariquindá (Acantholobulusbermudensis, Austinixa leptodactyla, Callinectes exasperatus, Hexapanopeus caribbaeuseUca maracoani) e com apenas uma espécie (Armases rubripes) exclusiva para o manguezal do Rio Mamucabas. Outros autores, estudando a diversidade de Decapoda em manguezais próximos entre si (Coelho, 1965/66; Ferreira & Sankarankutty, 2002; Colpo et al., 2011), também observaram diferentes composições específicas. Enquanto em grandes escalas latitudinais a temperatura é o principal fator explicativo das diferenças na composição específica, em escala espacial, as variações são melhor explicadas pela composição/idade do bosque de manguezal, heterogeneidade de seu substrato, disponibilidade de alimento, influência das marés, relações presa-predador, interações interespecíficas e grau de impacto ambiental (Abele, 1974; Boschi, 2000; Ashton et al., 2003).
Apesar da proximidade geográfica dos manguezais onde os caranguejos foram amostrados no presente trabalho, houve uma diferença na composição específica entre eles, com cinco espécies encontradas exclusivamente nos manguezais do Rio Ariquindá (Acantholobulusbermudensis, Austinixa leptodactyla, Callinectes exasperatus, Hexapanopeus caribbaeuseUca maracoani) e com apenas uma espécie (Armases rubripes) exclusiva para o manguezal do Rio Mamucabas. Outros autores, estudando a diversidade de Decapoda em manguezais próximos entre si (Coelho, 1965/66; Ferreira & Sankarankutty, 2002; Colpo et al., 2011), também observaram diferentes composições específicas. Enquanto em grandes escalas latitudinais a temperatura é o principal fator explicativo das diferenças na composição específica, em escala espacial, as variações são melhor explicadas pela composição/idade do bosque de manguezal, heterogeneidade de seu substrato, disponibilidade de alimento, influência das marés, relações presa-predador, interações interespecíficas e grau de impacto ambiental (Abele, 1974; Boschi, 2000; Ashton et al., 2003).
Segundo Macintosh (1984), os caranguejos formam o maior componente da macrofauna de praias e manguezais, e, segundo Aveline (1980) e Jones (1984), esses organismos, juntamente com os moluscos, são os animais mais abundantes dos manguezais. Das famílias de Brachyura que vivem no ecossistema manguezal (Ocypodidae, Grapsidae, Gecarcinidae, Mictyridae, Panopeidae, Portunidae, Xanthidae e Ucididae) (Jones, 1984; Melo, 1996), apenas Gecarcinidae e Mictyridae não foram amostradas nos manguezais dos Rios Ariquindá e Mamucabas. Entretanto, a espécie Cardisoma guanhumiLatreille, 1828 (Gecarcinidae) ocorreu em amostragens extras realizadas em outras áreas dos manguezais desses rios. Isso demonstra a elevada riqueza de famílias nas áreas do presente estudo, o que corrobora Coelho (1965/66).
De entre os crustáceos da Infraordem Brachyura, as Superfamílias Ocypodoidea, Grapsoidea e Xanthoidea foram as mais representativas no presente trabalho, assim como observado por diversos autores (Coelho, 1965/66; Jones, 1984; von Prahl et al., 1990; Ashton et al.,2003; Nagelkerken et al., 2008). De acordo com Kristensen (2008), a fauna bentônica dos manguezais é dominada por esses caranguejos, entre os quais os Ocypodoidea escavam tocas no substrato. Os Grapsoidea incluem caranguejos herbívoros, que retêm, enterram e ingerem folhas e algas (Kristensen & Alongi, 2006), previnindo a perda de nutrientes e uma aceleração dos processos de decomposição. As tocas afetam a topografia e a biogeoquímica do sedimento, modificando a drenagem e a disponibilidade de nutrientes (Botto & Iribarne, 2000). Segundo Ferreira & Sankarankutty (2002), essas tocas formam um sistema de túneis anastomosados, que cruzam o substrato dos manguezais, demonstrando a importância desses animais ao ecossistema. Além disso, os caranguejos são denominados biengenheiros dos manguezais, por afetarem a química e a estrutura do sedimento (Kristensen, 2008).
No presente estudo, os Ocypodoidea destacaram-se em ambos os estuários por apresentarem elevadas riquezas de espécies (09 e 08 nos manguezais dos Rios Ariquindá e Mamucabas, respectivamente). São caranguejos típicos dos estuários e manguezais do mundo, inclusive do Brasil (Jones, 1984; Melo, 1996; Calado & Sousa, 2003; Bezerra et al., 2010; Colpo et al., 2011). O gênero Uca, por exemplo, foi representado por 07 espécies: U. burgersi, U. cumulanta, U. leptodactyla, U. maracoani, U. rapax, U. thayerie U. victoriana. Segundo Castiglioni et al. (2010), 09 espécies de Ucaocorrem em Pernambuco, entre as quais apenas duas espécies não foram registradas no presente estudo: U. (Minuca) mordax(Smith, 1870) e U. (Minuca) vocator(Herbst, 1804). Provavelmente, tais espécies não tenham sido capturadas pelo fato de ocorrerem em áreas de manguezal caracterizadas por menores salinidades ao longo da costa brasileira (Masunari & Dissenha, 2005). Com base nessas observações, pode-se inferir que a diversidade observada para o gênero no presente trabalho foi bem expressiva.
A espécie de caranguejo mais abundante nos dois estuários em estudo foi U. thayeri, corroborando informações de Rodrigues et al. (1994), para o Rio Camboriú (SC). Entretanto, de acordo com Melo (1996), a espécie U. rapax geralmente é a mais abundante do gênero, o que foi confirmado por Oshiro et al. (1998), na Baía de Sepetiba, e Bedê et al. (2008), no Manguezal do Itacuruçá (RJ). Muitas vezes, U. victorianaé identificada erroneamente como U. rapax,o que pode superestimar os valores de abundância desta última espécie. Castiglioni et al. (2010) registram a primeira ocorrência de U. victorianapara os estados da Bahia e de Pernambuco, porpondo alguns caracteres morfológicos diagnósticos para essas espécies e outra também muito semelhante (U. burgersi).
Além das espécies do gênero Uca,outras duas espécies de Ocypodoidea ocorreram na área de estudo: Ucides cordatuse Ocypode quadrata. A primeira, conhecida popularmente como caranguejo-uçá, é um importante componente nos manguezais de todo o Brasil, especialmente no Nordeste, onde é muito apreciada na culinária (Araújo & Calado, 2008). Essa espécie tem sido capturada intensamente em várias localidades brasileiras, conduzindo a espécie à sobrexplotação (Araújo et al.,2012b; Castiglioni et al., 2013). Apesar de sua reduzida abundância registrada nos manguezais em estudo, essa espécie foi extremamente abundante em outras áreas desses mesmos manguezais, onde pôde ser capturada por métodos mais específicos (braceamento e gancho). Já a segunda espécie (maria-farinha) foi considerada rara e pouco frequente no manguezal do Ariquindá, e rara e esporádica no manguezal de Mamucabas. É uma espécie típica do supralitoral de praias arenosas (Melo, 1996), embora também possa ser registrada, eventualmente, em ambientes estuarinos (Almeida et al., 2006).
A superfamília Grapsoidea apresentou 07 e 08 espécies (manguezais de Ariquindá e Mamucabas, respectivamente). São caranguejos encontrados não apenas em estuários e manguezais, mas também em praias rochosas e em ambientes de água doce (Jones, 1984; Melo, 1996; Calado & Sousa, 2003; Colpo et al., 2011). Dentre os grapsóideos, destacaram-se duas espécies: Sesarma rectum (abundância no Rio Ariquindá) e Armases angustipes (frequência no Rio Mamucabas). Porém, ambas ocorreram nos dois estuários, corroborando Melo (1996), que afirma que essas duas espécies ocorrem em simpatria.
A superfamília Xanthoidea também se destacou nos dois estuários analisados, com 06 e 04 espécies para os manguezais de Ariquindá e Mamucabas, respectivamente. Os Panopeidae ocorreram no presente estudo, com suas espécies registradas em fundos lamosos, como o substrato do manguezal, sendo, por isso, conhecidos, em inglês, como 'mud crabs' (Melo, 1996; Schubart et al.,2000; Calado & Sousa, 2003). Os gêneros de Panopeidae são morfologicamente similares, por convergência em função do habitat e dos hábitos semelhantes (Schubart et al., 2000), dificultando sua identificação. Entretanto, no presente estudo, todos os exemplares puderam ser identificados ao nível específico.
A superfamília Portunoidea também esteve representada em ambos os estuários por exemplares do gênero Callinectes. As espécies C. danaee C. exasperatussão frequentes no litoral pernambucano (Araújo et al., 2011), encontradas principalmente em ambientes estuarinos, mas também são encontradas em manguezais (Melo, 1996), como observado no presente trabalho.
Com base nos índices ecológicos e no número de espécies registradas, a diversidade de caranguejos dos dois manguezais pôde ser considerada média, corroborando a hipótese H1. Os valores obtidos evidenciaram compatibilidade com os obtidos em outros manguezais ao longo da costa brasileira (Figura 8), e até mesmo superiores aos manguezais protegidos da Malásia e Tailândia (Ashton et al.,2003), onde os valores de diversidade (H') variaram de 1,09 a 1,36 bits.ind-1. De acordo com a teoria da heterogeneidade espacial, quanto mais heterogêneo e complexo é um dado ambiente, mais diversa será a sua fauna (Simpson, 1964). Esse foi o caso dos manguezais, um ecossistema rico em microhabitats diferentes. Segundo Abele (1974), a diversidade de Decapoda nos manguezais só não supera os valores já registrados em ambientes ainda mais complexos do que eles (p. ex., recifes de coral e o intertidal rochoso), mas é maior do que os valores que são comumente obtidos para praias arenosas e áreas vegetadas com Spartina Schreb. (Poaceae).
A diversidade dos manguezais em estudo não pode ser considerada alta devido à elevada dominância de Uca thayeri, uma vezque apresentou a maior abundância total (Ariquindá: 1.411 exemplares; e Mamucabas: 1.300 exemplares), refutando a hipótese H2. Segundo Macintosh et al. (2002), a dominância de uma espécie pode ser um indicativo de estresse ambiental, pelo destaque de uma espécie oportunista em detrimento de outras menos tolerantes a variações ambientais. Entretanto, segundo esses autores, a diversidade dos grapsóides, em especial Sesarmidae, sinaliza um ambiente estável nos dois estuários estudados, onde apresentaram boa representatividade, como já discutido anteriormente.
No manguezal de Mamucabas, onde predominou o mangue-brancoLaguncularia racemosa(L.) C.F. Gaertn. (Combretaceae), o número de espécies foi inferior ao do Rio Ariquindá, onde a espécie arbórea dominante foi o mangue-vermelho, Rhizophora mangleL. (Rhizophoraceae). Alguns estudos apontam que, em manguezais mais preservados (e/ou maduros), as comunidades de Brachyura são mais ricas, apresentando dominância do mangue-vermelho, enquanto, em manguezais instáveis ambientalmente (e/ou jovens), ocorre redução da riqueza dos Brachyura, coincidindo com uma dominância do mangue-branco (Macintosh et al., 2002; Colpo et al.,2011). Tais observações também explicam o menor número de espécies no manguezal de Mamucabas, sendo um indicativo de que os impactos ambientais encontrados nesse estuário já começam a afetar a comunidade de crustáceos braaquiúros.
Além das diferenças observadas na composição de espécies entre os estuários, existem diferenças em cada estuário, entre as estações de coleta. Cada estação apresentou seu grupo de espécies mais relevantes. Essas diferenças dentro de cada estuário, provavelmente, se devam à alta heterogeneidade estrutural do manguezal (Laegdsgaard & Johnson, 1995), tanto espacial quanto temporal. Os braquiúros apresentam preferências ecológicas muito específicas, com algumas espécies ocupando mais de um microhabitat (p. ex., tocas, árvores, troncos podres etc.), embora cada um desses substratos tenha sua fauna característica, ainda que os diferentes tipos estejam muito próximos (Coelho, 1965/66; Branco, 1990; Oshiro et al., 1998). Portanto, a diferente composição de espécies vegetais, a natureza do substrato e a distância da margem do rio em cada estação também podem ter colaborado para o resultado obtido no presente estudo.
No presente trabalho, as espécies mais abundantes apresentaram tendência a se agrupar. Isso foi visível com as espécies do gênero Uca, que formaram grupos bem definidos nos manguezais dos estuários estudados (Ariquindá: U. burgersi, U. cumulanta, U. leptodactyla, U. rapaxe U. thayeri; e Mamucabas: U. burgersi, U. leptodactyla, U. rapax, U. thayerie U. victoriana).É sabido que os chama-marés são gregários e simpátricos (Crane, 1975; Bedê et al., 2008; Colpo et al.,2011), habitando simultaneamente uma mesma região geográfica sem que haja cruzamento entre seus indivíduos. Dentre as espécies identificadas no presente trabalho, sabe-se que U. leptodactylae U. cumulantasão simpátricas no Complexo Estuarino Lagunar Mundaú Manguaba (AL) (Calado & Sousa, 2003); U. rapaxé simpátrica com cinco outras espécies no Golfo do México e com U. burgersiem praias arenosas (Thurman, 1987, 2002); U. burgersitambém é simpátrica com U. mordax, da Guatemala ao sul do Brasil (von Hagen, 1982), embora esta última não tenha sido registrada no presente estudo. Possivelmente, nos manguezais do Município de Tamandaré (PE), existe simpatria entre os chama-marés, o que explicaria o agrupamento de suas espécies.
Pode-se inferir que as duas comunidades de Brachyura estudadas foram muio influenciadas pela natureza do substrato, sendo um dos fatores abióticos mais importantes na definição de uma comunidade bêntica de uma região (Carvalho & Couto, 2011). Tal aspecto já foi relatado desde a década de 30, quando Oliveira (1939) observou que cada grupo de espécies habita um substrato específico, o que já foi corroborado por outros autores (Oshiro et al., 1998; Bedê et al., 2008; e Colpo et al., 2011). Dentre as espécies mais representativas, nota-se que quatro caranguejos semiterrestres (Armases angustipes, A. rubripes, Goniopsis cruentatae Sesarma curacaoense) foram mais abundantes no ecótono entre o manguezal e a restinga, onde o substrato era mais arenoso. Essas espécies possuem significativas adaptações comportamentais, morfológicas, fisiológicas ou bioquímicas que permitem atividade extendida fora d’água (Burggren & McMahon, 1988), podendo se afastar mais da margem do manguezal em direção à restinga. Por outro lado, os representantes de Panopeidae ("mud crabs") foram mais abundantes nos ambientes lamosos, sendo menos adaptados à exposição fora d'água por períodos prolongados, estando sempre em contato com a umidade do substrato.
5. Conclusão
Apesar da proximidade entre os dois estuários, foram detectadas diferenças na composição das espécies de Brachyura, com menor diversidade associada ao Manguezal Mamucabas, cujo estuário tem sofrido a influência de diversos impactos. Entre eles, destacam-se o desmatamento da vegetação nativa, a deposição de resíduos sólidos, a ocupação imobiliária crescente, além do represamento parcial de parte do curso do rio.
A diversidade e a ecologia dos crustáceos braquiúros, principais representantes no ecossistema manguezal, mostram alterações sensíveis quando sujeitos aos impactos ambientais, sendo, assim, importantes bioindicadores de qualidade ambiental. Confirmando tal característica, verificou-se, para Mamucabas, uma redução dos índices ecológicos, particularmente na diversidade e na riqueza de espécies. As espécies típicas de manguezal Acantholobulus bermudensis, Austinixa leptodactyla, Callinectes exasperatus, Hexapanopeus caribbaeuse Uca maracoani não foram encontradas no manguezal do Mamucabas. Comparando os resultados obtidos com aqueles disponíveis para outros manguezais, nota-se que, em ambos os estuários estudados, a diversidade pode ser considerada média, estando dentro do esperado para o Nordeste brasileiro.
A comparação das espécies mais abundantes nas áreas estudadas também evidenciou alterações sensíveis para o manguezal de Mamucabas. Como exemplo, podemoscitar o caso de U. thayeri, que, neste manguezal, apresentou maturidade sexual com tamanhos pouco superiores aos do Ariquindá, indicando que a população em Mamucabas esteja se beneficiando da maior disponibilidade de matéria orgânica oriunda da poluição (Araújo et al.,2012a). Na espécie U. cordatus, o fator de condição também foi significativamente menor em Mamucabas, indicando menor saúde para os exemplares desse estuário (Araújo et al.,2012b).
Algumas das espécies coletadas no presente estudo apresentam importância econômica, sendo utilizadas na alimentação (p. ex., Callinectes danae, C. exasperatus, Goniopsis cruentatae Ucides cordatus), enquanto as demais espécies, ainda que com ausência de importância econômica, apresentam relevância ecológica, participando na teia trófica dos manguezais. Tan&Ng (1994) sugeriram que a manutenção da diversidadede caranguejos é importante para a saúde dos manguezais. Portanto, torna-se fundamental o estabelecimento de um plano de manejo nos dois estuários, assim como a contenção dos impactos ambientais, em especial em Mamucabas.
Todos os resultados indicam que o manguezal de Mamucabas apresenta algum impacto. No entanto, os dados sugerem que eles ainda são leves e estão atuando há pouco tempo, indicando que a situação do manguezal de Mamucabas não é grave. Entretanto, esse estuário ainda é considerado por muitos autores como não impactado, o que o presente estudo demonstra também ser incorreto, ressaltando a importância da mitigação dos impactos existentes. Para tal, propõe-se aqui as seguintes medidas, para ambos os estuários, em especial para o do Rio Mamucabas:
- Maior controle das construções imobiliárias irregulares no entorno do manguezal pela Prefeitura de Tamandaré, Governo do Estado de Pernambuco (Secretarias de Infraestrutura e do Meio Ambiente) e órgãos estaduais competentes (p. ex., CPRH), com o estabelecimento de multas ou outras punições aos que fizerem a supressão da vegetação, protegida por vários instrumentos legais, tanto federais quanto estaduais;
- Intensificação da coleta seletiva, reciclagem e compostagem de resíduos sólidos descartados no manguezal, por meio de ações conjuntas envolvendo o CPRH, o IBAMA, a Secretaria do Meio Ambiente e projetos ambientais da Prefeitura de Tamandaré (PE) (p. ex., Programa Agente Jovem Ambiental), além do estabelecimento de multas ou outras punições àqueles que despejarem esses dejetos na área em questão; e
- Criação de planos de manejo e sustentabilidade em áreas de manguezal, tendo em vista sua importância ecológica e econômica, com foco em espécies como Ucides cordatus, Goniopsis cruentatae de espécies do gênero Callinectes, que têm sido exploradas inadvertidamente, de maneira descontrolada e insustentável, em vários manguezais do Estado de Pernambuco. Entre as ações está o desenvolvimento de estudos que visem estabelecer os tamanhos mínimos de captura, intensificação da fiscalização durante o período de defeso de U. cordatus, entre outras.
Além disso, nove espécies foram registradas pela primeira vez para a região de Tamandaré (PE), o que ressalta a importância dos estudos de diversidade. Esses estudos, associados às medidas de proteção anteriormente propostas, são importantes, se considerarmos que os crustáceos participam da teia trófica de diversos animais, entre eles o homem, com vistas à manutenção da diversidade de caranguejos, considerada importante para a saúde dos manguezais.
Agradecimentos
A primeira autora é grata à CAPES (Coordenação de Aperfeiçoamento de Pessoal de Nível Superior), pela concessão da bolsa que tornou possível a sua dedicação ao doutorado. A terceira autora é grata ao CNPq (Conselho Nacional de Desenvolvimento Científico e Tecnológico), pela concessão da bolsa que tornou possível a sua dedicação ao DCR. Os autores são gratos ao PPGO/UFPE (Programa de Pós-Graduação em Oceanografia), em especial aos Doutores Jesser Fidelis e Aline Barreto, pelas sugestões no manuscrito; às Dras Cristiane Farrapeira, UFRPE, e Tereza Calado, UFAL, igualmente pelas sugestões no manuscrito. À Fundação de Amparo à Ciência e Tecnologia do Estado de Pernambuco (FACEPE), pelo apoio financeiro (APQ: 0108-2.04/07). A Adriano Martins, pelo auxílio durante as coletas de campo. Todas as amostragens do estudo foram realizadas de acordo com as leis federais e estaduais aplicáveis (ICMBio 14340-1).
Referências bibliográficas [ Links ]
Almeida, A.O.; Coelho, P.A.; Santos, J.T.A.; Ferraz, N.R. (2006) - Crustáceos decápodos estuarinos de Ilhéus, Bahia, Brasil. Biota Neotropica (ISSN: 1676-0603), 6(2):24p, FAPESP, São Paulo, SP, Brasil. [ Links ]
Araújo, M.S.L.C.; Calado, T.C.S. (2008) - Bioecologia do caranguejo-Uçá Ucides cordatus (Linnaeus) no Complexo Estuarino Lagunar Mundaú/Manguaba (CELMM), Alagoas, Brasil. Revista da Gestão Costeira Integrada, 8(2):169-181. DOI: 10.5894/rgci141 [ Links ]
Araújo, M.S.L.C.; Castiglioni, D.S.; Coelho, P.A. (2012b) - Width-weight relationship and condition factor of Ucides cordatus (Crustacea, Decapoda, Ucididae) at tropical mangroves of Northeast Brazil. Iheringia Série Zoologia (ISSN: 0073-4721), 102:277-284, Fundação Zoobotânica do Rio Grande do Sul, Porto Alegre, RS, Brasil. Disponível on-line em http://www.scielo.br/pdf/isz/v102n3/v102n3a05.pdf [ Links ]
Araújo, M.S.L.C.; Coelho, P.A.; Castiglioni, D.S. (2012a) - Relative growth and determination of morphological sexual maturity of the fiddler crab Uca thayeri Rathbun (Crustacea, Ocypodidae) in two mangrove areas from Brazilian tropical coast. Pan-American Journal of Aquatic Sciences (ISSN: 1809-9009), 7(3):156-170, Rio Claro, SP, Brasil. Disponível on-line em http://www.panamjas.org/pdf_artigos/PANAMJAS_7(3)_156-170.pdf [ Links ]
Araújo, M.S.L.C.; Negromonte, A.O.; Barreto, A.V.; Alves-Junior, F.A. (2011) - Os siris (Crustacea; Brachyura; Portunidae) do Canal de Santa Cruz, Pernambuco, Brasil. Anais do I CONABIO / IV SIMCBIO, 1:563-572, UNICAP, Recife, PE, Brasil. [ Links ]
Ashton, C.A.; Hogarth, P.J.; Macintosh, D.J. (2003) - A comparison of brachyuran crab community structure at four mangrove locations under different management systems along the Melaka Straits-Andaman Sea coast of Malaysia and Thailand. Estuaries, 26(6):1461-1471. DOI: 10.1007/BF02803654 [ Links ]
Aveline, L.C. (1980) - Fauna de manguezais brasileiros. Revista Brasileira de Geografia (ISSN: 0034-723x), 42(2):786-821, IBGE, Rio de Janeiro, RJ, Brasil. [ Links ]
Bedê, L.M.; Oshiro, L.M.Y.; Mendes, L.M.D.; Silva, A.A. (2008) - Comparison of the population structure of the species of Uca (Crustacea: Decapoda: Ocypodidae) in the mangrove of Itacuruçá, Rio Janeiro, Brazil. Revista Brasileira de Zoologia(ISSN: 0101-8175), 25(4):601-607, Sociedade Brasileira de Zoologia, Curitiba, PR, Brasil. Disponível on-line em http://www.scielo.br/pdf/rbzool/v25n4/04.pdf [ Links ]
Bertini, G.; Fransozo, A.; Melo, G.A.S. (2004) - Biodiversity of brachyuran crabs (Crustacea: Decapoda) from non-consolidated sublittoral bottom on the northern coast of São Paulo State, Brazil.Biodiversity and Conservation, 13(12):2185-2207. DOI: 10.1023/B:BIOC.0000047900.96123.34 [ Links ]
Bezerra, L.E.A.; Dias, C.B.; Moraes, J. O.; Matthews-Cascon, H. (no prelo) - Distribuição espacial do caranguejo Uca maracoani(Latreile, 1802-1803) (Brachyura: Ocypodidae) em três manguezais do Nordeste do Brasil. Revista de Gerenciamento Costeiro Integrado(ISSN: 1677-4841), Número especial 2, Manguezais do Brasil, Itajaí, SC, Brasil. [ Links ]
Boschi, E.E. (2000) - Species of decapod crustaceans and their distribution in the American marine zoogeographic provinces. Revista de Investigación y Desarrollo Pesquero(ISSN: 0325-6375), 13:7-136, INIDEP, Mar del Plata, Argentina. Disponível on-line em http://www.oceandocs.net/bitstream/1834/2606/1/ Rev Invest INIDEP 13.pdf [ Links ]
Botto, F.; Iribarne, O. (2000) - Contrasting effect of two burrowing crabs (Chasmagnathusgranulata and Uca uruguayensis) on sediment composition and transport in estuarine environments.Estuarine, Coastal and Shelf Science, 51(2):141-151. DOI: 10.1006/ecss.2000.0642 [ Links ]
Branco, J.O. (1990) - Aspectos ecológicos dos Brachyura (Crustacea: Decapoda) no manguezal do Itacorubi, SC-Brasil. Revista Brasileira de Zoologia(ISSN: 0101-8175), 7(1):165-179, Sociedade Brasileira de Zoologia, Curitiba, PR, Brasil.Disponível on-line em http://www.scielo.br/pdf/rbzool/v7n1-2/v7n1,2a16.pdf [ Links ]
Branco, J.O.; Freitas-Júnior, F.; Fracasso, H.A.A.; Barbieri, E. (2011) - Biodiversidade no estuário do Saco da Fazenda, Itajaí-SC. O Mundo da Saúde(ISSN: 1980-3990), 35:31-41, Centro Universitário São Camilo, São Paulo, SP, Brasil. Disponível on-line em http://bvsms.saude.gov.br/bvs/artigos/biodiversidade_ estuario_saco_fazenda_itajai.pdf [ Links ]
Burggren, W.W.; McMahon, B.R. (1988) - Biology of the land crabs.479p., Cambridge University Press, Cambridge, U.K. ISBN: 978-0521112925. [ Links ]
Calado, T.C.; Sousa, E.C. (2003) - Crustáceos do Complexo Estuarino-Lagunar Mundaú/Manguaba, Alagoas. 116p., FAPEAL, Maceió, AL, Brasil. ISBN: 978-8589619011. [ Links ]
Calder, D.R.; Maÿal, E.M. (1998) - Dry season distribution of hydroids in a small tropical estuary, Pernambuco, Brazil.Zoologische Verhandelingen(ISSN: 0024-1652), 323:69-78, Rijksmuseum van Natuurlijke Historie, Leiden, Holanda. Disponível on-line em http://dare.uva.nl/cgi/arno/show.cgi?fid=148902 [ Links ]
Carmo, T.M.S. (1987) - Os manguezais ao Norte da Baía de Vitória, Espírito Santo. Publicações ACIESP, 54(1):173-194, Academia de Ciências do Estado de São Paulo, São Paulo, SP, Brasil. [ Links ]
Carvalho, F.L.; Couto, E.C.G. (2011) - Environmental variables influencing the Callinectes(Crustacea: Brachyura: Portunidae) species distribution in a tropical estuary-Cachoeira River (Bahia, Brazil). Journal of the Marine Biological Association of the United Kingdom,91(4):793-800. DOI: 10.1017/S0025315410001700 [ Links ]
Castiglioni, D.S.; Almeida, A.O.; Bezerra, L.E.A. (2011) - More common than reported: range extension, size–frequency and sex-ratio of Uca (Minuca) victoriana (Crustacea: Ocypodidae) in tropical mangroves, Brazil. Marine Biodiversity Records, 3(e94):8p. DOI: 10.1017/S1755267210000874
Castiglioni, D.S.; Silva-Castiglioni, D.; Oliveira, P.J.A. (2013) - Biologia reprodutiva de Ucides cordatus (Linnaeus, 1763) (Crustacea, Brachyura, Ucididae) em duas áreas de manguezal do litoral sul do Estado de Pernambuco, Brasil. Revista da Gestão Costeira Integrada, 13(4):433-444. DOI: 10.5894/rgci400 [ Links ]
Clarke, K.R. (1993) - Non-parametric multivariate analyses of changes in community structure. Australian Journal of Ecology(ISSN: 0307-692X), 18:117-143, Ecological Society of Australia, Windsor, Austrália. Disponível on-line em http://stat.wvu.edu/~gmerovic/WMAN633_Clarke_1993.pdf [ Links ]
Cobo, V.J.; Fransozo, A.; Mantelatto, F.L.M.; Pinheiro, M.A.A.; Santos, S.; Góes, J.M. (1993) - Composição dos braquiúros (Crustacea, Decapoda) no manguezal formado pelos rios Comprido e Escuro, Ubatura, SP. Publicações ACIESP, 87(1):146-150, Academia de Ciências do Estado de São Paulo, São Paulo, SP, Brasil. [ Links ]
Coelho-Filho, P.A.; Coelho, P.A. (1997) - Estudo sobre a família Eriphiidae no Brasil (Crustacea - Decapoda - Brachyura). Trabalhos Oceanográficos da UFPE, 25:195-203, Universidade Federal de Pernambuco, Recife, PE, Brasil.Disponível on-line em http://www.revista.ufpe.br/tropicaloceanography/artigos_completos_resumos_t_d/25_1997_coelho_filho.pdf [ Links ]
Coelho-Santos, M.A.; Coelho, P.A. (2001) - Crustacea Decapoda of the Paripe river estuary, Pernambuco, Brazil. Hydrobiologia, 449(1-3):77-79. DOI: 10.1023/A:1017536902549 [ Links ]
Coelho, P.A. (1963/64) - Distribuição dos crustáceos decápodos na área de Barra das Jangadas. Trabalhos do Instituto Oceanográfico da UFPE (ISSN: 1679-3013), 5/6:159-173, Universidade Federal de Pernambuco, Recife, PE, Brasil. Disponível on-line em http://www.revista.ufpe.br/tropicaloceanography/artigos_completos_resumos_t_d/5_6_1966_coelho 3..pdf [ Links ]
Coelho, P.A. (1965/66) - Os crustáceos decápodos de alguns manguezais de Pernambuco. Trabalhos do Instituto Oceanográfico da UFPE (ISSN: 1679-3013), 7/8: 71-90, Universidade Federal de Pernambuco, Recife, PE, Brasil.
Disponível on-line em http://www.revista.ufpe.br/tropical oceanography/artigos_completos_resumos_t_d/7_8_1965_1966_coelho_2.pdf
Coelho, P.A.; Coelho-Santos, M.A. (1990) - Crustáceos decápodos e estomatópodos do rio Paripe, Itamaracá-PE. Anais da Sociedade Nordestina de Zoologia, 3:43-61, Sociedade Nordestina de Zoologia, Maceió, AL, Brasil. [ Links ]
Coelho, P.A.; Ramos-Porto, M. (1995) - Crustáceos da região de Tamandaré, estado de Pernambuco, Brasil. Boletim Técnico Científico do CEPENE(ISSN: 0104-6411), 3(1):56-80, CEPENE, Tamandaré, PE, Brasil. Disponível on-line em http://www4.icmbio.gov.br/cepene/modulos/boletim/visualiza.php?id_arq=14 [ Links ]
Coelho, P.A.; Ramos, M.A. (1972) - A constituição e a distribuição da fauna de decápodos do litoral leste da América do Sul entre as latitudes 5o N e 39o S. Trabalhos Oceanográficos da UFPE, 13:133-236, Universidade Federal de Pernambuco, Recife, PE, Brasil. Disponível on-line em http://www.revista.ufpe.br/tropicaloceanography/artigos_completos_resumos_t_d/13_1972_coelho_3.pdf [ Links ]
Colpo, K.D.; Chacur, M.M.; Guimarães, F.J.; Negreiros-Fransozo, M.L. (2011) - Subtropical Brazilian mangroves as a refuge of crab (Decapoda: Brachyura) diversity. Biodiversity Conservation, 20(13):3239-3250. DOI: 10.1007/s10531-011-0125-x [ Links ]
CPRH. (1999) - Diagnóstico sócio-ambiental e ZEEC - Zoneamento Ecológico Econômico Costeiro Litoral sul de Pernambuco. 91p. Companhia Pernambucana do Meio Ambiente/GERCO, Recife, PE, Brasil. Disponível on-line em http://www.cprh.pe.gov.br/central_servicos/centro_documentacao_informacao_ambiental/central_downloads/39749;34001;020709;0;0.asp [ Links ]
CPRH. (2001) - Diagnóstico Sócio-Ambiental do litoral norte de Pernambuco. 211p, Companhia Pernambucana do Meio Ambiente/GERCO, Recife, PE, Brasil. Disponível on-line em http://www.cprh.pe.gov.br/central_servicos/centro_documentacao_informacao_ambiental/central_downloads/39749;34001;020709;0;0.asp [ Links ]
Crane, J. (1975) - Fiddler crabs of the world. Ocypodidae: genus Uca. 736p., Princeton University Press, New Jersey, EUA. ISBN: 978-0691081021. [ Links ]
Ferreira, A.C.; Pimenta, H.C.D. (2005) - Recuperação e valorização das nascentes do Rio Jaguaribe em Natal/RN. Anais do 23º Congresso Brasileiro de Engenharia Sanitária e Ambiental,13p., Associação Brasileira de Engenharia Sanitária e Ambiental, Rio de Janeiro, RJ, Brasil. Disponível on-line em http://www.bvsde.paho.org/bvsacd/abes23/IV-058.pdf [ Links ]
Ferreira, A.C.; Sankarankutty, C. (2002) - Estuarine carcinofauna (Decapoda) of Rio Grande do Norte, Brazil. Nauplius(ISSN 0104-6497), 10(2):121-129, Sociedade Brasileira de Carcinologia, Cruz das Almas, BA, Brasil. Disponível on-line em http://www.crustacea.org.br/wp-content/uploads/2014/02/nauplius-v10n2a04.FerreiraSankarankutty.pdf [ Links ]
Grego, C.K.S.; Feitosa, F.A.N.; Silva, M.H.; Cunha, M.G.G.S.; Nascimento-Filho, G.A. (2009) - Fitoplâncton do ecossistema estuarino do Rio Ariquindá (Tamandaré, Pernambuco, Brasil): variáveis ambientais, biomassa e produtividade primária. Atlântica(ISSN: 2236-7586), 31(2):183-198, FURG, Rio Grande, RS, Brasil. Disponível on-line em http://www.seer.furg.br/atlantica/article/viewFile/1544/682 [ Links ]
IBAMA. (1989) - Unidades de conservação do Brasil. Parques Nacionais e Reservas Biológicas.pp.151-153., Instituto Brasileiro do Meio Ambiente e dos Recursos Naturais Renováveis, Brasília, DF, Brasil. [ Links ]
Jones, D.A. (1984) - Crabs of the mangal ecosystem. In: F. D. Por & I. Dor (org.), Hydrobiology of the mangal, pp.89-109, W. Junk Publishers, Boston, MA, U.S.A. ISBN: 978-9061937715. [ Links ]
Kristensen, E.; Alongi, D.M. (2006) - Control by fiddler crabs (Uca vocans) and plant roots (Avicennia marina) on carbon, iron and sulfur biogeochemistry in mangrove sediment.Limnology and Oceanography(ISSN: 0024-3590), 51:1557-1571, ASLO, Waco, TX, EUA. Disponível on-line em http://aslo.org/lo/ toc/vol_51/issue_4/1557.pdf [ Links ]
Kristensen, K. (2008) - Mangrove crabs as ecossystems engineers; with emphasis on sediment process. Journal of Sea Research (ISSN: 1385-1101), 59:30-43, NIOZ Royal Netherlands Institute for Sea Research, Texel, Holanda. Disponível on-line em http://www.researchgate.net/publication/222563452_Mangrove_crabs_as_ecosystem_engineers_with_emphasis_on_sediment_processes/file/d912f51275c19d555d.pdf [ Links ]
Laegdsgaard, P.; Johnson, C.R. (1995) - Mangrove habitats as nurseries: unique assemblages of juvenile fish in subtropical mangroves in eastern Australia. Marine Ecology Progress Series(ISSN: 0171-8630), 126:67-81, John Wiley & Sons, Oldendorf, Alemanha. Disponível on-line em http://eprints.utas.edu.au/ 1262/1/laegdsgaard-johnson.pdf [ Links ]
Macintosh, D.J. (1984) - Ecology and productivity of Malaysian mangrove crab populations (Decapoda: Brachyura). Proceedings of the Asian Symposium on Mangrove Environment - Research and Management, 354-377, Universiti Malaya, Kuala Lumpur, Malaysia. [ Links ]
Macintosh, D.J.; Ashton, E.C.; Havanon, S. (2002) - Mangrove rehabilitation and intertidal biodiversity: a study in the Ranong mangrove ecosystem, Thailand. Estuarine, Coastal and Shelf Science, 55(3):331-345. DOI: 10.1006/ecss.2001.0896 [ Links ]
Maida, M.; Ferreira, B.P. (1997) - Coral reefs of Brazil: an overview. Proceedings of the 8th International Coral Reef Symposium, 1:263-274. ISBN: 978-0935868906. [ Links ]
Margalef, R. (1958) - Information theory in ecology. Society for General Systems Research (ISSN: 0072-0798), 3:36-71, International Society for the Systems Sciences, Pocklington, Reino Unido. [ Links ]
Margalef, R. (1963) - On certain unifying principles in ecology. American Naturalist (ISSN: 0003-0147),97:357-374, American Society of Naturalists, Chicago, EUA.Article Stable URL: http://www.jstor.org/stable/2459227 [ Links ]
Masunari, S.; Dissenha, N. (2005) - Alometria no crescimento de Uca mordax(Smith) (Crustacea, Decapoda, Ocypodidae) na Baía de Guaratuba, Paraná, Brasil. Revista Brasileira de Zoologia(ISSN: 0101-8175), 22(4):984-990, Sociedade Brasileira de Zoologia, Curitiba, PR, Brasil. Disponível on-line em http://www.scielo.br/pdf/rbzool/v22n4/a26v22n4.pdf [ Links ]
Melo, G.A.S. (1996) - Manual de identificação dos Brachyura (caranguejos, siris) do litoral brasileiro. 604p., Plêiade / FAPESP, São Paulo, SP, Brasil. ISBN: 978-8515025909. [ Links ]
Nagelkerken, I.; Blaber, S.J.M.; Bouillon, S.; Green, P.; Haywood, M.; Kirton, L.G.; Meynecke, J.O.; Pawlik, J.; Penrose, H.M.; Sasekumar, A.; Somerfield, P.J. (2008) - The habitat function of mangroves for terrestrial and marine fauna: a review. Aquatic Botany(ISSN: 0304-3770), 89:155-185, Elsevier, Amsterdã, Holanda. Disponível on-line em https://lirias.kuleuven.be/bitstream/123456789/203707/1/Nagelkerken_et_al_2008.pdf [ Links ]
Ng, P.K.L.; Guinot, D.; Davie, P.J.F. (2008) - Systema Brachyurorum: Part I. An annotated checklist of extant brachyurans crabs of the world. The Raffles Bulletin of Zoology (ISSN: 0217-2445), 17:1-286, Lee Kong Chian Natural History Museum, Singapura, Singapura. Disponível on-line em http://www.vliz.be/imisdocs/publications/133883.pdf [ Links ]
Oliveira, L.P.H. (1939) - Contribuição ao conhecimento dos crustáceos do Rio de Janeiro. Gênero Uca(Decapoda: Ocypodidae). Memórias do Instituto Oswaldo Cruz(ISSN: 0074-0276), 34(1):115-148, Instituto Oswaldo Cruz, Ministério da Saúde, Rio de Janeiro, RJ, Brasil. Disponível on-line em http://www.scielo.br/pdf/mioc/v34n1/tomo34(f1)_115-148.pdf [ Links ]
Oshiro, L.M.Y.; Silva, R.; Silva, Z.S. (1998) - Composição da fauna de braquiúros (Crustacea; Decapoda) dos manguezais da Baía de Sepetiba-RJ. Nauplius(ISSN: 0104-6497),, 6:31-40, Sociedade Brasileira de Carcinologia, Cruz das Almas, BA, Brasil. Disponível on-line em http://www.crustacea.org.br/wp-content/uploads/2014/02/nauplius-v06n1a05.Oshiro.et_.al_.pdf [ Links ]
Pielou, E.C. (1969) - An introduction to mathematical ecology. 286p., Wiley Interscience, New York, NY, U.S.A. ISBN: 0471689181. [ Links ]
Rodrigues, A.M.T.; Pereira, M.T.; Wegner, P.Z.; Branco, J.O.; Clezar, L.; Silva, M.H.; Sierra, E.J.S. (1994) - Manguezal do Rio Camboriú: preservação e controle da qualidade ambiental. 65p., IBAMA/CEPSUL, Itajaí, SC, Brasil. [ Links ]
Santos, M.C.F.; Botelho, E.R.O.; Ivo, C.T.C. (2001) - Biologia populacional e manejo da pesca de aratu, Goniopsis cruentata(Latreille, 1803) (Crustacea: Decapoda: Grapsidae) no litoral Sul de Pernambuco-Brasil. Boletim Técnico Científico do CEPENE(ISSN: 0104-6411),9(1):87-123, CEPENE, Tamandaré, PE, Brasil. Disponível on-line em http://www4.icmbio.gov.br/cepene/index.php?id_menu=51&arquivo=modulos/boletim/res.php&id_arq=72 [ Links ]
Schaeffer-Novelli, Y. (ed.) (1995) - Manguezal, ecossistema entre a terra e o mar. 64p., Caribbean Ecological Research, São Paulo, SP, Brasil. [ Links ]
Schaeffer-Novelli, Y. (1999) - Grupo de ecossistemas: manguezal, marisma e apicum. 119p., PRONABIO/PROBIO, São Paulo, SP, Brasil. Disponível on-line em http://www.anp.gov.br/brnd/round5/round5/guias/perfuracao/5round/refere/manguezal_marisma_apicum.pdf [ Links ]
Schubart, C.D.; Neigel, J.E.; Felder, D.L. (2000) - Molecular phylogeny of mud crabs (Brachyura: Panopeidae) from the northwestern Atlantic and the role of morphological stasis and convergence.Marine Biology(ISSN: 1432-1793),137(1): 11-18, Springer, Kiel, Alemanha. Disponível on-line em http://www.uni-regensburg.de/Fakultaeten/nat_Fak_III/Zoologie/Heinze/Staff/ChristophSchubart/pdf/MarBiol-2000.pdf [ Links ]
Shannon, C.E. (1948) - A mathematical theory of communication. The Bell System Technical Journal(ISSN: 1538-7305), 27:379-423, American Telephone and Telegraph Co., Nova Iorque, NY, U.S.A. Disponível on-line em http://www.enseignement.polytechnique.fr/informatique/profs/Nicolas.Sendrier/X02/TI/shannon.pdf [ Links ]
Simpson, E.H. (1949) - Measurement of diversity. Nature,163(4148):688. DOI: 10.1038/163688a0 [ Links ]
Simpson, G.G. (1964) - Species density of North American recent mammals. Systematic Zoology(ISSN: 0039-7989), Oxford University Press, Oxford, Reino Unido, 13:57-73. Disponível on-line em http://biology.unm.edu/jhbrown/Documents/511 Readings/Simpson1964.pdf [ Links ]
Tan, C.G.; Ng, P.K. (1994) - An annotated checklist of mangrove brachyuran crabs from Malaysia and Singapore.Hydrobiologia, 285(1):75-84. DOI: 10.1007/BF00005655 [ Links ]
Thurman, C.L. (1987) - Fiddler Crabs (Genus Uca) of Eastern Mexico (Decapoda, Brachyura, Ocypodidae). Crustaceana (ISSN: 0011-216x), 53(1):94-105, Brill, Bedfordshire, Reino Unido. Disponível on-line em http://www.jstor.org/ stable/20104280 [ Links ]
Thurman, C.L. (2002) - Osmoregulation in six sympatric fiddler crabs (genus Uca) from the Northwestern Gulf of Mexico. MarineEcology, 23(4):269-284. DOI: 10.1046/j.1439-0485.2002.02785.x [ Links ]
Vergara-Filho, W.L.; Alves, J.R.P. (1994) - Composição e distribuição dos caranguejos (Crustacea, Decapoda, Brachyura) em manguezais impactados da Baía da Guanabara. II-Manguezal do rio Iguaçú, Duque de Caxias, Rio de Janeiro. Publicações da ACIESP, 87(1):151-156, Academia de Ciências do Estado de São Paulo, São Paulo, SP, Brasil. [ Links ]
von Hagen, H.O. (1982) - Visual and acoustic display in Uca mordax and U. burgersi, sibling species of neotropical fiddler crabs. I. Waving display. Behaviour(ISSN: 0005-7959), 83(3):229-250, Brill, Atlanta, GA, EUA. Disponível on-line em http://www.jstor.org/stable/4534228 [ Links ]
von Prahl, H.; Cantera, J.R. & Contreras, R. (1990) - Manglares y hombres del Pacífico Colombiano. 193p., Folio Ltd., Santafé de Bogotá, Colombia, ISBN: 9589129099. [ Links ]
Zar, J.H. (1996) -Biostatistical analysis. 663p., Prentice Hall, Upper Saddle River, NJ, EUA. ISBN: 013081542X. [ Links ]
*Submission: 21 JAN 2014; Peer review: 20 MAR 2014; Revised: 22 JUN 2014; Accepted: 22 JUN 2014; Available on-line: 16 SET 2014
Anexo
1 O artigo “Diversidade e distribuição dos Crustacea Brachyura dos manguezais dos rios Ariquindá e Mamucabas, litoral sul de Pernambuco, Brasil”, de Araújo et al. (2014), tem informação de suporte disponível on-line em http://www.aprh.pt/rgci/rgci-493_Araujo_SuplMat
This article contains supporting information online at http://www.aprh.pt/rgci/rgci-493_Araujo_SuplMat














