Introdução
Nos países desenvolvidos, o aumento da esperança média de vida tem sido acompanhado por um incremento das doenças limitadoras da vida (cancro, insuficiências de órgão, doenças neurodegenerativas, etc.) e das doenças crónicas, como a hipertensão arterial, a diabetes mellitus, a dislipidemia, as perturbações da ansiedade e da depressão, entre outras. Todas estas doenças crónicas, progressivas e/ou incuráveis, isoladamente ou em associação, cursam com complexidade,1-4 polimedicação e sobrecarga terapêutica.5
Nos indivíduos com doenças crónicas é possível haver prescrição, por um lado, de medicamentos para tratar e/ou prevenir exacerbações e comorbilidades; por outro, de medicamentos para controlar os sintomas associados à patologia e à progressão clínica.6-7 Neste contexto, a polimedicação é um cenário frequente, existindo um aumento de medicação potencialmente inapropriada (MPI) e outras consequências negativas.5,8-10
A MPI engloba a medicação que é prescrita: i) sem indicação clínica ou com indicação errada; ii) por períodos demasiado curtos ou longos; iii) em doses incorretas; iv) com um elevado risco de reações adversas medicamentosas (RAM), incluindo interações medicamentosas (IMED); v) com custo acrescido para o serviço de saúde.1-3
Nas doenças avançadas e irreversíveis também podem considerar-se MPI os fármacos utilizados para prevenção primária, secundária ou aqueles sem benefício a curto prazo, uma vez que a esperança de vida de muitos doentes é limitada, mormente se for considerado o tempo necessário para existir benefício clínico e a referenciação tardia para as equipas de cuidados paliativos (CP).1
Para a deteção da MPI existem várias ferramentas disponíveis, sendo a STOPPFrail (Screening Tool of Older Persons Prescriptions in Frail adults with limited life expectancy) uma das mais recentes. Esta ferramenta congrega 27 critérios que foram desenvolvidos com base na necessidade de identificar a MPI num grupo de pessoas com complexidade crescente.11-12
São escassos os estudos que abordam a prevalência da MPI nos doentes seguidos na comunidade por equipas de CP, sendo raramente utilizada a STOPPFrail. É relevante aprofundar o conhecimento sobre esta realidade no contexto comunitário para que se possam desenvolver estratégias de redução da MPI e das suas potenciais consequências negativas.
O objetivo deste estudo foi determinar a prevalência da MPI e o número de IMED em idosos, acompanhados por equipas domiciliárias de CP, durante os últimos doze meses de vida.
Material e métodos
Estudo quantitativo, descritivo, observacional e retrospetivo. A amostra foi de conveniência, constituída por doentes com ≥ 65 anos que faleceram entre 1 de janeiro de 2016 e 31 de dezembro de 2018 e que eram acompanhados por uma Equipa Comunitária de Suporte em Cuidados Paliativos da Região Autónoma dos Açores.
Foram registados dados individuais relativos a: idade, género, lista de problemas de saúde, medicação prescrita nos últimos doze meses de vida. Foi usada a classificação internacional das doenças do ICD-10-CM.13
Todos os medicamentos foram agrupados segundo a classificação farmacocinética que consta do Prontuário Terapêutico da Autoridade Nacional do Medicamento e Produtos de Saúde, vulgo Infarmed®.14
Para identificar a MPI foram utilizados os 27 critérios da STOPPFrail.11-12 Para identificar as IMED foi usado o programa Lexi-interact® (Lexi-Comp©, Inc., Hudson, Ohio, EUA). Segundo este, existem cinco níveis de IMED: os níveis X, D e C dizem respeito a IMED que poderão ser clinicamente significativas, ditas «potenciais»; o nível B congrega as IMED sem impacto clínico, não sendo necessária qualquer ação clínica; o nível A significa que não há IMED conhecidas.
A análise descritiva dos dados foi feita com o programa IBM SPSS Statistics® v. 26.0 (IBM Corporation©, Armonk, NY, EUA). Os dados qualitativos foram apresentados com frequências e percentagens; os dados quantitativos com medianas e amplitudes interquartis (AIQ).
O estudo foi aprovado pela Comissão de Ética do Centro Académico de Medicina de Lisboa e pela Comissão de Ética da Unidade de Saúde da Ilha Terceira.
Resultados
Resultados gerais
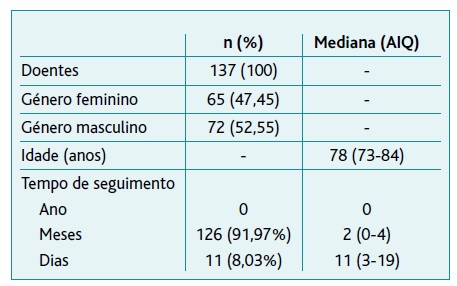
A amostra foi de 137 doentes, sendo 72 homens (52,55%) com idade mediana de 78 anos. A maioria (91,97%) dos doentes teve um acompanhamento de < 12 meses, com uma mediana de dois meses (Tabela 1).
Foram classificados 591 problemas de saúde, com mediana de quatro por doente (AIQ 3-6), 217 doenças limitadoras de vida e 374 comorbilidades. Das doenças limitadoras de vida, 58,06% (n=126) foram neoplasias, sobretudo do sistema digestivo (35,71%, n=45). A maioria das comorbilidades foi do sistema circulatório (86,13%, n=118) e doenças endócrinas (81,75%, n=112).
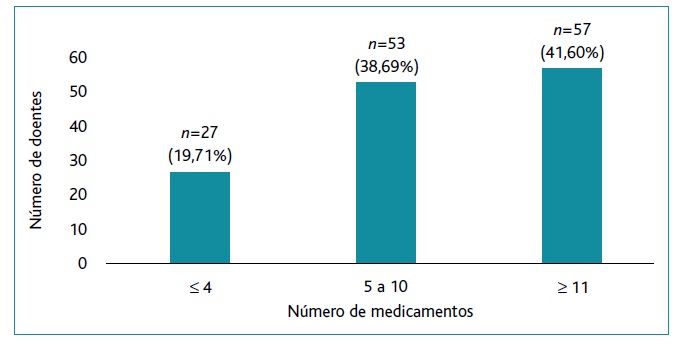
Foram prescritos 1.127 fármacos, com uma mediana de oito fármacos/doente (AIQ 5-10,5). A maioria dos doentes (80,29%) teve prescritos ≥ cinco medicamentos (Figura 1). Os medicamentos mais prescritos foram: opioides (48,18%, n=66), ansiolíticos (48,18%, n=66) e inibidores da bomba de protões (IBP) (45,98%, n=63).
Do total de medicamentos prescritos não se encontrou evidência clínica clara para 131 prescrições (11,62%).
Medicação potencialmente inapropriada
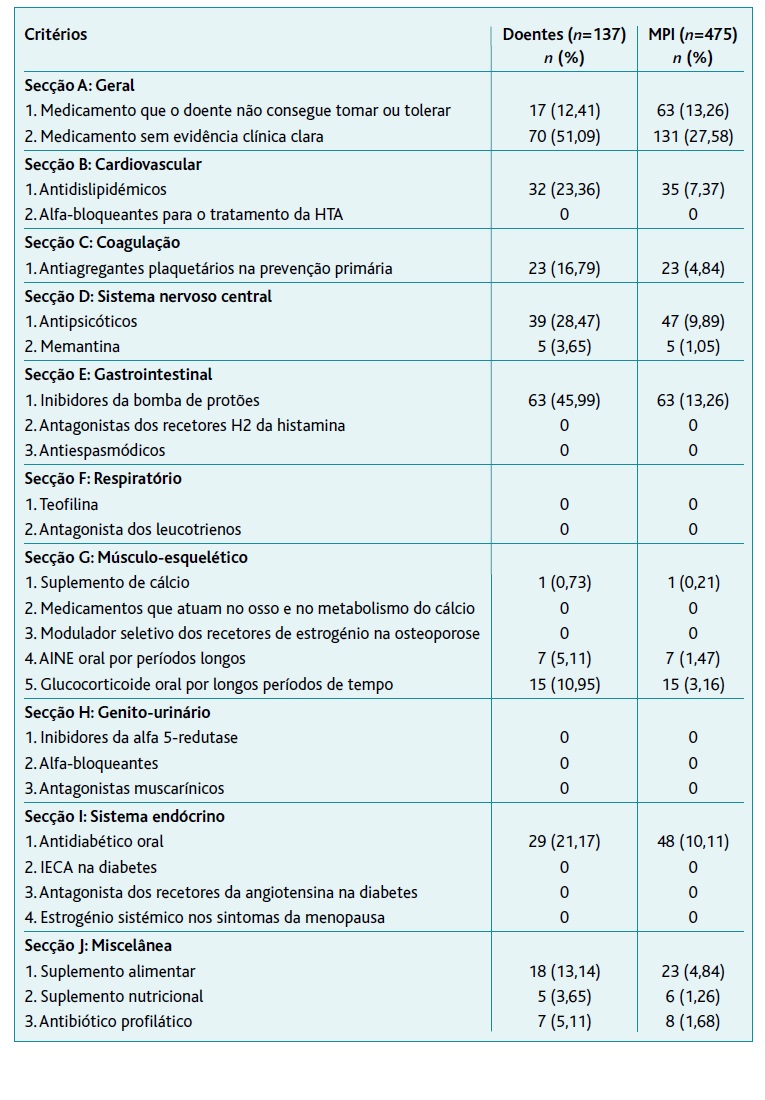
A prescrição de MPI envolveu 475 fármacos e ocorreu em 124 idosos (90,51%). Destes, 101 (81,45%) reuniram ≥ dois critérios (mediana de quatro critérios, AIQ 1-5). Os critérios mais identificados foram o «A2: Medicamento sem evidência clínica clara» em 70 doentes (51,09%) e o «E1: Inibidores da Bomba de Protões» em 63 doentes (45,99%). Dos 27 critérios, 13 não foram reportados (Tabela 2).
Metade da MPI foi representada por: IBP (13,26%, n=63), antidiabéticos orais (10,11%, n=48), antipsicóticos (9,89%, n=47), antidislipidémicos (7,37%, n=35, sendo 31 estatinas), antiagregantes plaquetários na prevenção primária (4,84%, n=23) e suplementos alimentares (4,84%, n=23, sendo todos vitamínicos) (Tabela 2).
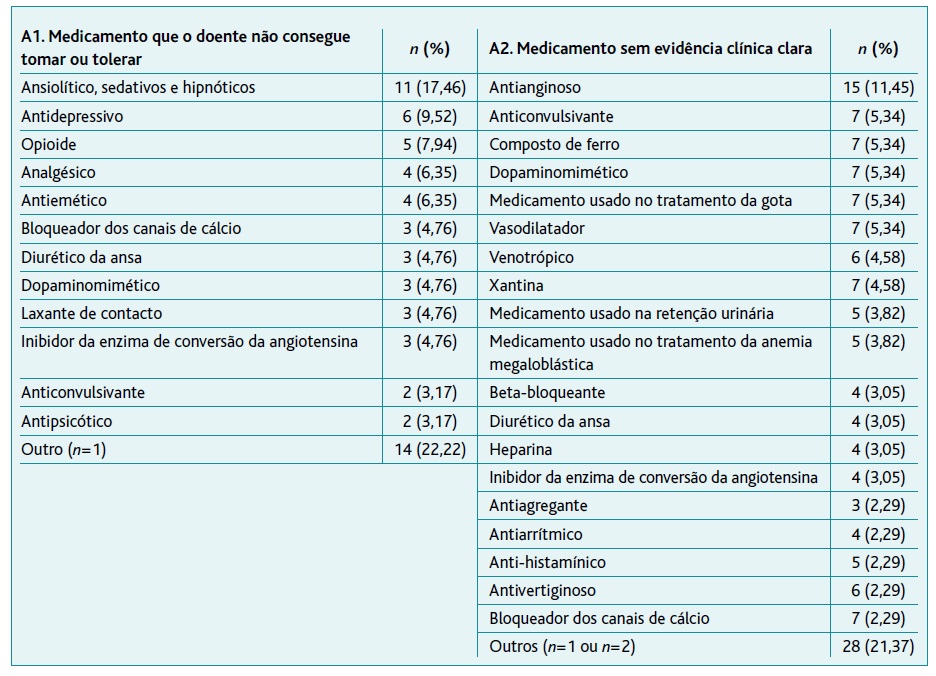
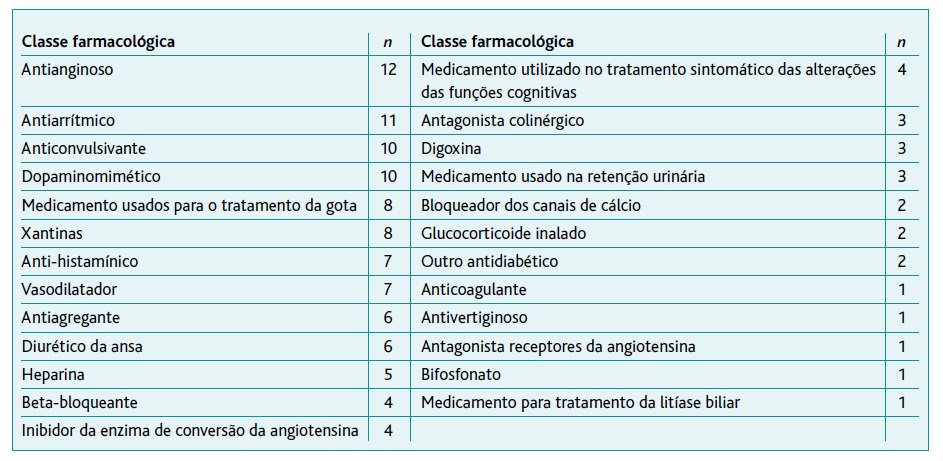
Dos medicamentos que os doentes não conseguiram tomar ou tolerar (critério A1) destacam-se: ansiolíticos, sedativos e hipnóticos (17,46%, n=11); antidepressivos (9,52%, n=6) e opioides (7,94%, n=5). Dos medicamentos sem evidência clínica clara (critério A2), os mais frequentes foram: antianginosos, anticonvulsivantes, compostos de ferro, dopaminomiméticos, anti-gotosos e vasodilatadores (Tabela 3).
Interações medicamentosas
Houve 1.107 IMED em 120 doentes (87,59%). Em 117 doentes (85,40%) foram registadas 1.011 potenciais IMED (91,33%). Apenas três doentes tiveram IMED sem impacto clínico (nível B). A maioria das IMED foi de nível C (70,91%) e de nível D (18,52%), existindo em 112 doentes (81,75%) e 74 doentes (54,01%), respetivamente. A IMED potencial mais rara foi do nível X (1,90%) em 14 doentes (10,22%) (Tabela 4).
TABELA 4 Distribuição dos 120 doentes que registaram interações medicamentosas (Parte A) e distribuição da globalidade das 1.107 interações medicamentosas (Parte B)
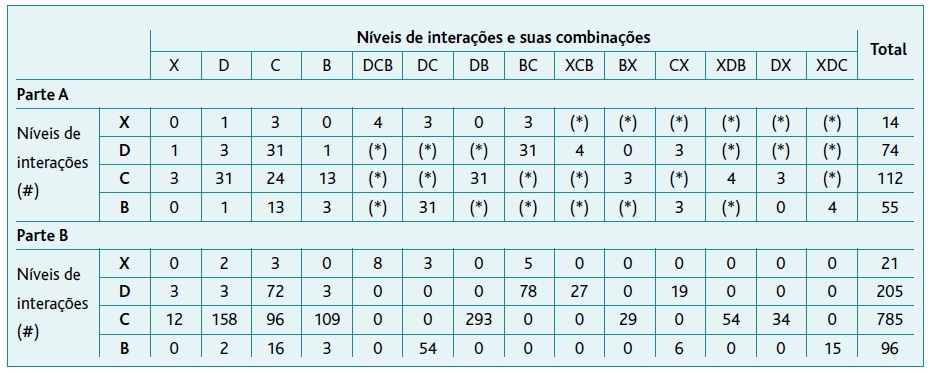
A MPI esteve envolvida nas IMED de 98 doentes (71,53%) e em 473 de todas as potenciais IMED (46,79%), sendo 371 do nível C, 90 do nível D e 12 do nível X. Dos 117 doentes com potenciais IMED, a MPI mais frequente esteve representada por medicação sem evidência clínica clara (critério A2) em 45 doentes (38,46%) e antipsicóticos (critério D1) em 38 doentes (32,48%).
Os medicamentos sem evidência clínica clara (critério A2) foram encontrados em 122 das potenciais IMED (12,07%) sendo que, em aproximadamente um terço destes casos, as classes farmacológicas mais frequentes foram: antianginosos, anticonvulsivantes, antiarrítmicos e dopaminomiméticos (Tabela 5).
Discussão
Nos últimos doze meses de vida de idosos seguidos por equipas de CP verificou-se que em cada dez doentes: nove tiveram MPI, cinco tiveram prescrições sem evidência clínica clara, quatro tomaram um IBP, oito tiveram IMED. A MPI esteve envolvida nas IMED de sete em cada dez doentes. A MPI representou quase metade das IMED clinicamente significativas.
Medicação potencialmente inapropriada
A prevalência de 90,51% da MPI foi bastante superior à encontrada noutros estudos - de 16% a 88,5% - realizados no âmbito dos CP, quer na comunidade quer no hospital.8,10,12,15-22 Estas variações devem-se aos diferentes métodos usados nas investigações, mormente em relação a: seleção dos doentes; tipo de doença em causa; tipologia dos cuidados (primário, secundário ou terciário); critérios para identificar a MPI; momento da trajetória da doença; seguimento e tratamento dos doentes por diferentes profissionais de saúde; tempo de seguimento em CP; expectativas e preferências dos doentes; entre outros métodos.
A ferramenta STOPPFrail, além de apoiar a prescrição de medicamentos em doentes com esperança de vida limitada, é fácil de usar, de tamanho curto, organizada por sistemas, eficiente em termos de tempo e, portanto, mais viável de implementar na prática clínica diária.23 Estudos recentes que usaram a STOPPFrail mostraram uma prevalência de MPI de 67% a 80%, o que pode indicar uma boa adaptação da ferramenta aos doentes em CP e suas medicações.12 A STOPPFrail, como outras ferramentas, deve funcionar como guia, quer no momento de início quer de continuação da medicação, não devendo excluir, nem substituir, uma avaliação clínica global, que é essencial para determinar a MPI.
Têm sido associados ao aumento da MPI alguns elementos clínicos e sociodemográficos, nomeadamente: idade avançada, género feminino, insónia, perturbações da ansiedade, síndroma depressivo, quedas, dor e deterioração cognitiva.16 No entanto, o uso do STOPPFrail não revelou diferenças de MPI em função de: género, síndromas geriátricos, comorbilidades e tipo de doença que necessita de CP.18
A maioria dos estudos, abordando a MPI em CP, foi realizada em contexto hospitalar. O internamento hospitalar está normalmente associado a uma agudização do estado geral, pelo que é de esperar que haja um aumento de medicação para controlo sintomático, sendo assim explicadas as elevadas prevalências de MPI, de 80% a 88%.12,16,19 São necessários mais estudos que envolvam outros contextos para além do hospitalar.
Um dos fatores de risco para a MPI é a polimedicação.18,24 Esta é geralmente abordada numa perspetiva numérica, sem ter em conta as classes farmacológicas envolvidas, os estados da doença e as comorbilidades. Isto dificulta a avaliação da segurança e adequação da medicação ao contexto clínico, condicionando a comparação da polimedicação apropriada versus inapropriada.24 Por conseguinte, a polimedicação deve ser vista de modo crítico, podendo ser apropriada nos idosos com multimorbilidade sempre que: 1) seja aplicada uma abordagem holística no ato da prescrição; 2) o uso da medicação seja otimizado e a medicação prescrita de acordo com a melhor evidência; 3) seja questionando o benefício pretendido com o tratamento, com o objetivo de melhorar a qualidade de vida.25-28
Nas doenças crónicas, à medida que ocorre a progressão clínica e se aproxima o fim de vida (FDV), a prioridade médica deve concentrar-se no controlo do sofrimento evitável e na garantia da melhor qualidade de vida. Este facto pode explicar o aumento do número de medicamentos que se observa no FDV, em que a taxa de doentes a tomar ≥ 10 medicamentos/dia passa de 30,2% para 47,2% no último mês de vida.29 Este aumento observa-se em várias classes farmacológicas, muitas delas fundamentais nos serviços de CP, como antipsicóticos, ansiolíticos, opioides, glucocorticoides, antieméticos e laxantes.17,29-32 Neste estudo, as classes farmacológicas mais prescritas foram: ansiolíticos (48,18%), opioides (48,18%) e IBP (45,98%). Os opioides corresponderam a 8,96% de toda a prescrição (n=101) e os ansiolíticos a 7,01% (n=79).
A elevada prevalência de MPI documentada teve como contribuintes a medicação preventiva e aquela destinada a tratar as comorbilidades. Nas doenças crónicas em fases avançadas, quando a situação é considerada irreversível, e privilegiando o adequado controlo sintomático, deve existir uma diminuição dos fármacos modificadores da doença incurável e dos fármacos com intuito preventivo. Todavia, tal nem sempre sucede, podendo estes fármacos significar 25% da medicação dos doentes em FDV.12 A literatura indica que as classes farmacológicas mais presentes na MPI são: estatinas, antiagregantes, anti-hipertensores, vasodilatadores, antidiabéticos orais, IBP, suplementos minerais e vitamínicos, medicamentos usados no tratamento da osteoporose e gota.2,29,31,33-35 Neste estudo confirmou-se que as classes farmacológicas mais frequentes no tratamento preventivo e/ou das comorbilidades, e causadoras de MPI, foram: IBP em 45,99% (n=63), estatinas em 22,63% (n=31), antidiabéticos orais em 21,17% (n=29), antiagregantes em 19,71% (n=27) e suplementos alimentares em 13,14% dos casos (n=18). Pese embora estes dados, é sabido que existem alguns medicamentos que permitem modificar a doença, controlar as comorbilidades e assegurar o controlo sintomático, como os beta-bloqueantes (uso nas palpitações) e os antidiabéticos (uso na hiperglicemia sintomática). Destarte, é pertinente aclarar a indicação de cada medicamento do idoso, de forma a avaliar corretamente a sua adequação, evitando precocemente a MPI e as IMED.
Interações medicamentosas
As IMED podem surgir associadas à MPI, podendo contribuir para: declínio funcional e cognitivo, redução da qualidade e do tempo de vida, sobrecarga terapêutica, idas recorrentes ao serviço de urgência, hospitalização não programada e aumento dos custos em saúde.2,8-9,11,36 Neste estudo a prevalência de IMED foi de 85,40% (n=117), bastante superior à encontrada na literatura que varia de 2,69% a 75% no âmbito dos CP.37-42 O risco de IMED aumenta com o número de medicamentos, sendo de 83,30% em doentes a fazer ≥ 11 medicamentos.42
Constatou-se que 46,78% das IMED podiam considerar-se evitáveis. Na medicação crónica as classes farmacológicas consideradas como MPI, e mais frequentemente envolvidas nas IMED, são: anticoagulantes, insulina, antagonistas da dopamina e anticolinérgicos.37,40,43 Neste estudo foram os antianginosos, os antiarrítmicos, os anticonvulsivantes e os dopaminomiméticos.
O conhecimento e a compreensão dos medicamentos mais associados às IMED, os seus mecanismos de ação e os sintomas secundários podem ajudar os médicos na escolha idónea dos fármacos, na identificação precoce das IMED, na monitorização e ajuste da medicação, principalmente dos princípios ativos mais usados em CP, como a metoclopramida e o haloperidol.40
A presença de MPI, de acordo com a STOPPFrail, não mostrou ser um fator de risco para as RAM na admissão hospitalar.18 Este facto pode dever-se à circunstância de alguns medicamentos com risco elevado de RAM, ou margem terapêutica estreita (digoxina, insulina, anticoagulantes, quimioterapia, entre outros), não serem considerados nos critérios STOPPFrail.18
Medicação potencialmente inapropriada: classes farmacológicas
As classes farmacológicas responsáveis por cerca de um terço da MPI foram: IBP (13,26%), antidiabéticos orais (10,11%) e antipsicóticos (9,89%). Num estudo que também usou a STOPPFrail verificou-se o predomínio de: IBP (22,87%), antidislipidémicos (20,25%), suplementos de cálcio (14,46%) e antipsicóticos (6,61%).12 Em estudos que usaram outros critérios e outras ferramentas foram reportadas como prevalentes as classes: antidemenciais (100%), IBP (50%), anti-hipertensores (27% a 44%), antidislipidémicos (31% a 97%), medicina alternativa/complementar (31%) e bifosfonatos (27%).44-45
Medicamentos sem evidência clínica clara (critério A2)
Do total de medicamentos prescritos, 131 (11,62%) não possuíam uma evidência clínica clara, contribuindo para 27,58% da MPI. Outros estudos mostraram que 22,8% a 43,8% dos medicamentos não tinham uma indicação clínica evidente.18,38,43 Constatou-se que os medicamentos mais prescritos, embora sem evidência clínica, eram usados no tratamento de doenças crónicas, como antianginosos, anticonvulsivantes, compostos de ferro e vasodilatadores. Assim, salienta-se a necessidade de avaliar rigorosamente a situação clínica do idoso e decidir sobre o putativo benefício da medicação crónica no FDV.
Inibidores da bomba de protões: prescrição nos últimos 12 meses de vida
Os IBP foram causa de MPI em 63 doentes (45,99%). No FDV não existe um consenso em relação ao uso de IBP,25,46 havendo casos de início de prescrição nesta fase da vida.30 A elevada prevalência de utilização de IBP pode estar associada ao tratamento de sintomas como dispepsia, prevenção ou tratamento de úlceras gástricas associadas à toma de anti-inflamatórios não esteroides (em sete doentes) e administração de glucocorticoides (em 15 doentes) no FDV. No contexto dos CP, os IBP podem estar indicados na prevenção e tratamento da doença de refluxo gastro-esofágico induzida por quimioterapia, no tratamento das hemoptises e na recidiva de hemorragia digestiva em doentes com história de úlcera péptica.47
Antipsicóticos: prescrição nos últimos 12 meses de vida
Os antipsicóticos foram considerados como MPI em 39 doentes (28,47%). O seu uso nos idosos com demência é frequente, com prevalências de 27% a 30% em lares de idosos.48-49 No entanto, não existe consenso para a prescrição de antipsicóticos no FDV, havendo quem não advogue o seu uso na demência avançada49 e quem defenda que podem ser apropriados.25,46
Estatinas: prescrição nos últimos 12 meses de vida
As estatinas, para além dos IBP, representam as classes de fármacos cuja prescrição é frequentemente inapropriada no FDV,2,20uma vez que o seu benefício demora a ser alcançado. No entanto, o diagnóstico de uma doença limitadora de vida não diminui a sua desprescrição,50 com prevalências de utilização de 20,25% a 97%.12,17,21,44,50-52 Existem, porém, recomendações sobre a não prescrição destes medicamentos em doentes com esperança de vida limitada,53 com evidência sobre a segurança da sua desprescrição, culminando na melhoria da qualidade de vida e na redução de custos em saúde.54
Vantagens e limitações do estudo
A principal vantagem do estudo reside no conhecimento que possibilitou relativamente à prevalência da MPI e às IMED no contexto domiciliário, assim como na utilização de uma ferramenta recente, a STOPPFrail, em doentes vulneráveis.
Existem algumas limitações. O estudo foi realizado numa área geográfica restrita, o que limitou o tamanho da amostra, cuja seleção não foi probabilística. O estudo foi retrospetivo, pelo que os dados e as variáveis consideradas foram somente as que constavam do processo clínico dos doentes. A ausência, a não atualização ou os erros de informação dos registos podiam ter induzido um viés de informação e, consequentemente, erros de interpretação. Estes factos limitam a generalização dos resultados.
Ademais, não foram avaliados o estado funcional ou a fragilidade dos doentes, que consubstancializam aspetos fundamentais na tomada de decisão terapêutica e na análise da adequação da medicação prescrita.
Os doentes com < 65 anos foram excluídos do estudo, uma vez que tal era conveniente para aplicar os critérios STOPPFrail. Esta ferramenta não está validada para a população Portuguesa. Além disso, a STOPPFrail é recente, pelo que a comparação com outras ferramentas não pode ocorrer de modo simplista, por existirem diferenças nos critérios e nos limites de idade, não sendo valorizados alguns medicamentos de janela terapêutica estreita e responsáveis por IMED.
Algumas destas limitações poderão ser ultrapassadas com a realização de estudos prospetivos, procurando respostas não só em relação ao objetivo deste estudo, como também relativamente aos outcomes associados à MPI, como as IMED e as RAM.
Implicações para o futuro
O uso da ferramenta STOPPFrail pode ajudar os profissionais de saúde a identificar a MPI, independentemente da área de especialidade e da experiência profissional. O conhecimento sobre a MPI na população frágil é crucial para o desenvolvimento de novas orientações clínicas e para a implementação de guias de desprescrição e estratégias para reduzir a MPI.30