Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Revista de Ciências Agrárias
versão impressa ISSN 0871-018X
Rev. de Ciências Agrárias vol.42 no.2 Lisboa jun. 2019
https://doi.org/10.19084/rca.17183
ARTIGO
Resistência induzida ao pulgão-do-algodoeiro em cultivares de algodão colorido
Induced resistance to aphid cotton on colored cotton cultivars
Eliana Alcantra1,*, Jair Campos Moraes2, Alexander Machado Auad3, Alex Antônio Silva4 e Roberta Alvarenga2
1 Universidade Vale do Rio Verde – UninCor, Agronomia, Três Corações, Minas Gerais, Brasil
2 Universidade Federal de Lavras, Departamento de Entomologia, Lavras, Minas Gerais, Brasil
3 Embrapa - Centro Nacional de Pesquisa de Gado de Leite, Laboratório de Entomologia, Juiz de Fora, Minas Gerais, Brasil
4 Universidade Federal de Lavras, Departamento de Biologia, Lavras, Minas Gerais, Brasil
(*E-mail: prof.eliana.alcantra@unincor.edu.br; lialcantra@yahoo.com.br)
RESUMO
Objetivou-se avaliar a resistência de cultivares de algodão colorido por meio de indutores químicos. Diferentes cultivares de algodão foram plantados em vasos e mantidas em sala climatizada (temperatura diurna de 28±2oC e noturna de 25±2oC; 70±10 % de U.R. e 12 horas de fotofase). Ácido silícico ou acibenzolar-S-methyl foram aplicados nas plantas e estas foram ofertadas para o afídeo Aphis gossypii. O delineamento experimental foi em esquema fatorial envolvendo três cultivares de algodão e dois indutores de resistência com 10 repetições por tratamento. Os parâmetros biológicos observados foram mortalidade ninfal, duração do estado ninfal, períodos pré-reprodutivo, reprodutivo e pós-reprodutivo, longevidade e número total de ninfas produzidas. Os teores de fenóis e lenhina presentes nas folhas foram quantificados. Observou-se maior duração do período ninfal, menor número médio de ninfas produzidas e maior mortalidade ninfal no tratamento com ASM. O silício e ASM promoveram aumento no teor de lenhina na cv. BRS Verde. Contudo, no que se refere aos fenóis apenas o silício proporcionou aumento, na cv. BRS Verde. Assim, a aplicação de ASM afetou negativamente parâmetros biológicos de A. gossypii, por meio do aumento de lenhina nas plantas e a cv. BRS Verde se apresentou como uma melhor cultivar a ser utilizada, acumulando maiores teores de lenhina e fenóis.
Palavras-chave: acibenzolar-S-methyl, Aphis gossypii, silício.
ABSTRACT
The aim of this study was to evaluate the resistance induced by chemical inducers on cultivars of colored cotton. The cotton was planted in pots and kept in a climate-controlled room (28±2oC daytime temperature, 25±2oC night temperature, 70±10 % R.H.; and 12 hours of photoperiod). Silicon and acibenzolar-S-methyl were applied to the plants that were offered to Aphis gossypii afterwards. The bioassays were conducted in a randomized design in a factorial arrangement, with three cultivars of cotton and two resistance inducers, with ten repetitions. The biological parameters observed were: ninfal mortality, duration of nymphal stage, and pre-reproductive, reproductive and post-reproductive periods, longevity and total number of nymphs produced. The lignin and phenol content in the leaves were quantified. The longest duration of the nymphal period, the lower number of nymphs produced, and the major mortality were observed in the ASM treatment. Silicon and ASM promoted an increase in lignin content in the cv. BRS Verde. Thus, the ASM application affected negatively biological parameters of A. gossypii, by increasing the lignin content in plants. The cv. BRS Verde is a better cutivar to be used, because it accumulated higher lignina and phenol contents.
Keywords: acibenzolar-S-methyl, Aphis gossypii, silicon.
INTRODUÇÃO
O algodoeiro é a cultura fibrosa mais importante no mundo e é cultivada em quase todos os países tropicais e subtropicais, sendo considerada para muitos países em desenvolvimento uma fonte de renda essencial (Oerke, 2006).
Existem inúmeros fatores que podem reduzir a produção do algodoeiro, entre esses estão os artrópodes-praga que causam prejuízos consideráveis na produção. Entre o complexo de insetos-praga que ataca o algodoeiro, o pulgão Aphis gossypii (Glover 1877) se destaca, podendo provocar perdas de até 40% (Pessoa et al., 2004). O algodão é considerado uma das culturas em que mais se utilizam tratamentos inseticidas, por não ser cultura para consumo alimentar (Sobhy et al., 2012). Para o controle desses insetos-praga, métodos alternativos que visam reduzir doses e custos de aplicações de inseticidas estão sendo estudados. Uma estratégia alternativa é o uso de indutores de resistência. A indução de resistência é um processo de defesa das plantas no qual um estresse ou uma injúria diminui a preferência ou o desempenho do herbívoro (Karban e Myers, 1989). Essa indução pode ser feita, entre outras formas, por meio de adubações com fontes de silício e do uso do composto éster 2-metil benzo-(1,2,3)-tiadiazole-7-carbotioico, designado também como acibenzolar-S-methyl (ASM).
O silício após absorvido é translocado e depositado logo abaixo da cutícula, formando uma dupla camada silício-cutícula que confere uma proteção contra o ataque de insetos herbívoros e microrganismos (Epstein, 1994, 1999; Ranganathan et al., 2006; Ma e Yamaji, 2006). Há evidências que este elemento químico é capaz de ativar enzimas oxidativas como peroxidases, polifoloxidase e fenilalanina-amonialiase, que são precursoras da síntese de lenhina , suberina, tanino, quinonas, flavonóides e fitoalexinas, conferindo assim, respostas de defesa da planta a insetos e patógenos (Gomes et al., 2005).
O ASM é um composto sintético análogo ao ácido salicílico que está envolvido na ativação de resistência sistêmica adquirida, em plantas (Gorlach et al., 1996). Este produto é o primeiro representante de uma geração de protetores de plantas eficientes na indução de resistência (Lyon e Newton, 1997).
Ainda são escassos os estudos com a utilização do silício e do ASM no controle de insetos sugadores, principalmente sobre seu efeito no desenvolvimento do pulgão A. gossypii e no desenvolvimento do algodoeiro. No entanto, pesquisas com esses produtos e outras espécies de pulgões têm demonstrado resultados promissores. Em sorgo e em trigo foi possível observar que a aplicação de silício reduziu a preferência e a reprodução de Schizaphis graminum (Rondani 1852) (Carvalho et al., 1999; Basagli et al., 2003). Camargo et al. (2008) constataram efeito da aplicação de silício no comportamento de Cinara atlantica (Wilson 1919) em plantas de Pinus taeda. A eficiência do ASM na redução da oviposição e no desenvolvimento da mosca-branca Bemisia tabaci (Gennadius 1889) foi atribuída a aumentos significativos nos níveis da atividade de enzimas peroxidase 1,3-glucanase (Inbar et al., 2001; Correa et al., 2005).
Dessa forma, hipotetiza-se que a aplicação de silício ou ASM proporciona um aumento nos teores de lenhina e fenóis nas plantas de algodão colorido, induzindo resistência a A. gossypii. Assim com o presente trabalho objetivou-se avaliar cultivares de algodão colorido, tratadas com silício e acibenzolar- S-methyl, quanto á resistência a A. gossypii.
MATERIAL E MÉTODOS
Obtenção de plantas e aplicação dos indutores de resistência
Em sala climatizada (temperatura diurna de 28±2oC e noturna de 25±2oC; 70±10 % de Umidade Relativa; e 12 horas de fotofase) foram distribuídos aleatoriamente sobre bancada, vasos de polietileno com capacidade para 2 kg de substrato, formulado com solo (latossolo vermelho) e esterco bovino curtido, na proporção de 3:1. Cada vaso foi semeado com seis sementes de algodão, das cultivares BRS Safira, BRS Verde e BRS Rubi. Diariamente as plantas foram irrigadas a fim de suprir suas necessidades hídricas. Essas plantas foram utilizadas para o ensaio de biologia do afídeo e determinação dos teores de lenhina e fenóis.
As soluções de ácido silícico, na dosagem equivalente a 3 x 103 kg SiO2/ha e 0,2% (0,9g / 450 mL de água para 30 vasos) de ASM (BION® que contém 50% de acibenzolar-S-methyl) foram aplicadas quando o primeiro par de folhas estava expandido. A solução de ácido silícico foi aplicada ao redor das plântulas. O ASM foi aplicado por meio de pulverizador manual até o escorrimento da calda. Os vasos que constituíram o controle (testemunha) receberam água na mesma quantidade.
Biologia de Aphis gossypii
Seis dias após a aplicação dos indutores de resistência, três adultos, no período reprodutivo, retirados de folhas de algodão de criação de manutenção do laboratório do Departamento de Entomologia da UFLA, foram transferidos para placas de Petri de 5 cm de diâmetro, contendo um disco (3 cm) foliar de algodoeiro correspondente a cada tratamento. Os discos foram fixados, com a parte abaxial para cima, em uma lâmina de ágar: água a 1%. As placas com os pulgões, vedadas com filme de PVC perfurado com alfinete para evitar a umidade excessiva da placa, foram mantidas em câmaras climatizadas a 25±2ºC, UR de 70±10 % e fotofase de 12 horas.
Após 24 h da infestação dos pulgões adultos, estes foram retirados, as ninfas entretanto nascidas foram contadas e apenas uma ninfa foi mantida nos discos foliares para a avaliação diária do seu desenvolvimento. Os discos foliares foram trocados a cada 96 h para o fornecimento de alimento adequado para a ninfa de A. gossypii. O delineamento experimental foi fatorial envolvendo três cultivares de algodão (BRS Safira, BRS Verde e BRS Rubi) e dois indutores de resistência (silício e acibenzolar-S-methyl) e a testemunha com 10 repetições por tratamento. Os parâmetros biológicos observados diariamente foram: mortalidade ninfal; duração do estado ninfal, períodos pré-reprodutivo, reprodutivo e pós- reprodutivo; longevidade e número total de ninfas produzidas.
Teores de lenhina e fenóis
Após seis dias da aplicação dos indutores, a parte aérea das plantas correspondentes a cada tratamento, em dez repetições, foi coletada e acondicionada em sacos de papel. O material foi seco em estufa (60ºC) até peso constante e, logo em seguida, foi moído, etiquetado, e enviado ao Laboratório de Produtos Vegetais do Departamento de Ciências dos Alimentos da UFLA para determinação dos teores de fenóis e lenhina. Para a determinação de fenóis foi utilizado o método de Folin-Denis, conforme AOAC (1990) e o de van Soest (1967) para lenhina.
Análise estatística: Os dados foram submetidos à análise de variância e as médias comparadas pelo teste de Scott-Knott (P ≤ 0,05), sendo os de mortalidade transformados em arco-seno √(x/100), antes da análise. Os valores médios são apresentados não transformados.
RESULTADOS E DISCUSSÃO
A interação entre cultivares e indutores não foi significativa para nenhum dos parâmetros biológicos verificados. No entanto, ao avaliar isoladamente os fatores, observaram-se diferenças significativas entre os indutores nos parâmetros mortalidade (P < 0,001; F = 10,835), período ninfal (P = 0,005; F = 5,693) e número total de ninfas (P = 0,011; F = 4,844) (Quadro 1), sendo os valores mais elevados para periodo ninfal e mortalidade ninfal dos pulgões alimentados com plantas tratadas com ASM em comparação ao silício e testemunha. O ASM promoveu redução no número total de ninfas quando comparado com o silício e a testemunha. Quando as plantas foram tratadas com silício, não foram verificadas diferenças significativas para todos os parâmetros biológicos do pulgão A. gossypii em comparação com a testemunha.
Também se verificaram diferenças significativas no número total de ninfas entre cultivares de algodoeiro (P = 0,039; F = 3,406). Pulgões quando alimentados com plantas da cv. BRS Verde apresentaram um maior número total de ninfas.
Estes resultados são semelhantes aos obtidos por Ranger et al. (2009) que não observaram efeitos do silício no período pré-reprodutivo e na sobrevivência do pulgão Myzus persicae (Sulzer 1776) em plantas de Zinnia elegans. No entanto, Costa e Moraes (2006) e Goussain et al. (2005) verificaram efeito do silício no desenvolvimento de S. graminum em plantas de trigo tratadas com silício. A fecundidade de pulgões M. persicae também foi reduzida em plantas de batata que receberam adubação silicatada (Gomes et al., 2008). De acordo com Dias et al. (2014), a adubação com silício também afetou fecundidade, período reprodutivo e longevidade de Sitobion avenae (Fabricius 1775). Alguns autores como Amado e Rizental (2015) e Panizzi e Parra (2009) relataram que a barreira formada pelo silício nas plantas não se constitui, aparentemente, em fator de resistencia de plantas a insetos sugadores. Portanto, é provável que os efeitos de indutores, a exemplo do silício, não sejam totalmente efetivos em todas as plantas, dado a variedade do sistema defensivo das mesmas. Além disso, não se deve esperar que os indutores sejam eficazes contra todos os insetos, devido às suas habilidades de superar o sistema defensivo das plantas (Inbar et al., 1998; Civolani et al., 2010). Outro fato a ser considerado, é que o algodoeiro não é caracterizado como uma planta acumuladora de silício.
O ASM promoveu uma maior duração do estado ninfal (P = 0,005; F = 5,693), um menor número total de ninfas (P = 0,019; F = 4,254) e uma maior mortalidade (P < 0,001; F = 10,835) quando comparado com o silício e a testemunha. Os demais parâmetros, período pré-reprodutivo (P = 0,3078; F = 1,230), reprodutivo (P = 0,6602; F = 0,605), pós-reprodutivo (P = 0,5687; F = 0,740) e longevidade (P = 0,6350; F = 0,642) não foram alterados quando os insetos foram alimentados com plantas tratadas com silício e ASM. Estes resultados se assemelham aos observados por Costa e Moraes (2006) que verificaram redução significativa no número médio de ninfas e na taxa de crescimento do pulgão S. graminum em plantas de trigo tratadas com ASM. Martins et al. (2015) também observaram efeito do ASM na redução de A. gossypii em cultivares de algodoeiro. Em pepino, a aplicação de ASM também afetou negativamente a biologia da mosca-branca B. tabaci pelo aumento do período de desenvolvimento ninfal e da mortalidade, tanto ninfal quanto total (Correa et al., 2005). Também Boughton et al. (2006) observaram, como no presente trabalho, redução na fecundidade total e na taxa de crescimento da população de uma outra espécie de pulgão, no caso M. persicae, em plantas de tomate tratadas com ASM.
Os efeitos promovidos para A. gossypii em plantas tratadas com ASM pode estar ligado ao aumento de substâncias deterrentes nas plantas tratadas, que são capazes de inibir a alimentação e causar redução no número de descendentes. Compostos sintéticos, a exemplo do ASM, podem ativar, similarmente aos indutores bióticos, os genes que codificam resistência em plantas (Kessmann et al., 1994). Esse fato foi evidenciado por Inbar et al. (2001) que verificaram relação na redução da oviposição da mosca-branca B. tabaci devido ao grande aumento dos níveis de quitinases, peroxidase e β-1,3-glucanase em plantas de algodão branco convencional tratadas com ASM. Segundo Kombrink e Somssich (1997), estas enzimas desempenham um papel fundamental nos sistemas de defesa de plantas contra agentes patogênicos. Em insetos, as quitinases podem danificar as estruturas quitinosas, a exemplo da membrana peritrófica, que funciona como barreira física à abrasão causada pelos alimentos e à entrada de patógenos nas células do epitélio do intestino médio (Ary et al., 1989). A indução da atividade de quitinases pode interferir no desenvolvimento, alimentação e crescimento do inseto (Shapiro et al., 1987; Wang et al., 1996). Com relação aos danos de proteinases em insetos, estas afetam negativamente a digestibilidade e disponibilidade de proteínas para insetos herbívoros (Duffey e Felton, 1991). Em algodão, Plymale et al. (2007) constataram que a aplicação de ASM aumentou significativamente a atividade de peroxidases. Outros autores também verificaram um aumento da atividade das enzimas peroxidases e β-1,3-glucanase, em plantas de tomate e em macieira, sugerindo que ASM fornece proteção às plantas (Brisset et al., 2000; Araujo e Menezes, 2009).
Ao avaliar o teor médio de lenhina em folhas das cultivares de algodão colorido observou-se interação significativa entre os fatores (P < 0,001, F = 20,186), ou seja, as cultivares tratadas e não tratadas com indutores apresentaram diferentes porcentagens de lenhina em sua composição (Figura 1A). Quando as cultivares não foram tratadas (testemunha), verificou-se que a cv. BRS Rubi apresentou maior teor de lehnina, comparando com as cvs. BRS Safira e BRS Verde (P < 0,001; F = 19,227). Porém, esta quantidade de lenhina naturalmente existente não foi suficiente para causar alterações nos parâmetros biológicos estudados.
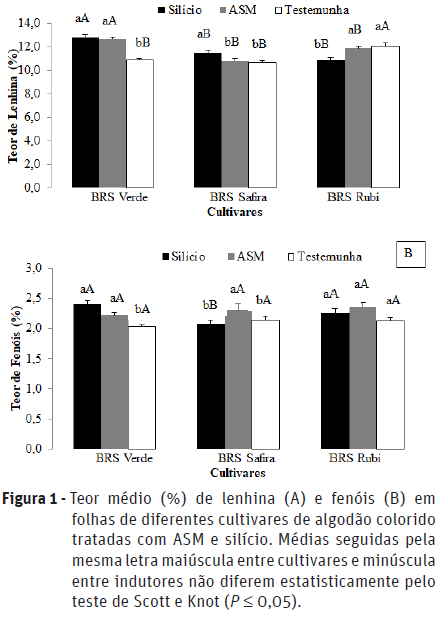
Em relação à aplicação de ASM, a cv. BRS Verde apresentou maior teor de lenhina (P < 0,001; F = 23,921), seguido pelas cvs. BRS Rubi e BRS Safira. Quando se aplicou silício, a cv. BRS Verde também apresentou o maior teor de lenhina, comparando com as outras cultivares (P < 0.001; F = 25,697).
Estes resultados são semelhantes aos relatados por Moraes et al. (2009) que verificaram aumentos na produção de lenhina em plantas de soja tratadas com silício e ASM. O aumento do teor de lenhina devido à aplicação de silício também foi observado em plantas de batata, visando à indução de resistência ao pulgão M. persicae (Gomes et al., 2008). Tatagiba et al. (2014) investigaram o efeito do silício na resistência de plantas de arroz a infecções fúngicas e também verificaram o potencial do silício no aumento da produção de lenhina. Segundo Epstein (1999), os mecanismos de defesa estimulados pelo silício incluiem, além da acumulação de lenhina, o aumento de compostos fenólicos, tais como as quitinases e peroxidases. No presente trabalho, não foi quantificada a atividade de peroxidases; somente foi determinado o teor de lenhina. Porém, é de conhecimento que as peroxidases estão envolvidas na produção e polimerização de lenhina (Bowles, 1990). Sendo assim, quantificar os teores de lenhina das plantas é uma forma indireta de se verificar a atividade de peroxidases das mesmas.
A respeito do indutor ASM, há pesquisas que evidenciam também este aumento de peroxidases. Plymale et al. (2007) verificaram um aumento significativo de peroxidases em algodão tratado com ASM. Do mesmo modo, Brisset et al. (2000) objetivando o controle de doenças bacterianas, obtiveram aumento de peroxidases em macieiras tratadas com ASM.
Em referência aos resultados da aplicação de indutores, observou-se que a cv. BRS Verde apresentou diferenças significativas de acumulação de lenhina em relação à sua testemunha (P < 0,001; F = 34,412), quando tratadas com silício e ASM. A cv. BRS Safira apresentou maior acumulação de lenhina quando tratada com silício (P = 0,0127; F = 4,572), diferindo da cv. BRS Rubi, que apresentou maiores teores quando tratada com ASM (P < 0,001; F = 10,391).
Da mesma forma, foi constatada interação significativa entre os indutores e cultivar de algodão para a porcentagem de fenóis (P = 0,0135; F = 3,362). No entanto, não foram constatadas diferenças significativas no teor de fenóis (P = 0,3979; F = 0,932) para aquelas plantas que não receberam os indutores de resistência (testemunha) e para aquelas em que foi aplicado ASM (Figura 1B). Contudo, a aplicação de silício proporcionou um aumento significativo de fenóis nas cvs. BRS Verde e BRS Rubi quando comparadas com a cv. BRS Safira (P = 0,0042; F = 5,828). O teor de fenóis foi significativamente maior na cv. BRS Verde em plantas em que foram aplicadas os indutores (P = 0,0011; F = 7,365), diferindo da cv. BRS Safira que apresentou o maior teor de fenóis somente quando tratadas com ASM e da cv. BRS Rubi que não apresentou diferenças significativas entre os indutores e a testemunha. A aplicação de silício também proporcionou um aumento significativo de fenóis nas cvs. BRS Verde e BRS Rubi.
Estes resultados corroboram os encontrados por Pinto et al. (2012) que consideraram ser promissora a aplicação de silicio para a proteção de genótipos de cacau para pulgões por incrementar os teores de fenóis nas plantas tratadas com silicato de potássio. E também estão de acordo com os encontrados por Gomes et al. (2008) e Moraes et al. (2009) os quais verificaram que a aplicação de silício aumentou a percentagem de fenóis em plantas de batata e soja, respectivamente.
Segundo revisão realizada por Etesami e Jeong (2018) é possível associar o efeito do silício na regulação da biossíntese de lenhina com a habilidade de algumas plantas em absorver e acumular silício. Este fato ainda requer mais estudos, mas sabe-se que o tipo de planta com relação a ser ou não acumuladora de silício pode estar associado com o aumento ou redução da síntese de lenhina.
Entretanto, ressalta-se que o efeito deterrente obtido nesta pesquisa quando aplicado o indutor ASM não está relacionado com o teor de fenóis nas plantas de algodão colorido, visto que este indutor não alterou estatisticamente a quantidade deste composto.
Contudo, como verificado, o aumento do teor de lenhina na cv. BRS Verde provocada pelo ASM induziu resistência às plantas de algodão colorido ao pulgão A. gossypii, em virtude das interferências na duração do período ninfal e no número total de ninfas. O aumento do período ninfal indica um alimento não adequado e, consequentemente, interfere na reprodução, implicando em um menor crescimento populacional dos insetos (Boughton et al., 2006).
CONCLUSÃO
O silício não foi capaz de alterar nenhum parâmetro biológico dos afídeos. Porém, a aplicação de ASM pode proporcionar uma proteção às plantas de algodão, afetando negativamente parâmetros biológicos do pulgão A. gossypii, por meio do aumento de lenhina nas plantas e se caracterizando como uma ferramenta disponível em programas de manejo de pragas. A cv. BRS Verde se apresentou como uma melhor cultivar a ser utilizada, visto que foi capaz de acumular maiores teores de lenhina e fenóis.
Referências bibliográficas
Amado, D. & Rizental, M. (2015) - Silício como indutor de resistência a Aphis gossypii (Hemiptera: Aphididae) e Bemisia tabaci (Hemiptera: Aleyrodidae) em algodoeiro. Connection on line revista eletrônica do UNIVAG, n. 12, p. 106-112. http://dx.doi.org/10.18312%2F1980-7341.n12.2015 [ Links ]
AOAC (1990) - Official methods of analysis. 15a ed. Association of Official Analytical Chemists. Washington, D.C., 1298 p. [ Links ]
Araujo, F.F.D. & Menezes, D. (2009) - Indução de resistência a doenças foliares em tomateiro por indutores biótico (Bacillus subtilis) e abiótico (acibenzolar-s-metil). Summa Phytopathologica, vol. 35, n. 3, p. 169-172. http://dx.doi.org/10.1590/S0100-54052009000300001 [ Links ]
Ary, M.B.; Richardson, M. & Shewry, P.R. (1989) - Purification and characterization of an insect a-amylase inhibitor/endochitinase from seeds of job’s tears (Coix lachryma-jobi). Biochimica Biophysica Acta, vol. 999, n. 3, p. 260-266. https://doi.org/10.1016/0167-4838(89)90007-1 [ Links ]
Basagli, M.A.B.; Moraes, J.C.; Carvalho, G.A.; Ecole, C.C. & Gonçalves-Gervásio, R.C.R. (2003) - Effect of sodium silicate on the resistance of wheat plants to green- aphid Schizaphis graminum (Rond.) (Hemiptera: Aphididae). Neotropical Entomology, vol. 32, n. 4, p. 659-663. http://dx.doi.org/10.1590/S1519-566X2003000400017 [ Links ]
Boughton, A.J.; Hoove, R.K. & Felton, G.W. (2006) - Impact of chemical elicitor applications on greenhouse tomato plants and population growth of the green peach aphid, Myzus persicae. Entomologia Experimentalis et Applicata, vol. 120, n. 3, p. 175-188. https://doi.org/10.1111/j.1570-7458.2006.00443.x [ Links ]
Bowles, D.J. (1990) - Defense-related proteins in higher plants. Annual Review of Biochemistry, vol. 59, p. 873-907. https://doi.org/10.1146/annurev.bi.59.070190.004301 [ Links ]
Brisset, M.N.; Cesbron, S.; Thomson, S.V. & Paulin, J.P. (2000) - Acibenzolar-s-methyl induces the accumulation of defense-related enzymes in apple and protects from fire blight. European Journal of Plant Pathology, vol. 106, n. 6, p. 529-536. http://dx.doi.org/10.1023/A:1008728119087 [ Links ]
Camargo, J.M.M.; Moraes, J.C.; Oliveira, E.B.; Iede, E.T. (2008) - Resistência induzida ao pulgão-gigante-do- pinus (Hemiptera: Aphididae) em plantas de Pinus taeda adubadas com silício. Bragantia, vol. 67, n. 4, p. 927-932. http://dx.doi.org/10.1590/S0006-87052008000400015 [ Links ]
Carvalho, S.P.; Moraes, J.C. & Carvalho, J.G. (1999) - Efeito do silício na resistência do sorgo (Sorgum bicolor) ao pulgão-verde Schizaphis graminum (Rond.) (Homoptera: Aphididae). Anais da Sociedade Entomológica do Brasil, vol. 28, n. 3, p. 505-510. http://dx.doi.org/10.1590/S0301-80591999000300017 [ Links ]
Civolani, S.; Marchetti., E; Chicca, M.; Castaldelli, G.; Rossi, R.; Pasqualini, E.; Dindo, M.L.; Baronio, P. & Leis, M. (2010) - Probing behaviour of Myzus persicae on tomato plants containing Mi gene or BHT- treated evaluated by electrical penetration graph. 2010. Bulletin of Insectology, vol. 63, n. 2, p. 265-271. [ Links ]
Correa, R.S.B.; Moraes, J.C.; Auad, A.M. & Carvalho, G.A. (2005) - Silicon and acibenzolar-s-methyl as resistance inducers in cucumber against the whitefly Bemisia tabaci (Gennadius) (Hemiptera: Aleyrodidae) biotype A. Neotropical Entomology, vol. 34, n. 3, p. 429-433. http://dx.doi.org/10.1590/S1519-566X2005000300011 [ Links ]
Costa, R.R. & Moraes, J.C. (2006) - Efeitos do ácido silícico e do acibenzolar-s-methyl sobre Schizaphis graminum (Rondani) (Hemiptera: Aphididae). Neotropical Entomology vol. 35, n. 6, p. 834-839. http://dx.doi.org/10.1590/S1519-566X2006000600018 [ Links ]
Dias, P.A.S.; Sampaio, M.V.; Rodrigues, M.P.; Korndorfer, A.P.; Oliveira, R.S.; Ferreira, S.E. & Korndorfer, G.H. (2014) - Induction of resistance by silicon in wheat plants to alate and apterous morphs of Sitobion avenae (Hemiptera: Aphididae). Environmental Entomology, vol. 43, n. 4, p. 949-956. http://dx.doi.org/10.1603/EN13234 [ Links ]
Duffey, S.S. & Felton, G.W. (1991) - Enzymatic antinutritive defenses of the tomato plant against insects. In: Hedin, P.A. (Ed.) - ACS Symposium series American Chemical Society. Washington. p. 166-197. [ Links ]
Epstein, E. (1994) - The anomaly of silicon in plant biology. Proceedings of the National of Academy of Sciences, vol. 91, n. 1, p. 11-17. https://doi.org/10.1073/pnas.91.1.11 [ Links ]
Epstein, E. (1999) - Silicon. Annual Review of Plant Physiology and Plant Molecular Biology, vol. 50, p. 641-664. https://doi.org/10.1146/annurev.arplant.50.1.641 [ Links ]
Etesami, H. & Jeong, B.R. (2018) - Silicon (Si): Review and future prospects on the action mechanisms in alleviating biotic and abiotic stresses in plants. Ecotoxicology and Environmental Safety, vol. 147, p. 881–896. http://dx.doi.org/10.1016/j.ecoenv.2017.09.063 [ Links ]
Gomes, F.B.; Moraes, J.C.; Santos, C.D. & Antunes, C.S. (2008) - Uso de silício como indutor de resistência em batata a Myzus persicae (Sulzer) (Hemiptera: Aphididae). Neotropical Entomology, vol. 37, n. 2, p. 185-190. http://dx.doi.org/10.1590/S1519-566X2008000200013 [ Links ]
Gomes, F.B.; Moraes, J.C.; Santos, C.D. & Goussain, M.M. (2005) - Resistance induction in wheat plants by silicon and aphids. Scientia Agricola, vol. 62, n. 6, p. 547-551. http://dx.doi.org/10.1590/S0103-90162005000600006 [ Links ]
Görlach, J.; Volrath, S.; Knauf-beiter, G.; Hengy, G.; Beckhove, U.; Kogel, K.H.; Oostendorp, M.; Staub, T.; Ward, E.; Kessmann, H. & Ryals, J. (1996) - Benzothiadiazole, a novel class of inducers of systemic acquired resistance, activates gene expression and disease resistance in wheat. The Plant Cell Online, vol. 8, n. 4, p. 629-643. http://dx.doi.org/10.1105/tpc.8.4.629 [ Links ]
Goussain, M.M.; Prado, M. & Moraes, J.C. (2005) - Effect of silicon applied to wheat plants on the biology and probing behaviour of the greenbug Schizaphis graminum (Rond.) (Hemiptera: Aphididae). Neotropical Entomology, vol. 34, n. 5, p. 807-813. http://dx.doi.org/10.1590/S1519-566X2005000500013 [ Links ]
Inbar, M.; Doostdar, H.; Gerling, D. & Mayer, R.T. (2001) - Induction of systemic acquired resistance in cotton by BHT has a negligible effect on phytophagous insects. Entomologia Experimentalis et Applicata, vol. 99, n. 1, p. 65-70. https://doi.org/10.1046/j.1570-7458.2001.00802.x [ Links ]
Inbar, M.; Doostdar, H.; Sonoda, R.M.; Leibee, G.L. & Mayer, R.T. (1998) - Elicitors of plant defensive systems reduce insect densities and disease incidence. Journal of Chemical Ecology vol. 24, n. 1, p. 135-149. https://dx.doi.org/10.1023/A:1022397130895 [ Links ]
Karban, R. & Myers, J.H. (1989) - Induced plant responses to herbivory. Annual Review of Ecology and Systematics, vol. 20, p. 331-348. https://doi.org/10.1146/annurev.es.20.110189.001555 [ Links ]
Kessmann, H.; Staub, T.; Hoffmann, C.; Maetzke, T.; Herzog, J.; Ward, E.; Uknes, S. & Ryals, J. (1994) - Induction of systemic acquired disease resistance in plants by chemicals. Annual Review of Phytopathology vol. 32, p. 439-459. http://dx.doi.org/10.1146/annurev.py.32.090194.002255 [ Links ]
Kombrink, E. & Somssich, I.E. (1997). Pathogenesis-related proteins and plant defense. In: Carrol, G.C. & Tudzynski, P. (Eds.) - Plant relationships. Springer Berlin Heidelberg, Köln (Germany). pp. 107–128. [ Links ]
Lyon, G.D. & Newton, A.C. (1997) - Do resistance elicitors offer new opportunities in integrated disease control strategies? Plant Pathology, vol. 46, n. 5, p. 636-641. https://dx.doi.org/10.1046/j.1365-3059.1997.d01-63.x [ Links ]
Ma, J.F. & Yamaji, N. (2006) - Silicon uptake and accumulation in higher plants. Trends in Plant Science vol. 11, n. 8, p. 392- 397. https://doi.org/10.1016/j.tplants.2006.06.007 [ Links ]
Martins, G.L.M.; Tomquelski, G.V.; Papa, G. (2015) - Aplicação de acybenzolar-s-methyl em algodoeiro para controle de Aphis gossypii (Glover) e Ramularia areola (Atkinson). Revista de Agricultura Neotropical, vol. 2, n. 1, p. 53-59. https://doi.org/10.32404/rean.v2i1.245 [ Links ]
Moraes, J.C.; Ferreira, R.S. & Costa, R.R. (2009) - Indutores de resistência a mosca-branca Bemisia tabaci biótipo B (Genn., 1889) (Hemiptera: Aleyrodidae) em soja. Ciência e Agrotecnologia vol. 33, n. 5, p. 260-264. http://dx.doi.org/10.1590/S1413-70542009000500009 [ Links ]
Oerke, E.C. (2006) - Crop losses to pests. The Journal of Agricultural Science, vol. 144, n. 1, p. 31-43. https://doi.org/10.1017/S0021859605005708 [ Links ]
Panizzi, A.R. & Parra, J.R.P. (2009) - Bioecologia e nutrição de insetos: base para o manejo integrado de pragas. Embrapa Informação Tecnológica, Brasília, 1164 p. [ Links ]
Pessoa, L.G.A.; Souza, B.; Carvalho, C.F. & Silva, M.G. (2004) - Aspectos da biologia de Aphis gossypii Glover, 1877 (Hemiptera: Aphididae) em quatro cultivares de algodoeiro, em laboratório. Ciência e Agrotecnologia, vol. 28, n. 6, p.1235-1239. http://dx.doi.org/10.1590/S1413-70542004000600003 [ Links ]
Pinto, D.G.; Aguilar, M.A.G.; Souza, C.A.S.; Silva, D.M., Siqueira, P.R.; Cao, J.R.; Zanetti, L.V. (2012) - Alterações fisiológicas após aplicação de silício em cacau e sua influência na preferência por pulgões. Revista Ceres, vol. 59, n. 3, p. 360-367. http://dx.doi.org/10.1590/S0034-737X2012000300010 [ Links ]
Plymale, R.C.; Felton, G.W. & Hoover, K. (2007) - Induction of systemic acquired resistance in cotton foliage does not adversely affect the performance of an entomopathogen. Journal of Chemical Ecology, vol. 33, n. 8, p. 1570-1581. http://dx.doi.org/10.1007/s10886-007-9329-7 [ Links ]
Ranganathan, S.; Suvarchala, V.; Rajesh, Y.B.R.D.; Srinivasa, P.M.; Padmakumari, A.P. & Voleti, S.R. (2006) - Effects of silicon sources on its deposition, chlorophyll content, and disease and resistance in rice. Biologia Plantarum, vol. 50, n. 4, p. 713-716. http://dx.doi.org/10.1007/s10535-006-0113-2 [ Links ]
Ranger, C.M.; Singh, A.P.; Frantz, J.M.; Cañas, L.; Locke, J.C.; Reding, M.E. & Vorsa, N. (2009) - Influence of silicon on resistance of Zinnia elegans to Myzus persicae (Hemiptera: Aphididae). Environmental Entomology, vol. 38, n. 1, p. 129-136. https://doi.org/10.1603/022.038.0116 [ Links ]
Shapiro, M.; Preisler, H.K. & Robertson, J.L. (1987) - Enhancement of baculovirus activity on gypsy moth (Lepidoptera: Lymantriidae) by chitinase. Journal of Economic Entomology vol. 80, n.6, p. 1113-1116. https://doi.org/10.1093/jee/80.6.1113 [ Links ]
Sobhy, I.S.; Erb, M.; Sarhan, A.A.; El-husseini, M.M.; Mandour, N.S. & Turlingd, T.C. (2012) - Less is more: treatment with BHT and laminarin reduces herbivore-induced volatile emissions in maize but increases parasitoid attraction. Journal of Chemical Ecology, vol. 38, n. 4, p. 348-360. https://doi.org/10.1007/s10886-012-0098-6 [ Links ]
Tatagiba, S.D.; Rodrigues, F.A.; Filippi, M.C.C.; Silva, G.B. & Silva, L.C. (2014) - Physiological responses of rice plants supplied with silicon to Monographella albescens Infection. Journal of Phytopathology, vol. 162, n. 9, p. 596-606. https://doi.org/10.1111/jph.12231 [ Links ]
van Soest, P.J. (1967) – Development of a comprehensive system of feed analysis and its application to forage. Journal of Animal Science, vol. 26, n. 1, p. 119-128. https://doi.org/10.2527/jas1967.261119x [ Links ]
Wang, X.; Ding, X.; Gopalakrishnan, B.; Morgan, T.D.; Johnson, L.; White, F.F.; Muthukrishnan, S.; Kramer, K.J. (1996) - Characterization of a 46 kda insect chitinase from transgenic tobacco. Insect Biochemistry and Molecular Biology, vol. 26, n. 10, p. 1055-1064. https://doi.org/10.1016/S0965-1748(96)00056-2 [ Links ]
Agradecimentos
Ao Conselho Nacional de Desenvolvimento Científico e Tecnológico – CNPq pelo apoio financeiro ao projeto e à Fundação de Amparo a Pesquisa de Minas Gerais - FAPEMIG pela concessão de bolsas.
Recebido/received: 2018.08.12
Aceite/accepted: 2019.02.08














