INTRODUÇÃO
A urticária crónica espontânea (UCE) é definida pela ocorrência espontânea diária ou quase diária de lesões maculopapulares eritematosas e pruriginosas com ou sem angioedema por um período igual ou superior a 6 semanas, sem fator desencadeante externo aparente 1,2.
A UCE apresenta uma prevalência aproximada de 1%, sendo mais frequente no sexo feminino 1,3,4. O diagnóstico de UCE é clínico, mediante uma história clínica e exame objetivo cuidados, sem necessidade de exames complementares de diagnóstico (1,5.
A UCE tem um significativo impacto na qualidade de vida dos doentes, interferindo nas atividades profissionais, escolares e sociais do dia-a-dia. Estudos realizados para avaliar a qualidade de vida em doentes com UCE indicam que a doença afeta negativamente a quantidade e qualidade do sono e a autoestima, podendo levar a alterações psiquiátricas, como ansiedade e depressão 1,3,6. O estudo AWARE demonstrou o impacto real da UCE em doentes portugueses refratários ao tratamento com anti- histamínicos H1 (anti-H1), com 30% dos doentes a reportarem um impacto elevado ou extremamente elevado da doença na sua qualidade de vida 7.
O controlo dos sintomas é o objetivo principal do tratamento. As recentes diretrizes nacionais (Grupo Português de Estudos de Urticária-GPEU) e europeias (EAACI/GA²LEN/EDF/WAO) recomendam como terapêutica de primeira linha para a UCE o uso de anti-H1 de segunda geração não sedativos, até dose quádrupla da dose diária recomendada 1,2. No entanto, até cerca de 40% destes doentes podem não alcançar o controlo da doença apenas com anti-H1 8,9.
O omalizumab (OMA), anticorpo monoclonal anti-IgE humanizado recombinante, é a opção terapêutica eficaz e bem tolerada, recomendada e aprovada para doentes com UCE refratária aos anti-H1 com idade igual ou superior a 12 anos, na dose de 300mg 4/4 semanas 1,2,10,11.
De acordo com a resposta clínica do doente, ajustes subsequentes de dose ou frequência de administração poderão ser realizados a cada 3-6 meses, com possível suspensão do OMA na remissão da UCE 1. Estudo recente de Brás R, Costa C et al, que incluiu 138 doentes com UCE, mostrou existir boa tolerância nos ajustes da terapêutica com OMA, possibilitando um aumento da eficácia desta terapêutica 12.
O resumo das características do medicamento do OMA foi atualizado em janeiro 2019, passando a incluir uma utilização mais flexível fora do contexto hospitalar, com a possibilidade de autoadministração (AA) de seringa pré--cheia por parte do doente ou pelo seu cuidador 10.
No cenário pandémico recentemente vivido, assistiu-se à implementação de medidas que visassem a minimização do risco de exposição individual 13. Neste contexto, a prática da AA de OMA foi agilizada e progressivamente instituída no nosso Serviço.
Neste estudo, pretendeu-se avaliar o grau de satisfação de doentes seguidos num centro UCARE a realizar terapêutica com OMA em AA para UCE, fazendo-se uma caracterização das principais vantagens da AA, bem como os fatores limitantes da administração hospitalar percecionadas por estes doentes. Adicionalmente, efetuou-se uma avaliação do controlo da UCE e segurança da terapêutica com OMA na modalidade de AA.
MATERIAL E MÉTODOS
Realizou-se um estudo observacional retrospetivo de doentes com UCE seguidos no Centro UCARE do nosso Serviço de Imunoalergologia, no período de janeiro a junho de 2021, onde foram incluídos todos os doentes com idade superior ou igual a 18 anos em AA de OMA no domicílio por um período igual ou superior a 12 semanas e após duas sessões de ensino de AA e supervisionado pela equipa de enfermagem em Hospital de Dia (HD).
Os procedimentos seguidos neste estudo estavam de acordo com os regulamentos estabelecidos pela Comissão de Investigação Clínica e Ética e Associação Médica Mundial (Declaração de Helsínquia revista em 2013). Após obtenção do consentimento livre e esclarecido dos doentes, foi aplicado um questionário constituído por 30 perguntas em entrevista telefónica realizada ao doente, complementado com a consulta dos seus processos clínicos para caracterização clínica e demográfica dos doentes, caracterização da terapêutica com OMA e perspetiva dos doentes sobre a AA de OMA, avaliação do controlo da urticária e qualidade de vida (QoL) dos doentes e avaliação da segurança do OMA em AA.
A terapêutica com OMA foi caracterizada atendendo a aspetos diretamente associados ao esquema terapêutico instituído a cada doente e adicionalmente a fatores relacionadas com a administração de OMA em HD versus em AA, onde se incluíram o tempo e custos mensais com as deslocações e os dias de absentismo laboral anual associados a estas deslocações.
A perspetiva dos doentes sobre a AA de OMA atendeu às vantagens e preocupações percecionadas, bem como às sugestões propostas pelos doentes para melhoria do processo associado à AA de OMA.
O controlo da urticária e o impacto na QoL dos doentes com UCE sob terapêutica com OMA em AA, foram avaliados com base nos resultados em T0 (última administração em HD) e T1 (12 semanas após iniciar AA) dos seguintes questionários validados para a língua portuguesa (propriedade de MOXIE GmbH), preenchidos pelo doente (patients reports outcomes measures - PROM): score de atividade da urticária em sete dias (UAS7), teste de controlo da urticária (UCT) e índice de qualidade de vida em dermatologia (DLQI) 14,15. O controlo da urticária foi considerado para scores de UAS7 ≤ 6 ou UCT ≥ 12 1,2.
A avaliação da segurança do OMA em AA foi obtida com base na identificação de reações adversas reportadas.
Os resultados obtidos baseiam-se em análises descritivas apresentadas em números e percentagens de doentes.
RESULTADOS
No período de inclusão, entre janeiro e junho de 2021, foram identificados 106 doentes com UCE a realizar tratamento regular com OMA. Dos doentes referidos, 25 (23,6%) encontravam-se a realizar AA do OMA há pelo menos 12 semanas, tendo sido por isso elegíveis para o presente estudo.
Características demográficas e clínicas dos doentes elegíveis
Na Tabela 1 apresentam-se as características demográficas e clínicas dos doentes incluídos neste estudo. Os 25 doentes inquiridos tinham uma média de idades de 48,2 ±11 (29 - 68) anos, havendo apenas um doente com mais de 65 anos (68 anos). Verificou-se um predomínio do sexo feminino (84%).
Relativamente à escolaridade e situação profissional, verificou-se que a maioria dos doentes (76%) eram profissionalmente ativos (64% por conta de outrem e 12% por conta própria), com habilitações sobretudo ao nível do ensino básico ou licenciatura (com 40% e 36% dos doentes, respetivamente). O tempo médio de duração da UCE era de 7,4 ±3,9 anos.
Tabela1. Características demográficas e clínicas dos doentes
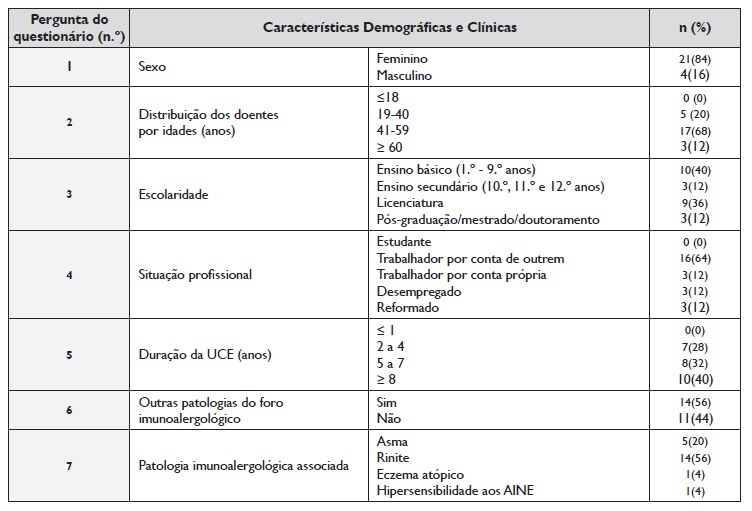
UCE - Urticária crónica espontânea; AINE - Anti-inflamatórios não esteroides
A maioria dos doentes (72%) apresentava o diagnóstico de UCE há pelo menos 5 anos, e 56% apresentava outras comorbilidades do foro imunoalergológico, destacando-se a rinite alérgica como a patologia mais frequentemente associada (56%).
Terapêutica com OMA e a perspetiva do doente sobre a AA
As questões relacionadas com a administração do OMA encontram-se detalhadas na Tabela 2. A duração média do tratamento com OMA era de 3,2 ±1,9 anos, estando a maioria dos doentes (76%) sob terapêutica com OMA entre 2 e 4 anos. No período em que os doentes realizaram terapêutica com OMA em HD, 76% deslocavam-se ao hospital por meios próprios, despendendo em média 78±51,9 minutos/ deslocação. O tempo despendido por deslocação foi superior a 2 horas em 40% dos casos, com custos associados superiores a 10 euros e absentismo laboral >6 dias/ano referidos por 56% e 28% dos doentes, respetivamente.
Tabela 2 Terapêutica com omalizumab e a perspetiva do doente sobre a autoadministração
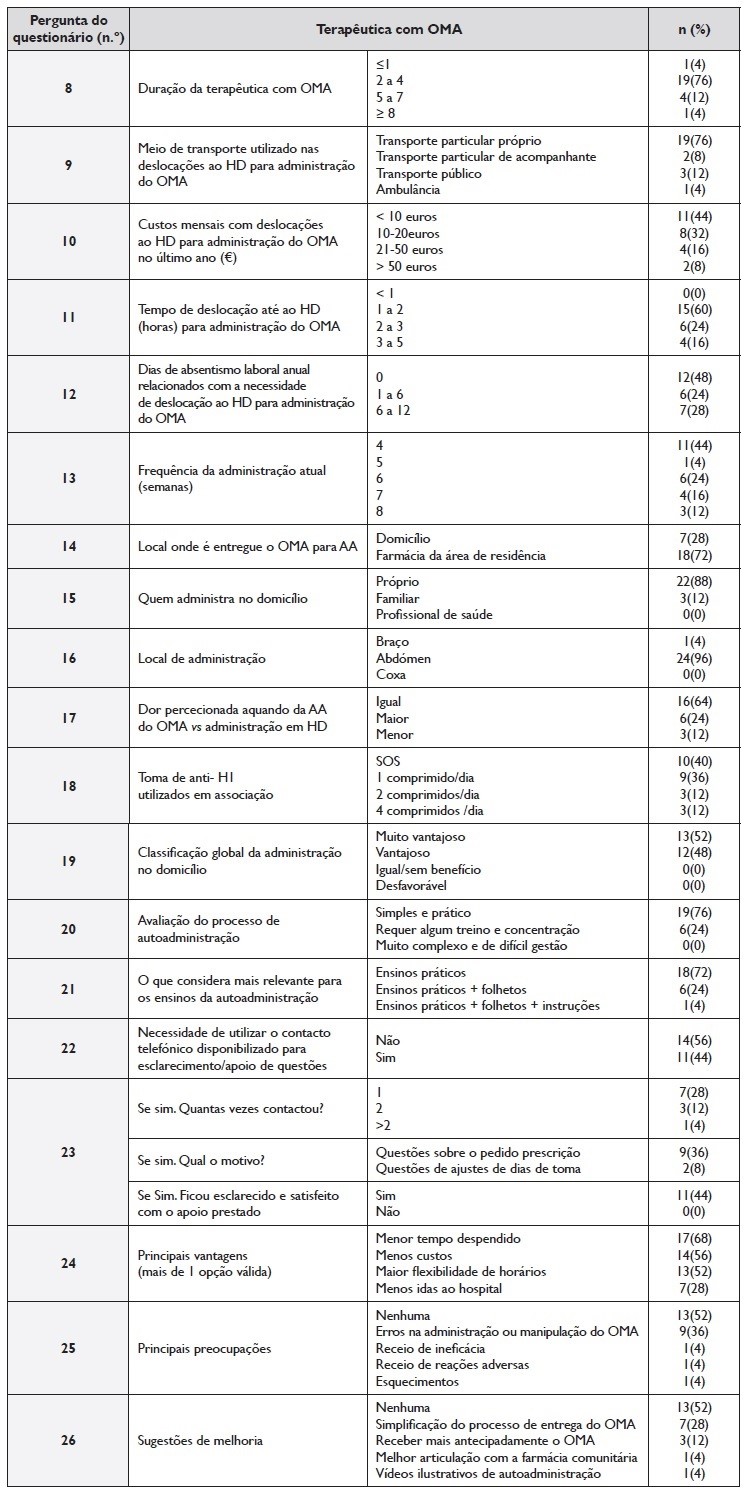
OMA - Omalizumab; AA - Autoadministração; HD - Hospital de Dia de Imunoalergologia; anti-H1- Anti-histamínicos H1 de segunda geração não sedativos
Aquando do questionário por entrevista telefónica, o OMA era levantado na farmácia comunitária por 72% dos doentes, com os restantes 28% a receber a terapêutica no domicílio. Dos 25 doentes incluídos, 44 % encontravam-se em AA de OMA com uma periodicidade de 4/4 semanas, 24% de 6/6 semanas e 12% a cada 8 semanas. A AA de OMA era em 88% dos casos feita pelo próprio, sendo a região do abdómen o local de administração predominante (96%), e com a maioria dos doentes (64%) a percecionar que a dor na AA era de intensidade igual e 24% superior, em comparação com a percecionada na administração em HD. De acordo com a escala numérica de dor (de 0 a 10), a dor sentida na AA obteve a seguinte avaliação por parte dos doentes: 0/10 (1 doente); 1/10 (11 doentes); 2/10 (7 doentes); 3/10 (2 doentes); 4/10 (1 doente) e 5/10 (3 doentes). Já em HD a avaliação registada foi: 0/10 (1 doente); 1/10 (14 doentes); 2/10 (5 doentes); 3/10 (2 doentes) e 5/10 (3 doentes).
Verificou-se que a AA de OMA foi considerada vantajosa por todos os doentes, sendo mesmo descrita como muito vantajosa por 52% dos doentes.
Relativamente à avaliação do processo de AA (Figura 1a), este foi considerado um método simples e prático pela maioria (76%) dos doentes e como um processo que requer algum treino e concentração pelos restantes doentes (24%).
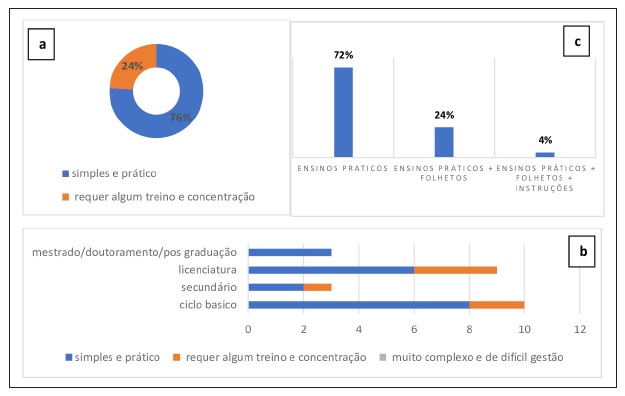
Figura 1 Avaliação do processo de autoadministração do omalizumab a) geral b) de acordo com a escolaridade dos doentes c) relevância das metodologias de aprendizagem
Neste último grupo (6/25 doentes), a necessidade de treino e concentração não foi referida pelos doentes com grau académico superior a licenciatura (Figura 1b). Quando questionados sobre a relevância das diferentes metodologias para apoio à aprendizagem da AA (Figura 1c), a maioria (72%) dos doentes valorizaram exclusivamente os ensinos práticos, tendo os restantes considerado os folhetos disponibilizados pelo hospital e/ou o folheto informativo do medicamento um importante complemento.
Embora a maioria (56%) dos doentes referissem que não tiveram necessidade de esclarecimento de dúvidas adicionais após os treinos iniciais, 44% reportaram ter
sentido esta necessidade, sendo que 16% contactaram pelo menos duas vezes o serviço de apoio disponibilizado (HD e médicos assistentes), em que todos os doentes ficaram satisfeitos com o apoio prestado. Verificou-se, contudo, que este pedido de apoio se prendeu sobretudo com questões burocráticas de pedidos de prescrição (36% dos doentes) e não com questões relacionadas com a técnica de AA de OMA.
As principais vantagens e preocupações apontadas pelos doentes relativamente à AA de OMA podem ser visualizadas na Figura 2. Relativamente às vantagens, o menor tempo despendido e a redução dos custos foram as principais vantagens apontadas (68 e 56%, respetivamente), seguindo-se a maior flexibilidade de horários e a redução do número de idas ao hospital, com 52 e 28%, respetivamente. O menor tempo despendido com o tratamento não foi valorizado pelo grupo de doentes desempregados, que em contrapartida valorizou sobretudo a redução dos custos.

Figura 2 Perspetiva dade pelo doente sobre AA do OMA a) vantagens b) vantagens de acordo com a situação profissional dos doentes c) preocupações de acordo com escolaridade dos doentes e) sugestões de melhoria
No que concerne às preocupações relacionadas com a AA (Figura 2c) verificou-se que em 57% dos casos nã existiram receios ou preocupações associadas a este procedimento.
Os erros de administração ou manipulação do OMA representaram 28% do total das preocupações apresentadas. Apenas um doente referiu preocupações relacionadas com esquecimentos, outro referiu receio de ineficácia da terapêutica em AA e um outro referiu receio de reações adversas.
Na tentativa de procurar uma associação entre as principais preocupações e a escolaridade dos participantes (Figura 2d), ainda que sem qualquer poder conclusivo,
dada a dimensão da amostra, verificou-se que preocupações relacionadas com possíveis reações adversas ao OMA em AA foram referidas por um doente pertencente ao grupo de grau académico superior a licenciatura.
Adicionalmente, a preocupação com possível ineficácia da terapêutica com OMA foi referida por um doente pertencente ao grupo com licenciatura e o esquecimento foi considerado como uma preocupação para um único doente pertencente ao grupo com ensino secundário.
No que diz respeito a sugestões para melhoria deste processo (Figura 2e), 52 % dos doentes consideraram-se totalmente satisfeitos na modalidade de AA do OMA e 28% sugeriu melhoria na simplificação do processo de entrega do OMA.
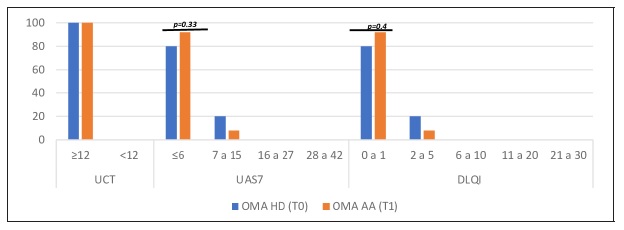
Controlo da UCE e segurança da terapêutica com OMA em AA Ainda em HD, todos os doentes apresentavam bom controlo da UCE, com UCT ≥12 (Tabela 3). Os dados da Tabela 2 reforçam o bom controlo da UCE conseguido nestes doentes, onde se verifica que 40% já se encontravam sem terapêutica anti-H1 diária, tendo mesmo alguns doentes conseguido alargar o intervalo entre administrações de OMA: 5 semanas em (1 doente), 6 semanas (6 doentes), 7 semanas (4 doentes) e 8 semanas (3 doentes).
Tabela 3 Controlo da urticária crónica espontânea e segurança da terapêutica com omalizumab
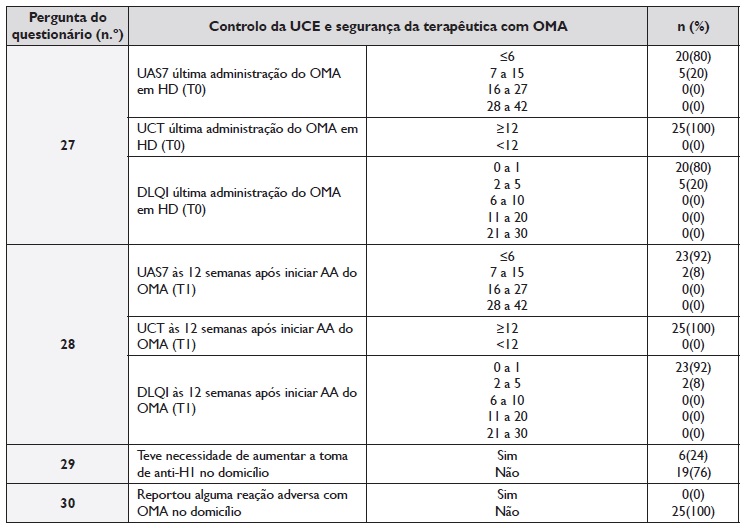
UCE - Urticária crónica espontânea; OMA - Omalizumab; HD - Hospital de Dia de imunoalergologia; AA - Autoadministração; UAS7 - Atividade da urticária nos últimos 7 dias; UCT - Teste de controlo da urticária; DLQI - Índice de qualidade de vida em dermatologia; anti-H1 - Anti-histamínicos H1 de segunda geração não sedativos
Os dados da Tabela e Figura 3 permitem verificar que a transição para AA de OMA possibilitou uma melhoria, ainda que não estatisticamente significativa, na evolução dos scores de controlo da UCE e QoL reportados pelos doentes (PROM). No período avaliado, verificou-se que para além de todos os doentes terem mantido o score UCT ≥12, 12% dos doentes com UAS7 entre 7-15 passaram a ter UAS ≤6 e 12% com DLQI entre 2-5 passaram a ter um DLQI entre 0-1. De destacar, no entanto, que 24% dos doentes referiram ter sentido necessidade de aumentar a dose de anti-H1, apesar deste aumento ter sido apenas pontual e na proximidade da administração subsequente de OMA. Relativamente à segurança, não foram reportadas reações adversas do OMA em AA.
DISCUSSÃO
No período em que decorreu o estudo, os doentes com UCE em AA de OMA representavam 23,6% do total de doentes com UCE sob tratamento com OMA no nosso Serviço de Imunoalergologia. Globalmente, os doentes inquiridos consideraram a possibilidade de AA como vantajosa ou mesmo muito vantajosa, apontando o menor tempo despendido e a redução de custos com as deslocações como as principais vantagens.
A ausência de absentismo laboral é outro aspeto relevante resultante da instituição da modalidade de AA. Estes resultados estão em conformidade com os apresentados por Gonçalves M et al 16, relativo à administração extra-hospitalar de OMA e por Timmerman et al 17 e Silva I et al 18 na AA de OMA na asma grave.
Na maioria dos doentes, o processo de administração foi considerado simples e prático, tendo sido os ensinos práticos realizados em HD (complementado com os folhetos disponibilizados) o aspeto mais valorizado para essa aprendizagem. Em conformidade com esta avaliação, 52% de doentes consideraram não existir nenhuma preocupação relacionada com a AA.
Este estudo reforça ainda os resultados apresentados num estudo retrospetivo prévio realizado no Reino Unido por Denman S et al 19, onde se incluíram 137 adultos doentes com UCE e que concluiu que a AA de OMA no domicílio é uma alternativa efetiva e segura à administração hospitalar, com consequente menor impacto na vida diária destes doentes.
Ainda relativamente à segurança da terapêutica com OMA, de facto não seria expectável o desenvolvimento de nenhum efeito adverso deste tratamento na modalidade de AA em relação com a administração em HD.
Ainda assim, a mudança do contexto de administração para ambiente domiciliário poderia tornar os doentes mais suscetíveis a reportar eventuais efeitos adversos suspeitos, o que não se verificou.
Por fim, e não menos importante, destacam-se as sugestões apresentadas pelos utentes relativas ao processo associado à AA de OMA, onde as questões mais burocráticas relacionadas com o pedido de OMA foram apontadas como aspetos a melhorar. A sua valorização poderá possibilitar uma maior otimização de todo o circuito envolvido neste processo, apesar de já ser visto pelos seus utilizadores como muito vantajoso.
Neste trabalho são abordados vários aspetos de extrema importância para prática clínica hospitalar, sendo até à data, e de acordo com a exaustiva revisão bibliográfica dos autores, o primeiro estudo na UCE realizado em Portugal com estes objetivos e que se refere exclusivamente a AA do omalizumab no domicílio, possibilitando conhecer a realidade nacional.
CONCLUSÕES
O controlo clínico e ausência de impacto na QoL dos doentes, documentado pela evolução do registo dos PROM, aliado à inexistência de reações adversas reportadas, permite inferir que a eficácia e segurança do OMA foi mantida na AA.
Estes dados, associados à maior satisfação dos doentes, reforçam a importância e relevância da instituição desta medida.
Estudos adicionais com maior número de participantes poderão dar robustez aos resultados obtidos neste primeiro estudo e incluir a avaliação do benefício da redução do absentismo laboral, ganho de tempo individual e consequente redução dos custos para o doente resultante da aplicação desta medida. Adicionalmente, seria pertinente uma quantificação do impacto da AA de OMA no orçamento hospitalar, avaliando os custos adicionais com a organização do processo e envio da medicação aos utentes, em paralelo com a redução da despesa com prestação de cuidados por profissionais de saúde e com uma maior rentabilização da ocupação do HD.