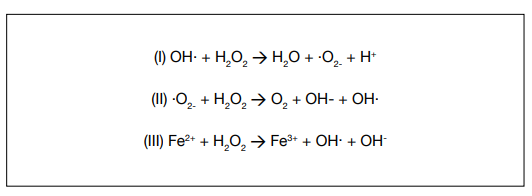INTRODUÇÃO
A infertilidade é uma doença do sistema reprodutivo masculino e/ou feminino definida pela incapacidade de atingir uma gravidez após 12 meses ou mais de relações sexuais regulares desprotegidas. No caso de casais com mais de 35 anos, este tempo é reduzido para 6 meses. Atualmente, verifica-se um crescente número de pessoas que sofrem de infertilidade, e as preocupações aumentam a nível mundial. Estima-se que afete 1 em cada 6 casais, existindo uma contribuição igual do homem e da mulher para o número de casos (1-3).
A infertilidade pode ter diferentes etiologias, e por vezes, pode não ser possível estabelecer uma causa. Estima-se que cerca de 20% dos casos de infertilidade tenham origem no homem ou na mulher, sendo que 15% se definem por infertilidade sem causa aparente (ISCA) ou Idiopática, e 20 a 30% pela combinação de fatores adversos do casal (4). Desta forma, para um determinado casal, poderá existir uma única causa em qualquer dos parceiros, ou uma combinação de fatores que impedem a conceção ou a continuidade da gravidez.
No que diz respeito às causas mais comuns nas mulheres, pode-se observar ciclos menstruais irregulares e anovulação, endometriose e obstrução da trompa de Falópio. Nos homens, as causas mais comuns correspondem a alterações fisiológicas, na mobilidade, e na contagem dos espermatozoides (4).
A origem destas causas pode estar associada ao estilo de vida moderno ou a alterações metabólicas, que se observam frequentemente com o aumento da idade materna, obesidade, diabetes, ansiedade, consumo de álcool, tabaco e exposição aos poluentes ambientais, incluindo os que atuam como desreguladores endócrinos. Um fator comum a estas condições é a produção excessiva de espécies reativas de oxigénio (ERO) que podem dar origem ao stress oxidativo se a capacidade antioxidante do indivíduo for insuficiente ou ineficaz na realização de reações de oxidação-redução (5). Este ambiente está associado ao desenvolvimento de inflamação sistémica de baixo grau, aumentando o risco de infertilidade (6).
Acredita-se que o stress oxidativo pode contribuir para a infertilidade ao interferir em processos que são fundamentais na reprodução, incluindo espermatogénese, foliculogenése, fertilização, implantação e placentação (5)
Assim, o objetivo da presente revisão de literatura é estudar se existe uma associação entre o stress oxidativo e a incidência de infertilidade.
METODOLOGIA
A pesquisa foi realizada na base de dados Pubmed, entre fevereiro e abril de 2023. Utilizou-se como palavras-chave: "oxidative stress", "fertility", "infertility", "female infertility" e "male infertility". Não foi considerado um limite temporal do tempo de publicação. Foram incluídos apenas estudos na língua inglesa e estudos realizados em humanos, tendo sido excluídos estudos em animais. Foram encontrados 212 artigos. Com base no título e leitura do resumo foram selecionados 77 artigos, e após a leitura completa dos últimos, foram selecionados 37 artigos para integrar o presente trabalho de revisão. Foram ainda adicionados 5 artigos de forma manual.
Espécies Reativas de Oxigénio, Stress Oxidativo e Fertilidade
As ERO foram identificadas por Fenton em 1894. No entanto, a reação em cadeia de processos produtivos de ERO foi primeiramente mencionada por Haber e Willstatter em 1931. Em 1949, Weiss aceitou a reação proposta, desde então conhecida como reação de Haber-Weiss (Figura 1) (7).
A adição de um eletrão ao oxigénio (O2 ) forma o radical anião superóxido (O2 °), a forma primária de ERO. Por sua vez, o O2 ° é convertido a radical hidroxil (OH°), radical peroxil (ROO°), peróxido de hidrogénio (H2 O2 ) ou, em alguns casos, a peróxidos de nitrogénio (NOx). A produção de ERO pode resultar do metabolismo energético, particularmente durante a fosforilação oxidativa, através da nicotinamida adenina dinucleótido fosfato (NADPH) e de várias outras oxidases (8). As ERO sofrem posteriormente processos de oxidação-redução (redox) em cascata mediados por antioxidantes, originando moléculas mais estáveis. Perante um organismo em homeostase, as espécies reativas de oxigénio promovem a expressão de mtRNA, contribuíndo consequentemente para o aumento de mitocôndrias (9). Contudo, o desequilíbrio celular entre a produção de ERO e os antioxidantes pode levar a uma acumulação das primeiras, originando o stress oxidativo. De entre os vários tipos de ERO, consideram-se especialmente tóxicas para as células o O2° e o H2O2 (6). Em excesso, as ERO estão associadas a danos no ADN, peroxidação lipídica, e danos em diversas proteínas, sendo consequentemente correlacionadas com o desenvolvimento de uma série de patologias crónicas, como o alzheimer, diabetes mellitus tipo 2, e infertilidade (10).
A origem das ERO é natural e endógena. No entanto, existem outras fontes de ERO, nomeadamente o tabaco, a poluição, o uso de pesticidas, e desreguladores endócrinos como bisfenóis e outros aditivos plásticos, parabenos e ftalatos. Desequilíbrios nutricionais, excessos alimentares, privação de energia e exercício físico excessivo, e o envelhecimento também afetam o metabolismo das ERO (8). O stress oxidativo ocorre com a produção excessiva de ERO ou perante uma reduzida concentração de antioxidantes.
Existem dois tipos de antioxidantes no organismo: antioxidantes não enzimáticos e antioxidantes enzimáticos. Os enzimáticos incluem superóxido dismutase (SOD), glutationa peroxidase (GPx), catalase (CAT) e glutationa redutase (GSR), que podem causar a redução de H2 O2 a água e álcool. Os não enzimáticos são por exemplo o ascorbato (vitamina C), alfa-tocoferol (vitamina E), beta-caroteno, glutationa, taurina, entre outros (10).
Como exemplo da atividade de um antioxidante não enzimático, descreve-se o alfa-tocoferol, que promove a rutura de cadeia e inibe a peroxidação lipídica nas membranas, eliminando os radicais peroxil (RO-) e alkoxil (ROO-). A capacidade do alfa-tocoferol para manter uma taxa estável de redução do radical peroxil na membrana, depende da reciclagem de alfa-tocoferol por agentes redutores externos como por exemplo o ascorbato ou os compostos de tiol (11). Neste sentido, o polimorfismo nas enzimas antioxidantes ou a restrição dietética de micronutrientes podem desempenhar um papel importante na predisposição para o stress oxidativo, e consequentemente para as complicações da gravidez (12).
No que diz respeito ao sistema reprodutor, o stress oxidativo pode afetar a qualidade dos gametas, oócitos, espermatozoides, embriões e os respetivos ambientes. Por outro lado, pode afetar o desenvolvimento embrionário precoce e a implantação, o que por sua vez pode comprometer a taxa de gravidez (4). Adicionalmente, tem sido associado com o impacto negativo da estimulação ovariana, assim, no potencial desenvolvimento de oócitos na fertilização in vitro (FIV) (13).
Stress Oxidativo e Infertilidade Masculina
Estima-se que quantidades elevadas de ERO contribuam para 30 a 80% dos casos diagnosticados de infertilidade masculina (14). Os espermatozoides são muito propensos à oxidação, uma vez que são células incapazes de restaurar os danos induzidos pelo stress oxidativo, por não possuírem sistemas de reparação citoplasmáticos-enzimáticos. Adicionalmente, as suas membranas celulares são predominantemente ricas em ácidos gordos poli-insaturados (PUFAs), o que as torna altamente suscetíveis a peroxidação lipídica. Na presença de stress oxidativo, verifica-se uma rápida perda de adenosina trifosfato (ATP), com consequentes aumentos dos defeitos morfológicos dos espermatozoides, redução da motilidade, e limitação da sua viabilidade (15).
Os danos no ADN de espermatozóides promovem uma limitação significativa na fertilidade natural, e estão relacionados com efeitos adversos clínicos como a infertilidade, abortos recorrentes, mortalidade infantil, doenças genéticas na descendência, entre outros (16).
As fontes endógenas de ERO seminal são produzidas principalmente por leucócitos ou por espermatozoides anormais ou imaturos (17). Por outro lado, as principais fontes exógenas correspondem a aspetos relacionados com o estilo de vida como o tabagismo, consumo excessivo de bebida alcoólica, má alimentação, vida sedentária, stress psicológico, assim como obesidade, fatores ambientais como exposição à radiação eletromagnética e toxinas, e idade paterna avançada (acima de 40 anos) (16). Na verdade, ao contrário das mulheres cuja fertilidade diminui com o avançar da idade, o homem produz espermatozoides durante toda a vida, a partir da puberdade. Contudo, vários estudos sugerem que as defesas antioxidantes diminuem com a idade, oferecendo uma permissa justificativa para o envolvimento do stress oxidativo na patogénese das alterações reprodutivas do homem associadas ao envelhecimento (16, 18).
Por outro lado, é importante ressalvar que a inflamação é uma das principais causas da infertilidade masculina. Durante a inflamação, os níveis de mediadores pró-inflamatórios no trato reprodutor masculino são maiores que o habitual, e essas respostas inflamatórias no sistema genital masculino estão indissociavelmente ligadas ao stress oxidativo (19).
Por sua vez, a presença de inflamação crónica no trato geniturinário pode estar associada a patologias como a varicocele e a leucocitospermia. A varicocele é uma condição em que o plexo venoso pampiniforme no interior do cordão espermático se dilata e se torce de forma anormal. A prevalência é de 15 a 20% em homens saudáveis, aumentando significativamente para 25 a 40% em homens com problemas reprodutivos, resultando num aumento dos níveis de ERO no sémen e uma diminuição da capacidade antioxidante (20).
A leucocitospermia corresponde ao aumento da quantidade de leucócitos no esperma. Os leucócitos produzem ERO para combater a infecção e destruir agentes patológicos, resultando num aumento significativo. Estima-se que cerca de 10 a 20% dos homens inférteis tenham concentrações elevadas de leucócito seminal, que podem ser causadas por infeções ou respostas inflamatórias (21, 22).
Stress Oxidativo e Infertilidade Feminina
O stress oxidativo influencia todo o sistema reprodutivo da mulher. No ovário, está relacionado com a restrição da maturação folicular e do crescimento do oócito, menor número de oócitos disponíveis, síndrome do ovário poliquístico (SOP) e aumento anormal da hormona folículo-estimulante (FSH). Nos oócitos, atua na fragmentação de ADN, dano do fuso meiótico, aneuploidia dos oócitos, disfunção mitocondrial e diminuição da taxa de fertilização. No útero, a presença de stress oxidativo reduz a possibilidade de implantação, podendo também estar relacionado com endometriose, pré-eclampsia, restrição do crescimento fetal, placentação anormal e abortos espontâneos. Adicionalmente, no embrião, este fenómeno metabólico inibe o processo embrionário precoce, e promove a apoptose, diminuição da produção de ATP, alterações epigenéticas, e diminuição da formação e da qualidade dos blastoncistos (23).
Os efeitos adversos do stress oxidativo no trato reprodutor feminino têm sido bem documentados ao longo dos anos. Sugere-se que a produção de ERO seja influenciada pelo citocromo p450, e o próprio corpo lúteo parece ser também umas das principais fontes. O stress oxidativo tem efeito direto no oócito, no embrião e na implantação, causando peroxidação lipídica da membrana celular, oxidação das proteínas celulares e danos no ADN (24).
Adicionalmente, o envelhecimento ovariano, a ovulação recorrente e a obesidade são também fontes de ERO nos ovários, assim como os fatores ambientais, tabagismo, consumo de bebidas alcoólicas e alimentação desequilibrada (25).
O envelhecimento leva ao aumento da produção de ERO e diminuição da atividade dos sistemas antioxidantes. A acumulação de danos no ADN é um dos fatores-chave na deterioração da qualidade dos oócitos com a idade, assim como a disfunção mitocondrial. A idade é o fator intrínseco mais importante que afeta a função ovárica e a fertilidade. Com o envelhecimento, o número de folículos primordiais diminui exponencialmente, enquanto que a frequência de aneuploidia nos oócitos aumenta, levando a uma redução significativa das taxas de gravidez e das taxas de nados-vivos. Vários trabalhos demonstram que a fertilidade de uma mulher diminui linearmente em cerca de 10% por ano após os 35 anos, chegando a apenas 1% de fertilidade aos 43 anos (26).
O desequilíbrio entre agentes oxidantes e antioxidantes é visto em mulheres que sofrem de SOP, e esse stress oxidativo é devido a diversas anormalidades metabólicas como a obesidade, hiperinsulinémia e dislipidémia. A SOP é uma doença endócrina, cuja prevalência varia entre 5 a 13% durante a idade reprodutiva. A sua associação com a infertilidade é comum, ocorrendo em 70 a 80% das mulheres. O aumento de ERO está associado ao aumento de citocinas próinflamatórias e mediadores de inflamação, como o tumor necrosis factor-alpha (TNF-α) e ativação da via de sinalização celular do nuclear factor kappa-B (NF-kB), promovendo o processo inflamatório. Os mediadores inflamatórios estimulam a produção andrógena no ovário, levando ao hiperandrogenismo típico da SOP. Consequentemente, um ciclo vicioso é criado no epitélio ovariano, resultando na formação de quistos, baixa qualidade ovariana folicular e infertilidade (27, 28).
Atualmente é amplamente aceite que o stress oxidativo pode implicar na fisiopatogenia da endometriose. A endometriose é uma doença inflamatória pélvica, dependente de estrógenio, caracterizada pela implantação e crescimento do tecido endotelial fora da cavidade uterina. Afeta cerca de 10 a 15% das mulheres em idade reprodutiva. Os sintomas mais comuns são dor pélvica e infertilidade, assim como dismenorreia e dispareunia. O stress oxidativo é induzido pela translocação de macrófagos, eritrócitos e tecido endotelial apoptótico para a cavidade peritoneal através da menstruação retrógrada, pelo que a produção peritoneal de ERO pode estar envolvida na endometriose (29).
ANÁLISE CRÍTICA
No presente estudo, foi realizada uma revisão da literatura mais recente, que aborda e relaciona o stress oxidativo com a infertilidade, tanto masculina como feminina. É um tema bastante atual e de extrema relevância para um melhor entendimento da infertilidade, e dessa maneira, contribui na procura de melhores estratégias no tratamento da referida condição clínica.
Como mencionado anteriormente, os espermatozóides são extremamente vulneráveis à oxidação, gerando stress oxidativo. Um recente estudo foi capaz de comprovar essa questão ao avaliar a associação entre baixa motilidade do esperma com níveis elevados de citocinas pró- inflamatórias e níveis elevados do marcador oxidativo malondialdeído (MDA) (30). Adicionalmente, pacientes com varicocele apresentaram melhores parâmetros seminais após o tratamento da doença e apresentaram menores níveis de peroxidação lipídica e de danos de ADN (31). A varicocele causa isquémia da veia espermática que leva a maiores quantidades de citocinas inflamatórias e óxido nítrico e de essa forma desencadeiam a ativação da resposta inflamatória, o recrutamento de leucócitos e, consequentemente, a formação de ERO (20).
No sistema reprodutor feminino o stress oxidativo demonstra um impacto negativo na reposta ovariana. Foi observado no fluido folicular uma menor atividade de enzimas antioxidantes, como a glutationa transferase, glutationa redutase e glutationa peroxidase em mulheres com baixa reserva ovariana, em comparação com mulheres saudáveis, além de concentrações elevadas de marcadores oxidativos e de citocinas pró-inflamatórias. O fluido folicular cria o microambiente para o oócito em desenvolvimento, e tem um impacto direto na qualidade do oócito, implantação e no desenvolvimento embrionário inicial. Um desequilíbrio na produção de ERO no fluido folicular, portanto, pode ter um efeito adverso no processo da fertilidade (32).
Marcadores de stress oxidativo são anormais em mulheres com SOP, sugerindo que o stress oxidativo pode ser participante da fisiopatogenia da doença (33), assim como relatado em uma revisão sistemática e meta-análise em que mulheres com SOP demonstravam ter níveis circulantes elevados de marcadores bioquímicos como a homocisteína e MDA, e menores níveis de glutationa (34). Adicionalmente, mulheres com endometriose verificaram um aumento significativo de peroxidação lipídica, visível pelo aumento da concentração de MDA, e uma diminuição na capacidade total antioxidante, tanto no soro como o fluido folicular, em comparação com o controlo saudável (35). A superprodução de ERO também pode impactar negativamente o sucesso de técnicas de reprodução assistida (36,37). Noutro estudo, Ahelik e colaboradores (38) tiveram como objetivo verificar níveis de stress oxidativo em ambos os parceiros de casais submetidos a técnicas de reprodução assistida. Como resultado, os biomarcadores de stress oxidativo medidos encontravam-se aumentados em condições clínicas adversas, como infeção no trato genital, endometriose, mioma uterino e tabagismo. Além disso, foram observados níveis mais elevados de stress oxidativo em ambos os parceiros quando as gravidezes bioquimicamente detetáveis não evoluíram para clinicamente detetáveis.
Tendo em consideração os trabalhos descritos, pode-se considerar que o elevado nível de stress oxidativo parece afetar negativamente o resultado da fertilização, e poderá fazer sentido integrar a avaliação da presença de stress oxidativo em pacientes submetidos a técnicas de reprodução assistida. Neste sentido, poder-se-ia selecionar pacientes com maior taxa de sucesso e/ou aqueles que requerem terapias antioxidantes, o que levaria a uma melhoria dos resultados de sucesso dessas técnicas de fertilização, assim como a fertilidade natural.
Similarmente, foi verificado que níveis elevados de antioxidantes no fluido folicular foram associados positivamente com melhores resultados de FIV, assim como o estado de stress oxidativo nos casais foi associado negativamente a várias hormonas reprodutivas e ao estado de tabagismo (39). Dessa forma, reforça-se que a deteção de biomarcadores de stress oxidativo podem ter aplicações na avaliação clínica de pacientes que se submetem a FIV, tais como as causas da infertilidade, o perfil hormonal, a taxa de fertilização, a implantação e número de nados-vivos. A alteração da produção de hormonas reprodutivas pode ser explicada pelo fato de que níveis elevados de stress oxidativo podem afetar o funcionamento do eixo hipotálamo-hipófise-gonodal (40).
Tendo em conta o importante papel que o stress oxidativo desempenha na etiologia da disfunção do esperma e do oócito, o estudo de revisão de Aitken (13) relatou que os antioxidantes podem apresentar um papel terapêutico, tanto na regulação dos resultados da FIV, como no impacto do envelhecimento na fertilidade. In vitro, foi demonstrado que uma variedade de antioxidantes aumenta a fertilidade dos oócitos após a maturação. Foram registrados impactos positivos na administração de alfa-tocoferol isolado ou em combinação com outros antioxidantes (ácido alfa-lipólico, hipotaurina e N-acetil cisteína), ácido 9-cis-retinoico, coenzima Q10, melatonina, ácido rasmarínico e o flavonoide antioxidante dos cítricos, a hisperitina.
No entanto, segundo uma meta-análise da Cochrane realizada em 2022, existe uma evidência baixa sobre os benefícios do uso de suplementação de antioxidantes em homens subférteis. Dos 67 estudos incluídos no artigo, apenas 20 estudos relataram, uma gravidez clínica, e destes, apenas 12 relataram taxas de nascimento com vida. Neste sentido, ainda são necessários mais ensaios clínicos aleatórios controlados por placebo para clarificar o papel exato dos antioxidantes (41).
Corroborando com estes dados, outra meta-análise da Cochrane (2020) sobre o uso de suplementos antioxidantes, desta vez na subfertilidade feminina, também relatou baixa evidência sobre sua eficácia. Foram incluídos 67 estudos randomizados com um total de 7760 mulheres, e foram investigados diferentes antioxidantes tais como N-acetil cisteína (NAC), melatonina, L-arginina, mio-inositol, carnitina, selénio, vitamina E, vitaminas do complexo B, vitamina C, vitamina D juntamente com cálcio, coenzima Q10 e ácidos gordos da família ômega 3. Segundo o estudo, os antioxidantes tiveram uma ligeira associação com o aumento de taxas de nascimento e de gravidez clínica. No entanto, a qualidade da evidência foi baixa e com uma heterogeneidade de moderada a alta, uma vez que os ensaios incluíram mulheres com diferentes indicações e diferentes tipos de antioxidantes (42).
CONCLUSÕES
A partir da presente revisão é possível afirmar que o stress oxidativo desempenha um papel importante na infertilidade feminina e masculina, constituindo implicações claras para a prevenção, diagnóstico e resolução terapêutica de tais condições. Neste sentido, no que diz respeito ao papel da nutrição neste contexto, seria importante a realização de mais ensaios clínicos duplo-cegos randomizados nesta temática, com o intuito de compreender verdadeiramente o papel destas moléculas contra os danos do stress oxidativo no sistema reprodutor, e avaliando dessa forma, a possibilidade de integrar determinados antioxidantes como estratégia para o tratamento e/ou prevenção da infertilidade.