Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Nascer e Crescer
versão impressa ISSN 0872-0754
Nascer e Crescer vol.25 no.2 Porto jun. 2016
ARTIGOS DE REVISÃO / REVIEW ARTICLES
Reações de hipersensibilidade a meios de contraste em idade pediátrica
Hypersensitivity reactions to contrast media in children
Maria Miguel AlmiroI,IV; Catarina MaiaII,IV; Liliana BrancoIII,IV; Cláudia PedrosaII,IV; Jorge RomarizII,IV; Fátima PraçaII,IV; Herculano CostaII,IV
I S. de Pediatria, Centro Hospitalar Baixo Vouga. 3814-501 Aveiro, Portugal. mariamiguelaa@gmail.com
II S. de Pediatria, Centro Hospitalar de Vila Nova de Gaia/Espinho. 4400-129 Vila Nova de Gaia, Portugal. catarinammaia@gmail.com; claudiampedrosa@yahoo.com; jaromariz@gmail.com; fatimapraca@sapo.pt herculano.costa@chvng.min-saude.pt
III S. de Pediatria, Hospital da Senhora da Oliveira – Guimarães, Centro Hospitalar Alto Ave. 4835-044 Guimarães, Portugal. brancoliliana@hotmail.com
IV Unidade de Imunoalergologia e Pneumologia Pediátrica, Centro Hospitalar de Vila Nova de Gaia/Espinho. 4400-129 Vila Nova de Gaia, Portugal. herculano.costa@chvng.min-saude.pt
RESUMO
Introdução: Os procedimentos diagnósticos e terapêuticos com utilização de produtos de contraste são muito frequentes na prática clínica. Qualquer um destes agentes pode ser responsável por reações de hipersensibilidade, com um amplo espetro de gravidade.
Objetivos: Revisão da epidemiologia, manifestações clínicas, diagnóstico e prevenção das reações de hipersensibilidade aos produtos de contraste em idade pediátrica.
Desenvolvimento: Os produtos de contraste incluem meios radiológicos e não radiológicos. Ambos os grupos podem causar reações de hipersensibilidade imediata (quando ocorrem na primeira hora após exposição) e não imediata (quando ocorrem após a primeira hora). Imunologicamente aparentam ser mediadas por IgE e por células T, respetivamente. A investigação alergológica tem como objetivo confirmar o potencial agente causal e identificar agentes alternativos. Esta processa-se sequencialmente através da história clínica, testes cutâneos e possível prova de provocação. Em casos de alergia confirmada, estes meios devem ser evitados.
Conclusões: A abordagem sistematizada em caso de hipersensibilidade a produtos de contraste permite reduzir o número de reações adversas subsequentes, bem como a utilização de produtos alternativos com maior segurança.
Palavras-chave: Contraste iodado; Gadolínio; Hipersensibilidade imediata; Hipersensibilidade não imediata; Meios de contraste; Prova de provocação; Sulfato de bário; Testes cutâneos.
ABSTRACT
Introduction: Even though diagnostic and therapeutic contrast-enhanced procedures are very frequently performed in clinical practice, the underlying contrast media may be associated with a wide range of hypersensitivity reactions.
Objective: Overview of epidemiology, clinical presentation, diagnosis and prevention of hypersensitivity reactions to contrast media in pediatric population.
Results: There are two major groups of contrast media: radiologic and non-radiologic, and both may cause hypersensitivity reactions. These reactions can be differentiated according to the time interval between contrast administration and the first appearance of symptoms as: immediate (when they occur during the first hour after administration) or non-immediate (when they occur between one hour up to ten days after administration). IgE-mediated and T cell-mediated immunologic mechanisms appear to be involved in these reactions, respectively. Clinical management aims to determine potential culprit and to identify alternative contrast agents via detailed anamnesis, skin tests and even a possible provocation test. In confirmed cases the culprit preparation should be avoided.
Conclusions: A systematic approach to cases of hypersensitivity reaction to contrast media contributes to prevent recurrent reactions and to administrate alternative contrast media more safely.
Keywords: Barium Sulfate; Contrast media; Delayed Hypersensitivity; Gadolinium; Immediate Hypersensitivity; Provocation test; Radiocontrast media; Skin tests.
INTRODUÇÃO
Anualmente, em todo o mundo, são realizados cerca de 75 milhões de procedimentos diagnósticos e terapêuticos com meios de contraste (MC).1–3
O espetro de fármacos incluído na denominação de meio de contraste inclui meios radiológicos (que absorvem raios X; exemplo: produtos iodados) e meios não radiológicos (utilizados em exames sem radiação; exemplo: gadolínio). Estes diferentes produtos são utilizados consoante o objetivo da investigação imagiológica, a faixa etária do doente e os fatores de risco associados (história anterior de reações adversas a meios de contraste, insuficiência renal, diabetes ou insuficiência cardíaca congestiva, entre outros).2,4,5
Qualquer produto de contraste administrado por via endovenosa, retal, oral ou por contacto direto, apesar de ser considerado seguro, pode ser responsável por desencadear manifestações de hipersensibilidade.1,2 Os meios de contraste mais utilizados são os meios radiológicos iodados e por esse motivo são os meios com maior número de reações adversas descritas e com mais estudos realizados.
Apesar das reações adversas serem pouco frequentes, quando ocorrem podem ser graves e fatais, podendo recorrer numa segunda exposição ao mesmo agente.1,2,6,7 Por esse motivo, qualquer reação de hipersensibilidade após utilização de meios de contraste deve ser exaustivamente investigada em Consulta de Imunoalergologia.
A investigação alergológica tem dois objetivos fundamentais: confirmar o potencial agente causal (para que este possa ser evitado, de forma a prevenir recorrências); e identificar agentes alternativos (opções que não causem reações de hipersensibilidade).
OBJETIVOS E MÉTODOS
Revisão dos conceitos de reações de hipersensibilidade a meios de contraste, apresentando uma proposta de abordagem diagnóstica em idade pediátrica.
Efetuou-se pesquisa de normas de orientação clínica/guide- lines, revisões sistemáticas, metanálises e ensaios clínicos controlados, nas bases de dados da Guidelines Finder, Cochrane Library e Pubmed, publicados nos últimos dez anos, em inglês, português, espanhol ou francês, com os termos MeSH Barium Sulfate, Contrast media, Gadolinium, Radiocontrast media, Immediate Hypersensitivity, Delayed Hypersensitivity, Skin test e Provocation test.
DESENVOLVIMENTO
Caracterização dos meios de contraste
Meios de Contraste Radiológico (MCR)
Incluem substâncias com capacidade de absorver raios X. A escolha dos elementos apropriados limitou-se ao iodo, ao bário (utilizado unicamente sob a forma de sais insolúveis e não absorvíveis) e ao tândalo (utilizado em broncografia), atendendo a que estes elementos combinam uma capacidade de absorção de radiação satisfatória com uma tolerância orgânica aceitável.4
Produtos Iodados
A estrutura química comum à maioria destes compostos é a molécula de benzeno à qual se ligam vários átomos de iodo (ha- bitualmente 3).2,4 Existem várias propriedades físicas e químicas que os caracterizam, diferenciam e que devem ser considera- das, nomeadamente: 2,3,8–11
- Carga da molécula iodada: iónica/não iónica;
- Estrutura molecular: monómeros/dímeros;
- Radiopacidade: depende da concentração do iodo na solução de contraste, resultante do número de átomos de iodo na molécula;
- Viscosidade: consiste na resistência à perfusão do fluido, importante em particular na população pediátrica (aumentar a temperatura do meio de contraste reduz a viscosidade e melho- ra a tolerabilidade);
- Osmolalidade: depende do número das partículas em so- lução, sobretudo iões, podendo atingir valores 5 a 8 vezes superiores à osmolalidade plasmática. Estes meios podem subdividir-se em meios com alta osmolalidade, baixa osmolalidade ou iso-osmolalidade. Salienta-se que os meios iso-osmolares (pela aproximação à osmolalidade plasmática) apresentam osmolalidade inferior aos meios de baixa osmolalidade.
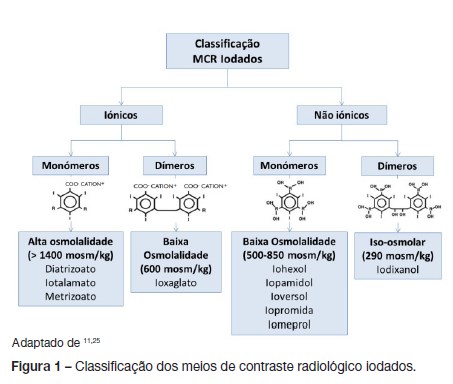
O objetivo a atingir com estes contrastes é obter a mais alta radiopacidade com a menor osmolalidade possível.4 Considerando conjuntamente as características: carga da molécula, estrutura molecular e osmolalidade, os produtos de contraste podem dividir-se em 4 grupos (Fig. 1):4,11
- Monómeros iónicos de alta osmolalidade (≥ 1400 mosm/ kg), são os meios de contraste convencionais, como o diatrizoato, iotalamato e metrizoato.
- Dímeros iónicos de baixa osmolalidade (600 mosm/kg), como o Ioxaglato.
- Monómeros não-iónicos de baixa osmolalidade (500850 mosm/kg), como o Iohexol, Iopamidol, Ioversol, Iopromida e Iomeprol.
- Dímeros não-iónicos iso-osmolares (290 mosm/kg), como o Iodixanol.
Os meios de contraste iodados recomendados para utilização em idade pediátrica são os monómeros não iónicos de baixa osmolalidade, atendendo ao menor número de reações adversas descritas.12,13 Os meios com estas características disponíveis em Portugal são: Iopamidol (Iopamiro®, Scanlux®), Ioversol (Optiray®), Iopromida (Ultravist®) e o Iomeprol (Iomeron®).4 Num estudo multicêntrico realizado nos Estados Unidos o meio mais utilizado em idade pediátrica foi o Ioversol.13
Produtos Baritados
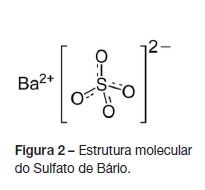
Os meios de contraste derivados do bário são os mais fre- quentemente utilizados para estudo do sistema digestivo em idade pediátrica (Fig.2).4 Podem ser administrados por via oral, retal ou através de ostomias, sob a forma de suspensões preparadas extemporaneamente ou já prontas para uso.4 Na suspeita de perfurações estes são contraindicados, sendo preferível utilizar meios iodados. As características mais importantes das suspensões de bário são o tamanho das partículas (pode variar desde décimos até algumas dezenas de micrómetro) e a viscosidade, que determinam a velocidade de sedimentação das partículas e a sua maior ou menor capacidade de revestir as mucosas.4,10
– Meios de Contraste Não Radiológicos (MCNR)
Este grupo é necessariamente heterogéneo, abrangendo compostos utilizados em ecografia, ressonância magnética nuclear e em medicina nuclear.4 Pela sua importância em idade pediátrica, os derivados do gadolínio serão os abordados.
Os meios de contraste utilizados em ressonância magnética são derivados do gadolínio e são geralmente considerados seguros em doentes com contraindicações à utilização de meios iodados, atendendo a que o risco de uma reação adversa a um meio de contraste com gadolínio é inferior ao risco a uma reação após exposição a um meio de contraste iodado.4-6,10,11 Apesar disso, as reações adversas graves podem ocorrer.5,6
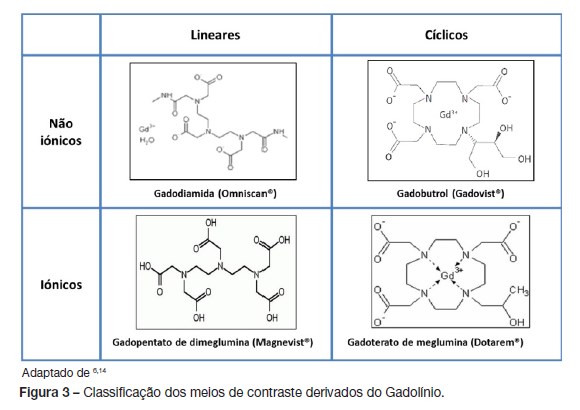
Como os meios de contraste iodados, os MCNR podem ser diferenciados consoante as suas propriedades físicas e químicas. Classificam-se de acordo com: a sua estrutura bioquímica (linear/cíclica); osmolalidade (630 a 1970 mosmol/kg); carga iónica (iónicos/não iónicos), viscosidade e ligação à albumina (Fig. 3).4,10,11
No entanto, estas propriedades físicas são menos relevantes, atendendo a que o volume utilizado nestes estudos é muito inferior ao necessário nos exames com meios iodados 5. A ve- locidade de perfusão habitualmente também é inferior, pelo que reduz os efeitos de extravasamento e lesão vascular.10
A farmacocinética da maioria é semelhante: são meios hidrófilos, com boa distribuição no espaço extracelular e excretados inalterados pelo rim. Existem exceções importantes, nomeadamente: o Gadoxetato dissódico, que penetra no hepatócito e tem excreção renal, biliar e fecal (mais utilizado em imagiologia hepática); o Gadobenato dimeglumina, que pela sua capacidade de ligação fraca e transitória às proteínas séricas e penetração hepatocitária é utilizado para visualizar o fígado, sistema nervoso central e coração; e o Gadobutrol, que pela sua elevada ligação à albumina (80-90%), se utiliza para estudos vasculares.6,11
Os meios de contraste derivados do gadolínio disponíveis para utilização em idade pediátrica (a partir dos 2 anos de idade) em Portugal são: Gadopentato de dimeglumina (Magnevist®), Gadobutrol (Gadovist®) e o Gadoterato de meglumina (Dotarem®).4,14 Em caso de necessidade de utilização de meios de contraste em idade inferior, a situação deve ser cuidadosamente avaliada pelo médico, sendo o meio mais recomendado o Gadoterato de meglumina (Dotarem®).14
Classificação das reações adversas a meios de contraste
Os meios de contraste podem causar uma grande diversidade de reações adversas, no entanto a fisiopatologia da gran- de maioria permanece desconhecida. Por este mesmo motivo existem vários sistemas de classificação baseando-se na gravidade da reação, no tempo decorrido entre administração do fármaco e o início da reação, manifestações clínicas ou suposto mecanismo fisiopatológico. Assim sendo, é possível dividir estas reações em 3 grandes grupos: reações tóxicas (incluindo vaso-vagais); reações de hipersensibilidade e as reações inespecíficas de origem indeterminada ou doenças não relacionadas (exemplo urticária crónica idiopática) (Fig. 4).1–3,11
As reações tóxicas a MC, também denominadas reações fisiológicas, estão relacionadas com as propriedades químicas dos diferentes meios de contraste (exemplo: osmolalidade), sendo dependentes da dose e da velocidade de perfusão. Estas são mais frequentes com os MCR iodados, podendo também ocorrer com derivados do gadolínio.5 São geralmente autolimitadas e incluem sensação de calor, náusea, vómitos, convulsões, arritmias e toxicidade orgânica (tiroideia, nefro e neurotoxicidade). Estas manifestações não são contraindicação para uma nova exposição ao meio de contraste. As reações vaso-vagais são muitas vezes incluídas neste grupo. Este último tipo de reação é relativamente comum e associado a um aumento do tónus vagal, diminuição da atividade dos nós sinoauricular e auriculoventricular, com inibição da condução auriculoventricular. Estas alterações fisiológicas resultam em sensação de desmaio, hipotensão e bradicardia. Os sintomas melhoram com a diminuição da velocidade de perfusão e não são contraindicação para reexposição ao MC.1,2,11
As reações de hipersensibilidade são idiossincráticas, independentes da dose ou da velocidade de infusão, podendo ocorrer mesmo com quantidades mínimas e sem exposição prévia ao meio de contraste. Podem ser diferenciadas de acordo com o tempo entre a exposição ao MC e o aparecimento de sintomas em 2 grandes grupos: reações imediatas (quando ocorrem na primeira hora) ou reações não imediatas (quando ocorrem entre uma hora e os 10 dias subsequentes).1,2,11
Fisiopatologia das Reações de Hipersensibilidade
- Reações de Hipersensibilidade Imediata (RHI)
O mecanismo deste tipo de reações permanece desconhecido e sob investigação. Considerou-se como causas possíveis: o efeito direto do MC nas membranas dos mastócitos, relacionado com a sua osmolalidade e estrutura química (pseudoalergia); a ativação do complemento; a formação de bradicininas; ou um mecanismo IgE mediado.7 Existem algumas evidências indiretas de que estas reações possam ser causadas por um mecanismo IgE mediado, nomeadamente por: associação destas reações à libertação de histamina pelos mastócitos e basófilos; extensa ativação in vitro dos mastócitos de doentes com estas reações; doentes com RHI a meios de contraste têm níveis elevados de histamina e triptase, correlacionando-se esta elevação com a gravidade da reação; e testes cutâneos positivos para MC em doentes com RHI graves.1,8,11
- Reações de Hipersensibilidade Não Imediata (RHNI)
A maioria destas reações aparenta ser mediada por células T, atendendo a que a sua manifestação clínica mais típica consiste num exantema maculopapular, que se assemelha a outras reações alérgicas a fármacos mediadas por células T. O início da erupção cutânea costuma ser entre 2 a 10 dias após a primeira exposição a MC e 1 a 2 dias após uma reexposição ao mesmo princípio, sendo este mecanismo compatível com uma resposta alérgica com uma fase de sensibilização.2,7 Em muitos casos, a repetição da exposição ao MC a que se associou uma RHNI resulta numa segunda reação semelhante. Outro aspeto que reforça este mecanismo imunológico consiste na histopatologia destes exantemas e na positividade dos testes cutâneos (isolamento de células CD4 e CD8 nestes locais quando biopsiados).1,8,11
Manifestações Clínicas
As reações de hipersensibilidade imediata a meios de con- traste manifestam-se tipicamente como anafilaxia. A maioria dos doentes com este tipo de reações apresenta-se com prurido e urticária, e em algumas situações com angioedema. Os sinto- mas gastrointestinais como náusea, vómitos, dor abdominal ou diarreia podem ocorrer. As reações mais graves envolvem os sistemas respiratório e cardiovascular e caracterizam-se por dispneia, broncoespasmo, hipotensão e taquicardia, podendo, em caso de choque anafilático, associar-se a alteração do estado de consciência.1–3,5,11,15 Cerca de 70% destas reações ocorrem nos primeiros 5 minutos após a administração de contraste, e cerca de 96% das reações graves ou fatais ocorrem nos primeiros 20 minutos.7,16 As RHI podem ser classificadas, independentemente do seu mecanismo fisiopatológico, consoante a sua gravidade de acordo com a Escala de Ring e Messmer em quatro Graus (I-IV) (Tabela 1) ou segundo a Sociedade Europeia de Radiologia Urogenital em 3 graus (ligeira, moderada e grave).5,15
A maioria dos doentes com reações de hipersensibilidade não imediata apresenta um exantema maculopapular ou outros sintomas cutâneos ligeiros (eritema, urticária e/ou angioedema), podendo estas manifestações ocorrer entre algumas horas a alguns dias após a administração de contraste.5,7 Estas reações podem classificar-se, de acordo com a sua gravidade, em: ligeiras (quando nenhuma terapêutica é necessária), moderadas (boa resposta terapêutica sem necessidade de internamento) ou graves (necessidade de internamento para estabilização clínica).2 Os exantemas mais específicos após a exposição a contraste incluem: exantema simétrico intertrigo-flexural associado a fármacos (SDRIFE), eosinofilia com sintomas sistémicos associada a fármacos (DRESS), eritema exsudativo multiforme, síndrome de pele escaldada ou doença do enxerto contra o hospedeiro.7 A maioria destas reações são ligeiras a moderadas e autolimitadas. No entanto podem ocorrer reações graves como vasculite, síndrome de Stevens-Johnson, necrólise epidérmica tóxica e erupções papulo-pustulares. Embora ocorram raramente, os sintomas sistémicos que se manifestam mais tardiamente (como hipotensão, febre, dor abdominal ou dispneia), bem como as reações bifásicas foram associadas a exposição a contrastes iodados.1–3,8,11
Epidemiologia
As reações adversas após a utilização de MC são frequen- tes; no entanto a frequência de reações de hipersensibilidade difere consoante o tipo de meio utilizado e a via de administração escolhida, sendo muito mais frequentes com meios iodados e com administração endovenosa.6
Figura 5 – Algoritmo de atuação – reações de hipersensibilidade a MC.
A osmolalidade e a carga iónica dos MCR iodados têm sido as suas propriedades mais relevantes.3,7 Reações imediatas ligeiras foram descritas em 12,7% dos doentes que receberam compostos com mono-iodados iónicos, mas apenas em 0,7-3,1% dos que receberam compostos não iónicos.7,11 Por sua vez, as reações imediatas graves foram descritas em 0,1-0,4% dos procedimentos que utilizaram compostos iónicos, mas apenas em 0,02-0,04% das situações em foi utilizado MCR não iónico.7,8,11 As RHI tanto em adulto como crianças costumam ser de intensidade ligeira, mas mesmo assim, as reações fatais de hipersensibilidade continuam a ocorrer em 1-3 casos por cada 100.000 administrações de MCR (iónico e não iónico).7,11,12 A frequência de reações de hipersensibilidade não imediata reportadas varia de forma importante entre publicações. A maioria destas consiste em sintomas cutâneos e estima-se que ocorram entre 1-3% dos doentes expostos a MCR.7,8,11 As reações de hipersensibilidade são menos frequentes em crianças. 1,3,11 Em idade pediátrica, descreve-se uma incidência de RHI após utilização de MCR iodados de baixa osmolalidade entre 0,18% e 0,9.6,12,13
As reações de hipersensibilidade a meios derivados do gadolínio são predominantemente do tipo imediato, raras e de inten- sidade ligeira.6 Não obstante, as reações graves podem também ocorrer.6 A incidência estimada das reações de hipersensibilidade a meios derivados do gadolínio em idade pediátrica ronda os 0,04%.6 São muito raros os casos descritos de hipersensibilidade aos meios com sulfato de bário.17
Investigação Diagnóstica
A investigação diagnóstica, apesar de nem sempre conclusiva, tem dois objetivos fundamentais: confirmar o potencial agente causal, de forma a evitar novas exposições e prevenir recorrências; e identificar agentes alternativos para os quais o doente não evidencie hipersensibilidade.
O estudo deve ser realizado entre dois a seis meses após a reação de hipersensibilidade, pois este intervalo associa-se a uma maior frequência de positividade nos testes cutâneos.1,2 A investigação na Consulta de Imunoalergologia compreende: História clínica; Testes laboratoriais; Testes cutâneos (Prick Teste, Testes Intradérmicos, Patch Teste) e Provas de provocação (Fig.5).
História clínica
A anamnese deve permitir: identificar o meio de contraste utilizado; determinar o intervalo de tempo entre as administra- ções e início dos sintomas; caracterizar a reação; determinar possíveis alergias prévias e antecedentes patológicos relevantes. O único fator de risco bem estabelecido para reações de hipersensibilidade consiste em ter tido uma reação prévia, independentemente do tipo de meio de contraste utilizado.1–3,8 Salienta-se que o facto de ter tido uma reação de hipersensibilidade imediata prévia não é fator de risco para uma reação não imediata, nem o facto de ter tido uma reação não imediata é fator de risco para ter uma reação imediata.1–3,8
Outros fatores de risco a considerar incluem: asma, outras doenças alérgicas (rinite, dermatite atópica, alergias alimentares), insuficiência renal, diabetes ou insuficiência cardíaca congestiva.3,12 Manifestações de alergia a marisco ou ao iodo não conferem um risco maior que as restantes doenças alérgicas.18
- Testes laboratoriais
Atualmente não existe nenhum método disponível para uma avaliação serológica específica deste tipo de reações. A avaliação da triptase sérica imediatamente após o episódio inicial (30 minutos a 2 horas; com repetição da avaliação 3 horas depois) constitui um marcador útil nas reações de hipersensibilidade imediata, por ser um sinal sugestivo de anafilaxia (valor preditivo positivo de 93%, valor preditivo negativo de 54%).1,2,11
- Testes cutâneos
Os testes cutâneos são o melhor método disponível para demonstrar um mecanismo imunológico nas reações de hipersensibilidade imediata, tendo em conta a sua alta especificidade (96-100%) e moderada sensibilidade (26-50%).1,2,11 Nas rea- ções não imediatas a sensibilidade é ligeiramente inferior (2247%).1,2,11 Um teste positivo é usualmente interpretado como indicativo de sensibilização alérgica. A reatividade cruzada é frequente, pelo que devem ser testados vários meios de contraste (se possível um de cada tipo) na tentativa de selecionar um pro- duto sem reatividade, para uma possível utilização bem tolerada no futuro (valor preditivo negativo de 96,6% nas RHI). 1,2,5,7,19
Estes testes apenas estão validados para testar meios de contraste radiológico iodados (Tabela 2).
Os Prick teste, ou testes cutâneos por picada, devem ser realizados com o MCR suspeito não diluído.16 Este é o gold-standard para o diagnóstico de reações IgE mediadas. Uma reação positiva neste tipo de teste é rara. A técnica consiste em picar perpendicularmente a pele da face anterior do antebraço com uma lanceta prick de 1 mm através de uma gota do MCR suspeito não diluído (formulação endovenosa). Os controlos utilizados são soro fisiológico (controlo negativo) e histamina (10 mg/ml, controlo positivo). Considera-se o teste positivo se o diâmetro da pápula for ≥ 3mm, acompanhado de eritema, com controlos positivo e negativo adequados.1,2,11,20
Posteriormente, se os testes anteriores forem negativos, de- vem realizar-se os testes intradérmicos. Nestes utiliza-se MCR com concentração de iodo entre 300-320 mg/ml (formulação endovenosa) diluído em soro fisiológico na proporção de 1/10. A técnica consiste em injetar 0,03-0,05 ml do fármaco diluído na superfície anterior do antebraço, deixando uma pequena pápula (3-4 mm de diâmetro) que é marcada inicialmente com caneta. É considerado um resultado positivo um aumento do diâmetro ≥ 3 mm em relação à pápula inicial com eritema local na leitura inicial e induração eritematosa na leitura tardia, com controlos adequados.1,2,11,16,20
Os Patch teste, ou testes epicutâneos, devem ser realizados com MCR não diluído. A técnica consiste em embeber papel de filtro no MRC suspeito não diluído (formulação endovenosa), colocando-o dentro de uma câmara de alumínio. Posteriormente aplicá-los na região interescapular com a ajuda de adesivo (não limpar a pele antes). Leitura efetuada 15 minutos após a remoção do adesivo (48h após a sua colocação) e 24h após a remoção do adesivo (72h após a sua colocação). Os doentes devem ser reavaliados se apresentarem alguma reação noutro intervalo de tempo. O registo do resultado deve ser efetuado de acordo com a International Contact Dermatitis Research Group (ICDRG) Criteria.20,21 Se o resultado for duvidoso, é necessário repetir o teste.1,2,11,16,20
Atendendo à baixa frequência de positividade, recomenda-se a realização dos testes intradérmicos e Patch simultaneamente.1,2,11
Estudos recentes sugerem que é possível fazer investiga- ção semelhante com meios derivados do gadolínio.16,22 Esta investigação deve iniciar-se com a realização de Prick Test com meio não diluído, e se os testes forem negativos prosseguir o estudo com Testes Intradérmicos nas diluições 1:1000, 1:100 e 1:10 (concentrações não irritativas).16 Parece haver um valor preditivo negativo importante.22
Prova de provocação
Nas reações de hipersensibilidade imediata as provas de provocação não são recomendadas, independentemente da sua gravidade, tendo em conta que mesmo quantidades mínimas de contraste podem gerar anafilaxia.1,11,16 Por sua vez, em caso de reação de hipersensibilidade não imediata as provas de provocação validam os testes cutâneos e são recomendadas. Assim sendo, um teste cutâneo positivo para um determinado MCR implica que este não seja utilizado novamente; no entanto um teste negativo não garante tolerância, pelo que os testes de provocação são uma ferramenta útil na avaliação destes doentes.1,11,16
Este tipo de procedimentos deve ser apenas realizado em centros com capacidade de monitorização do doente, tratamento de emergência e quando novo exame de imagem seja necessário. Exemplo de prova de provocação endovenosa com meio de contraste sem reatividade nos testes cutâneos: Dia 1 administrar 1/10 da dose total; Dia 2 administrar 1/2 da dose total; Dia 3 administrar a dose total (Dose média para tomografia computadorizada: adulto 120 ml; criança 24 mL; a dose pode variar consoante o grupo de trabalho) e realizar o exame de ima- gem pretendido.19
Prevenção
Após a investigação realizada na consulta deve ser facultado ao doente um documento que o identifique como alérgico, bem como informação escrita sobre a investigação realizada e conclusões do estudo.8
Num doente que teve uma anafilaxia, a abordagem mais segura é a evicção do agente suspeito, bem como dos res- tantes meios com reatividade nos testes cutâneos.8 Em caso de necessidade de novo procedimento, deve utilizar-se, sempre que possível, uma investigação imagiológica alternativa ou um agente alternativo sem reatividade nos testes cutâneos (apesar de testes negativos não garantirem tolerância, têm um elevado valor preditivo negativo).7,8,11 O protocolo de pré-tratamento (anti-histamínico e corticoide endovenoso) não é consensual, atendendo a que este não previne reações graves de hipersensibilidade, particularmente em crianças.3,5,8,13,23
Contudo, mesmo após uma avaliação detalhada, pode não se encontrar evidência de alergia a um agente específico. Nesses casos, a abordagem futura implica evitar os agentes de alto risco e considerar as precauções gerais. Atualmente, a escolha de um MC de baixa osmolaridade tem sido associada a menor frequência de reações adversas e de hipersensibilidade.5,12 Em locais em que esta utilização não seja universal, sugere-se a utilização de meios hipo ou iso-osmolares em doentes com fatores de risco, nomeadamente: doentes com patologia alérgica; doentes medicados com beta bloqueantes, anti-inflamatórios não esteroides ou interleucina 2; doentes com reação prévia a outros materiais e/ou fármacos; situações em que o clínico considere adequada a sua administração (idade pediátrica, diabetes, insuficiências renal e cardíaca).3,8,19,23,24 Também é recomendável que os doentes asmáticos tenham a sua patologia controlada antes da realização do procedimento.3,8,19,23,24
CONCLUSÕES
Atendendo ao número de procedimentos realizados mundialmente com meios de contraste, a observação de reações de hipersensibilidade a estes agentes pode ocorrer com alguma frequência. O seu espetro de gravidade é amplo, incluindo manifestações ligeiras e transitórias e, mais raramente, apresentações graves e potencialmente fatais.
Apesar da evidência na literatura ser escassa, principalmente na população pediátrica, os autores gostariam de salientar, com esta revisão, que uma abordagem sistematizada em caso de hipersensibilidade a produtos de contraste contribui para uma possível redução do número de reações adversas subsequentes, bem como a uma utilização mais segura de produtos alternativos.
REFERÊNCIAS BIBLIOGRÁFICAS
1. Brockow K, Sánchez-Borges M. Hypersensitivity to Contrast Media and Dyes. Immunol Allergy Clin North Am. 2014; 34: 547-64. [ Links ]
2. Brockow K, Romano A, Aberer W, Bircher AJ, Barbaud A, Bonadonna P, et al. Skin testing in patients with hypersensitivity reactions to iodinated contrast media a European multicenter study. Allergy. 2009; 64: 234-41. [ Links ]
3. Pradubpongsa P, Dhana N, Jongjarearnprasert K, Janpanich S, Thongngarm T. Adverse reactions to iodinated contrast media: prevalence, risk factors and outcome the results of a 3-year period. Asian Pac J Allergy Immunol. 2013; 31: 299306. [ Links ]
4. Comissão do Formulário Hospitalar Nacional de Medicamentos. Meios de Diagnóstico. In: Formulário Hospitalar Nacional de Medicamentos, 9ª edição. Infarmed Autoridade Nacional do Medicamento e Produtos de Saúde I.P.; 2006. p. 227-46. Disponível em: http://www.infarmed.pt/formulario/formulario.pdf. [ Links ]
5. European Society of Urogenital Radiology. ESUR guidelines on contrast media. Version 8.1. Agosto 2015 (acesso a 12 de Dezembro de 2015). Disponível em: http://www.esur.org/guidelines/pt/index.php#a. [ Links ]
6. Dillman JR, Ellis JH, Cohan RH, Strouse PJ, Jan SC. Frequency and severity of acute allergic-like reactions to gadolinium-containing IV contrast media in children and adults. AJR Am J Roentgenol. 2007; 189: 1533-8. [ Links ]
7. Brockow K. Immediate and delayed cutaneous reactions to radiocontrast media. Chem Immunol Allergy. 2012; 97: 18090. [ Links ]
8. Christiansen C. Hypersensitivity reactions to iodinated contrast media: an Update. In: Pichler WJ (ed). Drug Hypersensitivity. Basel: Karger; 2007. p. 233-41. [ Links ]
9. Vervloet D, Pradal M, Castelain M. Drug allergy. 2nd ed. Uppsala, Sweden: Pharmacia and Upjohn; 1999. p. 197-207. [ Links ]
10. Cohan RH, Dillman JR, Hartman RP, Jafri SZ, Wang CK, Newhouse JH, et al. American College of Radiology Manual on Contrast Media. American College of Radiology. Version 9. 2013. [ Links ]
11. Vionnet J, Petitpierre S, Fumeaux A, Meuli R, Spertini F, Comte D. Allergies aux produits de contraste radiologiques. Rev Med Suisse. 2013; 812-8. [ Links ]
12. Dillman JR, Strouse PJ, Ellis JH, Cohan RH, Jan SC. Incidence and severity of acute allergic-like reactions to IV nonionic iodinated contrast material in children. AJR Am J Roentgenol. 2007; 188: 1643-7. [ Links ]
13. Trout AT, Dillman JR, Ellis JH, Cohan RH, Strouse PJ. Patterns of intravenous contrast material use and corticosteroid premedication in children-a survey of Society of Chairs of Radiology in Childrens Hospitals (SCORCH) member institutions. Pediatr Radiol. 2011; 41: 1272-83. [ Links ]
14. Towbin AJ. The use of gadolinium-based contrast agents in children. Appl Radiol. 2015; 44(5) Suppl: 6-8. [ Links ]
15. Ring J, Messmer K. Incidence and severity of anaphylactoid reactions to colloid volume substitutes. Lancet. 1977; 1: 466-9. [ Links ]
16. Brockow K, Garvey LH, Aberer W, Atanaskovic-Markovic M, Barbaud A, Bilo MB, et al. Skin test concentrations for systemically administered drugs an ENDA/EAACI Drug Allergy Interest Group position paper. Allergy. 2013; 68: 70212. [ Links ]
17. Schwartz EE, Seth N, Glick SN, Foggs MB, Silverstein GS. Hypersensitivity Reactions after Barium Enema Examination. AJR Am J Roentgenol. 1984; 143: 103-4. [ Links ]
18. Baig M, Farag A, Sajid J, Potluri R, Irwin RB, Khalid HMI. Shellfish allergy and relation to iodinated contrast media: United Kingdom survey. World J Cardiol. 2014; 6: 107-11. [ Links ]
19. Prieto-García A, Tomás M, Pineda R, Tornero P, Herrero T, Fuentes V, et al. Skin Test-Positive immediate hypersensitivity reaction to iodinated contrast media: The role of controlled challenge testing. J Investig Allergol Clin Immunol. 2013; 23: 183-9. [ Links ]
20. Barbaud A, Gonçalo M, Bruynzeel D, Bircher A. Guidelines for performing skin tests with drugs in the investigation of cutaneous adverse drug reactions. Contact Derm. 2001; 45: 321-8. [ Links ]
21. Wilkinson DS, Fregert S, Magnusson B, Bandmann HJ, Calnan CD, Cronin E, et al. Terminology of contact dermatitis. Acta Derm Venereol. 1970; 50: 287-92. [ Links ]
22. Chiriac A-M, Audurier Y, Bousquet P-J, Demoly P. Clinical value of negative skin tests to gadolinium contrast agents. Allergy. 2011; 66: 1504-6. [ Links ]
23. Lindsay R, Paterson A, Edgar D. Preparing for severe contrast media reactions in children Results of a national survey, a literature review and a suggested protocol. Clin Radiol. 2011; 66: 340-8. [ Links ]
24. Li A, Wong CS, Wong MK, Lee CM, Au Yeung MC. Acute adverse reactions to magnetic resonance contrast media- gadolinium chelates. Br J Radiol. 2006; 79: 368-71. [ Links ]
25. Grainger RG. Imaging, Intravascular radiological iodinated contrast media. In: Diagnostic radiology: A textbook of medical. In: Churchill Livingston, Oxford. 2001. p. 27. [ Links ]
Endereço para correspondência
Maria Miguel Almiro Serviço de Pediatria
Centro Hospitalar de Baixo Vouga
Avenida Artur Ravara, 3814-501 Aveiro
Email: mariamiguelaa@gmail.com
Recebido a 12.06.2015 | Aceite a 22.01.2016














