Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Revista Portuguesa de Saúde Pública
versão impressa ISSN 0870-9025
Rev. Port. Sau. Pub. vol.31 no.2 Lisboa dez. 2013
https://doi.org/10.1016/j.rpsp.2012.12.004
ARTIGOS REVISÃO
Nanomateriais manufaturados: novos desafios para a saúde pública
Manufactured nanomaterials: New challenges for public health
Henriqueta Louroa*, Teresa Borgesb, Maria João Silvaa
aUnidade de Investigação & Desenvolvimento, Departamento de Genética Humana, Instituto Nacional de Saúde Dr. Ricardo Jorge, Lisboa, Portugal
bDivisão de Saúde Ambiental e Ocupacional, Direção-Geral da Saúde, Lisboa, Portugal
RESUMO
Os nanomateriais manufaturados (NM) apresentam propriedades físico-químicas específicas que lhes conferem caraterísticas mecânicas, óticas, elétricas e magnéticas únicas e vantajosas para aplicações industriais e biomédicas. Contudo, o desenvolvimento exponencial das nanotecnologias contrasta com a ainda insuficiente avaliação de risco para a saúde humana e para o ambiente, conduzindo a preocupações em termos de saúde pública. Esta revisão procura sintetizar o conhecimento atual sobre a toxicidade dos NM, identificar as lacunas ainda existentes e descrever o contributo da nanotoxicologia para o enquadramento regulamentar dos NM, de modo a garantir a sua utilização segura e a minimização dos riscos para a saúde pública.
Palavras-chave:Nanomateriais manufacturados, Saúde pública, Segurança, Efeitos genotóxicos, Nanotoxicologia
ABSTRACT
The manufactured nanomaterials (NM) have specific physicochemical properties that confer unique mechanical, optical, electrical and magnetic characteristics that are beneficial for biomedical and industrial applications. However, the exponential developments of nanotechnologies contrast with the still insufficient risk assessment for human health and the environment, leading to concerns in terms of public health. This review summarizes the current knowledge on the toxicity of NM, identifying remaining gaps and describing the contribution of nanotoxicology to the regulatory framework of NM, in order to ensure their safe use and reduction of risks to public health.
Keywords: Manufactured nanomaterials. Public health. Safety. Genotoxic effects. Nanotoxicology.
Introdução
A exposição da população humana a partículas exógenas de dimensões da ordem dos nanómetros, os nanomateriais, pode ser considerada ubiquitária: tais partículas encontram-se no ar que respiramos e também nos produtos de consumo que usamos diariamente. Os nanomateriais podem ter origem natural ou antropogénica, sendo que o primeiro grupo engloba, por exemplo, nanomateriais produzidos e libertados nas emissões vulcânicas, nos fogos florestais e alguns vírus, enquanto o segundo inclui os que são produzidos em consequência de atividades humanas, tais como nos processos de refinação, soldadura, confeção de alimentos ou combustão automóvel1. Presentemente, as atenções focam-se preferencialmente nos nanomateriais manufaturados (neste texto designados por NM) que englobam aqueles que são sintetizados deliberadamente para um fim específico1, porque constituem um novo desafio, em termos de saúde pública. Efetivamente, depositam-se grandes expectativas nas tecnologias baseadas nestes NM (nanotecnologias) como impulsionadoras do crescimento económico dos países industrializados, devido ao seu potencial para melhorar a qualidade e o desempenho de muitos tipos de produtos e de processos. Assim, o estímulo crescente ao desenvolvimento, produção e aplicação em grande escala de NM, bem como a sua utilização numa vasta gama de produtos de consumo e em biomedicina, tem conduzido, inevitavelmente, ao aumento da exposição humana e à disseminação no ambiente, sendo o seu potencial impacto ainda desconhecido. Este facto justifica a necessidade de realizar estudos que permitam garantir uma utilização segura dos nanomateriais, durante todo o seu ciclo de vida, protegendo o ambiente e a saúde humana.
Nanomateriais e nanotecnologia
O prefixo 'nano-', com origem na palavra grega νάνοζ (anão), significa, no meio científico, uma medida de 10-9 unidades. Contudo, a procura de uma definição para «nanomaterial» tem gerado alguma polémica. Numa tentativa de obviar a essas inconsistências, a Comissão Europeia emitiu em 2011 uma recomendação sobre a definição de nanomaterial (NM), que se transcreve: «por «nanomaterial», entende-se um material natural, incidental ou fabricado, que contém partículas num estado desagregado ou na forma de um agregado ou de um aglomerado, e em cuja distribuição número-tamanho 50% ou mais das partículas têm uma ou mais dimensões externas na gama de tamanhos compreendidos entre 1 nanómetro e 100 nanómetros»2.
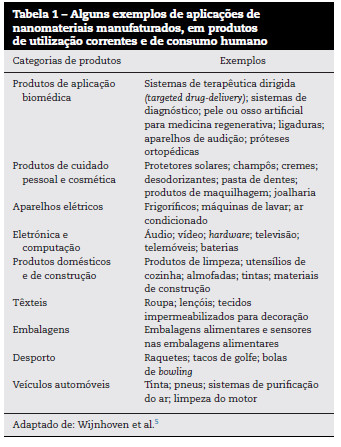
Se as propriedades dos materiais, em geral, dependem da sua composição físico-química e do meio ambiente na interface (estado físico, temperatura, pressão), no caso dos NM as suas propriedades distintas e atrativas devem-se, fundamentalmente, à reduzida dimensão das partículas e a modificações ao nível da estrutura que conduzem a um aumento da área superficial em relação ao volume, tendo por consequência um aumento do número de moléculas/átomos na superfície. Esta característica confere-lhes propriedades de superfície únicas, que, por sua vez, modificam a sua reatividade, frequentemente melhorando as suas propriedades mecânicas, óticas, elétricas e magnéticas, comparativamente às dos materiais com a mesma composição físico-química mas de dimensões maiores3, 4. Estas modificações de reatividade têm dado uma contribuição significativa para o desenvolvimento e produção em quantidades significativas de uma geração de produtos inovadores contendo NM, com um vasto campo de aplicações em áreas como a eletrónica, a alimentação, a cosmética e a biomedicina5, tal como se especifica na Tabela 1. A título de exemplo, o dióxido de titânio é utilizado na forma «nano» em protetores solares exibindo as mesmas propriedades de filtro ultravioleta que a forma convencional, com a vantagem de ser invisível na pele6. Estes NM são usados nos protetores solares desde 19906 e inserem-se numa das categorias de produtos que tem tido um maior incremento, a dos «produtos de cuidado pessoal e cosméticos»5. Outro exemplo é a utilização de nanotubos de carbono para controlar ou aumentar a condutividade de materiais, com aplicações variadas que vão desde embalagens antiestáticas até aparelhos eletrónicos.
A clara expansão deste mercado nos últimos anos é visível na base de dados da Woodrow Wilson «Nanotechnology Consumer Products Inventory», onde são identificados 1 317 produtos contendo NM, produzidos por 587 empresas em 30 países7. Relativamente a produtos de consumo humano contendo NM, o seu número no mercado europeu cresceu 6 vezes nos últimos 3 anos, totalizando 858 produtos em 20105. Para além disso, a crescente aplicação dos NM à biomedicina, a nanomedicina4, preconiza cuidados de saúde mais eficientes e menos dispendiosos. Assim, plataformas como a «European Technology Platform on NanoMedicine»8 têm surgido um pouco por todo o mundo, na expectativa de desenvolver novas soluções terapêuticas com o consequente valor acrescentado para a saúde humana e para a sociedade.
A maioria da produção e utilização de NM, especialmente por grandes multinacionais, tem ocorrido nos Estados Unidos da América (49%), sendo a União Europeia (UE) responsável por 30% do mercado produtor9. Entre 2000 e 2010, os 5 principais requerentes de patentes na área da nanotecnologia foram a IBM, a Samsung Electronics, a TDK Corp, a Canon KK e a Fujitsu Ltd10. A atividade de patenteamento na área da bionanotecnologia em 2003 era liderada por empresas americanas, com 70% de patenteamento10. Em 2008, 5 anos depois, a atividade de patenteamento teve um aumento de 160% com 7399 patentes registadas10. Relativamente a Portugal, o número de patentes é bastante inferior, ou seja, foram pedidas apenas 14 patentes10.
Na tentativa de melhor caracterizar a situação portuguesa relativamente à produção e ao desenvolvimento de NM, uma pesquisa no site http://www.nanowerk.com (consulta em 24 Mar 2012) revela a rede de investigação existente em Portugal, bem como a existência de 3 empresas especificamente envolvidas na produção de nanomateriais. No entanto, tudo leva a crer que este seja um cenário incompleto devido à inexistência de um sistema centralizado de dados, a nível nacional. Um trabalho muito recente analisou os projetos de I&D realizados sobre NM em Portugal11, em que se concluiu que, entre 2006-2009, foram financiados 108 projetos no domínio das nanotecnologias, dos quais somente 2 abordavam o tema da nanossegurança. Portugal participou ainda em 24 projetos de I&D no âmbito do 7.° programa-quadro da UE e numa ação concertada sobre a segurança de NM promovida pela Agência Executiva para a Saúde e Consumidores (Executive Agency for Health and Consumers, EAHC) da Comissão da UE11. Estes números sugerem o elevado interesse nacional, em particular na área das aplicações em nanotecnologia.
Pelo que foi mencionado, reconhece-se que o crescente desenvolvimento, produção e utilização de NM manufaturados tem conduzido a um aumento real da exposição humana, especialmente no contexto ocupacional, com consequências para a saúde ainda desconhecidas. No entanto, a informação sobre os níveis de NM a que a população humana pode estar sujeita ainda é escassa12, quer relativamente aos consumidores, quer aos locais de trabalho ou ao ambiente.
Exposição humana a nanomateriais manufaturados e potenciais efeitos na saúde
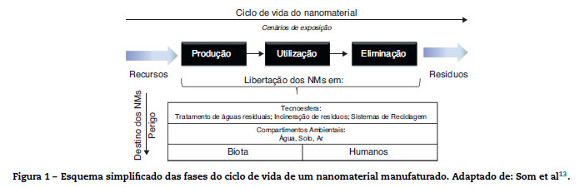
A exposição humana a NM pode ocorrer durante as várias fases do ciclo de vida do NM (Figura 1), desde a síntese, produção e inclusão nos produtos (exposição ocupacional) até à utilização desses mesmos produtos (exposição do consumidor); a eliminação dos NM e consequente acumulação no ambiente poderá constituir ainda uma fonte de exposição humana13 (exposição ambiental). A presença de NM no ar pode dever-se a processos de erosão de materiais fabricados ou à produção/utilização/manipulação de pós-nanoparticulados em processos industriais, sendo que a via inalatória constitui a via de exposição humana mais relevante, particularmente, em contexto ocupacional14. Em relação à exposição por via oral, sabe-se que os NM incorporados em alimentos, suplementos alimentares ou mesmo em embalagens alimentares, bem como os originários de solos ou águas contaminadas, poderão ser absorvidos através do intestino de mamíferos14 e, assim, originar, eventualmente, efeitos sistémicos. A via transdérmica é também importante14, quer em termos ocupacionais quer quando se trata da utilização de produtos de cosmética e higiene pessoal contendo NM na sua composição, apesar de o conhecimento sobre a capacidade de os NM penetrarem (ou não) na pele permanecer ainda inconclusivo.
Se, por um lado, foi estimado que, entre 1981-83, cerca de 2,7 milhões de trabalhadores se encontravam expostos a nanomateriais de dióxido de titânio nos EUA15, por outro lado, apenas temos conhecimento de um estudo nos EUA que se preocupou em avaliar a exposição inalatória e dérmica aos nanotubos de carbono durante a manipulação de material não refinado16. Na UE, a Agência Europeia para a Segurança e Saúde no Local de Trabalho (European Agency for Safety and Health at Work, EU-OSHA) estima que entre 300 000 a 400 000 postos de trabalho lidam diretamente com a nanotecnologia. Os nanomateriais fabricados são manuseados em muitos mais locais de trabalho ao longo da cadeia de abastecimento e 75% desses locais de trabalho são pequenas e médias empresas (http://osha.europa.eu/pt/press/press-releases/risks_of_very_small, consulta em 23 Jun 2012). No Reino Unido, um outro estudo identificou 53 empresas envolvidas em manufaturar, processar ou utilizar NM em 2005, para além de mais 55 envolvidas na I&D associada à nanotecnologia9. Em França, de acordo com um estudo do Instituto Francês de Investigação e Segurança (INRS), a produção industrial de nanomateriais envolve entre 2000 e 4000 trabalhadores17. Por sua vez, o ponto da situação para os países nórdicos (Dinamarca, Finlândia, Islândia, Noruega, Suécia) foi apresentado no relatório de Schneider18, mostrando a existência de uma grande diversidade de cenários de exposição humana durante o ciclo de vida dos NM, envolvendo não só trabalhadores mas também utilizadores. Em Portugal, que se conheça, não existem dados publicamente disponíveis sobre exposição a NM.
Para além disso, na maioria dos países, a colocação da designação «nano» nos rótulos dos produtos de consumo não é fundamentada legalmente e, de acordo com o relatório do Instituto Holandês para a Saúde Pública e Ambiente (RIVM), alguns produtos com esta indicação não contêm realmente NM, enquanto outros incorporam NM e não o referem19. Não existe, portanto, um sistema de rastreabilidade que possibilite aos consumidores estarem corretamente informados sobre a presença de NM nos produtos existentes no mercado e, como tal, estarem cientes da possibilidade de estarem expostos a esses materiais, dificultando a perceção e a comunicação do risco.
Do que ficou exposto, é inequívoco que, por um lado, as nanotecnologias têm já um enorme impacto económico e estão a ser alvo de uma expansão que é impossível de reverter e que, por outro, a exposição humana a uma ampla variedade de NM é já uma realidade que não pode ser ignorada. Por sua vez, a EU-OSHA refere a exposição ocupacional aos NM como o risco emergente mais premente20, considerando existir necessidade de investigação de todo o ciclo de vida de modo a identificar todas as situações de exposição dos trabalhadores, bem como as implicações na sua saúde.
Após a absorção e uma vez no interior do organismo, as nanoparticulas, em consequência das suas pequenas dimensões, têm a capacidade de se translocarem para o sistema circulatório e linfático, podendo atingir diversos órgãos e tecidos, incluindo o cérebro1. Diversos estudos em roedores têm investigado as consequências da exposição aos NM, essencialmente por inalação, relativamente à ocorrência de lesões nos pulmões, inflamação e formação de tumores12, tendo globalmente confirmado o potencial tóxico dos NM. A resposta inflamatória que tem como consequência a produção de radicais livres de oxigénio (ROS) e de azoto é, de facto, a via mais evidente que correlaciona a exposição a NM com a ocorrência de lesões nos tecidos e que, ao causar lesões no genoma das células21, tem o potencial de contribuir para o desenvolvimento de neoplasias. De facto, este tipo de resposta dos tecidos, quando em contacto com NM, tem levado ao estabelecimento de analogias com os conhecidos casos da silicose e asbestose em que a inflamação crónica pode levar a genotoxicidade, mutações, morte celular e cancro22. A estrutura fibrosa de alguns NM, semelhante a asbestos, acentua esta analogia.
No que se refere a outros efeitos na saúde humana, até à data, com base em diversas experiências in vivo sobre a toxicidade dos NM, pode sugerir-se que uma variedade de patologias do sistema respiratório e cardiovascular estejam potencialmente associadas à exposição aos NM, tais como mesotelioma, tumores benignos e enfarte do miocárdio21.
Os nanomateriais no contexto da saúde pública
Análise de risco
Considerando o paradigma de análise de risco (risk analysis) convencional, que incorpora 3 componentes &-avaliação do risco (risk assessment), gestão do risco e comunicação do risco23&- tem surgido a dúvida sobre a sua aplicabilidade ao caso dos NM. A avaliação do risco inclui a identificação do perigo, através de estudos sobre a toxicidade dos NM, a avaliação da exposição humana e, por último, a caracterização do risco, através de estudos de índole mais mecanística.
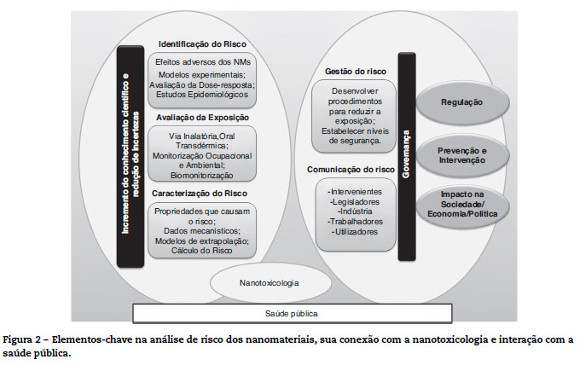
Relativamente à toxicidade dos NM, tem-se assumido que estes apresentam, pelo menos, a mesma toxicidade que os materiais na forma não «nano». No entanto, a observação de que os mesmos constituintes, quando estruturados na forma «nano», revelam propriedades físico-químicas distintas das do material de origem, com consequente alteração potencial da sua reatividade nos sistemas biológicos4, coloca em causa a aplicabilidade das metodologias convencionais à avaliação de efeitos adversos dos NM, gerando também incertezas sobre a robustez dos resultados já publicados. Assim, tais especificidades dos NM devem ser consideradas para uma adequada avaliação de risco, através do conhecimento gerado pela nanotoxicologia4, conforme se sugere na Figura 2.
Neste contexto, a Resolução do Parlamento Europeu, de 24 de abril de 2009, a propósito dos aspetos regulamentares dos nanomateriais, destaca a ausência de informação e de conhecimentos científicos suficientes para tal extrapolação na área dos NM, aconselhando a intervenção da Comissão das Comunidades Europeias para colmatar estas falhas e adequar a legislação existente24.
Ainda em 2009, com base no Regulamento REACH sobre Registo, Avaliação, Autorização e Restrição dos Químicos (Registration, Evaluation, Authorisation and Restriction of Chemicals), a UE iniciou projetos de implementação do REACH para NM (REACH Implementation Project on Nanomaterials, RIPoN) com vista a adaptar os guias de orientação REACH aos NM. Estas ações de implementação visaram fornecer informação científica relevante à Agência Europeia dos Químicos (ECHA), nomeadamente no sentido de adaptar os protocolos experimentais do REACH aos NM. Foi concluído ainda que substâncias nas formas nano devem ser registadas separadamente, independentemente do seu volume e sempre que as suas propriedades forem diferentes da substância original.
Atualmente, de acordo com o REACH25, a avaliação da segurança dos nanomateriais deve seguir a metodologia de avaliação de risco adotada para os químicos convencionais, que se baseia nos seguintes pontos: 1) avaliação de efeitos; 2) avaliação da exposição; e 3) caracterização do risco.
No que diz respeito à avaliação de efeitos (passo 1), o quociente de risco (risk characterisation ratio, RCR) é considerado aceitável quando o valor estimado da exposição é inferior à dose/concentração do agente em que não se observou efeito adverso (no observed adverse effect level, NOAEL) no estudo experimental levado a cabo para avaliar o endpoint em estudo (p. ex., toxicidade por inalação, genotoxicidade), ou seja, quando RCR < 1. No caso de ser necessário efetuar ensaios in vivo ou vitro para avaliar os efeitos, torna-se necessário caracterizar primeiro o NM em estudo, recolhendo informação sobre os parâmetros físico-químicos mais relevantes e que poderão influenciar a toxicidade, tais como distribuição de tamanhos, estado de agregação/aglomeração, forma, área superficial, reatividade, solubilidade em água, carga superficial e estabilidade. Salienta-se desde já, no entanto, que o poder preditivo em termos de toxicidade, do binómio propriedades intrínsecas-efeitos observados é ainda baixo, devido à já referida insuficiente evidência científica24 e à falta de protocolos experimentais validados, impossibilitando a extrapolação de resultados ou a associação de um determinado perfil toxicológico a um certo(s) tipo(s) de NM26.
Para avaliar a exposição (passo 2), torna-se necessário identificar todas as potenciais fontes de exposição. Neste sentido, é importante conhecer o processo de fabrico, as atividades envolvidas e os diferentes cenários de exposição, assim como identificar as vias de exposição mais prováveis. Este tipo de informação também é relevante para decidir a estratégia de teste adequada (que estudos e que vias de administração) e a elaboração de recomendações sobre medidas de prevenção do risco. Estas podem incluir o uso de equipamento de proteção individual com especificações definidas (máscaras de proteção nível 3 -FFP3), uso de filtros HEPA, e ainda a implementação de medidas operacionais tais como a extração forçada de ar no posto de trabalho&-LEV (local exhaust ventilation), redução da duração das tarefas e, de uma maneira geral, formação relativa a boas práticas de fabrico.
Logo após a implementação do RIPoN, uma análise de incerteza demonstrou que existem lacunas no conhecimento em quase todos os aspetos relacionados com potenciais riscos para a saúde e o ambiente associados aos NM27. Mais recentemente, a Comunicação da Comissão das Comunidades Europeias sobre aspetos reguladores dos nanomateriais28 expressou a mesma incerteza, ao salientar a existência de lacunas relativamente às questões de segurança dos NM, salvaguardando a possibilidade de modificar a legislação existente mediante novas informações. é também referido o esforço internacional que se encontra em curso para avaliação e gestão dos riscos associados à exposição a estes materiais, por forma a garantir a sua utilização em consonância com elevado nível de saúde pública, segurança e proteção dos consumidores, trabalhadores e ambiente.
Presentemente, perante os novos produtos baseados em nanomateriais e as incertezas no que se refere à sua segurança aplica-se, de uma forma geral, o princípio da precaução, enquadramento utilizado para a regulação de tecnologias emergentes que possam constituir potenciais ameaças graves para a saúde ou para o ambiente29. O princípio da precaução preconiza a necessidade de atuar para reduzir perigos potenciais antes de existir uma prova cabal do perigo, tendo em consideração os prováveis custos e benefícios da ação versus inação.
Lamentavelmente, são variados os exemplos de um passado recente em que tecnologias emergentes com enorme potencial para aplicações industriais ou médicas se revelaram tardiamente como nocivas para o ser humano e para o ambiente. Um desses exemplos foi a produção e ampla utilização das fibras de asbestos para fins industriais e revestimentos na construção civil, que se verificou na segunda metade do século XX. Apesar de repetidos alertas quanto aos seus potenciais efeitos adversos para o homem, estes foram ignorados, prevendo-se, em consequência, um acréscimo da ordem dos milhares de casos de mesotelioma e de cancro do pulmão, nos próximos 25 anos. Outro caso paradigmático é o dos raios-X, cuja utilização se banalizou após a sua descoberta no final do século XIX, dadas as suas potencialidades para diagnóstico e terapêutica. Embora os seus efeitos agudos tenham sido precocemente reconhecidos, os efeitos crónicos, resultantes da exposição repetida, foram ignorados durante mais de 50 anos, sendo que apenas em 1949 o International Commission on Radiation Protection (ICRP) reconheceu que se deveria minimizar a exposição ao raio-X devido ao seu efeito cancerígeno. Contudo, só em 1996 foi publicada a Diretiva Europeia sobre radiação ionizante baseada nos limites de dose estabelecidos pelo ICRP alguns anos antes, cuja implementação se tornou mandatória para todos os Estados-Membros30. Em qualquer destes casos, as consequências só se tornaram evidentes décadas após as primeiras exposições ocorrerem, devido aos longos períodos de latência dos processos cancerígenos, impedindo a ação no sentido de minimizar ou impedir a exposição. Até que ponto os alertas que foram surgindo nos casos ilustrados poderiam ter conduzido a ações precoces para reduzir os perigos, a um custo mais baixo para a sociedade, se tivesse sido aplicado o princípio da precaução? Assim, deveremos ter aprendido com estes exemplos e, face ao novo desafio colocado pela crescente produção e utilização de nanomateriais, importará expandir a base do conhecimento através de avaliações integradas que permitam gerar evidência para que os decisores e todas as partes interessadas possam prever as consequências possíveis da regulamentação e das ações e inações. Enquanto a incerteza persistir quanto aos potenciais efeitos adversos dos NM, procura-se que a aplicação do princípio da precaução permita o equilíbrio entre os riscos que possam vir a ser reconhecidos e os benefícios societais que deles advêm.
Na prática, a aplicação do princípio da precaução implica a implementação de medidas de prevenção baseadas na redução da exposição humana, ao longo de todas as fases do ciclo de vida do NM, tendo em conta as vias de exposição de maior preocupação e incluindo, necessariamente, planos de emergência em caso de acidente. O National Institute for Occupational Safety and Health (NIOSH) recomendou o desenvolvimento e a implementação de medidas de proteção temporárias no caso da exposição ocupacional29.
Contudo, urge que sejam tomadas decisões regulamentares com base em evidência científica, caso seja identificado algum risco para a saúde humana, pelo que é premente aprofundar os estudos epidemiológicos e toxicológicos sobre NM. Tratando-se de materiais manufaturados para utilização em produtos de uso humano, tem de ser considerado para esta avaliação o continuum da investigação, desenvolvimento e produção até ao consumidor, bem como todos os seus intervenientes, propondo-se para esse fim o enquadramento ilustrado na Figura 2. Neste enquadramento, a governança de potenciais riscos para a saúde associados aos NM deve ser adaptativa, à medida que o conhecimento científico progride, de modo a assegurar uma adequada análise do risco em tempo útil, considerando as características específicas dos nanomateriais sem menosprezar os seus grandes benefícios societais.
Toxicidade dos nanomateriais: a nanotoxicologia
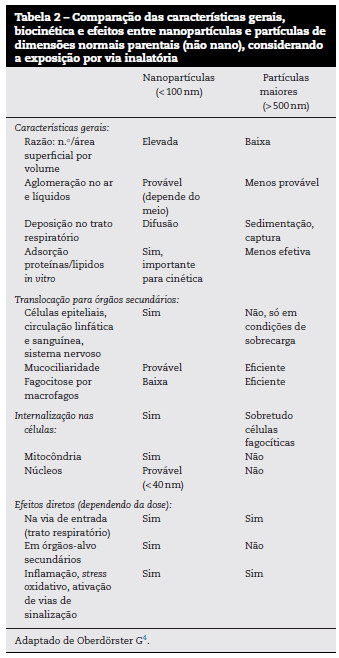
Datam de 1990 dois trabalhos na revista científica Journal of Aerosol Science, que sugeriam a ideia de que as partículas inaladas de diâmetro inferior a 100 nanómetros produziam uma resposta exacerbada nas células pulmonares (Ferin et al., 1990 e Oberdörster et al., 199031). A associação entre os efeitos biológicos e a dimensão das partículas, sugerido por estes autores, tem sido progressivamente confirmada através de outros estudos31. Na Tabela 2 resumem-se as principais características, biocinética e efeitos biológicos das nanopartículas, em comparação com os seus análogos de dimensão superior a 500 nanómetros, que se considera terem maior impacto no seu perfil toxicológico e modo de ação. Salientam-se, assim, as 2 características fundamentais dos NM que condicionam também a sua toxicidade31, designadamente, a dimensão das partículas e o seu comportamento dinâmico em meio gasoso e líquido4, 31. O comportamento dinâmico dos nanomateriais, ou seja, a sua capacidade de formação de agregados ou aglomerados, determina a dimensão real das partículas que vão interagir com os sistemas biológicos4. Enquanto os agregados de NM consistem em partículas primárias unidas por ligações químicas fortes (tipo covalente), nos aglomerados as partículas primárias estão unidas por forças de van der Waals fracas, sendo as suas propriedades fortemente influenciadas pelo meio em que se encontram4. Assim, as propriedades químicas dos NM, tais como hidrofobicidade, funcionalização, carga, estado de dispersão e adsorção de proteínas na sua superfície, são determinantes para a sua aptidão para serem absorvidos, metabolizados e eliminados ou acumulados no organismo. Estas propriedades podem, no entanto, ser modificadas de um modo dinâmico quando em condições biológicas ou ambientais distintas32. Por este motivo, mesmo quando o perfil toxicológico dos constituintes de um NM é conhecido, podem existir casos em que os seus efeitos na saúde e no ambiente sejam distintos relativamente aos dos mesmos constituintes na forma não nanométrica.
Como foi anteriormente referido, a deposição de NM nos tecidos pode desencadear uma resposta inflamatória em que células como macrófagos e neutrófilos são recrutados para o local do contacto, levando ao stress oxidativo a nível celular (produção de ROS) que, por sua vez, podem causar alterações no genoma das células adjacentes, produzindo efeitos genotóxicos secundários. Em situações de inflamação crónica, o stress genotóxico será permanente, com consequente acumulação de alterações genéticas que facilitarão o processo de transformação das células em direção a um fenótipo maligno. Contudo, mesmo na ausência de uma resposta inflamatória, os NM podem induzir, primariamente, efeitos genotóxicos mediados por stress oxidativo, através da sua interação com constituintes celulares, incluindo as mitocôndrias e oxidases NADPH ligadas à membrana celular ou através da depleção de antioxidantes (e.g., glutationo). Sabe-se, por exemplo, que os iões metálicos de transição contidos na composição de muitos NM (e.g., cádmio, crómio, cobalto, cobre, ferro, níquel, titânio e zinco) podem ser libertados, causando a conversão dos metabolitos do oxigénio celular em ROS33. Jacobsen et al.34 demonstraram a indução de ROS em células expostas a negro de carbono, nanotubos de carbono de parede simples e fulerenos C60. Até que ponto, na situação de exposição por via inalatória a NM, este tipo de mecanismo de transformação celular pode ser generalizado, ainda permanece uma questão em aberto que deverá ser objeto de investigação futura.
Para além das lesões oxidativas no DNA, também os efeitos genotóxicos diretos dos NM podem contribuir de forma determinante para gerar instabilidade genética que, por sua vez, pode contribuir para o desenvolvimento de processos cancerígenos. Teoricamente, a capacidade de penetração dos NM nos sistemas celulares será superior à dos seus análogos não nanométricos, permitindo-lhe atravessar as membranas celulares e atingir o núcleo, onde poderão interagir diretamente com o genoma da célula ou com as proteínas nucleares. Os NM que não consigam transpor a membrana nuclear poderão, ainda assim, ter acesso ao DNA e proteínas nucleares no decurso do processo mitótico, podendo originar fenómenos de aneuploidia. Este tipo de acontecimentos foi já descrito para os NM de dióxido de titânio e sílica que penetram no núcleo e causam a formação de agregados de proteínas intranucleares, levando à inibição da replicação, transcrição e proliferação celular33. Estudos mais recentes sugerem que o dióxido de titânio é capaz de se inserir também nas bases de DNA, ligando-se aos nucleótidos e alterando a estrutura secundária do DNA35. Outro exemplo diz respeito às nanopartículas de ouro que parecem exibir a capacidade de se ligarem ao DNA, quer exteriormente, quer intercalando-se parcialmente na cadeia de DNA36. Apesar destes efeitos observados, outros estudos, porém, têm revelado resultados negativos para as mesmas classes de NM.
Embora os mecanismos descritos, consistindo numa ação primária direta ou indireta dos NM sobre o genoma ou numa ação secundária, via resposta inflamatória, tenham vindo a ser propostos com base em evidências experimentais, ainda persistem muitas incertezas que justificam uma intensificação dos estudos sobre os potenciais efeitos adversos destes materiais com vista a uma correta avaliação de risco.
Perante esta fragilidade do conhecimento, tem-se assistido a uma conjugação de esforços de organismos internacionais, como o Centro para o Controlo de Doenças (Center for Disease Control, CDC), a OCDE e a UE, no sentido de promover projetos e grupos de trabalho com vista a assegurar a utilização segura dos NM. Neste contexto, a nanotoxicologia &- visando a avaliação dos efeitos adversos dos NM no organismo humano e ecossistemas, levando em consideração as especificidades destes, para proteger a saúde &- tem vindo a desenvolver-se como uma área de relevo no âmbito da saúde pública4. Esta área recente da toxicologia deverá produzir o conhecimento científico dos mecanismos de ação dos NM nos sistemas biológicos, que contribuirá para a realização de uma análise de risco, conforme esquematicamente representado na Figura 2. Assim, a nanotoxicologia irá contribuir para uma abordagem preditiva, como a proposta por Nel et al. (2012). De acordo com este autor, a necessidade de uma plataforma para a investigação das interações na interface nano/bio pode ser respondida através de metodologias com elevado rendimento (High-Throughput Screening) para o rastreio in vitro das propriedades toxicológicas dos NM, fundamentadas no seu modo de ação, procurando prever-se quais as propriedades físico-químicas dos NM que podem conduzir a patologias in vivo37. Espera-se que a utilização deste tipo de nanotoxicologia preditiva permita, futuramente, estabelecer uma abordagem de safe-by-design38 que pressupõe a síntese de NM seguros após modificação das propriedades responsáveis pela sua toxicidade. Para isso, é essencial conhecer o seu modo de ação, bem como as propriedade(s) diretamente associadas à sua toxicidade, para que se possam modificar, minimizando os efeitos tóxicos e promovendo a síntese de NM seguros, que terão, ainda assim, de ser analisados quanto à sua segurança.
Avaliação da genotoxicidade e potencial carcinogénico dos nanomateriais
Segundo o Joint Research Center (JRC), a avaliação de segurança dos nanomateriais deve ser enquadrada ao nível da investigação básica e translacional, procurando produzir-se conhecimento sobre os mecanismos de toxicidade específicos dos NM e aplicar esse conhecimento para reduzir os seus impactos na saúde38. Assim, sugere o desenvolvimento de metodologias inovadoras para análise de riscos nanoespecíficos e a validação de modelos in vitro e in vivo recorrendo a NM de referência38. Por outro lado, os muitos esforços internacionais realizados têm vindo a produzir uma grande quantidade de dados sobre a toxicidade das diversas classes de NM, sendo de estimular também a adequada partilha e difusão do conhecimento, incluindo a apresentação de resultados negativos, e a realização de meta-análises de toda esta a informação39. Por fim, preconiza-se como prioridades de investigação a definição de curvas dose-resposta em órgãos alvo e sistemas complexos, recorrendo a materiais bem caracterizados38.
Por outro lado, os pareceres emitidos pelo Comité Científico para os Riscos Emergentes e Identificados de Novo3 (Scientific Committee on Emerging and Newly Identified Health Risks, SCENIHR) e pela UE destacam as nanopartículas livres e os NM de baixa solubilidade como uma preocupação prioritária no contexto do risco humano e ambiental.
Uma das principais preocupações relativamente aos efeitos adversos dos NM na saúde humana é o seu potencial efeito carcinogénico, que importa avaliar e caracterizar. Contudo, os ensaios de carcinogénese são demorados (cerca de 2 anos) e muito dispendiosos, uma vez que se baseiam na exposição de um elevado número de animais ao agente em estudo e na observação do estado de saúde ao longo da sua vida, com vista à deteção da eventual formação de tumores. Dado que a carcinogénese é um processo complexo, com múltiplos passos, em que estão frequentemente envolvidas mutações em genes críticos e instabilidade genómica, grande parte dos agentes carcinogénicos atua por uma via genotóxica, i.e., através da indução de lesões irreversíveis no genoma cuja acumulação contribui para a tumorigénese. Estabelecida a associação entre genotoxicidade e carcinogénese, foram desenvolvidos ensaios de genotoxicidade (de curto termo) para permitir prever de uma forma mais rápida e económica o efeito carcinogénico de qualquer agente físico, químico ou biológico. Assim, a avaliação da segurança no que se refere ao seu efeito genotóxico é geralmente baseada numa combinação de ensaios que permitem avaliar 3 tipos de alterações genéticas com particular relevância na determinação de cancro: mutação génica e clastogenicidade (quebra cromossómica) e aneuploidia (perda cromossómica). Dado que um único teste é insuficiente para caracterizar estes três eventos-chave, têm sido propostas várias abordagens baseadas na combinação de testes de genotoxicidade de curto termo in vitro e in vivo, conforme preconizado na revisão das linhas orientadoras elaboradas pelo grupo de trabalho da International Conference on Harmonisation of Technical Requirements for Registration of Pharmaceuticals for Human Use (ICH)40, 41 e, mais recentemente, da Organização Mundial de Saúde/Programa Internacional de Segurança Química (OMS/IPCS)42. Ensaios deste tipo têm vindo a ser realizados utilizados no Departamento de Genética Humana do Instituto Nacional de Saúde Dr. Ricardo Jorge com vista à caracterização de efeitos genotóxicos de agentes físicos, químicos e biológicos e seus mecanismos de ação a nível molecular, celular e do organismo43, 44.
No entanto, as considerações expostas sobre as propriedades específicas dos NM conduzem novamente à questão que tem sido amplamente discutida no meio científico4, 45, 46: será a metodologia atual de avaliação de risco utilizada na UE para os compostos químicos diretamente aplicável aos NM, ou deverá ser modificada para se adequar às características específicas dos NM?
A resposta a esta questão depende, por um lado, da existência de conhecimento científico detalhado sobre o comportamento dos NM nos sistemas biológicos similares aos humanos, ou que sejam extrapoláveis para a espécie humana. Por outro lado, implica a validação das metodologias de avaliação de toxicidade, em especial de genotoxicidade, já existentes, bem como da sua capacidade para detetarem os efeitos dos NM nesses sistemas biológicos. Surgiu, assim, a nanogenotoxicologia, que tem o objetivo de avaliar o potencial genotóxico dos NM tentando, em paralelo, esclarecer as propriedades físico-químicas mais relevantes para esse tipo de efeitos33.
Globalmente, numa primeira abordagem, procura-se realizar a avaliação dos efeitos genotóxicos dos NM, utilizando os ensaios e os modelos experimentais já validados33. Contudo, a maioria dos estudos publicados tem revelado resultados muito diversos e até contraditórios para uma mesma classe de NM, evidenciando limitações inerentes à especificidade de trabalhar com materiais à escala nano, bem como diferenças na execução experimental que dificultam a comparação dos resultados, não permitindo uma análise conclusiva. As secções seguintes ilustram estas dificuldades, através da informação relativa à avaliação da segurança dos NM de dióxido de titânio e de nanotubos de carbono, amplamente utilizados em produtos de consumo.
O caso dos nanomateriais de dióxido de titânio
Existem vários tipos de pigmento branco de dióxido de titânio, utilizados na produção de tintas e revestimentos. O dióxido de titânio é usado também em papel, plástico, cerâmica, borracha, tinta de impressoras, revestimentos do chão, catalisadores, tecidos e têxteis, cosméticos (e.g. em protetores solares), corantes alimentares, medicamentos e componentes eletrónicos47. Os diferentes nanomateriais de dióxido de titânio, embora com a mesma composição química, podem apresentar-se com 4 estruturas cristalinas diferentes: rutilo, anatase, broquite ou dióxido de titânio (B)1, sendo que as formas rutilo e anatase são as mais frequentemente usadas em produtos de consumo.
Recentemente, o National Institute for Occupational Safety and Health (NIOSH)43 recomendou limites de exposição de 0,3 mg/m3 de ar para o dióxido de titânio nas formas nano. O limite de exposição em Portugal para esta substância é de 10 mg/m3 de ar, considerando o TWA (8-h tempo médio ponderado)15.
Como referimos anteriormente, embora não existam dados atuais sobre a exposição de trabalhadores aos NM de dióxido de titânio, os dados de 1981-83 indicam que 2,7 milhões de trabalhadores estavam potencialmente expostos a estes NM15, especialmente por via inalatória. No entanto, de acordo com a revisão recente da NIOSH, os 5 estudos epidemiológicos já realizados sobre a exposição dos trabalhadores e da população aos nanomateriais de dióxido de titânio (em pó) não evidenciaram um risco acrescido de mortalidade ou morbilidade por cancro do pulmão43. Assim, a NIOSH considera não existir evidência suficiente para classificar os NM de dióxido de titânio como potenciais agentes carcinogénicos em contexto ocupacional47. Porém, na classificação da Agência Internacional para a Investigação em Cancro (International Agency for Research on Cancer, IARC), o dióxido de titânio na forma nano é considerado como «possivelmente carcinogénico para humanos» (Grupo 2 B), pois, muito embora não exista evidência adequada para a sua carcinogenicidade em humanos, há evidência suficiente de efeitos carcinogénicos em animais15. No que se refere ao seu potencial genotóxico, a investigação até ao momento não foi conclusiva: enquanto vários estudos realizados em bactérias revelaram não existir genotoxicidade induzida pelo dióxido de titânio15, 47, foram já reportados efeitos positivos em células eucariotas e em animais. Os diferentes resultados refletem, possivelmente, diferentes características dos NM investigados, como a forma cristalina ou a pureza, diferentes procedimentos usados para a sua dispersão em meio aquoso (p. ex. meio para cultura celular ou veículo para administração em animais), diferentes vias de exposição, nem sempre explicitadas na literatura, ou ainda diferenças entre os modelos experimentais utilizados. Globalmente, o «corpo de evidência» relativamente à existência ou não de genotoxicidade associada aos NM de dióxido de titânio, bem como o modo como essa genotoxicidade surge, necessita ainda ser esclarecido.
Outro tipo de efeitos adversos a considerar, em termos de impacto a longo termo para o ambiente e para a saúde humana, é a desregulação endócrina. Num estudo recente, Wang et al. (2011) observaram que uma exposição prolongada a NM de dióxido de titânio afetou negativamente a reprodução de peixes-zebra e a sobrevivência dos embriões, independentemente da concentração48. Ainda que as condições de exposição não tenham sido igualmente seguidas para o grupo de controlo, os resultados da análise histológica e do estudo de expressão génica permitiram, respetivamente, caracterizar um atraso na foliculogénese bem com um perfil de expressão génica compatível com alterações da maturação e da função dos ovários dos peixes expostos a dióxido de titânio, confirmando que este NM pode ser tóxico ao nível do sistema reprodutor dessa espécie. Assim, sugere-se que a contaminação de ambientes aquáticos com NM de dióxido de titânio, mesmo em baixas doses, pode ter impacto na reprodução das espécies, efeito que, até ao momento, não tinha sido descrito, constituindo mais um motivo para a investigação do potencial impacto dos NM no ambiente e na saúde humana.
O caso dos nanotubos de carbono e o paradigma dos asbestos
Os nanotubos de carbono (CNT) são um tipo de nanomateriais manufaturados cujas aplicações têm vindo a aumentar muito significativamente. Consistem em cilindros de carbono à escala nano, constituídos por grafenos, podendo variar na sua forma, dimensão, características físicas, revestimentos, composição química ou funcionalização49. Os nanotubos de carbono de parede simples (SWCNT) têm um diâmetro de cerca de 1 nm, sendo formados por um só cilindro, enquanto os nanotubos de carbono de parede múltipla (MWCNT) são constituídos por numerosos SWCNT concêntricos, possuindo diâmetros de cerca de 2-100 nm; existem ainda as nanofibras de carbono com diâmetros entre 40 e 200 nm50. Os CNT são mecanicamente muito resistentes, flexíveis e bons condutores de eletricidade, o que permite a sua utilização em diversas aplicações, nomeadamente, em compósitos reforçados, sensores e eletrónica50.
Durante o seu ciclo de vida, os CNT podem atingir o ambiente, não se sabendo, porém, como se comportam na cadeia alimentar51. Não existem dados de estudos epidemiológicos ou de biomonitorização até à data14 que apontem para efeitos adversos no Homem.
No entanto, as semelhanças no tamanho e forma entre os CNT e as fibras de asbestos têm gerado preocupações sobre a sua segurança. A principal questão deriva não só da sua dimensão nano, mas também da estrutura fibrosa que os torna semelhantes, neste aspeto, aos asbestos. Num estudo recente, após injeção intraperitoneal de MWCNT em ratinhos, foi mesmo sugerido um mecanismo de patogenicidade semelhante ao dos asbestos. Porém, em vez de se desenvolver cancro, verificou-se antes a encapsulação dos CNT pelas células multinucleadas do sistema imunitário, numa aparente «fagocitose frustrada». Em contraste, Takagi et al., após exposição de ratinhos p53+/− (que se sabe serem sensíveis aos asbestos) a uma dose elevada de MWCNTs, observaram a indução de mesotelioma, uma neoplasia maligna associada à exposição a asbestos52. Mais recentemente, os trabalhos de Muller et al. não revelaram indução de carcinogénese em ratos expostos a MWCNT53, ficando assim por esclarecer a questão da analogia com os asbestos.
A carcinogénese induzida por fibras é, provavelmente, um processo complexo envolvendo um stress genotóxico de longo termo. Poder-se-á assumir que as fibras do NM são genotóxicas primariamente através da interação direta com o DNA, o aparelho mitótico ou via stress oxidativo e, secundariamente, em consequência da resposta inflamatória. Considerando o paradigma das fibras, sustentado na inflamação crónica como precursora do processo carcinogénico, vários estudos têm investigado a ocorrência de respostas inflamatórias após exposição de animais a CNTs. Inicialmente, os estudos de Muller53 mostraram a indução de inflamação por instilação intratraqueal de MWCNT. Ensaios em ratos expostos por inalação de MWCNT demonstraram a ocorrência de lesões no pulmão (inflamação e formação de granulomas), embora não tenham revelado toxicidade sistémica54. Porter et al. (2010) observaram também inflamação pulmonar e fibrose em ratinhos expostos a MWCNT55. Por outro lado, em ratinhos C57BL/6, outros autores não verificaram inflamação dos pulmões nem lesões, mas sim alterações imunitárias sistémicas após inalação de MWCNT56. Porém, estudos de toxicogenómica identificaram a exposição a MWCNT como causa de alterações da expressão génica num conjunto de biomarcadores de cancro do pulmão em ratinhos57. Os estudos de Ryman-Rasmussen et al. (2009) sugeriram que uma inflamação alérgica preexistente poderia aumentar a sensibilidade à inalação de MWCNT, efeito confirmado no estudo de Park et al58.
Relativamente a genotoxicidade, existem muitas evidências de indução de lesões no DNA pelos MWCNT, mas ainda existem resultados contraditórios. Por exemplo, ensaios de mutagénese em bactérias e ensaios citogenéticos em linfócitos humanos (análise de micronúcleos e trocas de cromatídeos irmãos) revelaram-se negativos59. Contudo, a exposição de linfócitos humanos a MWCNT aumentou a incidência de quebras no DNA de um modo dependente da dose, com concomitante declínio da proliferação celular56. Estudos de genotoxicidade em linhas celulares humanas derivadas do epitélio respiratório revelaram também resultados positivos60. Ou seja, também no caso dos nanotubos de carbono, os dados são inconsistentes e existe a necessidade de esclarecer as suas propriedades e mecanismos de genotoxicidade para garantir a segurança da sua utilização.
Nanotoxicologia: as lacunas e os progressos no conhecimento
Grande parte dos trabalhos publicados sobre nanotoxicologia não descreve adequadamente a caracterização físico-química dos NM testados, tais como tamanho, forma, composição química, cristalinidade e propriedades de superfície (e.g., área, porosidade, carga, funcionalização), que condicionam fortemente a sua cinética e atividade biológica. Para além disso, aspetos relacionados com o procedimento experimental, tais como o método de preparação e controlo de dispersões dos NM, as condições de exposição, a falta de controlos positivos e a utilização de metodologias ainda não estandardizadas, podem ser determinantes nos resultados obtidos. Por exemplo, a agregação dos NM pode condicionar mecanismos como a eliminação efetiva das partículas maiores pelos macrófagos. Muitos estudos são conduzidos em intervalos de concentrações muito elevadas, favorecendo a agregação e, consequentemente, reduzindo a sua potencial toxicidade4. Por isso, em muitos dos estudos poderão não ser detetados efeitos mais subtis que podem ocorrer a baixas concentrações, com risco para a saúde humana, como é o caso da indução de lesões no DNA em células somáticas ou em células germinais, que podem contribuir a longo prazo para, respetivamente, o desenvolvimento de um processo cancerígeno ou para o aparecimento de doenças hereditárias na descendência.
Procurando responder a algumas destas necessidades de conhecimento, iniciou-se em 2010 a Ação Concertada Europeia «NANOGENOTOX- Safety Evaluation of Manufactured Nanomaterials by Characterisation of their potential Genotoxic Hazard» (projeto cofinanciado pela EAHC e 11 Estados-Membros da UE, no qual o INSA participa como representante de Portugal). Este projeto pretende colmatar a escassez de conhecimento científico relativamente aos potenciais riscos para a saúde associados aos NM e contribuir, assim, para a melhoria da saúde e segurança dos cidadãos, no que diz respeito à utilização de nanomateriais. O plano de trabalho inclui o recurso a um painel de NM de dióxido de titânio, de sílica e de nanotubos de carbono, que serão adequada e completamente caracterizados do ponto de vista físico-químico e cuja dispersão em meio aquoso será otimizada no âmbito do projeto, para minimizar a variabilidade inerente a esses fatores. Os parâmetros toxicocinéticos serão caracterizados em modelos murinos para análise da biopersistência e identificação de órgãos-alvo. Por sua vez, a potencial genotoxicidade desses NM será avaliada utilizando-se uma combinação de ensaios de genotoxicidade estandardizados, quer em linhas celulares quer em roedores. Assim, espera-se obviar a maioria das limitações apontadas aos estudos anteriores e produzir dados consistentes que permitam o estabelecimento de metodologias robustas, isto é, específicas e sensíveis, para caracterização dos potenciais efeitos genotóxicos dos NM, contribuindo também para a avaliação de risco. Em complemento, espera-se também fornecer suporte científico para apoiar as decisões regulamentares que é urgente delinear, à escala europeia.
Conclusões
Verifica-se, presentemente, um incremento significativo no desenvolvimento, produção e utilização de nanomateriais manufaturados a nível mundial. A nanotecnologia foi identificada, em vários relatórios de referência, como um fator-chave de desenvolvimento, fornecendo a base para a inovação em termos de aplicações e produtos, nomeadamente, na área da medicina e produtos de consumo, sendo atualmente considerada essencial para a competitividade num mercado global. No entanto, o desenvolvimento sustentado e a comercialização e aceitação dos seus produtos, por parte da sociedade em geral, tem como pré-requisito basear-se em processos e usos seguros para o homem e com baixo impacto para o ambiente. Ora, como vimos, embora a informação sobre os níveis de NM a que a população humana se encontra exposta (em contexto ambiental ou ocupacional) seja ainda escassa, existem vários estudos in vitro e in vivo que indiciam efeitos biológicos adversos dos NM com potencial impacto na saúde humana. Assim, as necessidades «societais57 previstas para o futuro dos nanomateriais manufaturados relacionam-se, por um lado, com o desenvolvimento de novas aplicações e, principalmente, com o desenvolvimento um paradigma de nanotoxicologia preditiva que permita evitar os seus potenciais efeitos adversos, garantindo a sua utilização segura durante todo o seu ciclo de vida. Para esse fim, é necessária uma congregação de esforços que permita, por um lado, preencher as lacunas do conhecimento acerca dos potenciais efeitos nocivos dos NM e, por outro, estabelecer níveis de exposição aceitáveis para a preservação da saúde humana e do ambiente. Enquanto não for rigorosamente demonstrada a segurança dos nanomateriais, isto é, perante a incerteza quanto ao risco decorrente da exposição a nanomateriais, deverá aplicar-se o princípio da precaução visando a proteção da saúde pública.
Neste contexto, a nanotoxicologia poderá dar um contributo inestimável relativamente à avaliação dos efeitos nocivos dos NM e, em particular, os estudos de genotoxicidade poderão fornecer evidências quanto ao potencial de os NM contribuírem para o desenvolvimento de doenças crónico-degenerativas e genéticas e, em particular, de cancro. Contudo, devido à complexidade associada às suas propriedades físico-químicas únicas, a caracterização da genotoxicidade destes materiais e a comparação dos resultados de diversos estudos constitui um desafio para cientistas e reguladores. Em resposta a esse desafio, a construção de repositórios de NM de referência e a sua partilha entre a comunidade científica afigura-se como essencial para possibilitar a comparação interlaboratorial dos efeitos observados para um mesmo NM ou para uma classe de NM. Para além disso, a complexidade inerente à nanotoxicologia tem vindo a ser ultrapassada através de uma abordagem alargada e multidisciplinar, envolvendo a integração de resultados de toxicocinética e toxicodinâmica com os da caracterização exaustiva das propriedades físico-químicas dos NM e do seu comportamento dinâmico em meios biológicos. Dessa integração têm vindo a surgir conhecimentos sobre as interações dos NM com os sistemas biológicos e os mecanismos de ação subjacentes aos efeitos observados, ao nível tecidular, celular e molecular, contribuindo para um reforço da evidência científica sobre a potencial toxicidade dos NM. Deste modo, poderão ser preenchidas as lacunas de conhecimento acerca da toxicidade dos NM e ser estabelecida uma evidência alicerçada numa base de conhecimento científico sólido, em consonância com a visão de uma toxicologia do século XXI61. Esta plataforma de evidência permitirá abordar o segundo desafio que surge para a saúde pública: efetuar uma avaliação de risco ao longo do ciclo de vida dos NM, desde a sua síntese e produção até à sua eliminação, com a ponderação dos riscos colocados a todos os intervenientes em contexto ocupacional, ambiental ou de consumidor/utilizador.
Por sua vez, a liderança e a coordenação das ações de análise de risco deve ser centralizada, quer ao nível nacional, quer europeu, envolvendo todas as partes interessadas, nomeadamente, a indústria, as associações empresariais, os investigadores, as autoridades de saúde, os consumidores e os reguladores. Tal análise pressupõe o registo dos produtos e produtores de NM e, bem assim, a determinação das exposições reais a que o ser humano pode estar sujeito, procurando estabelecer níveis de exposição aceitáveis para a preservação da saúde humana e do ambiente. Preconiza-se a implementação de algumas medidas de base, com vista a contribuir para a avaliação de risco, tais como: 1) organizar um registo nacional de todas as unidades industriais produtoras e utilizadoras de NM; 2) implementar um registo nacional de produtos de consumo humano contendo NM; 3) efetuar o registo de trabalhadores potencialmente expostos a NM na realização das suas tarefas e, logo que possível, fazer uma estimativa da sua exposição; 4) envolver a indústria para fornecer informação sobre as abordagens utilizadas para avaliação dos riscos de exposição aguda (acidental) e planos de contingência em caso de acidente, bem como os riscos de exposição crónica (baixas doses), incluindo medidas preventivas; 5) estabelecer uma base de dados de casos clínicos associados a efeitos nefastos de exposição a nanomateriais; e 6) monitorizar eventuais efeitos a longo prazo associados à exposição crónica a NM.
Finalmente, importa partilhar o conhecimento através da construção de bases de dados partilhadas e de repositórios de informação sobre as metodologias de avaliação de risco, resultados de investigação e medidas de vigilância e estimular a sua disseminação no meio científico e na sociedade62.
Contudo, o conhecimento atual ainda não é suficientemente sólido para permitir uma regulação da produção e aplicação das variadas classes de nanomateriais totalmente baseada na evidência científica. Neste caso, a adoção do princípio da precaução pode ajudar em simultâneo a inovação e a ciência. Como foi anteriormente referido, este princípio preconiza a necessidade de agir perante uma situação de incerteza de perigo potencialmente grave ou irreversível para a saúde ou para o ambiente, com o objetivo de o reduzir antes de se vir a provar cabalmente que ele existe de facto, tendo em conta os custos e benefícios da ação e da inação. Este princípio inclui elementos como: 1) investigação e monitorização para deteção precoce dos perigos associados aos NM; 2) redução geral da carga ambiental; 3) promoção de uma produção de NM ecológica e inovadora; e 4) princípio da proporcionalidade, onde os custos das ações para prevenir os perigos não deverão ser desproporcionados relativamente aos seus prováveis benefícios. Embora por vezes se tema que uma abordagem precaucionária possa asfixiar a inovação, ela pode, na realidade, proporcionar oportunidades de compreensão de sistemas complexos emergentes, tendo em conta as necessidades humanas, com menores custos para a saúde e para o ambiente. Assim, acomodar a avaliação de risco no processo de inovação tecnológica poderá ajudar a ultrapassar a relação controversa entre inovação e regulação.
Um outro desafio prende-se com o desenvolvimento de metodologias inovadoras, em especial abordagens de elevado rendimento, forte poder preditivo e custo controlado que possibilitem antecipar o risco associado à colocação no mercado de novos NM que vão sendo desenvolvidos. Significa isto que é necessário implementar métodos de avaliação de uma eventual toxicidade numa fase precoce do desenvolvimento do NM, antes de entrar na fase de produção industrial, para evitar grandes perdas económicas decorrentes de uma descoberta tardia de toxicidade e poder dirigir a síntese no sentido de obter moléculas mais seguras. De facto, considerando o elevado potencial de aplicações dos NM, deverá recorrer-se aos dados da nanotoxicologia, no sentido de dirigir a síntese de nanomateriais manufaturados que sejam safe-by-design, isto é, eliminando as características responsáveis pela sua toxicidade e possibilitando o progresso tecnológico e «societal» que a aplicação dos novos nanomateriais prenuncia.
Na área da saúde pública, a evidência científica não é em si mesma suficiente &- é necessário também atuar atempadamente e tomar decisões regulamentares relativamente os NM que permitam uma governança de risco mais adaptativa e eficaz. Não apenas a avaliação de risco, mas também a gestão do risco e a comunicação do risco, deverão ser reformuladas perante estes novos materiais. é essencial também a partilha de informação fidedigna entre todas as partes envolvidas para uma ação política efetiva e também a participação ativa de todos, incluindo dos cidadãos atentos e informados, nas tomadas de decisão. Acima de tudo, a saúde pública terá de assegurar a interligação e o equilíbrio entre a evolução tecnológica e a garantia da segurança dos nanomateriais e das nanotecnologias, por forma a que possamos beneficiar da inovação assegurando a proteção do ambiente e da saúde humana.
Bibliografía
1. Buzea C, Pacheco II, Robbie K. Nanomaterials and nanoparticles: sources and toxicity. Biointerphases. 2007; 2:MR17-71. [ Links ]
2. Comissão Europeia. Recomendação da Comissão de 18 de Outubro de 2011 sobre a definição de nanomaterial. JOUE. 2011; L275:38-40.
3. SCENIHR-Scientific Committee on Emerging and Newly Identified Health Risks. Risk assessment of products of nanotechnologies. Brussels: European Commission; 2009 (consultado 4 Set 2011). Disponível em: http://ec.europa.eu/health/archive/ph_risk/committees/04_scenihr/docs/scenihr_o_023.pdf. [ Links ]
4. Oberdörster G. Safety assessment for nanotechnology and nanomedicine: concepts of nanotoxicology. J Intern Med. 2010; 267:89-105. [ Links ]
5. Wijnhoven SWP, Dekkers S, Kooi M, Jongeneel WP, de Jong WH. Nanomaterials in consumer products: update of products on the European market in 2010. Bilthoven, NL: National Institute for Public Health and the Environment; 2011. (RIVM Report; 340370003/2010) (consultado 7 Set 2011). Disponível em: http://www.rivm.nl/bibliotheek/rapporten/340370003.pdf. [ Links ]
6. TGA, Therapeutic Goods Administration. A review of the scientific literature on the safety of nanoparticulate titanium dioxide or zinc oxide in sunscreens. Canberra, AU: Department of Health and Ageing. Australian Government; 2009 (consultado 27 Jan 2011). Disponível em: http://www.tga.gov.au/pdf/review-sunscreens-060220.pdf. [ Links ]
7. Woodrow Wilson International Center for Scholars. Consumer products inventory. Washington, DC: Project on Emerging Nanotechnologies; 2012 (consultado 15 Mar 2012). Disponível em: http://www.nanotechproject.org/inventories/consumer/. [ Links ]
8. European Commission. European Technology Platform on NanoMedicine. Nanotechnology for Health. Brussels: European Commission; 2008 (consultado 15 Mar 2012). Disponível em: http://cordis.europa.eu/nanotechnology/nanomedicine.htm. [ Links ]
9. Aitken RJ, Chaudhry MQ, Boxall AB, Hull M. Manufacture and use of nanomaterials: current status in the UK and global trends. Occup Med (Lond). 2006; 56:300-6. [ Links ]
10. Eugénio J, Fatal V. Evolução da nanotecnología: abordagem nacional e internacional. Lisboa: Instituto Nacional da Propriedade Industrial; 2010 (consultado 15 Set 2011). Disponível em: http://www.marcasepatentes.pt/files/collections/pt_PT/1/300/303/Evolu%C3%A7%C3%A3o%20da%20Nanotecnologia%20-%20Abordagem%20Nacional%20e%20Internacional.pdf. [ Links ]
11. Casimiro E, Santos S. Investigação em nanotecnologia & nanosegurança em Portugal (poster). In: Encontro Nacional de Nanotoxicologia 'E2N 2011', Fórum do Pólo Tecnológico de Lisboa, 7 e 8 de Fevereiro de 2011. Lisboa: Instituto Nacional de Saúde Dr. Ricardo Jorge (INSA), Direcção-Geral da Saúde (DGS), Instituto Superior Técnico (IST) e Laboratório Nacional de Energia e Geologia (LNEG); 2011. [ Links ]
12. Handy RD, Shawn BJ. Toxic effects of nanoparticles and nanomaterials: implications for public health, risk assessment and the public perception of nanotechnology. Health, Risk & Society. 2007; 9:125-44. [ Links ]
13. Som C, Berges M, Chaudhry Q, Dusinska M, Fernandes TF, Olsen SI, et-al. The importance of life cycle concepts for the development of safe nanoproducts. Toxicology. 2010; 269:160-9. [ Links ]
14. Becker H, Herzberg F, Schulte A, Kolossa-Gehring M. The carcinogenic potential of nanomaterials, their release from products and options for regulating them. Int J Hyg Environ Health. 2011; 214:231-8. [ Links ]
15. International Agency for Research on Cancer. Carbon black, titanium dioxide and talc. Lyon: World Health Organization; 2010. (IARC Monographs on the evaluation of carcinogenic risks to humans; 93). [ Links ]
16. Maynard AD, Baron PA, Foley M, Shvedova AA, Kisin ER, Castranova V. Exposure to carbon nanotube material: aerosol release during the handling of unrefined single-walled carbon nanotube material. J Toxicol Environ Health A. 2004; 67:87-107. [ Links ]
17. Brasseur G, Bondéelle A. La revolution «Nano». Travail&Sécurité. 2010; 708:21-33.
18. Schneider T. Evaluation and control of occupational health risks from nanoparticles. TemaNord 2007:581. Copenhagen: Nordic Council of Ministers; 2007. [ Links ]
19. Oomen A, Bennink , Van Engelen M, Sips JA. Nanomaterial in consumer products: detection characterisation and interpretation. Bilthoven, NL: National Institute for Public Health and the Environment; 2012. (RIVM Report 320029001/2011). [ Links ]
20. European Agency for Safety and Health at Work. Expert forecast on emerging chemical risks related to occupational safety and health: European risk observatory report. Brussels: European Agency for Safety and Health at Work; 2009. [ Links ]
21. Pietroiusti A. Health implications of engineered nanomaterials. Nanoscale. 2012; 4:1231-47. [ Links ]
22. Jacobsen NR. Mutagenicity, genotoxicity and inflammation caused by nanoparticles. Thesis. Copenhagen: Faculty of Health Sciences. University of Copenhagen; 2008. [ Links ]
23. WHO. Human health risk assessment toolkit: chemical hazards. Ottawa: WHO; 2010. [ Links ]
24. Resolução do Parlamento Europeu, de 24 de abril de 2009, sobre aspectos regulamentares dos nanomateriais. Jornal Oficial da União Europeia. (8.7.2010) C 184 E/82- C 184 E/89.
25. European Commission. Nanomaterials in REACH. Brussels: European Commission; 2009. [ Links ]
26. Van Benthem J. The effect of REACH implementation on genotoxicity and carcinogenicity testing. Bilthoven, NL: National Institute for Public Health and the Environment; 2008. (RIVM Report 601200008/2007) (consultado 20 Mar 2012). Disponível em: http://www.rivm.nl/bibliotheek/rapporten/601200008.pdf. [ Links ]
27. Grieger KD, Baun A, Owen R. Redefining risk research priorities for nanomaterials. J Nanopart Res. 2010; 12:383-92. [ Links ]
28. European Commission. Opinion on safety of nanomaterials in cosmetic products. Brussels: Health and Consumer Protection DG Directorate C: Public Health and Risk Assessment; 2007. [ Links ]
29. Warshaw J. The trend towards implementing the precautionary principle in US regulation of nanomaterials. Dose Response. 2012; 10:384-96. [ Links ]
30. European Environment Agency. Late lessons from early warnings: the precautionary principle 1896-2000. Environmental Issue Report (2001) 22. [ Links ]
31. Maynard AD, Warheit DB, Philbert MA. The new toxicology of sophisticated materials: nanotoxicology and beyond. Toxicol Sci. 2011; 120(Suppl 1):S109-29. [ Links ]
32. Zhu M, Nie G, Meng H, Xia T, Nel A, Zhao Y. Physicochemical properties determine nanomaterial cellular uptake transport and fate. Acc Chem Res. 2012. (Epub ahead of print). [ Links ]
33. Singh N, Manshian B, Jenkins GJ, Griffiths SM, Williams PM, Maffeis TG, et-al. NanoGenotoxicology: the DNA damaging potential of engineered nanomaterials. Biomaterials. 2009; 30:3891-914. [ Links ]
34. Jacobsen NR, Pojana G, White P, Møller P, Cohn CA, Korsholm KS, et-al. Genotoxicity, cytotoxicity, and reactive oxygen species induced by single-walled carbon nanotubes and C(60) fullerenes in the FE1-Muta®Mouse lung epithelial cells. Environ Mol Mutagen. 2008; 49:476-87. [ Links ]
35. Li N, Ma L, Wang J, Zheng L, Liu J, Duan Y, et-al. Interaction between nano-anatase TiO(2) and liver DNA from mice in vivo. Nanoscale Res Lett. 2009; 5:108-15. [ Links ]
36. Biver T, Eltugral N, Pucci A, Ruggeri G, Schena A, Seccoa F, et-al. Synthesis, characterization, DNA interaction and potential applications of gold nanoparticles functionalized with acridine orange fluorophores. Dalton Trans. 2011; 40:4190-9. [ Links ]
37. Nel A, Xia T, Meng H, Wang X, Lin S, Ji Z, et-al. Nanomaterial toxicity testing in the 21st century: use of a predictive toxicological approach and high-throughput screening. Acc Chem Res. 2012. [ Links ]
38. Joint Research Center. Impact of engineered nanomaterials on health: considerations for benefit-risk assessment - EASAC Policy Report - JRC Reference Report. Brussels: European Union; 2011 (consultado 12 Mar 2012). Disponível em: http://publications.jrc.ec.europa.eu/repository/bitstream/111111111/22610/1/impact%20of%20engineered%20nanomaterials%20on%20health.pdf. [ Links ]
39. Hankin S, Boraschi D, Duschl A, Lehr C-M, Lichtenbeld H. Towards nanotechnology regulation: publish the unpublishable. Nano Today. 2011; 6:228-31. [ Links ]
40. European Medicines Agency. ICH Topic S 1 A- The need for carcinogenicity studies of pharmaceuticals. London: European Medicines Agency; 1996 (consultado 20 Set 2011). Disponível em: http://www.ema.europa.eu/docs/en_GB/document_library/Scientific_guideline/2009/09/WC500002699.pdf. [ Links ]
41. European Medicines Agency. ICH Topic S1B- Carcinogenicity: Testing for Carcinogenicity of Pharmaceuticals. London: European Medicines Agency; 1998 (consultado 20 Set 2011). Disponível em: http://www.ema.europa.eu/docs/en_GB/document_library/Scientific_guideline/2009/09/WC500002735.pdf. [ Links ]
42. Eastmond DA, Hartwig A, Anderson D, Anwar WA, Cimino MC, Dobrev I, et-al. Mutagenicity testing for chemical risk assessment: update of the WHO/IPCS Harmonized Scheme. Mutagenesis. 2009; 24:341-9. [ Links ]
43. Louro H, Faustino I, Dias A, Boavida MG, Silva MJ. Poly (ADP-ribose) polymerase-1 deficiency does not affect ethylnitrosourea mutagenicity in liver and testis of lacZ transgenic mice. Environ Mol Mutagen. 2010; 51:322-9. [ Links ]
44. Louro H, Silva MJ. Cost/benefit of mutation induction under PARP1 deficiency: from genomic instability to therapy. NY: Nova Science Publishers, Inc.; 2011. [ Links ]
45. Maynard AD, Aitken RJ, Butz T, Colvin V, Donaldson K, Oberdörster G, et-al. Safe handling of nanotechnology. Nature. 2006; 444:267-9. [ Links ]
46. Oberdörster G, Oberdörster E, Oberdörster J. Concepts of nanoparticle dose metric and response metric. Environ Health Perspect. 2007; 115:A290. [ Links ]
47. NIOSH. National Institute for Occupational Safety and Health. Occupational exposure to titanium dioxide. Atlanta, GA: Department of Health and Human Services. Centers for Disease Control and Prevention National Institute for Occupational Safety and Health; 2011. (Current Intelligence Bulletin; 63). [ Links ]
48. Wang J, Zhu X, Zhang X, Zhao Z, Liu H, George R, et-al. Disruption of zebrafish (Danio rerio) reproduction upon chronic exposure to TiO2 nanoparticles. Chemosphere. 2011; 83:461-7. [ Links ]
49. NIOSH. National Institute for Occupational Safety and Health. Occupational exposure to carbon nanotubes and nanofibers. Atlanta, GA: Department of Health and Human Services. Centers for Disease Control and Prevention National Institute for Occupational Safety and Health; 2010. (Current Intelligence Bulletin; 60). [ Links ]
50. The Royal Society. The Royal Academy of Engineering. Nanoscience and nanotechnologies: opportunities and uncertainties. London: The Royal Society; 2004.(consultado 12 Mar 2012). Disponível em: http://www.occup-med.com/content/pdf/1745-6673-6-7.pdf. [ Links ]
51. Helland A, Wick P, Koehler A, Schmid K, Som C. Reviewing the environmental and human health knowledge base of carbon nanotubes. Environ Health Perspect. 2007; 115:1125-31. [ Links ]
52. Takagi A, Hirose A, Nishimura T, Fukumori N, Ogata A, Ohashi N, et-al. Induction of mesothelioma in p53+/- mouse by intraperitoneal application of multi-wall carbon nanotube. J Toxicol Sci. 2008; 33:105-16. [ Links ]
53. Muller J, Delos M, Panin N, Rabolli V, Huaux F, Lison D. Absence of carcinogenic response to multiwall carbon nanotubes in a 2-year bioassay in the peritoneal cavity of the rat. Toxicol Sci. 2009; 110:442-8. [ Links ]
54. Ma-Hock L, Treumann S, Strauss V, Brill S, Luizi F, Mertler M, et-al. Inhalation toxicity of multiwall carbon nanotubes in rats exposed for 3 months. Toxicol Sci. 2009; 112:468-81. [ Links ]
55. Porter DW, Hubbs AF, Mercer RR, Wu N, Wolfarth MG, Sriram K, et-al. Mouse pulmonary dose- and time course-responses induced by exposure to multi-walled carbon nanotubes. Toxicology. 2010; 269:136-47. [ Links ]
56. Mitchell LA, Gao J, Wal RV, Gigliotti A, Burchiel SW, Mcdonald JD. Pulmonary and systemic immune response to inhaled multiwalled carbon nanotubes. Toxicol Sci. 2007; 100:203-14. [ Links ]
57. Pacurari M, Qian Y, Porter DW, Wolfarth M, Wan Y, Luo D, et-al. Multi-walled carbon nanotube-induced gene expression in the mouse lung: association with lung pathology. Toxicol Appl Pharmacol. 2011; 255:18-31. [ Links ]
58. Park MV, Lankveld DP, van Loveren H, de Jong WH. The status of in vitro toxicity studies in the risk assessment of nanomaterials. Nanomedicine (Lond). 2009; 4:669-85. [ Links ]
59. Szendi K, Varga C. Lack of genotoxicity of carbon nanotubes in a pilot study. Anticancer Res. 2008; 28:349-52. [ Links ]
60. Cveticanin J, Joksic G, Leskovac A, Petrovic S, Sobot AV, Neskovic O. Using carbon nanotubes to induce micronuclei and double strand breaks of the DNA in human cells. Nanotechnology. 2010; 21:015102. [ Links ]
61. Lindberg HK, Falck GC, Suhonen S, Vippola M, Vanhala E, Catalán J, et-al. Genotoxicity of nanomaterials: DNA damage and micronuclei induced by carbon nanotubes and graphite nanofibres in human bronchial epithelial cells in vitro. Toxicol Lett. 2009; 186:166-73. [ Links ]
62. En: Roco M., Mirkin C.A., Hersam M.C., editors. WTEC Panel Report on Nanotechnology research directions for societal needs in 2020: retrospective and outlook. Washington, DC: World Technology Evaluation Center. Springer; 2010. [ Links ]
*Autora para correspondência. henriqueta.louro@insa.min-saude.pt













