Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Revista de Ciências Agrárias
versão impressa ISSN 0871-018X
Rev. de Ciências Agrárias vol.34 no.2 Lisboa jul. 2011
Efecto del sustrato sobre las propiedades biológicas en la planta de fresa
Fátima Martínez1, Silvia Castillo2, Silvia Pérez2, Pedro Palencia1, Eusebio Carmona2, José Ordovás2 e Manuel Avilés2
1Dpto. de Ciencias Agroforestales. E.P.S. "La Rábida". Universidad de Huelva. 21819. Palos de la Frontera. Huelva. fatima.martinez@dcaf.uhu.es;
2Dpto. de Ciencias Agroforestales. Universidad de Sevilla. E.T.S.I.A. Ctra. Utrera Km 1, s/n. 41013. Sevilla. aviles@us.es
RESUMEN
El objetivo de este trabajo fue evaluar el efecto que diferentes sustratos ejercen sobre las características microbiológicas en la rizosfera de la planta de fresa en un sistema de cultivo sin suelo cerrado. Se ensayaron 3 sustratos: compost de corcho más cascarilla de arroz 1:1 v:v (CC), turba (T) y fibra de coco (FC). Se evaluó la comunidad microbiana y las propiedades químicas de los sustratos. El CC presentó valores de pH significativamente superiores a la FC y a la T y una densidad de bacterias copiotrofas, Bacillus sp. y actinomycetes oligotrofos superior a la de la T, tanto al inicio del ensayo como a los 2.5 meses de cultivo. La T mostró una densidad de hongos superior al CC, tanto al inicio del ensayo como a los 2.5 meses de cultivo. El sustrato de FC mostró a los 2.5 meses de cultivo mayor densidad de bacterias copiotrofas, Pseudomonas fluorescentes y hongos en la rizosfera que en la no rizosfera.
Palabras clave: control biológico, cultivo sin suelo.
Effect of growth media on biological properties in strawberry plants
ABSTRACT
The aim of this research was to study the effect of different growth media on the microbiologic characteristics in rhizosphere of strawberry plants in closed soilless growing systems. We used 3 substrates: composted cork and rice hulls (CC) (1:1 v:v), peat (P) and coir fiber (CF). Chemical variables and microbial community profile of the growth media were evaluated. The CC showed a higher pH than CF and P. At the beginning and at two and a half months after transplantation, copiotrophic bacteria, Bacillus sp. and oligotrophic actinomycetes were higher in CC than in P. At the beginning and at two and a half months after transplantation fungi were higher in P than in CC. At two and a half months after transplantation, in CF copiotrophic bacteria, fluorescent Pseudomonas sp. and fungi were higher in rhizosphere than in non-rhizosphere substrate.
Keywords: biological control, soilless growing systems.
INTRODUCCIÓN
La eliminación de los sustratos utilizados en un cultivo sin suelo (CSS) al final de su vida representa, en algunos casos, un problema. Así, por ejemplo, la lana de roca no es biodegradable y sus residuos son nocivos para la salud humana. No ocurre lo mismo con los restos de sustratos orgánicos (turbas) que sí son biodegradables y pueden ser incorporados al suelo como enmienda orgánica (Marfá, 2000). Sin embargo, la turba es un recurso no renovable por lo que se deben buscar sustratos alternativos, procedentes de recursos renovables, que contribuyan a una mayor sostenibilidad del CSS. Por ello, se ha emprendido una búsqueda de materiales locales que las puedan sustituir en numerosas partes del mundo, con la ventaja añadida de reducir los costes de producción. No en vano, ya existen limitaciones en las extracciones de las turberas, dentro de las políticas de protección del medio ambiente de los países productores, tanto por el impacto ambiental de la extracción en sí, como por ser las turberas importantes sumideros de anhídrido carbónico (Abad, 1991). En este contexto, han adquirido especial importancia los residuos agroindustriales (Raviv et al., 1986). Una característica a destacar de los sustratos a base de compost es su capacidad supresora frente a las principales enfermedades fúngicas de origen edáfico de las plantas (Hoitink et al., 1996).
El término supresivo se aplica a aquellos suelos o sustratos en los que las enfermedades, causadas por determinados patógenos no se manifiestan o lo hacen mínimamente, a pesar de que los fitopatógenos están naturalmente presentes o artificialmente introducidos, de cultivar un huésped susceptible y de que el ambiente aéreo sea favorable (Baker y Cook, 1974; Schroth y Hancock, 1981). Por el contrario, un medio conductivo es aquel que carece de supresividad (Huber y Schneider, 1982). El fenómeno de los suelos supresivos demuestra la efectividad de la actividad microbiana contra patógenos de suelo. En estos medios se impide una o varias etapas de la patogénesis o la supervivencia del patógeno.
La supresividad de un suelo puede clasificarse según los mecanismos de control biológico (Hoitink et al., 1991; Garibaldi, 1983; Hoitink et al., 1993; Boehm et al., 1997; Baker y Cook, 1974) en: supresividad general y específica. La supresividad general se aplica cuando la supresión de la enfermedad se debe a la actividad de distintos grupos de microorganismos que son capaces de actuar como agentes de control biológico. Es decir, está directamente relacionada con la actividad biológica total en el medio en momentos críticos de la patogénesis, principalmente durante la germinación de los propágulos y el crecimiento rizosférico del fitopatógeno (Hoitink et al., 1991; Baker y Cook, 1974; Cook y Baker, 1983). La supresividad específica se aplica cuando la presencia de uno o unos pocos tipos de microorganismos pueden explicar la supresión de un patógeno o de la enfermedad que cause. Un caso de la supresión específica son los microorganismos que micoparasitan o los que inducen resistencia a la planta hacia algún patógeno. Así, se puede inducir la supresividad por introducción de determinados antagonistas seleccionados a los suelos o sustratos (Baker y Chet, 1982; Lewis y Papavizas, 1991; Becker y Schwinn, 1993; Cambell, 1994), existiendo una relación directa entre la supresividad, la actividad y la composición de la microflora del sustrato (Tuitert et al., 1998). A diferencia de la supresión natural, en ésta podemos obtener el agente causante de supresión e inocularlo a otro sustrato, consiguiendo así un sustrato supresivo a la enfermedad específica que produzca este patógeno (Baker y Cook, 1974).
El CSS en sustrato, fue concebido originalmente para su manejo a solución perdida. Sin embargo, debido a la preocupación cada vez mayor por el deterioro del medio ambiente dichos sistemas abiertos están siendo adaptados a las nuevas exigencias, por lo que cada día se impone con más fuerza la necesidad de la regeneración y reutilización de esta agua de drenaje en CSS cerrado.
En este trabajo se ha evaluado el efecto que diferentes sustratos ejercen sobre las características microbiológicas en la rizosfera de la planta de fresa en un sistema de CSS cerrado.
MATERIALES Y MÉTODOS
Los sustratos que se emplearon fueron un compost de corcho más cascarilla de arroz 1:1 v:v (CC), un sustrato de turba (T) y un sustrato de fibra de coco (FC). Los sustratos se ensayaron en un sistema de CSS cerrado. Para evaluar el posible efecto del sustrato se cuantifico la población cultivable de ciertos grupos econutritivos de microorganismos. Para la caracterización de la comunidad microbiana se escogieron diferentes grupos de microorganismos cultivables asociados a fenómenos de biocontrol; para ello se siguió el procedimiento de diluciones seriadas y siembra en medios semiselectivos descrito por Tuiter et al., (1998) con algunas modificaciones, expresándose en UFC (unidades formadoras de colonia) ml-1 de sustrato.
Los microorganismos cultivables que se cuantificaron a partir de los dos sustratos CC y T al inicio del cultivo, así como de la rizosfera y no rizosfera de la planta a los 2,5 meses de cultivo en el sustrato de fibra de coco fueron los siguientes: bacterias copiotróficas, Bacillus sp., Pseudomonas fluorescentes, bacterias y actinomycetes oligotróficos, bacterias y actinomycetes celulolíticos y hongos (Tuiter et al., 1998).
En el análisis microbiológico se utilizó la técnica de las suspensiones-diluciones en serie. El procedimiento para determinar la densidad de población de diferentes grupos de bacterias y hongos cultivables fue el siguiente:
La extracción se realizó colocando entre 5-10 g de muestra de sustrato en unerlenmeyer de 1000 ml. Posteriormente se añadió 250 ml de una solución de 0,1% de pirofosfato de sodio 10-hidratado (Na4P2O7·10 H2O). La solución extractante y el material de laboratorio que se utilizó fueron autoclavados a 120º C durante 30 minutos antes de su uso.
Otra muestra de sustrato previamente pesado (5 a 10 g), se llevó a estufa a 105º C durante 48 horas para determinar el porcentaje de humedad de éstas y así poder expresar los datos respecto al peso seco del sustrato. Las diluciones se realizaron conformando como 10-1 la suspensión de muestra con el extractante, y las sucesivas se realizaron diluyendo 1 ml de la dilución mayor anterior con 9 ml de un preparado de agar agua al 1% con agua destilada estéril y se agitó. Con esto se consiguió diluir 10 veces la concentración en cada dilución.
Las diluciones que se utilizaron fueron las mismas para los dos sustratos. Así, para Bacillus ssp. 10-1, 10-2, 10-3 y 10-4, Pseudomonas fluorescentes 10-1 y 10-2 y 2.10-3, bacterias y actinomycetes oligotróficos 10-1, 10-2, 10-3, 10-4 y 10-5, bacterias y actinomycetes celulolíticos 10-1, 10-2, 10-3 y 10-4y 10-5 y hongos 10-1, 10-2, 10-3 y 10-4. Para las bacterias copiotróficas se utilizó 10-4, 10-5, 10-6 y 10-7. En todos los casos, de cada una de las diluciones elegidas se analizaron 0,3 ml repartidos en 3 placas de Petri (de 9 cm de diámetro) a razón de 0,1 ml placa-1. En el caso de Pseudomonas fluorescentes se pipeteó 0,2 ml placa-1, y de igual modo se utilizaron 3 placas. Todo ello permite expresar el resultado del análisis de cada dilución como la media de 3 réplicas analíticas.
Al inicio del cultivo se realizó 2 repeticiones para el sustrato de T y 2 repeticiones para el sustrato de CC.
A los 2,5 meses de cultivo se determinó en el sustrato de FC la comunidad microbiana por la técnica de las suspensiones-diluciones en serie para la rizosfera y no rizosfera respectivamente. Se realizaron 3 repeticiones, contabilizándose 18 muestras para la rizosfera y 18 muestras para la no rizosfera.
La incubación de las placas se realizó en estufa a 25º C y en oscuridad, excepto las placas incubadas para el conteo de Pseudomonas fluorescentes que son expuestas a luz UV y 24º C. Los períodos de incubación fueron dos días para los Bacillus ssp. y para las Pseudomonas fluorescentes, una semana para los hongos y las bacterias copiotróficas y dos semanas para las bacterias y los actinomycetes oligotróficos y celulolíticos.
El conteo de las Pseudomonas fluorescentes se realizó observando las placas bajo luz UV para poder diferenciar las Pseudomonas fluorescentes de las que no lo son. Las bacterias copiotrofas se incubaron en agar nutritivo con 10 μg de benomilo (Energía e Industrias Aragonesas S.A., Madrid, España) por ml y 0,3 μl de Previcur (Propamocarb al 72.2%, Alcocer, España) por ml. Bacillus sp. también se incubaron en agar nutritivo después de que las suspensiones se calentaron 10 min a 80º C. Pseudomonas fluorescentes se incubaron bajo luz UV después de ser sembradas en agar King`s B (Cultimed, R. S. C., Montcada, Barcelona, España) con 10 μg de benomilo por ml, 0,3 μl de Previcur por ml, 50 μg de ampicilina (E. Merk, Darmstadt, Alemania) por ml y 12.5 μg de cloranfenicol (E. Merk, Darmstadt, Alemania) por ml. Bacterias y actinomycetes oligotrofos se incubaron en agar nutritivo concentrado al 0,01%, con 10 μg de benomilo por ml y 0,3 μl de Previcur por ml. Bacterias y actinomycetes celulolíticos se incubaron en agar celulosa consistente en 20 mg de polvo de fibra de celulosa (grado CF11; Whatman Internacional, Maidstone, Reino Unido) por ml; 1 mg de (NH4)2SO4 y CaCO3 por ml; 0,5 mg de MgSO4.7H2O, NaCl y K2HPO4 por ml; 10 μg de benomilo por ml; 0,3 μl de Previcur por ml y 15 mg de agar por ml. El conteo de hongos se hizo en PDA con 50 μg de oxytetracycline hydrochloride (Sigma Chemical Company, St Louis, Missouri) por ml y 1000 ppm de Tergitol-7 (Fluka Chemie, A.G.B. Buchs, Suiza).
La conductividad eléctrica (CE) y pH de los sustratos fue medido en extracto de agua (2:1; v:v), siguiendo el método descrito por Bunt (1988) y Gabriëls et al. (1991), respectivamente. Las variables químicas de los sustratos fueron determinadas al inicio del ensayo. Se tomaron 100 g de sustrato del que previamente habíamos determinado su peso seco y su densidad aparente, para así, calcular el volumen de sustrato. Conocido su volumen se agregó al sustrato dos veces su volumen en agua ultrapura desionizada y almacenamos a 25º C durante 6 h, para posteriormente determinar el pH (Ansorena, 1994). Para las medidas de pH y CE se realizaron dos repeticiones por sustrato al inicio del cultivo. Los valores de pH y CE pueden proporcionar una información importante sobre las características de los sustratos, e incluso revelar si existe o no alguna condición que favorezca o impida el desarrollo del hongo. La disponibilidad de nutrientes para la planta y para la comunidad microbiana está íntimamente ligada al pH.
La densidad aparente de los tres sustratos ensayados fue determinada al inicio del cultivo. Se realizaron dos repeticiones por sustrato. El valor obtenido para la T fue de 0,09 g ml-1 y de 0,277 g ml-1 para el CC, por último la FC presentó una densidad aparente de 0,16 g ml-1.
El diseño experimental fue de bloques totalmente al azar con 3 repeticiones. Cada repetición consistió en una línea de cultivo colgante de 6x0,10x0,10 m y un volumen de 10 L sustrato m-1 lineal. Cada línea contenía un total de 65 plantas de fresa (Fragaria x ananassa Duch.) de la variedad ‘Camarosa’. El material vegetal utilizado fue planta fresca con cepellón con tres o cuatro hojas verdaderas, obtenido mediante multiplicación en cultivo hidropónico y procedente de viveros de altura. El ensayo se realizó en un invernadero situado en Huelva, tipo túnel, de estructura metálica y cubierta ondulada de metacrilato, con 4,5 m de altura en cumbrera y 3,60 m en las bandas laterales. La ventilación practicada fue pasiva, a través de una cubierta abatible que permite una ventilación cenital y mecánica mediante extractores, contando además con un sistema de calefacción mediante aerotermos y de refrigeración por nebulización de agua (cooling system). El sistema de riego fue por goteros autocompensantes de 2,3 L h‑1 dispuestos a 0,30 m entre sí. Para el filtrado de los lixiviados se utilizó un filtro de arena que constaba de un metro de columna de agua sobre una capa de arena fina de un metro de espesor y que descansaba a su vez sobre dos capas de grava de 10 y 15 cm respectivamente.
Los análisis se realizaron al inicio y a los 2,5 meses de plantación. El análisis estadístico de los datos se ha realizado mediante análisis de la varianza y test de Tukey para separar las medias. Los datos fueron transformados para cumplir los requerimientos del ANOVA. Para ello se empleó el programa estadístico Statgraphics.
RESULTADOS
Se midieron las propiedades químicas de los sustratos al inicio del ensayo. Así, el sustrato de T presentó valores de CE significativamente inferiores a la FC y al sustrato de CC (Tabla 1). Sin embargo, el CC presentó valores de pH significativamente superiores a la FC y a la T (Tabla 1).
Tabla 1 - Propiedades químicas del sustrato evaluado al inicio del ensayo.
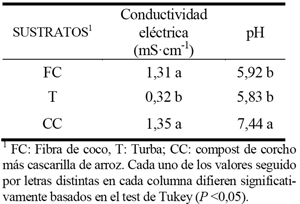
El sustrato de CC mostró una densidad de bacterias copiotrofas, Bacillus sp. y actinomycetes oligotrofos superior a la de la T, tanto al inicio del ensayo como a los 2,5 meses de cultivo (Tabla 2). La T mostró una densidad de hongos superior al CC, tanto al inicio del ensayo como a los 2,5 meses de cultivo (Tabla 2). En cambio, los actinomycetes celulolíticos y bacterias celulolíticas que inicialmente eran superiores en el CC que en la T, a los 2,5 meses de cultivo no mostraba población diferente en ambos, al contrario que las bacterias oligotrofas que inicialmente presentaban poblaciones iguales en ambos sustratos, y a los 2,5 meses de cultivo el CC presentó mayor población.
Tabla 2 - Densidades poblacionales de ciertos grupos de microorganismos de dos sustratos al inicio del ensayo y a los 2,5 meses de cultivo.
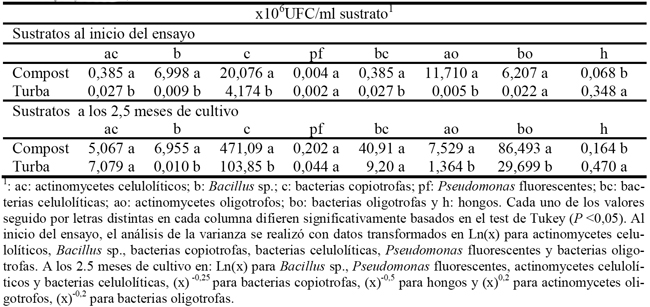
Detectamos una población de hongos totales en el CC menor que en la T (Tabla 2), lo que está en consonancia con un mejor comportamiento supresivo del compost (Tuitert et al., 1998).
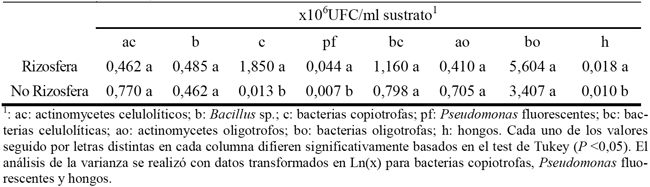
El sustrato de FC mostró a los 2,5 meses de cultivo mayor densidad de bacterias copiotrofas, Pseudomonas fluorescentes y hongos en la rizosfera que en la no rizosfera (Tabla 3).
Tabla 3 - Propiedades microbiológicas de la rizosfera y no rizosfera de la planta de fresa en sustrato de fibra de coco a los 2,5 meses de cultivo.
DISCUSIÓN
En numerosas ocasiones los compost de corcho se han relacionado con buenas características como sustratos hortícolas y han mostrado supresividad en ciertos patosistemas participados por hongos fitopatógenos de suelo (Avilés y Tello, 2001).
Las T, dado su pobreza en nutrientes y bajo pH, presentan generalmente escasa biomasa microbiana (Dickinson y Maggs, 1974; Kavanagh y Herlihy, 1975). Esto es corroborado por otros autores que indican que la reducida actividad biológica de las T se debe al elevado grado de estabilidad de éstas, especialmente las negras, constituidas por materiales orgánicos mucho más estabilizados que albergan menores poblaciones microbianas (Boehm et al., 1993).
La CE no es considerada un factor limitante de la supresividad en el CSS de fresa. La CE en este caso afectaría más a posibles desequilibrios nutricionales en el entorno radicular, los cuales podrían solventarse restableciendo el equilibrio nutricional en el entorno radicular. En este sentido, habrá que tener en cuenta la proporción entre iones en la solución nutritiva y la fracción de lavado. Ello unido a que el cultivo de fresa es reconocido como moderadamente sensible a la salinidad (0,5-1mS cm-1), podría originar niveles de salinidad en el sustrato capaces de crear estrés en la planta y reducir la producción en dichos sistemas. Esto es corroborado por otros autores que indican que los niveles de salinidad en el sustrato de FC reutilizado (segundo año de cultivo) son superiores respecto al sustrato nuevo (primer año de cultivo).
Según los resultados obtenidos se constata que el CC presentó valores de pH significativamente superiores a la FC y a la T. Esto podría ser favorable porque la asociación de altos valores de pH y/o la disponibilidad de Ca parece estar asociados con fenómenos de supresividad, hecho que ha sido constatado en plantas de fresa por otros autores (Jones et al., 1993).
Según otros autores las bacterias copiotrofas de la rizosfera y las Pseudomonas fluorescentes son antagonistas de Verticillium dahliae (Mercado-Blanco et al., 2004).
Otros autores indicaron que las altas poblaciones de bacterias copiotrofas y oligotrofas son propuestas como un indicador interesante en la supresión de enfermedades (Van Bruggen y Semenov, 1999; Kotsou et al., 2004).
Existen determinados microorganismos antagonistas que incrementan su población en suelos supresivos, y contribuyen al efecto supresivo del suelo. Entre estos microorganismos podemos citar los géneros fúngicos Trichoderma, Penicillium y Sporidesmium y las bacterias de los géneros Pseudomonas, Bacillus y Streptomyces (Agrios, 1997). Los Bacillus sp. son conocidos como antagonistas de Fusarium oxysporum. Parte del carácter supresivo del compost a este fitopatógeno puede ser debido a este microorganismo (Borrero et al., 2004).
Las poblaciones de actinomycetes y otras bacterias están favorecidas por un pH alto (Waksman, 1927). Muchos de estos microorganismos, al igual que los Bacillus sp. son antagonistas, ya que previenen la esporulación y el crecimiento vegetativo por compuestos tóxicos. Esto coincide con lo indicado por otros autores, que determinaron que los compost poseen efectos fungicidas. Estos compuestos fungitóxicos reducen la producción de esporangios y la liberación de zoosporas de Phytophthora sp. (Hoitink et al., 1977; Spencer y Benson, 1981, 1982).
Estos microorganismos también pueden competir por los nutrientes orgánicos e inorgánicos de la solución del suelo (Jones et al., 1993). Los efectos competitivos de bacterias, dependientes de un pH alto, se ha demostrado que se debe a una competición por nutrientes y en menor grado a la producción de antibióticos (Woltz y Jones, 1981).
Por tanto, las mayores cantidades de bacterias copiotrofas, Bacillus sp. y actinomycetes oligotrofos (Tabla 2) favorecido por el pH alto del CC (Tabla 1), podría explicar su mayor supresividad natural frente a la T como se describe en la literatura. Esto coincide con otros autores, que indicaron que la actividad microbiana, biomasa microbiana y el número total de actinomycetes a menudo han sido asociados con la supresión de enfermedades (Chen et al., 1988; Tuitert et al., 1998, Diab et al., 2003; Noble y Coventry, 2005; Pérez-Piqueres et al., 2006).
Esto podría justificarse con el mayor contenido de exudados radicales y depósitos que aportarían nutrientes a la microbiota (Ocamb y Kommedahl, 1994).
CONCLUSIONES
El elevado contenido de bacterias copiotrofas, Bacillus sp. y actinomycetes oligotrofos favorecido por el pH alto del CC, podría explicar su mayor supresividad natural frente a la T.
El sustrato de FC mostró a los 2,5 meses de cultivo mayor densidad de grupos de microorganismos cultivables asociados a fenómenos de biocontrol en la rizosfera que en la no rizosfera.
En general, el tipo de sustrato tiene un efecto notable sobre las características microbiológicas que rodean a la raíz de la planta fresa.
BIBLIOGRAFÍA
Abad, M. (1991) - Los sustratos hortícolas y las técnicas de cultivo sin suelo. In: Rallo, L. e Nuez, F. (Eds). La horticultura española en la C.E.. Córdoba, Sociedad Española de Ciencias Hortícolas, p. 271-280. [ Links ]
Agrios, N.G. (1997) - Plant pathology. 4th ed. San Diego, Academic Press, 635 p. [ Links ]
Ansonera, J. (1994) - Sustratos: propiedades y caracterización. Bilbao, España, Ediciones Mundi-Prensa, 172 p. [ Links ]
Avilés, M. y Tello, J.C. (2001) - El compostado de los residuos orgánicos. Su relación con las enfermedades de las plantas. In: Labrador, J. y Altieri, M.A. (Eds.) - Agroecología y Desarrollo. Madrid, Ed. Mundi-Prensa, p. 185-215. [ Links ]
Baker, K.F. yCook, R.J. (1974) - Biological control of plant pathogens. San Francisco, Freeman, 433 p. [ Links ]
Baker, R. y Chet, I. (1982) - Induction of suppressiveness. In: Schneider, R.W. (Ed.) - Suppressive Soils and Plant Disease. St. Paul, Minnesota, American Phytopathological Society Press, p. 35-50. [ Links ]
Becker, J.O. y Schwinn, F.J. (1993) - Control of soil-borne pathogens with living bacteria and fungi: status and outlook. Pest Management Science, 37: 355-363. [ Links ]
Boehm, M.J.; Madden, L.V. y Hoitink, H.A.J. (1993) - Effect of organic matter decomposition level on bacterial species diversity and composition in relationship to Pythium damping-off severity. Applied and Environmental Microbiology, 59: 4171-4179. [ Links ]
Boehm, M.J.; Wu, T.; Stone, A.G.; Kraakman, B.; Iannotti, D.A.; Wilson, G.E. Madden, L.V. yHotink, H.A.J. (1997) - Cross-polarized magic-angle spinning 13C nuclear magnetic resonance spectroscopic characterization of soil organic matter relative to culturable bacterial species composition and sustained biological control of Pythium root rot. Applied and Environmental Microbiology, 63: 162-168. [ Links ]
Borrero, C.; Trillas, M.I.; Ordovás, J.; Tello, J.C. y Avilés, M. (2004) - Predictive factors for the suppression of fusarium wilt of tomato in plant growth media. Phytopathology, 94: 1094-1101. [ Links ]
Bunt, A.C. (1988) - Media and mixes for container-grown plants: A manual on the preparation and use of growing media for pot plants. 2nd ed. London, Academic Division of Unwin Hyman Ltd, 309 p. [ Links ]
Cambell, R. (1994) - Biological control of soil-borne diseases: some present problems and different approaches. Crop protection, 13: 4-13. [ Links ]
Chen, W.; Hoitink, H.A.J.; Schmitthenner, A.F. y Tuovinen, O.H. (1988) - The role of microbial activity in suppression of damping-off caused by Pythium ultimum. Phytopathology 78: 314-322. [ Links ]
Cook, R.J. y Baker, K.F. (1983). The nature and practice of biological control of plant pathogens. St. Paul, Minnesota, American Phytopathological Society Press, 539 p. [ Links ]
Diab, H.G.; Hu, S. y Benson, D.M. (2003) - Suppression of Rhizoctonia solani on impatiens by enhanced microbial activity in composted swine waste-amended potting mixes. Phytopathology, 93: 1115-1123. [ Links ]
Dickinson, C.H. y Maggs, G.H. (1974) - Aspects of decomposition of Sphagnum leaves in an ombrophilous mire. New Phytologist, 73: 1249-1257. [ Links ]
Gabriëls, R.; Van Keirsbulck, W. y Verdonck, O. (1991) - Reference method for physical and chemical characterization of growing media: an international comparative study. Acta Horticulturae, 294: 147-160. [ Links ]
Garibaldi, A. (1983) - The use of suppressive soils as substrate for ornamental and flowering plants. Acta Horticulturae, 150: 103-111. [ Links ]
Hoitink, H.A.J.; Vandoren, D.M.J. y Schmitthenner, A.F. (1977) - Suppression of Phytophthora cinnamomi in a composted hardwood bark potting medium. Phytopathology, 67: 561-565. [ Links ]
Hoitink, H.A.J.; Inbar, Y. y Boehm, M.J. (1991) - Status of compost-amended potting mixes naturally suppressive to soilborne diseases of floricultural crops. Plant Disease, 75: 869-873. [ Links ]
Hoitink, H.A.J.; Boehm, M.J. y Hadar, Y. (1993) - Mechanisms of suppression of soilborne plant pathogens in compost-amended sustrates. In: Hoitink, H.A.J. y Keener, H.M. (Eds.) - Science and engineering of composting: desing, environmental, microbiological and utilization aspects. Worthington, Ohio, Renaissance Publications, p. 601-621. [ Links ]
Hoitink H.A.J.; Madden, L.V. y Boehm, M.J. (1996) - Relationships among organic matter decomposition level, microbial species diversity and soilborne disease severity. In: Hall, R. (Ed.) - Principles and practice of managing soilborne plant pathogens. St. Paul, Minnesota, American Phytopathological Society Press, p. 237-249. [ Links ]
Huber, D.M. y Schneider, R.W. (1982) - The description and occurrence of suppressive soils. In: Schneider, R.W. (Ed.) - Suppressive soil and plant disease. St. Paul, Minnesota, American Phytopathological Society Press, p. 1-7. [ Links ]
Jones, J.P.; Engelhard, A.W. y Woltz, S.S. (1993) - Management of Fusarium wilt of vegetables and ornamentals by macro and microelement nutrition. In: Engellhard, W.A. (Ed.) - Soilborne plant pathogens: Management of diseases with macro-and microelements. St. Paul, Minnesota, American Phytopathological Society Press, p. 18-32. [ Links ]
Lewis, J.A. y Papavizas, G.C. (1991) - Biocontrol of plant disease: the approach of tomorrow. Crop Protection, 10: 95-105. [ Links ]
Kavanagh, T. y Herlihy, M. (1975) - Microbiological aspects. In: Robinson, D.W. y Lamb, J.G.D. (Eds.) - Peat in horticulture. New York, Academic Press Inc., p. 39-40. [ Links ]
Kotsou, M.; Mari, I.; Lasaridi, K.; Chatzipavlidis, I.; Balis, C. y Kyriacou, A. (2004) - The effect of olive oil mill wastewater (OMW) on soil microbial communities and suppressiveness against Rhizoctonia solani. Applied Soil Ecology, 26: 113-121. [ Links ]
Marfá, O. (2000) - La recirculación en los cultivos sin suelo. Elementos básicos. In: Marfá, O. (Ed.) - Recirculación en cultivos sin suelo. Reus, Ediciones de Horticultura, p. 21-27. (Compendios de Horticultura 14). [ Links ]
Mercado-Blanco, J.; Rodríguez Jurado, D.; Hervás, A. y Jiménez Díaz, R.M. (2004) - Suppression of Verticillium wilt in olive planing stocks by root-associated fluorescent Pseudomonas sp.. Biological Control, 30: 474-486. [ Links ]
Noble, R. y Coventry, E. (2005) - Suppression of soil-borne plant diseases with compost: a review. Biocontrol Science and Technology, 15: 3-20. [ Links ]
Ocamb, C.M. y Kommedahl, T. (1994) - Growth of rhizosphere competent and incompetent Fusarium species from corn on carbon substrates. Phytopathology, 84: 508-514. [ Links ]
Pérez-Piqueres, A.; Edel-Hermann, V.; Alabouvette, C. y Steinberg, C. (2006) - Response of soil microbial communities to compost amendments. Soil Biology and Biochemistry, 31: 1363-1374. [ Links ]
Raviv, M.; Chen, Y. y Inbar, Y. (1986) - Peat and peat substitutes as growth media for container-grown plant. In: Chen, Y. e Avnimelech, Y. (Eds.) - The role of organic matter in modern agriculture. Dordrecht, Martinus Njhoff Publishers, p. 257-287. [ Links ]
Schroth, M.N. y Hancock, J.G. (1981) - Selected topic in biological control. Annual Review of Microbiology, 35: 453-476. [ Links ]
Spencer, S. y Benson, D.M. (1981) - Root rot of Aucuba japonica caused by Phytophthora cinnamomi and P. citricola and suppressed with bark media. Plant Disease, 65: 918-921. [ Links ]
Spencer, S. y Benson, D.M. (1982) - Pine bark, hardwood bark compost, and peat amendment effects on development of Phytophthora sp. and lupine root rot. Phytopathology, 72: 346-351. [ Links ]
Tuitert, G.; Szczech, M. y Bollen, G. J. (1998) - Suppression of Rhizoctonia solani in potting mixtures amended with compost made from organic household waste. Phytopathology, 88: 764-773. [ Links ]
Van Bruggen, A.H.C. y Semenov, A.M. (1999) - A new approach to the search for indicators of root disease suppression. Australasian Plant Pathology, 28: 4-10. [ Links ]
Waksman, S.A. (1927) - Principles of Soil Microbiology. Baltimore, MD, The Williams e Wilkins Co., 897 p. [ Links ]
Woltz, S.S. y Jones, J.P. (1981) - Nutritional requirements of Fusarium oxysporum: Basis for a disease control system. In: Nelson, P.E.; Toussoun, T.A. y Cook, R.J. (Eds.) - Fusarium: Diseases, Biology, and Taxonomy. Pennsylvania, The Pennsylvania State University Press, p. 340-349. [ Links ]














