Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Revista de Ciências Agrárias
versão impressa ISSN 0871-018X
Rev. de Ciências Agrárias vol.42 no.3 Lisboa set. 2019
https://doi.org/10.19084/rca.15278
ARTIGO
Método da hidrólise ácida na disponibilidade de nitrogênio em resíduos orgânicos
Acid hydrolysis method on the availability of nitrogen in organic wastes
Ruan Carnier1,#, Ronaldo S. Berton1, Aline R. Coscione1,*, Adriana M. M. Pires2 e Jessica Z. F. Corbo1
1 Instituto Agronômico (IAC) – Centro de qualidade e poluição do Solo – Campinas, SP – Brasil
2 Empresa brasileira de Pesquisa Agropecuária (EMBRAPA) – Departamento de Meio Ambiente – Jaguariuna, SP – Brasil
(*E-mail: aline@iac.sp.gov.br)
RESUMO
A estimativa do nitrogênio (N) disponibilizado para as plantas, oriundo de resíduos orgânicos, é usualmente mensurada com base em experimentos em casa de vegetação ou incubação aeróbia. Esses métodos são trabalhosos, de custo elevado e pouco práticos para rotinas de laboratório, exigindo abordagens alternativas. Partindo da hipótese de relação positiva entre frações orgânicas e N disponível, este trabalho teve como objetivo avaliar a qualidade do fracionamento químico do N, por meio do método da hidrólise ácida, em dez resíduos orgânicos. A hidrólise ácida fracionou a matéria orgânica dos resíduos em compartimentos lábeis e recalcitrante de N, os quais foram comparados à quantidade de N absorvida pelas plantas obtida pelo índice de recuperação de nitrogênio (IRN). Relações significativas foram observadas entre a frações lábil 1 (R² = 0,86; p=0,008) e lábil total (R² = 0,89; p=0,004) e os valores de IRN para os resíduos película de café, estercos de frango e bovino, pó de café, turfa e cama de frango.
Palavras-chave: método alternativo, fracionamento químico, absorção de nitrogênio
ABSTRACT
The nitrogen (N) available for plants from organic residues is usually estimated by greenhouse or aerobic incubation experiments. These methods are laborious, expensive and impracticable for laboratory routines, requiring alternative approaches. Following the hypothesis of positive relation between organic fractions and available N, the aim of this work was to evaluate the acid hydrolysis as an alternative method in comparison to the N absorbed by maize on a greenhouse experiment for 10 organic wastes. The acid hydrolysis fractionated the N of the wastes’ organic matter in labile and recalcitrant pools, which was compared to the amount of N absorbed by the plants measured by nitrogen recuperation index (NRI). There was a significant relationship between the labile pool 1 (R² = 0,86; p=0,008) and total labile pool (R² = 0,89; p=0,004) and the NRI values for the coffee silverskin, chicken and cattle manure, expired coffee powder, peat and poultry litter wastes.
Keywords: alternative method, chemical fractionation, nitrogen absorption
INTRODUÇÃO
O nitrogênio (N) pode ser considerado o nutriente mais importante devido à sua alta exigência pelas culturas (Fageria, 2009), de modo que sua aplicação e manutenção no solo é fundamental, principalmente nos solos tropicais altamente intemperizados. Dentre as adubações nitrogenadas, a ureia é o fertilizante mais utilizado no Brasil devido as suas vantagens comparativas em termos de oferta, facilidade de fabricação e custo final para o agricultor (Filho et al., 2010). Além da ureia, outros fertilizantes comumente utilizados são o nitrato de amônio e o sulfato de amônio (Cantarella, 2007). No entanto, mais de 80% dos fertilizantes nitrogenados consumidos no Brasil são importados (ANDA, 2017). Diante da forte dependência na importação desse nutriente na forma dos fertilizantes minerais, dos efeitos adversos por eles causados ao meio ambiente e da baixa eficiência do uso desse insumo, em que apenas 50% do total de N aplicado é aproveitado pelas plantas (Cantarella, 2007), pesquisas sobre o uso agrícola de resíduos orgânicos na agricultura geram interesse econômico e ambiental (Maluf et al., 2015; Pintado e Teixeira, 2015).
A adubação de origem orgânica com fonte de N deve ocorrer de forma criteriosa a fim de aumentar a eficiência do uso de N e evitar contaminação ambiental (Azeez e Averbeke, 2010). Existem diversas fontes utilizadas na adubação orgânica, como: lodo de esgoto, esterco de animais, resíduos vegetais, agroindustriais, entre outros (Yazid et al., 2017). Apesar da matriz orgânica variar entre os resíduos orgânicos, a característica comum é o predomínio do N orgânico em que, tal como no solo, cerca de 95 % do N se apresenta nesta forma (Togoro, 2016). Deste modo, somente após a ocorrência de processos de oxidação biológica, em que estas formas são transformadas (mineralizadas) em formas inorgânicas ou minerais, é que o azoto se encontra disponível para as plantas. Os métodos empregados para estimar o N disponibilizado para as plantas a partir de fertilizantes orgânicos ou resíduos aplicados ao solo mensuram o N potencialmente mineralizável por meio de experimentos em casa de vegetação ou métodos clássicos de incubação aeróbia (CETESB, 1999). Porém, estes métodos são trabalhosos e de custo elevado, geralmente de longa duração, de menor exequibilidade e pouco práticos para rotina de laboratório (Bergamasco, 2015).
Apesar do número crescente de estudos sobre métodos alternativos para estimativa do N, a maior parte das pesquisas são aplicadas a solos, sendo escassas as avaliações em resíduos orgânicos. Partindo da hipótese de que a composição da matéria orgânica do solo possui os mesmos compartimentos que os fertilizantes orgânicos ou resíduos que possam ser empregados com esta finalidade, alguns trabalhos vêm sendo desenvolvidos tendo como objetivo métodos alternativos para a estimativa do N disponível (Kuhnen, 2013; Pires et al., 2015, Mariano et al., 2017).
Rovira e Vallejo (2002) visando conhecer a recalcitrância da matéria orgânica do solo, estudaram a decomposição de resíduos vegetais incubados com solo, empregando o método da hidrólise ácida para caracterizar frações lábeis e recalcitrante. O método da hidrolise ácida consiste em um fracionamento químico para obtenção do N em frações por meio de extrações alcalinas e ácidas, caracterizando-as de acordo com o seu grau de humificação.
Considerando a importância em avaliar métodos alternativos para estimativa do N disponível em resíduos orgânicos e partindo da hipótese de relação positiva entre frações orgânicas e N disponível, este trabalho teve como objetivo avaliar a qualidade do fracionamento químico do N em resíduos orgânicos em termos do N disponibilizado para as plantas, obtido de ensaio em casa de vegetação.
MATERIAL E MÉTODOS
Foram realizados dois experimentos neste trabalho. O primeiro experimento realizado em laboratório, corresponde ao fracionamento do nitrogênio dos resíduos orgânicos estudados, pelo método da hidrólise acida. O segundo experimento tem por base um ensaio em casa de vegetação, cujas etapas estão descritas a seguir.
Ensaio de hidrólise ácida
Inicialmente selecionou-se dez resíduos orgânicos de origem diversificada visando heterogeneidade entre eles. Os resíduos orgânicos avaliados foram: lodo de esgoto seco termicamente, esterco de poedeira, esterco de frango, cama de frango, esterco bovino, torta de mamona, turfa, película de café, pó de café vencido e torta de filtro de usina de cana-de-açúcar. O lodo de esgoto seco termicamente é originário do tratamento do esgoto doméstico em lagoas aeradas. O esterco de poedeira é proveniente de galinhas confinadas em gaiolas para produção de ovos enquanto o esterco de frango é proveniente de aves confinadas para o abate e produção de carne. A cama de frango é composta por material vegetal (resto de culturas agrícolas) e recebe excretas, penas e outros resíduos gerados na respetiva criação. O esterco bovino é originário de animais criados em confinamento ou sob pastagem (não especificado). A torta de mamona é um subproduto do processo de descascamento e extração do óleo da mamona (Ricinus communis L.). A turfa é oriunda da decomposição de musgos, restos de árvores, plantas, etc., encontrada geralmente em regiões pantanosas. A película de café é um resíduo proveniente do beneficiamento do grão de café durante o processo de torrefação. O pó de café vencido é um produto fora das especificações de validade obtido em local de descarte. A torta de filtro de cana de açúcar é um material residual, obtido em filtros rotativos durante a produção do açúcar. Todos os resíduos orgânicos utilizados neste trabalho foram coletados no estado São Paulo – Brasil.
Os resíduos foram previamente secos ao ar, passados em peneira de malha 2 mm de abertura, homogeneizados e encaminhados para caracterização química. As análises, realizadas em triplicata, foram: umidade a 65 °C, nitrogênio total pelo método de Kjeldahl (NKj) (APHA, 2017) e nitrogênio inorgânico na forma amoniacal e nítrica (Mulvaney, 1996), ambos pelo método de destilação por arraste a vapor. O carbono orgânico total (COT) foi extraído por digestão com dicromato em bloco digestor e determinação por titulometria, como descrito por Nelson e Summers (1996). O pH foi determinado em água de acordo com a metodologia descrita por EPA (1995), na relação 1: 10 (resíduo: água). O nitrogênio inorgânico determinado por este método corresponde às formas solúveis de nitrogênio presente nas amostras, sendo extraído das amostras orgânicas com solução de KCl 1 mol/L, por agitação, durante 1 hora. Na primeira etapa determina-se o nitrogênio amoniacal, sendo que ao extrato é adicionada uma pequena quantidade de óxido de magnésio, seguindo-se de destilação a vapor. O destilado é recebido em solução de ácido bórico, contendo uma mistura de indicadores vermelho de metila e azul de bromocresol, seguindo-se da titulação com ácido sulfúrico padronizado. Para determinação de nitrato e nitrito (conjuntamente), ao mesmo tubo já destilado adiciona-se liga de Devarda (0% de Cu, 45% de Al e 5% de Zn), seguindo-se de nova destilação e titulação da mesma forma que para o N-amoniacal. Os valores dos parâmetros analisados para os resíduos em estudo são apresentados no quadro 1.
O método escolhido para avaliar os compartimentos de nitrogênio (lábeis e recalcitrante) foi baseado no descrito por Rovira e Vallejo (2002). No método original, são utilizadas amostras de solo e as frações lábeis são determinadas em analisador elementar CNS. Neste trabalho, o N presente nas frações lábil 1 e lábil 2 foi obtido por destilação a vapor na presença de óxido de magnésio e liga de Devarda adicionados de uma só vez ao extrato, segundo rotina similar ao descrito detalhadamente acima. As restantes etapas ocorreram de acordo com o procedimento original. Assim, para cada resíduo estudado, em triplicata, 1 g de cada resíduo foi pesado e colocado, individualmente, em tubos de Falcon de 50 ml. Um tratamento controlo, sem adição de resíduo, foi igualmente considerado. Na primeira hidrólise, para cada tubo, foram adicionados 20 mL de H2SO4 2,5 mol/L. Os tubos foram tapados e aquecidos em banho maria a aproximadamente 100 °C, por 30 minutos, sem agitação. Após esfriamento, à temperatura ambiente, os tubos foram centrifugados a 3000 rpm por 5 minutos e o sobrenadante separado. Ao resíduo sólido precipitado foram adicionados 20 ml de água deionizada seguida de uma nova centrifugação sendo o sobrenadante separado e adicionado ao primeiro sobrenadante, sendo a respetiva mistura designada de compartimento lábil 1. O resíduo precipitado foi seco a 60 °C e adicionados 2 ml de H2SO4 13 mol/L a cada tubo seguido de agitação, em agitador de bancada horizontal, a 170 rpm, durante um período de 12 horas. Após a agitação, água deionizada foi adicionada de modo a obter uma concentração de ácido equivalente a 1 mol/L seguida de aquecimento em banho maria a aproximadamente 100 °C, durante um período de 3 horas, com agitação esporádica. Em seguida foram centrifugados e separados como descrito anteriormente. O sobrenadante, resultante desta segunda hidrólise, foi denominado compartimento lábil 2 e o resíduo sólido restante foi seco a 60 °C e caracterizado como fração recalcitrante.
A fração recalcitrante de cada resíduo foi moída e passada em peneira ABNT 150, com abertura de malha de 0,02 mm. Posteriormente, foram determinados os teores de N total, por combustão seca, em analisador elementar LECO TruSPEC CN.
Ensaio em casa de vegetação
Para avaliação da eficiência da hidrólise ácida na disponibilidade de N nos resíduos orgânicos foi obtido um índice de recuperação de nitrogênio (IRN) por meio de ensaio um ensaio em casa de vegetação para base de comparação.
No experimento em casa de vegetação foram utilizados vasos com capacidade para 2 kg de solo e a cultura do milho como planta teste. O solo utilizado, um Latossolo Vermelho distrófico argilo-arenoso, foi seco ao ar e peneirado em malha de 2 mm (TFSA), para posterior caracterização química como descrito em Raij et al. (2001). As características principais obtidas foram: pH (CaCl2) 4,1; 27 g/dm3 de MO; 1,4 g/kg de N total; 54 mmolc/dm3 para CTC; 19% de V. A análise granulométrica foi realizada de acordo com Camargo et al. (1986) e permitiu classificar o solo como de textura média, sendo 557, 73 e 370 g/kg de areia, silte e argila, respectivamente, tendo em sua composição fração argila 1:1. Cerca de 2,7 g de calcário Dolomitico por vaso foram adicionados e deixados a incubar durante 10 dias, para elevar o grau de saturação de bases para valores de 70%. Foi, também, incluído para comparação um padrão mineral, nitrato de amônio (NH4NO3), na forma de um tratamento adicional além do tratamento sem adição de N (controle). Em todos os tratamentos com adição de N foram aplicados em quantidades equivalentes a 140 kg de N total/ha (correspondente a 450 mg de N/vaso). Para cada tratamento foram incluídas três repetições em blocos casualmente distribuídos. Todos os tratamentos foram deixados a incubar durante um período de 15 dias, após o qual uma adubação básica contendo 0,45; 0,4 e 0,17 g de K, P e S respectivamente na forma de sais e micronutrientes (2,0 µg de B; 6,3 µg de Cu; 0,1 µg de Mn; 12, 82 µg de Zn; 0,18 µg de Mo e 1 ,24 µg de Fe) por meio de solução. Posteriormente, procedeu-se o plantio da planta teste (milho, cultivar AG8676PR02), com uma densidade de 10 sementes de milho por vaso com espaçamento e profundidade de aproximadamente 2 cm. Após a germinação, foram deixadas 5 plantas de milho por vaso, distribuídas de maneira uniforme. No tratamento com adição do padrão mineral (nitrato de amônio), procedeu-se o fracionamento, com o objetivo de evitar efeitos de toxicidade por excesso de N. As aplicações foram feitas nos períodos de 3, 8, 13 e 20 dias após a germinação. Ao fim do período de 35 dias de cultivo realizou-se o corte da parte aérea, sendo o respectivo material vegetal em cada tratamento pesado, lavado para efeitos de análise. As amostras de parte aérea foram moídas e passadas em peneira de 2 mm de abertura para análise de NKj pelo método de destilação por arraste a vapor (Cantarela e Trivelin, 2001). A quantidade acumulada de N na parte aérea foi calculada com base na equação 1:

Em que Qa é a = quantidade acumulada de N na parte aérea por vaso (mg/vaso), ms a = massa seca (g) e C a = concentração de N na parte aérea (g/kg).
O Índice de recuperação de nitrogênio (IRN) foi calculado pela equação 2:

Em que IRN (%) é o = índice de eficiência agronômica, Q0 a = quantidade de N acumulada por vaso no tratamento controle (mg/vaso), Q1 a = quantidade de N acumulada por vaso tratados com as fontes de N (mg/vaso) e Q aplicado a = dose de N aplicada (450 mg de N/vaso).
Os dados obtidos na hidrólise ácida e no experimento em casa de vegetação foram submetidos a uma análise de variância e respectivo teste de comparação de médias, pelo método de Tukey (p ≤ 0,05). Os compartimentos lábeis 1, 2 e total (lábil 1 + lábil 2), obtidos na hidrólise ácida, foram relacionados (p ≤ 0,05) com os IRN’s obtidos no experimento em vaso por meio de regressão linear simples.
RESULTADOS E DISCUSSÃO
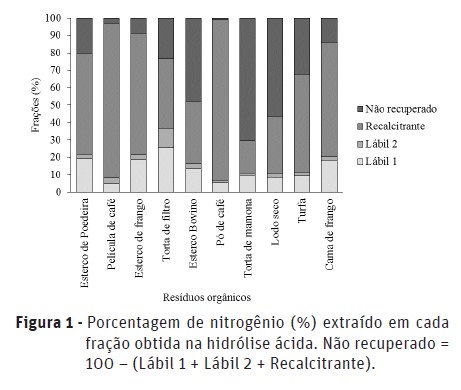
O fracionamento químico dos resíduos por hidrólise ácida é ilustrado na Figura 1. Com exceção do esterco bovino, a torta de mamona e o lodo seco, os restantes resíduos possuem uma maior concentração de N na fração recalcitrante, com os resíduos película e pó de café a revelarem maior porcentagem (88,8 e 92,2 %, respectivamente). A elevada recalcitrância desses resíduos está provavelmente relacionada com as suas características como verificado por Sánchez e Anzola (2012). Esses autores caracterizaram a película de café em duas variedades de café e encontraram elevado teor de N total, porém apenas uma pequena porcentagem do N era proteíco, caraterizado por uma maior labilidade (Canellas et al., 2001).
Em relação às frações lábeis, a fração lábil 1 representou um reservatório maior de N do que a fração lábil 2 em todos os resíduos. Na fração lábil 1 estão presentes os teores de nitrogênio solúvel, nas suas formas amoniacal ou nítrica (nitrato + nitrito). Dentre os dez resíduos estudados, aqueles que apresentaram maiores teores de nitrogênio solúvel durante a caracterização foram o lodo, a cama de frango e o esterco de poedeira, sendo que somente para este último, sua contribuição foi significativa em relação a concentração de N-Kjeldahl do resíduo, na ordem de 36% (Quadro 1).
A torta de filtro foi o resíduo que apresentou maior teor de N nas frações lábeis em relação aos outros resíduos, representando um valor próximo a 40% do total extraído na hidrólise ácida. Esse maior valor de N lábil pode ser explicado devido ao possível predomínio do N na forma de proteínas neste resíduo (Nardin, 2007), que são compostos menos recalcitrantes (Canellas et al., 2001) e, portanto, mais fáceis de serem hidrolisados.
Conforme mostrado na Figura 1, a extração do N por meio das frações lábeis e recalcitrante da hidrólise ácida não atingiu 100% do teor de N obtido pelo método de Kjeldahl contido no resíduo. Isso foi verificado principalmente para a torta de mamona e o lodo seco. Uma das prováveis fontes de erro está na determinação de N extraído das frações lábeis, que considerou que o material em solução após o fracionamento químico estaria presente somente nas formas nítrica e amoniacal. Dessa maneira, as formas orgânicas de N solúveis em ácido presentes nas frações lábeis, principalmente aminoácidos, tipicamente oriundos de hidrolise parcial de formas proteicas, provavelmente não foram recuperadas durante a destilação (Alfaia, 2006).
Para a película e o pó de café foram verificadas as maiores porcentagens de recuperação pelo método da hidrólise ácida, 97,1 e 99,1%, respectivamente. Isso é explicado pela principal presença de compostos orgânicos não proteicos (Alfaia, 2006; Sánchez e Anzola, 2012), que não foram hidrolisados pelo ácido sulfúrico e, consequentemente, incluídos na fração recalcitrante. A concentração de N resistente à hidrólise, determinada como fração recalcitrante, foi verificada por Rovira e Vallejo (2000) como um preditor eficiente da mineralização e, portanto, está diretamente relacionado com a disponibilização para as plantas.
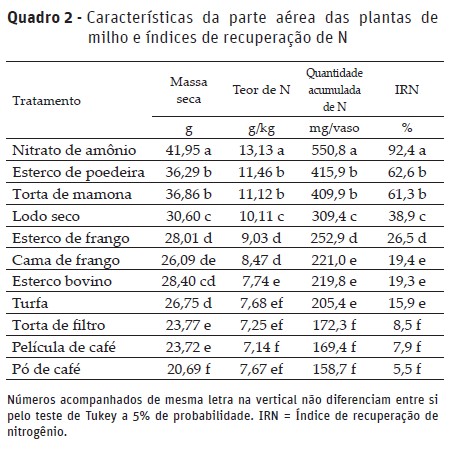
A disponibilização de N às plantas via IRN obtidos no experimento em casa de vegetação pode ser observada no Quadro 2. Para todos os parâmetros avaliados, os maiores valores foram obtidos para o tratamento com nitrato de amônio. Estes resultados são explicados pelo fato de todo N presente neste material estar sob formas minerais e, portanto, disponível para absorção das plantas, ao contrário dos resíduos orgânicos, os quais têm de ser oxidados através de processos biológicos (mineralização) para posterior absorção pelas plantas.
Entre os resíduos, os maiores valores encontrados para os parâmetros avaliados no experimento em casa de vegetação foram observados para o esterco de poedeira e torta de mamona, não havendo diferenças significativas entre eles, resultando em IRN’s de 62,6 e 61,3%, respectivamente, seguido pelo lodo seco com 38,9%. Os IRN’s obtidos para estes resíduos foram bastante superiores às quantidades de N extraídas nas frações lábeis por meio da hidrólise ácida. Esses dados indicam que, apesar destes resíduos possuírem relações C/N inferiores a 10, faixa em que se espera maior estabilização do material, esta isoladamente não foi suficiente para inferir a capacidade de degradação dos microrganismos (Cuttle et al., 2003; Leal et al., 2010). Para o esterco de poedeira, isso pode ser atribuído à elevada presença de nitrogênio inorgânico, correspondente a formas solúveis e prontamente disponíveis (cerca de 36% do N-Kj da composição do resíduo). Altos índices de recuperação de N foram também verificados por Figueroa (2008) em trabalho com trigo e milho, após a mineralização do N orgânico presente em esterco de poedeira.
Para a torta de mamona e para o lodo seco evidencia-se a presença de material mineralizável, não contabilizado com sucesso no fracionamento químico da hidrolise ácida. Bataglia et al. (1983), em estudo de resíduos orgânicos como fontes de nitrogênio para capim braquiária, observaram recuperação de N para a torta de mamona de 56,3%, valor próximo ao encontrado neste trabalho. Nesse mesmo trabalho os autores encontraram ainda uma eficiência de 20,1% para o lodo de esgoto, próximo da metade da eficiência encontrada neste presente trabalho para esse resíduo. Já Chiaradia et al. (2009), verificaram uma eficiência agronômica de 85% para o lodo de esgoto em área cultivada com mamona. Mesmo sendo lodos oriundos de tratamento aeróbio, com características semelhantes, verifica-se grande variabilidade entre a disponibilidade de N para as plantas.
Os menores valores de massa seca, teor de N e quantidade acumulada de N foram verificados para os resíduos película e pó de café e em consequência disso estes resíduos apresentaram, igualmente, menores valores de IRN (7,9 e 5,5% respectivamente), não havendo diferença significativa entre eles. Apesar da relação C/N desses materiais favorecerem a mineralização e disponibilização de N, estes resultados não foram observados. Esses dados dos resíduos da indústria do café estão de acordo com os dados apresentados anteriormente, em que a elevada recalcitrância e a provável presença de substâncias com propriedades alelopáticas e antimicrobianas como o tanino (Scalbert, 1991), possivelmente interferiram na degradação desses resíduos e, consequentemente, na disponibilidade de N. Efeitos alelopáticos foram observados por Chandra et al. (2013) na germinação de grão-de-bico (Cicer arietinum) e trigo (Triticum aestivum) em contato com extratos de grão de café, corroborando para os resultados obtidos neste trabalho.
As relações entre as frações da hidrólise e os IRN’s são ilustradas na Figura 2. Não houve regressão significativa para o conjunto total dos 10 resíduos (A, B e C). No entanto, ao retirar-se os resíduos esterco de poedeira, a torta de filtro, a torta de mamona e o lodo seco, verificou-se regressão significativa para a fração lábil 1 e lábil total (D e F), com valores de R2 de 0,86 e 0,89 respectivamente. Isso indica que durante a degradação dos resíduos orgânicos no solo, além dos compostos lábeis contendo N, os microrganismos são capazes de decompor compartimentos de N mais estáveis, que posteriormente serão absorvidos pelas plantas.
Com exceção da torta de filtro, para os outros três resíduos citados acima, os valores de IRN foram maiores do que os valores da fração lábil total, como já discutido anteriormente. De maneira contrária, para a torta de filtro encontrou-se maior porcentagem de N na fração lábil total, extraída pela hidrólise ácida, do que no experimento em casa de vegetação por meio do índice de eficiência. Esses resultados podem ser explicados pela alta relação C/N de 44, que favorece a imobilização de N, e pelos teores baixos de nitrogênio inorgânicos presentes nesse resíduo. O potencial de imobilização de N para a torta de filtro foi também verificado por Chacón et al. (2011) em trabalho de decomposição de fontes orgânicas. A associação desses fatores terá contribuído para a falta de relação entre os métodos avaliados para esses resíduos citados.
CONCLUSÕES
1-O fracionamento químico de N pelo método da hidrólise ácida foi eficiente na estimativa do N disponível às plantas para seis dos dez resíduos orgânicos estudados, sendo rápido e economicamente viável.
2-A rotina para determinação do nitrogênio presente nas frações lábeis deve considerar a presença de formas orgânicas parcialmente hidrolisadas e não somente as inorgânicas decorrentes da hidrolise completa.
3-O fracionamento químico de N pelo método da hidrólise ácida pode ser considerado promissor, mas um número maior de resíduos deve ser estudado para validação do método proposto
Referências bibliográficas
Alfaia, S.S. (2006) - Caracterização e distribuição das formas do nitrogênio orgânico em três solos da Amazônia central. Acta Amazonica, vol. 36, n. 2, p. 135-140. http://dx.doi.org/10.1590/S0044-59672006000200001 [ Links ]
APHA (2017) - Standard Methods for the Examination of Water and Wastewater, 23rd Edn. Washington, DC: American Public Health Association. [ Links ]
ANDA (2017) - Principais Indicadores Do Setor De Fertilizante. <http://anda.org.br/index.php?mpg=03.00.00> [ Links ].
Azeez, J.O. & Averbeke, W. van (2010) - Nitrogen mineralization potential of three animal manures applied on Sandy clay loam soil. Bioresource Technology, vol. 101, n. 14, p. 5645-5651. http://dx.doi.org/10.1016/j.biortech.2010.01.119 [ Links ]
Bataglia, O.C.; Berton, R.S.; Camargo, O.A. & Valadares, J.M.A.S. (1983) - Resíduos orgânicos como fontes de nitrogênio para capim-braquiária. Revista Brasileira de Ciência do Solo, vol. 7, p. 277-284. [ Links ]
Bergamasco, M.A.M. (2015) - Formas de N-orgânico em Latossolo em função de nitrogênio e de plantas de cobertura pré-safra do milho. Dissertação de Mestrado, Jaboticabal, Faculdade de Ciências Agrárias e Veterinárias – UNESP. 55p
Camargo, O.A.; Moniz, A.C.; Jorge, J.A. & Valadares, J.M.A.S. (1986) - Métodos de análise química, mineralógica e física de solos do Instituto Agronômico de Campinas. Boletim Técnico 106, Campinas: Instituto Agronômico, 94p. [ Links ]
Canellas, L.P.; Santos, G.A.; Rumjanek, V.M.; Moraes, A.A. & Guridi, F. (2001) - Distribuição da matéria orgânica e características de ácidos húmicos em solos com adição de resíduos de origem urbana. Revista Agropecuária Brasileira, vol. 36, n. 12, p. 1529-1538. http://dx.doi.org/10.1590/S0100-204X2001001200010 [ Links ]
Cantarella, H. & Trivelin, P.C.O. (2001) - Determinação de nitrogênio inorgânico em solo pelo método da destilação a vapor. In: Raij, B. van; Andrade, J.C.; Cantarella, H. & Quaggio, J.A. (Eds.) - Análise química para avaliação da fertilidade de solos tropicais. Instituto Agronômico, Campinas, Brasil, p. 270-276. [ Links ]
Cantarella, H. (2007) - Nitrogênio. In: Novais, R.F.; Alvarez, V.H.V.; Barros, N.F.; Fontes, R.L.F.; Centarutti, R.B. & Neves, J.C.L. (Eds.) - Fertilidade do solo. Viçosa, Minas Gerais, p. 375-470. [ Links ]
CETESB (1999) - Aplicação de lodos sistemas de tratamento biológico em áreas agrícolas - critérios para projeto e operação: manual técnico. Norma técnica P.4233, 34p. [ Links ]
Chacón, E.A.V.; Mendonça, E.S.; Silva, R.R.; Lima, P.C.; Silva, I.R. & Cantarutti, R. (2011) – Decomposição de fontes orgânicas e mineralização de formas de nitrogenio e fósforo. Revista Ceres, vol. 58, n. 3, p. 373-383.
Chandra, S.; Dey, P.; Chatterjee, P. & Bhattacharya, S. (2013) - Allelopathic activity of coffee against Cicer arietinum and Triticum aestivum. Advances in Biogical Research, vol. 7, n. 4, p. 129-133. https://doi.org/10.5829/idosi.abr.2013.7.4.73219 [ Links ]
Chiaradia, J.J.; Chiba, M.K.; Andrade, C.A.; Oliveira, C. & Lavorenti, A. (2009) - Produtividade e nutrição de mamona cultivada em área de reforma de canavial tratada com lodo de esgoto. Revista Brasileira de Ciência do Solo, vol. 33, n. 3, p. 701-709. http://dx.doi.org/10.1590/S0100-06832009000300022 [ Links ]
Cuttle, S.; Shepherd, M. & Goodlass, G.A. (2003) - Review of leguminous fertility-building crops, with particular reference to nitrogen fixation and utilization. In: DEFRA projects OF0316: The development of improved guidance on the use of fertility-building crops in organic farming. London, 167 p. [ Links ]
EPA (1995) - Test methods for evaluating solid waste, Physical/Chemical Methods. 3th ed. U.S. Environmental Protection Agency, Office of Solid Waste and Emergency Response. U.S. Government Printing Office: Washington, DC, SW-846. [ Links ]
Fageria, N.K. (2009) - Nitrogen. In: Fageria, N.K. (Ed.) - The use of nutrients in crop plants. CRC Press, New York, NY, USA, p. 31-77. [ Links ]
Figueroa, E. (2008) – Efeito imediato e residual de esterco de ave poedeira em cultura de grãos. Tese de Doutoramento. Passo Fundo, Faculdade de Agronomia e Medicina Veterinária da UPF. 129p.
Filho, M.C.M.; Tarsitano, M.A.A.; Buzetti, S.; Bertolin, D.C.; Colombo, A.S. & Nascimento, V. (2010) - Análise econômica da adubação nitrogenada em trigo irrigado sob plantio direto no cerrado. Revista Ceres, vol. 57, n. 4, p. 446-453. [ Links ]
Kuhnen, F. (2013) - Mineralização de nitrogênio de solos e de resíduo orgânico em laboratório e em campo. Tese de Doutoramento. Jaboticabal, Faculdade de Ciências Agrárias e Veterinárias. 75p. [ Links ]
Leal, M.A.A.; Mateus, J.S.; Aquino, A.M. & Santos, S.M. (2010) - Avaliação da recuperação de nitrogênio contido em diferentes fertilizantes orgânicos por meio de bioensaio. Boletim 63. Seropédica, RJ: Embrapa Agrobiologia, 20p. [ Links ]
Maluf, H.J.G.M.; Soares, E.M.B.; Silva, I.R.; Neves, J.C.L. & Silva, L. de O.G.S. (2015) - Decomposição de resíduos de culturas e mineralização de nutrientes em solo com diferentes texturas. Revista Brasileira de Ciência do Solo, vol. 39, n. 6, p. 1681-1689. http://dx.doi.org/10.1590/01000683rbcs20140657 [ Links ]
Mariano, E.; Otto, R.; Montezano, Z.F.; Cantarella, H. & Trivelin, P.C.O. (2017) - Soil nitrogen availability indices as predictors of sugarcane nitrogen requirements. European Journal of Agronomy, vol. 89, p. 25-37. https://doi.org/10.1016/j.eja.2017.06.004 [ Links ]
Mulvaney, R.L. (1996) - Nitrogen – Inorganic forms. In: Method of Soil Analysis: chemical methods. Part 3. D. L. Sparks. Madison: Soil Science Society of America, p. 1123-1184.
Nardin, R.R. (2007) - Torta de filtro aplicada em Argissolo e seus efeitos agronômicos em duas variedades de cana-de-açúcar colhidas em duas épocas. Dissertação de Mestrado. Campinas, Instituto Agronômico (IAC). 51p [ Links ]
Nelson, D.W. & Summers, L.E. (1996) - Methods of Soil Analysis. Part 3. Chemical Methods. Madison: Soil Science Society of America, n. 5, p. 961-1010. [ Links ]
Pintado, E.M. & Teixeira, J.A. (2015) - Valorização de subprodutos de a indústria alimentar: obtenção de ingredientes de valor acrescentado. Boletim de Biotecnologia. <https://repositorium.sdum.uminho.pt/bitstream/1822/35328/1/document_21039_1. [ Links ]pdf>
Pires, A.M.M.; Andrade, C.A.; Souza, N.A.P.; Carmo, J.B.; Coscione, A.R. & Carvalho, C.S. (2015) - Disponibilidade e mineralização do nitrogênio após aplicações sucessivas de lodo de esgoto no solo, estimadas por meio de incubação anaeróbica. Pesquisa Agropecuaria Brasileira, vol. 50, n. 4, p. 333-342. [ Links ]
Raij, B. van; Andrade, J.C.; Cantarella, H. & Quaggio, J.A. (2001) - Análise química para avaliação de fertilidade de solos tropicais. Campinas, Instituto Agronômico (IAC), 285p. [ Links ]
Rovira, P. & Vallejo, V.R. (2000) - Evaluating thermal and acid hydrolysis methods as indicators of soil organic matter quality. Communications in Soil Science and Plant Analysis, vol. 31, n. 1-2, p. 81-100. https://doi.org/10.1080/00103620009370422 [ Links ]
Rovira, P. & Vallejo, V.R. (2002) - Labile and recalcitrant pools of carbon and nitrogen in organic matter decomposing at different depths in soil: an acid hydrolysis approach. Geoderma, vol. 107, n. 1-2, p. 109-141. https://doi.org/10.1016/S0016-7061(01)00143-4 [ Links ]
Sánchez, D. & Anzola, C.V. (2012) – Caracterización química de la película plateada del café (Coffea arábica) en variedades Colombia y Caturra. Revista Colombiana de Química, vol. 41, n. 2, p. 211-226.
Scalbert, A. (1991) - Antimicrobial properties of tannins. Phytochemistry, vol. 30, n. 12, p. 3875-3883. https://doi.org/10.1016/0031-9422(91)83426-L [ Links ]
Togoro, A.H. (2016) - Previsão da mineralização de nitrogênio por métodos de incubação de solo o laboratório e no campo. Tese de Doutoramento. Jaboticabal, Faculdade de Ciências Agrárias e Veterinárias. 69p. [ Links ]
Yazid, N.A.; Barrena, R.; Komilis, D. & Sánchez, A. (2017) - Solid-state fermentation as a novel paradigm for organic waste valorization: A review. Sustainability, vol. 9, n. 2, art. 224. https://dx.doi.org/10.3390/su9020224 [ Links ]
Agradecimentos
O presente trabalho foi realizado com apoio da Coordenação de Aperfeiçoamento de Pessoal de Nível Superior - Brasil (CAPES) - Código de Financiamento 001.
Recebido/received: 2018.10.25
Aceite/accepted: 2019.05.01
# Parte da dissertação do primeiro autor