Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Revista de Ciências Agrárias
versão impressa ISSN 0871-018X
Rev. de Ciências Agrárias vol.42 no.3 Lisboa set. 2019
https://doi.org/10.19084/rca.18197
ARTIGO
Aspectos físicos e fisiológicos em sementes de Mimosa ophthalmocentra Mart. ex Benth.
Physical and physiological aspects in seeds of Mimosa ophthalmocentra Mart. ex Benth.
Narjara W. Nogueira1, Salvador B. Torres1, Rômulo M. O. Freitas2,*, Moadir S. Leite1 e Emanoela P. Paiva1
1 Universidade Federal Rural do Semi-Árido, Centro de Ciências Agrárias, Departamento de Ciências Agronômicas e florestais, CEP 59625-900, Mossoró, Rio Grande do Norte, Brasil
2 Instituto Federal de Educação, Ciências e Tecnologia do Ceará, Campus Crato, Departamento de Ensino, CEP 63115-500, Crato, CE, Brasil
(*E-mail: romulomagno_23@hotmail.com)
RESUMO
Objetivou-se caracterizar os aspetos físicos e fisiológicos de frutos e sementes de Mimosa ophthalmocentra por meio de avaliações biométricas, processos de absorção de água e quebra da dormência. Esta espécie é nativa da Caatinga brasileira, bioma pouco estudado e vulnerável, e apresenta elevado potencial energético para produção de álcool combustível e carvão vegetal. A caracterização biométrica teve por base 100 frutos e 100 sementes de dois lotes. Para a caracterização do processo de hidratação das sementes, com e sem desponte, realizou-se a curva de embebição. Para avaliação do melhor método de quebra de dormência das sementes foi utilizado o delineamento experimental foi inteiramente casualizado, em esquema fatorial 2 x 9 (anos de colheita x tratamentos pré-germinativos). Os tratamentos pré-germinativos de quebra de dormência das sementes, constituiu-se de desponte com tesoura e escarificação com lixa 80, na extremidade oposta ao hilo; água quente a 80 ºC por 3, 6 e 12 minutos e ácido sulfúrico (98%) durante 3, 6 e 12 minutos, além do tratamento testemunha (sementes intactas). Avaliou-se a porcentagem e índice de velocidade de germinação, comprimento da parte aérea e da raiz, massa seca da parte aérea, raiz e total. As sementes de M. ophthalmocentra apresentam baixa variação para os aspetos biométricos e as maiores variações ocorrem entre materiais vegetais. A germinação das sementes despontadas inicia-se após 19 horas de embebição, independentemente do material vegetal. A escarificação com lixa 80 ou o desponte com tesoura na extremidade oposta ao hilo são os procedimentos indicados para quebra de dormência em sementes de M. ophthalmocentra.
Palavras-chave: biometria, Caatinga, dormência, embebição, germinação.
ABSTRACT
This study aimed to characterize Mimosa ophthalmocentra fruits and seeds, the process of water absorption and set the best pre-germination treatment to overcome dormancy. This plant species is native of Brazilian Caatinga and has a high energetic value for alcohol production and vegetal coal. Biometric characterization was done with 100 fruits and 100 seeds from two lots. For the characterization of the seed hydration, the process was carried out soaking curve of seed lots with and without lopping. In order to evaluate the best method of breaking seed dormancy, a completely randomized experimental design was used in a 2 x 9 factorial scheme (harvest years x pre-germination treatments). We also evaluated nine pre-germinating treatments to overcome seed dormancy: control; cutting with scissors and scarification with sandpaper 80, at the opposite end to the hilum; hot water at 80 °C for 3, 6 and 12 minutes and sulfuric acid (98%) for 3, 6 and 12 minutes, and evaluated the percentage and speed of germination index, shoot length and root dry weight of shoot, root and total. The seeds of M. ophthalmocentra have low variation for biometric features and the larger variations occur from plant materials. Seed germination starts after 19 hours of imbibition, regardless of plant material. The scarification with sandpaper 80 or emerges with scissors at the opposite end to the hilum are the methods set out to overcome dormancy in M. ophthalmocentra seeds.
Keywords: biometrics, dormancy, Caatinga, germination, water absorption
INTRODUÇÃO
Mimosa ophthalmocentra Mart. ex Benth., conhecida popularmente por jurema-de-embira, é nativa da Caatinga, Brasil (Cavalcanti et al., 2009) e comumente encontrada em áreas de mata ciliar (Lacerda et al., 2007) e de regeneração (Sampaio et al., 2010). Por ser uma espécie com capacidade elevada de celulose e lignina é dotada de alto potencial energético para produção de álcool para combustível e carvão vegetal (Silva et al., 2011).
A Caatinga restringe-se ao território brasileiro e é proporcionalmente o bioma menos estudado, menos protegido (apenas 2% do seu território) e, sobretudo, continua sendo vítima de extenso processo de alteração e deterioração ambiental, provocado pelo uso insustentável dos seus recursos (Leal et al., 2003). Ainda segundo aqueles autores, o estudo e a conservação da biodiversidade desse bioma constituem um dos maiores desafios do conhecimento científico brasileiro.
A biometria de frutos e sementes constitui ferramenta importante para a caracterização das espécies. No tocante aos frutos, essa avaliação constitui um meio importante para detectar a variabilidade genética dentro de populações de uma mesma espécie; já a classificação das sementes por tamanho ou por massa pode ser uma estratégia para uniformizar a emergência das plântulas e selecionar as de maior vigor (Araújo et al., 2014), o que pode otimizar a propagação.
Outro fator relevante para a caracterização das espécies é o conhecimento do seu processo germinativo. Neste, a absorção de água pela semente é fundamental para a retomada das atividades metabólicas, cujo o padrão trifásico é constatado para a maioria das espécies. Neste, a fase I ocorre de forma rápida devido à diferença de potencial hídrico entre a semente e o substrato, a II é caracterizada por redução drástica na velocidade de absorção e marcada pela reativação do metabolismo e a fase III inicia-se com a emissão da raiz. Estas três fases formam a curva de absorção de água pela semente (Marcos-Filho, 2015).
A maioria das espécies da família Fabaceae apresenta dormência, sendo relatada a impermeabilidade do tegumento como principal impedimento à absorção de água e, consequentemente, à germinação de sementes das espécies desta família. Embora esta característica seja importante para a sobrevivência da espécie, torna-se um entrave quando se pretende multiplicá-la em escala comercial, sendo necessária a utilização de tratamentos pré-germinativos, a fim de superar este bloqueio e, assim, uniformizar a germinação.
O tratamento pré-germinativo ideal varia de acordo com o tipo de dormência e com a espécie. Para espécies com impermeabilidade no tegumento, os métodos frequentemente utilizados são o desponte (Farias et al., 2013; Câmara et al., 2015), a escarificação com lixa (Araújo et al., 2014; Coelho et al., 2016), a imersão em ácido sulfúrico (Azeredo et al., 2010; Costa et al., 2010; Torres et al., 2013; Cipriani et al. 2019) e a imersão em água quente (Oliveira et al., 2018).
Naqueles pressupostos, este estudo teve por objetivos caracterizar biometricamente frutos e sementes de M. ophthalmocentra, bem como o seu processo de absorção de água e definir o melhor tratamento pré-germinativo para a quebra da dormência.
MATERIAL E MÉTODOS
As sementes de M. ophthalmocentra foram obtidas a partir da colheita de frutos maduros (vagens) de 50 matrizes localizadas no município de Mossoró, RN (5o11'15'' S, 37o20'39'' W e altitude de 16 m), nos anos de 2013 e 2014, secas à sombra até 9% de umidade, acondicionadas em embalagens impermeáveis e armazenadas em ambiente controlado (temperatura de 10 ± 2 °C e umidade relativa do ambiente de 40%) durante todo o período experimental.
Os dados biométricos dos frutos e das sementes foram obtidos de uma amostra ao acaso de 100 frutos e 100 sementes de cada um dos dois lotes, medindo-se-se, uma a uma, o comprimento, largura e espessura, com auxílio de um paquímetro digital (precisão de 0,01 mm) e suas respectivas massas (mg) em balança de precisão (Araújo et al., 2014). Determinou-se também o número de segmentos por fruto e o número de sementes intactas por fruto por meio da contagem direta.
A curva de absorção de água pelas sementes de cada lote submetidas ou não ao desponte, em quatro repetições de 25 sementes, foram postas para embeber em rolos de papel toalha do tipo Germitest, umedecidos com água destilada na quantidade de 2,5 vezes a massa do papel seco e mantidas em câmaras de germinação do tipo Biochemical Oxygen Demand (B.O.D), sob temperatura de 30 ºC. As sementes foram pesadas em intervalos regulares de 60 minutos até que 50% destas apresentassem emissão de radícula (Araújo et al., 2014). A embebição foi considerada como o aumento de peso em relação ao peso inicial. Para a determinação do teor de água inicial das sementes, foi adotado o método da estufa a 105 °C ± 3 °C, por 24 horas (Brasil, 2009).
Na quebra da dormência, as sementes dos dois lotes foram submetidas aos seguintes tratamentos pré-germinativos: testemunha (sementes intactas); escarificação com lixa nº 80; desponte (corte com tesoura na extremidade oposta ao hilo); imersão em água quente (80 °C) por 3, 6 e 12 minutos; e imersão em ácido sulfúrico (98%) por 3, 6 e 12 minutos. Em seguida, as sementes foram semeadas, entre areia, em caixas plásticas transparentes (11 x 11 x 3,5 cm) do tipo Gerbox. A areia foi previamente lavada, esterilizada e umedecida a 60% de sua capacidade de retenção de água. O teste de germinação foi conduzido pelo período de 10 dias em germinadores, a 30 ºC e fotoperíodo de 8 horas/luz.
As variáveis analisadas foram: a) porcentagem de germinação - expressa em porcentagem de plântulas normais (Brasil, 2009); b) índice de velocidade de germinação - conduzido simultaneamente ao teste de germinação, sendo as plântulas avaliadas diariamente, a partir do início da germinação até o décimo dia após a semeadura e o índice calculado conforme a equação proposta por Maguire (1962); c) comprimento da parte aérea e de raiz - ao final do teste de germinação, todas as plântulas normais da unidade experimental tiveram o comprimento da raiz (base do colo à extremidade da raiz) e da parte aérea (base do colo à inserção dos cotilédones) medidos e os resultados expressos em cm; d) massa seca da parte aérea, da raiz e total de plântulas - todas as plântulas normais da unidade experimental foram fracionadas em raiz e parte aérea e postas para secar em estufa de circulação de ar forçado, regulada a 65 °C, até que obtivessem peso constante (48 horas), sendo posteriormente pesadas em balança analítica de precisão (0,01 g) e a massa seca total determinada pelo somatório das massas secas.
O delineamento experimental foi inteiramente casualizado, em esquema fatorial 2 x 9 (anos de colheita x tratamentos pré-germinativos) constituídos por quatro repetições de 25 sementes. Os dados obtidos foram submetidos à análise de variância pelo teste F e as médias comparadas pelo teste de Tukey, a 5% de probabilidade, com auxílio do programa computacional Sistema para Análise de Variância – SISVAR® (Ferreira, 2011). Para os dados da caracterização biometria e da absorção de água, utilizou-se estatística descritiva no programa Assistat®.
RESULTADOS E DISCUSSÃO
Dentro do mesmo lote, os parâmetros morfométricos das sementes de jurema-de-embira foram homogéneos, não apresentando grandes alterações. Entretanto, houve maiores variações entre os valores das sementes colhidas em anos distintos. Sendo assim, para a caracterização da espécie deve-se levar em consideração o material vegetal que está sendo utilizado (Quadro 1).
As variáveis com maior divergência entre os lotes foram o número médio de segmentos do fruto e o número de sementes intactas por fruto, com variação de 2,4 e 2,0, respectivamente. Provavelmente, essa variação entre os materiais deu-se em virtude de fatores climáticos e características genéticas, levando-se em conta que as colheitas foram realizadas em diferentes áreas do mesmo município nos dois anos. Embora no ano de 2013 tenha ocorrido maior precipitação do que em 2014, as precipitações de 2013 foram irregulares, concentradas entre os meses de maio e junho, com eventuais precipitações entre janeiro e março. Já as precipitações de 2014, embora menores, ocorreram de forma mais regular, entre janeiro e julho (INMET, 2015), o que pode ter favorecido a formação de frutos e sementes.
Em sementes de leguminosas, ao avaliar apenas um lote, resultados semelhantes foram obtidos por Costa et al. (2014) em Clitoria fairchidiana R. A. Howard e por Araújo et al. (2014) em Macroptilium martii Benth., em que os parâmetros morfométricos foram homogéneos, não apresentando grandes variações. Já Santos et al. (2009), avaliando a biometria de sementes de Tabebuia chrysotricha (Mart. Ex A. DC.) Standi., verificaram, de forma semelhante, diferenças significativas entre os materiais vegetais para todas as variáveis avaliadas (comprimento, largura, espessura e peso de sementes), atribuindo essas diferenças principalmente a efeitos genéticos e/ou ambientais.
Os frutos avaliados apresentaram comprimento médio de 5,6 ± 0,6 e 5,2 ± 0,5 cm, com predominância de frutos no intervalo de 5,5 a 6,0 e 5 a 5,5 cm; largura média de 5,2 ± 0,5 e 6,8 ± 0,8 cm e predominância entre 5,0 a 5,5 e 6,5 a 7,0 mm; espessura média de 0,7 ± 0,1 e 0,8 ± 0,1 mm, cuja predominância esteve entre 0,6 a 07 e 0,8 a 09 mm; peso médio de 92,9 ± 16,0 e 110,4 ± 24,8 mg, com predominando entre 80 a 95 e 95 a 110 mg; número médio de segmentos por fruto de 9,1 ± 1,2 e 6,7 ± 1,0, predominando em 9 e 7 segmentos e número médio de sementes por fruto de 7,6 ± 1,2 e 5,6 ± 1,8, com predominância de 7 e 6 sementes viáveis por fruto, considerando-se sempre as sementes de 2013 e 2014, respectivamente (Figura 1).
As sementes avaliadas apresentaram comprimento médio de 3,8 ± 0,3 e 4,4 ± 0,5 mm, com predominância entre 3,5 a 4,0 e 4,0 a 4,5 mm; largura média de 2,8 ± 0,2 e 3,4 ± 0,3 mm, predominando entre 2,6 a 2,9 e 3,2 a 3,5 mm; espessura média de 0,7 ± 0,1 e 0,7 ± 0,1 mm, predominando entre 0,8 a 0,9 e 0,6 a 0,7 mm; e peso médio de 7,0 ± 1,0 e 9 ± 2 mg, com predominância de 7 e 9 mg, considerando-se sempre as sementes de 2013 e 2014, respectivamente (Figura 2).
A ocorrência de grande variação dos caracteres fenotípicos, provavelmente associada à viabilidade genética, é típica de espécies alógamas, especialmente as não domesticadas e favorece a seleção de características em programas de melhoramento genético (Meletti e Brunckner, 2001). Por outro lado, essa variação pode influenciar de forma negativa a capacidade germinativa e estar associada a problemas reprodutivos da espécie.
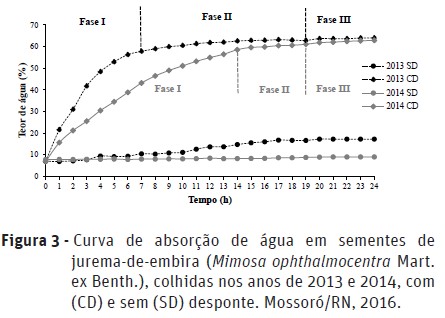
A curva de absorção de água pelas sementes de jurema-de-embira com desponte seguiu o padrão trifásico proposto por Bewley e Black (1994); já para as sementes sem desponte praticamente não apresentaram embebição (Figura 3).
Em relação aos anos de colheita, as sementes despontadas do ano de 2013 embeberam mais rapidamente, entrando na fase II com sete horas de embebição; a partir das 11 horas, houve pequeno ganho de água para as sementes sem desponte. As sementes despontadas de 2014 embeberam mais lentamente, entrando na fase II após 14 horas e não havendo ganho de água para as sementes sem desponte. Provavelmente, esta diferença entre o momento de entrada na fase II se deu pelo fato de as sementes de 2013 serem mais velhas.
A fase I é consequência do potencial matricial. Portanto, constitui-se em um processo físico, independentemente da viabilidade da semente, cujo tempo de permanência é muito variável de espécie para espécie (Bewley e Black, 1994). Nessa fase, a velocidade de absorção e a quantidade de água absorvida também podem variar em função da natureza do tegumento da semente (Coll et al., 2001).
De forma geral, durante a fase II, as sementes despontadas passaram por um período de teor de água constante e após esse período as sementes voltaram a absorver água, havendo então a protrusão da radícula, caracterizando assim o início da fase III e conclusão do processo trifásico da germinação. As sementes sem desponte não entraram na fase III durante o período de avaliação, já as sementes despontadas dos dois anos entraram na fase III após 19 horas de embebição. Assim, a fase II durou 12 horas nas sementes mais velhas (2013) e apenas 5 horas nas mais novas (2014).
A fase II é caracterizada pelas reduções drásticas da velocidade de hidratação e da intensidade da respiração (Araújo et al., 2014), e sua duração normalmente é até dez vezes mais longa que a fase I (Bewley e Black, 1994). No presente trabalho, este efeito não foi observado, provavelmente pelo fato de o tratamento pré-germinativo e a temperatura de embebição de 30 ºC terem acelerado o ganho de água e os eventos metabólicos e, com isso, reduzido o tempo de duração da fase II, sendo verificada uma média de 8,5 horas de duração da fase II, resultado semelhante ao verificado por Araújo et al. (2014) com Macroptilium martii Benth., em que a fase II durou apenas sete horas, contradizendo os pressupostos de Bewley e Black (1994).
Como já citado anteriormente, durante as primeiras 24 horas do processo de embebição não houve ganho de água nas sementes sem desponte colhidas em 2014. No entanto, para as sementes de 2013 sem desponte houve pequeno ganho de água. Este comportamento refletiu-se diretamente na germinação, onde sementes de 2013 não submetidas a tratamentos pré-germinativos (testemunha) tiveram 18% de germinação e as sementes de 2014 não germinaram (Quadro 2).
Em relação aos tratamentos pré-germinativos, as maiores porcentagens de germinação foram obtidas para sementes tratadas com lixa e submetidas ao desponte, sendo este comportamento verificado para os dois lotes. A porcentagem de germinação das sementes de 2014 expostas ao ácido sulfúrico por seis e doze minutos não diferiu da obtida para a lixa e o desponte. No entanto, este comportamento foi diferente para as sementes de 2013, onde apenas a lixa e o desponte foram superiores aos outros tratamentos. As menores porcentagens de germinação foram verificadas quando as sementes foram tratadas com água quente, independentemente do tempo e do ano de colheita, tendo as sementes de 2013 germinado menos do que as de 2014.
A ruptura do tegumento das sementes, causada pela lixa ou tesoura, contribui com o aumento da permeabilidade à água e aos gases, beneficiando, dessa forma, o processo de germinação (Carvalho e Nakagawa, 2012), A maior porcentagem de germinação em tratamentos submetidos ao desponte também foi verificada em sementes de Leucaena leucocephala (Lam.) de Wit. (Deminicis et al., 2006), Piptadenia stipulacea (Benth.) Ducke (Farias et al., 2013) e Macroptilium martii Benth. (Araújo et al., 2014).
As maiores velocidades de germinação foram verificadas em sementes tratadas com ácido sulfúrico durante 6 ou 12 minutos, independentemente do ano de colheita, tendo também as sementes de 2013 apresentado altos índices de velocidade de germinação quando escarificadas com lixa e desponte. A velocidade de germinação está associada à velocidade da entrada de água na semente e, consequentemente, à ativação dos processos metabólicos. Neste caso, diferentemente da lixa e do desponte, o ácido sulfúrico promoveu desgaste do tegumento em toda a extensão da semente, fazendo com que os processos de embebição e germinação fossem mais rápidos.
A maior velocidade de germinação de sementes submetidas ao desponte também foi verificada em sementes de L. leucocephala, (Deminicis et al., 2006) e P. stipulacea (Farias et al., 2013). Em sementes de M. martii, as maiores velocidades foram promovidas por sementes submetidas ao desponte ou tratadas com ácido sulfúrico (Araújo et al., 2014).
Para o comprimento da parte aérea, os maiores valores foram obtidos nos tratamentos lixa, desponte e ácido sulfúrico (3, 6 e 12 minutos), independentemente do ano, não diferindo também do tratamento com água quente durante 3 e 6 minutos para sementes colhidas em 2014. O tratamento com água quente durante 3 e 6 minutos proporcionou a formação de raízes mais longas em ambos os anos. A lixa, o desponte e o ácido sulfúrico por 3 e 6 minutos também proporcionaram maior formação de raízes para plântulas provenientes das sementes de 2014.
De forma semelhante, Farias et al. (2013) não verificaram diferença significativa para o comprimento da parte aérea de plântulas de P. stipulacea provenientes de sementes submetidas ao desponte, imersão em água quente e à escarificação com ácido. Já Nascimento et al. (2009) e Araújo et al. (2014) não verificaram diferença significativa para o comprimento da parte aérea e de raiz de plântulas provenientes de sementes submetidas ao desponte e à escarificação com ácido, em sementes de Parkia platycephala Benth. e M. martii, respectivamente.
Para a massa seca da parte aérea, não houve diferenças significativas entre os tratamentos para os anos de colheita, com exceção da testemunha de 2014, cuja germinação não ocorreu, motivando a não formação de plântulas e, consequentemente, de massa seca. Entre os anos, houve diferenças para a lixa, ácido sulfúrico por 6 minutos e água quente por 3 e 6 minutos, verificando-se maior acumulação de massa seca da parte aérea nas plântulas de 2014 (Quadro 3).
A massa seca das raízes das plântulas de 2014 comportou-se de forma semelhante à massa seca da parte aérea, não havendo diferenças significativas entre os tratamentos, com exceção da testemunha, cuja germinação foi nula. Para as plântulas de 2013, as menores acumulações de massa seca das raízes foram verificados na testemunha, seguidos da lixa, desponte e ácido sulfúrico por 12 minutos. Os outros tratamentos promoveram maior acumulação de massa seca de raízes, não diferindo estaticamente entre si.
De forma semelhante ao que foi verificado para a massa seca da parte aérea, para a massa seca total também não houve diferença estatística entre os tratamentos para as plântulas provenientes de sementes colhidas em 2013 e 2014, com exceção da testemunha, onde não houve germinação. Entre os anos de colheita, houve diferenças significativas para a lixa, ácido sulfúrico durante 6 minutos e água quente durante 3 e 6 minutos, onde se verificou maior acumulação de massa seca total nas plântulas de 2014.
A semelhança entre as massas secas da parte aérea e total para os tratamentos com ácido sulfúrico, água quente e desponte, também foram verificados em plântulas de P. stipulacea (Farias et al., 2013). Já em plântulas de M. martii, o desponte mostrou-se superior aos demais tratamentos (Araújo et al., 2014).
Embora a escarificação química por H2SO4 tenha promovido resultados positivos para algumas variáveis avaliadas, os métodos de escarificação com lixa e o desponte mostram-se mais promissores, pois apresentam facilidade de execução e baixo custo (Araújo et al., 2014); o uso do ácido sulfúrico confere riscos à saúde, necessitando de cuidados no manuseio e local apropriado de descarga (Dutra et al., 2012), além de possuir aquisição restrita, não sendo possível a comercialização ou aquisição desse produto sem as documentações necessárias.
CONCLUSÕES
1. As sementes de jurema-de-embira apresentam baixa variação para os aspetos biométricos e as maiores variações ocorrem entre materiais vegetais.
2. A germinação das sementes despontadas inicia-se após 19 horas de embebição, independentemente do material vegetal.
3. A escarificação com lixa 80 ou o desponte com tesoura na extremidade oposta ao hilo são os métodos indicados para quebra de dormência em sementes de jurema-de-embira.
Referências Bibliográficas
Araújo, A.M.S.; Torres, S.B.; Nogueira, N.W.; Freitas, R.M. O. & Carvalho, S.M.C. (2014) - Caracterização morfométrica e germinação de sementes de Macroptilium martii Benth. (Fabaceae). Revista Caatinga, vol. 27, n. 3, p. 124-131. [ Links ]
Azeredo, G.A.; Paula, R.C.; Veleri, S.V. & Moro, F.V. (2010) - Superação de dormência de sementes de Piptadenia moniliformis Benth. Revista Brasileira de Sementes, vol. 32, n. 2, p. 49-58. http://dx.doi.org/10.1590/S0101-31222010000200006 [ Links ]
Bewley, J.D. & Black, M. (1994) - Seeds: physiology of development and germination. 3. ed. New York, Plenum Press, 445 p. [ Links ]
Brasil (2009) - Regras para análise de sementes. Brasília, Ministério da Agricultura, Pecuária e Abastecimento, Secretaria de Defesa Agropecuária, 365 p.
Câmara, F.M.M.; Pereira, E.C.; Carneiro, J.V.; Oliveira, H.T.B.; Silva, R.M. & Pereira, G.A. (2015) - Métodos alternativos na superação de dormência em sementes de flamboyant. Agropecuária Científica no Semiárido, vol. 11, n. 3, p. 76-83. [ Links ]
Carvalho, N.M. & Nakagawa, J. (2012) - Sementes: ciência, tecnologia e produção. 5. ed. Jaboticabal, Funep, 409 p. [ Links ]
Cavalcanti, A.D.C.; Rodal, M.J.N.; Sampaio, E.V.S.B. & Costa, K.C.C. (2009) - Mudanças florísticas e estruturais, após cinco anos, em uma comunidade de Caatinga no Estado de Pernambuco, Brasil. Acta Botânica Brasílica, vol. 23, n. 4, p. 1210-1212. http://dx.doi.org/10.1590/S0102-33062009000400032 [ Links ]
Cipriani, V.B.; Garlet, J. & Lima, B.M. (2019) - Quebra de dormência em sementes de Chloroleucon acacioides e Senna macranthera. Revista de Ciências Agrárias, vol. 42, n. 1, p. 49-54. http://dx.doi.org/10.19084/RCA18238 [ Links ]
Coelho, M.F.B.; Azevedo, R.A.B.; Souza, J.W.N.; Barros, L.P. & Souza, A.S. (2016) - Métodos de superação de dormência de sementes de Schinopsis brasiliensis. Revista Verde de Agroecologia e Desenvolvimento Sustentável, vol. 11, n. 1, p. 14-17. https://doi.org/10.18378/rvads.v11i1.3910 [ Links ]
Coll, J.B.; Rodrigo, G.N.; Garcia, B.S. & Tames, R.S. (2001) - Fisiologia vegetal. 6. ed. Madrid, Ediciones Pirámide, 566 p. [ Links ]
Costa, L.G.; Silva, A.G. & Gomes, D.R. (2014) - Morfologia de frutos, sementes e plântulas, e anatomia das sementes de sombreiro (Clitoria fairchildiana). Amazonian Journal of Agricultural and Environmental Sciences, vol. 57, n. 4, p. 414-421. https://doi.org/10.4322/rca.1596 [ Links ]
Costa, P.A.; Lima, A.L.S.; Zanella, F.; Freitas, H. (2010) - Quebra de dormência em sementes de Adenanthera pavonina L. Pesquisa Agropecuária Tropical, vol. 40, n. 1, p. 83-88. [ Links ]
Deminicis, B.B.; Almeida, J.C.C.; Blume, M.C.; Araújo, S.A.C.; Pádua, F.T.; Zanine, A.M. & Jaccoud, C.F. (2006) - Superação da dormência de sementes de oito leguminosas forrageiras tropicais. Archivos de Zootecnia, vol. 55, n. 212, p. 401-404. [ Links ]
Dutra, T.R.; Massad, M. D.; Sarmento, M.F.Q. & Oliveira, J.C. (2012) - Emergência e crescimento inicial da canafístula em diferentes substratos e métodos de superação de dormência. Revista Caatinga, vol. 25, n. 2, p. 65-71. [ Links ]
Farias, R.M.; Freitas, R.M.O.; Nogueira, N.W. & Dombroski, J.L.D. (2013) – Superação de dormência em sementes de jurema-branca (Piptadenia stipulacea). Amazonian Journal of Agricultural and Environmental Sciences, vol. 56, n. 2, p. 160-165. http://dx.doi.org/10.4322/rca.2013.024
Ferreira, D.F. (2011) - Sisvar: a computer statistical analysis system. Ciência e Agrotecnologia, vol. 35, n. 6, p. 1039-1042. http://dx.doi.org/10.1590/S1413-70542011000600001 [ Links ]
Inmet (2015) - Dados da estação A318. Ministério da Agricultura, Pecuária e Abastecimento, MAPA, Mossoró (anos de 2013 e 2014). <http://www.inmet.gov. [ Links ]br/>.
Lacerda, A.V.; Barbosa, F.M. & Barbosa, M.R.V. (2007) - Estudo do componente arbustivo-arbóreo de matas ciliares da bacia do rio Taperoá, semiárido paraibano: uma perspectiva para a sustentabilidade dos recursos naturais. Oecologia Brasiliensis, vol. 11, n. 3, p. 331-340. [ Links ]
Leal, I.R.; Tabarelli, M. & Silva, J.M.C. (2003) - Ecologia e conservação da Caatinga. 1. ed. Recife, UFPE, 822p. [ Links ]
Maguire, J.D. (1962) - Speed of germination: aid in selection and evaluation for seed ling emergence and vigor. Crop Science, vol. 2, n. 2, p. 176-177. [ Links ]
Marcos-Filho, J. (2015) - Fisiologia de sementes de plantas cultivadas. 2. ed. Londrina, Abrates, 659 p. [ Links ]
Meletti, L.M.M. & Bruckner, C.H. (2001) - Melhoramento genético. In: Bruckner, C.H. & Picanço, M.C. (Orgs.) - Maracujá: tecnologia de produção, pós-colheita, agroindústria, mercado. Porto Alegre, Cinco Continentes, p. 345-385. [ Links ]
Nascimento, I.L.; Alves, E.U.; Bruno, R.L.A.; Gonçalves, E.P.; Colares P.N.Q. & Medeiros, M.S. (2009) - Superação da dormência em sementes de faveira (Parkia platycephala Benth). Revista Árvore, vol. 33, n. 1, p. 35-45. http://dx.doi.org/10.1590/S0100-67622009000100005 [ Links ]
Oliveira, K.J.B.; Lima, J.S.S.; Andrade, L.I.F., Costa, J.A.M.A. & Crispim, J.F. (2018) - Quebra de dormência de sementes de Delonix regia (Fabaceae). Revista de Ciências Agrárias, vol. 41, n. 3, p. 709-716. http://dx.doi.org/10.19084/RCA17302 [ Links ]
Sampaio, E.; Gasson, P.; Baracat, A.; Cutler, D.; Pareyn, F. & Lima, K.C. (2010) - Tree biomass estimation in regenerating areas of tropical dry vegetation in northeast Brazil. Forest Ecology and Management, vol. 259, n. 6, p. 1135-1140. https://doi.org/10.1016/j.foreco.2009.12.028 [ Links ]
Santos, F.S.; Paula, R.C.; Sabonaro, D.Z. & Valadares, J. (2009) - Biometria e qualidade fisiológica de sementes de diferentes matrizes de Tabebuia chrysotricha (Mart. Ex A. DC.) Standi. Scientia Forestalis, vol. 37, n. 82, p. 163-173. [ Links ]
Silva, L.B.; Santos, F.A.R.; Gasson, P. & Cutler, D. (2011) - Estudo comparativo da madeira de Mimosa ophthalmocentra Mart. ex Benth e Mimosa tenuiflora (Willd.) Poir. (Fabaceae-Mimosoideae) na caatinga nordestina. Acta Botânica Brasilica, vol. 25, n. 2, p. 301-314. http://dx.doi.org/10.1590/S0102-33062011000200006 [ Links ]
Torres, S.B.; Benedito, C.P.; Pereira, F.E.C.B. & Freitas, R.A. (2013) - Germination of Ravenala madagascariensis (Strelitziaceae) seeds submitted to chemical scarification. Seed Science and Technology, vol. 41, n. 1, p. 154-157. http://dx.doi.org/10.15258/sst.2013.41.1.17 [ Links ]
Recebido/Received: 2019.97.02
Aceitação/Accepted:2019.07.12