INTRODUÇÃO
O Brasil se destaca no panorama mundial quando se trata de produção e comercialização de grande número de espécies anonáceas (Zucareli et al., 2008). As anonáceas que produzem frutos comestíveis são plantas nativas de regiões tropicais e subtropicais das Américas (Sobrinho, 2014). Várias espécies do gênero Annona são nativas do Brasil e outras como a pinheira (Annona squamosa L.) foram introduzidas no Século XVII (Sobrinho, 2014). Devido à boa adaptação às condições edafoclimáticas e por despertar grande interesse no mercado nacional de frutas in natura, a cultura da pinheira difundiu-se em várias regiões do país, se estendendo da região Norte até o estado de São Paulo (Sobrinho, 2010). Além da anona, a cherimólia (Annona cherimola) e seus híbridos conhecidos como atemóias são também importantes frutos para o mercado de mesa (Lemos, 2014).
As regiões preferenciais de cultivo da pinheira estão localizadas em zonas quentes ou semiáridas com acentuado déficit hídrico na maior parte do ano (São José, 2014). Tais condições climáticas produzem estresse às plantas que respondem muito bem com uma série de adaptações que incluem fechamento dos estomas, proteção cerosa das folhas, abscisão foliar e sistema radicular profundo. Todavia, mesmo com todas essas adaptações o estresse hídrico promove uma redução na taxa de crescimento vegetativo das plantas (Peloso et al., 2017).
Da Silva Oliveira (2016) destaca a importância da cultura da anona, pois representa umas das mais relevantes alternativas de produção no semiárido, sendo responsável por empregar mão de obra justamente em regiões com problemas relacionados à seca. À medida que a população mundial cresce, ocorre um declínio no fornecimento de água para a produção agrícola, e o desenvolvimento de cultivares tolerantes e eficientes em uso de água é uma preocupação global (Barnabás, 2008).
O estresse é uma condição considerada como um afastamento expressivo das condições ótimas para a sobrevivência, que independente do grau em que ocorra, é responsável por induzir mudanças e respostas em todos os níveis funcionais do organismo, essas mudanças podem ser reversíveis num princípio, mas podem, também, se tornarem permanentes (Munns, 2002; Larcher, 2008; Taiz et al., 2017). Mesmo em casos em que o estresse ocorra somente de forma temporária, a resistência da planta torna-se cada vez menor conforme a duração do estresse (Bianchi et al., 2016). Quando a planta atinge o limite máximo da sua capacidade de se ajustar a tal condição desfavorável, os distúrbios que antes não se manifestavam aparecem na forma de doenças crônicas ou injúrias irreversíveis (Larcher, 2008).
As alterações fisiológicas que ocorrem nas plantas são os maiores indicativos de suas capacidades para resistir às adversidades causada pelo estresse (Chaumont e Tyerman, 2014; Kirkham, 2014). Isso porque a fotossíntese é responsável por fornecer energia necessária à manutenção e desenvolvimento da planta o comprometer esse processo, provoca redução no potencial de crescimento das mesmas (Soares de Melo et al., 2010). A deficiência hídrica nas plantas normalmente aumenta a resistência difusiva ao vapor de água, causada pelo fechamento estomático, provocando uma redução da transpiração, de forma a evitar maior perda de água, e consequentemente redução na fotossíntese (dos Santos e Schumacher, 2016).
Dentre os recursos essenciais para o desenvolvimento da planta a água é o mais limitante. A limitação de água é uma realidade em regiões semiáridas. Assim, a busca por soluções a este fator ambiental é baseada numa utilização mais eficiente dos recursos hídricos que é uma solução fundamental para o aumento da produtividade das plantas em ambientes com déficit hídrico (Sinclair et al., 2008).
Compreender os mecanismos subjacentes a essas diferentes respostas pode apoiar o projeto de novas ferramentas de gerenciamento e genótipos para agricultura de precisão moderna. Dada a importância dessas informações, e para melhor permear a produção de anona, houve a necessidade de se trabalhar com esses acessos com o objetivo de avaliar as alterações fisiológicas das plantas em crescimento inicial, caracterizando à nível de espécie e comparando as respostas entre os dois acessos.
MATERIAL E MÉTODOS
O experimento foi realizado em casa de vegetação cedida pela Embrapa (Unidade de Execução de Pesquisa - Rio Largo-AL) no Centro de Ciências Agrarias (CECA) da Universidade Federal de Alagoas (UFAL), campus Rio Largo - AL (coordenadas 09°28’02”S;35°49’43W e altitude de 127 metros) visando estabelecer a capacidade de crescimento e resistência ao estresse hídrico de plantas jovens de dois acessos de pinheira.
Durante o período experimental foram monitoradas as condições ambientais através de uma estação meteorológica automática, foram registrados: temperatura (ºC), humidade relativa do ar (%) e radiação solar (W m-2). Utilizando os dados de temperatura e humidade foi calculado o DPV (Déficit de Pressão de Vapor) do ar (KPa), utilizando a fórmula:
Onde:
es = Pressão de Vapor Saturado
e = Pressão de Vapor do ar;
T = Temperatura
HR = Humidade Relativa
O experimento foi conduzido com dois acessos de pinheira (Annona squamosa L.) existentes no banco de germoplasma de pinheira do CECA-UFAL: cv. Crioula (com cera nas folhas), amplamente utilizada nas áreas de cultivo comercial das zonas semiáridas do Nordeste, e a cv. Verdinha (sem cera nas folhas), ainda não cultivada comercialmente.
Foram utilizadas plantas jovens com dez meses de idade formadas a partir de sementes obtidas de frutos das duas cultivares. As plantas foram estabelecidas em vasos plásticos com capacidade para 20 litros, que tiveram a parte inferior furada para permitir a drenagem, e para melhor garantir o procedimento foi colocado brita no fundo do vaso com a finalidade de aumentar a porosidade e sobre a mesma foi colocada uma manta semipermeável para evitar a perda de solo pelo local de drenagem. O substrato foi preparado com solo e esterco curtido. As mudas foram podadas na mesma altura (35 cm) e desfolhadas para que partissem da mesma condição de tamanho, em seguida foram transplantadas nos vasos.
Foram estabelecidas duas épocas (inverno e verão) para a coleta das variáveis fisiológicas. Para as duas épocas foram estabelecidos intervalos de restrição hídrica baseados nas condições de clima, levando em consideração, principalmente, o déficit de pressão de vapor (DPV). Para o inverno os intervalos foram: 0 dias (controle), 5 dias (estresse leve), 10 dias (estresse moderado) e 15 dias (estresse máximo); e para avalição no verão usou-se: 0 dias (controle), 3 dias (estresse leve), 6 dias (estresse moderado) e 9 dias (estresse máximo). Após as avaliações feitas nas plantas estressadas elas foram reidratadas por 2 dias e feita uma nova observação das alterações fisiológicas.
Foi coletada uma amostra composta do substrato já pronto e levado para laboratório para se realizar uma caracterização das propriedades químicas e capacidade de retenção de água do solo (Quadro 1). A capacidade de retenção de água do solo foi determinada utilizando a metodologia do anel volumétrico (Claessen, 1997).
Quadro 1 Caracterização das propriedades químicas e capacidade de retenção de água do solo
| M.O Total (%) | pH | P | K | Ca | Mg | H+Al | Al | ||
|---|---|---|---|---|---|---|---|---|---|
| ---mg dm-3--- | -------------------- cmolcdm-3----------------- | ||||||||
| 4,43 | 6,1 | 179 | 111 | 5,5 | 1,2 | 1,8 | 0,0 | ||
| Tensão (MPA) | Humidade (%) | ||||||||
| 0,03 | 31,2 | ||||||||
| 1,5 | 5,8 | ||||||||
| DTA | 25,4 | ||||||||
Fonte: Central Analítica, Maceió - AL, 2017. DTA: Disponibilidade total de água
Em cada vaso foi colocado um cano de 50 mm de diâmetro e 15 cm de comprimento para monitoramento da humidade do solo durante todo o experimento. Esse monitoramento ocorreu por meio da sonda SM-200 (DELTA-T Devices, Cambridge - England), que avalia a humidade do solo em percentagem.
Todas as medições da fotossíntese foram realizadas aos 100 dias após o transplantio das mudas para os vasos. As leituras foram feitas em dois pontos de cada lado da nervura central da folha, na face adaxial da quarta folha totalmente expandida a partir do ápice (folha +4), no período entre 9:30 h e 10:00 h. Estimando o teor de clorofila total com um clorofilômetro portátil SPAD-502 (Minolta Corporation, Ramsey, USA).
As trocas gasosas, que inclui a condutância estomática (Gs), taxa de transpiração (E) e taxa de fotossíntese líquida (A), foram mensuradas utilizando um analisador de gases a infravermelho (IRGA) LI 6400XT (LI-COR, USA). As medições foram feitas em concentração de CO2 e humidade ambiente. A densidade de fluxo de fotões fotossintéticos no IRGA foi fixada em 1000 µmol m-2 s-1 com uma fonte de luz artificial.
Para as medidas de eficiência potencial e efetiva do PSII foi utilizada a segunda folha totalmente expandida. A eficiência quântica potencial do fotossistema II (Fv/Fm) foi medida às 4h da manhã e às 12h da tarde. As medidas foram realizadas com um fluorômetro portátil WALZ-PAM-2500 (Walz, Germany), que utiliza a medição de luz por modulação em amplitude de pulso, para promover o fechamento dos centros de reação do PSII (Maxwell e Johnson, 2000). Sendo a Fv/Fm mensurada após condicionamento das folhas ao escuro, com pinças de metal, durante 30 minutos. A eficiência quântica efetiva do PSII (ΦPSII) foi medida logo após as medidas de Fv/Fm no horário 12h30min nas mesmas folhas sob luz ambiente.
Os potenciais hídricos das folhas das plantas de pinheira foram medidos utilizando a bomba de pressão do tipo Scholander. A folha +3 (terceira folha totalmente expandida) foi coletada entre 4 e 5 h da manhã.
Análise estatística
O experimento foi organizado em desenho fatorial 4x2 (controle mais três níveis de estresse e dois acessos) e estabelecidos em delineamento inteiramente casualizados com seis repetições e uma planta por parcela. As médias obtidas foram comparadas pelo teste Fisher’s Least Significant Difference (LSD/Fisher) a 5% de probabilidade.
RESULTADOS E DISCUSSÃO
Neste estudo, as respostas ao estresse hídrico foram avaliadas a curto prazo, significando que uma resposta mais rápida à seca representa menos perda de água e mais chances de sobrevivência, sendo o fechamento estomático a primeira reação da planta a esta condição adversa, e como os estomas são os poros responsáveis pelas trocas gasosas entre planta e atmosfera, então todos os resultados dos fatores como fotossíntese, condutância estomática, transpiração e potencial hídrico da folha se relacionaram em pelo menos algum nível.
As características das trocas gasosas foram semelhantes nos dois acessos de pinheira estudados, em ambas ocorreu um decréscimo impactante da taxa fotossintética líquida (A) (Figura 1) durante a avaliação na época seca, verificando-se uma redução de 72,87% já no terceiro dia de restrição hídrica em comparação com as plantas do regime irrigado, sendo que aos 6 dias de estresse as plantas mantiveram a taxa fotossintética praticamente estável e durante o estresse máximo, observado aos 9 dias após a suspensão da irrigação, foi verificado outra queda acentuada da taxa fotossintética de 79,5% em comparação com aquela verificada aos 3 dias. Em trabalho realizado com A. squamosa avaliando a taxa fotossintética em pleno sol, Flori et al. (2012) encontrou resultados inferiores aos observados neste trabalho para plantas sob irrigação e valores aproximados aos encontrados para plantas sob condições de estresse hídrico por três dias, sendo aproximadamente 10 μmol CO2 m-2 s-1.
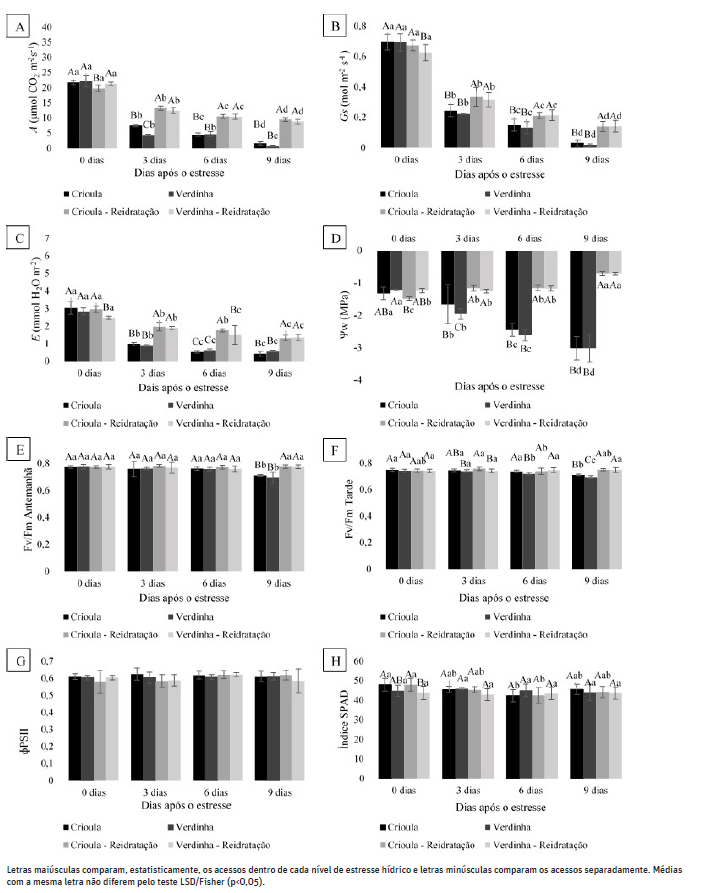
Figura 1 Fotossíntese (A) (A); Condutância estomática (Gs) (B) Transpiração (E) (C); Potencial hídrico foliar (D); Eficiência quântica potencial do PSII (Fv/Fm) na antemanhã (E) e de Tarde (F); Eficiência quântica efetiva do PSII (ɸPSII) ao meio dia (G) e índice SPAD (H) em acessos de anona submetidas ao estresse hídrico e reidratados na época seca.
Os resultados correspondentes à transpiração e condutância estomática obtiveram valores parecidos aos encontrados na taxa fotossintética, isso porque esses fatores estão intimamente relacionados. De acordo com Angelocci (2002), ao mesmo tempo em que as plantas perdem água na forma de vapor (transpiração) trocam dióxido de carbono e oxigênio com a atmosfera, sendo o CO2 a fonte de carbono na fotossíntese. E com os estomas fechados essa troca gasosa é reduzida (Peloso et al., 2017).
A taxa transpiratória nas condições de regime irrigado foi mais elevada nas plantas cerosas, no entanto, nestas foi menor quando submetidas ao estresse máximo, corroborando com o que foi descrito por Taiz et al. (2017), que o fechamento estomático pode não ser suficientes para evitar a transpiração em estresses mais severos, fazendo com que a transpiração cuticular se torne importante, reduzindo a perda de água pelo aumento do depósito de cera.
Os valores encontrados para a condutância estomáticas estão apresentados na Figura 1 (B). Ambos acessos obtiveram 0,69 mol H2O m-2.s-1 em regime irrigado e em estresse máximo a cv. Verdinha apresentou resultados inferiores ao observado para cv. Crioula. No entanto, não houve, diferença significativa, mas pode ser um indicativo de que há maior resistência à escassez hídrica em plantas com deposição de cera mais espessa nas folhas. Endres (2007) afirma que entre os fatores que mais influenciam a variação da condutância estomática e transpiração são a idade fisiológica das folhas, o DPV e a hidratação das plantas.
A época em que ocorreu essa avaliação com alto índice de radiação associado a um aumento do DPV explica o baixo potencial hídrico nas folhas relacionado à taxa transpiratória, isso porque o vapor d’água transpirado tem a função de regular a temperatura interna da folha, e de acordo com os dados meteorológicos (Figura 2) as plantas estavam expostas à uma intensa radiação solar causando o aumento da carga radiante e consequentemente o aumento da temperatura à níveis intoleráveis para as plantas, forçando a abertura estomática e a perda de água para atmosfera.
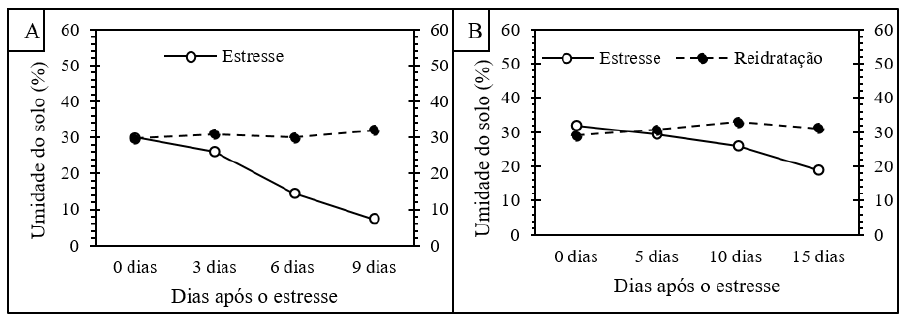
Figura 2 Umidade de solo com dois acessos de anona (A. squamosa) submetidas a estresse hídrico na época seca (A) e época chuvosa (B).
Do Carmo Araújo (2009) explica que a luz desempenha um papel muito importante na regulação de muitas enzimas cloroplásticas e que quando essa luz incide em excesso, pode causar distúrbios nos processos envolvendo às atividades fotossintéticas. Então mesmo as plantas sem suspenção de rega obtiveram potencial hídrico das folhas baixos, apresentando valores de -1,32 Mpa e -1,22 Mpa para os acessos cv. Crioula e cv. Verdinha respectivamente.
Endres (2007), avaliando a variação diária e sazonal da relação da água em pinheiras sob diferentes regimes de irrigação, observou valores máximos de potencial hídrico foliar na época seca de -2,90 MPa, valores semelhantes aos encontrados neste trabalho para mudas submetidas ao estresse máximo, que foi de -3,03 MPa em ambos acessos em humidade do solo próximo ao ponto de emurchecimento (Figura 2; Quadro 1).
O estresse máximo imposto às mudas de pinheira afetou a Fv/Fm na antemanhã, mantendo-se acima de 0,7 para a cv. Crioula e abaixo para a cv. Verdinha. Não houve queda acentuada na Fv/Fm até o sexto dia de estresse. Baker (1991) explica que em condições de estresse moderado a atividade potencial do fotossistema II não é prejudicado, no entanto, em condições de estresse mais severo, pode-se desencadear nas plantas um efeito fotoinibitório causado pelo decréscimo no rendimento quântico máximo do fotossistema II. A Fv/Fm avaliadas no período da tarde apresentou uma queda parecida com a observada na antemanhã, porém, o decréscimo foi mais uniforme e indicou valores menores para a cv. Verdinha.
Não houve interação entre os fatores avaliados, e apesar do acesso de anona cv. Crioula apresentar uma certa vantagem sob condições de estresse em comparação à cv. Verdinha, estatisticamente, os dois acessos obtiveram desempenho semelhante na maior parte das variáveis fisiológicas avaliadas, em todos os níveis de estresse. As maiores variações, no entanto, foram observadas entre os níveis de estresse dentro de cada acesso estudado.
Como resultados de reidratação, as plantas responderam muito bem à reposição de água, mesmo chegando a níveis críticos das alterações fisiológicas, sendo possível observar a capacidade das mudas de preservarem seu potencial vegetativo após um período de escassez hídrica.
Em relação a taxa fotossintética as mudas obtiveram maior recuperação nas plantas submetidas ao estresse máximo, sendo 1,63 e 0,80 μmol CO2 m-2s-1 elevando-se para 9,50 e 8,82 μmol CO2 m-2s-1 para cv. Crioula e cv. Verdinha, respectivamente.
A taxa transpiratória e a condutância estomática também aumentaram, porém, o tempo de recuperação não foi suficiente para que as plantas estressadas voltassem ao seu funcionamento normal. Durante a reidratação as plantas mais estressadas continuaram transpirando menos, provavelmente devido ao tempo necessário para ocorrer o ajuste osmótico, o que pode explicar o potencial hídrico foliar nas plantas sob estresse máximo, que foi de -3,03 MPa em ambos acessos para -0,71 e -0,72 MPa para cv. Crioula e cv. Verdinha, na devida ordem, mantendo maior conteúdo de água nas folhas que as plantas sob regime irrigado. Cerqueira (2004) estudando resposta de porta-enxertos de citrinos em déficit hídrico, constatou que no limoeiro cravo, as plantas que foram estressadas e posteriormente reidratadas apresentaram uma recuperação mais rápida no potencial hídrico foliar que foi aos 3 dias em comparação com a transpiração que houve uma recuperação quantificável apenas aos 4 dias após a reidratação.
Em relação a eficiência quântica potencial do PSII foi possível observar que as mudas sob estresse máximo se recuperaram muito bem, obtendo valores de Fv/Fm acima de 0,75 na avaliação da antemanhã. No entanto, as mudas apresentaram fotoinibição dinâmica no período da tarde, para regime irrigado e estresse de 6 dias para a cv. Crioula e regime irrigado e suspensão de água por 3 dias para a cv. Verdinha.
Para eficiência quântica efetiva do PSII (ɸPSII), os acessos de pinheira apresentaram variações. Verificou-se que nos tratamentos com a cv. Crioula em regime irrigado e estresse leve obteve menores valores no período de reidratação. O mesmo aconteceu na cv. Verdinha sob condições de estresses leve e máximo.
As avaliações feitas em época chuvosa mostram resultados bem diferentes aos encontrados em época seca. Isso porque as condições de clima retardaram o estresse hídrico devido à alta humidade relativa do ar, baixas temperaturas, baixa radiação e DPV.
Essas condições de ambiente favoreceram a taxa fotossintética (Figura 3). Para as plantas do tratamento controle houve um aumento de mais de 60% na taxa fotossintética das mudas avaliadas no inverno em comparação com aquelas analisadas em época seca. As plantas em estresse máximo no inverno, observados aos 15 dias de restrição hídrica, obtiveram taxa fotossintéticas superiores as observadas nas mudas avaliadas aos 3 dias após o estresse no verão, esses valores também foram superiores aos obtidos durante a reidratação das mudas no período seco.
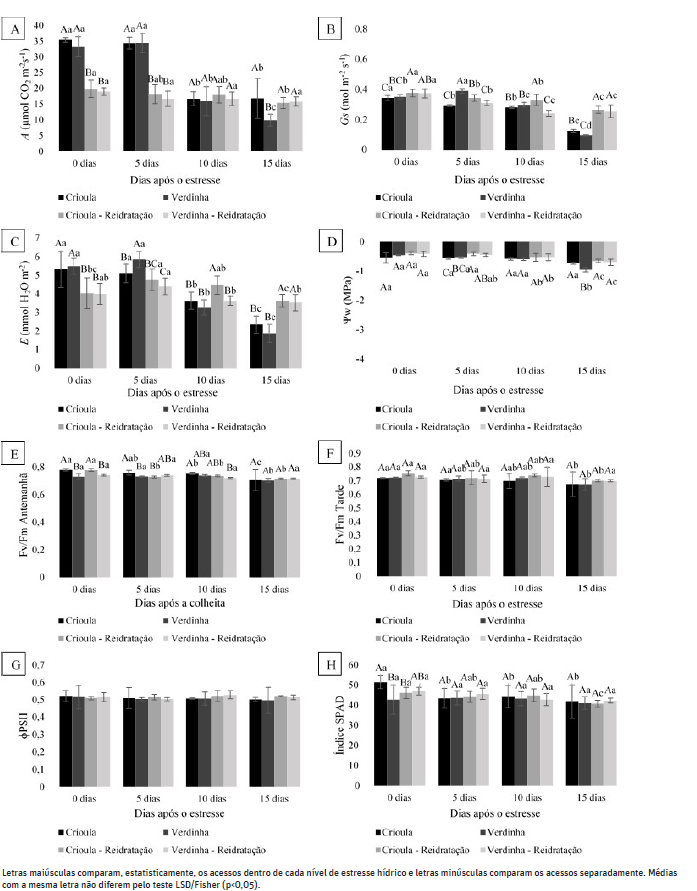
Figura 3 Fotossíntese (A) (A); Condutância estomática (Gs) (B) Transpiração (E) (C); Potencial hídrico foliar (D); Eficiência quântica potencial do PSII (Fv/Fm) na antemanhã (E) e de Tarde (F); Eficiência quântica efetiva do PSII (ɸPSII) ao meio dia (G) e índice SPAD (H) em acessos de anona submetidas ao estresse hídrico e reidratados na época chuvosa.
O mesmo comportamento fotossintético foi observado por Dan Tatagiba (2007) que avaliando o comportamento fisiológico em clones de eucalipto em época seca e chuvosa evidenciou maior taxa fotossintética nos clones avaliados em época chuvosa. Apesar da alta taxa fotossintética encontradas durante o inverno, a condutância estomática apresentou valores inferiores aos observados no verão para as plantas sob regime irrigado.
As mudas avaliadas em época chuvosa apresentaram maior transpiração em relação as mudas da época seca, isso deve-se, provavelmente, ao fato de que a anona é adaptada às condições de estresse hídrico, e em função das condições climáticas mais desfavoráveis no verão, com maior temperatura, radiação e DPV pode ter ativado seu mecanismo de defesa para evitar a desidratação. Diferente das avaliações no inverno, onde os valores de temperatura, radiação e DPV (Figura 3) eram baixos durante todo o dia, descartando a possibilidade de haver, ao menos, déficit hídrico temporário.
Dan Tatagiba (2007) também constatou maior transpiração em clones de eucalipto avaliados em época chuvosa. Como esperado, o potencial hídrico foliar se manteve bem mais elevado nos dois acessos comparados aos verificados em época seca, em função das condições climáticas. Mesmo em estresse máximo de 15 dias, as mudas obtiveram maior potencial hídrico que as de regime irrigado no verão.
O potencial hídrico permaneceu semelhante até os 10 dias de restrição hídrica, e apresentou diferença significativa apenas em estresse máximo, havendo uma redução de -0,18 MPa na cv. Crioula em comparação com o controle e -0,51 MPa para cv. Verdinha em relação ao seu controle. Houve diferença significativa também entre acessos, sendo que as planta do tratamento cv. Crioula manteve maior potencial hídrico em suas folhas.
Em relação a eficiência quântica potencial do PSII na antemanhã e durante a tarde, não houve alteração que indicasse danos no aparato fotossintético da planta em função do estresse hídrico.
Durante as avaliações realizadas no período de reidratação no inverno, foi possível notar uma queda acentuada da taxa fotossintética nos tratamentos controle e nas mudas submetidas ao estresse leve nos dois acessos. Essa baixa pode ser associada as condições de clima (Figura 3) que sofreram maior alteração nos últimos dias de avaliação, que ocasionou uma queda considerável na humidade relativa do ar e um aumento proeminente na radiação e DPV, além de um leve aumento de temperatura. Caindo de uma taxa fotossintética acima de 30 μmol CO2 m-2s-1 para menos de 20 μmol CO2 m-2s-1.
A condutância estomática manteve-se próxima à observada durante o estabelecimento do estresse para as mudas de controle, estresse leve e moderado. As plantas submetidas ao estresse máximo e reidratadas por dois dias elevaram os valores de condutância estomática de 0,12 e 0,09 mol m-2 s-1 para cv. Crioula e cv. Verdinha, respectivamente, para 0,26 mol m-2 s-1 em ambos acessos.
Os dados de transpiração mostraram maior equilíbrio durante a reidratação, sendo registrado um aumento nos dois últimos níveis de estresse e uma leve queda para as mudas de regime irrigado e estresse leve. Mesmo durante a reidratação o menor potencial hídrico foliar encontrado foi em níveis de estresse máximo de -0,66 e -0,70 MPa para as cv. Crioula e cv. Verdinha, nesta ordem. Apesar dessa baixa de potencial hídrico foliar, em nenhum momento este foi indicativo de estresse na planta.
Nogueira e Silva Junior (2001), avaliando genótipos de gravioleira sob condições naturais de cultivo observou taxa transpiratória máxima de 8,03 mmol H2O m-2 e potencial hídrico foliar de -0,67 MPa. Em trabalho realizado com plantas jovens de anona-blanca (Annona diversifolia Saff), Otero-Sánchez (2005) relacionou o potencial hídrico às trocas gasosas na planta, e no tratamento com potencial hídrico da folha igual a -0,43 MPa apresentou condutância estomática de 0,19 mol m-2 s-1, taxa transpiratória de 2,36 mmol H2O m-2 s-1 e taxa fotossintética de 3,80 μmol CO2 m-2 s-1, valores bem inferiores ao encontrados neste trabalho em plantas com o mesmo potencial hídrico foliar.
Os valores de Fv/Fm encontrados na antemanhã e no período da tarde foram semelhantes aos encontrados durante todo o trabalho, indicando que para anona o valor normal pode estar entre 0,70 e 0,80. Diferente do que foi indicado por Bolhar-Nordenkampf et al. (1989) e Do Carmo Araújo e Deminicis (2009) onde afirmam que os valores entre 0,75 e 0,85 são o mínimo necessário para permanecer na faixa de plantas saudáveis e livres de estresse.
A eficiência efetiva do PSII (ɸPSII) não indicou variações entre os acessos e os níveis. E o índice SPAD se manteve com os valores entre 40 e 47 para todos os tratamentos. Chiari Bertolli (2015) avaliou alterações fisiológica em espécie isohídraca pata-de-elefante por 54 dias em desidratação lenta e também não observou variação significativa para a eficiência efetiva do PSII (ɸPSII). Ribeiro (2002) encontrou valores normais entre 0,45 e 0,65 para a eficiência quântica efetiva do PSII (ɸPSII) em laranjeira ‘pera’.
CONCLUSÕES
O acesso de pinheira cv. Crioula apresentou maior deposição de cera nas folhas em comparação com a cv. Verdinha, mas não houve alterações fisiológicas que comprovassem maior adaptabilidade das primeiras em função da deposição de cera, sugerindo que as características de adaptação das pinheiras às condições de estresse hídrico sejam a nível celular.
As condições climáticas nas duas épocas de avaliação evidenciaram comportamentos fisiológicos diferenciados nas mudas de pinheira, que mesmo sendo uma planta tipicamente cultivada no semiárido apresentou maior desempenho fotossintético na época chuvosa.














