Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Arquivos de Medicina
versão On-line ISSN 2183-2447
Arq Med vol.27 no.1 Porto fev. 2013
ARTIGO DE REVISÃO
A importância dos biofilmes nas infeções nosocomiais – O estado da arte
Why Bio films are important in nosocomial in fections - the state of the art
A. Henriques1, C. Vasconcelos2, N. Cerca1
1IBB -Institute for Biotechnology and Bioengineering, Centre of Biological Engineering, University of Minho, Braga
2Serviço de pediatria, Centro Hospitalar S. João, Porto
RESUMO
As infeções nosocomiais são uma realidade constante no ambiente hospitalar. São responsáveis por um elevado número de casos de infeções e são notoriamente difíceis de erradicar. Um dos motivos pelos quais o tratamento das infeções nosocomiais é difícil deve-se ao facto de muitas destas infeções serem causadas por biofilmes microbianos. Os biofilmes podem ser definidos como comunidades de micro-organismos que vivem aderidos a uma superfície e envoltos numa complexa mistura de compostos tais como proteínas, polissacáridos e DNA extracelular. O crescimento de micro-organismos sob a forma de biofilmes dificulta a sua erradicação, pois estas estruturas podem ser consideradas adaptações dos micro-organismos, de forma a continuar no hospedeiro. É especialmente relevante ter em consideração as infeções causadas por biofilmes no contexto hospitalar, pois podem necessitar de abordagens diferentes para a sua erradicação. Este artigo de revisão tem como objetivo reunir o conhecimento existente do papel dos biofilmes microbianos nas infeções nosocomiais.
Palavras-chave: Biofilmes, infecções, nosocomial, resistência a antibióticos, staphylococcus aureus, staphylococcus epidermidis
ABSTRACT
Nowadays nosocomial infections are a reality in all hospital environments. They are the cause of a high number of infections, morbidity and mortality, and are recognised as being notoriously difficult to eradicate. One of the reasons for the problems in the treatment of nosocomial infection is the fact that many of the pathogens involved in this infections form biofilms. Biofilms are normally defined as communities of microorganisms adhered to a surface and surrounded by a polymeric matrix of extracellular components, such as proteins, polysaccharides and e DNA. The growth of microorganisms in biofilms makes their eradication difficult as this type of growth can be considered an adaptation of the pathogens in order to improve their persistence in the host. As such it is of special interest to account for the role of biofilms in nosocomial infections so that the appropriate approach can be taken in order to eradicate them. The aim of this article is to review the existing information on the prevalence of nosocomial infections potentially caused by biofilms.
Key-words: Biofilms. Infections, nosocomial, antibiotic resistance, staphylococcus aureus, staphylococcus epidermidis
1. O QUE SÃO INFEÇÕES NOSOCOMIAIS
O termo infeção nosocomial (do grego nosokomeion – local onde se tratam os doentes, hospital) é utilizado para definir infeções com origem hospitalar, ou seja, qualquer tipo de infeção adquirida pelo doente num hospital ou após a sua alta, se a infeção estiver diretamente relacionada com qualquer procedimento hospitalar, como é o caso de uma cirurgia.1 Nas últimas décadas passou a existir uma maior sensibilização do público em geral para este problema que é hoje reconhecido como um dos maiores flagelos mundiais, na área da saúde, com incidência em todo o mundo.2;3 O progresso científico tem aumentado a capacidade da comunidade médica em intervir em doentes mas também tem levado ao aumento involuntário do número de pacientes expostos a infeções nosocomiais.3-6
É reconhecido que a total erradicação das infeções nosocomiais é provavelmente impraticável,7 sendo que, em média, têm-se obtido reduções de cerca de 60%.8 Os cuidados para reduzir o elevado número de infeções nosocomais, envolvem desde medidas de qualificação da assistência hospitalar a medidas de vigilância sanitária, entre outras, tomadas tanto no âmbito local e como governamental.9-11 O impacto das doenças nosocomiais é enorme, em termos da saúde do paciente, assim como em aspetos sociais e económicos.3;5;8;11 para além do problema económico, a aquisição de infeções causadas por agentes patogénicos, que podem ter adquirido resistência a antibióticos, leva também à evolução de multirresistências que dificultam o tratamento dos doentes.1;12 O grande avanço das últimas décadas é o uso de material descartável e os métodos industriais de esterilização, que significaram constituem um grande progresso no controle das infeções.3 A criação de comissões para o controlo de infeções é hoje um requisito no sistema nacional de saúde em muitos países e inclui o desenvolvimento de sistemas de vigilância epidemiológica de infeções nosocomiais, reconhecido no relatório de 2005 da Direção Geral de Saúde sobre a prevalência de infeção.2
2. QUAL O PAPEL DOS BIOFILMES NAS INFEÇÕES
Há umas décadas atrás, o crescimento bacteriano era maioritariamente considerado como sendo planctónico, ou seja, numa suspensão em meio líquido.13 No entanto, hoje em dia, a maioria dos estudos reconhece que grande parte das populações bacterianas, independentemente do contexto em que se encontrem (ambiental, alimentar ou médico), tendem preferencialmente a formar agregados de várias espécies constituindo uma comunidade de micro-organismos.14;15 Esta comunidade, conhecida como biofilme, pode ser definida como um agregado de micro-organismos que crescem aderidos a uma superfície e revestidos de uma camada heterogénea de compostos extracelulares, definida como a matriz do biofilme.14 A formação de um biofilme numa superfície envolve várias etapas, sendo as principais a adesão inicial à superfície seguida da ligação intercelular, tal como representado na Figura 1.

2.1 Patofisiologia dos biofilmes
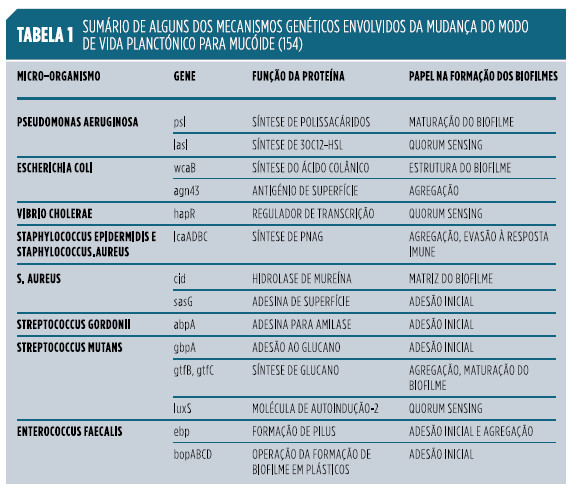
A passagem para um estilo de vida mucoide (associado ao biofilme) está muitas vezes relacionado com mudanças fenotípicas, como por exemplo, algumas bactérias deixam de possuir flagelos, necessários para uma mais ágil mobilidade.16;17 Estas estruturas estão normalmente associadas à existência planctónica, pois permitem às bactérias sobreviverem a condições adversas, deslocarem-se para evitar predadores e/ou procurarem nutrientes. Os mecanismos genéticos que acionam mudanças fenotípicas como a mudança do modo de vida planctónica para mucoide estão muitas vezes associados à densidade microbiana ou quorum Esta mudança de estilo de vida envolve uma complexa alteração de expressão genética que varia muito de espécie para espécie de bactérias, tal com descrito em diversos estudos.13;18-26 São muitos os mecanismos genéticos que regulam a passagem de células planctónicas para biofilmes,27-30 tal como exemplificado na Tabela 1.
Ao formarem uma comunidade de micro-organismos, as bactérias que vivem nos biofilmes passam a viver em grande proximidade com outras bactérias da mesma estirpe ou de espécies diferentes. Muitas desenvolveram mecanismos rudimentares de comunicação bacteriana, cujo fenómeno é conhecido por quorum sensing.31 De uma forma simplista, este fenómeno baseia-se no facto de certos membros do biofilme utilizarem a secreção de compostos metabólicos que vão agir como sinais de comunicação para os restantes membros da comunidade do biofilme.32 Inicialmente o quorum sensing foi descrito em bactérias Gram negativas, tendo recentemente já sido descrito que biofilmes compostos por bactérias Gram positivas, como o Staphylococcus aureus, também possuem esta capacidade.33
Uma das vantagens descritas do mecanismo de quorum sensing é a rápida adaptação a alterações ambientais.34 Outra vantagem evolutiva foi descrita como sendo possibilitar às populações de bactérias presentes no biofilme distinguirem self de nonself, isto é sentirem a densidade populacional de bactérias da mesma espécie/estirpe dentro de um biofilme que muitas vezes é composto por mais de um tipo de microorganimo.35 Esta capacidade de deteção da densidade ou quantidade de bactérias da mesma estirpe, através da concentração de produtos metabólicos segregados permite aos micro organismos gerir o seu metabolismo de forma a utilizar os recursos disponíveis mais eficientemente e também responder mais eficientemente a desafios, como por exemplo a agentes antimicrobianos,36 como discutido na secção seguinte.
2.2 Os biofilmes e a sua virulência
2.2.1 Adesão inicial
Um dos principais fatores de virulência dos biofilmes é a capacidade dos micro-organismos que o compõem de aderir a superfícies inertes, e de especial importância, de aderirem e colonizarem material médico invasivo como são é o caso dos cateteres, próteses ou pacemakers.37 Para as bactérias, a adesão a superfícies inertes é, em primeiro lugar, um mecanismo de sobrevivência.38 No entanto, é também um fator de virulência muito importante para as bactérias, uma vez que este passo promove a produção e secreção de moléculas como polissacáridos, proteínas e ácidos nucleicos que farão parte da matriz que envolve o futuro biofilme.38 Estas superfícies têm muitas vezes características de hidrofobicidade ou polaridade que favorecem a sua colonização por micro-organismos favorecendo a formação de biofilmes.39;40
2.2.2 Mecanismos de resistência antimicrobiana
Com a maturação do biofilme, este frequentemente adota uma forma tridimensional e heterogénea, tendo impacto direto na sua virulência. O caso mais estudado deste aumento de virulência prende-se com a resistência a antibióticos, cujos mecanismos ainda não claros aparentam ter origens múltiplas.41
Embora seja clara esta resistência ou tolerância aos antibióticos, até à data ainda pouco se sabe sobre os mecanismos de resistência dos biofilmes aos mesmos, sendo que parecem estar relacionados tanto com a sua estrutura como com alterações fisiológicas dos micro-organismos.7;42;43 Segundo diversos autores, as causas que têm sido descritas como responsáveis pela resistência são: a penetração limitada do agente antibiótico pela matriz do biofilme,44 a alteração da taxa de crescimento dos micro-organismos que compõem o biofilme41 assim como outras alterações fisiológicas, incluindo a expressão de possíveis genes de resistência.45
Muitas das infeções causadas por biofilmes são especialmente difíceis de erradicar, transformando-se em infeções recorrentes.7;14 Atualmente é largamente reconhecido o aumento da resistência a múltiplos antibióticos e, quando nos referimos a biofilmes, este problema é especialmente grave.46 Vários estudos compararam diretamente a taxa de morte de bactérias em suspensão e em biofilme, sendo que os biofilmes apresentaram elevadas taxas de resistência a vários antibióticos.46-52
As primeiras evidências indicavam que a própria estrutura tridimensional dos biofilmes, rodeados pela matriz extracelular, funcionaria como uma barreira para a penetração dos antibióticos, resultando num aumento da resistência.53-55 No entanto, hoje já é conhecido que a barreira difusiva dos biofilmes apenas contribui para uma fração dos casos descritos de resistência a antibióticos.56;57
2.2.3 Taxa de crescimento das bactérias que compõe os biofilmes
Uma das características dos biofilmes com implicações neste aumento da resistência está associada às diferentes taxas de crescimento dos micro-organismos que o compõem.58 Isto é relevante pois os micro-organismos que constituem os biofilmes não têm uma taxa de crescimento sincronizada, existindo uma diversidade de populações em diferentes fases do ciclo celular, o que torna mais difícil a sua erradicação completa por antibióticos,59 especialmente aqueles que estão dependentes da multiplicação microbiana. A fração de bactérias do biofilme, cujo ritmo metabólico é muito lento44;60 consegue desta forma resistir (e persistir) a tratamentos com agentes antimicrobianos. Estas populações podem ser classificadas como dormentes (células não cultiváveis) ou persistentes (células com um fenótipo mais resistente devido ao seu baixo metabolismo).61
2.2.4 O sistema imune e as Infeções causadas Por biofilmes
A estrutura dos biofilmes também já foi implicada no aumento da resistência à resposta imune do hospedeiro. Recentemente, foi descrito que um biofilme de Staphylococcus epidermidis, composto de forma heterogénica por células ativas, dormentes, ou mortas, é mais resistente ao ataque pelo sistema imunitário, em particular macrófagos.62;63 A resistência de biofilmes de S. epidermidis ao sistema imune tem vindo a ser associada à heterogeneidade e à matriz do biofilmes.64;65 O mesmo foi descrito para biofilmes de S. aureus.66
Um outro exemplo da influência do sistema imune na formação de biofilmes são os casos da fibrose cística e da doença pulmonar obstrutiva crónica (DpOc), onde alterações estruturais nos pulmões do hospedeiro, causado por uma alteração da resposta imune, favorecem a formação de biofilmes de micro-organismos como de Pseudomonas aeruginosa.67 De facto, foi descrito que a produção de alginato em biofilmes de P. aeruginosa é mais importante para a resistência do biofilme ao ataque pelo sistema imunitário do que para a formação do próprio biofilme.68
2.2.5 O papel da estrutura dos biofilmes na persistência da Infecção
Como foi referido anteriormente, a matriz dos biofilmes tem um papel preponderante na fisiologia destasestruturas.69-71 Alguns dos compostos que estão presentes nesta matriz são proteínas, polissacáridos, lípidos e ácidos nucleicos,72 variando frequentemente com as condições ambientais. A presença de proteínas é de extrema importância uma vez que já foi descrito que a sua presença pode alterar a atividade antimicrobiana de alguns antibióticos73 e, daí esta composição da matriz potencia a resistência dos micro-organismos que compõem o biofilme aos agentes antimicrobianos.69;70
A matriz assume ainda um papel mais importante quando se tem em consideração a presença de material genético (ácidos nucleicos) na sua composição.74 Estes componentes, juntamente com o aumento na proximidade das bactérias que compõem estas estruturas, aumentam a probabilidade de aquisição de novo material genético entre estirpes.75
Tomemos o exemplo dos biofilmes compostos por P. aeruginosa, que são reconhecidos como difíceis de tratar e causadores de infeções persistentes. Estas bactérias segregam compostos, a que podemos chamar fatores de virulência, como é o caso do pigmento ciânico, que eliminam bactérias de espécies semelhantes de forma a favorecer o crescimento das bactérias no biofilme que o estão a produzir, anulando a concorrência para a utilização de nutrientes.76 possuem ainda a capacidade de produção e secreção de ramnolipídeos que fazem parte do seu arsenal de compostos utilizados para quorum sensinge que lhe permite serem mais eficazes a colonizarem superficies como tubos endotraqueais e cateter venosos, para iniciarem uma infeção.77
Porque os mais diversos micro-organismos têm desenvolvido mecanismos extremamente eficazes para a colonização e persistência em dispositivos médicos (sumarizados na (Tabela 2) que são de utilização comum no dia a dia das intervenções hospitalares, muitos autores recomendam que a melhor abordagem ao controlo das infeções nosocomiais causadas por biofilmes passa pelo controlo da fonte da infeção, optando assim primariamente pela remoção do material invasivo com o forma de resolver a infeção.78

3. EXEMPLOS DE BIOFILMES NOSOCOMIAIS
Muitas infeções nosocomiais são causadas por estirpes de bactérias como por exemplo S. epidermidis, S.aureus, P.aeruginosa, espécies de Candida sp., Escherichia coli, entre outros, que são conhecidas pelas suas capacidades de formação de biofilmes.79-82 Um dos entraves à erradicação de biofilmes nosocomiais é compreender que os resultados de suscetibilidades a antibióticos tradicionalmente obtidos em laboratório são principalmente feitos em células em suspensão e não num biofilme, onde outras considerações têm de ser tomadas em conta como a permeabilidade dos biofilmes e a natureza mista destas estruturas, onde não existe apenas uma única estirpe de bactérias.7 isto significa que o tratamento de infeções nosocomiais causadas por biofilmes, com antibioterapia baseada em resultados laboratoriais clássicos terá certamente dificuldade em erradicar totalmente o biofilme, o que poderá levar à infeção recorrente.83
Existem muitos exemplos práticos de biofilmes causadores de doenças nosocomiais, nomeadamente a pneumonia associada ao ventilador.84 A pneumonia bacteriana de origem nosocomial ocorre tipicamente entre as 48 e 72 horas após a admissão num hospital e pode ser dividida em 2 subtipos: pneumonia associada ao uso de ventiladores, e pneumonia não-associada ao uso de ventiladores.4;84 O aparecimento de pneumonia facilmente duplica o período de hospitalização5;85 Um estudo realizado nos Estados Unidos da América revelou que o custo de tratamento da pneumonia associada ao uso de ventiladores custa em média 40 mil dólares por doente.86 A prevalência de pneumonia em lares de terceira idade também é alta, podendo totalizar 13-48% de todas as infeções nesse contexto.5;86 A cavidade oral é um reservatório importante de bactérias que podem causar infeções pulmonares.87 A presença de placa dentária, um conhecido biofilme com múltiplas espécies bacterianas, também influencia o início e progressão da pneumonia por causa da aspiração de bactérias do biofilme para o aparelho respiratório.86;87 No total, a mortalidade associada a pneumonia nosocomial estima-se em cerca de 25%.86;88;89
Enquanto que as pneumonias de origem não nosocomial são principalmente causadas por estirpes como Streptococcus pneumoniae, Haemophilus influenzae, e Mycoplasma pneumoniae, já na pneumonia nosocomial são isolados organismos frequentemente associados à cavidade oral como P. aeruginosa, S. aureus, e bactérias entéricas Gramnegativas.4;86 O percurso mais provável para a colonização do aparelho respiratório com bactérias normalmente encontradas na cavidade oral é feito pela micro-aspiração das bactérias presentes nos biofilmes orais que são aspiradas para o aparelho respiratório.86;90 Do ponto do vista microbiológico, a pneumonia precoce (presente no momento da entubação ou então logo após incubação) é caracterizada pela presença de espécies bacterianas como por exemplo o H. influenza, S aureus sensíveis à oxacilina e Strep. pneumoniae, enquanto a pneumonia tardia é caracterizada pela presença de alguns micro-organismos resistentes a antibioterapia como os MRSA, P. aeruginosa, Acinetobacter spp. e Enterobacter spp.91;92
Um outro caso onde os biofilmes representam um papel importante na doença está relacionado com as infeções do trato urinário.93 Atualmente, são a primeira ou segunda causa mais frequente de infeções nosocomiais.94 A utilização de cateteres urinários tornou-se comum nas últimas décadas, e utilizações que anteriormente eram breves e temporárias, passaram a ser de prazo mais alargado.95 A utilização frequente e por vezes desnecessária deste tipo de dispositivos aumenta o risco para os doentes do desenvolvimento de infeções, como as infeções urinárias que por vezes progridem para infeções mais graves como é o caso das urosepsis.96;97
Estirpes de micro-organismos frequentemente associadas a infeções urinárias são Proteus mirabilis e E. coli.95 No caso de P. mirabilis, já foi descrito que este possui um conjunto de genes de virulência associados à produção eficiente de biofilmes persistentes que o tornam especialmente bem adaptado para sobrevivência e proliferação no ambiente existente no sistema urinário.15 Segundo o relatório de 2005 da Direção Geral de Saúde, que reporta o estado das infeções nosocomiais em Portugal em 2003, as infeções em que E. coli foi identificada como responsável perfazem cerca de 15% de todas as infeções nos ocomiais.2 As estirpes de E. coli consideradas uropatogénicas, já foram descritas como capazes de formar biofilmes, o que contribui para a sua persistência e dificuldade de erradicação do aparelho urinário.93;98 O aumento da ocorrência de infeções urinárias com micro-organismos resistentes ao tratamento com antibióticos, aliado à dificuldade de erradicação de microorganismos causadores destas infeções devido à sua capacidade de formação de biofilmes, tem tornado este tipo de infeções um dos maiores desafios no tratamento de infeções nosocomiais.96
Outra das estirpes de bactérias muito estudada no campo dos biofilmes nosocomiais são os biofilmes de S. epidermidis, que conseguem facilmente colonizar dispositivos médicos como cateteres e causar infeções persistentes.43 O grupo de Staphylococcus coagulase negativos (SCN), no qual se insere S. epidermidis, são os micro-organismos causadores de infeção em 48-67% de pacientes com shunts do sistema nervoso central, e responsáveis por 50-70% das infeções associadas à utilização de cateteres.99 Os SCN também estão descritos como responsáveis por 40-50% das infeções de válvulas cardíacas100 e responsáveis por 20-50% das infeções resultantes de cirurgias de substituição de articulações.101 Um dos motivos que tem vindo a ser apontado pelo qual S. epidermidis é dos mais frequentes causadores de infeções por biofilmes prende-se com o facto de o reservatório deste micro-organismo ser a pele e membranas mucosas do ser humano.42;102;103 De facto, S. epidermidis foi considerado durante muito tempo como um organismo comensal, ou até mesmo benéfico para o ser humano, impedindo a colonização por parte de outros micro-organismos patogénicos.102 No entanto, estudos genéticos identificaram certos marcadores de virulência (operão icaABDC) presentes em isolados clínicos de origem nosocomial, ausentes nos isolados que normalmente habitam a flora humana,42;104 sugerindo a aquisição de fatores de virulência nas estirpes nosocomiais. O operão icaABDC também está presente em S. aureus,105 um conhecido patogéneo humano que, para além de causar infeções por biofilmes, possui um vasto leque de toxinas e pode causar, entre outros, endocardite aguda, pneumonia e é o responsável pelo síndrome do choque tóxico.106 A aquisição de novos fatores de virulência por bactérias que formam biofilmes foi inicialmente identificada em biofilmes orais.107 Existe também alguma evidência de possível transmissão horizontal de fatores de virulência relacionados com biofilmes em Staphyloccous spp.,108 pelo que é possível que a aquisição do operão icaABDC por isolados nosocomiais de S. epidermidis tenha tido origem no micro-organismo tradicionalmente virulento S. aureus.109
4. PREVALÊNCIA DE INFEÇÕES NOSOCOMIAIS DERIVADAS DE BIOFILMES A NÍVEL MUNDIAL
Estima-se que os biofilmes são a causa de uma grande percentagem de infeções nosocomiais.110 O facto é que uma grande parte destas infeções, nos EUA (cerca de 60%), são causadas pela utilização de dispositivos médicos ouimplantes cirúrgicos,como por exemplo válvulas cardíacas, pacemakers cardíacos, cateteres urinários, lentes de contacto, entre muitos outros.94;111
De acordo com a Organização mundial de Saúde, a qualquer altura existem mais de 1.4 milhões de pessoas doentes com infeções nosocomiais, representando entre 5 e 10% de todos os doentes admitidos em hospitais em países desenvolvidos e até 25% em países em desenvolvimento.112 Dessas infeções, 26% são infeções associadas ao sistema urinário, 20% são infeções de feridas cirúrgicas, 12% são resultado de pneumonia e 11% bacteriemias (dados de 2007).113 Um relatório da União Europeia da mesma altura registou cerca de 3 milhões de infeções nosocomiais das quais resultaram 50 mil mortes durante um ano.114
Embora nos dias de hoje exista um grande número de estudos sobre a prevalência de infeções nosocomiais a nível mundial,112;115-121 ou sobre a capacidade de micro-organismos causadores de doenças nosocomiais possuírem a capacidade de formar biofilmes, a relação direta entre os dois fenómenos (infeções nosocomiais e biofilmes) ainda não é investigada frequentemente.43;94;122;123 A maioria das publicações refere prevalências gerais de infeções nosocomiais, mas a percentagem destas infeções de facto atribuídas ao crescimento de biofilmes é desconhecida.124 Atualmente apenas podemos especular sobre possíveis casos de infeções nosocomiais causadas por biofilmes, usando como base o agente causador da infeção e a sua capacidade para formar biofilmes.45
Tomemos por exemplo o méxico, onde recentemente foi publicado um artigo sobre a prevalência de infeções nosocomiais em unidades de cuidados intensivos neonatais.125 Durante o período do estudo, a incidência de infeções nosocomiais na unidade de cuidados intensivos neonatais era cerca de 20%, sendo que destas infeções 30,4% estavam associadas a um cateter do sistema venoso central e 63.6% estavam associadas a pneumonias em doentes com ventilação assistida.125 Os três principais agentes infeciosos encontrados neste estudo foram S. epidermidis (37.1%), Enterococcus faecalis (14.8%), E. coli (11.1%). todas estas estirpes já foram anteriormente descritas como associadas à formação de biofilmes nosocomiais.3;42;93;125-127
Recentemente foi também publicado outro estudo sobre a prevalência de infeções nosocomiais em unidades de cuidados intensivos no Este da china.128 Uma vez mais, os micro-organismos descritos como causadores destas infeções eram todos potenciais formadores de biofilmes: P. aeruginosa, E. coli, S. epidermidis, S. aureus, Klebsiella pneumoniae, entre outros,128 mas neste estudo não foram testadas as capacidades de formação de biofilme desses isolados. Com valores de prevalência de infeções nosocomiais (3 a 27%) ligeiramente superiores à prevalência descrita para unidades semelhantes em países desenvolvidos (7.7 a 16.5%), é, no entanto, comparável às prevalências descritas para países da América do Sul (como a Argentina e o Brasil) e ligeiramente mais baixa que a taxa de prevalência descrita para a Índia.115;129
Em Portugal tem havido um aumento da consciencialização dos profissionais de saúde para uma prática clínica segura desde há muitos anos, seguindo primariamente as chamadas precauções padrão e as recomendações do centre for Disease control (cDc) de 19871;130 e utilizando sistematicamente barreiras apropriadas e técnicas que reduzam a probabilidade de exposição e infeção cruzada. Foi também criado um programa Nacional de controlo de infeção para dinamizar o combate à infeção nas instituições prestadoras de cuidados de saúde. Num documento do ministério da Saúde português intitulado infecção Nosocomial em Portugal: diagnóstico da situação/linhas de ação prioritárias2 é referido que em 2003 a prevalência de doenças nos ocomiais era de 8.4% nos doentes hospitalizados e cerca de 22.7% dos doentes já eram portadores de infeção na altura em que foram internados. Desta forma, cerca de 31% dos doentes no hospital constituem um risco de transmissão de infeção, no entanto a maioria destas infeções é causada pela flora microbiana endógena do doente ou por micro-organismos transmitidos no ambiente hospitalar.
Num estudo sobre boas práticas hospitalar, foi sugerido que a forma de funcionamento do hospital em causa (hospital Universitário de coimbra) poderia levar ao aumento da transmissão de infeções, uma vez que as taxas de ocupação das enfermarias seria muito elevada e os médicos e enfermeiros trabalhariam muitas vezes em rotatividade entre as urgências e o internamento.1 O mesmo estudo refere que os S. aureus resistentes à meticilina (MRSA) foram o micro-organismo mais frequentemente isolado em cultura, mesmo após a resolução clínica da infeção, a manutenção de culturas positivas foi, segundo interpretação dos autores, um indício de passagem de colonização em vários doentes.1 No entanto, este estudo não previu a possibilidade da formação de biofilmes. Na nossa perspetiva, esta é uma justificação igualmente plausível à indicada, devido às características dos biofilmes, aqui discutidas, nomeadamente a alta resistência aos antibióticos, resultante em infeções recorrentes e persistentes.7;12;42;43;93;126
Os MRSA são uma das estirpes causadoras de infeções nosocomiais que mais preocupações traz aos profissionais de saúde, devido à redução das alternativas terapêuticas.3;6;10;84;131 Neste momento estão identificadas 5 principais linhagens de MRSA no mundo: ibérica, Brasileira, húngara, Nova iorque/Japão, e pediátrica, responsáveis por surtos se infeções.132;133 O complexo clonal Brasileiro já foi detetado em muitos países, como a Argentina,134 Uruguai, Paraguai, chile, portugal,135 itália136 e República checa,137 e a sua disseminação parece o resultado da capacidade colonizadora das mucosas humanasedapele.84;138 Um estudo recente verificou que os membros deste complexo clonal de MRSA Brasileiro possuíam, invitro, uma maior capacidade de formar biofilmes, entre 3 a 4 vezes superior comparadas com estirpes de MRSA que não faziam parte de um complexo clonal causador de surtos de infeção.84 O facto de estas estirpes, com uma maior virulência, possuírem uma maior capacidade de formar biofilmes demonstra que o papel dos biofilmes em infeções nosocomiais pode estar principalmente relacionado com a sua capacidade de persistência e a dificuldade de tratamento devido às limitações causadas pela permeabilidade da matriz de polímeros que envolve as estirpes que compõem o biofilme.7;12;42
5. PREVENÇÃO E TRATAMENTO DE INFEÇÕES NOSOCOMIAIS CAUSADAS POR BIOFILMES
Um dos principais objetivos das terapêuticas antimicrobianas, sejam elas por infeções causadas por biofilmes ou não, é a redução da utilização de anti-bióticos através da sua utilização mais racional. Esta utilização implica reconhecer quais os agentes anti-microbianos mais eficientes para as diferentes situações e, como tal, existem agentes com um maior potencial para eficácia no tratamento de infeções causadas por biofilmes. O tratamento eficaz de infeções causadas por biofilmes passa não só pela escolha acertada do antibiótico a utilizar, mas também da concentração e período de tratamento. Ensaios clássicos de determinação de resistência antimicrobiana, como a determinação da concentração mínima inibitória, não são adequados para aferir da resistência dos biofilmes.47;65;139-142 Estudos recentes demonstraram que a utilização da azitromicina em concentrações sub-óptimas (abaixo do necessário para um efeito bacteriocida), para além de impedir a eliminação completa da infeção tem como consequência a seleção de bactérias com fenótipos resistentes que prevalecem e passam a ser as maiores fontes de infeção.143;144 É relevante também notar que concentrações subótimas de fluoroquinolonas foram consideradas úteis como profilaxia para impedir a formação de biofilmes de S. epidermidis.145 No entanto, existe a possibilidade de aumentar a pressão seletiva para a expansão de clones de bactérias resistentes ao antibiótico usado.7
A importância da resistência dos biofilmes aos antibióticos apresenta um duplo desafio no futuro próximo. Por um lado, novas terapias antimicrobianas necessitam de ser encontradas, tais como a utilização de novas superfícies médicas revestidas com compostos que inibem a formação de biofilme 146-148 ou a utilização de vírus específicos contra bactérias (bacteriofágos) com ação contra biofilmes.139;149-152 Estas novas estratégias promissoras poderão resultar numa diminuição significativa das infeções nosocomiais por biofilmes. No entanto, com um expectável aumento de pacientes internados nos hospitais, deverá haver cada mais uma consciencialização por parte dos profissionais de saúde no tratamento destas infeções, nomeadamente no que diz respeito às condições de assepsia e do tratamento abusivo com antibióticos, indicado como o principal responsável pelos recentes aumentos de microorganismos com resistências a antibióticos.153
Uma abordagem mais abrangente para o controlo da infeção passará necessariamente, pela remoção precoce dos dispositivos médicos de forma a controlar possíveis fontes de infeção, uma vez que o tratamento de infeções causadas por biofilmes nem sempre é eficaz como discutido anteriormente. O avanço da tecnologia médica e do desenvolvimento de dispositivos médicos mais resistentes à colonização microbiana e mais eficientes (que possam reduzir o tempo necessário para a resolução do problema) serão certamente um dos fatores mais importantes na abordagem ao tratamento e prevenção de infeções nosocomiais, assim como aprevenção da infeção e a profilaxia com os antibióticos e dosagem correta.145
A consciencialização de equipas médicas e de investigação científica para a prevalência de biofilmes. Nos casos de infeções nosocomiais no nosso país, permitirá no futuro um tratamento de doentes mais eficaz e um esforço da comunidade científica mais focado nos problemas práticos, com o objetivo da redução da incidência e mortalidade destas infeções.
AGRADECIMENTO
A. Henriques tem uma bolsa de pós-doutoramento financiada por fundos europeus e nacionais no âmbito do projeto com referência PTDC/BIA-MIC/098228/2008 (FCOMP-01-0124-FEDER-008991).
REFERÊNCIAS
1. Palavra F, Gens H, Fernandes C, et al. [Healthcare associated infection: emerging problem in a neurology department]. Acta med port 2010 July;23(4):613-24. [ Links ]
2. Instituto Nacional de Saúde Dr.Ricardo Jorge. Relatório de prevalência de infecção 2003. 2005. [ Links ]
3. Sydnor ER, Perl TM. Hospital epidemiology and infection control in acute-care settings. Clin Microbiol Rev 2011 January; 24(1):141-73. [ Links ]
4. Zeitoun SS, De Barros Al, Diccini S, et al. [Incidence of ventilator-associated pneumonia in patients using open-suction systems and closed-suction systems: a prospective study - preliminary data]. Rev Lat Am Enfermagem 2001 January;9(1):46-52. [ Links ]
5. El-Solh AA, Niederman Ms, Drinka P. Management of pneumonia in the nursing home. Chest 2010 December;138(6):1480-5. [ Links ]
6. Rasmussen RV, Fowler VG, Jr., Skov R, et al. Future challenges and treatment of Staphylococcus aureus bacteremia with emphasis on mrsa. Future microbiol 2011 January;6(1):43-56. [ Links ]. Future microbiol 2011 January;6(1):43-56.
7. Bryers JD. Medical biofilms. Biotechnol Bioeng 2008 may 1;100(1):1-18. [ Links ]
8. Pronovost P, Needham D, Berenholtz S, et al. An intervention to Decrease catheter-Related Bloodstream infections in the icu. N Engl J med 2006;355(26):2725-32. [ Links ]
9. Alp E, Leblebicioglu H, Doganay M, et al. Infection control practice in countries with limited resources. Ann clin microbiol Antimicrob 2011;10:36. [ Links ]
10.Dulon M, Haamann F, Peters C, et al. Mrsa prevalence in European healthcare settings: a review. Bmc infect Dis 2011;11:138. [ Links ]
11. Flanagan E, chopra t, mody l. Infection prevention in alternative health care settings. Infect Dis clin North Am 2011 march;25(1):271-83. [ Links ]
12. Smith K, Hunter Is. Efficacy os coommon hospital biocides with biofilms of multi-drug resistant clinical isolates. J med microbiol 2008;57:966-73. [ Links ]
13. Davey M, Otoole G. Microbial biofilms: from ecology to molecular genetics. Microbiology and molecular Biology Reviews 64, 847-867. 2000. [ Links ]
14. Costerton JW, Stewart PS, Greenberg Ep. Bacterial biofilms: a common cause of persistent infections. Science 1999 may 21;284(5418):1318-22. [ Links ]
15. Jacobsen SM, Shirtliff ME. Proteus mirabilis biofilms and catheter-associated urinary tract infections. Virulence 2011 September;2(5):460-5. [ Links ]
16. Sauer K, Camper AK, Ehrlich GD, et al. Pseudomonas aeruginosa displays multiple phenotypes during development as a biofilm. J Bacteriol 2002 february;184(4):1140-54. [ Links ]
17. Sauer K, camper A. Characterization of phenotypic changes in pseudomonas putida in responde to surface-associated growth. Journal of Bacteriology 183, 6579-6589. 2001. [ Links ]
18. Agladze K, Wang X, Romeo T. Spatial periodicity of Escherichia coli K-12 biofilm microstructure initiates during a reversible, polar attachment phase of development and requires the polysac¬charide adhesin pga. J Bacteriol 2005 December;187(24):8237-46. [ Links ]
19. Balaban N, Giacometti A, Cirioni O, et al. Use of the quorum-sensing inhibitor rnaiii-inhibiting peptide to prevent biofilm formation in vivo by drug-resistant Staphylococcus epidermidis. Journal of infect Diseas 187, 625-630. 2003. [ Links ]
20. Boles BR, Thoendel M, Roth AJ, et al. Identification of genes involved in polysaccharide-independent Staphylococcus aureus biofilm formation. Plos One 2010;5(4):e10146. [ Links ]
21. Cafiso V, Bertuccio T, Santagati M, et al. Agr-Genotyping and transcriptional analysis of biofilm-producing Staphylococcus aureus. Fems immunol med microbiol 2007 October;51(1):220-7. [ Links ]
22. Conlon Km, Humphreys H, Ogara JP. Icar encodes a transcriptional repressor involved in environmental regulation of ica operon expression and biofilm formation in Staphylococcus epider¬midis. J Bacteriol 2002 August;184(16):4400-8. [ Links ]
23. Conlon Km, Humphreys H, Ogara JP. Inactivations of rsbu and sara by is 256 represent novel mechanisms of biofilm phenotypic variation in Staphylococcus epidermidis. J Bacteriol 2004 September;186(18):6208-19. [ Links ]
24. Corona-izquierdo FP, Membrillo-hernandez J. A mutation in rpos enhances biofilm formation in Escherichia coli during exponential phase of growth. Fems microbiol lett 2002 may 21;211(1):105-10. [ Links ]
25. Costerton JW, Montanaro L, Arciola CR. Biofilm in implant infections: its production and regulation. Int J Artif Organs 2005 November;28(11):1062-8. [ Links ]
26.Handke L, Conlon K, Slater S, et al. Genetic and phenotypic analysis of biofilm phenotypic variotion in multiple Staphylococcus epidermidis isolates. Journal of medical microbiology 53, 367¬374. 2004. [ Links ]
27. Ogara JP. Ica and beyond: biofilm mechanisms and regulation in Staphylococcus epidermidis and Staphylococcus aureus. Fems microbiol lett 2007 may;270(1):179-88. [ Links ]
28. Wood TK. Insights on Escherichia coli biofilm formation and inhibition from whole-transcriptome profiling. Environ microbiol 2009 January;11(1):1-15. [ Links ]
29. Eberl L, Riedel K. Mining quorum sensing regulated proteins -Role of bacterial cell-to-cell communication in global gene regulation as assessed by proteomics. Proteomics 2011 August;11(15):3070-85. [ Links ]
30. Smith EG, Spatafora GA. Gene regulation in S. Mutans: complex control in a complex environment. J Dent Res 2012 february;91(2):133-41. [ Links ]
31. Nadell CD, Xavier JB, Levin SA. The Evolution of Quorum Sensing in Bacterial Biofilms. Plos Biology 2008;6(1):171-9. [ Links ]
32. Kiran MD, Adikesavan NV, Cirioni O, et al. Discovery of a quorum-sensing inhibitor of drug-resistant staphylococcal infections by structure-based virtual screening. Mol Pharmacol 2008 may;73(5):1578-86. [ Links ]
33. Antunes LC, Ferreira RB, Buckner MM, et al. Quorum sensing in bacterial virulence. Microbiology 2010 August;156(pt 8):2271-82. [ Links ]
34. Otto M. Quorum-sensing control in Staphylococci -a target for antimicrobial drug theraphy? Fems microbiol lett 2004;241:135-41. [ Links ]
35. Novick Rp, Geisinger E. Quorum sensing in staphylococci. Annu Rev Genet 2008;42:541-64. [ Links ]
36. Jayaraman A, Wood Tk. Bacterial quorum sensing: signals, circuits, and implications for biofilms and disease. Annu Rev Biomed Eng 2008;10:145-67. [ Links ]
37. Pavithra D, Doble M. Biofilm formation, bacterial adhesion and host response on polymeric implants-issues and prevention. Biomed mater 2008 September;3(3):034003. [ Links ]
38. Busscher HJ, Mei HC. How do bacteria know they are on a surface and regulate their response to an adhering state? Plos pathog 2012 January;8(1):e1002440. [ Links ]
39. Talsma SS. Biofilms on medical devices. Home healthc Nurse 2007 October;25(9):589-94. [ Links ]
40. Azeredo J, Oliveira R. The role of hydrophobicity and exopolymers in initial adhesion and biofilm formation. In: Stoodley p, lens p, moran A, mahony t, oflaherty S, editors. Biofilms in medicine, industry and Environmental Biotechnology -characteristics, Analysis and control.london: iwa publishing; 2003. P. 16-31. [ Links ]
41. Lewis K. Riddle of biofilm resistance. Antimicrob Agents chemother 2001 April;45(4):999-1007. [ Links ]
42. Otto M. Staphylococcal biofilms. Curr top microbiol immunol 2008;322:207-28. [ Links ]
43. Schoenfelder SMK, Lange C, Eckart M, et al. Success through diversity -how Staphylococcus epidermidis establishes as a nosocomial pathogen. International Journal of medical microbiology 2010;300:380-6. [ Links ]
44. Mah TF, Otoole GA. Mechanisms of biofilm resistance to antimicrobial agents. Trends microbiol 2001 January;9(1):34-9. [ Links ]
45. Donlan Rm, Costerton JW. Biofilms: survival mechanisms of clinically relevant microorganisms. Clin microbiol Rev 2002 April;15(2):167-93. [ Links ]
46. Stewart P, Costerton J. Antibiotic resistance of bacteria in biofilms. Lancet 358, 135-138. 2001. [ Links ]
47. Cerca N, Martins S, Cerca F, et al. Comparative assessment of antibiotic susceptibility of coagulase-negative staphylococci in biofilm versus planktonic culture as assessed by bacterial enumera¬tion or rapid Xtt colorimetry. J Antimicrob chemother 2005 August;56(2):331-6. [ Links ]
48. Anderl J, Franklin M, Stewart P. Role of antibiotic penetration limitation in Klebsiella pmeumoniae biofilm resistance to ampicillin and ciprofloxacin. Antimicrobl Agents chemother 44, 1818-1824. 2000. [ Links ]
49. Hoyle BD, Costerton J. Bacterial resistance to antibiotics: the role of biofilms. Prog Drug Res 37, 91-105. 1991. [ Links ]
50. Klingenberg C, Aarag E, Ronnestad A, et al. Coagulase-negative Staphylococcal sepsis in neonates: association between antibiotic resistance, biofilm formation and the host inflammatory response. Pediatr infect Dis J 2005 September;24(9):817-22. [ Links ]
51. Mulcahy H, Charron-mazenod L, Lewenza S. Extracellular DNA chelates cations and induces antibiotic resistance in pseudomonas aeruginosa biofilms. Plos Pathog 2008 November;4(11):e1000213. [ Links ]
52. Oconnell HA, Kottkamp GS, Eppelbaum JL, et al. Influences of biofilm structure and antibiotic resistance mechanisms on indirect pathogenicity in a model polymicrobial biofilm. Appl Environ microbiol 2006 July;72(7):5013-9. [ Links ]
53. De Beer D, Srinivasan R, Stewart ps. Direct measurement of chlorine penetration into biofilms during disinfection. Appl Environ microbiol 1994 December;60(12):4339-44. [ Links ]
54. Hoyle BD, Alcantara J, Costerton JW. Pseudomonas aeruginosa biofilm as a diffusion barrier to piperacillin. Antimicrob Agents chemother 1992 September;36(9):2054-6. [ Links ]
55. Suci PA, Mittelman MW, Yu FP, et al.investigation of ciprofloxacin penetration into pseudomonas aeruginosa biofilms. Antimicrob Agents chemother 1994 September;38(9):2125-33. [ Links ]
56. Canton R, Morosini MI. Emergence and spread of antibiotic resistance following exposure to antibiotics. Fems microbiol Rev 2011 September;35(5):977-91. [ Links ]
57. Martinez Jl, Rojo F. Metabolic regulation of antibiotic resistance. Fems microbiol Rev 2011 September;35(5):768-89. [ Links ]
58. Gilbert P, Collier PJ, Brown MR. Influence of growth rate on susceptibility to antimicrobial agents: biofilms, cell cycle, dormancy, and stringent response. Antimicrob Agents chemother 1990 October;34(10):1865-8. [ Links ]
59. Keren I, Kaldalu N, Spoering A, et al. Persister cells and tolerance to antimicrobials. Fems microbiol lett 2004 January 15;230(1):13-8. [ Links ]
60.Keren I, Shah D, Spoering A et al.Specialized persister cells and the mechanism of multidrug tolerance in Escherichia coli. J Bacteriol 2004 December;186(24):8172-80. [ Links ]
61. Lewis K. Persister cells, dormancy and infectious disease. Nat Rev microbiol 2007;5:48-55. [ Links ]
62. Cerca F, Andrade F, França A, et al. Staphylococcus epidermidis biofilms with higher proportions of dormant bacteria induce a lower activation of murine macrophages. J med microbiol 2011;60:1717-24. [ Links ]
63.Shiau Al, Wu Cl. The inhibitory effect of staphylococcus epidermidis slime on the phagocytosis of murine peritoneal macrophagesis interferon-independent. Microbiol immunol 1998;42(1):33-40. [ Links ]
64. Vuong C, Kocianova S, Voyich JM, et al. A crucial role for exopolysaccharide modification in bacterial biofilm formation, immune evasion, and virulence. J Biol chem 2004 December 24;279(52):54881-6. [ Links ]
65. Cerca N, Jefferson K, Oliveira R, et al. Comparative antibody-mediated phagocytosis of staphylococcus epidermidis cells grown in a biofilm or in the planktonic state. Infect immun 2006;74:4849-55. [ Links ]
66. Leid JG, Shirtliff Me, Costerton JW, et al. Human leukocytes adhere to, penetrate, and respond to Staphylococcus aureus biofilms. Infect immun 2002 November;70(11):6339-45. [ Links ]
67. Jesaitis AJ, Franklin Mj, Berglund D, et al. Compromised host defense on pseudomonas aeruginosa biofilms: characterization of neutrophil and biofilm interactions. J immunol 2003 October 15;171(8):4329-39. [ Links ]
68. Leid JG, Willson Cj, Shirtliff Me, et al.The exopolysaccharide alginate protects pseudomonas aeruginosa biofilm bacteria from ifn-{gamma}-mediated macrophage killing. J immunol 2005 December 1;175(11):7512-8. [ Links ]
69. Mah T, Otoole G. Mechanisms of biofilm resistance to antimicrobial agents. Trends in microbiology 9, 34-39. 2001. [ Links ]
70. Richards JJ, Melander C. Controlling Bacterial Biofilms. Chembiochem 2009;10(14):2287-94. [ Links ]
71. Sutherland I. Biofilm exopolysaccharides: a strong and sticky framework. Microbiology 2001 January;147(pt 1):3-9. [ Links ]
72. Branda SS, Vik S, Friedman L, Kolter R. Biofilms: the matrix revisited. Trends microbiol 2005 January;13(1):20-6. [ Links ]
73. Gilbert P, Das J, Foley I. Biofilm susceptibility to antimicrobials. Adv Dent Res 1997 April;11(1):160-7. [ Links ]
74. Flemming hc, Wingender J. The biofilm matrix. Nature 2010;8:623-33. [ Links ]
75. Stoodley p, Sauer K, Davies DG, et al. Biofilms as complex differentiated communities. Annu Rev microbiol 2002;56:187-209. [ Links ]
76. Kohler T, Donner V, Van Delden C. Lipopolysaccharide as shield and receptor for R-pyocin-mediated killing in pseudomonas aeruginosa. J Bacteriol 2010 April;192(7):1921-8. [ Links ]
77. Kohler T, Guanella R, Carlet J, et al. Quorum sensing-dependent virulence during pseudomonas aeruginosa colonisation and pneumonia in mechanically ventilated patients. Thorax 2010 August;65(8):703-10. [ Links ]
78. Pronovost p, Needham D, Berenholtz S, et al.An intervention to decrease catheter-related bloodstream infections in the icu. N Engl J med 2006 December 28;355(26):2725-32. [ Links ]
79. Cerca N, Pier GB, Vilanova M, et al. Quantitative analysis of adhesion and biofilm formation on hydrophilic and hydrophobic surfaces of clinical isolates of Staphylococcus epidermidis. Res microbiol 2005 may;156(4):506-14. [ Links ]
80. Cerca N, Maira-litran T, Jefferson KK, Grout et al. Protection against Escherichia coli infection by antibody to the Staphylococcus aureus poly-N-acetylglucosamine surface polysaccharide. Proceedings of the National Academy of Sciences of the United States of America 104, 7528-7533. 2007. [ Links ]
81. Del Pozo Jl, Rouse Ms, Mandrekar JN, et al. Effect of electrical current on the activities of antimicrobial agents against pseudomonas aeruginosa, Staphylococcus aureus, and Staphylococcus epidermidis biofilms. Antimicrob Agents chemother 2009 January;53(1):35-40. [ Links ]
82. Henriques M, Cerca N, Azeredo J, et al. Influence of sub-inhibitory concentrations of antimicrobial agents on biofilm formation in indwelling medical devices. Int J Artif Organs 2005 Novem¬ber;28(11):1181-5. [ Links ]
83. Trautner BW, Darouiche RO. Catheter-associated infections: pathogenesis affects prevention. Arch intern med 2004 April 26;164(8):842-50. [ Links ]
84. Amaral Mm, Coelho Lr, Flores Rp, et al. The predominant variant of the Brazilian epidemic clonal complex of methicillin-resistant Staphylococcus aureus has an enhanced ability to produce biofilm and to adhere to and invade airway epithelial cells. J infect Dis 2005 September 1;192(5):801-10. [ Links ]
85. Rello J, Ollendorf DA, Oster G, et al. Epidemiology and outcomes of ventilator-associated pneumonia in a large US database. Chest 2002 December;122(6):2115-21. [ Links ]
86. Paju S, Scannapieco Fa. Oral biofilms, periodontitis, and pulmonary infections. Oral Dis 2007 November;13(6):508-12. [ Links ]
87. Zuanazzi D, Souto R, Mattos Mba, et al. Prevalence of potential bacterial respiratory pathogens in the oral cavity of hospitalised individuals. Arch Oral Biol 2010;55:21-8. [ Links ]
88. Klompas M. Prevention of ventilator-associated pneumonia. Expert Rev Anti Infect Ther 2010 July;8(7):791-800. [ Links ]
89. Muscedere JG, Day A, Heyland DK. Mortality, attributable mortality, and clinical events as end points for clinical trials of ventilator-associated pneumonia and hospital-acquired pneumonia. Clin infect Dis 2010 August 1;51 Suppl 1:S120-S125. [ Links ]
90. Bonten Mj. Healthcare epidemiology: Ventilator-associated pneumonia: preventing the inevitable. Clin Infect Dis 2011 January 1;52(1):115-21. [ Links ]
91. Trouillet Jl, chastre J, Vuagnat A, et al. Ventilator-associated pneumonia caused by potentially drug-resistant bacteria. Am J Respir crit care med 1998 february;157(2):531-9. [ Links ]
92. Craven DE, Steger KA. Ventilator-associated bacterial pneumonia: challenges in diagnosis, treatment, and prevention. New horiz 1998 may;6(2 Suppl):S30-S45. [ Links ]
93. Frank DN, Wilson SS, St Amand Al, et al. Culture-independent microbiological analysis of foley urinary catheter biofilms. Plos One 2009;4(11):e7811. [ Links ]
94. Guggenbichler Jp, Assadian O, Boeswald M, et al. Incidence and clinical implication of nosocomial infections associated with implantable biomaterials -catheters, ventilator-associated pneumonia, urinary tract infections. Gms Krankenhhyg interdiszip 2011;6(1):Doc18. [ Links ]
95. Jacobsen Sm, Stickler DJ, mobley hl, et al. Complicated catheter-associated urinary tract infections due to Escherichia coli and proteus mirabilis. Clin microbiol Rev 2008 January;21(1):26-59. [ Links ]
96. Stickler DJ. Bacterial biofilms in patients with indwelling urinary catheters. Nat clin pract Urol 2008 November;5(11):598-608. [ Links ]
97. Srinivasan S, Liu C, Mitchell Cm, et al. Temporal variability of human vaginal bacteria and relationship with bacterial vaginosis. Plos One 2010;5(4):e10197. [ Links ]
98. Ong CL, Ulett GC, Mabbett AN, et al. Identification of type 3 fimbriae in uropathogenic Escherichia coli reveals a role in biofilm formation. J Bacteriol 2008 february;190(3):1054-63. [ Links ]
99. Ogara Jp, Humphreys H. Staphylococcus epidermidis biofilms: importance and implications. J med microbiol 2001 July;50(7):582-7. [ Links ]
100. Nataloni M, Pergolini M, Rescigno G, et al. Prosthetic valve endocarditis. J cardiovasc med (hagerstown ) 2010 December;11(12):869-83. [ Links ]
101. Aragon-Sanchez J, Lazaro-martinez Jl, Hernandez-herrero Mj, et al. Clinical significance of the isolation of Staphylococcus epidermidis from bone biopsy in diabetic foot osteomyelitis. Diabet foot Ankle 2010;1. [ Links ]
102. Otto m. Staphylococcus epidermidis--the accidental pathogen. Nat Rev microbiol 2009 August;7(8):555-67. [ Links ]
103. Dryden Ms. Complicated skin and soft tissue infection. J Antimicrob chemother 2010 November;65 Suppl 3:III35-III44. [ Links ]
104. Galbart J,Allignet J, Tung H, et al. Screening for Staphylococcus epidermidis markers discriminating between skin-flora strains and those responsible for infections of joint prostheses. Journal of infectious Diseases 182, 351-355. 2000. [ Links ]
105. Cerca N, Jefferson K, Pier D, et al. Molecular basis for preferential protective efficacy of antibodies directed to the poorly-acetylated form of staphylococcal poly-N-acetyl-(1-6)-glucosamine (pnag). Infection and immunity 75, 3406-3413. 2007. [ Links ]
106. Kraus D, Peschel A. Staphylococcus aureus evasion of innate antimicrobial defense. Future microbiol 2008 August;3(4):437-51. [ Links ]
107. Roberts Ap, Pratten J, Wilson M, et al.transfer of a conjugative transposon, tn5397 in a model oral biofilm. Fems microbiol lett 1999 August 1;177(1):63-6. [ Links ]
108. Gill SR, Fouts DE, Archer Gl, et al. Insights on evolution of virulence and resistance from the complete genome analysis of an early methicillin-resistant Staphylococcus aureus strain and a biofilm-producing methicillin-resistant Staphylococcus epidermidis strain. J Bacteriol 2005 April;187(7):2426-38. [ Links ]
109. Tormo Ma, Knecht E, Gotz F,et al. Bap-dependentbiofilm formation by pathogenic species of Staphylococcus: evidence ofhorizontal gene transfer? Microbiology 2005 July;151(pt 7):2465-75. [ Links ]
110. Bryers JD, Ratner BD. Bioinspired implant material befunddle bacteria. Asm News 2004;70:232-7. [ Links ]
111. Vuong C, Otto M. Staphylococcus epidermidis infections. Microbes infect 2002 April;4(4):481-9. [ Links ]
112. World health Organization (who). Nosocomial infections. 2005. [ Links ]
113. Klevens Rm, Edwards JR, Richards Cl, Jr., et al. Estimating health care-associated infections and deaths in U.S. hospitals, 2002. Public health Rep 2007 march;122(2):160-6. [ Links ]
114. Vincent Jl, Bihari DJ, Suter Pm, et al.The prevalence of nosocomial infection in intensive care units in Europe. Results of the European prevalence of infection in intensive care (Epic) Study. Epic international Advisory committee. Jama 1995 August 23;274(8):639-44. [ Links ]
115. Agarwal R, Gupta D, Ray P, et al. Epidemiology, risk factors and outcome of nosocomial infections in a Respiratory intensive care Unit in North india. J infect 2006 August;53(2):98-105. [ Links ]
116. CDC. National nosocomial infections surveillance (nnis) system report, data summary from january 1992 through june 2004, issued october 2004. Amj infect control 2004 december;32(8):470-85. [ Links ]
117. De Oliveira AC, Kovner CT, Da Silva RS. Nosocomial infection in an intensive care Unit in a Brazilian University hospital . Rev latino-Am Enfermagem 2010;18(2):233-9. [ Links ]
118. Giamberardino Hig, Cesário Ep, Carmes ER et al. Risk factors for Nosocomial infection in trauma patients. Braz J of infect Diseas 2007;11(2):285-9. [ Links ]
119. Lisboa T, Faria M, Hoher JA, et al. The prevalence of nosocomial infection in intensive care Units in the State of Rio Grande do Sul. Rev Brasil terap intens 2007;19(4):414-20. [ Links ]
120. Oncul O, Ulkur E, Acar A, et al. Prospective analysis of nosocomial infections in a Burn care Unit, turkey. Indian J med Res 2009;130:758-64. [ Links ]
121. Wisplinghoff H, Bischoff T, Tallent Sm, et al. Nosocomial bloodstream infections in ushospitals: analysis of 24, 179 cases froma prospective nationwide surveillancestudy. Clin infec Dis 2004 August 1;39(3):309-17. [ Links ]
122. Amaral SM, Cortes AQ, Pires FR. Nosocomial pneumonia: importance of the oral environment. J Bras pneumol 2009 November;35(11):1116-24. [ Links ]
123. Kuroki R, Kawakami K, Qin L, et al. Nosocomial bacteremia caused by biofilm-forming Bacillus cereus and Bacillus thuringiensis. Intern med 2009;48(10):791-6. [ Links ]
124. Goossens h. European status of resistance in nosocomial infections. Chemotherapy 2005 July;51(4):177-81. [ Links ]
125. Gonzalez-Saldana N, Castaneda-Narvaez Jl, Saltigeral-Simental P, et al. [Impact of nosocomial infection decrease in neonatology]. Salud publica mex 2010 August;52(4):290-1. [ Links ]
126. Mohamed JA, huang DB. Biofilm formation by enterococci. J med microbiol 2007;56:1581-8. [ Links ]
127. Tay Mk, Lee Jy, Wee Iy, et al. Evaluation of intensive care unit-acquired urinary tract infections in Singapore. Ann Acad med Singapore 2010 June;39(6):460-5. [ Links ]
128. Ding JG, Sun Qf, Li Kc, et al. Retrospective analysis of nosocomial infections in the intensive care unit of a tertiary hospital in china during 2003 and 2007. Bmc infect Dis 2009;9:115. [ Links ]
129. Rosenthal VD, Guzman S, Orellano Pw. Nosocomial infections in medical-surgical intensive care units in Argentina: attributable mortality and length of stay. Am J infect control 2003 August;31(5):291-5. [ Links ]
130. Aires S, Carvalho A, Aires E, et al. [Evaluation of the knowledge and attitudes to the standard precautions for infection control of the healthcare workers of a portuguese central and university hospital]. Acta med port 2010 march;23(2):191-202. [ Links ]
131. Kock R, Becker K, Cookson B, et al. Methicillin-resistant Staphylococcus aureus (mrsa): burden of disease and control challenges in Europe. Euro Surveill 2010 October 14;15(41):19688. [ Links ]
132. Da Silva Coimbra Mv, Silva-Carvalho MC, Wisplinghoff H, et al. Clonal spread of methicillin-resistant staphylococcus aureus in a large geographic area of the United States. J hospinfect 2003 february;53(2):103-10. [ Links ]
133. Dominguez Ma, De Lh, Linares J, et al. Spread and maintenance of a dominant methicillin-resistant Staphylococcus aureus (mrsa) clone during an outbreak of mrsa disease in a Spanish hospital. J clin microbiol 1994 September;32(9):2081-7. [ Links ]
134. Da Silva Coimbra Mv, Teixeira La, Ramos Rl, et al. Spread of the Brazilian epidemic clone of a multiresistant mrsa in two cities in Argentina. J med microbiol 2000 february;49(2):187-92. [ Links ]
135. Aires de Sm, Sanches Is, Ferro Ml, et al. Intercontinental spread of a multidrug-resistant methicillin-resistant Staphylococcus aureus clone. J clin microbiol 1998 September;36(9):2590-6. [ Links ]
136. Campanile F, Cafiso V, Cascone C, et al. [Clonal diffusion and evolution of meca and tn554 polymorphisms in methicillin-resistant Staphylococcus aureus in italy]. Infez med 2001 march;9(1):30-8. [ Links ]
137. Melter O, Santos S, I, Schindler J, et al. Methicillin-resistant Staphylococcus aureus clonal types in the czech Republic. J clin microbiol 1999 September;37(9):2798-803. [ Links ]
138.Uhlemann Ac, Porcella Sf, Trivedi S, et al. Identification of a highlytransmissible animal-independentstaphylococcus aureus St398 clone withdistinct genomic and cell adhesion properties. Mbio 2012;3(2). [ Links ]
139. Cerca N, Oliveir Ar, Azeredo J. Susceptibility of staphylococcus epidermidisplanktoniccellsand biofilmstothelyticactionofstaphylococcus bacteriophage K. Lett Applmicrobiol.inpress 2007. [ Links ]
140. Gomes Fia, Teixeira P, Azeredo J, et al. Effect of farnesol on planktonic and Biofilm cells of Staphylococcus epidermidis. Current microbiology 2009;59:118-22. [ Links ]
141. Resch A, Rosenstein R, Nerz C, et al. Differential gene expression profiling of Staphylococcus aureus cultivated under biofilm and planktonic conditions. Appl Environ microbiol 2005 may;71(5):2663-76. [ Links ]
142. Sillankorva S, Oliveira R, Vieira M, et al. Bacteriophage f-S1 infection of pseudomonas fluorescens planktonic cells versus biofilms. Biofouling 2004;20:133-8. [ Links ]
143. Pankuch GA, Jueneman SA, Davies Ta, et al. In vitro selection of resistance to four beta-lactams and azithromycin in Streptococcus pneumoniae. Antimicrob Agents chemother 1998 November;42(11):2914-8. [ Links ]
144. Gillis RJ, Iglewski Bh. Azithromycin retards pseudomonas aeruginosa biofilm formation. J clin microbiol 2004 December;42(12):5842-5. [ Links ]
145. Yassien M, Khardori N. Interaction between biofilms formed by Staphylococcus epidermidis and quinolones. Diag microb infect Diseas 40, 79-89. 2001. [ Links ]
146. Baveja J, Wilcox M, Hume E, et al. Furanones as potential anti-bacterial coating on biomaterials. Biomaterials 25, 5003-5012. 2004. [ Links ]
147.Gollwitzer H, Ibrahim K, Meyer H, et al. Antibacterial poly (D,l-lacticacid) coating of medical implants using abiodegradable drug delivery technology. J antimicrob chemother 51,585-591.2003. [ Links ]
148. Shi L, Ardehall R, Caldwell K, et al. Mucin coating on polymeric material surfaces to suppress bacterial adhesion. Colloids and Surfaces B: Biointerfaces 17, 229-239. 2000. [ Links ]
149. Azeredo J, Sutherland Iw. The use of phages for the removal of infectious biofilms. Curr pharm Biotechnol 2008 August;9(4):261-6. [ Links ]
150. Curtin JJ, Donlan Rm. Using bacteriophages to reduce formation of catheter-associated biofilms by Staphylococcus epidermidis. Antimicrob Agents chemother 2006 April;50(4):1268-75. [ Links ]
151. Del Pozo Jl, Alonso M, Arciola Cr, et al.. Biotechnological war against biofilms. Could phages mean the end of device-related infections? Int J Artif Organs 2007 September;30(9):805-12. [ Links ]
152. Lu TK, Collins JJ. Dispersing biofilms with engineered enzymatic bacteriophage. Proc Natl Acad Sci USA 2007 July 3;104(27):11197-202. [ Links ]
153. Huttner B, Goossens G, Verheif T, et al. Characteristics and outcomes of public campaigns aimed at improving the use of antibiotics in outpatients in high-income countries. Lancet infect Dis 2010;10(1):17-31. [ Links ]
154. ]. Cerca N, Jefferson KK. Que vantagens têm os microrganismos em formar um biofilme? In: Azevedo NF, Cerca N, editors. Biofilmes - Na saúde, no ambiente, na indústria. 1st ed. Porto: publindustria; 2012. P. 11-6. [ Links ]
Nuno Cerca Instituto de Bioengenharia e Biotecnologia (IBB), Centro de Engenharia Biológica Universidade do Minho, campus de Gualtar, Braga
Email: nunocerca@ceb.uminho.pt














