Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Arquivos de Medicina
versão On-line ISSN 2183-2447
Arq Med vol.29 no.1 Porto fev. 2015
CASOS CLÍNICOS/ /SÉRIE DE CASOS
Cabazitaxel no tratamento do cancro da próstata metastático resistente à castração
Cabazitaxel in the treatment of metastatic castration-resistant prostate cancer
Sara Meireles1, Isabel Augusto1, Catarina Fernandes1, Andreia Coelho1, Carlos Silva2, Margarida Damasceno1
1Serviço de Oncologia Médica, Centro Hospitalar de São João, Epe
2Serviço de Urologia, Centro Hospitalar de São João, Epe
RESUMO
Introdução: As opções terapêuticas no cancro da próstata metastático resistente à castração (mCPRC), uma vez refratário à quimioterapia com docetaxel, eram até recentemente limitadas. O cabazitaxel é um taxano da nova geração que demonstrou benefício na sobrevivência global destes doentes. Os autores pretendem descrever a sua experiência quanto à eficácia e tolerância deste agente no tratamento do mCPRC após docetaxel.
Métodos: Estudo retrospetivo dos doentes com mCPRC que iniciaram tratamento com cabazitaxel entre Janeiro de 2011 e Janeiro de 2012 no Centro Hospitalar de São João. A análise de sobrevivência foi efetuada pelo método Kaplan-Meier.
Resultados: Doze doentes efetuaram tratamento com cabazitaxel. A mediana de idades no início do tratamento foi de 70 anos (60-75) e 10 doentes tinham ECOG performance status 0-1. A taxa de resposta do PSA foi 64% e a taxa de redução de PSA >50% foi 57%. Com um follow-up de 14 meses, a taxa de progressão foi 55% e a mediana de tempo para a progressão foi 7 meses. A mediana da sobrevivência livre de progressão (SLP) e da sobrevivência global (SG) foram de 8 (IC 95% 3.4-12.7) e 14 (IC 95% 7.3-20.2) meses, com uma SLP e SG ao 1 ano de 40% e 58% respetivamente. Os efeitos laterais mais frequentes foram a anemia (83%), neutropenia (25%) e a diarreia (25%).
Conclusão: A nossa experiência revela que o cabazitaxel é uma opção terapêutica de benefício comprovado na doença refratária à quimioterapia com docetaxel, com taxas de resposta e tolerância comparáveis ao estudo de aprovação.
Palavras-chave: cancro da próstata, metastático, cabazitaxel
ABSTRACT
Background: Until recently, patients with metastatic castration-resistant prostate cancer (mCRPC) had limited therapeutic options once they became refractory to docetaxel chemotherapy. Cabazitaxel is a new generation taxane with benefit on overall survival of these patients. The authors report the clinical experience from the institution regarding to efficacy and tolerability of this agent in treatment of mCRPC after docetaxel.
Methods: Retrospective review of patients with mCRPC who started cabazitaxel treatment between January 2011 and January 2012 in Centro Hospitalar São João. Survival analysis was performed by Kaplan-Meier method.
Results: twelve patients were submitted to cabazitaxel treatment. The median age was 70 years old [60-75] and 10 patients had ECOG performance status 0-1. PSA response rate was 64% and PSA reduction rate > 50% was 57%. After a follow-up of 14 months, the progression rate was 55% with a median time to progression of 7 months. The median of progression free survival (PFS) and overall survival (OS) was 8 months (CI 95% 3.4-12.7) and 14 months (CI 95% 7.3-20.2). The 1-year PFS and OS was 40% and 58% respectively. The most common adverse events were anemia (83%), neutropenia (25%) and diarrhea (25%).
Conclusion: Our experience shows that cabazitaxel is a therapeutic option with benefit in refractory disease to docetaxel chemotherapy with response rates and tolerability comparable to its approval study.
Key-words: prostate cancer, metastatic, cabazitaxel
Introdução
Em Portugal, o cancro da próstata é a neoplasia mais frequente no homem e representa a terceira causa mais comum de morte oncológica.1
Apesar dos avanços, o docetaxel mantém-se um tratamento de referência no mCPRC.2 As opções terapêuticas nos doentes refratários ao docetaxel eram até recentemente limitadas. Contudo, vários agentes têm demonstrado benefício na sobrevivência destes doentes.3-6
O cabazitaxel é um taxano da nova geração aprovado após o ensaio TROPIC, que demonstrou, associado à prednisona, melhorar a sobrevivência global (SG) destes doentes relativamente a mitoxantrone e prednisona.3 Comparativamente aos outros taxanos, apresenta ainda actividade potencial em doença metastática cerebral e leptomeníngea, ultrapassando a barreira hemato-encefálica em modelos pré-clínicos.7
Os autores pretendem reportar os resultados da sua instituição quanto à eficácia e tolerância do cabazitaxel no mCPRC, seguindo-se uma revisão da literatura.
Métodos
Procedeu-se ao estudo retrospetivo dos doentes com diagnóstico de mCPRC que iniciaram tratamento com cabazitaxel (25 mg/m2 cada 21 dias e prednisolona 5mg 2id) no Serviço de Oncologia Médica do Centro Hospitalar de São João entre Janeiro de 2011 e Janeiro de 2012.
A colheita de dados foi efetuada com base nos processos clínicos. Analisaram-se os seguintes parâmetros: idade, ECOG performance status, tipo de metastização, número de linhas terapêuticas prévias, número de ciclos de docetaxel, data de início de tratamento com cabazitaxel, valor de PSA inicial e após 3 meses, número de ciclos de cabazitaxel, motivo de adiamento e /ou descontinuação de tratamento, efeitos adversos, data de término do tratamento, data e causas de óbito.
Os principais objetivos consistiram na avaliação da taxa de resposta do PSA, taxa de progressão, sobrevivência livre de progressão (SLP) e SG. Foram ainda analisados os principais efeitos laterais.
A resposta do PSA foi definida como redução >25% do valor inicial do PSA e avaliada aos 3 meses. A progressão foi definida após 2 elevações consecutivas do PSA, com ou sem progressão imagiológica. A avaliação da metastização óssea foi efetuada através de cintigrafia óssea.
A análise de sobrevivência foi realizada pelo método Kaplan-Meier. A SLP e a SG foram calculadas desde a data de início do tratamento com cabazitaxel até à data de progressão ou óbito, respetivamente.
Na análise estatística recorreu-se ao programa SPSS (Statistical Package for the Social Sciences) versão 19.0.
Resultados
Doze doentes iniciaram tratamento com cabazitaxel. A mediana de idades no início do tratamento foi de 70 anos (60-75) e 10 doentes tinham ECOG performance status de 0-1. A metastização óssea estava presente em todos os doentes. Três doentes tinham associada metastização visceral e quatro tinham metastização ganglionar.
A mediana de ciclos efetuados de docetaxel foi de 9 e apenas dois doentes efetuaram mais de duas linhas terapêuticas prévias.
O tempo mediano desde o diagnóstico inicial até ao início do cabazitaxel foi de 43 meses e a mediana do número de ciclos efetuados foi de 8 (2-18).
A resposta máxima do PSA foi atingida em média no 4º ciclo. A taxa de resposta do PSA aos 3 meses foi de 64%, com uma taxa de redução de PSA >50% de 57%.
Com follow-up de 14 meses, registou-se uma taxa de progressão de 55% e um tempo mediano para a progressão de 7 meses.
A mediana da SLP foi de 8 meses (IC 95% 3.412.7) com SLP ao 1 ano de 40% (Figura 1). A mediana da SG foi de 14 meses (IC 95% 7.3-20.2) com SG ao 1 ano de 58% (Figura 1).
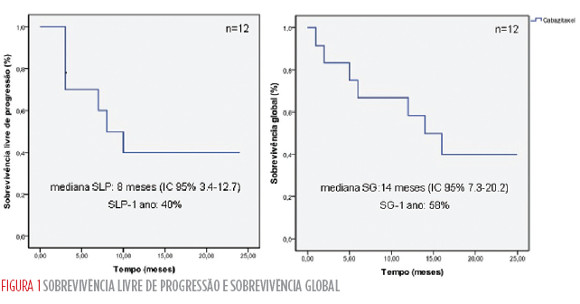
Os efeitos laterais mais frequentes foram a anemia (83%), neutropenia (25%) e a diarreia (25%) e ocorreram maioritariamente nos 3 primeiros ciclos. Dois doentes tiveram neutropenia grau 3 e nenhum teve neutropenia febril.
A Tabela 1
apresenta os efeitos adversos objetivados com cabazitaxel.
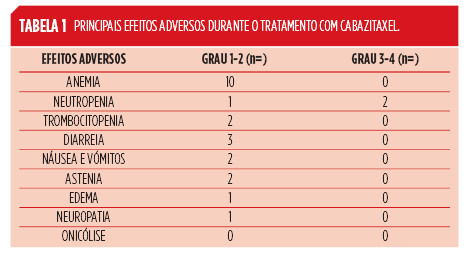
O ciclo de quimioterapia foi adiado em 3 doentes (trombocitopenia e neutropenia: 1; infecção: 2) e um doente apresentou anemia grau 2 com necessidade de redução de dose em 20%.
Nenhum doente necessitou de descontinuar tratamento por toxicidade, seis doentes descontinuaram por progressão e dois por estabilização de doença.
Dos sete doentes que faleceram, verificou-se progressão de doença em quatro e, nos restantes, registou-se tromboembolismo pulmonar, sépsis e neoplasia gástrica. A taxa de mortalidade foi de 58,7%.
Discussão
O número de casos de cancro da próstata tem vindo a aumentar significativamente. Em Portugal, são diagnosticados 5140 novos casos por ano.1
Menos de 5% dos doentes apresentam metastização ao diagnóstico, embora 40% venham a desenvolver metástases após tratamento local.8
Na doença metastática, a abordagem clínica está dependente da resposta à castração. Contudo, a resistência à castração desenvolve-se inevitavelmente, com duração de resposta mediana de 12 a 24 meses.8
O tratamento com docetaxel (75 mg/m2 a cada 21 dias) e prednisolona (5mg 2id) estabeleceu-se como tratamento standard nos doentes com mCPRC, desde os ensaios TAX327 e SWOG9916.2,9
Até aos últimos 3 anos, a abordagem dos doentes que progrediam após docetaxel era diversa. A reintrodução de docetaxel tornou-se numa estratégia alternativa para aqueles com eficácia prévia a este taxano (progressão após 6 meses).10-13 Os doentes eram também frequentemente tratados com mitoxantrone (12 mg/m2 a cada 21 dias) e prednisolona (5 mg 2id) para controlo sintomático.
O cabazitaxel, taxano com baixa afinidade para a glicoproteína-P, demonstrou ter maior actividade nos tumores resistentes ao docetaxel.7 O ensaio prospectivo TROPIC comparou cabazitaxel e prednisona com mitoxantrone e prednisona em doentes previamente tratados com docetaxel, tendo sido demonstrado benefício na SG a favor do cabazitaxel (15.1 vs 12.7 meses), com 30% da redução no risco de morte (HR=0.70;IC 95% 0.59-0.83; P< 0.0001).3 Uma atualização recente mostrou que aos 2 anos de follow-up, as curvas de sobrevivência mantêm-se divergentes.14 Além disso, o cabazitaxel teve um impacto positivo no controlo da dor, com um perfil de segurança consistente com as outras quimioterapias e uma baixa taxa de neuropatia.14
Recentemente foi iniciado o ensaio clínico FIRStAnA, que pretende comparar cabazitaxel e prednisona na dose 25 mg/m2 ou 20 mg/m2 com docetaxel e prednisona relativamente à SG nos doentes sem quimioterapia prévia.
O acetato de abiraterona e a enzalutamida vie-ram demonstrar também benefício clínico após falência do tratamento com docetaxel. Uma análise interina do estudo COU-AA-301 demonstrou que o acetato de abiraterona aumentava significativamente a SG em 3,9 meses em comparação com placebo (14.8 vs 10.9 meses, HR=0.65 p<0.001).5
No estudo AFFIRM, a mediana da SG para o grupo da enzalutamida foi de 18.4 meses versus 13.6 para o grupo placebo.6 Apesar de representarem atualmente novas opções terapêuticas, ainda não exista consenso quanto à melhor abordagem após quimioterapia com docetaxel.
Na nossa casuística de tratamento com cabazitaxel, apesar das limitações de um estudo retrospetivo e do tamanho da amostra, foram objetivadas taxas de resposta e um perfil de segurança comparáveis ao ensaio TROPIC. A sobrevivência dos nossos doentes veio confirmar o claro benefício evidenciado no ensaio de aprovação deste fármaco, com uma mediana que se aproxima do resultado observado (14.0 vs 15.1 meses).
Os efeitos adversos mais comuns de grau 3/4 no TROPIC foram a neutropenia (82% cabazitaxel vs 58% mitoxantrone), a leucopenia (68% vs 42%), a anemia (11% vs 5%) e a diarreia (6% vs <1%).3 A nossa análise mostrou toxicidades comparáveis e, apesar da mediana do número de ciclos de docetaxel efectuados (9 vs 7 ciclos) ter sido superior ao ensaio TROPIC, a hematoxicidade de grau 3/4 foi pouco significativa, não se verificando nenhuma neutropenia febril. A percentagem de doentes que descontinuou tratamento por efeitos adversos no TROPIC foi de 18%.3 No nosso estudo, a maioria descontinuou por progressão, não se objetivando nenhum caso por efeitos secundários.
Assim, a nossa experiência revela que a utilização do cabazitaxel na prática clínica apresenta um benefício comparável ao estudo de aprovação, constituindo uma opção terapêutica nos doentes refratários ou resistentes ao docetaxel.
Com a maior disponibilidade de agentes, acresce a necessidade de ensaios randomizados que definam a melhor sequência de tratamento, para maximizar o valor das atuais terapêuticas.
Referências
1. Ferlay J, Shin HR, Bray F, Forman D, Mathers C and Parkin DM. GLOBOCAN 2008 v2.0, Cancer Incidence and Mortality Worldwide: IARC Cancerbase no. 10[Internet]. Lyon, France: International Agency for Research on Cancer; 2010. [ Links ]
2. Tannock IF, de Wit R, Berry WR, et al. Docetaxel plus prednisone or mitoxantrone plus prednisone for advanced prostate cancer. N Engl J Med 2004;351:1502–12. [ Links ]
3. de Bono JS, Oudard S, Ozguroglu M et al. Prednisone plus cabazitaxel or mitoxantrone for metastatic castration-resistant prostate cancer progressing after docetaxel treatment: a randomised open-label trial. Lancet 2010; 376: 1147–1154. [ Links ]
4. de Bono JS, Logothetis CJ, Molina A et al. Abiraterone and increased survival in metastatic prostate cancer. N Engl J Med 2011; 364:1995–2005. [ Links ]
5. Fizazi K, Scher HI, Molina A et al. Abiraterone acetate for treatment of metastatic castration-resistant prostate cancer: final overall survival analysis of the COU-AA-301 randomised, double-blind, placebo-controlled phase 3 study. Lancet Oncol 2012; 13:983–992. [ Links ]
6. Scher HI, Fizazi K, Saad F et al. Increased survival with enzalutamide in prostate cancer after chemotherapy. N Engl J Med 2012; 367:1187–1197. [ Links ]
7. Paller CJ, Antonarakis ES. Cabazitaxel: a novel second-line treatment for metastatic castration-resistant prostate cancer. Drug Design, Development and Therapy 2011; 5:117-124. [ Links ]
8. DeVita VT, Lawrence TS, Rosenberg SA. DeVita, Hellman, and Rosenbergs cancer: principles and practice of oncology. ed 9. Philadelphia, PA: Wolters Kluwer Health/Lippincott Williams&Wilkins; 2011. [ Links ]
9. Petrylak DP, Tangen CM, Hussain MH et al. Docetaxel and estramustine compared with mitoxantrone and prednisone for advanced refractory prostate cancer. N Engl J Med 2004; 351:1513–20. [ Links ]
10. Loriot Y, Massard C, Gross-Goupil M, et al. The interval from the last cycle of docetaxel-based chemotherapy to progression is associated with the efficacy of subsequent docetaxel in patients with prostate cancer. Eur J Cancer 2010; 46:1770–2. [ Links ]
11. Buonerba C, Palmieri G, Di Lorenzo G. Docetaxel rechallenge in castration-resistant prostate cancer: scientific legitimacy of commonclinical practice. Eur Urol. 2010; 58:636–7. [ Links ]
12. Eymard JC, Oudard S, Gravis G, et al. Docetaxel reintroduction in patients with metastatic castration-resistant docetaxel-sensitive prostate cancer: a retrospective multicentre study. BJU Int. 2010; 106:974–8. [ Links ]
13. Ohlmann CH, Markert E, Gerharz M, et al. Improving the efficacy of targeted trials by multiple-marker analysis in castration-resistant prostate cancer. Urol Oncol 2011; 29:664-669. [ Links ]
14. Bahl A, Oudard S, Tombal B et al. Impact of cabazitaxel on 2-year survival and palliation of tumour-related pain in men with metastatic castration-resistant prostate cancer treated in the TROPIC trial. Annals of Oncology 2013; 00: 1–7. [ Links ]
Sara Meireles
Serviço de Oncologia Médica do Centro Hospitalar S. João, e.p.e. Al. Prof. Hernâni Monteiro, 4200-319 Porto. E-mail: sarameireles@hotmail.com
Data de recepção / reception date: 10-12-2013
Data de aprovação / approval date: 24-10-2014












