Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Revista Portuguesa de Imunoalergologia
versão impressa ISSN 0871-9721
Rev Port Imunoalergologia vol.21 no.1 Lisboa jan. 2013
Estudo comparativo de métodos de rastreio de atopia em doentes com rinite (ImmunoCAP® Rapid versus Phadiatop® e testes cutâneos em picada)
Comparative study of survey methods for atopy in patients with rhinitis (ImmunoCAP® Rapid versus Phadiatop® and skin prick tests)
José Geraldo Dias1,Susana Lopes Silva1, Sofia Luz1, Sara Pereira da Silva1, Amélia Spínola Santos1, Elisa Pedro1,Conceição Pereira Santos2, Manuel Pereira Barbosa1
1 Serviço de Imunoalergologia, Hospital de Santa Maria, Centro Hospitalar Lisboa Norte
2Unidade de Imunologia Clínica, Instituto de Medicina Molecular, Faculdade de Medicina de Lisboa
RESUMO
Introdução:Cerca de 75% dos casos de rinite têm etiologia alérgica. O diagnóstico de alergia respiratória permite a optimização terapêutica. O ImmunoCAP® Rapid é um método in vitro que permite determinar qualitativamente a presença de IgE específica no sangue total. Objectivo: Avaliar a sensibilidade, especificidade, valor preditivo negativo e valor preditivo positivo do ImmunoCAP® Rapid para identificação de atopia numa população com rinite, em comparação com Phadiatop®, relativamente aos testes cutâneos em picada (TCP) (gold standard); avaliar também a concordância entre TCP e ImmunoCAP® Rapid. Métodos: Estudo transversal, randomizado, com 40 adultos com rinite observados em consulta de Imunoalergologia, dos quais 30 tinham TCP positivos para aeroalergénios. Todos os indivíduos efectuaram Phadiatop®, ImmunoCAP® Rapid e TCP com os alergénios Dermatophagoides pteronyssinus, epitélios de cão e de gato, Blatella germanica, Alternaria alternata, Phleum pratense, Parietaria judaica, Olea europaea, Artemisia vulgaris e Betula verrucosa. Consideraram-se positivos TCP com diâmetro médio da pápula ≥ 3mm relativamente ao controlo negativo. Resultados: Idade média de 34 ± 11 anos, 53% do género feminino. Sensibilidade e valor preditivo negativo do ImmunoCAP® Rapid para o diagnóstico de atopia: 90% e 77% (Phadiatop®: 93% e 83%). Especificidade e valor preditivo positivo: 100% em ambos os métodos. A análise por alergénio dos resultados do ImmunoCAP® Rapid e TCP revelou uma concordância média de 88,8% ± 7,4%. O ImmunoCAP® Rapid não identificou pelo menos uma sensibilização em 25 de 30 doentes, totalizando -se 40 resultados negativos com TCP positivos. Conclusão: Atendendo à sua sensibilidade e valor preditivo negativo, o ImmunoCAP® Rapid poderá ser considerado um método aceitável para rastreio de atopia em doentes com rinite. A análise do seu desempenho por aeroalergénio revelou, no entanto, que comparativamente aos TCP, não permite identificar a sensibilização a todos os aeroalergénios clinicamente relevantes numa elevada percentagem de doentes.
Palavras-chave: Atopia, especificidade, ImmunoCAP® Rapid, sensibilidade, valor preditivo negativo, valor preditivo positivo.
ABSTRACT
Background: About 75% of rhinitis patients suffer from allergies. Respiratory allergy diagnosis allows therapeutic optimization. ImmunoCAP® Rapid is an in vitro assay for qualitative determination of specific IgE in human whole blood. Aim: To evaluate sensitivity, specificity, negative predictive value and positive predictive value of ImmunoCAP® Rapid in the identification of atopy in patients with rhinitis, comparing to Phadiatop®, assuming skin prick tests (SPT) as gold standard; to evaluate correlation between SPT and ImmunoCAP® Rapid results for each aeroallergen. Methods: Cross-sectional, randomized study with 40 adult patients with rhinitis observed in the Immunoallergology outpatient unit, 30 of them with positive SPT to at least one aeroallergen. All patients underwent Phadiatop®, ImmunoCAP® Rapid and SPT for Dermatophagoides pteronyssinus, dog and cat dander, Blatella germanica, Alternaria alternata, Phleum pratense, Parietaria judaica, Olea europaea, Artemisia vulgaris and Betula verrucosa. SPT ≥ 3mm than negative control were considered positive. Results: Average age of 34 ± 11 years, 53% female. Sensitivity and negative predictive value of ImmunoCAP® Rapid in the identification of atopy: 90% and 77% (Phadiatop®: 93% and 83%). Specificity and positive predictive value: 100% in both methods. Analysing allergens individually, ImmunoCAP® Rapid and SPT disclosed a mean agreement of 88.8% ± 7.4%. ImmunoCAP® Rapid failed to identify at least one sensitization in 25 of 30 patients, totalizing 40 negative results with positive SPT. Conclusion: Considering its sensitivity and negative predictive value, ImmunoCAP® Rapid might be considered an acceptable method to investigate atopy in patients with rhinitis. However, the analysis of its performance for each aeroallergen revealed, comparatively to SPT, that ImmunoCAP® Rapid does not allow to identify all clinically relevant sensitizations in a considerable percentage of patients.
Keywords: Atopy, ImmunoCAP® Rapid, negative predictive value, positive predictive value, sensitivity, specificity.
INTRODUÇÃO
A rinite pode ser definida como uma inflamação da mucosa nasal e é caracterizada clinicamente por rinorreia (anterior e/ou posterior), crises esternutatórias, obstrução e prurido nasal, reversíveis espontaneamente ou com tratamento. Várias causas não alérgicas podem originar estas manifestações, incluindo infecções, alterações hormonais, agentes físicos, anomalias anatómicas ou determinados fármacos1.
A rinite alérgica é a forma mais comum de rinite não infecciosa e resulta de uma resposta mediada por anticorpos IgE específicos para alergénios1. Cerca de 75% dos casos de rinite têm etiologia alérgica, sendo esta a mais comum das doenças alérgicas2, afectando cerca de 20 a 30% da população mundial3, estimando-se uma prevalência global de até 30% na população europeia4. Também em Portugal, paralelamente ao aumento da prevalência de outras patologias alérgicas, a prevalência da rinite alérgica tem aumentado progressivamente nos últimos anos. Em 2004, a prevalência de rinite em Portugal atingia 26,1% da população (28,2% das mulheres e 22,2% dos homens)4.
É bem conhecida a interacção entre as vias respiratórias superiores e inferiores, contribuindo para a frequente associação entre rinite e asma. Cerca de 80% dos asmáticos têm rinite e até 40% dos doentes com rinite têm asma1.
Para além de factor de risco para asma, a rinite alérgica está frequentemente associada a outras co-morbilidades, como a sinusite ou a conjuntivite alérgica1.
O diagnóstico de rinite alérgica é feito através da história clínica (essencial), complementada com testes in vivo e in vitro. Para diagnóstico de atopia estão disponíveis testes de rastreio in vitro que permitem determinar a existência de anticorpos IgE específicos circulantes para misturas de aeroalergénios e/ou de alergénios alimentares aos quais a sensibilização é mais frequente. O doseamento de IgE total é também um método in vitro disponível mas com utilidade muito limitada no rastreio de atopia, tendo em conta a sua fraca sensibilidade5, pelo que não será considerada neste trabalho.
Para identificar as sensibilizações individuais de cada doente, os testes cutâneos em picada (TCP), que evidenciam na pele a existência de anticorpos IgE específicos para determinados alergénios, são considerados o método gold standard1, podendo ainda recorrer-se ao doseamento de IgE sérica específica para um determinado alergénio (método in vitro).
A maioria dos doentes com rinite é observada nos cuidados de saúde primários, sendo de extrema importância que neste contexto estejam disponíveis meios auxiliares de diagnóstico adequados à correcta identificação dos casos de rinite com provável etiologia alérgica.
O ImmunoCAP® Rapid (Phadia – Thermo Fisher Scientific, Uppsala, Suécia) é um dispositivo para avaliação de doentes com sintomas sugestivos de alergia, comercializado em Portugal desde 2009. Este método permite determinar qualitativamente a presença de anticorpos IgE específicos no sangue, a partir de uma pequena amostra de sangue capilar, com resultados ao fim de 20 minutos. Está disponível um dispositivo para avaliação de adultos que testa a sensibilização a 10 aeroalergénios (Dermatophagoides pteronyssinus, epitélio de cão, epitélio de gato, Blatella germanica, Alternaria alternata, Phleum pratense, Parietaria judaica, Olea europaea, Artemisia vulgaris e Betula verrucosa) e um dispositivo recomendado para avaliação de crianças que não testa a sensibilização a Blatella germanica e a Alternaria alternata, mas que associa leite de vaca e clara de ovo.
OBJECTIVO
Este estudo pretende avaliar a sensibilidade, a especificidade, o valor preditivo negativo e o valor preditivo positivo do ImmunoCAP® Rapid na identificação de atopia numa população com rinite, em comparação com a determinação de Phadiatop® inalante. Assumiu-se como método gold standard a concordância da clínica com o resultado dos TCP para aeroalergénios.
Adicionalmente, determinou-se a concordância entre os TCP e o ImmunoCAP® Rapid individualmente para todos os aeroalergénios testados.
MÉTODOS
Foi efectuado um estudo transversal randomizado que incluiu 40 adultos com diagnóstico de rinite observados em primeira consulta de Imunoalergologia (53% do género feminino; idade média de 34 ± 11 anos; idade mínima de 18 e máxima de 65 anos). O diagnóstico de rinite foi efectuado pelo médico, com base nos critérios propostos pelo ARIA (AllergicRhinitis and its Impact on Asthma)1.
Todos os doentes foram submetidos ao ImmunoCAP® Rapid (Phadia – Thermo Fisher Scientific, Uppsala, Suécia) para adultos e a TCP (extractos Bial -Aristegui®, Bilbau, Espanha) na face anterior do antebraço para os 10 aeroalergénios do ImmunoCAP® Rapid. Os doentes não estavam sob terapêutica com anti-histamínico nos cinco dias que antecederam os testes. A todos os doentes foi colhida uma amostra de sangue venoso para determinação de Phadiatop® inalante, que determina a existência de anticorpos IgE específicos circulantes para a seguinte mistura de aeroalergénios: Dermatophagoides pteronyssinus, epitélios de cão e de gato, Alternaria tenuis, Penicillium notatum, Phleum pratense,Cynodon dactylon, Parietaria officinalis, Plantago lanceolata, Ambrosia elatior, Cryptomeria japonica e Betula verrucosa.
O resultado do ImmunoCAP® Rapid foi lido em todos os doentes pelo mesmo observador, que desconhecia os resultados dos TCP e do Phadiatop® inalante. Foram considerados positivos TCP com diâmetro médio da pápula ≥ 3mm relativamente ao controlo negativo em leitura aos 15 minutos, de acordo com as recomendações da European Academy ofAllergy and Clinical Immunology6 e Immuno-CAP® Rapid com pelo menos uma banda num alergénio, independentemente da sua intensidade.
Trinta doentes com TCP positivos para pelo menos um aeroalergénio foram classificados como atópicos. Os restantes 10 doentes tinham TCP negativos para todos os aeroalergénios testados, constituindo o grupo controlo.
Determinaram-se e compararam-se os resultados dos índices de sensibilidade, especificidade, valor preditivo negativo e valor preditivo positivo do ImmunoCAP® Rapid e do Phadiatop® inalante no rastreio de atopia, assumindo como método gold standard os TCP. Foi ainda avaliada a concordância entre os TCP e o ImmunoCAP® Rapid individualmente para cada um dos aeroalergénios testados.
RESULTADOS
Realizaram-se 400 leituras com o ImmunoCAP® Rapid (10 aeroalergénios testados para cada doente). Com este método, obteve-se uma sensibilidade de 90% e um valor preditivo negativo (VPN) de 77% na identificação de atopia (não identificou como alérgicos 3 doentes em 30), valores ligeiramente inferiores aos da sensibilidade e do VPN do Phadiatop®, que foi de 93% e de 83%, respectivamente.
Os dois métodos apresentaram especificidade e valor preditivo positivo (VPP) de 100% no rastreio de atopia (quadro 1).
Quadro 1
Nos indivíduos atópicos, a sensibilização predominante detectada pelos TCP, foi para Dermatophagoidespteronyssinus (77%), seguindo-se para Phleum pratense (53%) e para os epitélios de cão e de gato (cada um com 43%). No que diz respeito ao Dermatophagoides pteronyssinus, o Immuno-CAP® Rapid evidenciou um VPN de 76% e um VPP de 100% na identificação de sensibilização a este aeroalergénio.
Para a identificação de atopia obteve-se uma concordância de 92% entre o ImmunoCAP® Rapid e os TCP, correspondente a 37 resultados concordantes em 40 doentes.
Nos indivíduos atópicos, a análise por aeroalergénio dos resultados do ImmunoCAP® Rapid e dos TCP revelou uma concordância média de 88,8 ± 7,4%, variando entre 72,5% para o epitélio do cão e 100% para a Alternaria alter nata (Figura 1).
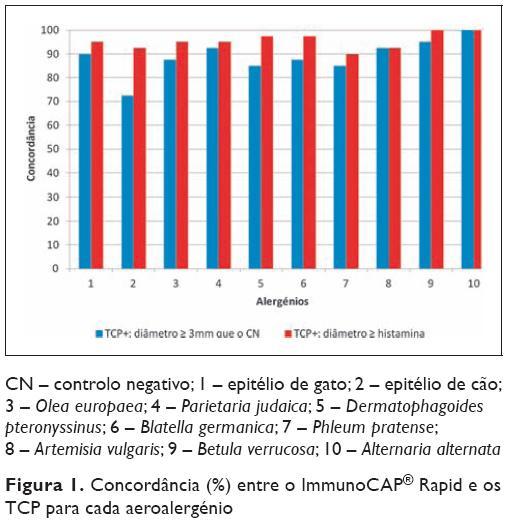
Nesta população, a concordância entre o ImmunoCAP® Rapid e os TCP foi de 85% para a sensibilização a Dermatophagoides pteronyssinus. Porém, considerando positivos os TCP com diâmetro superior ou igual ao da histamina (método muitas vezes usado na prática clínica), a concordância média entre os dois métodos aumentou para 95,5 ± 3,3%. Nos doentes não atópicos, a concordância entre o ImmunoCAP® Rapid e os TCP foi de 100%.
Relativamente aos TCP, o ImmunoCAP® Rapid não identificou pelo menos uma sensibilização em 25 dos 30 doentes atópicos (83%), totalizando-se 40 resultados negativos com TCP positivos. Dos 25 doentes em que o ImmunoCAP® Rapid não identificou pelo menos uma sensibilização, 11 (44%) tinham história de exacerbação sazonal da rinite, com TCP positivos para pólenes (Olea europaea, Phleum pratense ou Parietaria judaica) e ImmunoCAP® Rapid negativo. O número de resultados negativos no ImmunoCAP® Rapid com TCP positivos diminui para 9, se considerarmos positivos os TCP com diâmetro superior ou igual ao da histamina.
Ainda relativamente à análise por aeroalergénio, em 400 determinações de IgE específicas no ImmunoCAP® Rapid obtiveram-se cinco resultados positivos com TCP negativos para o aeroalergénio em causa.
DISCUSSÃO
O ImmunoCAP® Rapid permite, numa primeira avaliação de doentes com rinite, não só diferenciar a etiologia dos sintomas (alérgica ou não alérgica), como também quais as possíveis sensibilizações. Permite ainda que o médico proponha de imediato medidas de evicção alergénica, com planos dirigidos a alergénios específicos. Para melhor esclarecimento do perfil de sensibilização do doente, face a um controlo inadequado dos sintomas ou para avaliação de indicação para imunoterapia específica, o doente deverá ser referenciado a consulta de Imunoalergologia.
Num estudo recente, com 185 crianças com rinite moderada a grave os autores referem uma sensibilidade do ImmunoCAP® Rapid para identificação de atopia de 93% e uma especificidade de 100%7. Noutro estudo, destinado a avaliar o desempenho do ImmunoCAP® Rapid para rastreio de atopia numa população de 215 crianças entre 1 e 14 anos de idade com episódios recorrentes de sibilância, foi determinado o Phadiatop® infantil e doseadas a IgE total e as IgE específicas para os 10 alergénios presentes no ImmunoCAP® Rapid. As crianças foram identificadas como atópicas de acordo com os seus sintomas e sinais e pelo menos um doseamento de IgE específica positiva (≥ 0,35 kU/L). A sensibilização predominante foi o Dermatophagoides pteronyssinus (39%). A sensibilidade para o diagnóstico de sensibilização a este alergénio foi de 90% e a especificidade de 88%. A sensibilidade do ImmunoCAP® Rapid para estudo de atopia foi de 91%, do Phadiatop® infantil foi de 96% e da IgE total de 68%, concordante com as conhecidas limitações deste método8.
Um outro trabalho foi efectuado com o objectivo de determinar a validade do ImmunoCAP® Rapid na avaliação de atopia numa população de 175 crianças com rinite, eczema ou episódios recorrentes de sibilância. Os doentes foram avaliados numa única consulta em dois centros de referência de alergologia pediátrica. Comparou-se o resultado do ImmunoCAP® Rapid como método de estudo de atopia com o diagnóstico efectuado pelo médico especialista.
O ImmunoCAP® Rapid apresentou uma sensibilidade para o diagnóstico de atopia de 94%, com uma taxa de falsos positivos de 1%9.
No presente estudo, o ImmunoCAP® Rapid obteve valores de sensibilidade e de especificidade para a identificação de atopia semelhantes aos descritos na literatura7-9, onde estão também reportados valores de sensibilidade para o rastreio de atopia semelhantes para o ImmunoCAP® Rapid e para o Phadiatop® 9.
A sensibilidade e o valor preditivo negativo do ImmunoCAP® Rapid para a avaliação de atopia foram ligeiramente inferiores aos do Phadiatop®. A especificidade e o valor preditivo positivo destes dois métodos foram bastante elevados.
Como já largamente referenciado na literatura, o doseamento de IgE total não é um bom método de rastreio de atopia devido à sua fraca sensibilidade, na medida em que indivíduos atópicos podem ter níveis considerados normais de IgE total5,10, razão pela qual não o incluímos no nosso estudo. Relativamente ao Phadiatop® inalante, apresenta uma sensibilidade semelhante ao ImmunoCAP® Rapid, podendo ser utilizado no rastreio de doença atópica, não permitindo, no entanto, identificar o perfil de sensibilização do doente, podendo ser necessária a realização de exames adicionais11-13.
Em 400 determinações de IgE específicas no Immuno-CAP® Rapid, apenas se detectaram 5 resultados positivos com TCP negativos, o que corresponde a uma taxa de falsos positivos de 1,2%, valor semelhante ao previamente publicado9. Resultados falsos positivos de TCP podem ser justificados por dermografismo ou reacções irritativas e falsos negativos por extractos de má qualidade, medicação com determinados fármacos, certas doenças que atenuam a resposta cutânea ou devido a técnica imprópria1. Importa realçar que o ImmunoCAP® Rapid pode ser bastante útil quando não é possível realizar os TCP, como acontece nos doentes sob terapêutica com anti-histamínicos ou anti-depressivos (em que a sua suspensão pode não ser apropriada), doentes com dermografismo, urticária ou eczema generalizados, com infecção cutânea aguda ou durante a gravidez. Nestes casos, a identificação de IgE específica para aeroalergénios comuns através do ImmunoCAP® Rapid, pode ser feita numa avaliação inicial, com resultados imediatos, por parte do médico prestador de cuidados primários de saúde. É importante salientar que TCP ou ImmunoCAP® Rapid positivos por si só, apenas traduzem sensibilização a determinado alergénio, sendo sempre necessário correlacionar com a história clínica e exame físico para se estabelecer um diagnóstico correcto1.
Concluindo, o ImmunoCAP® Rapid é um método rápido, acessível e de fácil execução, que atendendo aos seus valores de sensibilidade e VPN, poderá ser considerado um método aceitável para rastreio de atopia em doentes com rinite. A análise do seu desempenho por aeroalergénio revelou, no entanto, que comparativamente aos TCP, o ImmunoCAP® Rapid pode não permitir a identificação de todas as sensibilizações a aeroalergénios clinicamente relevantes numa elevada percentagem de doentes (83%). Este aspecto é fundamental se tivermos em conta que grande parte dos doentes cuja sensibilização não foi identificada pelo ImmunoCAP® Rapid, tinha um perfil de sensibilização a ácaros e pólenes. Nestes doentes é desejável delinear estratégias para um melhor controlo da doença, nomeadamente com base em medidas de evicção. Estes resultados não poderão ser extrapolados para uma população de doentes de uma Consulta de Medicina Geral e Familiar, em que a condição de atópico terá previsivelmente uma prevalência diferente da população deste estudo. Considera-se assim imprescindível a referenciação a uma consulta de Imunoalergologia para um estudo alergológico posterior, para melhor caracterização do perfil de sensibilização do doente, com vista a uma optimização terapêutica.
REFERÊNCIAS
1. Bousquet J, Khaltaev N, Cruz AA, Denburg J, Fokkens WJ, Togias A, et al. Allergic Rhinitis and its Impact on Asthma (ARIA) 2008 Update (in collaboration with the World Health organization, GA2LEN and AllerGen). Allergy 2008;63(Suppl 86):8-160. [ Links ]
2. Mølgaard E, Thomsen SF, Lund T, Pedersen L, Nolte H, Backer V. Differences between allergic and nonallergic rhinitis in a large sample of adolescents and adults. Allergy 2007;62:1033-7. [ Links ]
3. Mösges R, Klimek L. Todays allergic rhinitis patients are different: new factors that may play a role. Allergy 2007;62:969-75. [ Links ]
4. Morais -Almeida M, Loureiro C, Todo -Bom A, Nunes C, Pereira C, Delgado L, et al. Avaliação da prevalência e caracterização da rinite em utentes dos cuidados de saúde primários de Portugal Continental – estudo ARPA. Rev Port Imunoalergologia 2005;13:69-80. [ Links ]
5. Tang RB, Wu KK. Total serum IgE, allergy skin testing, and the radioallergosorbent test for the diagnosis of allergy in asthmatic children. Ann Allergy 1989;62:432-5. [ Links ]
6. Dreborg S. Allergen standardization and skin tests. EAACI position paper. Allergy 1993;48(Suppl.14):49-82. [ Links ]
7. Eigenmann PA, Kuenzli M, DApuzzo V, Kehrt R, Joerg W, Reinhardt M, et al. The ImmunoCAP Rapid wheeze/rhinitis child test is useful in the initial allergy diagnosis of children with respiratory symptoms. Pediatr Allergy Immunol 2009;20:772-9. [ Links ]
8. Diaz -Vazquez C, Torregrosa-Bertet MJ, Carvajal-Urueña I, Cano-Garcinuño A, Fos-Escrivà E, García-Gallego A, et al. Accuracy of ImmunoCAP Rapid in the diagnosis of allergic sensitization in children between 1 and 14 years with recurrent wheezing: the IReNE study. Pediatr Allergy Immunol 2009;20:601-9. [ Links ]
9. Sarratud T, Donnanno S, Terracciano L, Trimarco G, Martelli A, Petersson CJ, et al. Accuracy of a point -of -care testing device in children with suspected respiratory allergy. Allergy Asthma Proc 2010;31:11-7. [ Links ]
10. Fajraoui N, Charfi MR, Khouani H, Abouda M, Kerkenil Y, Zouari B. Contribution of serum total immunoglobulin E measurement in the diagnosis of respiratory allergic diseases. Tunis Med 2008;86:32 -7. [ Links ]
11. Bchir F, Chabbou A, Basly W, Guilloux L, Kamel A, Jeguirim MS, et al. The role of phadiatop in the screening of respiratory allergy. Arch Inst Pasteur Tunis 1989;66:25-31. [ Links ]
12. Campillo Navarrete R, Silva RI, Castillo F. Phadiatop: a new in vitro test for diagnosing respiratory allergy. Rev Alerg 1991; 38:128-30. [ Links ]
13. Cantani A, Ferrara M, Barbieri C, Monteleone A, Businco L. Evaluation of new test (Phadiatop) for the screening of respiratory allergic disorders in children. Ann Allergy 1990;64:158-61. [ Links ]
José Geraldo Dias
Serviço de Imunoalergologia
Hospital de Santa Maria, Centro Hospitalar Lisboa Norte
Av. Prof. Egas Moniz
1649-035 Lisboa
E-mail: ze.geraldodias@gmail.com
AGRADECIMENTOS
Os autores agradecem à Thermo Fisher Scientific (Phadia) a cedência dos dispositivos ImmunoCAP® Rapid.
Financiamento: Nenhum.
Declaração de conflitos de interesse: Nenhum
Data de recepção / Received in: 06/03/2012
Data de aceitação / Accepted for publication in: 29/08/2012














