Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Revista Portuguesa de Imunoalergologia
versão impressa ISSN 0871-9721
Rev Port Imunoalergologia vol.21 no.2 Lisboa abr. 2013
Utilização conjunta do CARAT e função respiratória na avaliação do controlo da asma e rinite
Use of CARAT and lung function tests to assess control of asthma and rhinitis
Ana Pereira1, Carla Martins1, João Fonseca1,2,3
1Serviço de Imunoalergologia, Centro Hospitalar São João, Porto
2 Departamento de Ciências da Informação e da Decisão em Saúde, Faculdade de Medicina, Universidade do Porto
3 Imunoalergologia, Instituto e Hospital CUF Porto
RESUMO
Fundamentos: Questionários estandardizados e avaliação funcional respiratória são ferramentas essenciais na avaliação do doente com sintomas de asma e/ou rinite. Objectivos: 1) descrever os parâmetros funcionais respiratórios e resultados do CARAT numa série consecutiva de casos de asma e/ou de rinite; 2) estudar nestes doentes a associação entre o CARAT e função respiratória. Métodos: Estudo descritivo, retrospectivo, incluindo os adultos que realizaram espirometria com broncodilatação (BD) entre Fevereiro 2011 e Julho 2012 no serviço de Imunoalergologia de um hospital universitário; os participantes foram convidados a responder ao CARAT como parte da avaliação. As espirometrias com BD e a fracção exalada de óxido nítrico (FeNO) foram realizadas de acordo com as recomendações da ERS/ATS. Controlo da asma e rinite foi definido como pontuação global no CARAT(T) ≥24; controlo das vias aéreas superiores (CARAT(S)) se pontuação >8, e inferiores (CARAT(I)) se pontuação >15. Resultados: Foram incluídos 1200 indivíduos, com idade média (desvio padrão) de 39,3 (14,6) anos; 49% tinham diagnóstico de asma e rinite (AR), 13% asma isolada e 13% rinite isolada. A mediana (variação inter-quartil) do FeNO foi mais elevada nos indivíduos com AR comparando com indivíduos com asma ou rinite isoladas. A prevalência de mau controlo foi superior a 75% nos participantes com diagnóstico de asma, rinite e AR; 60% dos indivíduos com asma isolada apresentavam mau controlo das vias aéreas superiores. A correlação entre as pontuações do CARAT(I) e a %FEV1 foi fraca quando considerando todos os participantes (coeficiente de correlação (CC)=0,174); o subgrupo com correlação mais elevada foi o dos indivíduos com exacerbações recentes (CC=0,359). Conclusões: A maioria dos doentes apresentou pontuações baixas no CARAT. Uma elevada proporção de doentes com diagnóstico de asma apresentou baixa pontuação no CARAT(S), sugerindo subdiagnóstico e/ou desvalorização das queixas nasais. Os doentes com exacerbações recentes apresentaram as correlações mais elevadas entre o CARAT e a %FEV1.
Palavras-chave: Asma, espirometria, FeNO, questionário, rinite.
ABSTRACT
Background:Standardized questionnaires and lung function are essential tools in the evaluation of patients with asthma and/or rhinitis. Objectives: 1) to describe lung function parameters and results of CARAT in a consecutive series of asthma and/or rhinitis cases; 2) to study, in these patients, the correlation between lung function tests and CARAT results. Methods: Descriptive, retrospective study, including all the adults that performed spirometry with bronchodilation (BD) test between February 2011 and July 2012 in the Immunoallergy Department of a university hospital; individuals were asked to complete CARAT. Spirometry and exhaled fraction of nitric oxide (eNO) were performed according to the ERS/ATS recommendations. Control of asthma and rhinitis was defined by CARAT total score (CARAT (T)) ≥24; upper airways (S) control if CARAT (S) > 8; lower airways (I) control if CARAT (I) >15. Results: Overall, 1200 individuals were included, with mean age (standard deviation) 39.3 (14.6) years; 49% has asthma and rhinitis (AR) diagnosis, 13% asthma alone and 13% rhinitis alone. The median (interquartil variation) of eNO has higher in those with AR, when comparing with individuals with asthma or rhinitis alone. The prevalence of poor control was higher than 75% in all the diagnosis groups; 60% of those with asthma alone presented poor control of upper airways symptoms. Correlation between CARAT (I) and %FEV1 was weak when considering all the participants (correlation coefficient (CC)=0.174); the highest CC was found in those with recent exacerbation (CC=0.359). Conclusions: Most of the patients presented low scores in CARAT. A high proportion of individuals with asthma alone presented low CARAT (S) scores, suggesting underdiagnosis of rhinitis. Individuals with recent exacerbations presented the highest correlation between CARAT scores and %FEV1.
Keywords: Asthma, eNO, questionnaire, rhinitis, spirometry.
INTRODUÇÃO
As recomendações mais recentes da Global Initiative for Asthma (GINA)1 destacam que o principal objetivo no tratamento da asma é atingir e manter o controlo clínico.
Na GINA, a classificação do controlo baseia-se na presença/ausência de sintomas de asma durante o dia, limitação das actividades, sintomas noturnos/acordares, necessidade de medicação de alívio, exacerbações e função pulmonar (volume expiratório forçado no primeiro segundo – FEV1 – ou fluxo expiratório máximo – PEF)1. O uso de medidas objectivas de avaliação de sintomas e função respiratória seria, portanto, a forma mais adequada de avaliar o controlo da asma. Nas recomendações do Expert Panel Report 3 (EPR3)2 é sugerido que cada uma dessas medidas permite avaliar diferentes domínios do controlo da asma. Os questionários de controlo de sintomas, por exemplo o Asthma Control Test – ACT3 ou o Asthma Control Questionnaire – ACQ4, permitem uma avaliação do dano causado pela doença; as provas funcionais respiratórias são geralmente usadas na avaliação do risco, correspondendo a uma medida de previsão de eventos adversos no futuro.
Apesar do carácter complementar da avaliação funcional respiratória e dos questionários de sintomas, nem sempre há possibilidade de utilização de ambas as medidas.
Torna-se portanto essencial perceber de forma adequada a associação entre elas. Estudos anteriores mostraram uma correlação fraca entre os valores da percentagem do previsto do volume expiratório forçado no primeiro segundo (%FEV1) e o resultado de questionários de avaliação do controlo da asma5 -7. Esse achado apoia a existência de diferentes domínios na avaliação do controlo.
Atingir e manter o controlo da asma implica, para além da avaliação e tratamento adequados da doença, a identificação e abordagem de patologias concomitantes que possam interferir no seu controlo. A rinite alérgica está frequentemente associada à asma e o seu controlo interfere no controlo da asma8. A necessidade de abordar concomitantemente a asma e a rinite (AR) alérgica é enfatizada nas recomendações do Allergic Rhinitis and its Impact on Asthma (ARIA)8,9; no entanto os instrumentos disponíveis para avaliar objectivamente o controlo da AR alérgica são escassos. O questionário Controlo da Asma e Rinite Alérgica – Teste (CARAT)10,11 é o único questionário validado que avalia concomitantemente o controlo da asma e da rinite alérgica. Este questionário foi desenvolvido em Portugal; o seu desenvolvimento e validação envolveu mais de 100 especialistas portugueses em AR alérgica10 e mais de 200 doentes10,11. Actualmente está a ser traduzido em múltiplas línguas, permitindo uma utilização em vários países12.
Não encontramos nenhum estudo publicado que tenha avaliado a associação entre os resultados do questionário CARAT e parâmetros espirométricos e de inflamação brônquica.
OBJECTIVOS
O objectivo principal deste trabalho é descrever os parâmetros funcionais respiratórios e os resultados do questionário CARAT numa série consecutiva de doentes com asma e/ou rinite seguidos numa consulta de Imunoalergologia de um hospital universitário. Como objectivo secundário pretende-se estudar associações entre os resultados do questionário CARAT, os parâmetros espirométricos e a fracção exalada de óxido nítrico (FeNO).
MÉTODOS
Desenho de estudo
Estudo observacional, retrospectivo, tendo como popu lação alvo os doentes com asma e rinite seguidos no Serviço de Imunoalergologia (SIA) do Centro Hospitalar São João (CHSJ). A seleção dos doentes foi feita com base no registo do laboratório de provas funcionais respiratórias do SIA, considerando a totalidade das avaliações funcionais respiratórias realizadas entre 1 de Fevereiro de 2011 e 10 de Julho de 2012 (período total incluído de 17 meses). Durante esse período todos os doentes que realizaram espirometria com prova de broncodilatação (BD) foram convidados a preencher o questionário CARAT como parte integrante da avaliação. Foram colhidos dados relativos a parâmetros espirométricos (percentagem do previsto do FEV1 (%FEV1), classificação da espirometria, resultado da prova de BD), descrição de características demográficas e antropométricas (idade, género, índice de massa corporal – IMC), resultados do CARAT, outras avaliações realizadas (por exemplo, medição da fracção exalada de óxido nítrico – FeNO), diagnóstico clínico, estado de atopia, medicação em curso e exacerbações recentes.
Instrumentos de avaliação
Questionário CARAT. O CARAT é um questionário de auto-preenchimento que avalia o controlo da AR nas últimas 4 semanas; é constituído por 10 questões divididas em dois scores: o score 1 (CARAT (S)), constituído por 4 questões relativas a sintomas das vias aéreas superiores, e o score 2 (CARAT (I)), incluindo 4 questões especificamente relacionadas com sintomas das vias aéreas inferiores, 1 com impacto dos sintomas no sono e 1 com uso de medicação adicional (avaliadas em conjunto)11. Na versão final todas as questões são pontuadas numa escala de Likert com 4 pontos; a pontuação total (CARAT (T)) pode variar entre 0 e 30 pontos, correspondendo, respectivamente, ao pior e melhor controlo possíveis.
Espirometria com prova de broncodilatação. Todas as espirometrias foram realizadas de acordo com as recomendações da European Respiratory Society/American Thoracic Society (ERS/ATS)13 usando um espirómetro Jaeger, MasterScope® (VIASYS Healthcare, Hoechberg, Alemanha).
As provas de BD foram realizadas com 400μg de salbutamol administrados através de câmara expansora, excepto quando havia contra-indicação para administração de beta-adrenérgico (arritmia, intolerância ou hipersensibilidade ao salbutamol, entre outros); nessas situações foi feita broncodilatação com 80μg de brometo de ipratrópio em câmara expansora. A espirometria pós-broncodilatação foi realizada 15 minutos após a administração de salbutamol e 30 minutos após administração de brometo de ipratrópio.
Medição da fracção exalada de óxido nítrico (FeNO). A medição do FeNO foi feita de acordo com as recomendações da ERS/ATS, usando medição online com fluxo constante de 50mL/s; o aparelho usado foi um Niox (Aerocrine AB, Solna, Suécia).
Colheita de dados
Os dados relativos a parâmetros espirométricos, características antropométricas, resultados do CARAT e medição do valor de FeNO foram colhidos por consulta da base de dados de registo habitualmente usada no laboratório de avaliação funcional. Os dados relativos a diagnóstico clínico, estado de atopia, terapêutica em curso e exacerbações foram obtidos por revisão dos processos clínicos eletrónicos (Sistema de Apoio ao Médico, SAM), incluindo registos clínicos das consultas médicas no SIA e codificação diagnóstica disponível no sistema, de acordo com o ICD-9 (International Classification of Diseases, version 9); nos doentes em que não foi possível classificar o estado de atopia com base na informação dos registos clínicos, os resultados dos estudos analíticos disponíveis foram também revistos. Na revisão dos processos, foram considerados os dados relativos a tratamentos em curso de forma regular na altura da avaliação funcional ou tratamentos transitórios passiveis de interferir nos resultados (por exemplo cursos de corticóide oral); sempre que havia informação explícita nos registos clínicos indicando ausência total de adesão ao tratamento nas 2 semanas anteriores às provas funcionais respiratórias foi considerado que os doentes não estavam sob tratamento habitual.
Definições e classificações
As definições das variáveis usadas são apresentadas no Quadro 1.
As espirometrias foram classificadas em normais, obstrução de pequenas vias aéreas (com FEV1 normal), alteração ventilatória restritiva, alteração ventilatória mista e obstrutivas ligeira (FEV1 ≥70%), moderada (50% ≤FEV1 <70%) e grave (FEV1 <50%). A classificação em alteração ventilatória obstrutiva foi baseada na relação entre o volume expiratório forçado no primeiro segundo e a capacidade vital forçada (FEV1/FVC), considerando que uma relação FEV1/FVC <70% traduz obstrução das vias aéreas; a classificação da gravidade da obstrução foi adaptada a partir da recomendada pela ATS / ERS13. A classificação em alteração ventilatória restritiva foi feita considerando a percentagem do previsto do FVC (restrição se 80%) e a classificação em alteração ventilatória mista baseou-se na presença de FVC <80% e numa relação FEV1/FVC <70%; esta classificação é limitada pela ausência de dados pletismográficos.
As provas de broncodilatação foram classificadas de acordo com recomendações ATS / ERS13, considerando como critério de positividade a presença de um aumento de pelo menos 200mL e 12% no FEV1.
Os valores de FeNO foram interpretados com a ajuda da aplicação FeNO interpretation Aid14, que permite estimar a percentagem do previsto para o FeNO (%FeNO) utilizando os valores de referência publicados por Olin et al15; esta estimativa entra em consideração com características individuais do doente, tais como idade e altura. As %FeNO foram posteriormente classificadas em normal (até 150% do previsto), inflamação provável (entre 151 e 300%) e inflamação presente (>300%). Adicionalmente, os valores de FeNO foram classificados de acordo com as recomendações da ATS16 publicadas em 2011; esta classificação inclui 3 classes: baixo (FeNO<25 ppb) – baixa probabilidade de inflamação eosinofílica; intermédio (25≤FeNO≤50) – interpretar com cautela; e alto (FeNO>50 ppb) – elevada probabilidade de inflamação.
Participantes
Foram incluídos todos os doentes com idade igual ou superior a 18 anos que realizaram espirometria com prova de broncodilatação no laboratório de provas funcionais do SIA durante o período do estudo. Foram excluídos os doentes com incapacidade para realizar a manobra espirométrica ou incapazes de completar autonomamente o questionário CARAT (por exemplo por analfabetismo, cegueira, défice cognitivo, entre outros) (Figura 1). Não foi possível excluir os doentes com patologias concomitantes passíveis de interferir com o controlo da asma e/ou rinite. Todos os doentes incluídos eram seguidos no SIA; não foi estabelecido um tempo mínimo de seguimento para inclusão no estudo. Nos doentes com mais de uma avaliação no período do estudo foi incluída apenas a mais recente.
Análise estatística
A análise estatística foi feita utilizando o programa SPSS (IBM® SPSS, Chicago, IL, Estados Unidos da América), versão 19.
O índice de massa corporal foi recodificado em classes de acordo com uma simplificação da classificação sugerida pela Organização Mundial de Saúde17; as classes usadas foram: magreza (IMC <18,5), peso normal (18,5 ≤IMC <25), excesso de peso (25≤ IMC <30) e obesidade (IMC ≥30).
Foram usadas medidas descritivas adequadas aos vários tipos de variáveis, incluindo proporções e intervalos de confiança a 95% (variáveis categóricas), médias e desvios padrão (variáveis contínuas com distribuição normal) e medianas e variações inter-quartil (variáveis contínuas com distribuição não normal). Foi feita comparação de proporções usando o teste de qui-quadrado e comparação de médias usando o teste t-student para amostras independentes.
Para comparação de mais de 2 grupos foi usado o ANOVA (Analysis of Variance). Foram usadas barras de erro a 95% para representar a média [intervalo de confiança a 95%] das pontuações do CARAT de acordo com o diagnóstico médico. As associações entre os resultados do CARAT e a percentagem do previsto do FEV1, entre os resultados do CARAT e os valores de FeNO e entre a %FEV1 e FeNO foram calculadas usando a correlação de Spearman e representadas, quando aplicável, através de coeficientes de correlação (CC); adicionalmente foi feita análise para subgrupos de indivíduos, considerando o diagnóstico médico, género, índice de massa corporal, estado de atopia, tratamento em curso e exacerbações.
Foram calculadas proporções de discordância na comparação das duas formas de classificação do FeNO (classificação ATS e percentagem do previsto).
Um p<0,05 foi considerado como estatisticamente significativo.
RESULTADOS
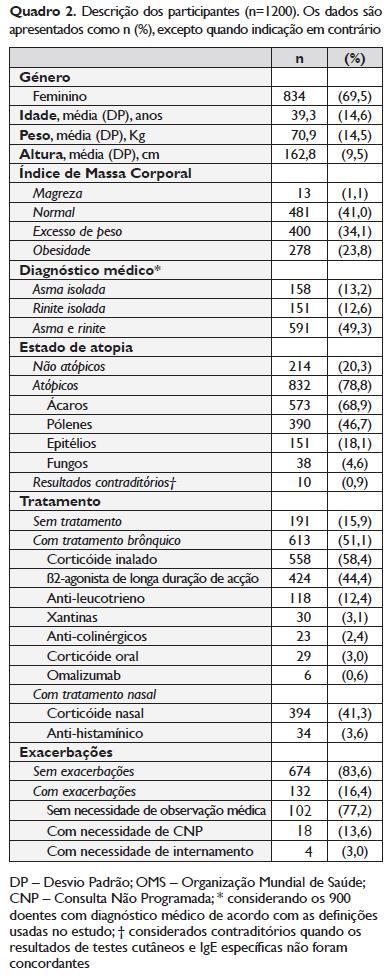
Foram incluídos 1200 indivíduos (Figura 1), cujas características estão descritas no Quadro 2; noventa e um porcento dos doentes incluídos tinham pelo menos uma consulta no SIA prévia àquela em que foi feita a avaliação funcional respiratória. Quarenta e nove porcento dos participantes tinham diagnóstico médico de AR, 13% de asma isolada e 13% de rinite isolada.
Em média, a %FEV1 foi mais elevada nos indivíduos com rinite isolada e mais baixa nos participantes com asma isolada (Quadro 3). Quase 70% dos indivíduos com asma tinham espirometria com alterações (vs. 3% dos com rinite e 41% dos com AR). Quatro porcento dos participantes com rinite, sem registo de diagnóstico de asma, tiveram prova de broncodilatação positiva.
A mediana (variação inter-quartil – VIQ) do FeNO foi mais elevada nos indivíduos com asma e rinite quando comparada com indivíduos com asma ou rinite isoladas (Quadro 3). Nos indivíduos atópicos o FeNO foi significativamente mais alto do que nos não atópicos (27(14 -55)ppb vs. 14(8 -27) ppb, respectivamente); esta diferença manteve -se na comparação entre classes do FeNO, nas duas classificações usadas (p<0,001 em ambas). A proporção de discordância entre a classificação do FeNO usando a percentagem do previsto e a classificação da ATS foi de 15,1%.
Não se encontraram diferenças estatisticamente significativas nas pontuações médias do CARAT (T) entre os indivíduos com asma, rinite e AR (Quadro 3 e Figura 2). Os participantes com rinite apresentavam uma pontuação média significativamente mais elevada no CARAT (I) e mais baixa no CARAT (S), quando comparados com os indivíduos com asma e com AR (Figura 2). A prevalência de mau controlo considerando o CARAT (T) foi superior a 75% nos participantes com diagnóstico de asma, rinite e AR. Sessenta porcento dos indivíduos com asma isolada apresentavam mau controlo dos sintomas das vias aéreas superiores. Mais de 93% (124) dos indivíduos com história de exacerbações apresentavam mau controlo no CARAT (T) (vs. 78% dos que não tiveram exacerbações); o odds ratio [intervalo de confiança a 95%] (OR[IC95%]) para exacerbações nos indivíduos com mau controlo foi de 4,3 (2,1 -9,0).
As correlações entre as pontuações do CARAT e a %FEV1 para todos os incluídos e para os indivíduos com asma e rinite estão representadas no Quadro 4. As correlações foram globalmente mais elevadas e significativas para o CARAT (I), apresentando o valor mais elevado nos indivíduos com exacerbações recentes (CC=0,359); nos participantes do género feminino, nos não atópicos e nos indivíduos com obesidade (considerando todos os incluídos) as correlações do CARAT (I) foram superiores a 0,200. As correlações da %FEV1 com a pontuação CARAT (S) foram, na maior parte dos casos, não significativas.
As correlações entre as pontuações do CARAT e os valores de FeNO foram não estatisticamente significativas, quer para o total de incluídos quer para os subgrupos analisados (incluindo categorias de diagnóstico médico – asma, rinite, asma e rinite; género; índice de massa corporal; estado de atopia; tratamento em curso; e exacerbações) (dados não apresentados).
Foi encontrada uma correlação significativa, negativa, entre os valores de FeNO e %FEV1 nos indivíduos não atópicos com asma e rinite (CC= -0,510; p=0,007); nos atópicos a correlação não foi estatisticamente significativa (CC=0,092, p=0,216). Se forem considerados todos os indivíduos incluídos, independentemente do diagnóstico, o significado estatístico não se mantém.
DISCUSSÃO
A prevalência de mau controlo dos sintomas de asma e rinite em indivíduos observados em consulta de Imunoalergologia de um hospital universitário foi elevada para todos os diagnósticos considerados. Tal como esperado, a correlação entre as pontuações do CARAT e a %FEV1 foi fraca quando considerando todos os participantes, no entanto, foi mais elevada nos indivíduos com exacerbações recentes.
Atingir o controlo clínico da asma e rinite é o principal objectivo do tratamento1, no entanto, vários estudos têm mostrado prevalências elevadas de mau controlo da AR, mesmo em indivíduos tratados1,18,19. Neste estudo, a prevalência global de mau controlo, avaliada pelo CARAT (T), foi superior a 80%. Estes resultados poderão traduzir uma maior gravidade das patologias respiratórias nos indivíduos seguidos em consulta de especialidade, existindo no entanto outros fatores a considerar, tais como adesão ao tratamento e comorbilidades1,8,20.
A elevada prevalência de mau controlo dos sintomas nasais em indivíduos com diagnóstico de asma sugere uma desvalorização por parte do doente e/ou médico dos sintomas de rinite, apesar das recomendações já existentes8. A ausência de medidas simples, validadas e facilmente disponíveis para diagnóstico objectivo de rinite poderá estar na base deste subdiagnóstico e consequente sub-tratamento. A elevada prevalência de atopia era esperada pelo local de realização do estudo (consulta de Imunoalergologia) e o predomínio de sensibilização a ácaros está de acordo com dados de estudos anteriores para Portugal21.
Este é o primeiro estudo que reporta dados sobre a correlação do CARAT com parâmetros da avaliação funcional respiratória. A correlação fraca entre a pontuação do CARAT e os valores de %FEV1 e de FeNO está de acordo com os dados publicados relativamente a outros questionários de controlo5,6. Esta baixa correlação pode ser explicada, tal como anteriormente referido, considerando que o controlo da asma apresenta diferentes domínios22: o dano, habitualmente avaliado com questionários de controlo validados (nos quais se inclui o CARAT), e o risco, frequentemente avaliado através da espirometria22.
A avaliação do risco pretende estimar a probabilidade de exacerbações, perda irreversível de função respiratória e hospitalizações. A correlação encontrada entre os resultados do CARAT e a %FEV1 nos indivíduos com exacerbações, mais elevada do que nos restantes grupos, sustenta uma possível utilização do CARAT na avaliação de risco da patologia respiratória nos doentes com asma. No en tanto, são necessários mais estudos para confirmar esta hipótese.
Esta é a maior série publicada reportando dados sobre a utilização do CARAT na avaliação do controlo de asma e rinite em doentes observados em consulta hospitalar diferenciada.
É também o primeiro estudo que mostra uma associação entre o mau controlo no questionário CARAT e o risco de exacerbações da asma ou rinite. Este estudo é limitado pelo carácter retrospectivo e por se basear em revisão de processos clínicos, sem intervenção do médico assistente ou avaliação médica do controlo na data da avaliação funcional respiratória; a inclusão de uma avaliação médica do controlo, preferencialmente independente e em ocultação, nomeadamente sem conhecimento do resultado do CARAT ou das provas funcionais, seria uma mais–valia para o estudo. A existência de registos clínicos incompletos, sem referência explícita ao diagnóstico do doente, necessária para cumprir os critérios de diagnóstico usados neste estudo, e a presença de erros de codificação, poderão justificar algumas inconsistências nos resultados encontrados. Por outro lado, a medicação em curso no momento da avaliação baseia-se, também, apenas nos registos clínicos; esta forma de colheita dos dados relativos ao tratamento, sem informação fornecida pelo próprio doente, não permite excluir adequadamente possíveis situações de má-adesão terapêutica ou de automedicação que podem ter interferido nos resultados, quer do CARAT, quer da avaliação funcional respiratória.
Foi tentado ultrapassar a limitação condicionada pelos registos clínicos incompletos usando o maior número possível de alternativas em termos de definições dos diagnósticos ou estado de atopia; esta decisão, pretendendo aumentar a sensibilidade levou à perda de especificidade das definições.
Neste estudo a %FEV1 foi o único parâmetro avaliado, desvalorizando outros possíveis parâmetros de interesse5.
Atualmente está a ser programado um estudo prospectivo multicêntrico que permitirá confirmar os resultados apresentados. Esse estudo permitirá também a avaliação da relação entre o CARAT e outras variáveis da avaliação funcional respiratória, nomeadamente a variação do FEV1 após broncodilatação.
CONCLUSÃO
A elevada prevalência de mau controlo das vias aéreas superiores nos doentes com asma sugere subdiagnóstico e/ou desvalorização da patologia nasal. Os doentes com exacerbações recentes apresentaram as correlações mais elevadas entre os resultados do CARAT e a %FEV1.
REFERÊNCIAS
1. Global Initiative for Asthma (GINA), National Heart Lung and Blood Institute (NHLBI). Global strategy for asthma management and prevention. 2006; Available from: www.ginasthma.com. [ Links ]
2. National Asthma E, Prevention P. Expert Panel Report 3 (EPR-3): Guidelines for the Diagnosis and Management of Asthma-Summary Report 2007. J Allergy Clin Immunol 2007;120:S94-138. [ Links ]
3. Nathan RA, Sorkness CA, Kosinski M, Schatz M, Li JT, Marcus P, et al. Development of the asthma control test: A survey for assessing asthma control. J Allergy Clin Immunol 2004;113:59 -65. [ Links ]
4. Juniper EF, OByrne PM, Guyatt GH, Ferrie PJ, King DR. Development and validation of a questionnaire to measure asthma control. Eur Respir J 1999;14:902 -7. [ Links ]
5. Rodrigo GJ, Arcos JP, Nannini LJ, Neffen H, Broin MG, Contrera M, et al. Reliability and factor analysis of the Spanish version of the Asthma Control Test. Ann Allergy Asthma Immunol 2008;100:17 -22. [ Links ]
6. Shirai T, Furuhashi K, Suda T, Chida K. Relationship of the Asthma Control Test with pulmonary function and exhaled nitric oxide. Ann Allergy Asthma Immunol 2008;101:608 -13. [ Links ]
7. Picado C, Badiola C, Perulero N, Sastre J, Olaguíbel JM, López Viña A, et al. Validation of the spanish version of the asthma control questionnaire. Clin Ther 2008;30:1918 -31. [ Links ]
8. Bousquet J, Khaltaev N, Cruz AA, Denburg J, Fokkens WJ, Togias A, et al. Allergic Rhinitis and its Impact on Asthma (ARIA) 2008. Allergy 2008;63:8 -160. [ Links ]
9. Bousquet J, Schünemann HJ, Zuberbier T, Bachert C, Baena –Cagnani CE, Bousquet PJ, et al. Development and implementation of guidelines in allergic rhinitis – an ARIA -GA2LEN paper. Allergy 2010;65:1212 -21. [ Links ]
10. Nogueira -Silva L, Martins SV, Cruz -Correia R, Azevedo LF, Morais-Almeida M, Bugalho -Almeida A, et al. Control of allergic rhinitis and asthma test – a formal approach to the development of a measuring tool. Respir Res 2009;10:52. [ Links ]
11. Fonseca JA, Nogueira -Silva L, Morais -Almeida M, Azevedo L, Sa –Sousa A, Branco -Ferreira M, et al. Validation of a questionnaire (CARAT10) to assess rhinitis and asthma in patients with asthma. Allergy 2010;65:1042-8. [ Links ]
12. Fonseca J. A, Correia de Sousa J, Sá -e -Sousa A, Burnay E, Tsiligianni I, Nogueira-Silva L, et al. Cross-cultural adaptation of Control of Rhinitis and Asthma Test (CARAT). Prim Care Respir J 2011;20:11. [ Links ]
13. Miller MR, Hankinson J, Brusasco V, Burgos F, Casaburi R, Coates A, et al. Standardisation of spirometry. Eur Respir J 2005;26:319-38. [ Links ]
14. Fonseca J, Alving K, Jacinto T, Burnay E, Farinha P, Sa e Sousa A, et al. FENO Interpretation Aid. CINTESIS; Available from: http://feno.med.up.pt. [ Links ]
15. Olin AC, Bake B, Toren K. Fraction of exhaled nitric oxide at 50 mL/s: reference values for adult lifelong never-smokers. Chest 2007;131:1852-6. [ Links ]
16. Dweik RA, Boggs PB, Erzurum SC, Irvin CG, Leigh MW, Lundberg JO, et al. An Official ATS Clinical Practice Guideline: Interpretation of Exhaled Nitric Oxide Levels (FeNO) for Clinical Applications. Am J Respir Crit Care Med 2011;184:602-15. [ Links ]
17. World Health Organization. Obesity: preventing and managing the global epidemic. Geneve: WHO; 2000. [ Links ]
18. Siroux V, Boudier A, Bousquet J, Vignoud L, Gormand F, Just J, et al. Asthma control assessed in the EGEA epidemiological survey and health -related quality of life. Respir Med 2012;106:820-8. [ Links ]
19. Demoly P, Gueron B, Annunziata K, Adamek L, Walters RD. Update on asthma control in five European countries: results of a 2008 survey. Eur Respir Rev 2010;19:150 -7. [ Links ]
20. Benninger C, Parsons JP, Mastronarde JG. Vocal cord dysfunction and asthma. Curr Opin Pulm Med 2011;17:45 -9. [ Links ]
21. Pereira C, Valero A, Loureiro C, Davila I, Martinez -Cocera C, Murio C, et al. Iberian study of aeroallergens sensitisation in allergic rhinitis. Eur Ann Allergy Clin Immunol 2006;38:186 -94. [ Links ]
22. Wojtczak HA, Wachter AM, Lee M, Burns L, Yusin JS. Understanding the relationship among pharmacoadherence measures, asthma control test scores, and office -based spirometry. Ann Allergy Asthma Immunol 2012;109:103 -7. [ Links ]
Ana Pereira
Serviço de Imunoalergologia
Centro Hospitalar São João
Alameda Prof. Hernâni Monteiro
4200 -319 Porto
E-mail: ambrpereira@gmail.com
Financiamento: Nenhum.
Declaração de conflito de interesses: Nenhum.
Nota: Prémio SPAIC – AstraZeneca 2012 (1.º Prémio)
Data de recepção / Received in: 31/07/2012
Data de aceitação / Accepted for publication in: 05/10/2012














