Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Revista Portuguesa de Imunoalergologia
versão impressa ISSN 0871-9721
Rev Port Imunoalergologia vol.21 no.4 Lisboa dez. 2013
ARTIGO ORIGINAL
O uso de anestésico local não afecta o resultado dos testes intradérmicos
The use of local anesthetics does not affect intradermal tests results
Mariana Couto1,2, Diana Silva1, Ana Ferreira1, Eunice Castro1,3, Alice Coimbra1, Josefina Rodrigues Cernadas1,3
1 Serviço de Imunoalergologia, Centro Hospitalar São João, Porto
2 Serviço e Laboratório de Imunologia, Faculdade de Medicina da Universidade do Porto
3 Unidade de Imunoalergologia, Hospital Privado Boavista, Porto
RESUMO
Introdução: Os testes intradérmicos (TID), embora dolorosos, são essenciais no diagnóstico de alergia a fármacos e a veneno de himenópteros (VH). A utilização de anestésico tópico demonstrou reduzir significativamente a dor associada aos testes cutâneos. Objectivo: Determinar os efeitos de um patch anestésico com prilocaína e lidocaína (EMLA®) no resultado dos TID de diagnóstico de alergia a fármacos e VH. Métodos: Estudo transversal controlado, incluindo doentes com suspeita de alergia a fármacos ou VH que realizaram TID durante o seu estudo diagnóstico. Foi assinado consentimento informado. Colocou -se anestésico tópico, de acordo com as recomendações do fabricante, durante 1 hora, e repetiram-se na zona anestesiada os TID previamente positivos, controlos positivo (testes cutâneos por picada com histamina 10mg/mL) e negativo (TID com SF). Foi realizado o mesmo procedimento em doentes com TID negativos para avaliar falsos positivos. Resultados: Em 44 doentes (30 mulheres, idade média 44±19 anos) realizaram -se 53 TID: 45 com fármacos e 8 com VH. A média da pápula com histamina sem EMLA® foi de 4,9mm [IC95% 4,5;5,2] e com EMLA® de 4,8mm [IC95% 4,4;5,1]. O aumento do diâmetro médio das pápulas nos TID com fármacos foi de 4,9mm [IC95% 4,0;5,9] sem anestésico e de 4,9mm [IC95% 3,8;6,0] com anestésico. Com VH sem EMLA®, o aumento médio das pápulas foi de 3,9mm [IC95% 2,7;5,1] e com EMLA® de 4,7mm [IC95% 2,9;6,5]. Não se registaram diferenças entre os testes com e sem EMLA® na histamina (p=0,36), controlos salinos (p=0,40) e TID (p=0,72). Nenhum dos TID previamente negativos apresentou positividade com o anestésico e vice-versa. Conclusões: Este é o primeiro estudo a avaliar o uso de anestésico local nos resultados dos TID no âmbito do diagnóstico de alergia a fármacos e a VH. Comprovou-se que não interfere nos resultados. A sua introdução na prática clínica permitirá melhorar o conforto dos doentes.
Palavras-chave: Alergia a fármacos, alergia a veneno de himenópteros, anestésico local, testes intradérmicos.
ABSTRACT
Introduction: Intradermal tests (IDT), although painful, are essential for the diagnosis of drug and hymenoptera venom allergy. The use of topical anesthetics significantly reduces the pain associated with skin tests. Objective: To determine the effects of an anesthetic patch with prilocaine and lidocaine (EMLA®) on the results of IDT used for the diagnosis of drug and venom allergy. Methods: Cross -sectional controlled study including patients with suspected drug or venom allergy which underwent IDT during diagnostic workup. Informed written consent was obtained. The topical anesthetic was placed according to the manufacturers instructions for 1 hour. The IDT that were positive, as well as positive (histamine 10mg/dL skin prick test) and negative controls, were repeated on the anesthetized area. The same procedure was performed on patients with negative IDT to assess false positives. Results: Forty-four patients (30 female, average age 44±19 years) performed 53 IDTs: 45 with drugs and 8 with hymenoptera venom. The average wheal diameter of histamine without EMLA® was 4.9mm [IC95% 4.5;5.2] and with EMLA® 4.8mm [IC95% 4.4;5.1]. The increase in average wheal diameter of the IDT with drugs was 4.9mm [IC95% 4.0;5.9] without anesthesia and 4.9mm [IC95% 3.8;6.0] with anesthesia. Regarding venoms, the average increase without EMLA® was 3.9mm [IC95% 2.7;5.1] and with EMLA® 4.7mm [IC95% 2.9;6.5]. No differences were found between tests performed with and without EMLA® with respect to histamine (p=0.36), saline controls (p=0.40), and IDT (p=0.72). None of the previously negative IDTs were positive with the use of EMLA® or vice versa. Conclusions: This is the first study to evaluate the use of a local anesthetic on IDT results for diagnostic work -up of drug and venom allergy. Its use did not interfere with test results. The introduction in clinical practice will allow improving patient comfort.
Keywords: Drug allergy, intradermal tests, local anesthetic, venom allergy.
INTRODUÇÃO
Dentro das reacções adversas a medicamentos estão incluídas as de natureza alérgica, que pelas suas caraterísticas podem implicar um desafio diagnóstico. A abordagem destas reacções baseia-se na história clínica, mas esta, de forma isolada, frequentemente não é sufi ciente para identificar o agente, pois não raras vezes diferentes fármacos são administrados simultaneamente.
Por outro lado, o quadro clínico de hipersensibilidade a fármacos é muito heterogéneo. Deve proceder-se sempre à identifi cação da relação entre a administração do medicamento e os sintomas, bem como a clarificação do mecanismo patofisiológico subjacente à reacção. Desta forma, reduzem-se evicções desnecessárias pela possibilidade de uma reacção alérgica e contribui-se para o esclarecimento da epidemiologia e da fisiopatologia da alergia a fármacos1. O gold-standard para o diagnóstico é a prova de provocação ao fármaco suspeito, mas a sua utilização é frequentemente limitada pela possibilidade de ocorrência de reacções graves. Os testes cutâneos, incluindo os testes intradérmicos (TID), embora validados apenas para alguns grupos de fármacos, são largamente utilizados por serem métodos convenientes de avaliação de sensibilização, além da capacidade adicional de promoverem uma perspectiva sobre o mecanismo imunológico1,2. Quanto à alergia a veneno de himenópteros (VH), a realização de testes cutâneos é recomendada para esclarecimento diagnóstico3.
O diagnóstico implica a realização de testes cutâneos por picada (TCP), prosseguindo-se para TID se os primeiros forem negativos, sendo que a sensibilidade diagnóstica destes é de 90% ou mesmo superior4-8.
É, portanto, consensual e reconhecida a importância dos TID no processo diagnóstico de alergia a fármacos e VH. Porém, os TID são dolorosos, o que por vezes limita o seu uso1. Nos últimos anos, a medicina evoluiu e tem sido dada particular atenção à prevenção da dor iatrogénica.
Assim, os actos diagnósticos ou terapêuticos, como punções venosas, punções lombares, cateterização de artéria radial, vacinação, remoção de drenos pleurais, são muitas vezes precedidos, tanto em crianças como em adultos, da aplicação de anestésico tópico EMLA® (Eutectic Mixture of Local Anesthetics), um creme que contém lidocaína e prilocaína (AstraZeneca, Rueil-Malmaison, França)9-19. Em estudos prévios, esta formulação de anestésico tópico já demonstrou reduzir significativamente a dor associada a testes cutâneos de alergia20-22.
No entanto, porque os anestésicos locais actuam sobre a pele alterando a perfusão basal cutânea e a sua regulação23, especulou-se que a utilização de EMLA® para aliviar a dor causada pelos TID podia alterar a resposta da pápula e/ou eritema, por modificar o recrutamento de células sensibilizadas ao local. Portanto, a sua utilização no contexto do diagnóstico de alergia a fármacos ou VH foi abandonada. No entanto, esta questão nunca foi investigada, e esta prática tem assentado apenas em especulações.
O objectivo do presente trabalho foi determinar, em doentes com suspeita de alergia a fármacos ou VH, os efeitos de um patch de anestésico tópico contendo prilocaína e lidocaína sobre a pápula dos TID realizados com fármacos e VH, bem como a pápula dos controlos positivo e negativo.
MÉTODOS
Desenho do estudo e características dos doentes
Estudo transversal controlado, efectuado no Serviço de Imunoalergologia do Centro Hospitalar São João, entre Maio de 2010 e Maio de 2012. Foram incluídos doentes referenciados para realizar testes cutâneos por suspeita de reacções de hipersensibilidade imediata a fármacos ou VH, com idade superior a 8 anos de idade (TID em crianças mais jovens não são normalmente realizados no nosso Serviço, devido à dor associada ao procedimento).
Aqueles que apresentaram resultados positivos nos TID foram convidados a participar, tendo sido fornecida informação escrita sobre o estudo, assinado consentimento informado e recolhidos os dados clínicos. Os doentes foram controlos de si mesmos e os TID repetidos no próprio dia no braço contralateral, após colocação do patch EMLA®. Consideraram -se critérios de exclusão: reacções de hipersensibilidade tardia, gravidez ou amamentação, reacções de hipersensibilidade anteriores aos anestésicos locais, reacções prévias graves durante realização de TID, doentes com meta -hemoglobinemia, reacções de hipersensibilidade conhecida a outros componentes do patch EMLA® (carboxipolimetileno, hidróxido de sódio, óleo de rícino de polietilenoglicol 35 e água purificada) e todos sob qualquer terapêutica sistémica com potencial de interferir com o resultado dos TID1.
Foi incluída secundariamente uma amostra de doentes com história de reacções de hipersensibilidade imediata a fármacos, mas TID negativos, para avaliar a possível ocorrência de resultados falsos positivos com a utilização de anestésico tópico.
O estudo foi realizado em conformidade com a Declaração de Helsínquia de investigação médica envolvendo Seres Humanos.
Procedimentos e avaliação
O patch é um disco de celulose absorvente, saturado com 1 g de emulsão EMLA® a 5% e consiste num sistema de emulsão de óleo -água, no qual a fase com óleo é composta por uma mistura eutéctica das formas de base de lidocaína (25 mg/g) e prilocaína (25 mg/g); como excipientes contém carboxipolimetileno, hidróxido de sódio, 19 mg/g de óleo de rícino de polietilenoglicol 35 e água purificada.
Antes da realização do TID, o patch< foi aplicado de acordo com as recomendações do fabricante durante 1 hora na face anterior do antebraço.
Os TID foram efectuados de acordo com as recomendações internacionais da Academia Europeia de Alergologia e Imunologia Clínica (EAACI)1, tendo também sido realizadas injecções intradérmicas de controlo salino (controlo negativo). Vinte minutos depois, era observado o local e considerada uma reacção positiva se tivesse ocorrido um aumento da pápula inicial, igual ou superior a 3 mm, associado a eritema1. O resultado era demarcado com caneta e decalcado com fita transparente, sendo arquivado em papel. Posteriormente calculou-se o diâmetro médio das pápulas inicial e final, medindo o maior diâmetro e o seu perpendicular com uma régua milimétrica1. Foram realizados exactamente os mesmos passos na área anestesiada, após remoção do EMLA®.
O controlo positivo foi realizado com recurso à técnica de TCP, utilizando histamina (10mg/mL, Leti® Laboratórios, Madrid, Espanha) na face anterior do antebraço.
Quinze minutos depois, o resultado era delineado com caneta e decalcado com fita transparente, sendo também arquivado em papel. Posteriormente calculou-se o diâmetro médio da pápula final, medindo o maior diâmetro e o seu perpendicular com uma régua milimétrica. Foram realizados exactamente os mesmos passos na área anestesiada, após remoção do EMLA®.
Registaram-se os efeitos adversos (que incluem palidez no local de aplicação do anestésico, eritema, discreto edema ou dermatite de contacto).
Análise estatística
Na análise estatística foi utilizado o SPSS – statistical package version 20.0 for Windows (IBM SPSS, Chicago, Estados Unidos da América). As variáveis contínuas são apresentadas como médias e intervalo de confiança (IC) a 95%, ou desvio -padrão no caso específico da variável idade. Foi aplicada transformação logarítmica quando se verificou a não -normalidade da amostra, e apresentada a mediana.
No caso dos testes cutâneos por picada com histamina e dos TID com controlo salino, usou-se para fins estatísticos a pápula final (medida após 15 e 20 minutos, respectivamente).
No caso dos TID com fármacos e VH, utilizou-se o aumento da pápula ao fim de 20 minutos, tendo-se calculado da seguinte forma: diâmetro médio da pápula final – diâmetro médio da pápula inicial. Para comparar o aumento das pápulas com e sem EMLA®, utilizou-se o teste t de Student para amostras emparelhadas, ou o teste de Wilcoxon no caso de variáveis sem distribuição normal (p<0,05).
O tamanho da amostra foi calculado assumindo uma diferença entre os TID dos casos e controlos, e utilizando teste t de Student para amostras emparelhadas, de 0,5 mm, um desvio-padrão de 120 e um poder (1 – β) de 90% e um nível de significância de 0,05, tendo-se obtido um número de TID necessários de 44.
RESULTADOS
Foram incluídos 44 doentes (idade média 44±19 anos, todos caucasianos, 30 do sexo feminino), tendo sido realizados 53 TID. Destes, 37 apresentavam TID positivos com fármacos (14 com antibióticos, 10 com anestésicos gerais, 6 com anti-inflamatórios não esteróides, 3 com contrastes iodados e 4 com anti-histamínicos (anti -H) – 3 anti -H1 e 1 anti -H2) e 8 com VH (7 com extracto de abelha e 1 com extracto de vespa). Os restantes 8 TID foram realizados em doentes com TID previamente negativos (1 com piridoxina e os restantes com antibióticos). No Quadro 1 encontram-se representados os fármacos utilizados.
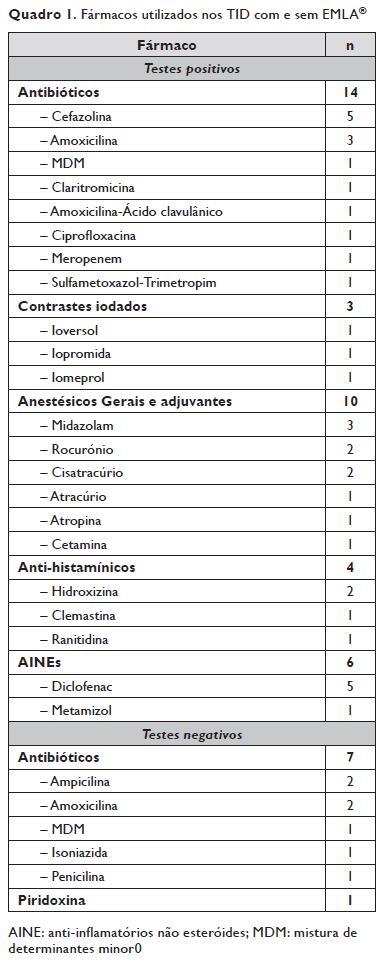
Não foram observadas diferenças nos testes cutâneos com e sem anestésico tópico no que diz respeito a TID com fármacos, VH, controlo salino ou TCP com histamina (Quadro 2). Em nenhum dos doentes se observou negativação dos TID previamente positivos.
De igual forma, nenhum dos oito doentes com TID negativos apresentou positividade nos TID realizados na área anestesiada.
Não foram reportados quaisquer efeitos laterais, imediatos ou tardios.
DISCUSSÃO
Este estudo mostra que a leitura dos TID não é significativamente afectada pelo uso de um patch anestésico contendo lidocaína e prilocaína, apesar da especulação teórica do seu papel em potencialmente reduzir o afluxo de células sensibilizadas24. Estudos anteriores tinham já evidenciado que a utilização de EMLA® diminuía de forma significativa a dor associada aos testes cutâneos20-22.
No entanto, nesses estudos, os TID foram realizados com aeroalergénios20 ou apenas com histamina e controlo negativo21,22. Esta é a primeira vez que se investiga a interferência do EMLA® na leitura de TID com fármacos e VH, tendo -se demonstrado que a sua utilização não influencia significativamente os resultados. Não foram identificados casos de resultados falsos negativos, nem ocorreu negativação de nenhum TID previamente positivo. Algumas limitações devem ser tidas em linha de conta. Como se tratou de um trabalho em ambiente real, que incluiu doentes referenciados à Unidade de Alergia a Fármacos, não foi possível seleccionar os fármacos ou VH a incluir. Por outro lado, apenas foi testada a mistura de lidocaína e prilocaína em patch, pelo que os resultados não podem ser generalizados a formulações em creme ou a outros anestésicos tópicos. Mais ainda, poder-se-ia ter utilizado uma escala visual analógica para quantificar a dor sem e com EMLA®, e nesse caso dever-se–ia ter procedido a um estudo em ocultação e controlado com placebo, mas a avaliação da dor não fazia parte do objectivo do trabalho por ter sido já demonstrado em literatura prévia20-22. Por esse motivo, foi realizado um estudo aberto.
Neste estudo destaca-se o facto de ser pioneiro e de carácter inovador, dado que é a primeira vez que se avalia a utilização de EMLA® nos resultados dos TID com fármacos e VH. Foi utilizada uma amostra de tamanho apropriado para determinar os efeitos da hipótese de estudo levantada. Por outro lado, a aplicação de um patch sempre com a mesma concentração dos anestésicos, garante a estandardização da quantidade de anestésico aplicada em cada doente. Mais ainda, os TID com e sem EMLA® foram realizados no próprio dia no mesmo doente; como os próprios doentes serviram de controlos de si mesmos, foi possível controlar eventuais efeitos confundidores que poderiam ocorrer se se tratasse de diferentes doentes ou distintas alturas. Foram incluídos apenas doentes caucasianos, de forma a evitar enviesamento dos resultados, uma vez que tem sido reportado que outras etnias, por exemplo a afro-americana, têm menor magnitude e duração dos efeitos anestésicos do EMLA®25. Não obstante o facto de não se terem incluído todas as classes de fármacos, nem um número adequado de fármacos em algumas das classes, ou de extractos de vespa, foi possível analisar um número considerável de TID. Serão naturalmente necessários, no futuro, estudos com amostras de maiores dimensões e multicêntricos para corroborar estes resultados, e generalizar a outras classes de fármacos, bem como corroborar a ausência de falsos negativos com a utilização de EMLA®.
Os estudos anteriores versando esta temática foram consensuais quanto à diminuição significativa da dor20-22, tendo no entanto divergido relativamente à leitura dos testes. Tal ocorreu nas situações em que era utilizada histamina na concentração de 0,1mg/mL e apenas com o eritema, não com o tamanho da pápula. Não se verificou, em nenhum desses trabalhos, diminuição da pápula dos TID com aeroalergénios, com controlo salino ou com histamina na concentração de 10mg/mL, utilizada e recomendada como controlo positivo. No entanto, estes trabalhos marcaram uma tendência de actuação desde então.
Com o nosso estudo demonstramos que a possibilidade de utilizar EMLA® deverá ser reconsiderada. Serão necessários mais estudos com amostras de maiores dimensões, até que possa ser considerada uma prática clínica generalizada, nomeadamente tendo em atenção o custo associado ao anestésico e o tempo necessário para a sua actuação e o reduzido número de doentes com alergia a VH incluído, mas em situações pontuais poderá ser considerado.
CONCLUSÕES
A utilização do penso impregnado EMLA® não afecta significativamente o tamanho da pápula nos testes intradérmicos com fármacos. De igual forma, não parece afectar o tamanho da pápula nos testes com veneno de himenópteros, embora neste caso a amostra seja pequena para inferir resultados definitivos. A aplicação de anestesia tópica parece ser, portanto, uma opção válida a considerar para a realização de testes intradérmicos. De
futuro, serão necessários mais estudos, com amostras de maiores dimensões e contemplando mais classes de fármacos, bem como mais extractos de veneno de himenópteros, para permitir generalizar esta opção, que se revelou segura e fidedigna, à prática clínica.
REFERÊNCIAS
1. Brockow K, Romano A, Blanca M, Ring J, Pichler W, Demoly P. General considerations for skin test procedures in the diagnosis of drug hypersensitivity. Allergy 2002;57:45-51. [ Links ]
2. Barbaud A, Reichert -Penetrat S, Trechot P, Jacquin -Petit MA, Ehlinger A, Noirez V, et al. The use of skin testing in the investigation of cutaneous adverse drug reactions. Br J Dermatol 1998;139:49 -58. [ Links ]
3. Bilo BM, Rueff F, Mosbech H, Bonifazi F, Oude -Elberink JN. Diagnosis of Hymenoptera venom allergy. Allergy 2005;60:1339-49. [ Links ]
4. Hunt KJ, Valentine MD, Sobotka AK, Lichtenstein LM. Diagnosis of allergy to stinging insects by skin testing with Hymenoptera venoms. Ann Intern Med 1976;85:56-9. [ Links ]
5. Patrizzi R, Muller U, Yman L, Hoigne R. Comparison of skin tests and RAST for the diagnosis of bee sting allergy. Allergy 1979;34:249-56. [ Links ]
6. Meriney D, Nall T, Wallace D, Rosenzweig D, Goel Z, Grieco MH. Comparison of venom and whole-body rast and intradermal testing in vespid -sensitive patients. Int Arch Allergy Appl Immunol 1980;62:442-52. [ Links ]
7. Wuthrich B, Wick H, Crass B, Wyss S. [Diagnosis of hymenoptera sting hypersensitivity. A comparison between case history, skin test results and specific IgE (RAST) with venon extracts (authors transl)]. Schweiz Rundsch Med Prax 1981;70:934-43. [ Links ]
8. Georgitis JW, Reisman RE. Venom skin tests in insect -allergic and insect -nonallergic populations. J Allergy Clin Immunol 1985;76:803-7. [ Links ]
9. Juhlin L, Evers H, Broberg F. A lidocaine -prilocaine cream for superficial skin surgery and painful lesions. Acta Derm Venereol 1980;60:544-6. [ Links ]
10. Rosdahl I, Edmar B, Gisslen H, Nordin P, Lillieborg S. Curettage of molluscum contagiosum in children: analgesia by topical application of a lidocaine/prilocaine cream (EMLA). Acta Derm Venereol 1988;68:149-53. [ Links ]
11. Halperin DL, Koren G, Attias D, Pellegrini E, Greenberg ML, Wyss M. Topical skin anesthesia for venous, subcutaneous drug reservoir and lumbar punctures in children. Pediatrics 1989;84:281-4. [ Links ]
12. Smith M, Gray BM, Ingram S, Jewkes DA. Double-blind comparison of topical lidocaine-prilocaine cream (EMLA) and lidocaine infiltration for arterial cannulation in adults. Br J Anaesth 1990;65:240-2. [ Links ]
13. Taddio A, Nulman I, Reid E, Shaw J, Koren G. Effect of lidocaineprilocaine cream (EMLA®) on pain of intramuscular Fluzone® injection. Can J Hosp Pharm 1992;45:227-30. [ Links ]
14. Taddio A, Robieux I, Koren G. Effect of lidocaine-prilocaine cream on pain from subcutaneous injection. Clin Pharm 1992;11:347-9. [ Links ]
15. Taddio A, Nulman I, Goldbach M, Ipp M, Koren G. Use of lidocaine -prilocaine cream for vaccination pain in infants. J Pediatr 1994;124:643-8. [ Links ]
16.Taddio A, Stevens B, Craig K, Rastogi P, Ben-David S, Shennan A, et al. Efficacy and safety of lidocaine -prilocaine cream for pain during circumcision. N Engl J Med 1997;336:1197-201. [ Links ]
17. Valenzuela RC, Rosen DA. Topical lidocaine -prilocaine cream (EMLA) for thoracostomy tube removal. Anesth Analg 1999;88:1107-8. [ Links ]
18. Halperin SA, McGrath P, Smith B, Houston T. Lidocaine –prilocaine patch decreases the pain associated with the subcutaneous administration of measles -mumps -rubella vaccine but does not adversely affect the antibody response. J Pediatr 2000;136:789-94. [ Links ]
19. Buckley MM, Benfield P. Eutectic lidocaine/prilocaine cream. A review of the topical anaesthetic/analgesic efficacy of a eutectic mixture of local anaesthetics (EMLA). Drugs 1993;46:126-51. [ Links ]
20. Sicherer SH, Eggleston PA. EMLA cream for pain reduction in diagnostic allergy skin testing: effects on wheal and flare responses. Ann Allergy Asthma Immunol 1997;78:64-8. [ Links ]
21. Wolf SI, Shier JM, Lampl KL, Schwartz R. EMLA cream for painless skin testing: a preliminary report. Ann Allergy 1994;73:40-2. [ Links ]
22. Simons FE, Gillespie CA, Simons KJ. Local anaesthetic creams and intradermal skin tests. Lancet 1992;339:1351-2. [ Links ]
23. Arildsson M, Asker CL, Salerud EG, Stromberg T. Skin capillary appearance and skin microvascular perfusion due to topical application of analgesia cream. Microvasc Res 2000;59:14-23. [ Links ]
24. Dubus JC, Mely L, Lanteaume A. Use of lidocaine-prilocaine patch for the mantoux test: Influence on pain and reading. Int J Pharm 2006;327:78-80. [ Links ]
25. Hymes JA, Spraker MK. Racial differences in the efectivness of a topically applied mixture of local anesthetics. Reg Anesthesia 1986;11:11-3. [ Links ]
Mariana Couto
Serviço de Imunoalergologia, Centro Hospitalar São João
Alameda Professor Hernâni Monteiro
4200-319 Porto
E-mail:marianafercouto@gmail.com
Financiamento: Nenhum.
Declaração de conflito de interesses: Nenhum.
Agradecimentos: Aos colegas do Serviço de Imunoalergologia que colaboraram neste projecto e aos doentes que aceitaram nele participar, e sem os quais a sua concretização não teria sido possível.
Data de recepção / Received in: 19/11/2012
Data de aceitação / Accepted for publication in: 20/01/2013
Nota: Prémio SPAIC – MSD 2012 / Melhor comunicação oral (1.º Prémio)














