Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Revista Portuguesa de Imunoalergologia
versão impressa ISSN 0871-9721
Rev Port Imunoalergologia vol.26 no.1 Lisboa mar. 2018
ARTIGO DE REVISÃO
Alergia a galactose‑α‑1,3‑galactose
Allergy to galactose‑α‑1,3‑galactose
Joana Pita, Alexandru Ciobanu, Carlos Loureiro, Ana Todo‑Bom
Serviço de Imunoalergologia, Centro Hospitalar e Universitário de Coimbra
RESUMO
O objetivo deste artigo é realizar uma revisão atualizada sobre a alergia a galactose‑α‑1,3‑galactose. Os autores efetuaram uma pesquisa na Pubmed e selecionaram 24 artigos nos últimos 5 anos. A galactose‑α‑1,3‑galactose (α‑gal) é um oligossacarídeo existente em mamíferos, exceto em humanos e primatas superiores. A hipersensibilidade à α‑gal difere de outras reações IgE‑mediadas pelo início tardio de sintomas e caracteriza‑se pela associação entre episódios documentados de picada de carraça e o desenvolvimento tardio de urticária, anafilaxia ou sintomas gastrointestinais duas a seis horas após a ingestão de carnes vermelhas. As reações ao cetuximab, um anticorpo monoclonal anti‑EGFR (epidermal growth factor receptor) ocorrem de forma imediata, na primeira administração devido à hipersensibilidade ao epitopo α‑gal. A utilidade dos testes cutâneos com extratos comerciais é limitada pela sua reduzida especificidade, pelo que o doseamento da IgE específica sérica a α‑gal é uma análise essencial para o diagnóstico e monitorização.
Palavras‑chave: α‑gal, carnes vermelhas, carraça, alergia, tardio.
ABSTRACT
The aim of this article is to review allergy to galactose‑α‑1,3‑galactose. The authors performed a search in Pubmed and selected 24 articles in the last 5 years. Galactose‑alpha‑1,3‑galactose (α‑gal) is an oligosaccharide present in mammals, except in humans and higher primates. α‑gal hypersensitivity differs from other IgE‑mediated reactions, particularly on the late‑onset of symptoms and is characterized by the association between a confirmed episode of tick bite and the posterior development of urticaria, anaphylaxis or gastrointestinal symptoms, two to six hours after red meat ingestion. Reactions to cetuximab, a monoclonal antibody against EGFR (epidermal growth factor receptor) occur immediately after the first administration, due to the presence of the epitope α‑gal. Skin prick tests utility is limited, as they are not highly specific, and dosing the serum specific IgE to α‑gal is an essential analysis for diagnosis and monitoring of the disease.
Keywords: α‑gal, red meat, tick, allergy, delayed.
INTRODUÇÃO
A galactose‑α‑1,3‑galactose, comummente conhecida como α‑gal, é um hidrato de carbono (oligossacarídeo) existente em glicolípidos e glicoproteínas de mamíferos. Não existe em humanos ou primatas superiores devido à perda de função do gene 3‑galactosiltransferase1,2,3.
A exposição a este oligossacarídeo ocorre com a ingestão de carne, vísceras e gelatina de origem em mamíferos não primatas – carne de vaca, porco, carneiro, cavalo e veado1,2,4. Outras fontes animais são o coelho, o esquilo, o canguru, a foca e a baleia2. Este epitopo pode estar ainda presente em fármacos (heparina sódica de origem suína ou bovina, soros coloides substitutos do plasma)4, vacinas (por exemplo na vacina para o vírus Herpes Zoster) e laticínios3,4,5,6.
HISTÓRIA DA α‑GAL
Este oligossacarídeo foi identificado por Karl Landsteiner em 1969 como componente de eritrócitos de coelho.
Estruturalmente muito semelhante ao grupo sanguíneo B, com a exceção de não apresentar um resíduo de fucose na sua estrutura2,7.
Este hidrato de carbono surgiu como um obstáculo à xenotransplantação devido à produção de anticorpos reativos IgM e IgG2 dirigidos aos órgãos de origem suína ou bovina, promovendo uma reação de rejeição hiperaguda através da ativação do complemento e citólise – uma reação dependente de anticorpos e mediada por células2,3,5‑7,8.
Vários eventos levaram ao estudo e à melhor compreensão da alergia a α‑gal1.
Os primeiros relatos de alergia a carnes vermelhas após picada de carraça surgiram no ano 2000.
Dados de 2003 reportam que 60 % das crianças em idade escolar de uma vila no Quénia apresentavam níveis de IgE específica a gato elevada, mas não referiam sintomas com a exposição a gato, associando o facto de que existiam poucos gatos na vila9.
Nos Estados Unidos da América (EUA), em 2005, surgiram relatos de reações alérgicas durante ou após a primeira administração de cetuximab, um anticorpo monoclonal específico para o recetor do fator de crescimento epidérmico (EGFR), utilizado no tratamento dos carcinomas da cabeça e pescoço e no cancro colo‑rectal10.
As reacções reportadas ocorreram em 15 % dos doentes tratados com este anticorpo monoclonal. Em 2007 estes casos tornaram‑se mais frequentes, com relatos de reacções alérgicas graves no Tennessee, Carolina do Norte, Arkansas, Missouri e Virgínia. A identificação da α‑gal como epitopo do cetuximab ocorreu apenas em 20081.
Em 2009, foram identificados 24 casos de anafilaxia de início tardio nos EUA e múltiplos casos de alergia a carnes vermelhas em Sydney (episódios após picada de carraça). A evidência científica de que a picada de carraça era responsável pelas reações IgE‑mediadas nos EUA ocorreu em 2010, e em 2014 foram realizadas provas de provocação oral para diagnóstico das reações alérgicas a carnes vermelhas de início tardio1.
DISTRIBUIÇÃO GEOGRÁFICA
A maioria dos casos de reações alérgicas a carnes vermelhas foi identificada nos EUA (estados da região Este, Sudeste e Centro‑oeste), França, Alemanha, Suécia, Japão, Coreia do Sul e Austrália1,3,9.
A alergia a α‑gal verificou‑se em 2000 doentes na Virgínia, Carolina do Norte, Europa, Austrália e Japão11. Dados recentes demonstraram a presença de α‑gal na saliva do Amblyoma sculptum, uma espécie de carraça que faz parte do complexo Amblyoma cajennense que inclui também espécies de carraça prevalentes na região do Canal do Panamá, onde também existem registos de reações a α‑gal3.
Na Austrália, dados de 2012 referem a identificação de 50 doentes cuja análise do soro confirma a presença de IgE específica a α‑gal e a sua associação a reacções alérgicas após a ingestão de carne de mamíferos, incluindo canguru12. No Japão e na Coreia foram reportados casos de anafilaxia de início tardio 5 a 7 horas após ingestão de carne de mamíferos. Realizaram‑se testes intradérmicos com cetuximab nas diluições de 5, 50, e 500 μg, com obtenção de resultados positivos em todas as concentrações, o que demonstra a presença de α‑gal3, epitopo responsável pelas reações tardias a carnes vermelhas e imediatas a cetuximab.
Foram também reportados casos de reações locais exuberantes a picada de carraça e reações de início tardio a carnes vermelhas em doentes da região de Nova Gales do Sul3.
Na Alemanha, identificaram‑se reações alérgicas ao cetuximab, bem como reações alérgicas a carne de vaca. Foi demonstrada laboratorialmente a ligação IgE‑cetuximab por western blot e esses resultados foram comparados aos imunoensaios de IgE‑α‑gal utilizando reagentes biotinilados12.
Em França, identificaram‑se três casos de doentes com IgE‑α‑gal aumentada em 2009. O estudo de Moneret‑Vautrin incluía outras carnes, de cabra, cavalo, porco e rim de vaca, como causa de reações à α‑gal de carácter grave e início tardio12. Na Suécia, Van Hage e colaboradores demonstraram que o oligossacarídeo existente na IgA do gato era a α‑gal.
Este grupo de investigadores utilizou anticorpos anti‑α‑gal em soro humano para marcar a α‑gal presente em carraças12.
No Centro Hospitalar e Universitário de Coimbra existem registos de três casos com IgE específica (sIgE) a α‑gal positiva desde 2015: um doente do sexo masculino, 72 anos com suspeita de alergia a carnes vermelhas (sIgE 5,51 kU/L), nascido no Quénia e trabalhador rural; negava picadas de carraça, mas apresentava um valor inicial de sIgE de 42 kU/L (análise realizada pela Thermofisher® em Espanha)13, e duas doentes do sexo feminino – uma com 68 anos e história de anafilaxia a carnes vermelhas (sIgE 0,60 kU/L), outra com 61 anos e queixas digestivas após ingestão de carnes vermelhas (sIgE 18,30 kU/L).
Ambas trabalhavam em ambiente rural. Ambas negavam picadas de carraça (últimos dois casos não foram publicados).
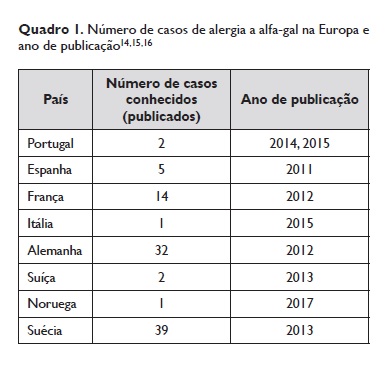
Foi reportado também um caso proveniente do Centro Hospitalar do Porto num doente de 76 anos, sem história conhecida de picada de carraça, com quadro clínico de urticária generalizada e diarreia 1 hora após ingestão de carne vermelha cozinhada. IgE específica a α‑gal 35,3kUA/L14. O Quadro 1 sumariza os casos de alergia a alfa‑gal na Europa.
CAUSAS DE ALERGIA A α‑GAL
A sugestão inicial de que haveria uma possível associação entre a picada de carraça e a hipersensibilidade a α‑gal surgiu da observação de que as áreas de maior prevalência da sensibilização a α‑gal correspondiam às áreas de maior incidência de febre-das-montanhas‑rochosas e dos seus vectores associados – Dermacentor variabilis (The brown dog tick) e Amblyoma americanum (The lone star tick)3.
No Sudeste dos EUA, a picada de carraça é a causa principal de reações IgE‑mediadas a α‑gal9.
Nesta região, a carraça mais comum é o Amblyomma americanum, mas estas espécies variam de acordo com a região geográfica.
A suportar a hipótese de implicação da carraça Amblyoma americanum encontrou‑se uma excelente correlação entre a IgE a α‑gal e a IgE ao extrato inteiro de Amblyomma americanum em doentes com história de alergia a carnes vermelhas. A mesma relação não foi encontrada para o Dermacentor variabilis3. De forma semelhante, não há conhecimento de nenhuma correlação entre o Ixodes scapularis, responsável pela doença de Lyme e a sensibilização a α‑gal3.
Na Europa, a carraça responsável por esta patologia é a Ixodes ricinus1,2,7,9.
O Quadro 2 sumariza as três teorias sobre a associação entre a picada de carraça e a reacção IgE‑mediada.

Commins descreve várias evidências que suportam o papel da picada de carraça no desenvolvimento da resposta IgE‑mediada a α‑gal, nomeadamente quatro casos com evidência epidemiológica de que a IgE específica a α‑gal aumenta após episódios documentados de picada de carraça, identificação de IgE específica a α‑gal em áreas onde as picadas de carraça são comuns, correlação entre IgE específica a α‑gal e a presença de anticorpos IgE a proteínas da carraça, semelhança entre a distribuição global das anafilaxias tardias a carnes vermelhas e a distribuição conhecida das várias espécies de carraça; presença de α‑gal após a marcação do trato gastrointestinal da Ixodes ricinus9.
IMPORTÂNCIA CLÍNICA DA α‑GAL
Até recentemente, pensava‑se que as reações de hipersensibilidade tipo I a oligossacarídeos fossem pouco prováveis, com base no conhecimento de que a sensibilização a determinantes dos hidratos de carbono por reatividade cruzada (CCD) não causa sintomas clínicos relevantes, mas apenas reatividade cruzada in vitro18.
No caso específico da α‑gal, porém, a existência de anticorpos específicos constitui um problema de saúde importante, dado que os doentes estão em risco de anafilaxia de início tardio com a ingestão de carnes vermelhas e produtos com gelatina de origem suína ou bovina, bem como também risco de anafilaxia imediata se expostos a anticorpos de origem murina ou soros coloides de origem bovina4. A utilização de materiais bioprostéticos como válvulas cardíacas de origem suína ou bovina, pode condicionar um risco elevado de reacções peri e pos‑operatorias em doentes altamente sensibilizados4,8.
A comprovação da sensibilização a α‑gal é importante para o diagnóstico de reações a carnes vermelhas de início tardio e reações a gelatinas de origem mamífera, bem como para a identificação do alergénio responsável por episódios repetidos de urticária ou anafilaxia1,2.
A IgE específica a α‑gal associa‑se essencialmente a duas formas de anafilaxia, explicitadas no Quadro 3.

O cetuximab é constituído por 21 estruturas distintas de oligossacarídeos, em que 30 % destas contêm um ou mais resíduos α‑1,3‑galactosil17.
Até recentemente, considerava‑se que os resíduos de α‑gal estivessem localizados apenas na porção Fab deste anticorpo monoclonal20, mas dados mais recentes mostram que estes resíduos podem encontrar‑se também na porção Fc5,19.
HIPERSENSIBILIDADE
Na Europa, as picadas de carraça da família Ixodidae constituem a causa principal de sensibilização, e é possível identificar o epitopo α‑gal no trato gastrointestinal do Ixodes ricinus21. Após uma picada, os níveis de IgE específica a α‑gal aumentam e podem ocorrer os sintomas de alergia. Se o doente evitar novas picadas, os níveis de IgE decrescem, e se ficar livre de picadas por um período de 1 a 2 anos os níveis de IgE específica podem decrescer até um nível onde a ocorrência de sintomas é pouco provável. Estes doentes podem até tolerar ingestão de carnes de mamíferos sem sintomas21.
Se ocorrer nova picada, os níveis de IgE específica voltam a aumentar21. John W. Steinke sugeriu vários mecanismos para a hipersensibilidade a α‑gal: contrariamente ao que acontece após uma prova de provocação oral com carne de porco, onde a urticária tem início apenas 2 horas após a prova de provocação, quando é administrado cetuximab podemos observar uma reação de início rápido em aproximadamente 20 minutos após o início da administração endovenosa deste anticorpo monoclonal17.
Esta resposta rápida é semelhante à resposta dos basófilos in vitro após ativação com glicoproteínas (tiroglobulina bovina ou cetuximab), que promovem uma reação com início em 25 minutos. Durante uma prova de provocação oral, os basófilos circulantes provocam uma sobrerregulação da expressão de CD63 num intervalo de tempo semelhante ao do início dos sintomas. As respostas de início retardado não são directamente relacionadas com a ação dos basófilos ou mastócitos17.
Parece provável que o oligossacarídeo seja absorvido através do tracto gastrointestinal e transportado para a circulação sanguínea de forma lenta17. Após o seu transporte para a circulação periférica, admite‑se que possa haver transporte para o ducto torácico por quilomicra, que parecem ser os responsáveis pelo início tardio dos sintomas17. Outro facto interessante é que as partículas de LDL transportam α‑gal na sua superfície e podem efetivamente causar a libertação de mediadores mastocitários, mas apenas em doentes com valores de IgE específica a α‑gal elevados17.
HIPÓTESES PARA A SENSIBILIZAÇÃO E ALERGIA A α‑GAL
Um dos aspetos interessantes na hipersensibilidade a α‑gal é que este síndrome parece desenvolver‑se igualmente em indivíduos atópicos e não atópicos3. Os mecanismos imunológicos que relacionam a exposição à carraça com a produção de IgE específica a α‑gal permanecem pouco compreendidos3.
De acordo com John Steincke et al, as respostas IgE‑mediadas podem ocorrer fora de centros germinativos maduros. O switch para IgE pode ocorrer em variadas localizações, como por exemplo na mucosa nasal.
Outros autores7 afirmam que as proteínas de transporte de lípidos VLDL e LDL também transportam α‑gal na sua superfície, o que promove uma reação de cross‑link com a IgE e a consequente libertação de mediadores mastocitários. Estes autores postulam que o desenvolvimento de sintomas parece correlacionar‑se mais com a desgranulação mastocitária do que com a ativação basofílica e que a ativação dos basófilos está relacionada com o tempo de início dos sintomas. A ativação dos basófilos pode portanto ser um marcador da presença de α‑gal na corrente sanguínea7.
De acordo com Kollman, a alergia a α‑gal parece ser mediada por uma resposta Th2 atípica, caracterizada pela elevação de IgE e IgG, particularmente IgG122. A resposta Th2 é iniciada por basófilos, e alguns doentes apresentam prurido após a ingestão de carne vermelha no local exato da picada de carraça. Este facto sugere que os basófilos, mastócitos ou eosinófilos permanecem no local da inoculação22.
Segundo Jeffrey Wilson e Platts‑Mills, há claras evidências de que as picadas de carraça promovem respostas Th2, apesar dos mecanismos serem pouco claros3. Resultados de estudos laboratoriais destes autores demonstraram existir um recrutamento de células T e neutrófilos no local da picada em 48 horas num hospedeiro naive. Surpreendentemente, os basófilos não eram as células predominantes3. Com base nos conceitos emergentes sobre imunidade tipo 2, que inclui fatores da imunidade inata e adaptativa, os autores postulam que haverá uma cascata inicial de citocinas, como TSLP, IL‑33 e IL‑25, que serão libertadas das células epiteliais como um sinal inicial para as células imunes hematopoiéticas. A resposta epitelial pode envolver reconhecimento de padrões moleculares associados a patogenos (PAMP) ou padrões moleculares associados a dano (DAMP) por recetores de reconhecimento de patogenos (PRR) expressados no epitélio.
Outros mediadores, como prostaglandinas ou leucotrienos, também podem ter um papel precoce nesta reação3. Há uma panóplia de constituintes da saliva da carraça que podem estar implicados, como prostaglandinas, lipocalinas, fosfolipases e adenosina, que podem atuar no epitélio e nas células imunes subepiteliais.
Uma possibilidade interessante é que a α‑gal tenha atividade PAMP intrínseca que promova a cascata da imunidade tipo 2.
DIAGNÓSTICO DE ALERGIA A α‑GAL
O sintoma mais predominante parece ser o prurido, mas os doentes também podem desenvolver urticária, angioedema, náuseas, diarreia ou mesmo anafilaxia recorrente1,5,7,16,17.
Reações urticariformes e anafilaxia de início tardio foram reportadas em variadas regiões do mundo. Estas ocorreram tipicamente 2‑6 horas após a ingestão de carne vermelha (carne de vaca, porco, carneiro, coelho, cavalo e canguru).
Na Europa, as vísceras de vaca e porco são consumidas tradicionalmente. Relatos anteriores mostram que particularmente o rim de porco é extremamente rico em α‑gal4.
Após a sua ingestão, os sintomas foram mais graves e de início mais rápido, quando comparado às reacções após a ingestão de carne do músculo esquelético4. Carnes vermelhas com maior conteúdo em gordura também causam reações alérgicas mais graves22. As partículas lipídicas entram na corrente sanguínea 3 a 4 horas após uma refeição, o que sugere que o tempo necessário para que ocorram sintomas pode refletir o tempo necessário para absorver e digerir a α‑gal.
Para além do facto de a ingestão de rim de porco e de vaca poder encurtar o início das manifestações clínicas, o início das reações também pode ser mais rápido se coexistirem alguns cofactores, detalhados no Quadro 4.

As reações locais de evolução longa no local da picada de carraça podem ser indicativas de síndrome α‑gal.
Nestes casos, a reação local pode persistir até 14 dias. Em indivíduos altamente sensibilizados, esta reação pode permanecer durante 8 semanas, resultando em lesões de grattage18.
Dado que os níveis de IgE específica e a sensibilização a α‑gal decrescem se não existir nova exposição à picada de carraça, aqueles doentes que evitam a reexposição poderão voltar a tolerar a ingestão de carne22. A monitorização regular da IgE específica a α‑gal pode predizer o risco de existir uma nova reacção alérgica grave22. Infelizmente, até atualmente, nem os testes cutâneos por picada, nem a quantificação da IgE específica a α‑gal, nem o ratio IgE específica/IgE total permitem a diferenciação entre doentes sensibilizados e reativos4.
Hilger e colaboradores analisaram a resposta IgE em proteínas purificadas da carne por ELISA e ELISA–inibição e identificaram duas proteínas transportadoras de IgE‑α‑gal no rim de porco: AP‑N (aminopeptidase N) e a ECA I (enzima conversora da angiotensina‑I) e confirmaram a sua importância na alergia a α‑gal pelo papel destas proteínas transportadoras na ativação de basófilos e testes cutâneos por picada4.
TRATAMENTO
É essencial que estes doentes possuam um dispositivo autoinjector de adrenalina, bem como anti‑histaminicos, corticoides e um cartão de anafilaxia, com descrição do desencadeante implicado e o tratamento que deve ser realizado7,23. Os doentes devem evitar a ingestão de carne de porco, carne de vaca, carneiro e outras fontes de carne de mamíferos não primatas.
Não será necessário evitar laticínios se o doente não apresentar sintomas com estes alimentos. As picadas de carraça devem ser evitadas através da utilização de repelente, vestuário apropriado, verificação da existência de carraças no vestuário ou na pele após atividades no exterior ou contacto com animais e ter atenção especial no período de abril a setembro, em que as carraças estão mais ativas. Relativamente ao cetuximab, pode ser realizada dessensibilização, se assim for necessário7,9.
CONCLUSÕES
Os alergénios major envolvidos na alergia a carne vermelha de mamíferos são albuminas séricas e imunoglobulinas.
A alergia a carnes vermelhas associada a α‑gal é rara e foi descrita apenas recentemente. Esta alergia apresenta várias características incomuns: o desencadeante, um oligossacarídeo, e o tempo de início dos sintomas.
Esta reação IgE‑mediada é única, dadas as suas manifestações de urticária ou anafilaxia de início tardio.
Pode ser difícil identificar uma causa imediata para estas reações, e em muitas delas existe uma história de picada de carraça com prurido posterior. Após algum tempo, os doentes iniciam sintomas de alergia 3 a 6 horas após a ingestão de carne vermelha.
Nesta síndrome peculiar os testes cutâneos têm importância limitada no diagnóstico, e os testes picada a picada bem como os doseamentos de IgE específica são essenciais para o diagnóstico, tratamento e evicção de futuras reações.
A evicção de picadas de carraça e o plano de emergência são importantes para a evolução clínica e para o tratamento desta patologia.
REFERÊNCIAS
1. Alpha‑gal (2012) http://www.phadia.com. Accessed 2 February 2017. [ Links ]
2. Platts‑Mills T, Schulyer A, Tripathi A, Commins S. Anaphylaxis to the carbohydrate side chain alpha‑gal. Immunol Allergy Clin N Am 2015;35:247‑60. [ Links ]
3. Wilson J, Schuyler A, Schroeder N, Platts‑Mills T. Galactose‑ α‑1,3‑galactose: atypical food allergen or model IgE hypersensitivity? Curr Allergy Asthma Rep 2017;17:8. [ Links ]
4. Hilger C, Swiontek K, Hentges F, Lehners C, Eberlein B, Morisset M, et al. Two galactose‑α‑1,3‑galactose carrying peptidases from pork kidney mediate anaphylactogenic responses in delayed meat allergy. Allergy 2016;71:711‑9. [ Links ]
5. Commins S. Invited Commentary: alpha‑Gal allergy: tip of the iceberg to a pivotal imune response.Curr Allergy Asthma Rep 2016;16:61. [ Links ]
6. Stone C, Hemler J, Commins S, Schulyer A, Phillips E, Peebles R, et al. Anaphylaxis after Zoster vaccine: implicating alfa‑gal allergy as a possible mechanism. J Allergy Clin Immunol 2017;139:1710‑3.e2 [ Links ]
7. Stewart P, McMullan K, Le Blanc S. Delayed red meat allergy: clinical ramifications of galactose‑α‑1,3‑galactose sensitization. Ann Allergy Asthma Immunol 2015;115:260‑4. [ Links ]
8. Mozzicato, S, Tripathi A, Posthumus J, Platts‑Mills T, Commins S. Porcine or bovine valve replacement in three patients with IgE antibodies to the mammalian oligosaccharide galactose‑alpha‑1,3‑galactose. J Allergy Clin Immunol Pract 2014;2:637‑8. [ Links ]
9. Commins S, Jerath M, Cox K, Erickson L, Platts‑Mills. Delayed anaphylaxis to alpha‑gal, an oligosaccharide in mammalian meat. Allergol Int 2016;65:16‑20.
10. Sim D, Lee J, Park KH, Jeong KY, Ye YM, Lee JH, Park JW. Accurate assessment of alpha‑gal syndrome using cetuximab and bovine thyroglobulin‑specific IgE. Mol Nutr Food Res 2017;61(10). [ Links ]
11. Flaherty M, Kaplan S, Jerath M. Diagnosis of life‑threatening alpha‑gal food allergy appears to be patient driven. J Prim Care Community Health 2017;8:345‑8. [ Links ]
12. Commins S, Platts‑Mills. Tick bites and red meat allergy. Curr Opin Allergy Clin Immunol 2013;13:354‑9.
13. Carrapatoso I, Bartolomé Zavala B, Ribeiro F, Martínez Quesada J, Segorbe Luís A. Allergy to red meat in adulthood: a case report. J Investig Allergol Clin Immunol 2014;24:192-211. [ Links ]
14. Abreu C, Cunha L, Bartolomé B, Falcão H. Anaphylaxis after consumption of red meat in patient with IgE antibodies specific for galactose‑α‑1,3‑galactose. EAACI Online Library 2015; 104942. [ Links ]
15. Van Nunen S. Tick‑induced allergies: mammalian meat allergy, tick anaphylaxis and their significance. Asia Pac Allergy 2015;5:3‑16. [ Links ]
16. Calamari A, Poppa M, Villalta D, Pravettoni V. Alpha‑gal anaphylaxis: the first case report in Italy. Eur Ann Allergy Clin Immunol 2015;47:161‑2. [ Links ]
17. Steinke J, Platts‑Mills T, Commins S. The alpha‑gal story: lessons learned from connecting the dots. J Allergy Clin Immunol 2015; 135:589‑97 [ Links ]
18. Fischer J, Biedermann T. Delayed immediate‑type hypersensitivity to red meat and innards: current insights into a novel disease entity. J Dtsch Dermatol Ges 2016;14:38‑44. [ Links ]
19. Commins S, James H, Stevens W, Shawna L, Pochan C, Land M, et al. Delayed clinical and ex vivo response to mammalian meat in patients with IgE to galactose‑alpha‑1,3‑galactose. J Allergy Clin Immunol 2014;134:108‑15.e11. [ Links ]
20. Gonzalez‑Quintela A, Laursen A, Vidal C, Skaaby T, Gude F, Linneberg A. IgE antibodies to alpha‑gal in the general adult population: relationship with tick bites, atopy and cat ownership. Clin Exp Allergy 2014;44:1061‑8. [ Links ]
21. Saleh H, Embry S, Nauli A, Atyia S, Krishnaswamy G. Anaphylactic reactions to oligosaccharides in red meat: a syndrome in evolution. Clin Mol Allergy 2012;10:5. [ Links ]
22. Kollmann D, Nagl B, Ebner C, Emminger W, Wöhrl S, Kitzmüller C, et al. The quantity and quality of α‑gal‑specific antibodies differ in individuals with and without delayed red meat allergy. Allergy 2017;72:266‑73. [ Links ]
23. Ferreira M, Neto L, Ribeiro R. Alergia a alfa‑gal: Uma revisão sistemática. Braz J Allergy Immunol 2015;3:241‑50. [ Links ]
24. Anaphylaxis: Guidelines from the European Academy of Allergy and Clinical Immunology. EAACI. www.eaaci.org. [ Links ]
Joana Sofia Pita
Rua das Parreiras, n.º 27, 1.º, Coimbra, Celas
3000‑326 Coimbra
Email: joana.s.pita@gmail.com
Financiamento: Nenhum.
Declaração de conflito de interesses: Nenhum.
Data de receção / Received in : 11/07/2017
Data de aceitação / Accepted for publication in: 17/09/2017














