INTRODUÇÃO
A dermatite atópica (DA) é uma doença muito comum no cão, com uma prevalência de 15%, valor que pode ser mais elevado em determinadas raças, como o Bouledogue Francês e o Retriever do Labrador, raças bastante populares hoje em dia1-3.
É uma doença crónica que implica muitas vezes um tratamento para a vida. Nos últimos anos, com os avanços na compreensão da fisiopatologia da dermatite atópica canina (DAc), sobretudo com a identificação do papel da interleucina (IL)-31, surgiram no mercado dois medicamentos, um farmacológico e um biológico, que em muito vieram contribuir no tratamento desta doença4-6. Um deles, o oclacitinib, um inibidor seletivo da enzima cinase de Janus, além de apresentar uma grande rapidez de ação, tem também algum efeito anti-inflamatório5,7. No entanto, é um fármaco oneroso, em que os custos associados mensais atingem atualmente cerca de 120€ no primeiro mês e os 90€ nos meses seguintes, num cão da raça Labrador (24-36 kg)8. Este custo torna-se muito pesado para as famílias e chega mesmo a impossibilitar em alguns casos o uso deste fármaco como uma opção para o animal. Num estudo realizado no Serviço de Dermatologia do Hospital Escolar Veterinário da Faculdade de Medicina Veterinária da Universidade de Lisboa verificou-se que, apesar de 92,5% dos tutores de cães com DA se encontrarem satisfeitos ou muito satisfeitos com o tratamento com este fármaco, para 75% deles os custos associados à terapêutica representavam um foco de preocupação, sendo que 42,5% referiram ter de limitar outras despesas para pagar o tratamento do seu cão9. Assim sendo, um protocolo que permitisse a sua utilização em dias alternados teria o potencial de reduzir o custo de manutenção do mesmo para metade. Contudo, por se tratar de uma ferramenta terapêutica muito dirigida para a IL-31, e assim, menos abrangente, pode não se demonstrar suficiente para atingir o controlo clínico em alguns casos. De facto, considera-se que o seu efeito anti-inflamatório é limitado7. A introdução de um fármaco com um poder anti-inflamatório mais potente, de forma complementar, no início do tratamento, poderá aumentar o sucesso do protocolo terapêutico7.
OBJETIVOS
No presente estudo pretendeu-se avaliar a possibilidade de adotar um protocolo terapêutico alternativo administrando oclacitinib em dias alternados, o que reduziria os custos de manutenção deste tratamento para metade. Secundariamente, pretendemos ainda avaliar se existe vantagem em administrar glucocorticoides orais no início deste novo protocolo com oclacitinib.
MÉTODOS E ANÁLISES
Animais
Foram incluídos cães de tutores que se apresentaram para consulta no Serviço de Dermatologia do HEV da FMV-ULisboa com diagnóstico de DAc, com base na anamnese, sinais clínicos e critérios de Favrot10, tendo sido excluídas outras doenças cutâneas pruriginosas, como a sarna sarcóptica e a dermatite alérgica à picada da pulga. Foram incluídos animais com gravidade lesional (Canine Atopic Dermatitis Extent and Severity Index, CADESI-04) com valores entre os 35 e 60 (doença moderada) e superiores a 60 (doença grave), grau de prurido (Pruritus Visual Analogic Scale, PVAS)≥3 e com autorização dos tutores, por meio de um consentimento informado escrito. Este estudo foi aprovado pela Comissão de Ética para a Investigação e Ensino (CEIE) da Faculdade de Medicina Veterinária.
Critérios de exclusão
Foram excluídos animais com menos de 12 meses, animais para reprodução no período de estudo ou em lactação. Também foram excluídos animais com doenças nas quais a administração de glucocorticoides orais ou oclacitinib estivesse contraindicada, como, neoplasias malignas, infeções graves, diabetes mellitus, hiperadrenocorticismo, leishmaniose, ou sensibilidade conhecida a qualquer uma destas substâncias.
Não foi permitida a administração de glucocorticoides tópicos ou anti-inflamatórios sistémicos durante a participação de animais no estudo. Foram ainda excluídos animais aos quais tivessem sido administrados glucocorticoides orais/tópicos ou ciclosporina nos últimos 28 dias, e ainda animais sujeitos a tratamentos com glucocorticoides administrados por via parentérica nos últimos 56 dias11,12. Foram, no entanto, permitidas a administração de ácidos gordos essenciais, imunoterapia específica e/ou champôs emolientes, caso o início destas terapêuticas precedesse o estudo e se se encontrassem já em fase de manutenção6,11,12.
Alocação
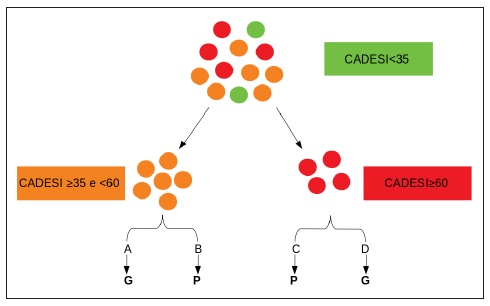
Foram realizados dois sorteios em paralelo (o sorteio AB e o sorteio CD), tendo em conta o valor de CADESI‑04 de cada animal, conforme o esquema representado na Figura 1. Os cães com CADESI-04 compreendido entre 35 e 60 (doença de grau moderado) foram alocados no sorteio AB, já os cães com CADESI-04 superior a 60 (doença grave) foram alocados no sorteio CD. De modo a uniformizar o grau da doença e o número de animais por grupo, foi utilizada a alocação em blocos no Randomizer.org. No final, o grupo P foi constituído pelos subgrupos B e C, sendo o grupo G constituído pelos subgrupos A e D. Aos grupos B e C foram administradas as cápsulas de placebo, sendo aos grupos A e D administradas as cápsulas de prednisolona. Todas as cápsulas eram idênticas em tamanho, cor e cheiro. As cápsulas foram preparadas de forma magistral pela Farmácia Martins, Calçada da Estrela, Lisboa.
PROTOCOLO
Na primeira fase do estudo, do Dia -30 (D-30) ao Dia 0 (D0), foi administrado, por via oral, oclacitinib segundo o protocolo-padrão (0,4-0,6 mg/kg, BID durante 14 dias, e SID nos restantes 16 dias) a ambos os grupos.
Nos primeiros 7 dias foi administrada ao grupo G prednisolona (1 mg/kg SID) por via oral e ao grupo P foi administrado um placebo idêntico no mesmo regime.
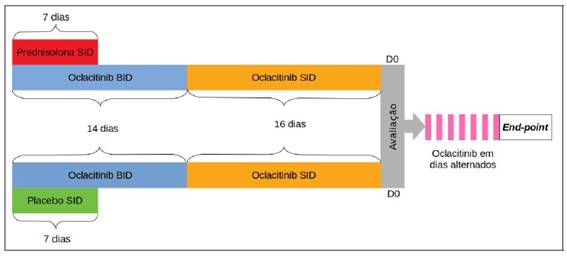
Se no final da primeira fase (D0) os animais se encontrassem estáveis, isto é, com CADESI‑04<35 e/ou valor de PVAS<3, passavam para a segunda fase do estudo. Nesta, todos os animais foram sujeitos a um protocolo de tratamento com oclacitinib em dias alternados até à recidiva do seu quadro clínico ou após 30 dias sob este mesmo protocolo (end-point). Nos casos em que se verificou recidiva, a data foi registada e os animais cessaram este tratamento. Na Figura 2 encontra-se esquematizado o protocolo utilizado.
Avaliação clínica
Os animais foram avaliados quanto à sua gravidade lesional com o auxílio do CADESI‑04(13), no D-30, D0 e end-point. Já o grau de prurido foi avaliado pelos respetivos tutores, nos mesmos pontos temporais, utilizando uma escala validada de prurido (PVAS)14, numerada de 0 a 10, sendo 0 um animal sem prurido e 10 um animal com prurido muito grave, quase contínuo, que não cessa, independentemente do que esteja a acontecer à sua volta.
O plano de contingência adotado pelo HEV devido à COVID-19 criou a necessidade de acompanhar alguns animais por teleconsulta, o que pode ter influenciado as pontuações de CADESI-04, como consequência das condições de contenção dos animais e visualização de lesões.
Análise estatística
A análise estatística foi realizada com recurso ao programa Statistical Package for the Social Sciences (SPSS) versão 26. Foi utilizado o teste não paramétrico Mann-Whitney U. Para todas as análises foram considerados estatisticamente significativos valores de p<0,05.
Caracterização da amostra
Grupo Placebo (P)
O grupo P foi inicialmente constituído por 9 animais, no entanto 2 deles foram excluídos por falta de adesão dos tutores ao protocolo de tratamento, passando este grupo a ser constituído por 7 animais. A mediana de idades neste grupo foi de 4 anos (intervalo entre 3 e 7 anos). Relativamente à duração da doença, verificou-se uma mediana de 2 anos (intervalo entre 1 e 5 anos). Em termos de raças, este grupo foi constituído por 4 retrievers do Labrador, 2 Shih-tzu e 1 Dálmata.
Quanto ao grau de prurido inicial (D-30), registou-se uma mediana de 7,9 (prurido moderado), com um intervalo entre 5,5 e 10,0. Já quanto aos valores de CADESI-04 no D-30, verificou-se uma mediana de 42 (doença moderada), com um intervalo entre 39 e 119.
Grupo Glucocorticoides (G)
O grupo G foi constituído por 9 animais, com uma mediana de idades de 5 anos (intervalo entre 2 e 7 anos). Relativamente à duração da doença, verificou-se uma mediana de 3 anos (intervalo entre 1 ano e 5 anos).
Em termos de raças, este grupo foi constituído por 4 Buldogues Francês, 1 Barbado da Terceira, 1 Pastor Alemão, 1 West Highland White Terrier, 1 Yorkshire Terrier e 1 animal sem raça definida.
Quanto ao grau de prurido inicial (D-30), registou-se uma mediana de 6,7 (prurido moderado), com um intervalo entre 4,7 e 10,0. Já quanto aos valores de CADESI-04 no D-30, registou-se uma mediana de 59 (doença moderada), com um intervalo entre 38 e 129.
Não se verificaram diferenças estatisticamente significativas entre os grupos para a idade, duração da doença, grau de prurido e gravidade lesional.
RESULTADOS
Tempo de tratamento com oclacitinib em dias alternados
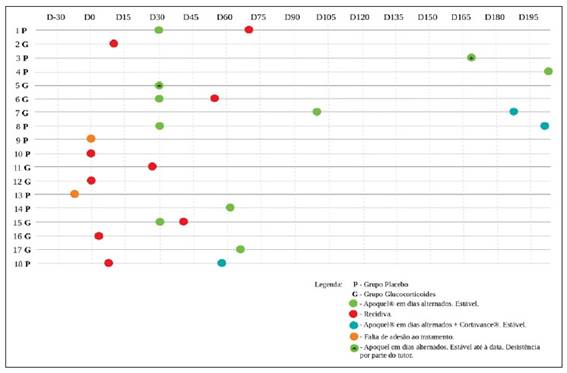
Quanto ao tempo de tratamento com oclacitinib em dias alternados, foi possível realizar este protocolo durante pelo menos 30 dias em 71% dos animais (5 do grupo P e 5 do grupo G). No grupo P apenas um animal não atingiu esta meta, com um tempo de tratamento de 7 dias. Já no grupo G, três animais não atingiram esta meta, registando-se valores de tempo de tratamento de 3, 11 e 27 dias (Figura 3).
Foi possível fazer um acompanhamento dos animais (follow-up) após os 30 dias estipulados para a duração do estudo. Considerando, assim, um período de tempo de pelo menos 60 dias (Figura 3), verificou-se a possibilidade de realizar o protocolo em dias alternados em cerca de 43% dos animais (4 do grupo P e 2 do grupo G).
No grupo P observou-se uma mediana de tempo de tratamento com oclacitinib em dias alternados de 66 dias (intervalo entre 7 e 219 dias). Já no grupo G, a mediana foi de 35 dias (intervalo entre 3 e 100 dias).
Em dois dos cães, um pertencente ao grupo P e outro ao grupo G, optou-se pela associação de um spray de aceponato de hidrocortisona a 0,0584% (Cortavance®), nos dias 31 e 101, respetivamente.
Não foram encontradas diferenças estatisticamente significativas entre os períodos de tratamento com oclacitinib em dias alternados dos dois grupos (p=0,241).
Grau de prurido
D0
No início do protocolo em dias alternados (D0), o grupo P apresentou uma mediana de grau de prurido de 2,3 (prurido muito ligeiro), com um intervalo entre 0,1 e 6,9. Foi ainda registado um cão que, pelo seu grau de prurido mais elevado, não pôde prosseguir para a segunda fase do estudo. Já no grupo G, observou-se também uma mediana de 2,3 (intervalo entre 1,1 e 5,0). Para além disso, um dos cães também não pôde prosseguir para a fase seguinte, pois os tutores não se encontravam satisfeitos com os resultados do tratamento.
As diferenças encontradas não foram estatisticamente significativas entre os valores de prurido dos dois grupos (p=0,936).
End-point
No end-point, o grupo P apresentou uma mediana de grau de prurido de 1,95 (prurido normal), com um intervalo entre 0,2 e 5,0.
Já no grupo G, verificou-se uma mediana de 3,1 (prurido muito ligeiro), com um intervalo entre 1,2 e 6,8. Não foram encontradas diferenças estatisticamente significativas entre os grupos (p=0,266).
CADESI-04
D0
Findo o primeiro mês de tratamento diário com oclacitinib, no grupo P observou-se uma mediana de valor de CADESI-04 de 13 (doença ligeira), com um intervalo entre 4 e 35. No grupo G, verificou-se uma mediana de 15 (doença ligeira), com um intervalo entre 5 e 35. As diferenças encontradas não foram estatisticamente significativas entre os valores de CADESI-04 dos dois grupos (p=0,898).
End-point
No end-point, no grupo P verificou-se uma mediana de CADESI-04 de 9 (doença em remissão), com um intervalo entre 2 e 18. No grupo G registou-se uma mediana de 13,5 (doença ligeira), com um intervalo entre 6 e 40. As diferenças encontradas não foram estatisticamente significativas entre os dois grupos (p=0,358).
Efeitos secundários
Apenas foram registados efeitos secundários em três animais. No grupo P, observaram-se dois animais com efeitos adversos no início do tratamento, num deles registou-se um episódio de vómitos, sendo registada poliúria e polidipsia noutro animal. No grupo G apenas se observou um animal com poliúria, polidipsia e polifagia no início do estudo.
DISCUSSÃO
Em 71% dos cães foi possível realizar um tratamento com oclacitinib em dias alternados durante pelo menos 30 dias, reduzindo para metade os custos mensais associados, potenciando deste modo a adesão dos tutores a esta ferramenta terapêutica. No entanto, quando considerado o período mais alargado de 60 dias com o tratamento em dias alternados, verificou-se uma diminuição da frequência relativa para os 43%. Pode tornar-se assim vantajoso aplicar este protocolo, sendo possível o espaçamento da medicação em grande parte dos cães, podendo ser necessário, a longo prazo, ajustar a frequência de administração, caso se verifique um agravamento dos sinais clínicos, pelo que o tratamento deve ser flexível e personalizado.
Não foram encontradas diferenças estatisticamente significativas entre os valores de grau de prurido e de CADESI-04 dos grupos P e G, no D-30, no D0 e no end-point. Assim sendo, por um lado, os grupos no início do estudo (D-30) eram muito comparáveis quanto à gravidade clínica. Contudo, os glucocorticoides não tiveram impacto quanto ao grau de melhoria dos animais. Seria esperado que a introdução de prednisolona no início da terapêutica facilitasse a realização de um protocolo de tratamento com oclacitinib em dias alternados, permitindo que este se realizasse durante períodos de tempo mais alargados, ou com uma maior redução a nível lesional7. Isto, principalmente, devido ao efeito de “ricochete” que pode acontecer cerca de 24 horas após a descontinuação abrupta de oclacitinib15, e estando também
registado um aumento expectável do grau de prurido após os 14 dias de administração do oclacitinib BID16. Contudo, no presente estudo não se verificou um efeito benéfico na adição dos glucocorticoides orais a este nível, tendo-se observado também um maior número de animais em que foi possível realizar o tratamento em dias alternados no grupo P, o que pode dever-se à distribuição desigual de raças entre os dois grupos. Devido ao acaso, a maior parte dos retrievers do Labrador foram alocados no grupo P, tendo todos os cães da raça Buldogue Francês sido alocados no grupo G. Na experiência dos autores observa-se que os Buldogues Franceses são uma raça que muitas vezes demonstra alguma resistência aos tratamentos para a DAc, apresentando também quadros clínicos maioritariamente inflamatórios, em que se verifica sobretudo eritema.
Para além disso, não foi possível adotar um plano terapêutico em dias alternados num período de tempo superior a 60 dias em nenhum cão desta raça, o que corrobora com o que foi referido.
O grupo P foi principalmente constituído por cães da raça retriever do Labrador, nos quais foi possível realizar o protocolo em dias alternados a longo prazo com sucesso (Figuras 4 e 5). Este facto pode tornar-se bastante relevante, pois os indivíduos desta raça normalmente apresentam um peso compreendido entre os 24 e os 36 kg(8), o que implica que um tratamento com oclacitinib assuma custos mais elevados. O tratamento em dias alternados possibilita, assim, uma redução deste custo para metade, o que poderá permitir que um maior número de animais receba um tratamento com oclacitinib e diminuia deste modo o encargo que o custo elevado destes fármacos implica para as famílias.

Figura 4 Retriever do Labrador do grupo P, no início do estudo (D-30), com eritema exuberante e alopecia autoinduzida, principalmente a nível das extremidades dos membros. CADESI-04: 83; Prurido: 6,7
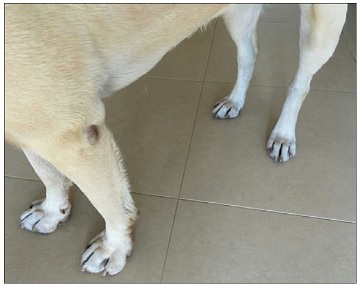
Figura 5 Retriever do Labrador do grupo P, após 30 dias de tratamento em dias alternados (end-point), com melhorias visíveis a nível das lesões cutâneas. CADESI-04: 5; Prurido: 0,2
A ausência de resposta ao oclacitinib, ou a resposta menos acentuada, observada em alguns indivíduos, pode eventualmente estar associada a uma predominância de outros mediadores do prurido em relação à IL-31. A componente genética pode ter uma grande influência na fisiopatologia da DAc e, consequentemente, no fenótipo clínico de cada animal. Os avanços no estudo do genoma permitiram investigar com maior detalhe a base genética da DAc, sabendo-se que existe uma rede complexa de vários genes, com múltiplas variantes17,18. A DAc é uma doença com uma base genética heterogénea que varia de raça para raça e entre pools genéticos geográficos, o que pode explicar as diferentes manifestações clínicas e respostas a tratamentos entre indivíduos e entre raças17-19. A DAc pode vir, assim, a ser separada em “endofenótipos” distintos, que poderão necessitar de abordagens terapêuticas diferentes20.
Adicionalmente, em dois animais, após saída do estudo, optou-se pela adição de um spray de aceponato de hidrocortisona a 0,0584% (Cortavance®), apenas aos fins de semana, nas zonas previamente afetadas. Estes dois animais continuam ainda sob este protocolo. A adição de Cortavance® a este protocolo pode ser, de facto, vantajosa, visto que poderá permitir períodos sem crises mais prolongados12. A introdução deste medicamento em spray no início do protocolo terapêutico (D-30) poderá também facilitar a transição para o protocolo em dias alternados, como já demonstrado por Takahashi e colaboradores21.
Quanto aos efeitos secundários, no grupo P registou-se um animal com episódios de vómito no início do tratamento e outro no qual o tutor descreveu PU/PD. Estes eventos
resolveram-se sem ser necessária qualquer tipo de intervenção.
Estes efeitos adversos registados no grupo P, ao qual apenas foi administrado oclacitinib, vão ao encontro daquilo que foi observado por Cosgrove et. al22. Já no grupo G, apenas se registou PU/PD e polifagia num dos animais no início do tratamento, algo expectável, visto os glucocorticoides orais terem sido administrados nos primeiros 7 dias aos animais pertencentes a este grupo23,24.
Limitações
Sendo este um estudo-piloto, a amostra pode ser considerada adequada, sendo salvaguardado que os resultados devem ser interpretados com cautela25. Para além disso, a amostra foi constituída por animais admitidos à consulta de referência no Serviço de Dermatologia do HEV da FMV‑ULisboa, onde se apresentam muitas vezes casos de DAc mais graves e complicados de gerir, atingindo valores de CADESI-04 ≥35 (doença de grau moderado e grave)13 e de grau de prurido ≥4 (prurido ligeiro a muito grave)14.
A escala de prurido, apesar de validada, apresenta sempre algum grau de subjetividade por si só, tendo alguns tutores apresentado alguma dificuldade no seu preenchimento, o que poderá ter levado a vieses na sua avaliação.
Teria ainda sido interessante realizar um maior acompanhamento dos animais, pelo menos quinzenal. No entanto, tal torna-se muitas vezes impossível devido à disponibilidade dos tutores e devido à agenda preenchida do Serviço de Dermatologia do HEV.
CONCLUSÕES
Existe potencial neste protocolo em dias alternados que permite reduzir custos para metade, possibilitando um maior acesso a esta ferramenta terapêutica inovadora, segura e muito eficaz. Não parece, contudo, existir benefício em associar prednisolona oral no início do tratamento.
Verificou-se que, entre as duas das raças com maior prevalência da DAc, o Buldogue Francês e o Retriever do Labrador, esta última apresenta um maior potencial de realizar o tratamento com oclacitinib em dias alternados, atingindo o controlo clínico e durante longos períodos de tempo.
São necessários estudos futuros que comparem o protocolo-padrão do oclacitinib com o protocolo experimental do presente estudo em termos de eficácia e segurança em diferentes raças de cães. Poderão ainda ser realizados estudos que englobem também cães com DA de grau ligeiro, isto é, com CADESI-04, compreendido entre 10 e 35.