ENQUADRAMENTO EPIDEMIOLÓGICO
A alergia às proteínas do leite de vaca (APLV) é a principal causa de alergia alimentar em idade pediátrica, podendo afetar até 3 a 5% das crianças nos primeiros anos de vida1-4. Na revisão sistemática e meta-análise de Nwaru e colaboradores1, referente à epidemiologia da alergia alimentar na Europa, foi identificada uma prevalência global de alergia ao leite autorreportada de 2,3%, reduzindo para 0,6% quando confirmada por prova de provocação oral. A APLV foi a alergia alimentar mais frequente nos países em análise, em particular em idade pré-escolar. Uma década depois, na revisão sistemática e meta-análise de Spolidoro e colaboradores4, a APLV persiste como principal causa de alergia alimentar na Europa, com uma prevalência global autorreportada de 3,1%, reduzindo para 0,3% quando confirmada por prova de provocação oral.
No nosso país, o leite de vaca é também o alimento mais frequentemente responsável por casos de alergia alimentar em idade pediátrica5,6, assim como é a principal causa de anafilaxia (32% das anafilaxias de etiologia alimentar em idade pediátrica) e a primeira causa de recorrência de anafilaxia na criança 7-10. Sendo o leite de vaca um alergénio alimentar ubiquitário, a APLV revela-se uma doença associada a redução marcada da qualidade de vida do doente e da família, impacto psicológico e social negativo, além de risco de vida, particularmente nas formas graves e persistentes3,11.
Embora na maioria das crianças a APLV resolva espontaneamente até aos cinco anos de idade, os quadros clínicos são cada vez mais persistentes, com mais de um terço dos casos a perdurar na adolescência12,13. Skripak e colaboradores realizaram um estudo prospetivo englobando 807 crianças com APLV mediada por imunoglobulina E (IgE), identificando taxas de resolução de apenas 42%, 64% e 79% em crianças com idades de 8, 12 e 16 anos, respetivamente12. Nos quadros mediados por IgE, o prognóstico é cada vez menos favorável à medida que aumenta a duração da doença12-14. Esta realidade torna-se ainda mais preocupante e geradora de marcada ansiedade no doente e na família15,16 quando a clínica é grave e a probabilidade de ocorrerem contactos acidentais com o alergénio oculto é elevada. Foram identificados como fatores de risco para a persistência da APLV a existência de asma12,17 e os níveis mais elevados de IgE específica sérica para leite de vaca, maior persistência associada a valores ≥ 5 kU/L e pior prognóstico se ≥ 20 kU/L (12), embora os valores variem entre as populações estudadas14,17,18.
Com a enorme variedade de produtos alimentares processados, a dieta de evicção de proteínas do leite de vaca (PLV) torna-se difícil de executar, estando associada a um elevado risco de ingestão acidental, nomeadamente na forma oculta, com consequentes reações adversas, que podem ser graves ou mesmo fatais13,19-21. Numa revisão efetuada no Reino Unido, com duração de vinte anos, o leite de vaca foi identificado como o principal responsável por anafilaxia fatal em crianças em idade escolar, tendo sido responsável por 17 dos 66 casos (26%) de morte por anafilaxia em idade escolar (20. Atualmente, o leite de vaca é globalmente considerado a principal causa de anafilaxia fatal em idade escolar, atingindo o maior risco na adolescência13,20,22.
INDICAÇÕES E CONTRAINDICAÇÕES
Para os casos de APLV persistente e grave, a abordagem terapêutica clássica, que assenta na dieta de evicção, torna-se insuficiente e associada a elevado risco de reação adversa grave por ingestão inadvertida de PLV, alergénio altamente disseminado nos alimentos processados. Deste modo, e pela facilidade de obtenção de uma matéria-prima barata e facilmente doseável em quantidades crescentes, justifica-se que o leite de vaca seja, indiscutivelmente, o alergénio alimentar mais investigado no âmbito dos protocolos de imunoterapia oral com alimentos.
Deve ser sempre obtida evidência da presença de IgE específica23 através da realização de testes cutâneos por picada e do doseamento de IgE específica sérica para leite total e PLV (caseína, alfa-lactoalbumina e beta-lactoglobulina).
Caso exista alguma dúvida sobre a tolerância atual às PLV, deve ser realizada uma prova de provocação oral com leite de vaca, após obtenção de consentimento informado. Embora a prova de provocação oral em dupla ocultação controlada com placebo seja considerada necessária para efeitos de estudos de investigação, a prova de provocação oral em protocolo aberto é, em geral, suficiente na prática clínica. A prova de provocação oral deve ser sempre realizada em hospital-de-dia, garantindo as condições de segurança indispensáveis ao diagnóstico e tratamento de eventuais reações adversas, incluindo anafilaxia.
Na avaliação destes doentes, é ainda importante alertar que na APLV está bem documentado um elevado grau de reatividade cruzada entre as caseínas do leite das diferentes espécies de mamíferos, pelo que a recomendação nestes doentes deve ser a evicção rigorosa de PLV e de búfala, cabra e ovelha24,25.
As indicações e contraindicações para a realização de imunoterapia com leite estão descritas na Tabela 1 3,13,26,27. A imunoterapia oral está indicada na APLV IgE-mediada, particularmente casos graves e persistentes que mantêm a reatividade clínica após os quatro a cinco anos de idade26,27. No entanto, alguns estudos têm incluído crianças com idades inferiores, e as normas de orientação da SEAIC (Sociedad Española de Alergología e Inmunología Clínica) propõem a idade superior a dois anos para o início da imunoterapia com leite13. Assim, apesar da elevada probabilidade de desenvolvimento de tolerância espontânea nesta faixa etária, em casos excecionais uma imunoterapia precoce pode ser considerada em função do prognóstico individual.
Tabela 1 Indicações e contraindicações da imunoterapia oral com leite3,13,26,27
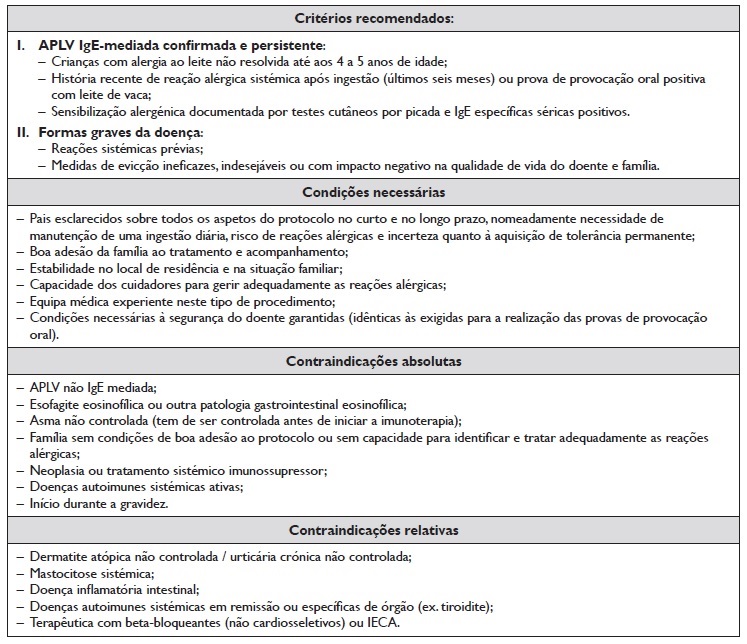
APLV: alergia às proteínas do leite de vaca; IECA: inibidores da enzima de conversão da angiotensina
Esta intervenção terapêutica específica deve ser criteriosamente utilizada, sempre em centros hospitalares especializados, com a necessária diferenciação e apoio permanente de uma equipa médica especializada e experiente, garantindo a máxima segurança e eficácia da intervenção13,26,27. São também condições necessárias, a disponibilidade e a compreensão de objetivos por parte do doente e prestadores de cuidados, assim como o conhecimento informado dos riscos associados e da necessidade de terapêutica de manutenção prolongada com o alimento23.
REVISÃO DE ESTUDOS
Nos últimos anos têm-se multiplicado as publicações sobre esta abordagem inovadora, existindo vários casos clínicos e estudos que confirmam elevadas taxas de sucesso na imunoterapia com leite de vaca (28-40), incluindo estudos controlados e aleatorizados31-33,35,36,39, bem como a persistência do efeito após vários anos de tratamento40-42, geralmente dependente da exposição diária mantida às PLV.
A maioria dos protocolos utiliza a via oral e alguns, em menor número, a via sublingual. Há muitas diferenças entre os protocolos publicados, nomeadamente no que diz respeito à idade de início e características dos doentes incluídos, dose inicial, ritmo de progressão, dose de manutenção, produto utilizado, entre outras. Na maioria dos estudos, o leite de vaca em natureza puro é o produto utilizado, não diluído, ou diluído a 1:10, 1:25 ou 1:100.
O leite baked, ou seja, cozinhado (com exposição a elevadas temperaturas [180ºC] e por um período extenso [cerca de 30 minutos]) em matriz de trigo, foi proposto por alguns autores por ser menos alergénico, ao alterar a estrutura dos epitopos conformacionais13,43, mas revelou menor eficácia para a dessensibilização3,44,45.
No entanto, Dantzer e colaboradores (39), em 2022, publicaram um protocolo com doses progressivas de leite baked em que obtiveram 73% de dessensibilização total, tendo sido utilizada adrenalina em 20% dos doentes. Importa referir que um dos critérios de inclusão no estudo era as crianças previamente tolerarem 3 mg de leite baked. Salienta-se que o consenso da WAO (World Allergy Organization) não recomenda a imunoterapia oral com leite baked 3. A utilização de leite aquecido também foi proposta por alguns autores pelo mesmo motivo, mas revelou igualmente menor eficácia para a dessensibilização46.
Têm sido publicados protocolos muito diversos de imunoterapia oral ao leite, todos eles incluindo uma fase de indução, que corresponde ao intervalo de tempo entre a primeira dose de leite de vaca e a dose-alvo e uma fase de manutenção em que o doente se encontra a ingerir diariamente a dose-alvo definida de leite de vaca durante anos. Nos protocolos convencionais, a fase de indução pode durar vários meses, com aumentos de dose diários ou a intervalos de poucas semanas. Nos protocolos rápidos (rush), os aumentos de dose fazem-se a cada 20 minutos até poucas horas. Existem, ainda, protocolos mistos que se iniciam com uma fase rápida seguida de uma abordagem convencional mais lenta23.
A dessensibilização ao leite através da imunoterapia oral caracteriza-se por um aumento transitório do limiar da dose do leite que pode desencadear a reação alérgica, ou seja, por uma redução reversível da reatividade clínica após exposição a doses progressivamente crescentes do leite, que pode ser perdida após interrupção da ingestão regular das PLV. O objetivo da imunoterapia, o estado
de tolerância permanente23, define-se como a ausência permanente da reatividade clínica ao leite, mesmo que este não seja consumido de forma regular. O sucesso da imunoterapia com o leite pode assim definir-se em dois níveis. No primeiro nível, ocorre a dessensibilização e o doente atinge a capacidade de tolerar a ingestão diária de uma quantidade normal de leite ou derivados (habitualmente 200mL, correspondendo a 6,4 - 7 g de PLV), voltando a reagir se a ingestão deixar de ser regular. No segundo nível, o doente atinge a tolerância permanente e o leite é tolerado sem reação, mesmo na ausência de ingestão regular de PLV.
Na literatura publicada observa-se alguma variabilidade nas taxas de sucesso, dependendo do tipo de protocolo, características da população tratada e critérios de avaliação dos resultados. Na Tabela 2 efetua-se uma revisão de alguns dos principais estudos publicados de imunoterapia oral e sublingual ao leite de vaca, avaliando dados como o tipo de estudo, a população incluída, o produto utilizado, a dose-alvo considerada, a eficácia e a segurança do estudo 29,31-36,38-40,46-52.
Tabela 2 Revisão de estudos de imunoterapia oral e sublingual ao leite de vaca: número de doentes incluído, tipo de estudo, idade da população incluída, produto utilizado, dose-alvo do estudo, eficácia (percentagem de doentes que conseguiram a dessensibilização) e segurança (anafilaxia e esofagite eosinofílica durante a dessensibilização)29,31-36,38-40,46-52
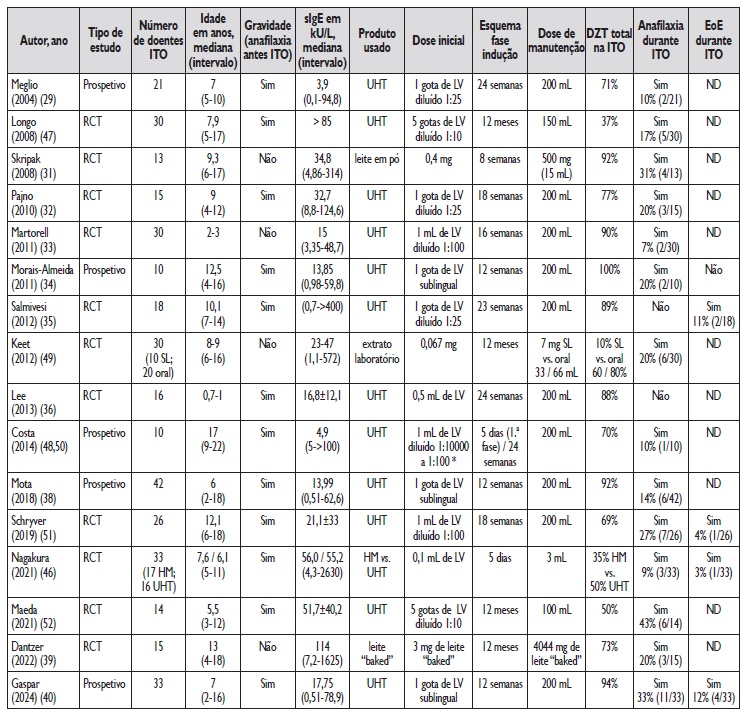
Dessensibilização total na ITO: Definida como a percentagem de doentes que atingiu a dose de manutenção
* dose correspondente à diluição superior à que foi reativa no teste cutâneo por picada-picada (de 1mL de LV diluído a 1:10000 a 1mL de LV diluído a 1:100)
DZT - dessensibilização; EoE - esofagite eosinofílica; ITO - imunoterapia oral; HM - leite aquecido (leite em pó, preparado por aquecimento a 125°C por 30 segundos e secagem por pulverização por 3 segundos); Leite em pó - leite em pó desnatado seco;
LV - leite de vaca; ND - não disponível; RCT - estudo controlado e aleatorizado; sIgE - imunoglobulina E específica para leite de vaca; SL - imunoterapia por via sublingual; UHT - leite de vaca puro ultrapasteurizado
Bauer e colaboradores, em 1999, publicaram o caso de uma adolescente de 12 anos com APLV IgE-mediada que foi submetida, com sucesso, a imunoterapia oral em protocolo rápido com duração de cinco dias em ambiente hospitalar, iniciando com 1mL de leite de vaca diluído a 1:100 até à dose-alvo de 200mL 28.
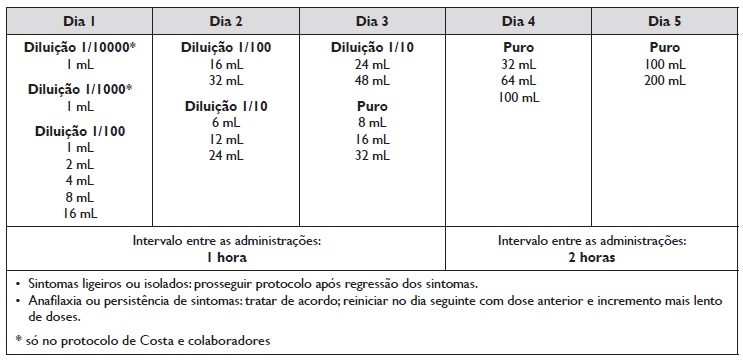
Martorell-Aragonés e colaboradores adaptaram o protocolo de Bauer e colaboradores (28) e, em 2007, apresentaram um estudo prospetivo de três anos de duração incluindo quatro crianças com APLV IgE-mediada grave que foram submetidas, com sucesso, a imunoterapia oral em protocolo rápido com duração de 5 dias em ambiente hospitalar, iniciando igualmente com 1mL de leite de vaca diluído a 1:100 até à dose-alvo de 200mL(30). Este protocolo é apresentado na Tabela 3 30 e foi, precisamente, o primeiro protocolo utilizado no nosso país. No estudo referido, este protocolo obteve 100% de dessensibilização total e evidência de diminuição progressiva da reatividade nos testes cutâneos por picada para o leite, e dos valores de IgE específica para caseína, tendo estes últimos negativado após 3 anos em três crianças estudadas30. No entanto, importa referir que três crianças tinham apenas dois anos ou menos de idade (duas crianças com dois anos e uma com 19 meses).
Tabela 3 Protocolo rápido de imunoterapia oral com leite de vaca de Costa e colaboradores (48,50) adaptado do protocolo de Martorell-Aragonés e colaboradores (30) (adaptado do protocolo de Bauer e colaboradores) 28
Um dos estudos iniciais sobre imunoterapia oral com leite de vaca, embora não controlado, foi publicado por Meglio e colaboradores em 2004 (29), tendo incluído 21 crianças (com idades superiores a cinco anos) com APLV IgE-mediada grave que foram submetidas a um protocolo lento com seis meses de duração, com início em 1 gota de leite diluído a 1:25 (correspondendo a 0,06mg de PLV) e término aos 180 dias com 200mL (6,4g de PLV). Em 15 das 21 crianças (71%) foi atingida a dose-alvo de 200mL (dessensibilização total), sendo que três crianças toleraram doses entre 40 e 80mL de leite (dessensibilização parcial). Quatro anos depois 41, os mesmos autores demonstraram que a dessensibilização se manteve em 14 das 20 crianças (65%), isto sempre dependente da ingestão regular de leite. Nestas 14 crianças ocorreu diminuição dos valores de IgE específica sérica para leite de vaca e, em seis casos, os testes cutâneos por picada negativaram, sendo propostos pelos autores como indicadores de bom prognóstico41.
Staden e colaboradores, em 2008, publicaram os resultados de um protocolo com uma fase de indução rápida(53), visando atingir 120mL de leite numa semana.
Em seis de nove crianças (67%) foi possível atingir a dose-alvo na primeira semana e, nas restantes, foi alcançada uma dessensibilização parcial (toleraram doses entre 3 e 40mL de leite). Ocorreram com frequência efeitos adversos, ligeiros e controlados com tratamento sintomático.
O estudo controlado de Longo e colaboradores(47), publicado em 2008, incluiu 30 crianças (com idades entre os cinco e os 17 anos) com formas graves de APLV IgE-mediada submetidas a imunoterapia oral com leite. Na inclusão, todas as crianças reagiam previamente a doses inferiores a 1mL no decurso de provas de provocação oral em dupla ocultação. O protocolo apresentado consistiu em duas fases: uma primeira fase rápida em ambiente hospitalar com duração de 10 dias (com início em 5 gotas de leite de vaca diluído a 1:10 e final em 20mL do leite puro); uma segunda fase lenta no domicílio, com aumento gradual da dose de 1mL a cada dois dias, até à dose-alvo de 150mL. Os pais possuíam um esquema escrito com o aumento das doses no domicílio e contacto telefónico da equipa disponível nas 24 horas. Após um ano, das 30 crianças que efetuaram imunoterapia oral, 11 (37%) alcançaram dessensibilização total e 53% dessensibilização parcial, totalizando 90%; no mesmo período, nenhuma das 30 crianças do grupo-controlo atingiu a tolerância. Em cinco crianças que efetuaram imunoterapia oral ocorreu anafilaxia, com necessidade de administração de adrenalina intramuscular (17%).
Posteriormente, foram publicados diversos estudos controlados de imunoterapia com o leite de vaca que confirmaram a eficácia desta intervenção terapêutica para aumentar o limiar de reatividade clínica, ou seja, assegurar a dessensibilização 31-33,35,36,54-60. Uma meta-análise publicada em 2022 54, que incluiu 469 crianças, englobando 11 estudos controlados e aleatorizados de imunoterapia oral com leite de vaca, demostrou um benefício significativo no que respeita à eficácia em termos de dessensibilização (73%) para a APLV (RR: 7,35; IC95%, 2,82-19,13). O benefício foi mais significativo nas crianças com mais de três anos de idade (RR: 18,05; IC95%, 6,48‑50,26).
As reações adversas foram frequentes, ocorrendo em 82% das crianças submetidas a imunoterapia oral ao leite, embora tenham sido maioritariamente ligeiras e autolimitadas. Ainda assim, a ocorrência de anafilaxia com necessidade de uso de adrenalina foi significativamente mais frequente (13%) nas crianças submetidas a imunoterapia oral ao leite, em comparação com a dieta de evicção ou o placebo (RR: 7,69, IC95%: 2,16-27,33).
Os protocolos em que o leite é administrado por via oral têm melhor eficácia do que os que utilizam a via sublingual, mas, em contrapartida, associam-se a maior risco de reações adversas49,54. Keet e colaboradores49 efetuaram um estudo controlado que comparou a eficácia da imunoterapia por via sublingual com a imunoterapia oral, incluindo um total de 30 crianças que receberam imunoterapia por via sublingual (7mg por dia) em monoterapia ou imunoterapia sublingual seguida da via oral (1 ou 2g por dia). O estudo revelou que a imunoterapia oral após a via sublingual foi mais eficaz para a dessensibilização (60 a 80% consoante 1 a 2g de PLV, comparativamente a apenas 10% na monoterapia sublingual) e a aquisição de tolerância permanente após seis semanas sem tratamento (10 a 33% consoante 1 a 2g, comparativamente a 0% na monoterapia sublingual). A frequência de reações sistémicas foi mais elevada no esquema com imunoterapia oral.
Uma outra abordagem proposta para reduzir a frequência de reações adversas sistémicas são os protocolos com dose baixa fixa61,62, comparativamente à dose-alvo habitual. Miura e colaboradores (62), publicaram em 2021 um estudo incluindo 33 crianças com APLV IgE-mediada grave que foram submetidas a imunoterapia com dose diária de 3mL de leite de vaca. Durante o seguimento, efetuado ao longo de 3 anos, a proporção de crianças que toleraram 25mL (em prova de provocação oral, após duas semanas de interrupção) aumentou anualmente (27%, 51% e 61% após um, dois e três anos de tratamento, respetivamente). Após três anos, ocorreu uma redução significativa dos valores de IgE específica para leite e para caseína e um aumento significativo dos valores de IgG4 para caseína. Porém, o interesse destes protocolos será apenas em termos de redução do risco associado a ingestões acidentais, pois não permitem uma dieta livre sem restrições de PLV, que é o objetivo prioritário da imunoterapia com leite de vaca. No entanto, em doentes de alto risco de anafilaxia, pode ser uma opção a longo prazo. Esta pode ser também uma opção preferida por alguns doentes que não pretendam uma dieta livre sem restrições de PLV e queiram apenas reduzir o risco de reação por exposição acidental.
Como referido, os protocolos publicados e as populações estudadas têm características muito diversas, mas a maioria dos estudos apresenta frequências de dessensibilização elevadas (superiores a 70%)29,31-36,38‑40,56.
Pelo contrário, são muito escassas as informações sobre resultados a longo prazo, nomeadamente no que respeita à eficácia quanto à aquisição de tolerância permanente35,54,56,59,63, à segurança quanto à ocorrência de reações alérgicas graves e uso de adrenalina durante a fase de manutenção e quanto à possibilidade de aparecimento de esofagite eosinofílica como efeito adverso indesejável após imunoterapia oral com leite. A meta-análise publicada pela WAO em 202263, que incluiu 13 estudos controlados e aleatorizados e 109 estudos observacionais de imunoterapia oral com leite de vaca, demonstrou um benefício significativo no que respeita à eficácia em termos de dessensibilização para a APLV (RR: 12,3; IC95%, 5,9-26), mas reduzindo para apenas 36% quanto à aquisição de tolerância permanente. A imunoterapia oral com leite aumentou o risco de anafilaxia (RR: 60; IC95%, 15-244) e a frequência do uso de adrenalina (RR: 35,2; IC95%, 9-136,5) e associou-se a uma frequência média de 6,9% de desenvolvimento de esofagite eosinofílica. Na revisão de estudos apresentados na Tabela 2, a frequência de anafilaxia durante imunoterapia com leite varia de 0 a 43% e a frequência de aparecimento de esofagite eosinofílica de 3 a 12%, sendo expectável que estudos com mais tempo de seguimento se associem a frequências mais elevadas da doença35,40.
PROTOCOLOS UTILIZADOS A NÍVEL NACIONAL
O primeiro protocolo de imunoterapia oral utilizado a nível nacional foi o protocolo rápido de Martorell‑Aragonés e colaboradores, publicado em 2007 30.
Este protocolo, apresentado na Tabela 3, consiste em 5 dias consecutivos no hospital-de-dia, utilizando o leite de vaca ultrapasteurizado, iniciando-se com diluições de 1:100, depois 1:10, em doses crescentes, seguindo-se o leite não diluído no terceiro dia, até à dose-alvo prevista de 200mL. Em 2011, Costa e colaboradores 48,50 apresentaram uma série de doentes submetidos a um protocolo adaptado de Martorell-Aragonés e colaboradores30, em que antes da imunoterapia oral com leite de vaca todos os doentes realizaram testes cutâneos por picada-picada com leite de vaca em natureza em diluições progressivas de 1:10000, 1:1000, 1:100, 1:10 e 1:1, de modo a encontrar a menor dose reativa, iniciando-se a fase rápida do protocolo com a dose correspondente à diluição superior à que foi reativa no teste cutâneo (exemplo: se positividade no teste cutâneo com a diluição 1:100, o protocolo inicia-se com a diluição 1:1000, exceto se o teste for positivo na diluição de 1:10000, a dose inicial da imunoterapia será com essa diluição, 1:10000), aumentando progressivamente a dose ao longo de 5 dias consecutivos no hospital-de-dia (Tabela 3).
Nos doentes que não atingiram na primeira fase os 200mL, segue-se uma segunda fase com aumento gradual semanal até à dose-alvo de 200mL.
Como referido, a imunoterapia oral com leite em alguns doentes com clínica grave de anafilaxia associou-se a ocorrência de anafilaxia com necessidade de administração de adrenalina intramuscular 31-33,47,48,56,63.
Neste sentido, e atendendo à menor ocorrência de reações adversas nos protocolos sublinguais comparativamente aos orais, foi elaborado um protocolo misto, sublingual e oral, utilizando o leite de vaca ultrapasteurizado puro, não diluído. O protocolo misto sublingual‑oral de imunoterapia com leite de vaca de Morais-Almeida e colaboradores, publicado em 2011 (34), revelou-se uma terapêutica inovadora, eficaz e segura. Este protocolo é apresentado na Tabela 4. Neste protocolo, as doses iniciais são sublinguais (contacto com a mucosa oral durante dois a cinco minutos, expelindo o alergénio no final), seguidas da ingestão oral de doses progressivamente crescentes de leite de vaca até à dose-alvo de 200mL por dia, estando previstas cinco visitas hospitalares num intervalo variável de 12 semanas. Na fase de indução, podem ser realizadas aplicações adicionais sublinguais ou orais quando necessário, nomeadamente se ocorrerem manifestações locais ou sistémicas significativas.
Tabela 4 Protocolo de imunoterapia sublingual-oral ao leite de vaca de Morais-Almeida e colaboradores (34)
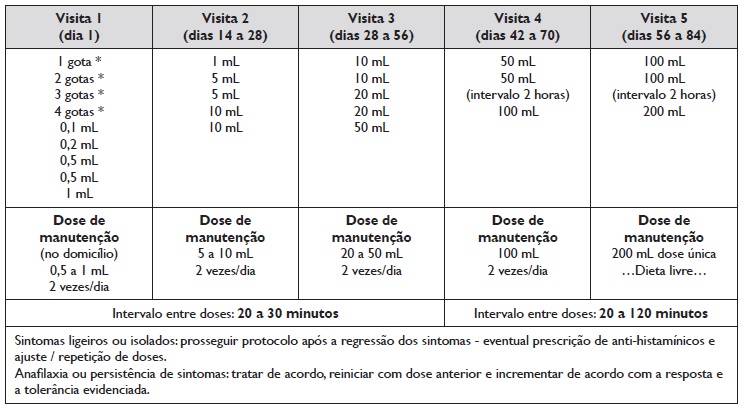
* doses sublinguais.
Nota: A programação das visitas hospitalares é variável, de acordo com a resposta ao tratamento e a conveniência do doente e da família. Estão previstas visitas adicionais e ajustes na progressão das doses. As doses de manutenção são realizadas no domicílio. O alergénio utilizado é o leite de vaca puro.
A dose-alvo de 200mL é a dose aceite como critério de sucesso da intervenção em ambos os protocolos, sendo esta dose consensualmente aceite pela maioria dos autores29,32,33,35,36,38,40,51. A programação das visitas é flexível, de acordo com a resposta ao tratamento e a conveniência do doente e da família, estando previstas visitas adicionais e ajustes na progressão das doses, quando necessário. A subida da dose, na fase de indução, decorre sempre em hospital-de-dia de Imunoalergologia.
O consentimento informado é obtido em todas as sessões do tratamento. É facultado o contacto telefónico da equipa médica nas 24 horas. Até à sessão seguinte, os doentes cumprem no domicílio a ingestão diária das doses atingidas em ambiente hospitalar na fase de indução, e depois na dose de manutenção, sempre após a refeição, evitando o exercício físico vigoroso nas duas horas subsequentes.
Todos os doentes dispõem de medicação de emergência para tratamento de reação alérgica (incluindo dispositivo autoinjetor de adrenalina, anti-histamínico e corticosteroide orais e, se doente asmático, broncodilatador beta2-agonista de curta ação inalado)13,34,64,65.
Em todos os doentes devem ser mantidas as suas terapêuticas de prevenção diária, incluindo terapêutica com anti-histamínico oral, e de agudização para as patologias alérgicas coexistentes.
No estudo de Morais-Almeida e colaboradores(34) foram incluídas 10 crianças, entre os 4 e os 16 anos (média etária de 10,9 anos), com APLV IgE-mediada persistente e grave, com clínica anterior de anafilaxia e manifestações alérgicas no último ano (por ingestão de leite como alergénio oculto, ou por realização de prova de provocação oral). Neste estudo, todas as crianças alcançaram a dose-alvo de 200mL, permitindo uma dieta sem restrições relativamente às PLV. Registaram-se, durante a fase de indução, reações alérgicas ligeiras a moderadas em 80% das crianças, resolvidas com terapêutica oral (anti-histamínicos e/ou corticosteroides) e reações de anafilaxia em 20% (um caso após exercício físico, dependente da ingestão de leite de vaca, e um caso por ingestão acidental de leite de vaca).
No estudo de Costa e colaboradores 50, foram incluídos 10 doentes com idades compreendidas entre os 9 e os 22 anos (média etária de 16,8 anos) com APLV IgE-mediada persistente e grave, com manifestações alérgicas nos últimos três meses (por exposição acidental ou em prova de provocação oral). Todos os doentes conseguiram cumprir a fase rápida (5 dias) do protocolo: cinco doentes atingiram os 200mL de leite de vaca, um alcançou 100mL, dois 45mL, um 40mL e um 10mL.
Após seis meses, 70% dos doentes obtiveram a dessensibilização total, tendo alcançado a dose-alvo de 200mL por dia, permitindo uma dieta sem restrições relativamente às PLV.
No estudo prospetivo de Mota e colaboradores(38), incluindo 42 doentes submetidos a imunoterapia com leite, com um tempo de seguimento de até 8 anos, a utilização do protocolo de Morais-Almeida e colaboradores34 confirmou-se eficaz e segura. A dessensibilização total foi obtida em 92% dos doentes, e durante a fase de manutenção registaram-se reações alérgicas em 45% dos casos, maioritariamente associadas a dois cofatores, exercício físico e infeções (respiratórias e gastrointestinais).
Neste estudo, foram identificados como fatores de risco para a ocorrência de reações alérgicas na fase de manutenção a existência de história prévia de anafilaxia e a coexistência de asma.
No estudo prospetivo de Gaspar e colaboradores(40), incluindo 33 doentes submetidos a imunoterapia com leite, com um tempo de seguimento de até 15 anos, a utilização do protocolo de Morais-Almeida e colaboradores34 confirmou-se igualmente eficaz e segura. A dessensibilização total foi obtida em 94% dos doentes, e durante a fase de manutenção registaram-se reações alérgicas em 77% dos doentes, com destaque para a ocorrência de anafilaxia em sete doentes, com um total de 11 episódios de anafilaxia durante a fase de manutenção, incluindo cinco episódios induzidos pelo exercício físico e quatro associados a ingestão acidental de proteínas do leite de cabra e de ovelha (três deles, em contexto de ingestão de queijo).
COFATORES E RECOMENDAÇÕES
Durante a realização da imunoterapia com leite de vaca, vários cofatores podem aumentar a permeabilidade intestinal, relacionando-se com a ocorrência de reações adversas inesperadas e potencialmente graves para doses previamente bem toleradas13,66. Estas reações, possíveis de ocorrer em qualquer fase do tratamento, têm sido mais frequentemente reportadas na fase de indução e no início da fase de manutenção, bem como sempre que ocorre um aumento da dose diária do leite.
O cofator mais descrito e caracterizado na imunoterapia oral com leite é o exercício físico13,38,42,67,68.
A realização de esforço físico pode estar relacionada com a ocorrência de quadros de urticária ou mesmo de anafilaxia induzida pelo exercício dependente da ingestão de PLV; por este motivo, deverá ser sempre recomendado a todos os doentes que seja respeitado um intervalo mínimo de duas horas entre a exposição ao leite e a prática de exercício físico vigoroso. Alguns consensos aconselham períodos mais prolongados, nomeadamente até três horas13,26 e mesmo até quatro horas3. No entanto, pela experiência dos autores, um intervalo de duas horas é suficiente, e prolongar por mais tempo a evicção de exercício físico em idade pediátrica não é viável na vida real.
Outros cofatores têm sido descritos na imunoterapia com leite de vaca, entre os quais o jejum, a febre, a existência de infeção aguda concomitante (particularmente infeções virais respiratórias ou gastrintestinais), a toma de fármacos anti-inflamatórios não esteroides, o stresse emocional, o cataménio, a ingestão de álcool (importante nos adolescentes) e a maior exposição a aeroalergénios a que o doente está sensibilizado (principalmente em época polínica)3,13,26,27,66.
As recomendações mais importantes que devem ser respeitadas para prevenir reações adversas durante a imunoterapia oral com leite estão enumeradas na Tabela53,13,26,27,66. A comunicação adequada entre o médico e o doente e seus familiares, assegurando o acesso direto à equipa médica a qualquer hora, bem como a informação sobre os fatores de risco e o ajuste permanente das doses, permite minimizar a ocorrência de reações adversas 23.
SEGUIMENTO: DA AVALIAÇÃO INICIAL À FASE DE MANUTENÇÃO
A imunoterapia oral com leite implica um seguimento de longa duração na fase de manutenção, com necessidade de assegurar a ingestão diária da dose do leite de vaca40,42,58,66. A maioria dos doentes necessita de manter a exposição diária às PLV para assegurar a dessensibilização.
Deve-se alertar que o estado de tolerância permanente pode não ser alcançado, existindo um estado de dessensibilização dependente da ingestão regular do leite 58,66, pelo que o doente e os seus cuidadores têm de ser continuamente motivados para a adesão ao tratamento. Na fase de manutenção, a opção de transitar para derivados do leite (como o iogurte) ou outros produtos alimentares comerciais com quantidades equivalentes de PLV (cerca de 6,4g por dia), que podem ser mais agradáveis em termos do paladar para o doente, tem-se revelado uma forma eficaz de assegurar a adesão ao tratamento58. Doses menos frequentes, ou seja, não diárias, ou diminuídas, ou seja, inferiores à dose-alvo, podem fornecer benefícios práticos ao doente para assegurar a adesão na fase de manutenção, mas podem afetar a dessensibilização58.
O objetivo da imunoterapia com leite de vaca é permitir uma dieta livre, sem restrições de PLV. No entanto, no início da fase de manutenção é importante alertar que o consumo de alimentos contendo PLV deve ser efetuado respeitando um intervalo mínimo de duas horas com a dose de manutenção estabelecida do leite 66.
Em relação aos derivados do leite, convém alertar para o problema do queijo, não só pela elevada concentração proteica, como pela possibilidade de ter na sua composição proteínas do leite de outras espécies de mamíferos (particularmente cabra e ovelha), às quais o doente submetido a imunoterapia com leite de vaca pode reagir 13,25,40. A dieta livre para as PLV deve manter a evicção de proteínas do leite de cabra, ovelha e búfala até ser confirmada a tolerância a estas proteínas.
Em doentes sensibilizados às proteínas do leite de outras espécies de mamíferos, no final do protocolo a tolerância deve ser avaliada por testes cutâneos por picada e se necessária prova de provocação oral, antes da introdução na dieta, exceto no caso de ser conhecida a tolerância a esses leites antes da imunoterapia ao leite de vaca 13.
A existência de fatores de risco, como asma, dermatite atópica ou rinite mal controladas, podem influenciar negativamente a tolerância durante o protocolo 3,13,27, motivos pelos quais não só durante a fase de indução, como também na fase de manutenção, o doente deve manter a terapêutica preventiva indicada no controlo de patologias coexistentes, incluindo terapêutica com anti-histamínico oral.
De igual modo, a possibilidade de ocorrência de reações não esperadas, nomeadamente associadas a cofatores, justifica que os doentes continuem a ser portadores do dispositivo autoinjetor de adrenalina, mesmo após a conclusão da fase de indução. É importante a atualização constante do plano de emergência, nomeadamente de acordo com o peso da criança, e a revisão do treino do dispositivo autoinjetor de adrenalina 11,64,65.
Os doentes e cuidadores devem ser informados sobre a importância dos cofatores, de forma a minimizar a ocorrência de reações alérgicas na fase de manutenção do protocolo (Tabela 5). A família deve escolher, de forma cuidadosa, a hora preferida para a toma da dose diária do leite, que tem de ser supervisionada pelos cuidadores, assegurando nunca ser dada em jejum e evitando o exercício físico nas duas horas seguintes.
Tabela 5 Recomendações durante a imunoterapia oral com leite de vaca para prevenir reações adversas relacionadas com Cofatores3,13,26,27,66

AINE: anti-inflamatórios não esteroides
Estudos de imunoterapia com leite têm demonstrado uma diminuição progressiva da reatividade cutânea (dimensão da pápula no teste cutâneo por picada) e dos valores de IgE específica sérica para o leite de vaca e a caseína, em comparação com os níveis basais30,38,40‑42,48,50,52,58,66.
Alguns estudos prospetivos demonstraram que os testes cutâneos ficaram negativos com a imunoterapia oral com leite30,40,41,66. Em paralelo, ocorre um aumento gradual dos valores de IgG4 específica sérica para o leite de vaca e a caseína31,32,40,42,48,50,58,66, sendo estes dados indicativos de uma dessensibilização bem-sucedida.
Assim, no âmbito do protocolo da imunoterapia com leite, deve constar a avaliação seriada através da realização de testes cutâneos por picada e IgE específicas séricas para o leite de vaca e as PLV (caseína, alfa-lactoalbumina e beta-lactoglobulina), nos seguintes tempos:
- avaliação basal,
- avaliação no final da fase de indução,
- avaliação na fase de manutenção, a cada seis meses no primeiro ano e depois a cada 12 meses 66.
Deve também ser efetuada a avaliação por testes cutâneos por picada e IgE específicas séricas para o leite de cabra e o leite de ovelha13,25 (não existindo extrato comercial, o teste cutâneo é feito com o alimento em natureza). Esta avaliação pode ser dispensada no início do protocolo, mas é imprescindível no final, para avaliar a tolerância a estas proteínas.
Se disponíveis, deve ser também incluída a avaliação das IgG4 específicas séricas para o leite de vaca a caseína, com o intuito de efetuar o estudo comparativo com a avaliação basal.
Em caso de doentes com refluxo gastroesofágico conhecido ou em caso de sintomas digestivos recorrentes, a realização de endoscopia digestiva alta com biópsias esofágicas com contagem de eosinófilos é imprescindível antes de iniciar o protocolo, para exclusão de esofagite eosinofílica que é uma contraindicação absoluta para a realização de imunoterapia oral com leite. Por outro lado, a evidência do desenvolvimento de esofagite eosinofílica em alguns doentes submetidos a imunoterapia oral com leite69-72 enfatiza a importância de alertar os doentes a cumprir este tratamento para o possível aparecimento de sintomas de disfunção esofágica sugestivos do desenvolvimento desta doença 73-75.
O seguimento do doente submetido a imunoterapia com leite deve ser mantido até perda da sensibilização alergénica documentada por testes cutâneos por picada negativos e IgE específicas negativas, ou até aquisição do estado de tolerância permanente, confirmado por período de evicção do alimento de cerca de quatro semanas, seguido de prova de provocação oral negativa66, o que não é habitualmente realizado na vida real no seguimento destas crianças, pela possibilidade de pôr em risco o estado de dessensibilização adquirido com o procedimento.
CONCLUSÕES
A imunoterapia oral, ou sublingual-oral, na APLV IgE- -mediada persistente tem-se revelado uma estratégia terapêutica eficaz e segura, apesar da frequência de reações alérgicas associadas. A imunoterapia com leite é o único tratamento com capacidade de modificar a história natural da doença, que confere proteção contra a ingestão inadvertida de PLV, especialmente na forma de alergénio oculto, o que permite uma melhoria da qualidade de vida, reduzindo o risco de vida e o impacto psicossocial negativo da APLV no doente e na família.
A APLV é a principal causa de alergia alimentar na criança, e no nosso país é a principal causa de anafilaxia e de recorrência de anafilaxia em idade pediátrica. A acrescentar, os quadros de APLV são cada vez mais persistentes, com vários casos a manter a alergia durante a segunda década de vida. Neste sentido, nos últimos anos têm-se multiplicado as publicações sobre imunoterapia oral com leite, existindo estudos que confirmam elevadas taxas de sucesso, bem como a persistência do efeito após vários anos de tratamento, apesar de geralmente dependente da exposição mantida às PLV. A maioria dos doentes necessita de cumprir a ingestão diária da dose de manutenção para manter a dessensibilização, que de forma consensual se considera os 200mL de leite, ou o equivalente de PLV em derivados do leite ou outros produtos alimentares comerciais.
A ocorrência de reações adversas é mais frequente nas ocasiões em que é realizado aumento de dose, na fase de indução, mas também pode acontecer na fase de manutenção após a ingestão de doses previamente toleradas.
A possibilidade de ocorrência de reações graves em ambulatório é uma realidade, mas o contacto permanente com a equipa médica tem permitido minimizar estas situações com o acompanhamento próximo e a gestão rápida e eficaz destes episódios. É importante o doente e a família conhecerem os principais cofatores e respeitarem as respetivas recomendações.
As crianças que mais beneficiam da imunoterapia com leite são aquelas com doença mais grave (história prévia de anafilaxia ou maior impacto da doença) e risco mais elevado de anafilaxia e de persistência da doença (valores mais elevados de IgE específica para leite e para caseína), precisamente as crianças que têm maior risco de reações adversas sistémicas no decurso da imunoterapia oral com leite.
Por todos estes motivos, o recurso a este tipo de intervenção terapêutica deve ser ponderado caso a caso.
A tomada de decisão deve ser compartilhada entre a família (e o doente, quando aplicável) e o médico. A imunoterapia com leite deve ser realizada por especialistas experientes, em condições adequadas e reservada a centros diferenciados de Imunoalergologia. O protocolo escolhido deve ser capaz de ser adaptado ao doente em específico. O pilar para o sucesso da imunoterapia com leite assenta na otimização da relação médico-doente/família, com equipa médica com disponibilidade permanente e capacidade de resposta rápida, e doente e cuidadores bem informados e motivados para a adesão ao tratamento.















