Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Nascer e Crescer
versão impressa ISSN 0872-0754
Nascer e Crescer v.20 n.2 Porto jun. 2011
Hematoma subdural em Pediatria Diagnosticar e tratar precocemente
Marisa Carvalho1, Ema Leal1, Margarida Santos1, José Ramos1, Luís Távora2, Deolinda Barata1
1 Unidade de Cuidados Intensivos Pediátricos
2 Serviço de Neurocirurgia, H Dona Estefânia, CH Lisboa Central
RESUMO
Introdução: O hematoma subdural agudo não traumático é uma entidade rara em Pediatria. A presença de sintomas neurológicos de instalação aguda associada a anticoagulação obriga à exclusão desta entidade.
Caso clínico: Apresentamos o caso de uma criança, do sexo masculino, de sete anos de idade, com prótese mitral mecânica, medicada com varfarina, que recorreu ao serviço de urgência por cefaleias intensas e progressivas, associadas a alteração no estado de consciência e convulsões. A nível laboratorial o INR (International Normalized Ratio) era de 4,2. Foi admitida na Unidade de Cuidados Intensivos Pediátricos (UCIP) em coma com anisocoria. Iniciou ventilação mecânica, medidas anti-edema cerebral e antiepilépticos.O exame de imagem mostrou hematoma subdural agudo à esquerda, com desvio da linha média. Foi submetida a craniotomia descompressiva, 56 horas após o início da sintomatologia, com recuperação clínica e actualmente sem sequelas.
Conclusão: Este caso clínico ilustra a importância da suspeição clínica de hematoma subdural em doentes anticoagulados, bem como a necessidade de optimização das condições cirúrgicas e da utilização das técnicas não invasivas na monitorização do nível de consciência.
Palavras-chave: anticoagulação, cardiopatia congénita, hematoma subdural.
Subdural hematoma in pediatrics – Early diagnosis and treatment
ABSTRACT
Introduction: Non-traumatic acute subdural hematoma is a rare entity in children. In the presence of acute neurological symptoms associated with long termanticoagulation, it is mandatory to rule out this entity.
Case report: We report the case of a seven-year-old boy, with mechanical mitral valve prosthesis under warfarin treatment, presenting severe and progressive headache associated with altered level of consciousness and seizures. Laboratory studies revealed a high value of International Normalized Ratio(INR: 4,2). He was admitted to the Pediatric Intensive Care Unit in a coma with anisocoria. He was mechanically ventilated and started on specific measures to reduce cerebral edemain addition to anticonvulsants. Cranial computerized tomography (CT scan) revealed acute left subdural hematoma, with midline shift. Fifty-six hours after the onset of symptoms, he was submitted to decompressive craniectomy. There was progressive clinical recovery with neurological and imaging improvement and an excellent outcome.
Discussion: This case illustrates the importance of the clinical suspicion of a subdural hematoma in patients treated with anticoagulants, as well as the need of optimizing surgical conditions and the use of non invasive techniques for monitoring the level of consciousness.
Keywords: anticoagulation, congenital heart disease, subdural hematoma.
INTRODUÇÃO
O hematoma subdural resulta da acumulação de sangue entre a membrana dural e o espaço subaracnoideu. Pode estender-se a vários lobos cerebrais, no entanto, encontra-se limitado pela foice do cérebro e pela tenda do cerebelo. Caracteristicamente, toma a forma de um crescente bicôncavo, ao contrário do hematoma epidural que tem uma forma biconvexa.
A hemorragia resulta da lesão de pequenos vasos, artérias ou veias (mais frequentemente estas últimas), com consequente sangramento para o espaço subdural e posterior aumento da pressão intracraniana, podendo resultar em morte por herniação cerebral. Pode ter uma evolução aguda, subaguda ou crónica (com instalação de um a três meses).
A etiologia varia com a idade da criança. Nos recém-nascidos pode ocorrer em 8% dos partos de termo e não é sinónimo de parto traumático. É frequentemente assintomático e desaparece em quatro semanas.(1) Em crianças com menos de dois anos, o traumatismo não acidental é a principal causa, pelo que a hipótese de maus tratos deve ser equacionada.(2) Em crianças mais velhas e adolescentes, o hematoma subdural resulta de acidentes que provocam traumatismos graves. Também pode ocorrer após pequenos traumatismos, sobretudo em crianças com factores de risco(3): alterações hematológicas (trombocitopenia, hemofilia, anticoagulação);retracção cerebral (drenagem ventricular no tratamento da hidrocefalia); atrofia cerebral, higroma subdural ou hematoma crónico (após hematoma agudo ou meningite), quisto aracnóideo, acidúriaglutárica tipo 1, osteogénese imperfeita, entre outras.
Por vezes, a história clínica não fornece informação que sugira uma hemorragia cerebral, o que pode atrasar o diagnóstico. Frequentemente, não há menção a traumatismo.
Na criança as manifestações clínicas principais são: febre, irritabilidade, letargia, convulsões, coma, défices neurológicos, abaulamento da fontanela, aumento do perímetro craniano, hematoma do couro cabeludo, anemia com palidez cutânea ou choque hemorrágico. Em crianças com menos de dois anos de idade deve ter-se um elevado índice de suspeição de maus tratos, aquando da realização do exame objectivo. A bradicardia, hipertensão e as alterações pupilares são sinais tardios pelo que não devemos esperar pelo seu aparecimento para suspeitar de hematoma subdural. A hemorragia retiniana pode estar presente em crianças vítimas de maus tratos, nomeadamente na criança abanada ("shaken baby").(4)
A punção lombar está contra-indicada e a tomografia axial computorizada cranioencefálica (TC-CE) confirma o diagnóstico revelando a típica imagem bicôncava, que pode estar associada a herniação, dependendo do tamanho do hematoma. O tratamento depende do estado clínico e dos achados radiológicos; a vigilância clínica, as medidas antiedema (restrição hídrica, normo/hiperventilação, manitol, cloreto de sódio hipertónico) ou craniotomia descompressiva podem ser as atitudes.(5) Quando a cirurgia está indicada, esta deve ocorrer com a máxima urgência. Se a atitude a tomar privilegiar o tratamento médico, e, se a criança tem um "score" inferior a oito na Escala de Coma de Glasgow - ECG, é obrigatória a monitorização da pressão intracraniana (PIC), além da vigilância clínica e monitorização dos sinais vitais. TC-CE seriadas podem ser necessárias para monitorizar a evolução ou decidir da necessidade de tratamento mais agressivo. O seguimento posterior destas crianças justifica-se pela possibilidade de poder surgir hematoma subdural crónico e/ou higroma subdural.
CASO CLÍNICO
Criança do sexo masculino, sete anos de idade, com defeito completo do septo auriculo-ventricular, sujeito a correcção cirúrgica três anos antes, tendo ficado com insuficiência mitral moderada. Cerca de dois meses antes do internamento, foi colocada prótese mitralmecânica. Medicada habitualmente com enalapril (5 mg, duas vezes/dia) e varfarina (5 mg/dia - três dias,alternando com 3,75 mg/dia - três dias) após colocação da prótese referida.
Recorreu a um serviço de urgência hospitalar, 48 horas antes do internamento, com febre (38ºC), otalgia, cefaleias intensas e episódio autolimitado de epistáxis. No exame objectivo, não apresentava alteração dos parâmetros vitais, estava queixosa, sem sinais de irritação meníngea, e com infecção das vias aéreas superiores.
Analiticamente revelava: hemoglobina (Hb) 9,8 g/dl; hematócrito (Hct) 30%; volume globular médio 73 fl; plaquetas 523000/µl; leucócitos 14730/µl com 84,5% de neutrófilos; proteína C reactiva (PCR) 7 mg/dl; tempo de protrombina (TP) 49,4s; INR 4,2; tempo de tromboplastina parcial activado (APTT) 76,4s. A telerradiografia do tórax era normal. Foi programada a redução da dose de varfarina para 2,5 mg/dia (três dias), alternando com 3,75 mg/dia (três dias), terapêutica antibiótica com amoxicilina 90 mg/kg/dia e reavaliação três dias depois ou antes se se verificasse agravamento clínico.
Cerca de 24h depois, é novamente observada por agravamento da intensidade da cefaleia e da prostração. Ao exame objectivo, encontrava-se febril, pouco reactiva, com rigidez da nuca e sem sinais focais. Analiticamente, observava-se: Hb 10,8 g/dl; Hct 29,7%, leucócitos 11770/µl com 84,5% de neutrófilos; plaquetas 495000/µl; PCR10 mg/dl, TP 94,7s; INR 8,25; APTT 73,6s. Iniciou terapêutica antibiótica com gentamicina (5 mg/kg/dia), cefotaxima(200 mg/kg/dia) e vancomicina (60 mg/kg/dia), assim como plasma fresco congelado, vitamina K e concentrado eritrocitário.
Foi transferida para UCIP do Hospital Dona Estefânia (HDE), no período pós-ictal de convulsão tonico-clónica generalizada, controlada com diazepam e fenobarbital, e, ainda, sem recuperação do estado de consciência ("score" de 5 na ECG), pupilas midriáticas, assimétricas, pouco reactivas, com posterior evolução para anisocória marcada (midríaseà esquerda). A fundoscopia era normal; os reflexos osteotendinosos eram difíceis de despertar. Não era visível hematoma no couro cabeludo. A restante observação não apresentava alterações. Por suspeita de hipertensão intracraniana devida a hemorragia secundária a alteração da coagulação, iniciou de imediato ventilação mecânica, medidas anti-edema cerebral e concentrado protrombínico(Octaplex® em dose adequada ao valor de INR) com vista a rápida normalização da coagulação para eventual cirurgia.
Na TC-CE, realizada duas horas após admissão na UCIP, apresentava hematoma subdural agudo à esquerda com desvio da linha média e sinais de encravamento do uncus (Figura 1).
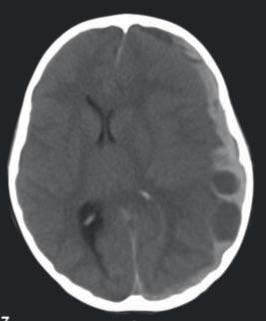
FIGURA 1 - Hematoma subdural agudo, hemisfério esquerdo, com desvio da linha médica, em TC-CE, corte axial
A craniotomia descompressiva ocorreu cerca de 45 minutos após a realização de TC-CE e da reversão da anticoagulação (56 horas após o início da sintomatologia). Realizada drenagem de todo o hematoma, sem visualização do ponto sangrante, com consequente expansão cerebral, constatando-se edema cerebral generalizado. No pós-operatório manteve as medidas anti-edema cerebral e ventilação mecânica durante quatro dias. Clinicamente, houve regressão da anisocoria e melhoria progressiva, apesar de às 48h de pós-operatório ter havido diminuição do nível de consciência. Fez TC-CE (Figura 2) que não apresentava alterações. Às 32h de pós-operatório, reiniciou anticoagulação com enoxaparina subcutânea (1 mg/kg/dose).
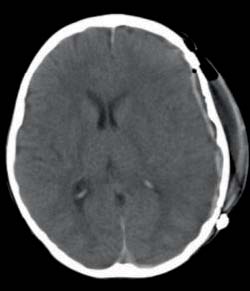
FIGURA 2 - Secção de TC-CE sobreponível à anterior, realizada 24 horas após a cirurgia, mostrando sequelas da intervenção e resolução do hematoma
A monitorização do nível de consciência foi também feita com Bispectral Index™ apresentando valores médios de 40, posteriormente mais elevados à medida que se tornava mais acordada.
Foi transferida, ao sétimo dia pós-operatório, para uma enfermaria de Pediatria, clinicamente bem, apenas com ptose palpebral esquerda da qual veio a recuperar, estando actualmente sem sequelas.
DISCUSSÃO
O caso ilustra:
1) A importância da suspeição clínica em doentes anticoagulados; a mais temível complicação do uso de anticoagulantes é a hemorragia intracraniana, sendo a intensidade da anti-coagulação o maior predictor de hemorragia cerebral. Valores de INR superiores a 3,5 aumentam a sua probabilidade de ocorrência(6), especialmente se associados a outros factores de risco (quedas, hipertensão arterial, mal formação vascular, entre outras). O elevado grau de suspeição, pela clínica altamente sugestiva de hipertensão intracraniana, justificam o início de medidas anti-edema cerebral antes da realização da TC CE.
2) A relevância da rápida optimização das condições cirúrgicas, para não protelar este procedimento quando está indicado; a descontinuação da terapêutica anticoagulante uns dias antes de uma cirurgia electiva é suficiente para normalizar a coagulação, no entanto, uma reversão rápida pode ser necessária em situações de emergência. É frequente o uso de plasma fresco congelado, vitamina K ou factor VII activado, mas a normalização do INR obtém-se mais rapidamente com o uso do complexo protrombínico. O tempo médio para reverter o INR é 30 minutos a uma hora. O complexo protrombínico é constituído por factor II, VII, IX e X.(7) Énecessário ter em conta o potencial risco trombótico que advém da administração destes fármacos.
3) A utilização de técnicas não invasivas de monitorização do nível de consciência; o BispectralIndex™, largamente usado em bloco operatório, avalia os efeitos dos anestésicos sobre a actividade do cérebro mediante análise da frequência de onda do electroencefalograma, ajudando a adequar a dose de anestésico. O seu valor varia de zero a 100, correspondendo zero a ausência de actividade cerebral e 100 a totalmente acordado. Recentemente, tem-se assistido ao seu uso em unidades de cuidados intensivos pediátricos sendo um complemento muito útil, quando disponível.(8,9)
4) A imprevisibilidade da evolução das patologias pediátricas; o hematoma subdural agudo tem uma taxa de mortalidadede 10 a 20%, sendo as sequelas muito frequentes. São factores de mauprognóstico a existência de coma, alterações pupilares, hipertensão intracraniana, alterações significativas na TC e o período até à cirurgia descompressiva. No caso clínico aqui apresentado, o tempo decorrido entre a apresentação dos sintomas e a cirurgia foi demasiado longo o que, ab initio, faria prever um desfecho desfavorável, ou até mesmo fatal, e que não aconteceu.
BIBLIOGRAFIA
1. Whitby EH, Griffiths PD, Rutter S, Smith MF, Sprigg A, Ohadike P, et al. Frequency and natural history of subdural haemorrhages in babies and relation to obstetric factors. Lancet 2004; 363:846-51. [ Links ]
2. Matschke J, Voss J, Obi N, Görndt J, Sperhake JP, Püschel K, et al. Non accidental head injury is the most common cause of subdural bleeding in infants <1 year of age. Pediatrics 2009; 124:1587-94. [ Links ]
3. Mark RP. Intracranial subdural hematoma in children: Epidemiology, anatomy, and pathophysiology. UpToDate 2009. Disponível em: http://www.uptodate.com/contents/intracranial- subdural-hematoma-in-children-epidemiology-anatomy-and-pathophysiology [ Links ]
4. Proctor MR. Intracranial subdural hematomain children: Clinical features, evaluation, and management. UpToDate 2009. Disponível em: http://www.uptodate.com/contents/intracranial-subdural-hematoma-in-children- clinicalfeaturesvaluationandmanagement?source=search_result&selectedTitle=1~150 [ Links ]
5. Rangel-Castilla L, Gopinath S, Robertson CS. Management of Intracranial Hypertension. Neurol Clin 2008; 26:521-41. [ Links ]
6. Flaherty ML, Tao H, Haverbusch M, Sekar P, Kleindorfer D, Kissela B, et al. Warfarin use leads to larger intracerebral hematomas. Neurology 2008; 71:1084-9. [ Links ]
7. Levy JH, Tanaka KA, Dietrich W. Perioperative hemostatic management of patients treated with vitamin K antagonists. Anesthesiology 2008; 109:918-26. [ Links ]
8. Sadhasivam S, Ganesh A, Robinson A, Kaye R, Watcha MF. Validation of the Bispectral Index Monitor for Measuring the Depth of Sedation in Children. Anesth Analg 2006; 102:383-8. [ Links ]
9. Hsia SH, Wu CT, Wang HS, Yan DC, Chen SC. The use of bispectral index to monitor unconscious children. Pediatr Neurol 2004; 31:20-3. [ Links ]
Marisa Carvalho














