Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Nascer e Crescer
versão impressa ISSN 0872-0754
Nascer e Crescer vol.23 no.2 Porto jun. 2014
ARTIGO DE REVISÃO / REVIEW ARTICLES
Alergia às proteínas do leite de vaca com manifestações gastrointestinais
Cow’s milk protein allergy with gastrointestinal manifestations
Sofia FerreiraI; Mariana PintoI; Patrícia CarvalhoII; Jean-Pierre GonçalvesIII; Rosa LimaIV; Fernando PereiraIV
IS. Pediatria e Neonatologia, CH Entre Douro e Vouga, 4520-211 Santa Maria da Feira, Portugal. E-mail: sofiafe@gmail.com; marianabrpinto@gmail.com
IIS. Pediatria, ULS Alto Minho, 4901-858 Viana do Castelo, Portugal. E-mail: patricia.pediatria@gmail.com
IIIS. Pediatria, H Braga, 4710-243 Braga, Portugal. E-mail: pierre_3.14r@hotmail.com
IVS. Gastrenterologia Pediátrica, Dep. Criança e do Adolescente, CH Porto, 4099-001 Porto, Portugal. E-mail: rosalima@netcabo.pt; facpereira@sapo.pt
RESUMO
A alergia às proteínas do leite de vaca (APLV) constituiu a alergia alimentar mais frequente em crianças com idade inferior a três anos, podendo as suas manifestações gastrointestinais ocorrer em qualquer idade.
Na suspeita clínica de APLV baseada na anamnese e exame físico, deve instituir-se dieta de eliminação durante um período variável consoante o quadro clínico, seguida de uma prova de provocação oral (PPO) que irá confirmar ou excluir o diagnóstico. Exames complementares como testes cutâneos e IgEs séricas específicas poderão ser necessários.
O tratamento baseia-se na dieta de eliminação e pressupõe aconselhamento nutricional e vigilância do crescimento. Habitualmente repete-se a PPO após três a 12 meses de dieta de eliminação, verificando-se aquisição de tolerância em mais de 80% das crianças aos três anos de idade.
O objetivo deste artigo é fazer uma breve revisão e atualização sobre as manifestações gastrointestinais da APLV em idade pediátrica, apresentando uma proposta de abordagem fundamentada em recomendações internacionais recentes.
Palavras-chave: Abordagem, alergia às proteínas do leite de vaca, crianças, manifestações gastrointestinais, prova de provocação oral.
ABSTRACT
Cow’s milk protein allergy (CMPA) is the leading cause of food allergy in children under three years of age, although its gastrointestinal manifestations may occur in all age groups.
In the suspicion of CMPA based on the anamnesis and physical examination, an elimination diet should be initiated for a variable length of time according to the clinical picture, followed by an oral food challenge (OFC) confirming or excluding the diagnosis. Complementary exams such as skin prick tests and specific IgE may be necessary.
Treatment is based on an elimination diet and demands nutritional counselling and growth monitoring. Usually an OFC is repeated after three to 12 months of elimination diet. Tolerance is achieved at three years of age in more than 80% of the children.
The aim of this work is to make a brief review and update on CMPA in pediatric age, proposing a management approach based on recent international recommendations.
Key-words: Children, cow’s milk protein allergy, gastrointestinal manifestations, management.
INTRODUÇÃO
A alergia alimentar constituiu um importante problema de saúde pública atingindo indivíduos de qualquer faixa etária. É defi da como um efeito adverso resultante de uma resposta imunológica específi que ocorre de forma reprodutível após exposição a um dado alimento e que é distinto de outras respostas adversas como a intolerância alimentar (não imune mediada e que envolve reações enzimáticas) ou reações mediadas por toxinas.(1,2)
A alergia às proteínas do leite de vaca (APLV) constitui a alergia alimentar mais frequente em crianças com idade inferior a três anos, todavia a APLV com manifestações gastrointestinais (GI) ocorre em qualquer idade.(3,4,5)
O diagnóstico correto, baseado em provas de tolerância oral, é extremamente importante, evitando situações de sobre ou subdiagnóstico e tratamento desadequado.(4-5)
A prevalência baseada apenas na perceção dos pais é muito superior à real, atingindo até 17% das crianças em idade pré-escolar.(3,6) Já a prevalência baseada em provas de provocação oral (PPO) varia entre 2 a 3% dos lactentes, 0,4 a 0,5% em lactentes sob leite materno exclusivo (LME) e menos de 1% em crianças com idade igual ou superior a seis anos.(3-5)
O leite de vaca (LV) engloba 20 proteínas potencialmente sensibilizantes, incluindo α-lactoalbumina, α-lactoglobulina, albumina de soro bovina, imunoglobulinas bovinas e caseínas.(4) Verifi homologia estrutural e consequentemente reatividade cruzada, com alergénios do leite de vários mamíferos (ex.: leite de ovelha, cabra, burra).(4) A APLV pode resultar de mecanismos Imunoglobulina E (IgE)-mediados, não IgE-mediados ou mistos. As formas mistas podem envolver mecanismos IgE-mediados ou celulares, habitualmente têm um início retardado ou crónico e incluem a gastroenteropatia e a esofagite eosinofílicas.(2,4)
A distinção destes mecanismos tem importância clínica, uma vez que a APLV IgE-mediada associa-se a maior risco de reações graves, maior risco de múltiplas alergias alimentares e sensibilização a alergénios inalantes no futuro.(4,5)
O objetivo deste artigo é fazer uma revisão e atualização sobre as manifestações gastrointestinais da APLV em idade pediátrica, apresentando uma proposta de abordagem fundamentada em recomendações internacionais recentes, enfatizando a importância de um diagnóstico correto, sempre que possível apoiado em provas de provocação oral.
Manifestações clínicas
O espectro é variável, não existindo sintomas ou sinais patognomónicos de APLV.
Frequentemente, as manifestações nas formas IgE-mediadas ocorrem nas primeiras tomas de leite, após uma fase de sensibilização, nas formas não IgE-mediadas o intervalo entre a ingestão e as manifestações clínicas é muito variável no tempo.(4,5) A APLV pode desenvolver-se em lactentes sob LME, sob aleitamento artificial (LA) ou quando as PLV são introduzidas durante a diversificação alimentar.(4,5) Os sinais e sintomas podem envolver diferentes sistemas – Quadro 1, estando os sintomas GI presentes em 32 a 60% dos casos, sintomas cutâneos em 5-90%, e anafilaxia em 0,8 a 9%.(7,8)

Manifestações gastrointestinais (GI)
As manifestações GI resultam de inflamação e/ou dismotilidade. Podem ser reações IgE-mediadas, não IgE-mediadas ou mistas.(5,10)
As reações imediatas (IgE-mediadas) incluem a síndrome de alergia oral e a alergia GI imediata. A síndrome de alergia oral caracteriza-se por edema e prurido dos lábios, palato, língua ou orofaringe e sensação de aperto na garganta.(4,10) A alergia GI imediata decorre com vómitos (mais frequente), diarreia, dor abdominal, isoladamente ou como parte de uma reação anafilática ou envolvendo outros sistemas.(4,10)
Estão definidos quatro tipos de fenótipos / síndromes GI não IgE-mediados e mistos associados às proteína da dieta, incluindo as PLV, com diferentes graus de gravidade, descritos no Quadro 2.(10,11) A enterocolite induzida por proteínas alimentares (food protein-induced enterocolitis syndrome FPIES) é rara, representando o final do espectro de gravidade destes fenótipos. Ocorre habitualmente em pequenos lactentes nos primeiros contactos com as PLV, caracterizando-se por vómitos incoercíveis, palidez, hipotonia e por vezes diarreia grave com sangue, uma a três horas após a ingestão.(4,10,11) Pode progredir para desidratação grave com choque em 15-20% dos casos.
Não há registo de casos em lactentes sob LM exclusivo.(4,10) Uma evolução mais insidiosa, ocorre na enteropatia induzida pelas PLV. O quadro clínico inclui diarreia sanguinolenta, má evolução ponderal, vómitos, por vezes hipoproteinemia, anemia, e mais tarde acidose metabólica. Podem estar presentes sinais clínicos de intolerância secundária à lactose, como eritema perianal. Em lactentes sob LM a apresentação clínica é mais benigna, com diarreia com raios de sangue, raramente anemia ligeira e hipoproteinemia, habitualmente sem afetar o crescimento e o estado geral.(4,10,11) A proctocolite induzida pela PLV é manifestação mais frequente e mais benigna deste grupo de síndromes. Tipicamente ocorre nas primeiras semanas a meses de vida, em lactentes saudáveis, com boa evolução ponderal e sem outros sintomas além de presença de sangue e muco em pequena/ moderada quantidade nas fezes, sem alteração do padrão das dejeções ou com diarreia ligeira. Ocasionalmente pode cursar com anemia ligeira. Embora mais raro e com quadro mais ligeiro também atinge lactentes sob LM.(2,4,10,11) A gastroenteropatia eosinofílica pode apresentar-se em qualquer idade, incluindo nos primeiros meses de vida, altura em que pode mimetizar o quadro de estenose hipertrófica do piloro com obstrução e vómitos pós-prandiais em jacto. A perda ou má evolução ponderal é frequente. Dependendo do envolvimento inflamatório os doentes podem apresentar dor abdominal, vómitos, diarreia, hemorragia digestiva baixa, anemia ferropénica e enteropatia perdedora de proteínas.(2)
Além destes, a esofagite eosinofílica pode ser uma manifestação de APLV, IgE-mediada ou não IgE-mediada.(4,5) Clinicamente carateriza-se por impacto alimentar, disfagia, recusa/ dificuldade alimentar, dor abdominal intermitente, vómitos, quadro clínico semelhante ao refluxo gastro-esofágico (RGE) sem resposta ao tratamento anti-refluxo. Embora o papel causal dos alergénios alimentares não esteja bem definido, em alguns casos, a evicção de alimentos específicos, nomeadamente o LV, pode resultar em normalização da mucosa e melhoria clínica.(12) As crianças com APLV podem ainda apresentar-se com sintomas/quadros clínicos que podem ser enquadrados no largo espectro da APLV, tais como: vómitos, diarreia crónica, síndrome de mal-absorção, má evolução estaturo-ponderal, RGE, cólicas e obstipação.(10)
Os casos de RGE grave referenciados para consultas de especialidade cursam com APLV numa percentagem que pode atingir os 56% em lactentes. Nestes casos, o LV induz disritmia gástrica e atraso de esvaziamento gástrico, agravando o RGE.(4,13,14)
A relação entre obstipação e APLV é controversa, no entanto, segundo alguns autores, algumas crianças com obstipação crónica refratária à terapêutica anti-obstipante podem apresentar APLV, verificando-se resposta clínica à dieta de eliminação. Habitualmente ocorre tolerância após um período de 12 meses.(4,11,15)
Relativamente às cólicas do lactente a relação é também controversa e apenas uma minoria dos casos de cólicas graves poderá estar associado a APLV, melhorando com dieta de eliminação.(4,16)
DIAGNÓSTICO
O diagnóstico baseia-se na história clínica, exame físico, dieta de eliminação e prova de provocação oral (PPO).(4,5,17,18) Deve colocar-se a suspeita de APLV na presença de um ou mais sintomas sugestivos (particularmente se persistentes e a envolver vários sistemas) e/ou ausência de resposta adequada ao tratamento prévio para eczema atópico, DRGE ou sintomas GI crónicos.(17,18)
A. Avaliação clínica
Na avaliação clínica deve dar-se especial atenção a algumas questões chave, entre as quais: a história pessoal e familiar de atopia; forma de apresentação idade de início, rapidez de instalação após introdução de PLV, duração, gravidade e frequência das manifestações, reprodutibilidade das manifestações; história alimentar LM vs LA, se LM rever dieta materna, idade da diversificação alimentar, etc.. É fundamental avaliar o crescimento, sinais de má nutrição e sinais/sintomas sugestivos de comorbilidades alérgicas.(4,5,17,18)
No caso de suspeita de APLV deve ser realizada dieta de eliminação, em que as PLV são totalmente eliminadas da dieta e é avaliada a resposta clínica. A duração da dieta para fins diagnósticos deve ser tão curta quanto possível, mas suficiente para avaliar a resposta clínica.
B. Prova de provocação oral
Após um período de dieta de eliminação, a PPO continua a ser o método gold-standard, e é atualmente o único método definitivo para confirmar ou excluir a alergia alimentar (valor preditivo positivo e negativo superior a 95%).(4,5,17-21) Consiste na administração de doses graduais de LV, começando com um volume inferior ao que poderá produzir sintomas, aumentado até atingir o equivalente a um volume adequado à idade. Idealmente deve ser realizada em meio hospitalar, sendo mandatório em situações de reações imediatas, reações graves ou imprevisíveis. Deve estar disponível material de reanimação.(19,20)
Existem três tipos de prova: PPO aberta, PPO com ocultação simples e PPO com dupla ocultação contra placebo. Na PPO aberta, todos os intervenientes sabem que vai ser testado leite de vaca (LV). Não deve ser usada na presença de sintomas subjetivos e/ou questionáveis, no entanto é a mais utilizada na prática clínica pela maior facilidade de execução. Na PPO com ocultação simples, utiliza-se LV e um placebo, conhecendo os profissionais de saúde qual está a ser testado, mas
os pais e a criança não sabem. Já na PPO com dupla ocultação contra placebo os profissionais de saúde, os pais e a criança não sabem se é o placebo ou o LV que está a ser testado. Embora seja a mais fiável, a sua aplicação é difícil e onerosa, sendo maioritariamente utilizada em protocolos científicos.
Em lactentes até aos 12 meses é administrado leite para lactentes ou de transição (com PLV), em crianças com idade superior a 12 meses LV ultrapasteurizado.(5)
Considera-se uma PPO positiva quando a introdução do LV reproduz os sintomas, confirmando-se o diagnóstico de APLV, e a dieta de eliminação deverá ser mantida até aos nove a 12 meses de vida ou durante seis meses, conforme o que ocorrer primeiro.(4,5,17,18) A prova é repetida posteriormente.
Se a PPO for negativa, ou seja, na ausência de sintomas durante toda a prova, mantém-se um volume diário de LV de cerca de 200 ml.(5) Na alta, devem ser dadas indicações aos pais sobre a possibilidade da ocorrência de reações tardias, devendo ser efetuada reavaliação clínica de acordo com a situação clínica.(19) Caso a criança se mantenha assintomática nas 48h a duas semanas seguintes, a dieta habitual com PLV pode ser retomada.
C. Exames auxiliares de diagnóstico
Além da PPO, nenhum dos testes diagnósticos, atualmente disponíveis, comprova ou excluí a APLV.(4,5,17,18,21)
As IgE específicas e os testes cutâneos / skin prick tests (SPT) indicam sensibilização, mas não diagnosticam APLV isoladamente, principalmente no que diz respeito às manifestações GI, em que a maioria das crianças tem IgE específicas negativas (<0,35 IU/L) e SPT negativos (diâmetro <3 mm).(1,4,5,10) Têm sim, valor prognóstico, verificando-se que níveis superiores de IgE específicas e maior diâmetro nos SPT indicam maior probabilidade de reações graves e persistência da alergia. O doseamento seriado de IgE específicas pode ter valor preditivo na aquisição de tolerância.(1,4,5,19) A utilização de monocomponentes moleculares de alergénios poderá ter valor prognóstico, com determinados epítopos candidatos a biomarcadores de tolerância.(22)
D. Exames endoscópicos, histológicos e outros
Exames endoscópicos, histológicos e outros podem estar indicados em crianças com manifestações GI persistentes, moderadas a graves, má evolução estaturo-ponderal ou anemia ferropénica, sem resposta à dieta de eliminação ou que coloquem dúvidas de diagnóstico.(5,21) Algumas indicações estão especificadas na Quadro 3.
As alterações macroscópicas e microscópicas, como atrofia da mucosa ou infiltrados eosinofílicos, não são específicas nem sensíveis para o diagnóstico de APLV.(5,10,21)
ABORDAGEM
De um modo geral, a abordagem da criança com suspeita de APLV está resumida no algoritmo da Figura 1. Em reações graves e/ou imediatas deve optar-se por dieta de eliminação e doseamento de IgE específicas ou SPT, realizando-se PPO diagnóstica se estes forem negativos e/ou persistirem dúvidas no diagnóstico.(1,4,5,21)
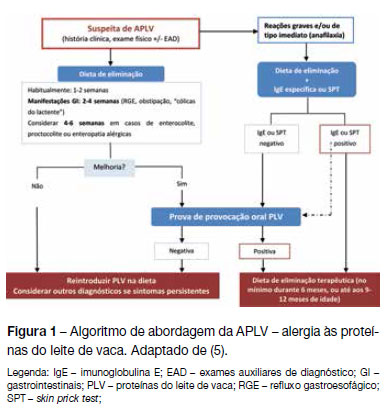
Em reações tardias ou quando a relação com as PLV não é tão evidente, está indicada a realização de PPO diagnóstica após um período de dieta de eliminação.(1,4,5,21) As IgE específicas ou SPT podem também utilizar-se nestes casos, tendo em atenção que serão negativos na maioria.
Na ausência de melhoria com a dieta de eliminação ou se a PPO for negativa, devem considerar-se outros diagnósticos, dependendo do quadro clínico: alterações anatómicas, doença celíaca ou outras enteropatias, insuficiência pancreática (como na fibrose quística), reações adversas alimentares não imunológicas (como mal absorção da frutose, intolerância secundária à lactose), reações alérgicas a outros alergénios, infeções, neoplasias e doenças metabólicas.(18)
A abordagem específica das manifestações GI está descrita na Quadro 4.

Dieta de eliminação diagnóstica
A duração da dieta de eliminação diagnóstica depende da gravidade e das características dos sintomas, de um modo geral opta-se por uma a duas semanas. Nas manifestações GI deve ser mantida por duas a quatro semanas. Nos casos de enterocolite, proctocolite ou enteropatia pode ser necessário um período de quatro a seis semanas.(5,21 Na presença de reações graves como anafilaxia ou FPIES a dieta deve manter-se por um mínimo de 12 a 18 meses antes da realização de PPO.(5,10)
Em lactentes sob aleitamento artificial devem ser utilizados fórmulas extensamente hidrolisadas (FeH) como 1ª linha. Se já foi iniciada a diversificação alimentar, eliminam-se todos os produtos com PLV.(5,23) Em casos de intolerância/recusa ou ausência de resposta à FeH deve considerar-se uma fórmula de aminoácidos (FAA).(5,17,18) As fórmulas de soja podem ser uma opção em lactentes com idade superior a seis meses, uma vez assegurada a sua tolerância e na impossibilidade de utilizar uma FeH (motivos económicos, dietas vegan ou recusa do lactente).(5,23) Em situações de enteropatia com diarreia pode coexistir intolerância secundária à lactose, devendo considerar-se uma FeH sem lactose.(5)
Nos lactentes sob aleitamento materno, este deve manter-se. Se já iniciou diversificação alimentar, eliminar os produtos com PLV. A mãe deve fazer dieta de eliminação de produtos lácteos e ovo, com aconselhamento nutricional.(5,17,18,23) Pode considerar-se FAA nos primeiros dias, por um máximo de duas semanas, em casos mais graves. Na ausência de resposta devem eliminar-se outros alergénios da dieta materna e considerar a utilização de uma FAA.(5,23)
Em crianças com mais de 12 meses, está recomendada uma dieta nutricionalmente equilibrada, sem LV ou alimentos que contenham PLV, devendo incluir uma FeH.(5) Em casos selecionados, as fórmulas de soja podem ser uma opção (recusa da FeH ou motivos económicos). Ponderar eliminar o ovo da dieta. O aconselhamento nutricional está recomendado, e se a criança não ingerir fórmula suficiente deve suplementar-se com cálcio.
A eliminação bem sucedida de alimentos requer a leitura cuidadosa dos rótulos. Deve ser explicado que em rótulos de alimentos processados termos como caseína, soro lácteo entre outros, significam a presença de PLV. Os alimentos que contêm lactose geralmente são seguros para o consumo, desde que não contenham outros componentes do LV.(5,23)
Em casos de esofagite eosinofílica ou suspeita de múltiplas alergias alimentares, considerar alimentação exclusiva com FAA até melhoria dos sintomas antes da PPO.(4,5,12)
Dieta de eliminação terapêutica e reavaliação com prova de provocação oral
Se a PPO diagnóstica foi positiva, a dieta de eliminação deve manter-se. No caso de dieta de eliminação materna, suplementar com cálcio (1000mg/dia) e providenciar aconselhamento nutricional.(5,23) De acordo com a gravidade e o mecanismo subjacente deve repetir-se a PPO após pelo menos três meses (ex.: IgE específica negativa e sintomas ligeiros) e até 12 meses (ex.: IgE específica positiva e sintomas graves).(4,5) Em manifestações mais graves (ex.: FPIES, anafilaxia) não se realiza PPO diagnóstica, mantendo-se a dieta de eliminação por 12 a 18 meses antes de testar a aquisição de tolerância com PPO.(5,10)
Caso a PPO seja positiva, mantém-se a dieta de eliminação. Os intervalos para as PPO subsequentes não são consensuais e dependem igualmente do quadro clínico. No entanto, de um modo geral repetem-se a cada seis a 12 meses.(4,5)
Em situações de ingestão acidental de produtos lácteos, com ou sem a ocorrência de sintomas credíveis, deve considerar-se antecipar ou adiar a PPO, respetivamente.
Não está recomendado o uso de leites de outros mamíferos (cabra, ovelha, burra), uma vez que existe reatividade cruzada com o LV e estes leites são nutricionalmente inadequados.(4,23)
Quanto à nova fórmula de arroz disponível, embora pareça eficaz e segura em crianças com APLV(24), os autores consideram que são necessários mais estudos que avaliem a sua segu- rança nutricional.25)
PREVENÇÃO
Na prevenção da APLV está recomendado o aleitamento materno exclusivo até aos seis meses. A diversificação alimentar deve ocorrer preferencialmente cerca dos seis meses de idade, nunca antes dos quatro meses. Não está recomendado por rotina dieta materna restritiva durante a gestação ou lactação ou adiar a introdução de outros alimentos potencialmente alergénicos.(2,26,27)
Atualmente não existe evidência científica suficiente para a suplementação com prebióticos ou probióticos, na prevenção da alergia alimentar.(28,29)
Alguns estudos mostram benefício na utilização de leites hidrolisados (parcial ou extensamente), para a prevenção de patologia alérgica em crianças de alto risco, mas não existe evidência suficiente para a sua recomendação por rotina.(30,31)
PROGNÓSTICO
O prognóstico é bom: aos três anos de idade verifica-se aquisição de tolerância em mais de 80% das crianças.(7,18,26,32) Os fatores de risco para persistência incluem a história familiar de atopia, a presença de manifestações graves, SPT com maior diâmetro, níveis mais elevados de IgE específicas e dose mais baixa para positividade na PPO.(4,18)
CONCLUSÃO
A alergia às proteínas do leite de vaca, nomeadamente com manifestações GI, pode ocorrer em qualquer idade, mas atinge principalmente crianças nos primeiros anos de vida. Apresenta um amplo espectro de gravidade, mas sempre com um grande impacto na vida das crianças e da família, tendo em conta a base láctea da alimentação pediátrica da sociedade atual. A abordagem das manifestações GI, na sua maioria não IgE-
-mediadas ou mistas, reveste-se de algumas particularidades. O diagnóstico correto, baseado em provas de provocação oral, é extremamente importante, evitando situações de sobre ou sub- diagnóstico e tratamento desadequado.
LISTA DE SIGLAS/ABREVIATURAS
APLV – alergia às proteínas do leite de vaca DRGE – doença de refluxo gastro-esofágico FAA – fórmula de aminoácidos
FeH – fórmula extensamente hidrolisada
FPIES – food protein-induced enterocolitis syndrome
GI – gastrointestinal (ais) IgE – imunoglobulina E
LA – leite/aleitamento artificial LM – leite/aleitamento materno
LME – leite/aleitamento materno exclusivo LV – leite de vaca
PLV – proteínas do leite de vaca PPO – prova de provocação oral RGE – refluxo gastro-esofágico SPT – skin prick tests
REFERÊNCIAS BIBLIOGRÁFICAS
1. Boyce JA, Assaad A, Burks AW, Jones SM, Sampson HA, Wood RA, et al. Guidelines for the diagnosis and management of food allergy in the United States: report of the NIAID sponsored expert panel. J Allergy Clin Immunol 2010; 126:S1-58. [ Links ]
2. Sampson HA. Update on food allergy. J Allergy Clin Immunol 2004; 113:805-19. [ Links ]
3. Rona RJ, Keil T, Summers C, David Gislason D, Zuidmeer L, Sodergren E, et al. The prevalence of food allergy: a meta-analysis. J Allergy Clin Immunol 2007; 120:638-46. [ Links ]
4. Fiocchi A, Brozek J, Schünemann H, Bahna SL, von Berg A, Beyer K, et al. World Allergy Organization (WAO) diagnosis and rationale for action against cows milk allergy (DRACMA) guidelines. WAO J 2010; 3:57-161. [ Links ]
5. Koletzko S, Niggemann B, Arato A, Dias JA, Heuschkel R, Husby S, et al. Diagnostic approach and management of cow´s milk protein allergy in infants and children: ESPGHAN GI Committee practical guidelines. J Pediatr Gastroenterol Nutr 2012; 55:221-9. [ Links ]
6. Roehr CC, Edenharter G, Reimann S, Ehlers I, Worm M, Zuberbier T, et al. Food allergy and non-allergic food hypersensitivity in children and adolescents. Clin Exp Allergy 2004; 34:1534-41. [ Links ]
7. Høst A. Frequency of cows milk allergy in childhood. Ann Allergy Asthma Immunol 2002; 89:33-7. [ Links ]
8. Kvenshagen B, Halvorsen R, Jacobsen M. Adverse reactions to milk in infants. Acta Paediatr 2008; 97:196-200. [ Links ]
9. National Institute for Health and Clinical Excellence. Diagnosis and assessment of food allergy in children and young people in primary care and community settings. London; 2011. Disponível em: http://www.nice.org.uk/CG116 [ Links ]
10. Caubet JC, Nowak-Wegrzyn A. Current understanding of the immune mechanisms of food protein-induced enterocolitis syndrome. Expert Rev Clin Immunol 2011; 7:317-27. [ Links ]
11. Troncone R, Discepolo V. Colon in Food Allergy. J Pediatr Gastroenterol Nutr 2009; 48:S89-91. [ Links ]
12. Liacouras CA, Furuta GT, Hirano I, Atkins D, Attwood SE, Bonis PA, et al. Eosinophilic esophagitis: updated consensus recommendations for children and adults. J Allergy Clin Immunol 2011; 128:3-20. [ Links ]
13. Farahmand F, Najafi M, Ataee P, Modarresi V, Shahraki T, Rezaei N. Cows Milk Allergy among Children with Gastroesophageal Reflux Disease. Gut Liver 2011; 5:298-301. [ Links ]
14. Salvatore S, Vandenplas Y. Gastroesophageal reflux and cow milk allergy: is there a link? Pediatrics 2002; 110:972-84. [ Links ]
15. Carroccio A, Iacono G. Review article: chronic constipation and food hypersensitivity – an intriguing relationship. Aliment Pharmacol Ther 2006; 24:1295-304. [ Links ]
16. Lucassen PL, Assendelft WJ. Systematic review of treatments for infant colic. Pediatrics 2001; 108:1047-8. [ Links ]
17. Caffarelli C, Baldi F, Bendandi B, Calzone L, Marani M, Pasquinelli P; et al. Cow´s milk protein allergy in children: a practical guide. Ital J Pediatr 2010; 36:5. [ Links ]
18. Vandenplas Y, Koletzko S, Isolauri E, Hill D, Oranje AP, Brueton M, et al. Guidelines for the diagnosis and management of cow´s milk protein allergy in infants. Arch Dis Child 2007; 92:902-8. [ Links ]
19. Nowak-Wegrzyn A, Assaad AH, Bahna SL, Bock SA, Sicherer SH, Teuber SS; Adverse Reactions to Food Committee of American Academy of Allergy, Asthma & Immunology. Work Group report: Oral food challenge testing. J Allergy Clin Immunol 2009; 123:S365-83. [ Links ]
20. Yum HY, Yang HJ, Kim KW, Song TW, Kim WK, Kim JH, et al. Oral food challenges in children. Korean J Pediatr 2011; 54:6-10. [ Links ]
21. Canani RB, Costanzo MD, Troncone R. The optimal diagnostic workup for children with suspected food allergy. Nutrition 2011; 27:983-7. [ Links ]
22. Sastre J. Molecular diagnosis in allergy. Clin Exp Allergy 2010; 40:1442-60. [ Links ]
23. Dupont C, Chouraqui JP, de Boissieu D, Bocquet A, Bresson JL, Briend A, et al. Dietary treatment of cows milk protein allergy in childhood: a commentary by the Committee on Nutrition of the French Society of Paediatrics. Br J Nutr 2012; 107:325-38. [ Links ]
24. Reche M, Pascual C, Fiandor A, Polanco I, Rivero-Urgell M, Chifre R, et al.The effect of a partially hydrolysed formula based on rice protein in the treatment of infants with cows milk protein allergy. Pediatr Allergy Immunol 2010; 21:577-85. [ Links ]
25. Savino F, Castagno E, Monti G, Serraino P, Peltran A, Oggero R, et al. Z-score of weight for age of infants with atopic dermatitis and cows milk allergy fed with a rice-hydrolysate formula during the first two years of life. Acta Paediatr Suppl 2005; 94:115-9. [ Links ]
26. Caldeira F, Cunha J, Ferreira MG. Alergia a proteínas de leite de vaca: um desafio diagnóstico. Acta Med Port 2011; 24: 505-10. [ Links ]
27. Kramer MS, Kakuma R. Maternal dietary antigen avoidance during pregnancy or lactation, or both, for preventing or treating atopic disease in the child. The Cochrane Database Syst Rev 2012; 9:CD000133. [ Links ]
28. Vanderhoof JA. Probiotics in allergy managment. J Pediatric Gastroenterol Nutr 2008; 47:S38-40. [ Links ]
29. Osborn DA, Sinn JK. Prebiotics in infants for prevention of allergic disease and food hypersensitivity. Cochrane Database Syst Rev 2007; 17:CD006474. [ Links ]
30. Osborn DA, Sinn J. Formulas containing hydrolysed protein for prevention of allergy and food intolerance in infants. Cochrane Database Syst Rev 2006; 18:CD003664. [ Links ]
31. Lowe AJ, Dharmage SC, Allen KJ, Tang ML, Hill DJ. The role of partially hydrolysed formula for the prevention of allergic disease: evidence and gaps. Expert Rev Clin Immunol 2013; 9:31-41. [ Links ]
32. Høst A, Halken S, Jacobsen HP, Christensen AE, Herskind AM, Plesner K. Clinical course of cows milk protein allergy/ intolerance and atopic diseases in childhood. Pediatr Allergy Immunol 2002;13:23-8. [ Links ]
Endereço para correspondência
Sofia Ferreira
Serviço de Pediatria/Neonatologia
Centro Hospitalar Entre Douro e Vouga
Rua Dr. Cândido Pinho
4520-211 Santa Maria da Feira, Portugal
E-mail: sofiafe@gmail.com
Recebido a 10.07.2013 | Aceite a 11.04.2014














