Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Nascer e Crescer
versão impressa ISSN 0872-0754
Nascer e Crescer vol.24 no.4 Porto dez. 2015
ARTIGO ORIGINAL / ORIGINAL ARTICLE
Transplantação renal pediátrica: experiência de um centro
Pediatric Renal Transplantation: A Single Center Experience
João NascimentoI; Liliana RochaI; Maria Sameiro FariaI; Paula MatosI; Teresa CostaI; Maria Lassalete MartinsIII; Manuela AlmeidaIII; Leonídio DiasIII; Conceição MotaII,III; A Castro HenriquesIII
I S. de Pediatria Médica do Centro Materno Infantil do Norte, Centro Hospitalar do Porto. 4099-001 Porto, Portugal nascimentojoao10744@gmail.com;
II S. de Nefrologia Pediátrica do Centro Materno Infantil do Norte, Centro Hospitalar do Porto. 4099-001 Porto, Portugal. liliana.oli.rocha@gmail.com; mariasameirofaria@gmail.com; piresmatos@hotmail.com; teresa.v.c.tavares@gmail.com; conceicaocmota@gmail.com;
III Unidade de Transplantação do Serviço de Nefrologia do Centro Hospitalar do Porto. 4099-001 Porto, Portugal. lasalet@gmail.com; manuela.almeida10@gmail.com; nefrologia@chporto.min-saude.pt; conceicaocmota@gmail.com;
ABSTRACT
Introduction: End-stage renal disease in children is associated with numerous comorbidities and with age-specific mortality rates approximately 30 times higher than in healthy children.
The first kidney transplantation in children was performed successfully in 1954. Surgical advances and new immunosuppressive medications have greatly improved patients and grafts survival in the last years.
Aim: Report Centro Hospitalar do Porto experience in pediatric renal transplantation in the last 30 years.
Methods: Epidemiological and clinical data of all patients younger than 18 years, transplanted between January 1984 and August 2013, were collected from our database. In order to analyze the transplantation outcome in our center we compare graft survival between decades (1984-89 / 1990-99 / 2000-09 / 2010-13). We also compare graft survival between two age groups of patients (0-10 years ; 11-17 years) at the time of surgery.
Results: One hundred thirty-nine patients (58.3% male) underwent 147 renal transplants (6.8% live donors). Congenital anomalies of the kidney and urinary tract (56.5%) and glomerulonephritis (18.4%) were the major causes of renal disease.
Uncensored graft survivals rates at 5, 10, 15 and 20 years were 84.7%, 71.1%, 60.0% and 51.0%, while patient survivals were 97.9%, 95.9%, 94.7% and 94.7% respectively.Graft survival improved over time and the difference between the decades was statistically significant (p=0.004). Despite the better survival in the group of patients older than 11 years, grafts survival difference between the two age groups was not statistically significant (p=0.697).
Conclusion: The results of our hospital are comparable to other international centers. Significant improvement in survival was observed over the time. It seems that an accurate follow-up of our patients helps to minimize the negative impact of adolescence on graft survival rates.
Keywords: pediatric renal transplantation; end-stage renal disease; graft survival
RESUMO
Introdução: A insuficiência renal crónica terminal está associada a numerosas comorbilidades e a um aumento do risco de mortalidade cerca de 30 vezes superior à população pediátrica geral.
O primeiro transplante renal bem sucedido em crianças foi realizado em 1954. Os progressos cirúrgicos e as novas terapêuticas imunossupressoras aumentaram a sobrevida dos doentes e do enxerto renal nos últimos anos.
Objectivos: Avaliação da experiência em transplantação renal em idade pediátrica do Centro Hospitalar do Porto nos últimos 30 anos.
Métodos: Estudo retrospetivo dos dados epidemiológicos e clínicos dos doentes pediátricos transplantados entre Janeiro de 1984 e Agosto 2013. Foi feita a análise da evolução temporal da atividade de transplantação através da comparação da sobrevida do enxerto por décadas de transplantação (1984-89 / 1990-99 / 2000-09 / 2010-13). Foi também comparada a sobrevida do enxerto em dois grupos etários (0-10 anos ; 11-17 anos) à data da transplantação.
Resultados: Cento e trinta e nove doentes (58.3% - sexo masculino) foram submetidos a 147 transplantes renais (6.8% de dador vivo). As anomalias congénitas do rim e trato urinário (56.5%) e as glomerulonefrites (18.4%) foram as causas principais de insuficiência renal.
A sobrevida do enxerto não censurada aos 5, 10, 15 e 20 anos foi 84.7%, 71.1%, 60.0% e 51.0% e a sobrevida do doente aos 5, 10, 15 e 20 anos foi 97.9%, 95.9%, 94.7% e 94.7%, respetivamente. A sobrevida do enxerto aumentou ao longo do tempo e a diferença entre as décadas foi estatisticamente significativa (p=0.004). Apesar da melhor sobrevida no grupo com idade superior a 11 anos, a diferença da sobrevida do enxerto entre os grupos etários não foi estatisticamente significativa (p=0.697).
Conclusão: Os resultados do Centro Hospitalar do Porto são comparáveis aos dos grandes centros de transplantação renal pediátrica. Observou-se uma melhoria dos resultados ao longo dos anos na nossa Unidade. A existência de um rigoroso processo de acompanhamento poderá ter ajudado a minimizar o impacto negativo da adolescência na sobrevida do enxerto.
Palavras-chave: transplantação renal pediátrica; insuficência renal crónica terminal; sobrevida do enxerto
INTRODUÇÃO
A doença renal crónica associa-se a diversas morbilidades que influenciam negativamente a qualidade de vida dos doentes e representam um risco acrescido de mortalidade. A evolução da doença é influenciada por inúmeros fatores, desde a idade do doente no momento do diagnóstico e gravidade da lesão renal inicial, a duração da doença renal até ao diagnóstico ou instituição de medidas terapêuticas, a suscetibilidade genética, o ónus que os períodos de intenso metabolismo como a primeira infância e puberdade acarretam para os rins, a existência e persistência concomitante de hipertensão e proteinúria, a perpetuação de uropatias obstrutivas, a ausência de controlo de doenças sistémicas e a ocorrência de infeções, quadros de desidratação ou exposição a fármacos nefrotóxicos.1
A perda cada vez maior de nefrónios funcionantes e a progressiva incapacidade regenerativa ou de substituição dos nefrónios restantes conduz à inevitável insuficiência renal e à necessidade, por vezes precoce, de terapêuticas de substituição renal.1,2 O transplante renal (TR), realizado pela primeira vez em crianças em 1954, representa atualmente a terapêutica de substituição renal de eleição, conferindo aos doentes com insuficiência renal crónica terminal (IRCT) em idade pediátrica benefícios consideráveis que incluem uma melhoria do crescimento e uma melhor qualidade de vida.2-5 O TR é também a modalidade de tratamento com melhor relação custo/efetividade.4,5
De facto, a melhor escolha de dadores e a preparação que antecede o procedimento cirúrgico, o aumento da experiência cirúrgica, a utilização de fármacos imunossupressores mais potentes e o melhor conhecimento da sua farmacocinética conduziu a uma alteração do paradigma da transplantação renal nos últimos anos, sendo hoje a criança o recetor que apresenta melhor sobrevida do enxerto renal.2,5-7
No entanto, o doente pediátrico possui ainda particularidades que aumentam o desafio do TR. Se por um lado a imaturidade do sistema imunológico pode ser vista como uma vantagem em relação à população adulta, existe um risco natural maior na população pediátrica de exposição a infeções que podem comprometer a viabilidade do aloenxerto e acarretar um risco maior de evolução para doença linfoproliferativa.2,3,8-10
Outro aspeto frequentemente descrito é a maior possibilidade de complicações hemodinâmicas e vasculares na fase de re-vascularização, sobretudo quando os dadores são crianças.8-10 Em termos urológicos, é necessário efetuar frequentemente correções cirúrgicas previamente ao transplante, nomeadamente cirurgias antirefluxo vesicoureteral, cistoplastias de aumento da bexiga e/ou nefrectomia de rim(s) nativo(s). A necessidade de cateterismos vesicais intermitentes em doentes com bexiga neurogénica e a maior suscetibilidade de infeções urinárias pós-transplante é uma complicação relevante nestes doentes.9,10 Por outro lado, a adolescência revela-se um desafio difícil para o nefrologista pediátrico que lida com a necessidade de monitorizar o cumprimento de esquemas terapêuticos exigentes.1,3,10 Por fim, embora a disponibilidade dos órgãos seja em última análise a maior limitação à transplantação, é importante referir que em Portugal o tempo de espera pré-TR para as crianças é menor quando comparado ao do adulto.
De acordo com o registo português de transplantação renal, o Centro Hospitalar do Porto é o centro nacional com maior número de transplantes renais efetuados na população pediátrica até à data, seguido do Centro Hospitalar de Lisboa Norte e do Centro Hospitalar Universitário de Coimbra.11,12
Pretendemos por isso, avaliar a experiência em transplantação renal em idade pediátrica do Centro Hospitalar do Porto (CHP) nos últimos 30 anos e comparar a sobrevida do doente e do enxerto renal do CHP com outros centros de referência internacional.
MÉTODOS
Estudo retrospetivo dos dados epidemiológicos (número total de TR, sexo, idade do recetor e dador na altura do transplante) e clínicos (etiologia da IRCT, tipo de dador, tempo de isquemia fria, tempo de internamento após TR, tempo de seguimento após TR, tipo de imunossupressão utilizada, causas para a falência do enxerto renal) dos doentes pediátricos (< 18 anos à data do transplante) transplantados entre Janeiro de 1984 e Agosto 2013. O método de Kaplan-Meier estimou a sobrevida do enxerto renal não censurada e a sobrevida do doente. O Log rank test foi utilizado para comparar a sobrevida do enxerto por décadas de transplantação (1984-89 / 1990-99 / 2000-09 / 2010-13) e entre dois grupos de doentes (<11 anos e >= 11anos à data do TR).
RESULTADOS
A atividade de transplantação renal no CHP iniciou-se em Janeiro de 1984, tendo até Agosto de 2013, sido efetuados 147 TR em 139 doentes (58.3% do sexo masculino). Em 10 (6.8%) casos o enxerto foi de dador vivo. No período de 1984-89, nas décadas de 1990-99, 2000-09 e no período 2010-13 foram realizados respetivamente, 13, 52, 53 e 29 transplantes.
No que diz respeito à etiologia da doença renal crónica nesta população, as anomalias congénitas do rim e do trato urinário (CAKUT) representaram 56.5% dos casos seguido das glomerulopatias com 18,4% dos casos. No grupo das CAKUT a distribuição foi a seguinte: pielonefrite/nefrite intersticial devido a refluxo vesicoureteral sem obstrução 56.1%; pielonefrite/ nefrite intersticial devido a uropatia obstrutiva - 10,6%; bexiga neurogénea - 12,1% e hipoplasia/displasia renal congénita com ou sem malformação urinária - 21,2%.
No grupo das glomerupatias, a glomerulosclerose segmentar focal foi a mais frequente com 13 (48,1%) casos.
As doenças renais quísticas, doenças metabólicas tubulointersticiais, síndrome hemolítico-urémico e outras etiologias representaram 8.8%, 6,8%, 3,3% e 2,2% respetivamente. Em 3.6% dos doentes a etiologia foi desconhecida.
A técnica cirúrgica utilizada em todos os TR consistiu numa abordagem extraperitoneal realizando-se um incisão oblíqua no hipogastro, à exceção dos doentes mais pequenos nos quais a opção foi a incisão de Rutherford-Morrison. O tempo médio de isquemia fria foi de 1053±612.5 minutos.
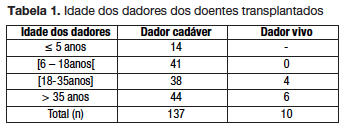
A idade mediana dos doentes no momento da cirurgia foi de 13.1 anos, oscilando entre 2.8 e 17.9 anos e a idade mediana dos dadores foi de 17.0 anos, oscilando entre 1.5 e 58 anos (tabela 1).
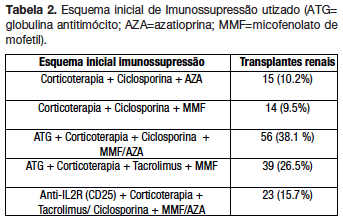
A terapêutica imunossupressora utilizada inicialmente, no período 1984-89, consistiu em prednisolona, azatioprina (AZA) e ciclosporina, tendo sido adicionado ao protocolo em 1990 indução com a globulina anti-timócito (ATG) ou com anticorpos monoclonais anti-IL2R (CD25). Em 2002, o micofenolato de mofetil (MMF) veio substituir a azatioprina e a partir do ano de 2004 o protocolo passou a incluir o tacrolimus como alternativa à ciclosporina. O esquema inicial de imunossupressão realizado pelos doentes está representado na tabela 2.
O tempo médio de internamento foi de 17 dias e o seguimento após TR foi de 9.7 anos.
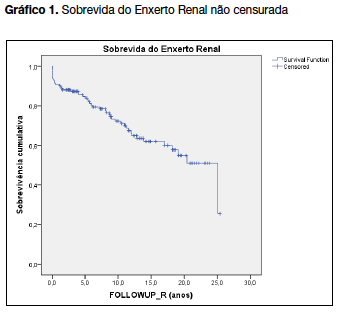
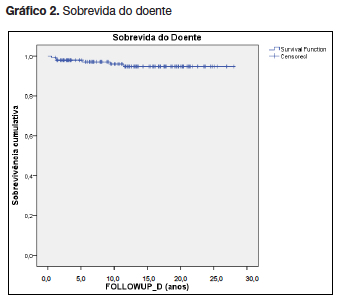
A sobrevida do enxerto renal não censurada aos 5, 10, 15 e 20 anos foi respetivamente 84.7%, 71.1%, 60.0% e 51% (gráfico 1). A sobrevida do doente aos 5, 10, 15 e 20 anos foi respetivamente 97.9%, 95.9%, 94.7% e 94.7% (gráfico 2).
A sobrevida do enxerto não foi significativamente diferente nas crianças (<11 anos) e nos adolescentes (>= 11 anos) à data do TR (p=0.697) (gráfico 3).
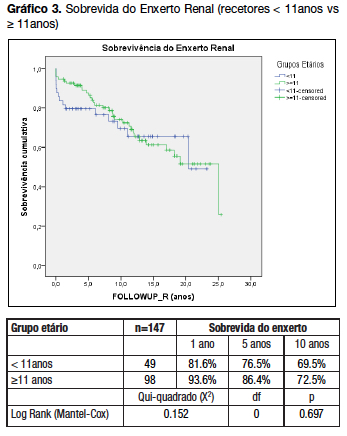
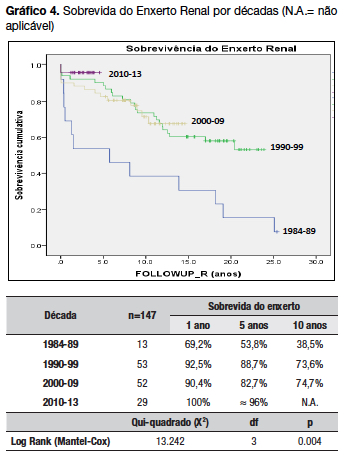
A diferença de sobrevida do enxerto renal por décadas foi estatisticamente significativa (p=0.004) (gráfico 4) com uma melhoria da sobrevivência ao longo dos anos.
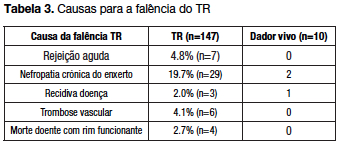
Verificou-se falência do enxerto renal em 33.3% dos casos da amostra (tabela 3).
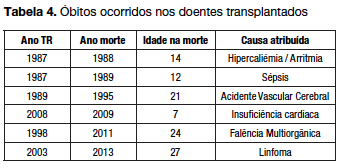
Ocorreram seis óbitos durante o período analisado, tendo metade dos casos ocorrido em idade pediátrica (tabela 4).
DISCUSSÃO
A incidência e a prevalência da insuficiência renal crónica terminal em terapêutica substitutiva renal são elevadas em Portugal e, de acordo com o registo europeu de 2012 da sociedade europeia de Nefrologia Pediátrica, estima-se que correspondam a 10.2:1.000000 (0-14anos) e 53.8:1.000000 (0-14 anos) respetivamente.13 Os números portugueses estão claramente acima da média europeia, cuja incidência estimada em 2012, era de 3.9:1.000000 (0-14anos) e a preval ência de 32.6:1.000000 (0-14 anos).13 De facto, de acordo com o recente estudo de Chesnaye N et al, Portugal ocupa um lugar de destaque e apresenta uma epidemiologia pr óxima da descrita nos pa íses nórdicos e Reino Unido.14
A etiologia da doença renal crónica varia com a idade e nas crianças difere da mais comumente associada aos adultos, onde a diabetes mellitus e a hipertensão ocupam um lugar de destaque.2
De acordo com o registo norte-americano (NAPRTCS – North American Pediatric Renal Trials and Collaborative Studies) as etiologias mais frequentes foram a agenesia/hipoplasia/displasia renal que representaram 15.8%, tendo a uropatia obstrutiva e a glomeruloesclerose focal segmentar representado 15.3% e 11.7%, respetivamente. Por último a nefropatia de refluxo representou a quarta etiologia mais frequente com uma prevalência de 5.2%.15
Na nossa série, as anomalias congénitas do trato urinário e as glomerulonefrites foram também as etiologias mais frequentes que motivaram a necessidade de TR.
O transplante renal de dador vivo apresenta os melhores resultados em termos de sobrevivência, representando 33% dos transplantes realizados nos Estados Unidos. Os pais representam 3/4 dos dadores vivos e 2/3 dos recetores correspondem a crianças caucasianas do sexo masculino. O grupo dos 13-17 anos representa a maioria dos recetores (39%), tendo-se assistido a um aumento do n úmero de dadores vivos n ão familiarmente relacio nados nas últimas décadas, correspondendo de acordo com os dados do NAPRTCS a um incremento de 3 dadores por ano durante o per íodo de 1987-1995 para 16 por ano presentemente.15 Por outro lado, nos Estados Unidos em 2005 uma nova pol ítica de alocação intitulada Share-35 alterou o paradigma da transplanta ção renal ao favorecer a transplantação proveniente de um dador adulto cadáver com menos de 35 anos para as crian ças, sendo estas apenas ultrapassadas por adultos recetores sem qualquer incompatibilidade antig énica, situações de transplante multi-orgão e adultos recetores altamente sensibilizados.15,16
Esta política permitiu reduzir o tempo de espera para as crianças e aumentar a sobrevida do enxerto. Contudo verificou-se também uma mudança de atitude com detrimento do transplante de dador vivo em relação ao dador cadáver. De facto os dados do OPTN (Organ Procurement and Transplant Network database) que avaliaram 18461 transplantes renais do programa Share-35 evidenciaram que a sobrevida do enxerto é maior quanto mais cedo o transplante é realizado (< 12 anos). Este aspeto poderá ser mais importante para a sobrevida do enxerto e a política Share teve sem dúvida o benefício de permitir diminuir as disparidades raciais existentes no tempo para a transplantação.16
Tradicionalmente o transplante de dador pediátrico cadáver com idade inferior a 5 anos e menos de 10Kg não estava recomendado, tendo em conta os riscos de trombose do enxerto e dificuldades técnicas do procedimento. Contudo a grande procura de órgãos para transplante tornou necessária a aceitação de potenciais doadores pediátricos cadáveres a fim de aumentar a oferta.16,17 A técnica de transplantação renal em bloco (2 rins de dador pediátrico cadáver) é referida na literatura em recetores pediátricos e adultos.17,18, Apesar de controversa, apresenta resultados satisfatórios, devendo ser utilizada em casos selecionados onde a urgência do transplante se impõe ao maior risco de complicações desses enxertos.
Em Portugal, de acordo com o artigo 10 do capítulo III da lei nº22/2007, são considerados potenciais dadores post mortem todos os cidadãos nacionais, os apátridas e estrangeiros residentes em Portugal que não tenham manifestado junto do Ministério da Saúde a sua qualidade de não dadores. No caso dos menores ou incapazes, é considerada válida a vontade expressa dos respetivos cuidadores legais.19
Este facto, veio acarretar que o pool de dadores cadáver é maior em número e poderá explicar que na nossa série o transplante de dador cadáver tenha persistido como a modalidade mais frequentemente realizada.
Outro aspeto a ter em conta é que apesar dos recetores pediátricos representarem uma pequena porção do pool de recetores, a lei portuguesa nº 66/2007 (2ª série) baseada num sistema de pontuação para selecção do par dador-recetor, concede uma maior prioridade às crianças e adolescentes com IRCT.20
Podemos afirmar que este panorama beneficia os centros pediátricos de transplante em termos de orgãos disponiveis, mas estamos cientes que esforços deverão ser feitos com o objetivo de aumentar o transplante de dador vivo.
Os eventos cardiovasculares foram responsáveis por metade das mortes ocorridas na amostra, o que está de acordo com o impacto da doença cardiovascular descrito noutras séries de doentes.2,15
No que diz respeito às doenças linfoproliferativas, de acordo com o estudo de Cleper R et al de 2012, os doentes com melhor sobrevida foram aqueles que desenvolveram uma doença linfo-proliferativa pós transplante de células B e cuja serologia para o EBV era negativa antes do transplante.21 Estes doentes desenvolveram um linfoma mais precocemente após o transplante (mediana 1.9 anos vs 6.3 anos), mas esse facto permitiu uma maior facilidade de diagnóstico.
Na tabela 2, o doente do sexo feminino que desenvolveu uma doença linfoproliferativa de células T com localização retroperitoneal diagnosticada 9 anos após o transplante era uma doente com serologia pré-transplante EBV positiva.
Verificou-se falência do enxerto renal em 30.0% dos TR de dador vivo e em 33.6% dos TR de dador cadáver. O reduzido número de transplantes de dador vivo não permite estabelecer comparações.
A nefropatia crónica do enxerto correspondeu à maior causa de falência do TR, o que está de acordo com dados descritos na literatura.15
Na amostra apresentada, verificou-se um aumento da sobrevida ao longo das décadas estatisticamente significativo. A existência de protocolos de imunossupressão bem definidos e a abordagem multidisciplinar com um apoio precoce do Serviço de Cuidados Intensivos são aspetos fulcrais que explicam a necessidade de acompanhar os doentes com IRCT em centros de referência. Um outro aspeto relevante é que a sobrevida do enxerto renal foi maior no grupo dos doentes transplantados depois dos 11 anos de idade, apesar da diferença não ter sido estatisticamente significativa.
Diversos estudos mostram que a pior sobrevida do enxerto renal é nos adolescentes atribuindo como razão principal para este facto a dificuldade que este grupo coloca no cumprimento terapêutico.1,15,22 Um processo de monitorização cuidadoso durante a adolescência assegura um acompanhamento eficaz podendo ser um fator decisivo presente no nosso hospital que poderá ajudar a explicar as curvas de sobrevida obtidas. Os resultados do TR no CHP são por isso encorajadores e comparáveis a outros centros de referência, tendo-se verificado uma melhoria da sobrevida ao longo dos anos.
REFERÊNCIAS BIBLIOGRÁFICAS
1. Massengill SF, Ferris M. Chronic kidney disease in children and adolescents. Pediatr Rev 2014; 35(1):16-29. [ Links ]
2. Dharnidharka VR, Fiorina P, Harmon WE. Kidney transplantation in children. N Engl J Med 2014; 371 (6):549-58. [ Links ]
3. Horslen S, Barr ML, Christensen LL, Ettenger R, Magee JC. Pediatric transplantation in the United States, 1996-2005. Am J Transplant 2007; 7:1339-58. [ Links ]
4. Schurman S, McEnery P. Factors influencing short-term and long-term pediatric renal transplantation survival. J Pediatr 1997; 130:455-6. [ Links ]
5. Roussey-Kesler G, Decramer S. Résultats de la transplantation rénale pédiatrique en France. Néphrologie & Thérapeutique 2011; 7:611-7. [ Links ]
6. Cochat P, Offner G. European best practices guidelines for renal transplantation (Part 2): Pediatrics (specific problems). Nephrol Dial Transplant 2002; 17:55-8. [ Links ]
7. Solez K, Colvin RB, Racusen LC et al. Banff 07 classification of renal allograft pathology: updates and future directions. Am J Transplant 2008; 8:753-60. [ Links ]
8. Branco F, Almeida F, Cavadas V, et al. Pediatric kidney transplantation: a single center experience with 134 procedures. Transplantation Proceedings 2013; 45:1057-9. [ Links ]
9. Gjertson DW, Cecka JM. Determinants of long-term survival of pediatric kidney grafts reported to the United Network for Organ Sharing kidney transplant registry. Pediatr Transplant 2001; 5:5-15. [ Links ]
10. Dharnidharka VR, Agodoa LY, Abbott KC. Effects of urinary tract infection on outcomes after renal transplantation in children. Clin J Am Soc Nephrol 2007; 2:100-6. [ Links ]
11. Macário F. Registo Português de transplantação renal 1980- 2014 – Gabinete de Registo da Sociedade Portuguesa de Nefrologia. Acessível em: http://www.spnefro.pt. [ Links ]
12. Afonso C, Mota C, Almeida M, Castro I. Registo Português de IRC Pediátrica em Tratamento de Substituição Renal (TSFR) 2013. Acessível em: www.spp.pt. [ Links ]
13. Registry of the European Society for Paediatric Nephrology and the European Renal Association and European Dialysis and Transplantation Association - ESPN/ERA-EDTA Annual report for 2012. Acessível em: http://www.espn-reg.org/index.jsp?p=pua [ Links ]
14. Chesnaye N, Bonthuis M, Schaefer F, et al. Demographics of paediatric renal replacement therapy in Europe: a report of the ESPN/ERA-EDTA registry. Pediatr Nephrol 2014; 29 (12): 2403-10. [ Links ]
15. Smith JM, Martz K, Blydt-Hansen TD. Pediatric kidney transplant practice patterns and outcome benchmarks, 1987-2010: a report of the North American Pediatric Renal Trials and Collaborative Studies. Pediatr Transplant 2013; 17 (2):149-57. [ Links ]
16. Moudgil A, Dharnidharka VR, Lamb KE, Meier-Kriesche HU. Best allograft survival from Share-35 kidney donors occurs in middle-aged adults and young children – na analysis of OPTN data. Transplantation 2013; 95:319-25. [ Links ]
17. Gallinat A, Sotiropoulos GC, Witzke O, et al. Kidney grafts from donors <= 5yr of age: single kidney transplantation for pediatric recipients or en bloc transplantation for adults? Pediatr Transplant 2013; 17:179-84. [ Links ]
18. Sharma A, Fisher RA, Cotterell AH, King AL, Maluf DG, Posner MP. En bloc kidney transplantation from pediatric donors: comparable outcomes with living donor kidney transplantation. Transplantation 2011; 92:564-9. [ Links ]
19. Artigo 10 do Capítulo III da Lei 22/2007. Acessível em: página 4149 do Diário da República 1ª série – Nº 124 – 29 de Junho de 2007. [ Links ]
20. Lei 66/2007 (2ª série). Acessível em: Diário da República 2ª aérie – Nº 66 – 3 de Abril de 2007. [ Links ]
21. Cleper R, Bem Shalom E, Landau D, et al. Post-transplantation lymphoproliferative disorder in pediatric kidney-transplant recipients – a national study. Pediatr Transplantation 2012; 16: 619-26. [ Links ]
22. Bell LE, Bartosh SM, Davis CL, et al. Adolescent transition to adult care in solid organ transplantation: a consensus conference report. Am J Transplant 2008; 8:2230-427 [ Links ]
Endereço para correspondência E-mail: nascimentojoao10744@gmail.com Recebido a 12.06.2015 | Aceite a 09.09.2015
João Miguel Nascimento:
Centro Hospitalar do Porto Serviço de Pediatria Médica do Centro Materno Infantil do Norte,
Largo Prof. Abel Salazar,
4099-001 Porto














