Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Medicina Interna
versão impressa ISSN 0872-671X
Medicina Interna vol.24 no.2 Lisboa jun. 2017
ARTIGOS DE REVISÃO / REVIEW ARTICLES
Vírus Zika: Emergência de um Velho Conhecido
Zika Virus: Emergence of an Old Known
Pedro Brogueira, Ana Cláudia Miranda
Serviço de Infecciologia e Medicina Tropical - Hospital de Egas Moniz - Centro Hospitalar de Lisboa Ocidental, E.P.E., Lisboa, Portugal
Resumo:
O vírus Zika foi descoberto há setenta anos, no Uganda, sendo a primeira infecção em humanos reportada em 1952, na Nigéria. O vírus foi sendo responsável por casos de infecção esporádicos em África e na Ásia. Em 2007 acontece a primeira epidemia por este vírus, numa ilha do Pacífico, que atingiu cerca de três quartos da população e onde se verificou um curso benigno e autolimitado da infecção. Seis anos mais tarde ocorre uma epidemia sem precedentes na Polinésia Francesa, entre 2013 e 2014, onde é descrita pela primeira vez a síndroma de Guillain-Barré como complicação associada à infecção. Nesta altura estima-se que o vírus tenha sido introduzido no Brasil onde, no final de 2015, foi verificada a associação entre microcefalia e a infecção por vírus Zika cuja evidência, bem como de outras malformações fetais, os estudos têm vindo a comprovar.
Actualmente verifica-se transmissão autóctone em mais de setenta países, através da transmissão vectorial por mosquitos do género Aedes. A transmissão da infecção por via sexual foi documentada em vários países com casos importados, contudo, não é conhecido o seu real contributo na actual pandemia devido à dificuldade em se determinar a sua ocorrência nos países onde ocorre transmissão vectorial.
A estratégia na prevenção da infecção e da sua disseminação passa, actualmente, por medidas ambientais de controlo de vectores e de protecção individual.
Palavras-chave:Infecção pelo Vírus Zika; Pandemias; Vírus Zika.
Abstract
Zika virus was first discovered in Uganda seventy years ago and the first human infection was reported in Nigeria in 1952. The virus has been responsible for sporadic infection cases in Africa and Asia. In 2007, for the first time since its discovery, Zika virus was responsible for infecting about three quarters of the population from a pacific island, where a benign and self-limited clinical course was verified. Six years later, an unprecedented epidemic occurred in French Polynesia, between 2013 and 2014. For the first time there were descriptions of Guillain-Barré syndrome as a complication associated with the infection. Zika virus is estimated to have been introduced in Brazil at this time. By the end of 2015, a rising number of cases of microcephaly and other fetal malformations reported in this country seem to be possibly related to the Zika epidemic, a fact with growing evidence.
At the moment, autochthonous transmission is known to occur in more than seventy countries by way of vectorial transmission through Aedes mosquitos. Sexual transmission has been reported in several countries with imported cases. However, its real impact in the current pandemic is not known, as it is difficult to determine the transmission in countries where vectorial transmission occurs.
Current strategies in prevention of the infection and its dissemination include vector control and individual protective measures.
Keywords:Pandemics; Zika Virus; Zika Virus Infection
Epidemiologia
O vírus Zika foi isolado pela primeira vez em 1947, numa floresta do Uganda, a partir de um macaco rhesus (Macaca mulatta) utilizado como sentinela num estudo sobre febre amarela.1 O vírus isolado foi denominado Zika 766 segundo o nome da floresta e o número do macaco. Em 1948, também numa tentativa de isolar o vírus da febre amarela, foi possível identificarna mesma região uma estirpe de vírus Zika a partir de mosquitos Aedes africanus (estirpe E/1).2 Esta estirpe foi inoculada por via subcutânea num macaco rhesus, cujo soro se revelou capaz de neutralizar a estirpe isolada a partir do mosquito e aquela isolada a partir do macaco 766. Estes achados mostram que provavelmente o vírus Zika circulava naquela região de forma endémica através de ciclo silvático entre os mosquitos e os macacos africanos locais.
Estudos de seroprevalência em animais e humanos, realizados nos anos 50, revelaram que o vírus Zika circula de forma endémica em África e em vários países da Ásia, dados confirmados pelo isolamento do vírus em mosquitos e hospedeiros vertebrados nesses países.3 No que respeita ao isolamento do vírus em humanos, o primeiro caso remonta a 1954, na Nigéria.4 Uma análise filogenética do vírus coloca a sua origem em 1920 no Uganda, tendo ocorrido duas introduções em tempos diferentes na África Ocidental, originando duas linhagens africanas distintas.5 A mesma análise filogenética coloca a hipótese do vírus ter migrado para este, da sua origem no Uganda para a Malásia em 1945 e daqui para a Micronésia em 1960, estabelecendo a linhagem asiática.5 Os primeiros casos reportados de infecção em humanos fora de África ocorreram apenas em 1977, em Java, na Indonésia,6 embora o vírus já tivesse sido isolado em mosquitos Aedes aegypti na Malásia,7 em 1969.
Durante décadas a doença por vírus Zika foi negligenciada, considerada uma infecção benigna e autolimitada, responsável por casos esporádicos em África e na Ásia. Em 2007 ocorreu a primeira epidemia associada ao vírus Zika, na ilha Yap8 (Micronésia), inicialmente interpretada como febre Dengue. A epidemia durou cerca de três meses e foram reportados 185 casos suspeitos de infecção por vírus Zika e uma taxa de seropositividade de cerca de 75% da população.9 A origem do surto não foi confirmada. Esta foi a primeira evidência de infecção por vírus Zika fora de África e da Ásia e a primeira epidemia em larga escala. Após este surto, foram reportados casos esporádicos em alguns países do sudeste asiático, nomeadamente na Tailândia, Malásia, Cambodja, Filipinas e Indonésia.10 Entre Outubro de 2013 e Abril de 2014 decorreu um segundo surto numa escala sem precedentes nas ilhas da Polinésia Francesa, afectando todos os arquipélagos, estimando-se mais de 30 000 casos de infecção (11,5% da população).11 Foram descritas pela primeira vez complicações neurológicas graves associadas à infecção como a síndroma de Guillain-Barré. A análise filogenética revelou que o vírus Zika responsável pelo surto da Polinésia Francesa era mais próximo das estirpes isoladas no Sudeste Asiático do que da estirpe da Ilha Yap, sugerindo uma introdução independente.12 Após o surto na Polinésia Francesa, o vírus dispersou-se por outras ilhas do Pacífico onde foram reportados casos em 2014, nomeadamente Nova Caledónia, Ilhas Cook e Ilha da Páscoa e, já em 2015, Ilhas Salomão, Vanuatu, Samoa e Fiji.3
Em Março de 2015 foram documentados os primeiros casos de transmissão autóctone no Brasil, no Estado do Rio Grande do Norte,13 marcando a chegada do vírus ao continente Americano. Na região do nordeste, desde o final de 2014, já vinham sendo descritos casos de doença exantemática aguda.14 A ampla distribuição de mosquitos do género Aedes (Aedes aegypti e Aedes albopictus) permitiu a emergência do vírus Zika no Brasil e a sua rápida dispersão. A análise filogenética do vírus circulante no Brasil13 revelou a sua maior proximidade com um isolado de 2013 da Polinésia Francesa, remetendo para a sua origem nas ilhas do Pacífico. Foram analisadas sequências de vírus circulantes nas Américas que revelaram uma homologia genética de 99% com a estirpe isolada na Polinésia Francesa.15,16 As estirpes de vírus Zika que circulam actualmente na América constituem o grupo do Hemisfério Ocidental,16 dentro da linhagem asiática, o que sugere a existência de um ancestral comum asiático que evoluiu e se distribui geograficamente na Ásia e nas ilhas do Pacífico e, a partir daqui, para o Novo Mundo. Admite-se que a introdução do vírus Zika possa ter ocorrido em 2014 durante o campeonato do mundo de canoagem, evento do qual o Brasil foi anfitrião e no qual participaram selecções de diversas ilhas do Pacífico afectadas na altura por surtos de vírus Zika (Polinésia Francesa, Nova Caledónia, Ilhas Cook e Ilha da Páscoa).17 Em Outubro de 2015 foram identificados casos de transmissão autóctone na Colômbia e, em pouco tempo, por toda a América do Sul e Central.
Em Novembro de 2015, o vírus Zika foi considerado responsável por um surto em Cabo Verde, descrevendo um trajecto migratório à volta do globo e retornando ao seu provável local de origem, África. Especula-se que este surto tenha ocorrido como resultado do fluxo de turistas provenientes de vários países para a ilha, entre os quais o Brasil. O vírus Zika permanece endémico noutros países africanos próximos de Cabo Verde, como é o caso do Senegal.3 Contudo, o comportamento epidémico do vírus sugere tratar-se de um vírus da linhagem asiática.
A evolução do vírus Zika representa uma infecção que durante décadas foi responsável por casos esporádicos e com impacto clínico irrelevante, confinada a uma banda tropical de alguns países de África e do Sudeste Asiático, que em menos de uma década foi responsável por epidemias em larga escala em algumas ilhas do pacífico e cuja emergência no continente americano resultou na sua dispersão por todo o globo (Figura 1). Ainda não foi possível apurar as condições que levaram ao comportamento pandémico do vírus Zika, mas estas serão provavelmente o resultado de factores genéticos do próprio vírus, ambientais e da imunidade das populações afectadas.
Classificação e Estrutura Viral
O vírus Zika é um vírus ARN de cadeia simples e polaridade positiva pertencente à família Flaviviridae.15 A esta família pertencem outros arbovírus (transmissão vectorial) responsáveis por doença no Homem, nomeadamente o vírus da febre amarela, vírus da Dengue, vírus do Nilo Ocidental e vírus da encefalite Japonesa.
O genoma viral codifica uma poliproteína que sofre clivagem para dar origem a três proteínas estruturais (C, PrM/M e E) e sete proteínas não estruturais (NS1, NS2A, NS2B, NS3, NS4A, NS4B e NS5).18
Os estudos filogenéticos permitiram identificar duas linhagens distintas: a linhagem Africana e a linhagem Asiática.15 Em 2007 foi efectuada pela primeira vez a sequenciação completa do seu genoma.19 Estudos genéticos sugerem que a actual estirpe pandémica, da linhagem Asiática, terá sofrido mutações que levaram à sua adaptação recente ao Homem.18
Ciclo de Vida e Transmissão Vectorial
O vírus Zika é um arbovírus (artropod born virus) e, como tal, a via preferencial de transmissão é a vectorial, através da mordedura de artrópodes. O vírus Zika foi isolado pela primeira vez em mosquitos arbóreos Aedes africanus em 1948, na floresta Zika (Uganda).2 Em África, o vírus Zika é mantido na natureza por via de um ciclo silvático entre primatas não humanos (principais reservatórios) e várias espécies de mosquitos que habitam a floresta, sendo os casos de infecção humana esporádicos.20 Contrariamente, os vectores responsáveis pelos surtos ocorridos nas ilhas no Pacífico e pela actual pandemia, após a rápida dispersão do vírus Zika pelas Américas, são mosquitos adaptados a ciclos urbanos do género Aedes, em que o Homem é o principal reservatório.8,13
O mosquito Aedes aegypti, responsável pela transmissão de outro flavivirus, o vírus da febre amarela, adaptou-se ao longo de milhares de anos ao ambiente doméstico para se reproduzir, colocando os ovos em reservatórios de água e alimentando-se de sangue humano, o que por sua vez levou à adaptação de alguns vírus para infectar o Homem.21 Esta adaptação evolutiva conduziu à emergência dos arbovírus em novos ecossistemas por todo o globo, como é agora o caso do vírus Zika, sendo o Aedes aegypti apontado como o principal vector na actual pandemia.22 Outra espécie de mosquito do género Aedes,que demonstrou potencial para transmissão do vírus Zika,é o Aedes albopictus,23,24 extremamente bem adaptado ao Homem e capaz de estabelecer ciclos de transmissão em ambiente urbano ou rural. Amplamente disseminado nomeadamente em climas temperados pode adquirir particular relevância e assumir-se como uma séria ameaça para a saúde pública a nível global.
Transmissão não Vectorial
A possibilidade de transmissão por via sexual foi desde cedo reconhecida, tendo em consideração o potencial epidémico do vírus Zika. O primeiro caso descrito foi o de uma mulher no Colorado (EUA) que adquiriu a infecção por via sexual através do marido, o qual teria sido infectado no Senegal através da picada de mosquitos.25 Este referiu sintomas de prostatite e hematospermia, contudo, o esperma não foi testado para a presença do vírus. A literatura descreve um total de 27 casos prováveis ou confirmados de transmissão sexual de vírus Zika.26 De facto, os estudos descrevem a possibilidade de shedding viral nos fluidos genitais para ambos os sexos apesar de, no caso da mulher, tal ocorrer até no máximo 13 dias após o início dos sintomas, não tendo sido possível isolar o vírus neste caso.27 Relativamente ao homem, existe evidência de persistência viral a longo prazo nas secreções genitais, tendo sido documentada a sua identificação até aos 188 dias após o início dos sintomas.28 Contudo, só foi possível isolar o vírus em cultura, ou seja, conferir a sua viabilidade, depois dos 69 dias após o início dos sintomas.28 A evidência disponível levanta a hipótese do vírus Zika poder estabelecer um reservatório em santuários imunológicos como é o caso do testículo, mantendo a sua capacidade de replicação. Tal poderá ter enorme impacto na capacidade de transmissão deste vírus e na sua expressão epidemiológica. Com base no actual conhecimento, deve colocar-se ênfase na prática de sexo seguro como medida de prevenção da transmissão do vírus Zika em áreas onde se conheça transmissão autóctone. Estas medidas devem também ser reforçadas em viajantes provenientes dessas áreas, sobretudo grávidas ou casais que pretendam engravidar (ver tópico Tratamento e Prevenção), de forma a prevenir a infecção na grávida e consequente transmissão ao feto (ver tópico Manifestações clínicas - microcefalia). Dados epidemiológicos do Rio de Janeiro revelaram uma maior probabilidade de aquisição da infecção por vírus Zika nas mulheres em idade sexual activa face aos homens na mesma faixa etária, não se verificando nos outros grupos etários, o que sugere o contributo da transmissão sexual.29
Para além do soro e do esperma, foi possível isolar o vírus Zika noutros fluidos corporais nomeadamente na saliva, urina ou leite, no entanto, o seu papel na transmissão da infecção ainda não foi documentado.
A capacidade de infecção pós-transfusional foi documentada para outros flavivírus nomeadamente o vírus da Dengue e o vírus do Nilo Ocidental. Também a aquisição da infecção por vírus Zika através de sangue ou outros produtos hemoderivados revelou ser possível com base em estudos baseados na detecção de ácidos nucleicos realizados em dadores de sangue, na Polinésia Francesa, durante o surto de 2013-2014.30 Entre 1505 amostras de dadores, todos assintomáticos na altura da doação, 42 (2,8%) revelaram-se positivas para vírus Zika (PCR).31 Não existem casos documentados de infecção pós-transfusional por vírus Zika.
Manifestações Clínicas
Os primeiros casos descritos de infecção no Homem ocorreram na Nigéria, em 1954, no contexto da investigação de uma epidemia não atribuível ao vírus Zika.4 Em 1956, um voluntário europeu de 34 anos, foi inoculado com a estirpe isolada em 1954 na Nigéria.31 Os sintomas descritos foram febre e cefaleia 82 horas após a infecção, sem evidência de exantema. O vírus foi isolado no sangue durante o período febril. O doente foi exposto mosquitos fêmea Aedes aegypti durante os períodos em que foi possível isolar o vírus, verificando-se incapacidade destes transmitirem a infecção, o que sugere que provavelmente a viremia seria baixa. Os surtos na ilha Yap e Polinésia Francesa, no século XXI, permitiram pela primeira vez avaliar clinicamente uma série considerável de casos. A infecção é assintomática em cerca de 80% dos casos.8
Os sintomas quando ocorrem são autolimitados e a infecção tem geralmente um curso benigno. Não existem casos descritos de complicações hemorrágicas ou choque. O exantema é o sintoma mais frequentemente descrito, tipicamente maculopapular, pruriginoso e com progressão centrífuga, durante 4 a 5 dias.8,10,32 O exantema é habitualmente precedido por febre, geralmente baixa (< 38,5ºC), e fadiga com duração máxima de uma semana.32,33 As artralgias são também uma das manifestações mais frequentes, envolvendo sobretudo as pequenas articulações das mãos e pés, associadas ou não a edema periarticular, com resolução geralmente ao fim de uma semana.32 Outro sintoma típico da infecção por Zika é a conjuntivite bilateral, não purulenta, mais comum nesta infecção comparativamente a outros arbovírus, durando uma a duas semanas.8,32,34 A sintomatologia tipo-Dengue dificulta o diagnóstico diferencial com outros arbovírus, nomeadamente Dengue e chikungunya, que geralmente são responsáveis por epidemias nas mesmas regiões do globo uma vez que partilham os mesmos vectores. O tempo de incubação pode ir de três dias, como verificado no caso experimental,31 até cerca de 10 dias, com base na observação da presença do vírus em amostras de dadores de sangue na Polinésia Francesa em 2013.30 A infecção por vírus Zika foi considerada historicamente como tendo um curso benigno até ao surto em larga escala ocorrido na Polinésia Francesa (2013- 2014) em que, pela primeira vez, se constataram complicações neurológicas graves associadas à infecção, como a síndroma de Guillain-Barré (SGB).35 No Brasil, o vírus é responsável por casos de transmissão autóctone desde pelo menos Março de 2015. Estudos observacionais conduzidos nos estados de Pernambuco e Bahia revelaram que a maioria dos doentes diagnosticados com SGB (51%) apresentou, entre Maio e Agosto de 2015, um quadro clínico associado a exantema, artralgia e febre, documentando-se num deles a presença de vírus Zika no líquido cefalorraquidiano (LCR) por técnica de biologia molecular.36
Microcefalia
Em Outubro de 2015, o estado de Pernambuco verificou um aumento inesperado dos casos de microcefalia em recém-nascidos.36 A incidência crescente de nados-vivos com microcefalia foi verificada em outros estados do Brasil em 2015 e, até à primeira semana de 2016, tinham sido registados 3530 casos de microcefalia em 20 estados, face a uma incidência anual de 163 casos documentada entre 2010 e 2014.37 Estas observações sugeriram uma associação entre os casos de microcefalia e a epidemia de vírus Zika no Brasil.
Desde a identificação dos primeiros casos no Brasil, vários estudos epidemiológicos sugeriram uma forte associação entre a infecção por vírus Zika durante a gravidez e a ocorrência de microcefalia no feto/recém-nascido. Um estudo retrospectivo com base em dados recolhidos na Polinésia Francesa relativos ao surto de 2013-2014 estimou, através de um modelo matemático, que o risco de microcefalia aumenta em 1% se a mãe for infectada durante o primeiro trimestre da gravidez.38 Embora o risco possa parecer baixo quando comparado com o risco de malformações congénitas associado à infecção, durante a gravidez, por CMV, rubéola ou parvovírus B19, o impacto na população pode ser significativo em virtude da elevada incidência da infecção por vírus Zika durante um período de surto, tendo sido documentadas incidências de 66% e de 74% na Polinésia Francesa e na ilha Yap (Micronésia), respectivamente.8,30,38 Um estudo observacional prospectivo, realizado no Brasil, analisou 345 grávidas entre Setembro de 2015 e Maio de 2016. Em 117 nados-vivos de 116 grávidas infectadas por vírus Zika, 49 (42%) revelaram malformações, a maioria do SNC, evidenciadas clínica ou imagiologicamente, no primeiro mês de vida (4/49 registaram microcefalia).39 Nenhum dos recém-nascidos no grupo controlo (grávida sem evidência de infecção) apresentou micro-cefalia.39 Outro estudo analisou retrospectivamente os dados de 1501 nados vivos suspeitos de microcefalia associada ao vírus Zika, desde Novembro de 2015 a Fevereiro de 2016, dos quais 602 foram considerados definitivos ou prováveis.40 Foi possível verificar que nos casos altamente prováveis ou definitivos era maior a probabilidade de haver história de exantema durante a gravidez e, quanto mais cedo este ocorresse, menor o perímetro cefálico ao nascer. Um aspecto importante foi a evidência de lesão neurológica, por alterações neuroimagiológicas, em recém-nascidos com perímetros cefálicos normais. Este achado levanta a hipótese de que, colocar o foco na microcefalia, pode levar a falhas no diagnóstico de recém-nascidos com infecção congénita por vírus Zika.40 Os perímetros cefálicos normais correlacionaram-se com exantemas reportados numa fase mais tardia da gestação.40 Existem na literatura casos bem documentados de transmissão vertical do vírus Zika, comprovada pela identificação por amplificação e sequenciação do vírus a partir de tecido fetal.41,42 Nestes casos foram observadas malformações do sistema nervoso central como microcefalia, lisencefalia, ventriculomegalia, hipoplasia cerebelar e microcalcificações. Numa série de 5 casos foram visualizados antigénios virais nos neurónios e células gliais degeneradas, não se identificando por imunohistoquímica vírus Zika fora do sistema nervoso central.41 A escassa resposta inflamatória no tecido cerebral e o efeito citopático específico distinguem o vírus Zika de outros vírus também responsáveis por infecções congénitas como o herpes simplex e o CMV.41
A evidência mais recente surge na forma de um estudo caso-controlo cujos resultados preliminares apontam para que a actual epidemia de microcefalia seja, de facto, resultado da infecção congénita por vírus Zika.43 Foi verificada a associação entre microcefalia e infecção intra-uterina por vírus Zika, confirmada laboratorialmente por IgM no LCR (não atravessa a barreira placentária), na presença de um grupo controlo seleccionado. Este estudo caso-controlo reforça a evidência epidemiológica, permitindo estabelecer uma relação de causalidade.43 A seroprevalência da infecção por vírus Zika foi estimada para a população em estudo (Recife). A seropositividade foi de 64% nas mães dos controlos, o que indica uma elevada prevalência da infecção nesta região, semelhante à que foi determinada nos surtos de Yap e da Polinésia Francesa.43
De acordo com dados da Organização Mundial de Saúde,44 desde o início da pandemia em 2015, foi documentada transmissão vectorial em 70 países ou territórios. Destes, em 29 foram reportados casos de microcefalia e outras malformações do sistema nervoso central potencialmente associados a infecção pre-natal.44 O Brasil é o país que reporta o maior número de casos.44
Síndroma de Guillain-Barré
Os primeiros casos de SGB associada ao vírus Zika foram observados durante o surto que ocorreu na Polinésia Francesa (2013- 2014). Um estudo caso-controlo realizado nesta altura identificou 42 casos de SGB entre Outubro de 2013 e Março de 2014.35 Admitindo uma taxa de ataque na população de 66%, baseada em estudos serológicos em dadores assintomáticos,30 estimou-se um risco de SGB associada ao Zika de 0,24 em cada 1000 infecções, semelhante ao risco descrito para a infecção por Campylobacter jejuni.35 A maioria dos doentes (88%) referiu sintomas da infecção por vírus Zika que precederam em média 6 dias o início dos sintomas neurológicos. Todos os doentes apresentaram a SGB do tipo neuropatia axonal motora (AMAN), fortemente associada à infecção por C. jejuni cuja patogénese assenta no mimetismo molecular. Curiosamente, neste estudo, menos de 50% das amostras de soro analisadas mostrou resposta auto-imune contra glicolípidos, sugerindo um mecanismo patogénico provavelmente diferente para um novo agente etiológico.35
No Brasil foram também identificados vários casos de SGB desde o início da epidemia em 2015. No total, 21 países já reportaram uma incidência crescente de SGB e/ou confirmação laboratorial de infecção por vírus Zika em doentes com SGB.44
Diagnóstico Laboratorial
O diagnóstico faz-se por meio de testes serológicos ou identificação do vírus por técnicas de biologia molecular (Figura 2 e Figura 3). No primeiro caso, a grande limitação prende-se com a possibilidade de reacções cruzadas com outros vírus da família Flaviviridae, nomeadamente o vírus da Dengue e o vírus da febre amarela. A interpretação dos testes serológicos pode ser complexa em indivíduos que residem ou que tenham permanecido em regiões onde co-circulam outros vírus, situação muito frequente dada a epidemiologia comum destas infecções. O diagnóstico serológico pode ser estabelecido através da detecção de anticorpos da classe IgM específicos para vírus Zika, detectáveis quatro a cinco dias após o início dos sintomas.45
Contudo, devido à possibilidade de reacções cruzadas, um título IgM positivo para vírus Zika deve ser confirmado por um teste de neutralização em placa.45 Em alternativa, a documentação de uma elevação para o quádruplo do título de anticorpos IgM para vírus Zika numa amostra de soro convalescente, colhida com um intervalo de 2 a 3 semanas, na ausência de elevação do título de anticorpos para outros flavivírus, constitui evidência de infecção recente por vírus Zika.46 Em indivíduos com história prévia de infecção ou imunização com outros flavivírus deve equacionar-se a possibilidade do fenómeno do pecado original antigénico, ou seja, a produção de anticorpos específicos para o vírus responsável pela infecção/imunização prévia em detrimento de uma resposta dirigida ao vírus actual, podendo condicionar falsos negativos.32 O gold standard do diagnóstico é a técnica de biologia molecular designada por RT-PCR (reverese transcriptase-protein chain reaction). A técnica consiste na detecção e amplificação do ARN do vírus. A pesquisa no soro é positiva em média cerca de três dias após o início dos sintomas, sendo possível identificar o vírus no soro até um máximo de onze dias.8 É possível detectar o ARN do vírus Zika na urina mesmo quando este já não é detectável no sangue, até 10 a 20 dias após o início dos sintomas. 47 Este achado traduz uma vantagem do diagnóstico por meio da identificação do vírus na urina, sobretudo nos casos se apresentam mais tardiamente na evolução natural da doença e após a fase aguda. A saliva constitui também uma alternativa para a detecção de ARN viral mas, para além do facto da sua colheita ser um método não invasivo, não demonstrou vantagem sobre o soro ou a urina relativamente à duração da detectabilidade do vírus.48
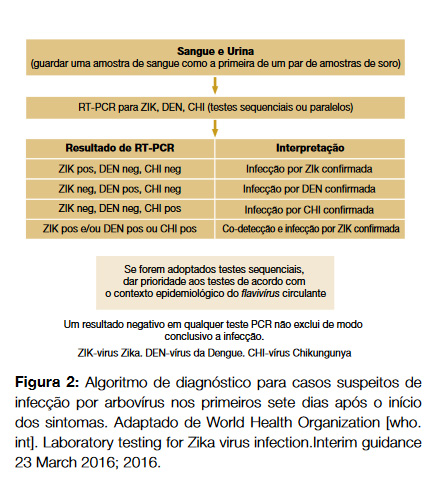
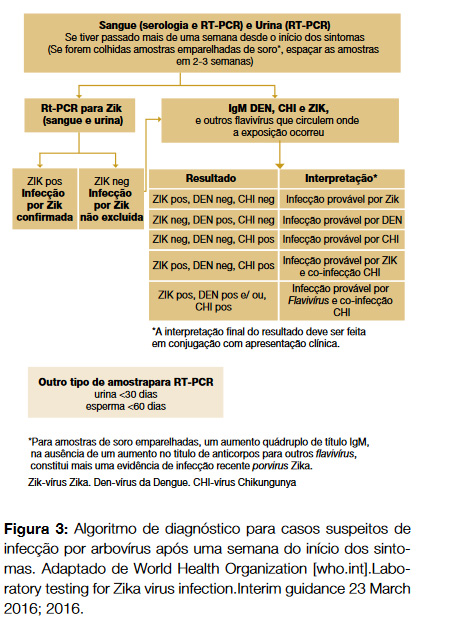
No caso da grávida, com ou sem sintomas, sempre que haja história de possível exposição ao vírus Zika, seja por estadia em regiões onde se conhece transmissão da infecção, ou por contacto sexual com um homem regressado de regiões em risco, esta deve ser testada para a ocorrência de infecção.49 Se sintomática, o diagnóstico laboratorial deve ser efectuado, independentemente do tipo de exposição, através da pesquisa de ARN viral por RT-PCR no soro ou na urina se os sintomas tiveram início há menos de duas semanas ou, através de testes serológicos (anticorpos IgM específicos), se RT-PCR negativa no caso anterior ou se os sintomas tiveram início há mais de 2 semanas.49 Relativamente às grávidas assintomáticas, o método varia consoante o intervalo de tempo decorrido desde a possível exposição. Nas grávidas que se apresentam nas primeiras duas semanas após a possível exposição a vírus Zika, deverá ser efectuada pesquisa de ARN por RT-PCR e, se negativa, pesquisa de anticorpos IgM específicos a realizar dentro de 2 a 12 semanas.49 Se a exposição ocorreu nas 2 a 12 semanas anteriores, procede-se primeiro à pesquisa de anticorpos IgM específicos e, se resultado positivo ou equívoco, procede-se à pesquisa de ARN de vírus Zika por RT-PCR na mesma amostra.49 Um resultado positivo ou equívoco de uma pesquisa de anticorpos IgM específicos deve sempre ser aferido por um teste de neutralização em placa, de modo a permitir a confirmação do diagnóstico. As grávidas cuja exposição tenha ocorrido há mais de 12 semanas, sintomáticas ou assintomáticas, deverão realizar um teste serológico com pesquisa de anticorpos IgM específicos. Neste contexto, e na presença de evidência de malformações fetais, deverá ser efectuada RT-PCR no soro ou urina da grávida.49 Contudo, um resultado negativo após 12 semanas do início dos sintomas não exclui infecção, dado o declínio do título de anticorpos e a baixa probabilidade de viremia, recomendando-se nestes casos um seguimento obstétrico com ecografias fetais a cada 3-4 semanas,49 o mesmo no caso de um resultado positivo independentemente do tempo de exposição. A realização de amniocentese para o diagnóstico de infecção congénita deverá ser considerada e individualizada caso a caso, não se conhecendo a sua sensibilidade e especificidade ou o seu valor preditivo positivo em relação ao desenvolvimento de malformações fetais.49 Os recém-nascidos de mães com provável infecção por vírus Zika devem ser avaliados quanto à presença do ARN viral no soro e urina e, se indicada a sua colheita por outro motivo, no líquido cefalo-raquidiano.49 Neste caso, a serologia IgM para Zika no soro e LCR deverá também ser obtida. A presença de vírus Zika pode também ser determinada por imunohistoquímica no cordão umbilical e placenta, confirmando infecção congénita.
Tratamento e Prevenção
O tratamento da infecção por vírus Zika assenta essencialmente em medidas de suporte, tendo em vista sobretudo a prevenção da desidratação. Não existe tratamento antiviral específico. As medidas farmacológicas resumem-se ao alívio sintomático, incluindo paracetamol e anti-histamínicos para a febre e prurido associado ao exantema.50 O uso de anti-inflamatórios não esteróides deve ser evitado até estar definitivamente excluída infecção por vírus Dengue, de modo a prevenir as complicações hemorrágicas associadas a esta. Tendo em conta a frequente co-circulação de outros arbovírus, o sucesso do tratamento e da prevenção de complicações reside no diagnóstico laboratorial específico. A associação de manifestações neurológicas graves, como a síndrome de Guillain-Barré, obriga à antecipação desde tipo de complicações, nomeadamente através da disponibilização de camas de cuidados intensivos que possam dar a resposta adequada numa situação de epidemia.
Motivado pelo seu potencial de complicações neurológicas graves e sério impacto no desenvolvimento fetal, existe actualmente um esforço a nível global no desenvolvimento de uma vacina eficaz contra o vírus Zika. O sucesso verificado anteriormente na implementação de vacinas contra outros flavivírus, como a vacina contra a febre amarela e a vacina contra a encefalite Japonesa, pressupõe algum optimismo na investigação de uma vacina contra o vírus Zika.50 No entanto, alguns aspectos particulares desta infecção podem levantar alguns obstáculos. A associação com a síndroma de Guillain-Barré exige uma melhor compreensão dos mecanismos imunológicos envolvidos. Neste contexto, a utilização de uma vacina viva atenuada, como é o caso da vacina contra a febre amarela, pode constituir um risco, sobretudo para grávidas e crianças pequenas.18 Outra possível limitação, dada a semelhança do vírus Zika com o vírus da Dengue, consiste no fenómeno da ampliação da infecção dependente de anticorpo, ou seja, no aumento da infectividade do vírus na presença de anticorpos gerados numa infecção primária ou imunização.51
Perante a inexistência de uma vacina ou de tratamento eficaz, o foco deve ser colocado nas medidas preventivas de protecção individual. Os viajantes que pretendam deslocar-se para países com transmissão activa de vírus Zika deverão ser aconselhados a tomar as devidas precauções na prevenção da picada de mosquitos.52,53 Neste contexto, é recomendado o uso de repelente de insectos contendo NN-dietil-meta-toluamida (DEET), seguro de utilizar inclusive na grávida durante o aleitamento. Nos locais de alojamento sem ar condicionado devem utilizar-se redes mosquiteiras, mesmo durante o dia. As grávidas são desaconselhadas a viajar para áreas de risco de transmissão, no entanto, na impossibilidade de adiar a viagem, devem adoptar as medidas gerais de evicção da picada e, para além disso, abstinência sexual ou uso do preservativo até ao final da gravidez.52,53 As mulheres que pretendam engravidar devem adiar o momento da concepção durante pelo menos 8 semanas após o regresso e, no caso do parceiro também se deslocar para área de risco, este período passa a pelo menos 6 meses.52,53 Os indivíduos que viajam para áreas com transmissão activa de vírus Zika devem adoptar medidas de prevenção da transmissão sexual através do uso do preservativo ou abstinência sexual durante oito semanas, no caso da mulher, e durante seis meses, no caso do homem.52,53 Após o regresso e até às duas semanas, os indivíduos que apresentem sintomas deverão ser avaliados clinicamente. As grávidas, mesmo assintomáticas, devem ser avaliadas quanto à ocorrência de infecção por vírus Zika e seguir um plano de seguimento obstétrico adequado.49 Recomenda-se ainda que todos os viajantes que regressem de uma área com transmissão activa para uma onde esteja presente um vector competente na transmissão, como é o caso da Região Autónoma da Madeira (Aedes aegypti), mantenham as medidas de evicção da picada de mosquitos durante três semanas, de modo a prevenir a transmissão para o vector.53
Tendo em conta o seu potencial de transmissão, a infecção pós-transfusional por vírus Zika deve ser prevenida com base na implementação de protocolos, inclusive nas regiões sem evidência de transmissão da infecção, que visem a garantia da segurança dos produtos hemoderivados em situações de epidemia.54
Considerações Finais
O vírus Zika constitui uma nova e séria ameaça de saúde pública a nível global, com importantes consequências nas populações afectadas. A síndroma de Guillain-Barré e as malformações fetais, onde se insere a microcefalia, registaram um aumento da sua frequência em várias regiões afectadas por epidemias por este vírus. A sua associação à infecção por vírus Zika apresenta um crescente nível de evidência, à medida que estudos observacionais e de caso-controlo vão sendo publicados.
A falta de imunidade das populações perante a emergência de um novo agente infeccioso, assim como a ampla dispersão de vectores competentes nas regiões afectadas, permitiu a sua rápida disseminação. A via de transmissão sexual pode ter sido, até agora, subestimada e pode vir a constituir uma importante barreira à erradicação do vírus. O desenvolvimento de uma vacina, aliado às medidas de controlo de vectores e à prática de sexo seguro, terá um impacto significativo no controlo e na prevenção da infecção por vírus Zika na população.
Referencias
1. Dick GW, Kitchen SF, Haddow AG. Zika virus. I. Isolations and serologicalspecificity. Trans R Soc Trop Med Hyg. 1952;46:509-20. [ Links ]
2. Dick GW. Epidemiological notes on some viruses isolated in Uganda; Yellow fever, Rift Valley fever, Bwamba fever, West Nile, Mengo, Semliki forest, Bunyamwera, Ntaya, Uganda S and Zika viruses. Trans R Soc Trop Med Hyg. 1953;47:13-48. [ Links ]
3. Musso D, Gubler DJ. Zika Virus. Clin Microbiol Rev. 2016;29:487-524. [ Links ]
4. Macnamara FN. Zika virus: a report on three cases of human infection during an epidemic of jaundice in Nigeria. Trans R Soc Trop Med Hyg. 1954;48:139-45. [ Links ]
5. Faye O, Freire CC, Iamarino A, Faye O, de Oliveira JV, Diallo M, et al. Molecular evolution of Zika virus during its emergence in the 20th century. PLoS Negl Trop Dis. 2014;8:e2636. [ Links ]
6. Olson JG, Ksiazek TG, Suhandiman, Triwibowo. Zika virus, a cause of fever in Central Java, Indonesia.Trans R Soc Trop Med Hyg. 1981;75:389-93. [ Links ]
7. Marchette NJ, Garcia R, Rudnick A. Isolation of Zika virus from Aedes aegypti mosquitoes in Malaysia. Am J Trop Med Hyg. 1969;18:411-5. [ Links ]
8. Duffy MR, Chen TH, Hancock WT, Powers AM, Kool JL, Lanciotti RS, et al. Zika virus outbreak on Yap Island, Federated States of Micronesia. N Engl J Med. 2009;360:2536-43. [ Links ]
9. Lanciotti RS, Kosoy OL, Laven JJ, Velez JO, Lambert AJ, Johnson AJ. Genetic and serologic properties of Zika virus associated with an epidemic, Yap State, Micronesia, 2007. Emerg Infect Dis. 2008;14:1232-9 [ Links ]
10. Plourde AR, Bloch EM. A Literature Review of Zika Virus. Emerg Infect Dis. 2016;22:1185-92. [ Links ]
11. Musso D, Nilles EJ, Cao-Lormeau VM. Rapid spread of emerging Zika virus in the Pacific area. Clin Microbiol Infect. 2014; 20:O595-6. [ Links ]
12. Gatherer D, Kohl A. Zika virus: a previously slow pandemic spreads rapidly through the Americas. J Gen Virol. 2016;97:269-73. [ Links ]
13. Zanluca C, Melo VC, Mosimann AL, Santos GI, Santos CN, Luz K. First report of autochthonous transmission of Zika virus in Brazil. Mem Inst Oswaldo Cruz. 2015; 110:569-72. [ Links ]
14. Heukelbach J, Alencar CH, Kelvin AA, de Oliveira WK, Pamplona de Góes CL. Zika virus outbreak in Brazil. J Infect Dev Ctries. 2016; 10:116-20. [ Links ]
15. Enfissi A, Codrington J, Roosblad J, Kazanji M, Rousset D. Zika virus genome from the Americas. Lancet. 2016;387:227-8. [ Links ]
16. Lanciotti RS, Lambert AJ, Holodniy M, Saavedra S, Signor Ldel C. Phylogeny of Zika virus in Western Hemisphere, 2015. Emerg Infect Dis. 2016;22:933-5. [ Links ]
17. Musso D. Zika Virus Transmission from French Polynesia to Brazil. Emerg Infect Dis. 2015;21:1887. [ Links ]
18. Abushouk AI, Negida A, Ahmed H. An updated review of Zika virus. J Clin Virol. 2016; 84: 53-8. [ Links ]
19. Kuno G, Chang GJ. Full-length sequencing and genomic characterization of Bagaza, Kedougou, and Zika viruses. Arch Virol. 2007;152:687-96. [ Links ]
20. Diallo D, Sall AA, Diagne CT, Faye O, Faye O, Ba Y et al. Zika virus emergence in mosquitoes in southeastern Senegal, 2011. PLoS One. 2014; 9: e109442. [ Links ]
21. Fauci AS,Morens DM. Zika Virus in the Americas – Yet Another Arbovirus Threat. N Engl J Med. 2016; 374: 601-4.
22. Hayes EB. Zika virus outside Africa. Emerg Infect Dis. 2009; 15: 1347-50. [ Links ]
23. Wong PS, Li MZ, Chong CS, Ng LC, Tan CH. Aedes (Stegomyia) albopictus (Skuse): a potential vector of Zika virus in Singapore. PLoS Negl Trop Dis. 2013; 7: e2348. [ Links ]
24. Heitmann A, Jansen S, Lühken R, Leggewie M, Badusche M, Pluskota B, et al. Experimental transmission of Zika virus by mosquitoes from central Europe. Euro Surveill. 2017; 22: pii 30437. [ Links ]
25. Foy BD, Kobylinski KC, Chilson Foy JL, Blitvich BJ, Travassos da Rosa A, Haddow AD, et al. Probable non-vector-borne transmission of Zika virus, Colorado, USA. Emerg Infect Dis. 2011;17:880-2. [ Links ]
26. Moreira J, Peixoto TM, Machado de Siqueira A, Lamas CC. Sexually acquired Zika virus: a systematic review. ClinMicrobiol Infect. In press [ Links ]
27. Nicastri E, Castilletti C, Balestra P, Galgani S, Ippolito G. Zika Virus Infection in the Central Nervous System and Female Genital Tract. Emerg Infect Dis. 2016;22:2228-30. [ Links ]
28. Arsuaga M, Bujalance SG, Díaz-Menéndez M, Vázquez A, Arribas JR. Probable sexual transmission of Zika virus from a vasectomised man. Lancet Infect Dis. 2016;16:1107. [ Links ]
29. Coelho FC, Durovni B, Saraceni V, Lemos C, Codeco CT, Camargo S, et al. Higher incidence of Zika in adult women than adult men in Rio de Janeiro suggests a significant contribution of sexual transmission from men to women. Int J Infect Dis. 2016; 51: 128-32. [ Links ]
30. Musso D1, Nhan T, Robin E, Roche C, Bierlaire D, Zisou K et al. Potential for Zika virus transmission through blood transfusion demonstrated during an outbreak in French Polynesia, November 2013 to February 2014. Euro Surveill. 2014; 19: pii 20761. [ Links ]
31. Bearcroft WG. Zika virus infection experimentally induced in a human volunteer. Trans R Soc Trop Med Hyg. 1956; 50: 442-8. [ Links ]
32. Zammarchi L, Spinicci M, Bartoloni A. Zika Virus: a Review from the Virus Basics to Proposed Management Strategies. Mediterr J Hematol Infect Dis. 2016; 8: e2016056. [ Links ]
33. Waddell LA, Greig JD. Scoping Review of the Zika Virus Literature. PLoS One.
2016; 11: e0156376. [ Links ]
34. Shuaib W, Stanazai H, Abazid AG, Mattar AA. Re-Emergence of Zika Virus: A Review on Pathogenesis, Clinical Manifestations, Diagnosis, Treatment, and Prevention. Am J Med. 2016; 129: 879.e7-879e12. [ Links ]
35. Cao-Lormeau VM, Blake A, Mons S, Lastère S, Roche C, Vanhomwegen J et al. Guillain-Barré Syndrome outbreak associated with Zika virus infection in French Polynesia: a case-control study. Lancet. 2016; 387: 1531-9. [ Links ]
36. Vargas A, Saad E, Dimech GS, Santos RH, Sivini MA, Albuquerque LC. Characteristics of the first cases of microcephaly possibly related to Zika virus reported in the Metropolitan Region of Recife, Pernambuco State, Brazil. Epidemiol Serv Saude. 2016; 25: 691-700. [ Links ]
37. Pan American Health Organization [paho.org]. Epidemiological update. Neurological syndrome, congenital anomalies, and Zika virus infection 17 January 2016; 2016 [consultado 31 Jan 2017]. Disponível em http://www.paho.org/hq/index.php?option=com_docman&task=doc_view&Itemid=270&gid=32879&lang=en. [ Links ]
38. Cauchemez S, Besnard M, Bompard P, Dub T, Guillemette-Artur P, Eyrolle Guignot D et al. Association between Zika virus and microcephaly in French Polynesia, 2013-15: a retrospective study. Lancet. 2016; 387: 2125-32. [ Links ]
39. Brasil P, Pereira JP Jr, Moreira ME, Ribeiro Nogueira RM, Damasceno L, Wakimoto M, et al. Zika Virus Infection in Pregnant Women in Rio de Janeiro. N Engl J Med. 2016; 375: 2321-34. [ Links ]
40. França GV, Schuler-Faccini L, Oliveira WK, Henriques CM, Carmo EH, Pedi VD, et al. Congenital Zika virus syndrome in Brazil: a case series of the first 1501 livebirths with complete investigation. Lancet. 2016; 388: 891-7. [ Links ]
41. Martines RB, Bhatnagar J, de Oliveira Ramos AM, Davi HP, Iglezias SD, Kanamura CT, et al. Pathology of congenital Zika syndrome in Brazil: a case series. Lancet. 2016; 388: 898-904. [ Links ]
42. Mlakar J, Korva M, Tul N, Popovic M, Poljšak-Prijatelj M, Mraz J, et al. Zika Virus Associated with Microcephaly. N Engl J Med. 2016; 374: 951-8.
43. de Araújo TV, Rodrigues LC, de Alencar Ximenes RA, de Barros DF, Montarroyos UR, de Melo AP, et al. Association between Zika virus infection and microcephaly in Brazil, January to May, 2016: preliminary report of a case-control study. Lancet Infect Dis. 2016; 16: 1356-63. [ Links ]
44. World Health Organization [who.int]. Situation Report Zika Virus Microcephaly Guillain-Barré Syndrome 20 January 2017; 2017 [consultado 31 jan 2017]. Disponível em http://apps.who.int/iris/bitstream/10665/253604/1/zikasitrep-20Jan17-eng.pdf?ua=1. [ Links ]
45. European Centre for Disease Control and Prevention [ecdc.europa.eu]. Interim guidance for healthcare providers and Zika virus laboratory diagnosis; 2016 [consultado 31 jan 2017]. Disponível em http://ecdc.europa.eu/en/publications/Publications/zika-virus-guidance-healthcare-providers-and-laboratory-diagnosis.pdf.
46. World Health Organization [who.int]. Laboratory testing for Zika virus infection. Interim guidance 23 March 2016; 2016 [consultado 31 jan 2017]. Disponível em http://apps.who.int/iris/bitstream/10665/204671/1/WHO_ZIKV_LAB_16.1_eng.pdf?ua=1. [ Links ]
47. Gourinat AC, O’Connor O, Calvez E, Goarant C, Dupont-Rouzeyrol M. Detection of Zika virus in urine. Emerg Infect Dis. 2015; 21: 84-6.
48. Musso D, Roche C, Nhan TX, Robin E, Teissier A, Cao-Lormeau VM. Detection of Zika virus in saliva. J Clin Virol. 2015; 68: 53-5. [ Links ]
49. Centers for Disease Control and Prevention [cdc.gov]. Update: Interim Guidance for Health Care Providers Caring for Pregnant Women with Possible Zika Virus Exposure — United States, July 2016; 2016 [consultado 31 jan 2017]. Disponível em https://www.cdc.gov/mmwr/volumes/65/wr/mm6529e1.htm.
50. Maharajan MK, Ranjan A, Chu JF, Foo WL, Chai ZX, Lau EY, et al. Zika Virus Infection: Current Concerns and Perspectives. Clin Rev Allergy Immunol. 2016; 51: 383-94. [ Links ]
51. Pierson TC, Graham BS. Zika virus: immunity and vaccine development. Cell.
2016; 167: 625-31. [ Links ]
52. European Centre for Disease Control and Prevention [ecdc.europa.eu]. Rapid risk assessment: Zika virus disease epidemic. Ninth update, 28 October 2016; 2016 [consultado 31 jan 2017]. Disponível em http://ecdc.europa.eu/en/publications/Publications/rapid-risk-assessment-zika-october-2016.pdf.
53. Dircção Geral da Saúde [dgs.pt]. Comunicado 22/12/2016 Zika recomendações para viajantes; 2016 [consultado 31 jan 2017]. Disponível em http://www.dgs.pt/paginas-de-sistema/saude-de-a-a-z/zika.aspx.
54. European Centre for Disease Control and Prevention [ecdc.europa.eu]. Zika virus and safety of substances of human origin – A guide for preparedness activities in Europe; 2016 [consultadoem 31 jan 2017]. Disponível em http://ecdc.europa.eu/en/publications/Publications/Zika-virus-safety-of-substances-of-human-origin.pdf.
Correspondência:Pedro Brogueira pbrogueira@gmail.com
Serviço de Infecciologia e Medicina Tropical
Hospital de Egas Moniz - Centro Hospitalar de Lisboa Ocidental, E.P.E., Lisboa, Portugal
Rua Da Junqueira 126, 1349-019 Lisboa
Protecção de Seres Humanos e Animais: Os autores declaram que não foram realizadas experiências em seres humanos ou animais.
Direito à Privacidade e Consentimento Informado: Os autores declaram que nenhum dado que permita a identificação do doente aparece neste artigo.
Conflitos de Interesse: Os autores declaram a inexistência de conflitos de interesse na realização do presente trabalho.
Fontes de Financiamento: Não existiram fontes externas de financiamento para a realização deste artigo.
Recebido: 01/02/2017
Aceite: 01/03/2017














