Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Medicina Interna
versão impressa ISSN 0872-671X
Medicina Interna vol.25 no.2 Lisboa jun. 2018
https://doi.org/10.24950/rspmi/revisao/240/2/2018
ARTIGOS DE REVISÃO / REVIEW ARTICLES
Cânulas Nasais de Alto Fluxo: Uma Alternativa de Oxigenoterapia na Insuficiência Respiratória Aguda
High Flow Nasal Cannula: An Alternative Oxygen Therapy in Acute Respiratory Failure
Pedro Pires1, Carmen Marques1, Josep Masip2,3
1Unidade Funcional Medicina 1.2, Hospital de São José-Centro Hospitalar de Lisboa Central, Lisboa, Portugal
2Servicio de Medicina Intensiva, Consorci Sanitari Integral, Sant Joan Despí, Barcelona; Universidade de Barcelona, Barcelona, Espanha
3Servicio de Cardiologia, Hospital Sanitas CIMA, Barcelona, Espanha
RESUMO
A oxigenoterapia por cânulas nasais de alto fluxo representa um importante avanço nas alternativas para o suporte ventilatório não-invasivo em doentes com insuficiência respiratória aguda. Este artigo pretende rever os principais efeitos fisiológicos associados a esta técnica, bem como os estudos que sustentam a sua aplicação em diferentes etiologias. A sua excelente tolerabilidade associada a bons resultados de eficácia na insuficiência respiratória hipoxémica poderão torná-la em indicação de primeira linha em situações particulares como a pneumonia, nos doentes imunocomprometidos, em casos de limitação para entubação oro-traqueal ou na estratégia de desmame ventilatório. Estudos promissores têm também demonstrado boa resposta noutras causas de insuficiência respiratória e noutros contextos fora do ambiente de Cuidados Intensivos. Trata-se assim duma alternativa viável à ventilação não-invasiva, com potencial de aplicabilidade num importante conjunto de doentes integrados no espectro clínico a cargo da Medicina Interna.
Palavras-chave: Cânula; Insuficiência Respiratória; Oxigenoterapia.
ABSTRACT
High flow nasal cannula oxygen therapy represents an important alternative in non-invasive ventilatory support for patients with acute respiratory failure. This article aims to review the main physiological effects of the technique and the studies that support its use in diverse underlying conditions. Due to its excellent tolerability and efficacy in cases of hypoxemic respiratory failure, it may become a first-line indication in special situations like pneumonia, in immunocompromised patients, patients with do-not-intubate orders or as an aid in invasive ventilation weaning. Some promising studies have also demonstrated a good clinical response with the use of this technique in patients with respiratory failure from other causes and outside the Intensive Care Unit. Hence, it seems to be a viable alternative to non-invasive ventilation, with potential applicability in a vast group of patients of the Internal Medicine field of action.
Keywords: Cannula; Oxygen Inhalation Therapy; Respiratory Insufficiency.
Introdução
A oxigenoterapia como terapêutica de suporte na insuficiência respiratória aguda (IRA) surge na sequência dos trabalhos de Beddoes e Watt,1 no Pneumatic Institute, em finais do século XVIII. Ao longo de mais de dois séculos, esta continua a representar uma pedra basilar na abordagem a doentes com insuficiência respiratória de diferentes etiologias.
No início do século passado, os pulmões de aço representaram a primeira forma generalizada de suporte ventilatório como resposta às epidemias de poliomielite. Com a evolução científica e tecnológica, a ventilação mecânica invasiva com pressão positiva rapidamente se tornou a terapêutica de escolha na insuficiência respiratória grave. Esta associa-se a diversas complicações, como por exemplo o baro ou o volutrauma. A técnica condiciona ainda a abolição dos mecanismos de defesa fisiológicos da via aérea superior e, frequentemente, a necessidade de sedo-analgesia, aumentando o risco de intercorrências infecciosas.
Para responder a estas preocupações surge nos últimos anos a necessidade de encontrar outras técnicas não-invasivas que ocupem o espaço entre a oxigenoterapia convencional e a ventilação mecânica invasiva.
A ventilação não-invasiva (VNI) representou um importante marco neste caminho, sendo fortemente recomendada2 em determinadas etiologias de IRA, como na exacerbação da doença pulmonar obstrutiva crónica (DPOC)3 ou no edema pulmonar agudo.4
Os avanços na oxigenoterapia convencional e o estabelecimento da VNI ao longo das últimas décadas tem permitido evitar a ventilação mecânica invasiva em casos de insuficiência respiratória aguda moderada a grave. Estas, contudo, apresentam ainda limitações importantes e que têm vindo a condicionar a sua aplicabilidade. A oxigenoterapia convencional tem o fluxo limitado a um máximo de 15 L/min, valores manifestamente insuficientes na falência respiratória,5 quer pela diluição do oxigénio (O2) fornecido a baixo fluxo com o ar ambiente,6 quer pelos efeitos secundários do oxigénio não aquecido e humidificado (especialmente a secura das mucosas).7
Também a VNI apresenta importantes taxas de intolerância à técnica, sendo as complicações mais frequentes as lesões cutâneas, a irritação ocular e a sensação de claustrofobia.8,9 Estas podem ser minimizadas pelo trabalho de uma equipa multidisciplinar experiente, adoptando estratégias de escalada da parameterização e de adaptação às diversas interfaces,10,11 mas não raras vezes justificando a necessidade de utilização de sedação em baixas doses.12 Por outro lado, em determinadas etiologias de insuficiência respiratória, como por exemplo na pneumonia, a evidência do benefício da VNI é muito limitado e a sua utilização restrita a grupos específicos.
De acordo com as diferentes etiologias de insuficiência respiratória aguda, a falência da VNI pode ser uma realidade em 5% a 60% dos casos.11 Na maioria destes doentes, a ventilação mecânica invasiva representava a única alternativa.
Nesse sentido, múltiplos trabalhos se têm vindo a debruçar sobre as cânulas nasais de alto fluxo (CNAF) como uma alternativa válida em doentes com IRA. Esta técnica, inicialmente desenvolvida em populações neonatais com bons resultados de eficácia e segurança,13,14 tem vindo a ganhar o seu espaço também em adultos. Esta revisão pretende assim debruçar-se sobre os efeitos fisiológicos e as possíveis indicações desta técnica, que poderá vir a ser de inegável utilidade para o internista, quer em contexto de Cuidados Intensivos, mas também nas Unidades de Cuidados Intermédios e nos Serviços de Urgência.
A Técnica
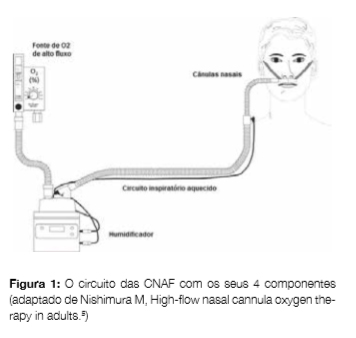
O circuito das CNAF baseia-se em quatro componentes essenciais: uma fonte de oxigénio de alto fluxo com misturador de ar, que permita definir o fluxo e a fracção inspiratória de oxigénio (FiO2) fornecida, um humidificador, um circuito inspiratório aquecido (a 37ºC) e cânulas nasais específicas (com um diâmetro mais largo face às cânulas nasais clássicas) para a técnica que permitem, em conjunto, fornecer oxigénio aquecido e humidificado em fluxos bem superiores aos da oxigenoterapia convencional (Fig 1). Este circuito permite fornecer um FiO2 até 1,0 e um fluxo máximo de 60 L/min.
No doente em falência respiratória aguda, deve-se partir de fluxos mais baixos de forma rapidamente crescente (permitindo uma adaptação do doente aos altos fluxos fornecidos) até ao máximo tolerado, estabelecendo-se paralelamente o FiO2 que se pretende atingir. Nesta fase, o doente deve encontrar-se sob estreita monitorização, avaliando a resposta clínica à técnica e permitindo a titulação do fluxo e do FiO2. Após estabilização clínica, o desmame deve iniciar-se com a diminuição do FiO2 e, só depois, do fluxo.15 Trata-se duma técnica de fácil aplicação com rápida curva de aprendizagem para os profissionais de saúde envolvidos.
Efeitos Fisiológicos
MELHOR CONTROLO SOBRE FIO2 FORNECIDA
Uma das grandes limitações da oxigenoterapia convencional prende-se com a impossibilidade de fornecer fluxos adequados às necessidades dum doente em IRA. Estas necessidades podem atingir fluxos de 30 a 100 L/min,5 sendo que a fracção alveolar de oxigénio (FAlvO2) acaba por ser inferior à FiO2 fornecida por um fenómeno de diluição com o ar ambiente e dependendo intimamente do padrão ventilatório do doente (nomeadamente da frequência respiratória e da respiração com boca aberta ou fechada, sendo a FiO2 maior na respiração com boca aberta por se crer que a cavidade nasal representa um reservatório anatómico de oxigénio).16,17 Num estudo em 10 doentes6 com hipoxemia crónica, Markovitz et al determinaram que, pelas medições dum cateter transtraqueal, O2 fornecido a 5 L/min por cânulas nasais apenas atingia um FiO2 de 32% (quando o esperado seria de 40%).
Assim, e sabendo-se que o FiO2 aumenta com o aumento de fluxo,16 quando este é administrado em baixo fluxo é muito difícil prever a FiO2 efectivamente fornecida. Este controlo pode ser crucial no manuseamento de um doente com insuficiência respiratória, em que a utilização duma técnica que nos garanta uma quantificação fidedigna do O2 fornecido pode ser fulcral na gestão e interpretação das respostas clínicas. Nesse sentido, Ritchie et al17 procuraram medir a FalvO2 em doentes com CNAF sob um FiO2 constante (60%) e com fluxos crescentes, constatando-se que acima dos 30 L/min a FAlvO2 se aproxima da FiO2 fornecida.
EFEITO PEEP (POSITIVE END-EXPIRATORY PRESSURE)
Desde cedo se suspeitou que um dos mecanismos através do qual a oxigenoterapia de alto fluxo melhoraria a oxigenação seria por gerar uma pressão positiva na via aérea como consequência dos elevados fluxos de oxigénio administrados de forma contínua.
O trabalho de Groves et al veio neste sentido, comprovando um aumento da pressão expiratória faríngea com o aumento de fluxo de oxigénio em 10 voluntários saudáveis.18 Os estudos de Parke et al19-22 corroboraram estes resultados, salientando-se uma relação linear crescente de aumento de pressão expiratória faríngea com o aumento de fluxo (11,9+/- 2,7 cm H2O a um fluxo máximo de 100 L/min).21 A posição da boca (aberta ou fechada) influencia decisivamente este gradiente de pressão, sendo superior na respiração com boca fechada, estimando-se que para cada aumento de fluxo de 10 L/min, aumente 0,69 cm H2O de pressão se boca fechada e 0,35 cm H2O se boca aberta. Por exemplo, um doente sob CNAF a respirar de boca fechada e sob um fluxo de 50 L/ min teria um incremento médio de 3,31+/-1,05 cm H2O de pressão na via aérea.22
Estes valores de pressão representam, contudo, valores inferiores quando comparados com os obtidos com a VNI.20 Chanques et al23 compararam as pressões na orofaringe em 10 doentes internados em Cuidados Intensivos sob CPAP Boussignac, cânulas nasais de alto fluxo e máscara com reservatório. Com o Boussignac as pressões da via aérea subiam consideravelmente nas duas fases da respiração, sendo que com as CNAF este aumento de pressão era mais modesto e apenas na expiração. O oxigénio em baixo fluxo não representava qualquer alteração nas pressões da via aérea. Estes resultados levantaram dúvidas sobre se este efeito-PEEP das CNAF era, na prática, fisiologicamente significativo.
Para tal, estudos em tomografia eléctrica de impedância21,24,25 procuraram esclarecer se o efeito na pressão expiratória tinha repercussão no volume pulmonar no final da expiração. Assim, este efeito PEEP representará um aumento de até 25% no volume pulmonar expiratório, traduzindo uma melhoria da capacidade pulmonar funcional e repercutindo um provável fenómeno de recrutamento alveolar. Este aumento de volume é proporcional ao fluxo administrado e estas alterações são reversíveis com a suspensão da técnica. Um estudo recente26 mostrou que a posição da boca (desvanecendo-se praticamente o efeito PEEP em doentes com a boca aberta), o fluxo e a complacência pulmonar eram os factores determinantes para garantir este efeito em diferentes pontos da via aérea.
WASHOUT DE DIÓXIDO DE CARBONO E DIMINUIÇÃO DE ESPAÇO MORTO ANATÓMICO
Tratando-se de um circuito aberto e apesar dos efeitos descritos nos volumes expiratórios pulmonares, a capacidade das CNAF proporcionarem um suporte ventilatório é mínimo. Assim, e perante uma técnica que utiliza altos fluxos de oxigénio, o risco de hipercapnia sempre foi uma preocupação. A maioria dos estudos, contudo, tem vindo a revelar valores estáveis de pressão parcial de dióxido de carbono (PCO2) associados à técnica,27-29 podendo mesmo apresentar-se diminuído.30 Esta deve-se essencialmente a duas condições determinantes: a diminuição do espaço morto anatómico e o eficiente washout de dióxido de carbono (CO2).
Com efeito, as cânulas nasais representam o único interface das técnicas não invasivas que não aumentam, por si só, o espaço morto.7 Por outro lado, a diminuição da frequência respiratória mantendo um volume corrente constante indica-nos diminuição da ventilação/minuto. A presença duma PCO2 que não se altera indica-nos uma ventilação alveolar estável, permitindo-nos inferir que existe diminuição da ventilação do espaço morto.29,31 Estudos animais30 e modelos in vitro da via aérea32,33 suportam a evidência dum washout de CO2 mais eficiente com relação linear com o aumento do fluxo fornecido.
HUMIDIFICAÇÃO E AQUECIMENTO DO AR INALADO
Uma das dificuldades na gestão da administração de fluxos de oxigénio superiores a 5 L/min são os efeitos secundários, descritos como pelo menos moderados em 50% dos casos.34 Os principais sintomas são a secura das mucosas (nasal, oral e faríngea), a hemorragia nasal, a cefaleia, o desconforto torácico e a tosse.35
Crê-se que esta sintomatologia está directamente relacionada com a administração de ar frio e seco e com o efeito directo deste na via aérea. Perante a inalação de ar com estas características, a resposta fisiológica é um aumento da resistência da via aérea superior, um mecanismo de defesa que permite retardar a passagem do ar e garantir a adequada humidificação e aquecimento quando este atinge as vias aéreas inferiores.36 Quando se perde esta barreira protectora, o efeito do ar frio e seco directamente aplicado nas vias aéreas inferiores associa-se a importante hiperrreactividade com broncoconstrição e diminuição significativa da complacência pulmonar.37 Sabe-se também que perante a administração de oxigénio em fluxos crescentes, a capacidade das vias aéreas superiores aquecerem e humidificarem o ar torna-se insuficiente38 e surgem os sintomas descritos.
Com efeito, estudos em animais39-42 demonstraram que a exposição a ar frio e seco em menos de 3h relaciona-se com perda de função mucociliar, desidratação da mucosa com lesão epitelial e reacção inflamatória local. Chidekel et al,43 num modelo in vitro de células epiteliais da via aérea humana expostas a diferentes graus de humidade relativa constataram que o grupo exposto a menor humidade apresentava histologicamente lesões de membrana e perturbação do metabolismo celular com significativa presença de mediadores pro-inflamatórios após 8 horas de exposição. Outro estudo44 em 11 voluntários saudáveis comprovou que a exposição a 30 minutos de ar não humedecido compromete significativamente a função mucociliar, quer pela desidratação das mucosas, pela alteração das propriedades do muco e pela diminuição da mobilidade dos cílios.
As cânulas nasais de alto fluxo, ao fornecerem oxigénio humidificado a 100% e com um circuito aquecido à temperatura corporal (37ºC), permitem ultrapassar os efeitos secundários da administração de altos fluxos de oxigénio. Com efeito, desde que o fluxo de O2 fornecido se aproxime do fluxo inspiratório do doente, é garantida uma humidificação adequada do ar inalado.45 Isto permite que as CNAF se associem de forma significativa a menores sintomas de secura das mucosas ou hemorragia nasal quando comparado com a oxigenoterapia convencional, tornando-a uma técnica melhor tolerada pelos doentes.46-48
Conforto
Desde o início da utilização desta técnica que se percebeu que um dos pontos-fortes que a mesma apresentava era uma melhoria do conforto com baixa taxa de efeitos adversos. Melhoria que era significativa em escalas analógicas após 30 minutos de técnica.27 Outro dado consistente nos diversos estudos e que está intrinsecamente relacionado com a melhoria do conforto prende-se com a diminuição da frequência respiratória (FR),24,49 sem hipercapnia ou compromisso da ventilação alveolar. Sztrymf et al50 estudaram 38 doentes com IRA com melhoria da assincronia toraco-abdominal e do score de dispneia ao final de 30 minutos sob CNAF. Itagaki et al,29 num estudo semelhante, também comprovaram diminuição significativa da FR e da assincronia toraco-abdominal (ATA) comparativamente à oxigenoterapia convencional. Estes indicadores traduzem uma melhoria do padrão respiratório, contribuindo para tal o sistema aquecido e humedecido utilizado pela técnica com diminuição da resistência das vias aéreas, a diminuição do espaço morto anatómico com uma ventilação mais eficaz e o efeito PEEP com recrutamento alveolar.
Noutro estudo,51 foi comparado o uso durante 30 minutos de VNI, CNAF e oxigenoterapia convencional por máscara de Venturi em 14 doentes com IRA. Constatou-se que, apesar da oxigenação melhorar significativamente com a VNI, os dados das escalas de conforto e dispneia eram significativamente melhores com as CNAF comparativamente à VNI e sem diferenças significativas relativamente à mascara de Venturi. Quando inquiridos sobre que técnica preferiria repetir no futuro, a grande maioria dos doentes (71%) escolheria as CNAF. Estes indicadores traduzem o papel das CNAF na insuficiência respiratória aguda garantindo um compromisso adequado entre a oxigenação (ainda que não sendo tão eficaz como a VNI) e o conforto dos doentes.
Em doentes com IRA, a presença de secreções respiratórias pode limitar a aplicação de determinadas técnicas, como a VNI.52 Também neste ponto as CNAF garantem um maior conforto aos doentes, permitindo não só a capacidade de expelir as secreções sem necessidade de interrupção da técnica mas também, pelo seu sistema de humidificação e aquecimento, ajudam a excreção das mesmas. Esta técnica permite ainda a ingesta hídrica e de alimentos sem limitações, não condiciona a comunicação verbal e possibilita a deambulação em pequenos espaços.
Indicações Clínicas
A) INSUFICIÊNCIA RESPIRATÓRIA HIPOXÉMICA
Múltiplos estudos se debruçaram sobre a aplicabilidade das CNAF em contexto de insuficiência respiratória hipoxémica (Tabela 1). As várias publicações têm consistentemente vindo a demonstrar melhoria da oxigenação e diminuição significativa da frequência respiratória em doentes com IRA de diferentes etiologias, quando comparada com a oxigenoterapia convencional.24,27,29,53,54 Sztrympf et al50 analisaram os resultados gasimétricos de 38 doentes com IRA previamente submetidos a oxigenoterapia por máscara com reservatório, assistindo-se a uma melhoria substancial da oxigenação na primeira hora, resultados que se mantinham consistentes às 24 horas.
Apesar disto, quando comparada com a VNI, esta ainda tem vindo a demonstrar melhoria mais significativa da oxigenação.41,55 Ainda assim, um estudo randomizado multicêntrico de não-inferioridade56 mostrou resultados semelhantes para as CNAF quanto à falência e à mortalidade associada a ambas as técnicas, estando a VNI mais associada a efeitos secundários significativos. Esta melhor tolerabilidade da técnica é bem patente num estudo retrospectivo57 em que doentes com IRA foram submetidos em primeira linha a VNI com uma taxa de intolerância de 38%. Estes doentes foram então submetidos a CNAF com uma grande taxa de sucesso (menos de 10% destes doentes necessitaram de intubação orotraqueal (IOT), provando a valia desta técnica como alternativa, evitando o recurso à ventilação invasiva.
Mais recentemente, estudos randomizados procuraram comparar a VNI, as CNAF e a oxigenoterapia convencional para insuficiência respiratória de diferentes etiologias. Schwabbauer et al51 randomizaram 14 doentes com falência respiratória para 30 minutos de CNAF, VNI e oxigenoterapia de baixo fluxo, constatando que a VNI tinha melhores resultados na oxigenação mas à custa de maior desconforto, apresentando as CNAF um bom compromisso entre oxigenação e tolerabilidade. O estudo FLORALI58 aleatorizou 310 doentes de diferentes centros com insuficiência respiratória não-hipercapnica (Pa/FiO2 < 300) para CNAF, VNI e oxigenoterapia convencional. A taxa de IOT foi inferior no grupo sob CNAF (38% vs 47% vs 50%) ainda que esta não se tenha revelado estatisticamente significativa. Numa análise post-hoc desta população, nomeadamente do subgrupo com falência respiratória mais grave (Pa/FiO2 < 200) as taxas de IOT dos doentes com CNAF revelaram-se significativamente inferiores às dois outros dois grupos.
Estes ensaios focam-se sobre diversas etiologias e diferentes gravidades de insuficiência respiratória. Análises mais específicas em séries mais pequenas de doentes têm permitido constatar a valia das CNAF em várias causas de falência respiratória. Um bom exemplo disso são os trabalhos em grupos de doentes com ARDS (acute respiratory distress syndrome),59,60 em que as taxas de falência da técnica se assemelharam às da VNI (40% a 55%). A insuficência cardíaca hipoxemiante foi também postulada como uma possível indicação para as CNAF. No edema pulmonar agudo (EAP) propriamente dito, os escassos resultados61 não mostram uma vantagem significativa das CNAF face à oxigenoterapia convencional (além de melhoria subjectiva da dispneia) pelo que a VNI se mantém como a indicação de primeira linha. Após uma estabilização inicial, contudo, estes doentes podem vir a necessitar de períodos mais alargados de VNI, com maior risco de intolerância da técnica, e nos quais as CNAF podem representar um método alternativo eficaz e seguro.62,63 Quanto aos doentes com patologia cardíaca de base importa referir o trabalho de Stéphan et al,56 um ensaio randomizado e multicêntrico em 830 doentes com IRA pós-cirurgia cardiotorácica, que mostrou uma não inferioridade da taxa de falência das CNAF relativamente à VNI (21,% vs 21,9%) nesta população específica.
Também no tromboembolismo pulmonar as preocupações com o elevado risco de deterioração hemodinâmica desaconselham o uso da VNI. Messika et al64 apresentou recentemente um estudo retrospectivo em 17 doentes com IRA hipoxémica por tromboembolismo pulmonar grave submetidos a CNAF. Todos estes registaram melhoria da oxigenação e diminuição da FR nas primeiras 2 horas de técnica sem alterações dos parâmetros hemodinâmicos, funcionando como terapêutica de suporte essencial e ponte até à realização de fibrinólise, não tendo havido necessidade de ventilação mecânica invasiva em nenhum doente.
Pela sua tolerabilidade e bons resultados preliminares, as CNAF despertaram particular interesse nos grupos de doentes em que a ventilação mecânica invasiva envolve elevados riscos, como os imunocomprometidos ou os doentes oncológicos. Num estudo em 50 doentes65 com insuficiência respiratória e decisão de não-intubação a utilização de CNAF como primeira linha mostrou melhoria significativa da oxigenação e só em 18% dos casos houve necessidade de escalar a terapêutica para VNI. Em 45 doentes com patologia hematológica e falência respiratória grave (Pa/FiO2 < 100) o insucesso das CNAF (67%) obteve valores semelhantes às da VNI em populações semelhantes.66 De igual modo, uma análise retrospectiva de 37 transplantados pulmonares com IRA mostrou uma taxa de falência de 59% (bem inferior à da oxigenoterapia convencional) sendo, numa análise multivariada, o uso de CNAF a única variável associada à diminuição do risco de IOT.47 Dois estudos retrospectivos67,68 com cerca de duas centenas de doentes oncológicos mostraram também resultados favoráveis com as CNAF. Um estudo observacional69 em 115 imunocomprometidos com falência res piratória tratados com CNAF ou VNI mostrou maiores taxas de IOT e mortalidade aos 28 dias no grupo sob VNI.
A maioria destes estudos centrou-se em doentes em ambiente de Cuidados Intensivos. Contudo, a tolerabilidade e os bons resultados das CNAF exigiram a sua avaliação em ambientes menos controlados e abrangendo uma população mais heterogénea. Alguns ensaios têm assim tentado demonstrar a aplicabilidade desta técnica noutros contextos, nomeadamente em Serviço de Urgência (Tabela 2). Dois estudos prospectivos com pequeno número de doentes demonstraram melhoria nas escalas de conforto e dispneia e, respectivamente, melhoria da oxigenação70 e da necessidade de hospitalização48 com o uso de CNAF compartivamente à oxigenoterapia convencional no Serviço de Urgência. No trabalho de Jones et al71 o grupo sob CNAF no SU revelou menor tendência para necessidade de ventilação mecânica invasiva.
Mais recentemente, um trabalho72 avaliou a utilização de CNAF em 67 doentes de enfermaria (dois terços dos quais em enfermarias de Medicina Interna) com insuficiência respiratória ou risco de deterioração respiratória, demonstrando semelhantes melhorias de FR, FC e SpO2.
Os dados acima referidos, apesar de se associaram a uma inegável potencialidade da técnica, devem ser interpretados com cautela. Os ensaios randomizados são escassos, sem grande poder e as populações estudadas são extremamente heterogéneas. Ainda recentemente duas meta-análises73,74 com mais de 2000 doentes com insuficiência respiratória não revelaram diferenças significativas nas taxas de intubação das CNAF comparativamente à oxigenoterapia convencional. Por outro lado, uma outra meta-análise75 com maior poder (18 estudos, n = 3881 doentes) mostrou menor taxa de intubação orotraqueal no grupo de doentes tratados com CNAF em comparação com a oxigenoterapia convencional. Estes dados são ainda mais relevantes sabendo-se que, no mesmo estudo, o grupo sob VNI não mostrou diferenças significativas face à oxigenoterapia em baixo fluxo.
B) INSUFICIÊNCIA RESPIRATÓRIA HIPERCÁPNICA
A abordagem de primeira linha à insuficiência respiratória aguda hipercápnica, em contexto de exacerbação de DPOC, é a ventilação não-invasiva, com forte evidência a favorecer o uso desta técnica.3 A utilização das CNAF neste contexto sempre foi vista de forma muito cautelosa pelos elevados fluxos de oxigénio envolvidos. Contudo, conforme já descrito, esta técnica parece ter um efeito benéfico na diminuição do espaço morto anatómico, com maior eficácia da ventilação alveolar e do trabalho respiratório e promovendo um maior washout de CO2 nas vias aéreas superiores. Estudos em DPOC estáveis e sem exacerbação mostraram que a utilização da técnica não se associava a alterações do PCO2.28,76 Na IRA hipercápnica em doentes que não toleravam a VNI as CNAF mostraram bons resultados em casos clínicos isolados de doentes DPOC e com patologia estrutural crónica.77-79 Um ensaio randomizado de Nilius et al49 estudou um grupo de doentes com DPOC e IRA hipercápnica, submetidos a HFNC a 20L/min ou oxigenoterapia convencional a 2 L/min, revelando melhoria significativas na diminuição da FR, no trabalho respiratório e sem alterações da PCO2 ou do pH. Assim, e apesar de nos doentes com estas características a VNI continuar a ser a indicação de primeira linha, os poucos estudos realizados mostram que a CNAF pode representar uma alternativa segura.
C) DESMAME VENTILATÓRIO
Pelos mecanismos fisiológicos acima descritos, crê-se que as CNAF possam ter um importante papel a desempenhar no período após a extubação de doentes críticos. Vários estudos randomizados46,80-82 têm vindo a demonstrar melhoria da oxigenação, das escalas de dispneia e da necessidade de escalar suporte ventilatório e re-intubação comparativamente ao uso de oxigenoterapia convencional. Jugava-se que este efeito seria mais eficaz em doentes com índice de massa corporal mais elevado24 pela maior propensão a desenvolver atelectasias após IOT. Num estudo randomizado em 115 doentes com índice de massa corporal > 30 pós-cirurgia cardíaca83 não se notaram diferenças significativas no score de atelectasias ou na oxigenação entre o grupo das CNAF e da oxigenoterapia convencional, revelando apenas uma ligeira melhoria na escala de dispneia às 8 horas favorável ao grupo sob CNAF. O estudo OPERA84 refreou um pouco as expectativas nesta matéria. Este ensaio randomizado em 220 doentes com risco moderado a elevado para complicações pulmonares submetidos a cirurgia abdominal major não revelou diferenças significativas entre as CNAF e a oxigenoterapia convencional na hipoxemia pós-extubação e nas complicações pulmonares a 7 dias. Mais recentemente, o estudo de Hernandez et al85 em 527 doentes com baixo risco de reintubação mostrou vantagem significativa no uso de CNAF comparativamente à oxigenoterapia convencional na taxa de reintubação às 72 horas (4,9% vs 12,2%). A mesma equipa desenvolveu um ensaio semelhante para doentes em alto risco de intubação,86 demonstrando também que as CNAF se associavam de forma independente à prevenção de reintubação às 72 horas comparativamente à oxigenoterapia convencional. Nesta sequência procurou-se também comparar a eficácia das CNAF neste contexto em relação ao uso da VNI.87 Este estudo randomizado com 604 doentes revelou taxas de reintubação significativamente inferiores no grupo sob CNAF.
D) APOIO NA REALIZAÇÃO DE TÉCNICAS INVASIVAS
A intubação orotraqueal num doente crítico é sempre um momento particularmente delicado e frequentemente associado a complicações graves. Os protocolos actuais recomendam um período de pré-oxigenação com insuflador manual mas, mesmo com o clínico mais experiente, a técnica exige sempre um período de apneia num doente já sob insuficiência respiratória aguda. As CNAF, pela sua configuração, permitem fornecer oxigenoterapia em alto fluxo sem qualquer influência na laringoscopia e, portanto, de forma contínua durante todo o procedimento. O trabalho de Miguel-Montanes et al88 em 101 doentes submetidos a IOT, randomizados para CNAF e oxigenoterapia de baixo fluxo mostram valores mais baixos de SpO2 e maior prevalência de hipoxemia grave com a oxigenoterapia convencional, sugerindo o benefício das CNAF neste procedimento.
A broncofibroscopia é também uma técnica delicada a realizar em doentes com insuficiência respiratória grave, com elevado risco de hipoxemia grave intra-procedimento. Contudo, por vezes, a realização de lavado bronco-alveolar para identificação de agentes microbiológicos pode ser crucial na estratégia diagnóstica e terapêutica. Assim, e pelo mesmo mecanismo subjacente à laringoscopia, a possibilidade de utilizar as CNAF de forma contínua durante a técnica tem sido utilizado em casos isolados com bons resultados.89,90 Um estudo randomizado77 mostrou melhoria significativa da oxigenação do grupo que realizou CNAF a 60 L/min, comparativamente com os doentes que realizaram um fluxo inferior (40 L/min) ou máscara de Venturi. Um outro ensaio randomizado mostrou a superioridade na oxigenação proporcionado pela aplicação de VNI antes e após o procedimento quando comparada com as CNAF91
E) PATOLOGIA RESPIRATÓRIA CRÓNICA
Os bons resultados das CNAF na IRA tem permitido extrapolar a sua aplicação para os doentes com patologia respiratória crónica. Com efeito, os poucos estudos existentes, e em poucos doentes, parecem ter um efeito benéfico na diminuição das exacerbações da DPOC e na melhoria da qualidade de vida e da função pulmonar.92,93 Por outro lado, os pneumopatias crónicos com hipoventilação nocturna também mostraram resultados favoráveis na melhoria da oxigenação e redução da hipercapnia no período nocturno, diminuição do índice de apneia/hipopneia e melhoria do padrão do sono sob CNAF.94
A Tabela 3 procura resumir as etiologias e populações específicas em que as CNAF têm vindo a mostrar uma consistente evidência de poderem vir a ser uma indicação de primeira linha e/ou uma alternativa segura à ventilação não-invasiva na IRA.
Efeitos Adversos
As CNAF são, conforme já referido, uma técnica extremamente bem tolerada pelos doentes, sem os efeitos secundários associados à VNI ou à oxigenoterapia convencional, trazendo um conjunto de vantagens em casos de IRA (Tabela 4). Há relatos de desconforto cervical ligeiro associado ao início da técnica27 mas que não justificaram interrupção das CNAF. Salienta-se ainda a presença de três casos de pneumotórax associado à utilização de CNAF no período neonatal, nunca tendo sido reportado esta complicação em adultos.95
Crê-se que o principal risco da utilização das CNAF é uma das suas grandes vantagens: a sua grande tolerabilidade e conforto pode mascarar situações mais graves e atrasar uma escalada de suporte ventilatório atempada (Tabela 4). Este alerta foi lançado pelo estudo retrospectivo de Kang et al96 que analisou 185 casos de falência de CNAF, divididos entre aqueles que foram entubados precoce (< 48 horas) ou tardiamente (> 48 horas). O grupo que foi entubado mais precocemente apresentava uma mortalidade significativamente inferior (39% vs 67%).
Apesar das múltiplas críticas ao desenho deste estudo a verdade é que se priorizou a necessidade de identificar factores preditores de falência da técnica. Estes indicadores podem ser tão precoces como a FR que não diminui ou a Pa/FiO2 que não aumenta ao fim de 1 hora.49 Outros estudos59,60,66,97 revelaram que índices de gravidade (APACHE II, SAPS II ou SOFA) mais elevados, o uso de vasopressores, a incapacidade de melhorar a oxigenação ou os parâmetros hemodinâmicos ao fim de 6 horas e a pneumonia bacteriana seriam factores preditores de maior risco de falência das CNAF. Assim, este tipo de doentes merece uma monitorização cautelosa e apertada, em especial nas primeiras horas sob a técnica, devendo manter um elevado grau de suspeição em doentes que, apesar de aparentarem estar mais confortáveis sob as CNAF, não melhoram os parâmetros de oxigenação e hemodinâmicos de forma significativa.
Conclusão
As CNAF surgem como uma técnica eficaz e segura na IRA, garantindo um compromisso aceitável entre melhoria da oxigenação e tolerabilidade dos doentes. A VNI continua a ser o método preferencial em grupos específicos, como a exacerbação da DPOC ou o edema agudo do pulmão. Nestes, o papel das CNAF poderá ser reservado como alternativa à ventilação mecânica invasiva nos casos de intolerância à VNI.
Os seus efeitos fisiológicos e o conforto da técnica deixam antever a possibilidade desta técnica poder ser utilizada em primeira linha noutras etiologias, como a pneumonia (onde a VNI tem evidência limitada), o ARDS, em doentes imunocomprometidos ou com limitação terapêutica, bem como como estratégia de desmame ventilatório. Os estudos actuais, realizados em populações pequenas e muito heterogéneas, deixam antever taxas de falência da técnica melhores face à oxigenoterapia convencional e que não parecem ser inferiores à VNI. A sua utilização no apoio à realização de determinadas técnicas invasivas ou em patologias crónicas também parece ter benefícios. A aplicabilidade desta técnica fora do contexto dos Cuidados Intensivos, como por exemplo no serviço de Urgência, tem mostrado bons resultados e poderá representar uma arma futura para o internista.
Trata-se, assim, da novidade mais relevante no mundo do suporte respiratório não-invasivo da última década, sendo necessários estudos randomizados robustos para comprovar as tendências acima descritas e melhor definir as reais potencialidades das CNAF.
Referencias
1. Beddoes T, Watt J. Considerations on the Medicinal uses of Factitious Airs, and on the Manner of Obtaining them in Large Quantities. Bristol: Bulgin and Rosser: 1795. [ Links ]
2. Rochwerg B, Brochard L, Elliott MW, Hess D, Hill NS, Nava S, et al. Official ERS/ATS clinical practice guidelines: noninvasive ventilation for acute respiratory failure. Eur Respir J. 2017 50: pii: 1602426. [ Links ]
3. Brochard L, Mancebo J, Wysocki M, Lofaso F, Conti G, Rauss A, Simonneau G, et al. Noninvasive ventilation for acute exacerbations of Chronic Obstructive Pulmonary Disease. N Engl J Med. 1995; 333:817-22. [ Links ]
4. Masip J, Betbesé AJ, Páez J, Vecilla F, Cañizares F, Padró J, et al. Non-Invasive pressure support ventilation versus conventional oxygen therapy in acute cardiogenic pulmonary oedema: a randomized trial. Lancet. 2000; 356:2126-32. [ Links ]
5. Nishimura M. High-flow nasal cannula oxygen therapy in adults. J Intensive Care. 2015; 3:15. [ Links ]
6. Markovitz GH, Colthurst J, Storer TW, Cooper CB. Effective inspired oxygen concentration measured via transtracheal and oral gas analysis. Respir Care. 2010; 55:453-9. [ Links ]
7. Nishimura M. High-flow nasal cannula oxygen therapy in adults: physiological benefits, indication, clinical benefits, and adverse effects. Respir Care. 2016 ; 61:529-41. [ Links ]
8. Gregoretti C, Confalonieri M, Navalesi P, Squadrone V, Frigerio P, Beltrame F, et al. Evaluation of patient skin breakdown and comfort with a new face mask for non-invasive ventilation: a multi-center study. Intensive Care Med. 2002 ; 28:278-84. [ Links ]
9. Nicolini A, Ferrera L, Santo M, Ferrari-Bravo M, Del Forno M, Sclifò F. Noninvasive ventilation for hypercapnic exacerbation of chronic obstructive pulmonary disease: factors related to noninvasive ventilation failure. Pol Arch Med Wewn. 2014;124:525-31. [ Links ]
10. Navalesi P, Fanfulla F, Frigerio P, Gregoretti C, Nava S. Physiologic evaluation of noninvasive mechanical ventilation delivered with three types of masks in patients with chronic hypercapnic respiratory failure. Crit Care Med. 2000; 28:1785-90. [ Links ]
11. Ozyilmaz E, Ugurlu AO, Nava S. Timing of noninvasive ventilation failure: causes, risk factors, and potential remedies. BMC Pulm Med. 2014;14:19. [ Links ]
12. Rocco M, Conti G, Alessandri E, Morelli A, Spadetta G, Laderchi A, et al. Rescue treatment for noninvasive ventilation failure due to interface intolerance with remifentanil analgosedation: a pilot study. Intensive Care Med. 2010; 36:2060-5. [ Links ]
13. Wilkinson D, Andersen C, O´Donnell CP, De Paoli AG, Manley BJ. High flow nasal cannula for respiratory support in preterm infants. Cochrane Database Syst Rev.2016 ;2:CD006405. [ Links ]
14. Mikalsen IB, Davis P, Oymar K. High flow nasal cannula in children: a literature review. Scand J Trauma Resusc Emerg Med. 2016;24:93. [ Links ]
15. Gotera C, Diaz Lobato S, Pinto T, Winck JC. Clinical evidence on high flow oxygen therapy and active humidification in adults. Rev Port Pneumol. 2013;19:217-27. [ Links ]
16. Wettstein RB,Shelledy DC,Peters JI. Delivered oxygen concentrations using low-flow and high-flow nasal cannulas. Respir Care. 2005; 50:604-9. [ Links ]
17. Ritchie JE, Williams AB, Gerard C, Hockey H. Evaluation of a humidified nasal high-flow oxygen system, using oxygraphy, capnography and measurement of upper airway pressures. Anaesth Intensive Care. 2011; 39:1103-10. [ Links ]
18. Groves N, Tobin A. High flow nasal oxygen generates positive airway pressure in adult volunteers. Aust Crit Care. 2007; 20:126-31. [ Links ]
19. Prke R, McGuinness S, Eccleston M. Nasal high-flow therapy delivers low level positive airway pressure. Br J Anaesth. 2009; 103:886-90. [ Links ]
20. Parke RL, McGuinness SP. Pressures delivered by nasal high flow oxygen during all phases of the respiratory cycle. Respir Care. 2013; 58:1621-4. [ Links ]
21. Parke RL, Bloch A, McGuinness SP. Effect of very-high-flow nasal therapy on airway pressure and end-expiratory lung impedance in healthy volunteers. Respir Care. 2015; 60:1397-403. [ Links ]
22. Parke RL, Eccleston ML, McGuinness SP. The effects of flow on airway pressure during nasal high-flow oxygen therapy. Respir Care. 2011; 56:1151-5. [ Links ]
23. Chanques G, Riboulet F, Molinari N, Carr J, Jung B, Prades A, et al. Comparison of three high flow oxygen therapy delivery devices: a clinical physiological cross-over study. Minerva Anestesiol. 2013;79:1344-55. [ Links ]
24. Corley A, Caruana LR, Barnett AG, Tronstad O, Fraser JF. Oxygen delivery through high-flow nasal cannulae increase end-expiratory lung volume and reduce respiratory rate in post-cardiac surgical patients. Br J Anaesth. 2011; 107:998-1004. [ Links ]
25. Riera J, Pérez P, Cortés J, Roca O, Masclans JR, Rello J. Effect of high-flow nasal cannula and body position on end-expiratory lung volume: a cohort study using electrical impedance tomography. Respir Care. 2013; 58:58996. [ Links ]
26. Luo JC, Lu MS, Zhao ZH, Jiang W, Xu B, Weng L, et al. Positive End-Expiratory Pressure Effect of 3 High-Flow Nasal Cannula Devices. Respir Care.2017; 62:888-95. [ Links ]
27. Roca O, Riera J, Torres F, Masclans JR. High-flow oxygen therapy in acute respiratory failure. Respir Care. 2010; 55:408-13. [ Links ]
28. Chatila W,Nugent T,Vance G,Gaughan J,Criner GJ. The effects of high-flow vs low-flow oxygen on exercise in advanced obstructive airways disease. Chest.2004 ; 126(4):1108-15 [ Links ]
29. Itagaki T, Okuda N, Tsunano Y, Kohata H, Nakataki E, Onodera M, et al. Effect of high-flow nasal cannula on thoraco-abdominal synchrony in adult critically ill patients. Respir Care. 2014; 59:70-4. [ Links ]
30. Frizzola M, Miller TL, Rodriguez ME, Zhu Y, Rojas J, Hesek A, et al. High-flow nasal cannula: impact on oxygenation and ventilation in an acute lung injury model. Pediatr Pulmonol. 2011; 46:67-74. [ Links ]
31. Biselli PJ, Kirkness JP, Grote L, Fricke K, Schwartz AR, Smith P, et al. Nasal high-flow therapy reduces work of breathing compared with oxygen during sleep in COPD and smoking controls: a prospective observational study. J Appl Physiol.2017; 122:82-8. [ Links ]
32. Spence C, Buchmann N, Jermy M. Unsteady flow in the nasal cavity with high flow therapy measured by stereoscopic PIV. Exp Fluids. 2012; 52:56979 [ Links ]
33. Möller W, Celik G, Feng S, Bartenstein P, Meyer G, Oliver E, et al. Nasal high flow clears anatomical dead space in upper airway models. J Appl Physiol.2015; 118:1525-32. [ Links ]
34. Chanques G, Constantin JM, Sauter M, Jung B, Sebbane M, Verzilli D, et al. Discomfort associated with underhumidified high-flow oxygen therapy in critically ill patients. Intensive Care Med. 2009; 35:996-1003. [ Links ]
35. Andres D, Thurston N, Brant R, Flemons W, Fofonoff D, Ruttimann A, et al. Randomized double-blind trial of the effects of humidified compared with nonhumidified low flow oxygen therapy on the symptoms of patient. Can Respir J. 1997; 4:76-80. [ Links ]
36. Fontanari P, Burnet H, Zattara-Hartmann MC, Jammes Y. Changes in airway resistance induced by nasal inhalation of cold dry, dry, or moist air in normal individuals. J Appl Physiol .1996; 81:1739-43. [ Links ]
37. Greenspan JS, Wolfson MR, Shaffer TH. Airway responsiveness to low inspired gas temperature in preterm neonates. J Pediatr. 1991; 118:443-5. [ Links ]
38. Rouadi P, Baroody FM, Abbott D, Naureckas E, Solway J, Naclerio RM. A technique to measure the ability of the human nose to warm and humidify air. J Appl Physiol.1999; 87:400-6. [ Links ]
39. Hirsch JA, Tokayer JL, Robinson MJ, Sackner MA. Effects of dry air and subsequent humidification on tracheal mucous velocity in dogs. J Appl Physiol. 1975; 39:242-6. [ Links ]
40. Van Oostdam JC, Walker DC, Knudson K, Dirks P, Dahlby RW, Hogg JC. Effect of breathing dry air on structure and function of airways. J Appl Physiol.1986; 61:312-7. [ Links ]
41. Barbet JP, Chauveau M, Labbé S, Lockhart A. Breathing dry air causes acute epithelial damage and inflammation of the guinea pig trachea. J Appl Physiol.1988; 64:1851-7. [ Links ]
42. Kilgour E, Rankin N, Ryan S, Pack R. Mucociliary function deteriorates in the clinical range of inspired air temperature and humidity. Intensive Care Med. 2004; 30: 1491-4. [ Links ]
43. Chidekel A, Zhu Y, Wang J, Mosko JJ,R odriguez E, Shaffer TH. The effects of gas humidification with high-flow nasal cannula on cultured human airway epithelial cells. Pulm Med. 2012; 2012:380686. [ Links ]
44. Salah B, Dinh Xuan AT, Fouilladieu JL, Lockhart A, Regnard J. Nasal mucociliary transport in healthy subjects is slower when breathing dry air. Eur Respir J.1988; 1:852-5. [ Links ]
45. Chikata Y, Izawa M, Okuda N, Itagaki T, Nakataki E, Onodera M, et al. Humidification performance of two high-flow nasal cannula devices: a bench study. Respir Care. 2014; 59:1186-90. [ Links ]
46. Maggiore SM, Idone FA, Vaschetto R, Festa R, Cataldo A, Antonicelli F, et al. Nasal high-flow versus Venturi mask oxygen therapy after extubation. Effects on oxygenation, comfort, and clinical outcome. Am J Respir Crit Care Med. 2014; 190:282-8. [ Links ]
47. Roca O, Acilu MG, Caralt B, Sacanell J, Masclans JR. Humidified high flow nasal cannula supportive therapy improves outcomes in lung transplant recipients readmitted to the intensive care unit because of acute respiratory failure. Transplantation.2015; 99:1092-8. [ Links ]
48. Rittayamai N, Tscheikuna J, Praphruetkit N, Kijpinyochai S. Use of High-Flow nasal cannula for acute dyspnea and hypoxemia in the Emergency Department. Respir Care. 2015; 60:1377-82. [ Links ]
49. Nilius G, Franke KJ, Domanski U, Rühle KH, Kirkness JP, Schneider H. Effects of nasal insufflation on arterial gas exchange and breathing pattern in patients with chronic obstructive pulmonary disease and hypercapnic respiratory failure. Adv Exp Med Biol.2013; 755:27-34. [ Links ]
50. Sztrymf B, Messika J, Bertrand F, Hurel D, Leon R, Dreyfuss D, et al. Beneficial effects of humidified high flow nasal oxygen in critical care patients: a prospective pilot study. Intensive Care Med.2011; 37:1780-6. [ Links ]
51. Schwabbauer N, Berg B, Blumenstock G, Haap M, Hetzel J, Riessen R. Nasal high-flow oxygen therapy in patients with hypoxic respiratory failure: effect on functional and subjective respiratory parameters compared to conventional oxygen therapy and non-invasive ventilation (NIV). BMC Anesthesiol.2014; 14:66 [ Links ]
52. Wood KE, Flaten AL, Backes WJ. Inspissated secretions: a life-threatening complication of prolonged noninvasive ventilation. Respir Care.2000; 45:491-3. [ Links ]
53. Sztrymf B, Messika J, Mayot T, Lenglet H, Dreyfuss D, Ricard JD. Impact of high-flow nasal cannula oxygen therapy on intensive care unit patients with acute respiratory failure: a prospective observational study. J Crit Care; 27:324.e9-13. [ Links ]
54. Parke RL,McGuinness SP,Eccleston ML. A preliminary randomized controlled trial to assess effectiveness of nasal high-flow oxygen in intensive care patients. Respir Care.2011; 56:265-70. [ Links ]
55. Frat JP, Brugiere B, Ragot S, Chatellier D, Veinstein A, Goudet V, et al. Sequential application of oxygen therapy via high-flow nasal cannula and noninvasive ventilation in acute respiratory failure: an observational pilot study. Respir Care.2015; 60:170-8. [ Links ]
56. Stéphan F, Barrucand B, Petit P, Rézaiguia-Delclaux S, Médard A, Delannoy B et al. High-flow nasal oxygen vs noninvasive positive airway pressure in hypoxemic patients after cardiothoracic surgery: A Randomized Clinical Trial. JAMA.2015; 313:2331-9. [ Links ]
57. Nagata K, Morimoto T, Fujimoto D, Otoshi T, Nakagawa A, Otsuka K, et al. Efficacy of High-Flow Nasal Cannula Therapy in Acute Hypoxemic Respiratory Failure: Decreased Use of Mechanical Ventilation. Respir Care. 2015; 60:1390-6. [ Links ]
58. Frat JP, Thille A, Mercat A, Girault C, Ragot S, Perbet S, et al. High-Flow Oxygen through Nasal Cannula in Acute Hypoxemic Respiratory Failure. N Engl J Med. 2015; 372:2185-96 [ Links ]
59. Rello J, Pérez M, Roca O, Poulakou G, Souto J, Laborda C, et al. High-flow nasal therapy in adults with severe acute respiratory infection: a cohort study in patients with 2009 influenza A/H1N1v. J Crit Care.2012; 27:434-9. [ Links ]
60. Messika J, Ben Ahmed K, Gaudry S, Miguel-Montanes R, Rafat C, Sztrymf B, et al. Use of High-Flow Nasal Cannula Oxygen Therapy in Subjects With ARDS: A 1-Year Observational Study. Respir Care.2015; 60:162-9. [ Links ]
61. Makdee O, Monsomboon A, Surabenjawong U, Praphruetkit N, Chaisirin W, Chakorn T, et al. High-Flow nasal cannula versus conventional oxygen therapy in emergency department patients with cardiogenic pulmonary edema: a randomized controlled trial. Ann Emerg Med.2017; 70:465-72. [ Links ]
62. Carratalá Perales JM, Llorens P, Brouzet B, Albert Jiménez AR, Fernández-Cañadas JM,Carbajosa Dalmau J, et al. High-Flow therapy via nasal cannula in acute heart failure. Rev Esp Cardiol.2011; 64:723-5. [ Links ]
63. Roca O, Pérez-Terán P, Masclans JR, Pérez L, Galve E, Evangelista A, et al. Patients with New York Heart Association class III heart failure may benefit with high flow nasal cannula supportive therapy: high flow nasal cannula in heart failure. J Crit Care.2013; 28:741-6. [ Links ]
64. Messika J, Goutorbe P, Hajage D, Ricard JD. Severe pulmonary embolism managed with high-flow nasal cannula oxygen therapy. Eur J Emerg Med.2017; 24:230-2. [ Links ]
65. Peters SG, Holets SR, Gay PC. High-flow nasal cannula therapy in do-not-intubate patients with hypoxemic respiratory distress. Respir Care.2013; 58:597-600. [ Links ]
66. Lee HY, Rhee CK, Lee JW. Feasibility of high-flow nasal cannula oxygen therapy for acute respiratory failure in patients with hematologic malignancies: A retrospective single-center study. J Crit Care.2015; 30:773-7. [ Links ]
67. Epstein AS, Hartridge-Lambert SK, Ramaker JS, Voigt LP, Portlock CS. Humidified high-flow nasal oxygen utilization in patients with cancer at Memorial Sloan-Kettering Cancer Center. J Palliat Med.201 ; 14:835-9. [ Links ]
68. Mokart D, Geay C, Chow-Chine L, Brun JP, Faucher M, Blache JL,et al. High-flow oxygen therapy in cancer patients with acute respiratory failure. Intensive Care Med.2015; 41:2008-10. [ Links ]
69. Coudroy R, Jamet A, Petua P, Robert R, Frat JP, Thille AW. High-flow nasal cannula oxygen therapy versus noninvasive ventilation in immunocompromised patients with acute respiratory failure: an observational cohort study. Ann Intensive Care.2016; 6:45. [ Links ]
70. Lenglet H, Sztrymf B, Leroy C, Brun P, Dreyfuss D, Ricard JD. Humidified high flow nasal oxygen during respiratory failure in the emergency department: feasibility and efficacy. Respir Care.2012; 57:1873-8. [ Links ]
71. Jones PG, Kamona S, Doran O, Sawtell F, Wilsher M. Randomized controlled trial of humidified high-flow nasal oxygen for acute respiratory distress in the emergency department: The HOT-ER Study. Respir Care.2016; 61:291-9. [ Links ]
72. Pirret AM, Takerei SF, Matheson CL, Kelly M, Strickland W, Harford J. Nasal high flow oxygen therapy in the ward setting: A prospective observational study. Intensive Crit Care Nurs. 2017; S0964-3397: 30082-9. [ Links ]
73. Huang HW, Sun XM, Shi ZH, Chen GQ, Chen L, Friedrich JO, et al. Effect of high-flow nasal cannula oxygen therapy versus conventional oxygen therapy and noninvasive ventilation on reintubation rate in adult patients after extubation: a systematic review and meta-analysis of randomized controlled trials. J Intensive Care Med.2017; 885066617705118. [ Links ]
74. Monro-Somerville T, Sim M, Ruddy J, Vilas M, Gillies MA. The Effect of High-Flow Nasal Cannula Oxygen Therapy on Mortality and Intubation Rate in Acute Respiratory Failure: A Systematic Review and Meta-Analysis. Crit Care Med.2017; 45:e449-e456. [ Links ]
75. Ni YN,Luo J,Yu H,Liu D,Ni Z,Cheng J et al. Can High-flow Nasal Cannula Reduce the Rate of Endotracheal Intubation in Adult Patients With Acute Respiratory Failure Compared With Conventional Oxygen Therapy and Noninvasive Positive Pressure Ventilation?: A Systematic Review and Meta-analysis. Chest.2017 ; 151(4):764-75. [ Links ]
76. Bräunlich J, Beyer D, Mai D, Hammerschmidt S, Seyfarth HJ, Wirtz H. Effects of nasal high flow on ventilation in volunteers, COPD and idiopathic pulmo
nary fibrosis patients. Respiration.2013 ; 85:319-25. [ Links ]
77. Boyer A, Vargas F, Delacre M, Saint-Léger M,C louzeau B, Hilbert G. Prognostic impact of high-flow nasal cannula oxygen supply in an ICU patient with pulmonary fibrosis complicated by acute respiratory failure. Intensive Care Med.2011;37:558-9. [ Links ]
78. Díaz-Lobato S, Folgado MA, Chapa A, Mayoralas Alises S. Efficacy of high-flow oxygen by nasal cannula with active humidification in a patient with acute respiratory failure of neuromuscular origin. Respir Care.2013;58:e164-7. [ Links ]
79. Millar J, Lutton S, O´Connor P. The use of high-flow nasal oxygen therapy in the management of hypercarbic respiratory failure. Ther Adv Respir Dis.2014;8:63-4. [ Links ]
80. Tiruvoipati R, Lewis D, Haji K, Botha J. High-flow nasal oxygen vs high-flow face mask: a randomized crossover trial in extubated patients. J Crit Care.2010;25:463-8. [ Links ]
81. Parke R, McGuinness S, Dixon R, Jull A. Open-label, phase II study of routine high-flow nasal oxygen therapy in cardiac surgical patients. Br J Anaesth.2013;111:925-31. [ Links ]
82. Rittayamai N, Tscheikuna J, Rujiwit P. High-flow nasal cannula versus conventional oxygen therapy after endotracheal extubation: a randomized crossover physiologic study. Respir Care.2014;59:485-90. [ Links ]
83. Corley A,Bull T, Spooner AJ, Barnett AG, Fraser JF. Direct extubation onto high-flow nasal cannulae post-cardiac surgery versus standard treatment in patients with a BMI ≥30: a randomised controlled trial. Intensive Care Med.2015;41:887-94.
84. Futier E, Paugam-Burtz C, Godet T, Khoy-Ear L, Rozencwajg S ,Delay JM, et al. Effect of early postextubation high-flow nasal cannula vs conventional oxygen therapy on hypoxaemia in patients after major abdominal surgery: a French multicentre randomised controlled trial (OPERA). Intensive Care Med.2016;42:1888-98. [ Links ]
85. Hernández G,V aquero C, González P, Subira C, Frutos-Vivar F, Rialp G, et al. Effect of Postextubation High-Flow Nasal Cannula vs Conventional Oxygen Therapy on Reintubation in Low-Risk Patients: A Randomized Clinical Trial. JAMA.2016;315:1354-61. [ Links ]
86. Fernandez R, Subira C, Frutos-Vivar F, Rialp G, Laborda C, Masclans JR, et al. High-flow nasal cannula to prevent postextubation respiratory failure in high-risk non-hypercapnic patients: a randomized multicenter trial. Ann Intensive Care.2017;7:47. [ Links ]
87. Hernández G, Vaquero C, Colinas L, Cuena R, González P, Canabal A, et al. Effect of postextubation high-flow nasal cannula vs noninvasive ventilation on reintubation and postextubation respiratory failure in high-risk patients: a randomized clinical trial. JAMA.2016;316:1565-74. [ Links ]
88. Miguel-Montanes R, Hajage D, Messika J, Bertrand F, Gaudry S, Rafat C, et al. Use of high-flow nasal cannula oxygen therapy to prevent desaturation during tracheal intubation of intensive care patients with mild-to-moderate hypoxemia. Crit Care Med.2015;43:574-83. [ Links ]
89. Lomas C, Roca O, Álvarez A, Masclans JR. Fibroscopy in patients with hypoxemic respiratory insufficiency: Utility of the high-flow nasal cannula. Respir Med CME.2009;2:121–4.
90. Miyagi K, Haranaga S, Higa F, Tateyama M, Fujita J. Implementation of bronchoalveolar lavage using a high-flow nasal cannula in five cases of acute respiratory failure. Respir Investig.2014;52:310-4. [ Links ]
91. Simon M, Braune S, Frings D, Wiontzek AK, Klose H, Kluge S. High-flow nasal cannula oxygen versus non-invasive ventilation in patients with acute hypoxaemic respiratory failure undergoing flexible bronchoscopy--a prospective randomised trial. Crit Care.2014;18:712. [ Links ]
92. Rea H, McAuley S, Jayaram L, Garrett J, Hockey H, Storey L, et al. The clinical utility of long-term humidification therapy in chronic airway disease. Respir Med.2010;104:525-33. [ Links ]
93. Storgaard LH, Frystyck M, Hockey H, Weinreich LM. Number of exacerbations in COPD patients on LTOT treated with a nasal high flow system. Eur Respir J. 2014; 44: 4730. [ Links ]
94. Nilius G, Franke KJ, Domanski U, Rühle KH, Kirkness JP, Schneider H. Effects of nasal insufflation on arterial gas exchange and breathing pattern in patients with chronic obstructive pulmonary disease and hypercapnic respiratory failure. Adv Exp Med Biol.2013;755:27–34.
95. Hegde S, Prodhan P. Serious air leak syndrome complicating high-flow nasal cannula therapy: a report of 3 cases. Pediatrics.2013;131:e939-44. [ Links ]
96. Kang BJ, Koh Y, Lim CM, Huh JW, Baek S, Han M, et al. Failure of high-flow nasal cannula therapy may delay intubation and increase mortality. Intensive Care Med.2015;41:623-32. [ Links ]
97. Hyun Cho W, Ju Yeo H, Hoon Yoon S, Lee S, SooJeon D, Seong Kim Y, et al. High-Flow Nasal Cannula Therapy for Acute Hypoxemic Respiratory Failure in Adults: A Retrospective Analysis. Intern Med.2015;54:2307-13. [ Links ]
Correspondência: Pedro Pires ptrpires@gmail.com
Unidade Funcional Medicina 1.2,
Hospital de São José-Centro Hospitalar de Lisboa Central, EPE
Rua José António Serrano, 1150-199, Lisboa
Conflitos de Interesse: Os autores declaram a inexistência de conflitos de interesse na realização do presente trabalho.
Conflicts of interest: The authors have no conflicts of interest to declare.
Fontes de Financiamento: Não existiram fontes externas de financiamento para a realização deste artigo.
Financing Support: This work has not received any contribution, grant or scholarship.
Direito à Privacidade e Consentimento Informado: Os autores declaram que nenhum dado que permita a identificação do doente aparece neste artigo.
Confidentiality of data: The authors declare that they have followed the protocols of their work center on the publication of data from patients.
Proteção de Seres Humanos e Animais: Os autores declaram que não foram realizadas experiências em seres humanos ou animais.
Protection of human and animal subjects: The authors declare that the procedures followed were in accordance with the regulations of the relevant clinical research ethics committee and with those of the Code of Ethics of the World Medical Association (Declaration of Helsinki).
Recebido: 02/11/2017
Aceite: 02/01/2018














