Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Medicina Interna
versão impressa ISSN 0872-671X
Medicina Interna vol.25 no.4 Lisboa dez. 2018
https://doi.org/10.24950/rspmi/revisao/151/4/2018
ARTIGOS DE REVISÃO / REVIEW ARTICLES
Ecografia à Cabeceira do Doente na Medicina Interna: Uma Mudança de Paradigma na Avaliação do Doente Agudo
Point-Of-Care-Ultrasound in Internal Medicine: A Paradigm Shift in the Evaluation of the Acute Patient
José Mariz1,2, Rafael Silva3, Miguel Romano4, António Gaspar5, António Pedro Gonçalves6, João Paulo Silva1, Marco António Carvalho-Filho7,8, Thiago Santos7, Jorge Teixeira1
1Serviço de Urgência do Hospital de Braga; Braga, Portugal
2Escola de Medicina da Universidade do Minho; Braga, Portugal
3Serviço de Medicina Interna, Centro Hospitalar e Universitário de Coimbra, Coimbra Portugal
4Serviço de Medicina Interna, Hospital Santa Luzia, Viana do Castelo, Portugal
5Serviço de Cardiologia do Hospital de Braga; Braga, Portugal
6Serviço de Urgência, Centro Hospitalar do Porto, Porto, Portugal
7Faculdade de Ciências Médicas, Unicamp, Campinas,Brasil
8Center for Education Development and Research in Health Professions - University of Groningen, Groningen, Holanda
RESUMO
A ecografia à cabeceira do doente apresenta-se como “o quinto pilar do exame físico”, juntamente com a inspeção, percussão, palpação e auscultação. Após o início de sua utilização nos anos 80 para avaliação do trauma abdominal, tornou-se prática diária na avaliação do doente crítico, tanto nas Unidades de Cuidados Intensivos quanto nos Serviços de Urgência, sendo, hoje, componente fundamental de diversos protocolos clínicos. Neste artigo, pretende-se mostrar as aplicações estabelecidas da ecografia à cabeceira do doente na avaliação de situações clínicas agudas, com foco nas implicações para a prática do médico internista. Pretende-se também deixar patente o impacto que a ecografia pode e deve ter na educação médica geral. Os autores têm a forte convicção que as competências aqui apresentadas farão parte, muito em breve, do núcleo de competências básicas de qualquer médico internista a exercer em Portugal.
Palavras-chave: : Doença Aguda; Ecografia; Medicina Interna/ educação; Serviço de Urgência Hospitalar
ABSTRACT
The point of care ultrasound (POCUS) presents itself as the fifth pillar of the physical examination, pairing with inspection, percussion, palpation and auscultation. After the initial usage, in the beginning of the 80’s for the evaluation of abdominal trauma, the POCUS became a daily practice in the critical patient evaluation, either in Critical Care Units or in Emergency Departments, assuming, nowadays, an important role of a large variety of clinical protocols. In this review, the authors propose to revise the established applications of POCUS and point out its practical consequences in medical daily routines as well as reaffirm the importance that it can and must have in pre- and post-graduated medical education. The authors strongly believe that the competences hereby presented will, shortly, be included in the core competences of internal medicine.
Keywords: Acute Disease; Emergency Service, Hospital; Internal Medicine/education; Point-of-Care System; Ultrasonography
Introdução
A ecografia à cabeceira do doente (EcoCD, o equivalente ao acrónimo internacional POCUS - point-of-care ultrasonography) introduz algo de novo e poderoso na forma de abordar o doente, funcionando como uma ferramenta que aumenta as capacidades diagnósticas do exame físico tradicional.1,2
A EcoCD é, assim, como que o quinto pilar do exame físico, juntamente com a inspeção, palpação, percussão e auscultação.2 A utilização da ecografia por médicos não imagiologistas, não cardiologistas ou não ginecologistas/ obstetras, começou nos finais dos anos 80 e início dos anos 90, sobretudo por cirurgiões gerais na avaliação do trauma abdominal. Por essa altura foi desenvolvido o protocolo Focused Assessement using Sonography in Trauma (FAST), método rápido e simples de pesquisa de hemorragia intra-abdominal3 e que posteriormente evoluiu para o extendend Focused Assessment using Sonography in Trauma (eFAST), que inclui a avaliação torácica para a deteção de pneumotórax.4 Desde então, mais de 20 especialidades desenvolveram orientações para uso da EcoCD no diagnóstico e tratamento de diversas condições patológicas, processo que decorreu a par da inovação tecnológica que introduziu novos aparelhos de ecografia mais portáteis e mais baratos.2,5
O uso da EcoCD surge assim neste contexto, permitindo tornar os cuidados médicos melhores, mais rápidos e mais seguros.6,7 Não se trata de romper com a metodologia tradicional, baseada na obtenção da história clínica e exame objetivo, uma vez que a EcoCD opera a partir da informação obtida nesses dois momentos fulcrais da relação médico-doente.8 Na medicina interna, isto reflete-se desde o apoio a procedimentos invasivos, ao processo do diagnóstico diferencial da dispneia aguda e do choque indiferenciado ou no tratamento da insuficiência cardíaca ou do doente séptico, para apenas referir alguns exemplos.9 Neste artigo, iremos focar as aplicações da EcoCD que estão relativamente bem estabelecidas na abordagem do doente agudo e que poderão ser da utilidade do médico internista. Realçamos também os aspetos relacionados com o impacto da EcoCD na educação médica, uma vez que não entendemos esta revolução sem a compreender em todo o seu espectro de aprendizagem. Não focaremos todos os aspetos técnicos da EcoCD, uma vez que estes devem ser propriamente aprendidos em cursos práticos e no estudo de manuais relevantes. Trata-se de uma revisão narrativa, baseada na própria experiência dos autores que aplicam diariamente a EcoCD na avaliação dos seus doentes, apoiando-se sempre que possível na medicina baseada na evidência.
1. Aplicações por Sistema Orgânico
1.1 Sistema Respiratório
ECOGRAFIA PULMONAR
A avaliação ecográfica do pulmão é das áreas da EcoCD mais importantes na avaliação do doente agudo. O termo “ecografia pulmonar” é o termo mais frequentemente aceite, muito embora os termos “ecografia torácica” ou “ecografia pleural” se encontrem na literatura e sejam equivalentes.10 O uso da ecografia pulmonar data de 1986, com trabalhos pioneiros na deteção de pneumotórax no cavalo11 e, desde aí, a sua aplicação em humanos, nomeadamente no doente agudo, tem sido evidenciada em inúmeros estudos científicos.12-16 O princípio sobre o qual a ecografia pulmonar foi construída assenta na interpretação de diferentes artefactos ecográficos de forma a construir diferentes padrões que nos poderão responder a questões clínicas prementes. Mas foi graças, sobretudo, aos trabalhos de Lichtenstein que a ecografia pulmonar teve o seu grande impulso, demonstrando-se mais precisa do que a auscultação pulmonar ou a telerradiografia do tórax na avaliação do edema pulmonar, da consolidação ou do derrame pleural no doente crítico.17,18 A abordagem básica consiste na identificação do deslizamento da pleura parietal sobre a pleura visceral, o chamado deslizamento pleural. Em seguida, é necessário saber identificar os artefactos mais comuns, reconhecendo as linhas A e B, o ponto alvéolo-pleural póstero-lateral (PLAP), o ponto pulmonar e a consolidação,19-22 os quais permitem enquadrar os achados ecográficos em padrões clínicos que em seguida revemos sumariamente.
Linhas A e deslizamento pleural. A ecografia pulmonar tem sido um exame complementar subaproveitado na patologia torácica, fruto da crença inicial num valor limitado dos ultrassons no pulmão devido à interposição de conteúdo gasoso.23 No entanto, a partir da interrogação de vários pontos pulmonares, semelhantes aos pontos da auscultação pulmonar, é possível gerar um mapa de artefactos da linha pleural que tem correlação com patologia pulmonar. No pulmão normal ventilado, a única estrutura detetada é a pleura, visualizada como uma linha hiperecóica horizontal, sendo produzido um artefacto de reverberação da linha pleural, representado pela repetição equidistante dessa linha hiperecóica, as chamadas linhas A (Fig 1a). A presença das linhas A por si só não significa que exista ventilação nessa área interrogada. Na ventilação, os folhetos da pleura têm um movimento síncrono com o ciclo respiratório e este movimento pode ser detetado com a ecografia, denominado como deslizamento pleural.16 Assim, a combinação da presença linhas A com deslizamento pleural, representa um sinal de conteúdo normal (ou excessivo) de ar no espaço alveolar, o designado padrão A.20 O deslizamento pleural também pode ser pesquisado através do modo M. Na sua presença, observa-se a zona superior da imagem, com linhas horizontais, correspondentes aos tecidos sub-cutâneos sem movimento e, a partir da linha pleural, um padrão granulado devido aos artefactos provocados pelo deslizamento pleural, chamado o sinal da praia (Fig 1b). Por outro lado, a presença de linhas A na ausência de deslizamento pleural é patológico, sendo o pneumotórax a patologia paradigmática com este perfil ecográfico. Na ausência de deslizamento pleural, todas as estruturas estão estáticas e, logo, toda a imagem demonstra linhas horizontais, visualizado em modo M como o sinal de estratosfera.22 É importante ressalvar que o perfil de linhas A sem deslizamento pleural não é exclusivo de pneumotórax, sendo que a pleurodese (quer se trate de pleurodese química, estados infeciosos e inflamatórios ou fibrose pulmonar) e a perda de volume pulmonar (por exemplo, na atelectasia completa, na obstrução por muco ou na pneumectomia) também cursam com ausência de deslizamento pleural.24 A ausência de deslizamento pleural não é assim específica para pneumotórax, mas a presença de deslizamento pleural exclui em definitivo o pneumotórax no local da interrogação ecográfica.22 Existe ainda um sinal muito específico para a presença de pneumotórax, o chamado ponto pulmonar, que corresponde ao ponto de transição na margem do pneumotórax entre a pleura deslizante e a pleura não deslizante. No entanto, na presença de pneumotórax de grande volume o pulmão encontra-se inteiramente colapsado não existindo uma margem de transição visualizável.25
Linhas B e edema pulmonar. A espessura dos septos interlobulares subpleurais no pulmão normal está abaixo do limite de resolução ecográfica, motivo pelo qual o padrão A é formado. No entanto, na presença de edema alveolar ou no pulmão inflamatório agudo, os septos encontram-se espessados pela acumulação de fluidos, quer por aumento da pressão hidrostática ou da permeabilidade capilar. Estes septos espessados permitem a propagação do ultrassom criando um artefacto que é denominado como linhas B (Fig 1c). A presença de 3 ou mais linhas B numa janela ecográfica é considerada patológica.22 Quando as linhas B surgem de forma aguda e bilateralmente, constituem o chamado padrão B, sendo a acumulação de fluidos a causa mais comum. Por essa razão, a sua presença é denominada muitas vezes como “pulmão húmido”. É importante realçar que a presença de linhas B com significado patológico pode dever-se a outras entidades, tais como a fibrose pulmonar, a doença pulmonar intersticial ou sequelas de infeções antigas. Adicionalmente, em doentes com insuficiência cardíaca descompensada, doença renal terminal ou sépsis, a contabilização das linhas B por campo ecográfico através da repetição da EcoCD permite a monitorização da congestão pulmonar.26,27 Por outro lado, como se entende pelo seu significado biológico, a presença de linhas B exclui pneumotórax nessa localização.
Consolidação pulmonar. Quando os alvéolos se encontram preenchidos por fluido e detritos ou se encontram colapsados, como na pneumonia ou na atelectasia, criam um meio favorável à propagação do ultrassom permitindo a visualização do pulmão. O parênquima do pulmão ganha uma ecogenicidade semelhante ao parênquima de hepatização ou padrão C. No entanto, o padrão C ou de “consolidação alveolar” é descritivo e não diagnóstico, uma vez que múltiplas entidades podem corresponder a este padrão.28 É importante assim identificar outros sinais ecográficos que permitam diferenciar entre consolidação pneumónica, atelectasia compressiva e atelectasia obstrutiva.29,30
Derrame pleural. A ecografia pulmonar permite também avaliar rapidamente a presença de derrame pleural simples ou complexo, podendo auxiliar a sua punção em melhores condições de segurança, como iremos focar mais à frente neste artigo. No doente em decúbito, deve ser cuidadosamente avaliado o interface entre diafragma e pulmão, logo acima do fígado e do baço, com atenção para não confundir derrame pleural com líquido livre peritoneal.16,19,31 Daí ser importante identificar o PLAP, que corresponde à área mais posteriormente acessível nos doentes em decúbito, permitindo a localização de líquido livre independentemente do seu volume.32 A observação de derrame pleural é geralmente evidente – e marcante para principiantes – verificando-se uma área anecóica entre o tecido mole e a linha pleural (Fig 1d).
Em resumo, os principais padrões e achados da ecografia pulmonar no doente com dispneia aguda, encontram-se descritos no protocolo BLUE (Bedside Lung Ultrasound in Emergency), elaborado por Lichtenstein e colaboradores.22 Este protocolo, mostrou uma sensibilidade de 97% e especificidade de 95% para o edema pulmonar cardiogénico, uma sensibilidade de 89% e uma especificidade de 97% para a doença pulmonar obstrutiva crónica (DPOC) /exacerbação da asma, uma sensibilidade de 89% e especificidade de 94% para a pneumonia, e uma sensibilidade de 88% e especificidade de 100% para o pneumotórax.22,33 Na avaliação do doente com dispneia aguda, o padrão de linhas B permite a diferenciação entre causa cardiogénica ou respiratória, uma vez que a exacerbação da DPOC, a embolia pulmonar, a pneumonia, o pneumotórax, produzem um padrão ecográfico de “não-B”.20,34 A correta interpretação dos artefactos descrita por Lichtenstein melhora assim o diagnóstico diferencial da dispneia no doente agudo. Resumimos a nomenclatura utilizada por este autor em contexto clínico na Tabela 1.
1.2 Sistema Cardiovascular
ECOCARDIOGRAFIA
A ecocardiografia constitui um método de eleição para a avaliação à cabeceira do doente com falência circulatória. O ecocardiograma permite uma avaliação cardíaca anatómica e funcional, a qual pode incluir uma avaliação hemodinâmica não invasiva.
No doente hemodinamicamente instável existe potencial de evolução para choque e morte em poucas horas. Assim, devem ser utilizados métodos de diagnóstico céleres, precisos e reprodutíveis, de forma a rapidamente instituir as atitudes terapêuticas adequadas.
Através de uma avaliação cardíaca anatómica e funcional dirigida, o ecocardiograma pode fornecer dados de extrema importância para a compreensão dos mecanismos subjacentes à instabilidade hemodinâmica de determinado doente, ou mesmo em contexto de pós-paragem cardiorrespiratória, permitindo assim a instituição imediata das medidas terapêuticas apropriadas. Mais especificamente, e no contexto do doente agudo, é possível obter sinais diretos ou indiretos de síndrome coronário, insuficiência cardíaca, tromboembolismo pulmonar, disseção aórtica, tamponamento pericárdico, entre outros.35,36
Foram os médicos intensivistas que cedo reconheceram as potencialidades do ecocardiograma com estudo Doppler (eco Doppler) para a abordagem inicial do doente em falência circulatória.37 À avaliação anatómica e funcional classicamente realizada, foi acrescentada a avaliação hemodinâmica com o estudo Doppler, nomeadamente cálculo do débito cardíaco, estimativa da pressão venosa central, cálculo das resistências vasculares periféricas e estimativa das pressões de enchimento do ventrículo esquerdo. Ao longo das últimas décadas, o eco Doppler tornou-se uma ferramenta cada vez mais disseminada nos cuidados intensivos na abordagem do doente em choque.35-39
Não cabe na extensão deste artigo o detalhe de todas as potencialidades do exame ecocardiográfico à cabeceira do doente, remetendo para esse fim a leitura das referências bibliográficas.40,41 Não obstante, a competência para realização de ecocardiograma é habitualmente separada em três níveis de experiência, reconhecendo-se ainda um nível prévio, mais básico, de ecocardiografia de emergência.42 Esta última remete-nos para a identificação de achados de fácil visualização, enquadrando-se o exame no despiste de diagnósticos específicos como o tamponamento cardíaco ou embolia pulmonar. A própria avaliação da função cardíaca não necessita ser exata ou quantitativa, estando perfeitamente validada uma avaliação qualitativa de tipo “eye-ball”.43 A ecocardiografia de emergência pode assim configurar-se como uma competência básica do médico internista, integrada nos protocolos de avaliação inicial dos doentes críticos, nomeadamente em contexto de suporte avançado de vida. No entanto, a realização de exames mais exaustivos requer níveis superiores de competência. A Fig 2 sumariza os diferentes níveis de competência em ecocardiografia.
VEIA CAVA INFERIOR
A EcoCD da veia cava inferior (VCI) permite uma determinação rápida e não invasiva da pressão na aurícula direita que pode ajudar na avaliação do estado volémico do doente agudo, bem como na avaliação da resposta a volume. A curva de aprendizagem da avaliação ecográfica da VCI é bastante rápida.44 Tecnicamente, são avaliados estaticamente o seu maior diâmetro e dinamicamente a sua variabilidade no ciclo respiratório (variabilidade respiratória da VCI, vrVCI).45 Por sua vez, classifica-se a vrVCI em mínima (pletórica), normal, ou inteiramente colapsável,46 usando como ponto de corte uma vrVCI normal > 50%. Para o parâmetro estático, usa-se como ponto de corte um diâmetro da VCI normal <= a 2,1 cm. Devido a grande variabilidade interpessoal do diâmetro estático da VCI foram criados vários índices que permitem correlacionar a variabilidade respiratória com o volume intravascular. O índice com maior evidência e mais utilizado no doente em choque e em ventilação espontânea é o índice de colapsabilidade da VCI (IcVCI): IcVCI (%) = [(diâmetro máximo expiratório – diâmetro mínimo inspiratório)/(diâmetro máximo expiratório)]x100.
Importa realçar que este índice tem maior utilidade nos extremos, com valores de IcVCI < 25% associado a fraca resposta a fluidos e valores de IcVCI >75% associado a estados de depleção de volume.45 A vrVCI pode ser avaliada em modo M ao nível imediatamente caudal da veia hepática (cerca de 3 cm distal à aurícula direita), e daí ser calculado o IcVCI, como ilustramos na Fig 3.
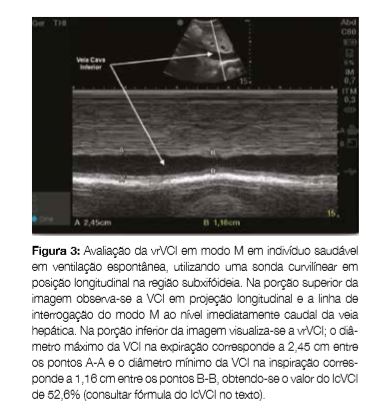
O maior benefício da avaliação da VCI reside na correlação com os achados pulmonares e cardíacos. Por exemplo, a ausência de dilatação da VCI na presença de derrame pericárdico no doente agudo, pode rapidamente excluir o tamponamento cardíaco como causa do choque.45,47 Por outro lado, uma VCI colapsada em paciente com contratilidade cardíaca normal e linhas B pulmonares difusas suporta o diagnóstico de edema pulmonar inflamatório.
O uso da avaliação ecográfica da VCI no contexto clínico certo, particularmente o relacionado com sala de emergência ou serviço de urgência com grande demanda de doentes, é útil, rápido e que nos seus extremos pode ser um potente auxílio na avaliação e decisão de tratamento do doente agudo. Não obstante, e independentemente do estado ventilatório do doente (por exemplo, existem dúvidas do seu valor no doente sob ventilação não invasiva),48 a avaliação ecográfica da VCI deve ser propriamente contextualizada para cada doente específico com a avaliação da ecografia pulmonar e cardíaca.
AORTA ABDOMINAL
A ecografia da aorta abdominal é o método de rastreio por excelência do aneurisma da aorta abdominal, devido a permitir uma medição precisa do seu diâmetro e a deteção de lesões da parede como trombos ou placas, e ainda por não envolver radiações, estar largamente disponível e ser de relativo baixo custo.49 A ecografia da aorta abdominal tem demonstrado uma elevada sensibilidade (97,5% - 100%) e especificidade (94,1% - 100%) para a deteção de aneurisma.50,51 No doente agudo, a patologia aórtica deve ser considerada sempre que este se apresente com desconforto abdominal, especialmente em doentes com fatores de risco, e com os sinais e sintomas característicos (dor lombar, hipotensão indiferenciada, massa abdominal pulsátil). A técnica de execução tem uma curva de aprendizagem bastante rápida, sendo que na maior parte dos casos em que há impossibilidade de observar a aorta abdominal isto se deve a fatores relacionados com o biótipo do doente e interposição gasosa das ansas intestinais.
AVALIAÇÃO DE LÍQUIDO LIVRE ABDOMINAL
No doente agudo não traumatizado, a presença de líquido livre peritoneal pode corresponder a vários diagnósticos relevantes, tais como insuficiência cardíaca congestiva, rutura de aorta abdominal, gravidez ectópica, doença hepática crónica descompensada, pancreatite, rutura de víscera oca ou hemorragia intra-abdominal espontânea, quadros estes que habitualmente causam ou condicionam descompensação cardiovascular/hemodinâmica. Esta análise consiste na avaliação de espaços potenciais nos quadrantes abdominais superiores à esquerda e à direita, bem como na pélvis. Locais específicos incluem o espaço entre o fígado e o rim (espaço hepatorrenal ou loca de Morrison), o espaço à volta do baço (espaço esplenorrenal) e a região posterior à bexiga (espaço reto-vesical/reto-vaginal ou fundo-de-saco de Douglas). Uma área anecóica em cada um destes espaços representa líquido livre intraperitoneal.52
AVALIAÇÃO DE TROMBOSE VENOSA PROFUNDA NOS MEMBROS INFERIORES
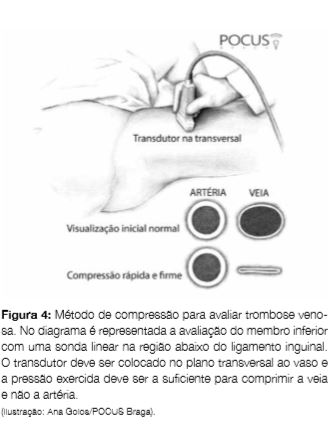
A deteção de trombose venosa profunda (TVP) dos membros inferiores (MI) com ecografia pode ser realizada com segurança por médicos não imagiologistas em contexto de urgência.53,54 Apresenta uma curva de aprendizagem rápida, devendo ser realizada pelo método de compressão (Fig 4) em duas regiões anatómicas, a saber, região inguinal (veia femoral) e fossa poplítea (veia poplítea), com ou sem a aplicação de Doppler.55 Ultimamente, têm surgido estudos que sugerem uma avaliação tripla, que integre a avaliação cardíaca, pulmonar e do sistema venoso dos MI de modo a melhorar o desempenho diagnóstico da embolia pulmonar.56
1.3 Sistema Genitourinário
ECOGRAFIA ABDOMINOPÉLVICA
As principais indicações para aplicação da EcoCD face a problemas do foro genitourinário na avaliação do doente agudo são a identificação de uropatia obstrutiva e de retenção urinária, na presença de história clínica e sinais clínicos que apontem para estas condições. A hidronefrose é a principal alteração a ser evidenciada na obstrução urinária.9 Assim, a EcoCD renal pode estreitar o diagnóstico diferencial em doentes que se apresentem com lesão renal, em anúria ou em algumas infeções do trato urinário.57 Apresenta extrema utilidade na avaliação da dor no flanco, estando incorporada em diversos algoritmos de avaliação na suspeita de cólica renal.58 No entanto, a visualização ecográfica dos ureteres apenas é parcial e cálculos do ureter médio são dificilmente visíveis.9
2. Técnicas Invasivas em Medicina Interna
2.1 Cateter Venoso Central
A utilização da ecografia na colocação de cateteres venosos centrais (CVC) na veia jugular interna (VJI), veia femoral (VF) e veia subclávia (VS) surge como resposta às limitações das técnicas tradicionais, que se baseiam na palpação do pulso arterial e nas relações anatómicas subjacentes,59 uma vez que 20% dos doentes apresentam variações anatómicas e uma percentagem relevante de doentes críticos e oncológicos apresentam trombose venosa. Estas limitações da técnica tradicional são facilmente superadas pela punção eco-guiada,60 permitindo assim diminuir o número de complicações (punção arterial, hematoma e trombose luminal). Uma recente revisão sistemática da Cochrane avaliou a punção eco-guiada versus por referências anatómicas nas três localizações: IVJ, VF e VS.61 A punção eco-guiada da VJI em comparação com técnica por referências anatómicas mostrou diminuir o número de complicações (4% vs 13,5%) e taxa de sucesso (97,6% vs 87,6%). Estes dados permitiram afirmar que existe beneficio na segurança e na taxa de sucesso na punção eco-guiada da VJI.61 Tais achados vão de encontro às linhas orientadoras de várias Sociedades Internacionais como a American College of Surgery, American Society of Anesthesiology e a American College of Critical Care62 que consideram a colocação de CVC eco-guiado na VJI, hoje em dia, a técnica gold standard. Já os resultados em outras localizações (VF e VS), apesar de demonstrarem benefícios tanto no número de complicações como na taxa de sucesso, não foram suficientemente robustos para os autores afirmarem que a técnica eco-guiada deveria ser adotada como gold standard em detrimento da técnica clássica.62
Para a colocação de CVC eco-guiado é sugerido uma abordagem sistemática de seis passos59:
1 – Estudo da anatomia local e identificação da veia desejada;
2 – Excluir a presença de trombo endoluminal, verificando a compressibilidade do vaso;
3 – Punção venosa eco-guiada em tempo real;
4 – Confirmar a posição da agulha no lúmen da veia;
5 – Confirmar a posição do fio-guia no lúmen da veia;
6 – Confirmar a posição do cateter no lúmen da veia.
A esta abordagem sistemática devem também estar associados rigorosos cuidados de assepsia como a utilização de manga e gel esterilizados em conjunto com as medidas já previamente adotadas na colocação tradicional de um CVC. Apesar de um perfil de segurança superior, a técnica eco-guiada apresenta certas complicações que devemos conhecer e identificar como o hematoma cutâneo, pneumotórax, hemotórax, infeção do cateter e punção arterial.63 No entanto, mesmo nestes casos, a EcoCD permite identificar as complicações da punção muito mais rapidamente. Portanto, tendo em conta as vantagens anteriormente referidas, será de assumir que a colocação de CVC eco-guiados passe rapidamente a ser a técnica de eleição para o internista obter de forma mais segura e eficaz um acesso venoso central.
2.2 Toracocentese, Paracentese e Punção Lombar
A toracocentese guiada por ultrassonografia é um dos procedimentos em que há mais experiência e resultados positivos. A ecografia torácica é hoje em dia o exame auxiliar de diagnóstico de excelência no que toca a abordagem do derrame pleural uma vez que é mais sensível que a radiografia de tórax64 e, apesar de ligeiramente menos sensível que a tomografia computorizada de tórax, pode ser facilmente realizado à cabeceira do doente e sem exposição a radiação ionizante.65 A adoção desta técnica permite reduzir o número de pneumotórax iatrogénico em comparação com a técnica tradicional (3% vs. 18%)66 e aumentar o sucesso na realização do procedimento diminuindo em muito o número de toracocenteses “secas”.67
A realização da toracocentese eco-guiada deve obedecer a regras simples como garantir a assepsia durante todo o procedimento e exclusão das contraindicações (infeção do local de punção, discrasia sanguínea). Deve ser utilizada uma sonda de baixa frequência como a curvilínea ou sectorial e, numa primeira avaliação, devemos observar o derrame na sua totalidade, de forma a classificar como livre ou loculado.68 Depois, deverá ser escolhido o local onde o derrame seja mais volumoso, devendo pelo menos ter 1 cm de espessura no ecrã e ser possível observar o diafragma no campo ecográfico para se proceder com segurança.69
Para além da toracocentese existem outros procedimentos que são cada vez mais realizados com orientação por ecografia como a paracentese e a punção lombar (PL). No caso da paracentese eco-guiada, a grande vantagem é permitir abordar derrames de menor volume ou loculados ao mesmo tempo que aumenta a taxa de sucesso70 e diminui o risco de complicações (hemorragia e perfuração intestinal).71
Já na PL, a realização eco-guiada prende-se com o fato da técnica com base em referências anatómicas estar associada a uma elevada taxa de insucesso especialmente em doentes obesos72 e a um número elevado de punções traumáticas.73 A utilização da ultrassonografia permite vencer essas limitações ao estudar a sono-anatomia do doente previamente à realização da PL, permitindo assim saber de antemão qual é a profundidade do ligamento amarelo e a correta localização dos espaços inter-espinhosos. Os benefícios da utilização da ultrassonografia na PL foram comprovados por Lee et al que mostraram uma taxa de sucesso de 100% na PL eco-guiada versus os 83% da PL guiada por referências anatómicas.74 Perante todos os fatos anteriormente enunciados, o internista vê-se hoje em dia confrontado com a necessidade de realizar, sempre que possível, grande parte dos procedimentos com o auxílio da ultrassonografia. Só assim estará a realizar um procedimento mais seguro para o doente e com uma maior taxa de sucesso.
3. Protocolos Específicos no Doente Agudo
Vários protocolos têm sido desenvolvidos para a avaliação do doente agudo não traumatizado, especialmente nas situações de choque indiferenciado e paragem cardiorrespiratória.22,52,75-78 De entre eles, salientamos o protocolo RUSH (Rapid Ultrasound for Shockand Hypotension),52 o qual baseia a avaliação em 3 aspetos fundamentais da fisiologia do doente em descompensação cardiocirculatória, simplificado na avaliação da “bomba”, do “tanque” e dos “tubos”.79 Neste protocolo, procede-se à obtenção de janelas ecográficas do coração, VCI, espaços hepatorrenal esplenorrenal e pélvica (com visualização da bexiga), pleura e aorta. Resumidamente, no doente agudo que não se apresente em paragem cardiorrespiratória, são obtidas janelas cardíacas nos vários eixos de modo a aferir a contractilidade global, o tamanho relativo dos ventrículos direito e esquerdo, e a presença de derrame pericárdico. A VCI é avaliada de modo a aferir a tolerância a fluidos. A ecografia pulmonar avalia a presença de pneumotórax, derrame pleural e, juntamente com avaliação do espaço hepatorrenal, esplenorrenal e pélvico, é avaliada a presença de líquido livre abdominal. A aorta abdominal é avaliada em toda a sua extensão para despistar o aneurisma e a dissecção. O exame pode ser completado em 2 minutos. Adicionalmente, e no contexto clínico apropriado, outras janelas podem ser adicionadas, como por exemplo, pesquisa de TVP nos MI na dispneia aguda ou presença de hidronefrose no doente séptico com dor no flanco. Na Fig 4 ilustramos as principais janelas ecográficas do protocolo RUSH.
4. Papel da Ecografia na Educação Médica
A EcoCD é uma realidade internacional e algumas escolas médicas de vanguarda criam oportunidades para que seus alunos desenvolvam familiaridade com esta técnica desde as cadeiras básicas, passando pela semiologia e propedêutica até utilização clínica da ecografia pelo estudante em casos clínicos reais nas cadeiras da medicina interna, cirurgia e emergência.80,81 Os impactos positivos desta inovação podem ser divididos nos seguintes aspetos:
- Compreensão fisiológica – para uma geração de estudantes que foi criada e estudou à frente de um ecrã, o ecógrafo é um facilitador da compreensão de conceitos fisiológicos que, se antes eram imaginados, agora podem ser diretamente visualizados. A inspiração profunda aumenta o retorno venoso para o coração direito pois a pressão intratorácica sofre uma queda relativa – agora o estudante consegue ver a variação do diâmetro da VCI, a distensão da aurícula direita e o aumento correspondente do débito do ventrículo direito. O ciclo cardíaco desce do etéreo para o concreto quando visualizado em todas as suas fases, curvas e movimentos ao vivo e a cores, com apoio do efeito Doppler (vermelho para o que vai e azul para o que vem).
- Compreensão fisiopatológica – sempre foi difícil para um estudante principiante integrar todas as modificações associadas à presença da doença. Pois agora o estudante consegue ver como na insuficiência cardíaca a contractilidade cardíaca está diminuída, as pressões de enchimento estão aumentadas e os líquidos se acumulam nas cavidades. Tudo isto pode ser visto em detalhe e, ao mesmo tempo, facilitando a integração dos achados numa narrativa clínica coerente. O diagnóstico diferencial dos estados de insuficiência respiratória é um exemplo de como esta técnica pode aproximar aprendizes a médicos mais experientes, ajudando a garantir a segurança dos doentes. Ao responder às perguntas pulmão seco versus pulmão húmido, contractilidade normal versus diminuída, enchimento ventricular normal versus baixo, com o ecógrafo, o aluno de medicina integra e conclui com muito mais facilidade.
- Motivação – O campo da psicologia cognitiva ensina-nos que a nossa motivação intrínseca para aprender depende da satisfação de três necessidades inerentes ao ser humano: autonomia, competência e necessidade de estabelecer relações.82 Deste modo, a EcoCD atua nestas três dimensões. Como a curva de aprendizagem é rápida, em pouco tempo os alunos conseguem usar o aparelho de forma independente. Aprendemos a analisar a ecografia mais rapidamente do que aprendemos a ouvir com o estetoscópio. Esta autonomia vem acompanhada pela sensação de competência quando o estudante se consegue equiparar precocemente em termos de precisão diagnóstica e em procedimentos a alunos mais experientes e jovens médicos. Finalmente, por ser à cabeceira do doente, a ecografia permite ao estudante de medicina abrir um canal de comunicação com o seu doente, e compartilhar com o maior interessado os componentes da sua patologia. O efeito colateral, mas positivo, é um doente com maior compreensão do que acontece consigo.
Alguns médicos mais conservadores sentirão medo de perder algo com a chegada da EcoCD. Esta pode despertar em alguns um ressentimento em relação à tecnologia, como se o percebido afastamento dos médicos em relação aos seus doentes fosse um subproduto do desenvolvimento tecnológico. Some-se a isso uma tendência conservadora da nossa classe em insistir em apresentar uma reação inicial aversiva à novidade, como se esta representasse uma ameaça ao nosso estilo tradicional e comprovadamente eficiente de fazer as coisas. Para os mais céticos podemos compartilhar a experiência da Universidade Estadual de Campinas, em que a EcoCD foi incorporada no curso de graduação. Os alunos passam muito mais tempo com os seus doentes, estão mais interessados em aprender os detalhes do exame físico e compartilham connosco um melhor entendimento da situação clínica dos doentes sob os seus cuidados (resultados apresentados no congresso anual da An International Association for Medical Education - AMEE - de 2015). Adicionalmente, em Portugal, e no âmbito da formação médica pós-graduada, os autores deste artigo possuem uma forte experiência na formação em EcoCD a médicos de várias especialidades, maioritariamente internistas. Com a realização dos nossos cursos práticos com forte componente hands-on demonstramos ganhos obtidos em conhecimento e na confiança nos participantes. Houve um desenvolvimento relevante de conhecimento através das aulas didáticas e da simulação, que foi sustentada com o treino em contexto real. No entanto, a aplicação da ecografia foi inferior ao esperado por escassez ou indisponibilidade de equipamentos (apresentação oral no 24º Congresso Nacional de Medicina Interna).
5.Conclusão
Os autores têm a forte convicção que as competências aqui apresentadas constituirão muito em breve o núcleo de competências básicas de qualquer médico internista a exercer em Portugal. A abordagem com a EcoCD não desvirtua, na opinião dos autores, a essência da medicina interna, a qual muito depende do contacto com o doente como um todo. Antes pelo contrário, entendemos que a EcoCD potencia a aproximação ao doente e torna o exame físico tradicional mais preciso e rigoroso. Muito embora apenas tenhamos focado os aspetos da EcoCD com maior implicação nos quadros de descompensação aguda, esta abordagem fornece os blocos básicos para que o internista possa construir a sua própria “casa” onde albergar novas aplicações. A introdução do novo paradigma de segurança em procedimentos invasivos é também salientada pelo uso da EcoCD. A educação médica é essencial para manter as competências atualizadas, sendo fundamental a incorporação do ensino da EcoCD na pré-graduação médica. Na nossa opinião, esta mudança veio para ficar.
Agradecimentos
Este artigo é o reflexo de um enorme trabalho de equipa, pelo que não podemos deixar de referir a contribuição, enquanto ainda estudantes de medicina na Escola de Medicina da Universidade do Minho, do Gil Sequeira, do Nuno Carvalho e do José Diogo Martins. Em particular, o José Diogo Martins foi o grande responsável pelo estudo do impacto da formação em EcoCD na pós-graduação médica, cujos resultados principais foram apresentados no 24º Congresso Nacional de Medicina Interna da Sociedade Portuguesa de Medicina Interna.
Referências
1. Kugler J. Price and the evolution of the physical examination. JAMA Cardiol.2018;3: 351. doi: 10.1001/jamacardio.2018.0002. [ Links ]
2. Narula J, Chandrashekhar Y, Braunwald E. Time to add a fifth pillar to bedside physical examination. JAMA Cardiol. 2018; 3: 346-50. doi: 10.1001/jamacardio.2018.0001. [ Links ]
3. Chen L, Malek T. Point-of-care ultrasonography in emergency and critical care medicine. Crit Care Nurs Q. 2018; 41: 94-101. doi: 10.1097/ CNQ.0000000000000190. [ Links ]
4. Kirkpatrick AW, Sirois M, Laupland KB Liu D, Rowan K, Ball CD, et al. Hand-held thoracic sonography for detecting post-traumatic pneumothoraces: The extended focused assessment with sonography for trauma (EFAST). J Trauma. 2004; 57: 288–95.
5. Moore CL, Copel JA. Point-of-care ultrasonography. N Engl J Med. 2011; 364: 749–57. doi: 10.1056/NEJMra0909487.
6. Blans MJ, Bosch FH. Ultrasound in acute internal medicine; time to set a European standard. Eur J Intern Med. 2017; 45: 51–3. doi: 10.1016/j. ejim.2017.09.040.
7. Adhikari S, Stolz L, Amini R, Blaivas M. Impact of point-of-care ultrasound on quality of care in clinical practice. Rep Med Imaging. 2014; 7: 81-93. [ Links ]
8. Bhagra A, Tierney DM, Sekiguchi H, Soni NJ. Point-of-care ultrasonography for primary care physicians and general internists. Mayo Clin Proc. 2016; 91: 1811–27. doi: 10.1016/j.mayocp.2016.08.023.
9. Arienti V, Camaggi V. Clinical applications of bedside ultrasonography in internal and emergency medicine. Intern Emerg Med. 2011; 6: 195– 201. doi: 10.1007/s11739-010-0424-3.
10. Blaivas M. Lung ultrasound in evaluation of pneumonia. J Ultrasound Med. 2012; 31: 823–6.
11. Rantanen NW. Diseases of the thorax. Vet Clin North Am: Equine Practice 1986; 2: 49–66.
12. Lichtenstein DA. Applications nouvelles de l´echographie en reanimation. Rev Pneumol Clin. 1997; 53: 63–8.
13. Diacon AH, Theron J, Bolliger CT. Transthoracic ultrasound for the pulmonologist. Curr Opin Pulm Med. 2005; 11: 307–12.
14. Soldati G, Testa A, Silva FR, Carbone L, Portale G, Silveri NG. Chest ultrasonography in lung contusion. Chest. 2006; 130: 533–8.
15. Arbelot C, Ferrari F, Bouhemad B, Rouby JJ. Lung ultrasound in acute respiratory distress syndrome and acute lung injury. Curr Opin Crit Care. 2008; 14: 70–4. doi: 10.1097/MCC.0b013e3282f43d05.
16. Volpicelli G, Elbarbary M, Blaivas M, Lichteinstein DA, Mathis G, Kirkpatrick AW, et al. International evidence-based recommendations for point-of-care lung ultrasound. Intensive Care Med. 2012; 38: 577–91. doi: 10.1007/s00134-012-2513-4.
17. Lichtenstein D, Goldstein I, Mourgeon E, Cluzel P, Grenier P, Rouby JJ. Comparative diagnostic performances of auscultation, chest radiogra
phy and lung ultrasonography in acute respiratory distress syndrome. Anesthesiology. 2004; 100: 9–15.
18. Winkler MH, Touw HR, van de Ven PM, Twisk J, Tuinman PR. Diagnostic accuracy of chest radiograph, and when concomitantly studied lung ultrasound, in critically ill patients with respiratory symptoms. A systematic review and meta-analysis. Crit Care Med. 2018; 46: e707-14. doi: 10.1097/ CCM.0000000000003129. [ Links ]
19. Piette E, Daoust R, Denault A. Basic concepts in the use of thoracic and lung ultrasound. Curr Opin Anaesthesiol. 2013; 26:
20. 20–30. doi: 10.1097/ACO.0b013e32835afd40.20. Gargani L, Volpicelli G. How I do it: Lung ultrasound. Cardiovasc Ultrasound. 2014; ;12:25. doi: 10.1186/1476-7120-12-25. [ Links ]
21. Dietrich CF, Mathis G, Blaivas M, Volpicelli G, Seibel A, Wastl D, et al. Lung artefacts and their use. Med Ultrason. 2016; 18:488–99.
22. Lichtenstein DA, Mezière GA. Relevance of lung ultrasound in the diagnosis of acute respiratory failure: The BLUE Protocol. Chest. 2008; 134: 117–25. doi: 10.1378/chest.07-2800.
23. Bugalho A, Semedo J, Alpendre J, Ribeiro JC, Carreiro L. Ultrasound chest disease. Rev Port Pneumol. 2010; 16: 589–606.
24. Volpicelli G. Sonographic diagnosis of pneumothorax. Intensive Care Med. 2011; 37: 224–32. doi: 10.1007/s00134-010-2079-y.
25. Lichtenstein D, Mezière G, Biderman P, Gepner A. The “lung point”: an ultrasound sign specific to pneumothorax. Intensive Care Med. 2000;
26: 1434–40. 26. Volpicelli G, Caramello V, Cardinale L, Mussa A, Bar F, Frascisco MF. Bedside ultrasound of the lung for the monitoring of acute decompensated heart failure. Am J Emerg Med. 2008; 26: 585–91. doi: 10.1016/j. ajem.2007.09.014.
27. Santos TM, Franci D, Coutinho CMG, Ribeiro DL, Schweller M, Matos-Souza JR, et al. A simplified ultrasound-based edema score to assess lung injury and clinical severity in septic patients. Am J Emerg Med. 2013; 31: 1656–60. doi: 10.1016/j.ajem.2013.08.053.
28. Cortellaro F, Colombo S, Coen D, Duca PG. Lung ultrasound is an accurate diagnostic tool for the diagnosis of pneumonia in the emergency department. Emerg Med J. 2012; 29: 19–23. doi: 10.1136/emj.2010.101584.
29. Chavez MA, Shams N, Ellington LE, Naithani N, Gilman RH, Steinhoff MC, et al. Lung ultrasound for the diagnosis of pneumonia in adults: a systematic review and meta-analysis. Respir Res. 2014;15:50. doi: 10.1186/14659921-15-50. [ Links ]
30. Lichtenstein D, Mezière G, Seitz J. The dynamic air bronchogram. Alungultrasound sign of alveolar consolidation ruling out atelectasis. Chest. 2009;135:1421-5. doi: 10.1378/chest.08-2281 [ Links ]
31. Havelock T, Teoh R, Laws D, Gleeson F, BTS Pleural Disease Guideline Group. Pleural procedures and thoracic ultrasound: British Thoracic Society Pleural Disease Thorax. 2010; 65(Suppl 2): i61–76. doi: 10.1136/ thx.2010.137026.
32. Lichtenstein DA. Lung ultrasound in the critically ill. Ann Intensive Care. 2014; 4: 1. [ Links ]
33. Lichtenstein DA. BLUE-Protocol and FALLS-Protocol: two applications of lung ultrasound in the critically ill. Chest. 2015; 147:1659–70. doi: 10.1378/ chest.14-1313.
34. Zanobetti M, Poggioni C, Pini R. Can chest ultrasonography replace standard chest radiography for evaluation of acute dyspnea in the ED? Chest. 2011; 139: 1140–7. doi: 10.1378/chest.10-0435.
35. Neskovic AN, Hagendorff A, Lancellotti P, Guarracino F, Varga A, Cosyns B, et al. Emergency echocardiography: the European Association of Cardiovascular Imaging recommendations. Eur Heart J Cardiovasc Imaging. 2013; 14:1–11. doi: 10.1177/2048872614568073.
36. Lancellotti P, Price S, Edvardsen T, Cosyns B, Neskovic AN, Dulgheru R, et al. The use of echocardiography in acute cardiovascular care: Recommendations of the European Association of Cardiovascular Imaging and the Acute Cardiovascular Care Association. Eur Heart J Acute Cardiovasc Care 2015; 4: 3–5. doi: 10.1177/2048872614568073.
37. Jardin F, Valtier B, Beauchet A, Dubourg O, Bourdarias JP. Invasive monitoring combined with two-dimensional echocardiographic study in septic shock. Intensive Care Med. 1994; 20: 550–4.
38. Vieillard-Baron A, Slama M, Cholley B, Janvier G, Vignon P. Echocardiography in the intensive care unit: from evolution to revolution? Intensive Care Med. 2008; 34: 243–9.
39. Dias FS, Rezende EA de C, Mendes CL, Silva JM, Sanches JL. Hemodynamic monitoring in the intensive care unit: a Brazilian perspective. Rev Bras Ter Intensiva. 2014; 26:360–6.
40. Arntfield RT, Millington SJ. Point of care cardiac ultrasound applications in the emergency department and intensive care unit-a review. Curr Cardiol Rev. 2012; 8: 98–108.
41. Kimura BJ. Point-of-care cardiac ultrasound techniques in the physical examination: better at the bedside. Heart. 2017; 103: 987–94. doi: 10.1136/ heartjnl-2016-309915.
42. Price S, Via G, Sloth E, Guarracino F, Breitkreutz R, Catena E, et al. Echocardiography practice, training and accreditation in the intensive care: document for the World Interactive Network Focused on Critical Ultrasound (WINFOCUS). Cardiovasc Ultrasound. 2008; 6: 49. [ Links ]
43. Gudmundsson P, Rydberg E, Winter R, Willenheimer R. Visually estimated left ventricular ejection fraction by echocardiography is closely correlated with formal quantitative methods. Int J Cardiol .2005; 101: 209–12.
44. Brennan JM, Blair JE, Goonewardena S, Ronan A, Shah D, Vasaiwala S, et al. A comparison by medicine residents of physical examination versus hand-carried ultrasound for estimation of right atrial pressure. Am J Cardiol. 2007; 99: 1614–6.
45. Stone MB, Huang J V. Inferior vena cava assessment: correlation with CVP and plethora in tamponade. Glob Heart. 2013; 8: 323–7.
46. Weekes AJ, Tassone HM, Babcock A, Quirke DP, Norton HJ, Jayarama K, et al. Comparison of serial qualitative and quantitative assessments of caval index and left ventricular systolic function during early fluid resuscitation of hypotensive emergency department patients. Acad Emerg Med. 2011; 18: 912–21. doi: 10.1111/j.1553-2712.2011.01157.x.
47. Himelman RB, Kircher B, Rockey DC, Schiller NB. Inferior vena cava plethora with blunted respiratory rResponse: a sensitive echocardiographic sign of cardiac tamponade. J Am Coll Cardiol. 1988; 12:1470–7.
48. Molokoane-Mokgoro K, Goldstein LN, Wells M. Ultrasound evaluation of the respiratory changes of the inferior vena cava and axillary vein diameter at rest and during positive pressure ventilation in spontaneously breathing healthy volunteers. Emerg Med J. 2018; 35: 297-302. doi: 10.1136/emermed-2016-205944. [ Links ]
49. Erbel R, Aboyans V, Boileau C, Bossone E, Bartolomeo RD, Eggebrecht H, et al. 2014ESC Guidelines on the diagnosis and treatment of aortic diseases: Document covering acute and chronic aortic diseases of the thoracic and abdominal aorta of the adult. The Task Force for the Diagnosis and Treatment of Aortic Diseases of the European Society of Cardiology (ESC). Eur Heart J 2014; 35: 2873–926. doi: 10.1093/eurheartj/ehu281.
50. Tayal VS, Graf CD, Gibbs MA. Prospective study of accuracy and outcome of emergency ultrasound for abdominal aortic aneurysm over two years. Acad Emerg Med. 2003; 10: 867–71.
51. Costantino TG, Bruno EC, Handly N, Dean AJ. Accuracy of emergency medicine ultrasound in the evaluation of abdominal aortic aneurysm. J Emerg Med. 2005; 29: 455–60.
52. Perera P, Mailhot T, Riley D, Mandavia D. The RUSH exam: rapid ultrasound in shock in the evaluation of the critically ill. Emerg Med Clin North Am. 2010; 28: 29–56.
53. Blaivas M, Lambert MJ, Harwood RA, Wood JP, Konicki J. Lower-extremity doppler for deep venous thrombosis-can emergency physicians be accurate and fast? Acad Emerg Med 2000; 7: 120-6. [ Links ]
54. Pomero F, Dentali F, Borretta V, Bonzini M, Melchio R, Douketis JD, et al. Accuracy of emergency physician-performed ultrasonography in the diagnosis of deep-vein thrombosis: A systematic review and meta-analysis. Thromb Haemost. 2013; 109: 137–45. doi: 10.1160/TH12-07-0473
55. Tapson VF, Carroll BA, Davidson BL, Elliot CG, Fedullo PF, Hales CA, et al. The diagnostic approach to acute venous thromboembolism. Clinical practice guideline. American Thoracic Society. Am J Respir Crit Care Med. 1999; 160: 1043–66.
56. Nazerian P, Vanni S, Volpicelli G, Giggli Z, Zanobetti M, Bartolucci M, et al. Accuracy of point-of-care multiorgan ultrasonography for the diagnosis of pulmonary embolism. Chest. 2014; 145:950–7. doi: 10.1378/chest.13-1087.
57. Noble VE, Brown DF. Renal ultrasound. Emerg Med Clin North Am. 2004; 22: 641–59.
58. Dalziel PJ, Noble VE. Bedside ultrasound and the assessment of renal colic: a review. Emerg Med J. 2013; 30: 3–8. doi: 10.1136/emermed-2012-201375.
59. Saugel B, Scheeren TWL, Teboul JL. Ultrasound-guided central venous catheter placement: a structured review and recommendations for clinical practice. Crit Care. 2017; 21: 225. doi: 10.1186/s13054-017-1814-y. [ Links ]
60. Mahan AF, McEvoy MD, Gravenstein N. Long-axis view for ultrasound-guided central venous catheter placement via the internal jugular vein. Rom J Anaesth Intensive Care. 2016; 23: 27–31.
61. Brass P, Hellmich M, Kolodziej L, Schick G, Smith AF. Ultrasound guidance versus anatomical landmarks for internal jugular vein catheterization. Cochrane Database Syst Rev 2015; 1: CD006962. doi: 10.1002/14651858. CD011447. [ Links ]
62. American Society Anesthesiologists Task Force on Central Venous Access, Rupp SM, Apfelbaum JL, Blitt C, Caplan RA, Connis RT, et al. Practice guidelines for central venous access: A report by the American Society of Anesthesiologists Task Force on Central Venous Access. Anesthesiology. 2012; 116: 539–73. doi: 10.1097/ALN.0b013e31823c9569.
63. French JLH, Raine-Fenning NJ, Hardman JG, Bedforth NM. Pitfalls of ultrasound guided vascular access: the use of three/four-dimensional ultrasound. Anaesthesia. 2008 ;63 :806–13. doi: 10.1111/j.1365-2044.2008.05513.x.
64. Gryminski J, Krakówka P, Lypacewicz G. The diagnosis of pleural effusion by ultrasonic and radiologic techniques. Chest.1976; 70 : 33–7.
65. Yu CJ, Yang PC, Wu HD, Chang DB, Kuo SH, Luh KT. Ultrasound study in unilateral hemithorax opacification: image comparison with computed tomography. Am Rev Respir Dis. 1993; 147: 430–4.
66. Raptopoulos V, Davis LM, Lee G, Umali C, Lew R, Irwin RS. Factors affecting the development of pneumothorax associated with thoracentesis. Am J Roentgenol. 1991; 156: 917–20.
67. Barnes TW, Morgenthaler TI, Olson EJ, Hesley GK, Decker PA, Ryu JH. Sonographically guided thoracentesis and rate of pneumothorax. J Clin Ultrasound. 2005; 33: 442–6.
68. Feller-Kopman D. Ultrasound-guided thoracentesis. Chest. 2006; 129: 1709–14.
69. Weingardt JP, Guico RR, Nemcek AA, Li YP, Chiu ST. Ultrasound findings following failed, clinically directed thoracenteses. J Clin Ultrasound. 1994; 22: 419–26.
70. Mercaldi CJ, Lanes SF. Ultrasound guidance decreases complications and improves the cost of care among patients undergoing thoracentesis and paracentesis. Chest.2013; 143: 532–8. doi: 10.1378/chest.12-0447.
71. Kurup AN, Lekah A, Reardon ST, Schimt GD, McDonald JS, Carter RE, et al. Bleeding rate for ultrasound-guided paracentesis in thrombocytopenic patients. J Ultrasound Med. 2015; 34: 1833–8. doi: 10.7863/ultra.14.10034.
72. Edwards C, Leira EC, Gonzalez-Alegre P. Residency training: a failed lumbar puncture is more about obesity than lack of ability. Neurology. 2015; 84: e69–72. doi: 10.1212/WNL.0000000000001335
73. Grau T, Leipold RW, Conradi R, Martin E. Ultrasound control for presumed difficult epidural puncture. Acta Anaesthesiol Scand. 2001; 45: 766–71.
74. Lee WS, Jeong WJ, Yi HY, Ryu S, Lee JW, Kim SW, et al. The usefulness of ultrasound-assisted lumbar puncture on adult patients in the emergency center: Comparison with classic lumbar puncture. J Korean Soc Emerg Med. 2008; 19: 562–8.
75. Rose JS, Bair AE, Mandavia D, Kinser DJ. The UHP ultrasound protocol: A novel ultrasound approach to the empiric evaluation of the undifferentiated hypotensive patient. Am J Emerg Med. 2001; 19: 299–302. doi: 10.1053/ajem.2001.24481.
76. Jones AE, Tayal VS, Sullivan DM, Kline JA. Randomized, controlled trial of immediate versus delayed goal-directed ultrasound to identify the cause of nontraumatic hypotension in emergency department patients. Crit Care Med. 2004; 32: 1703–8.
77. Jensen MB, Sloth E, Larsen KM, Schmidt MB. Transthoracic echocardiography for cardiopulmonary monitoring in intensive care. Eur J Anaesthesiol. 2004; 21: 700–7.
78. Hernandez C, Shuler K, Hannan H, Sonyika C, Likourezos A, Marshall J. C.A.U.S.E.: Cardiac arrest ultra-sound exam—A better approach to managing patients in primary non-arrhythmogenic cardiac arrest. Resuscitation. 2008; 76: 198–206.
79. Seif D, Perera P, Mailhot T, Riley D, Mandavia D. Bedside ultrasound in resuscitation and the rapid ultrasound in shock protocol. Crit Care Res Pract. 2012; 2012:503254. doi: 10.1155/2012/503254. [ Links ]
80. Hoppmann R, Blaivas M, Elbarbary M. Better medical education and health care through point-of-care ultrasound. Acad Med. 2012; 87: 134. doi: 10.1097/ACM.0b013e31823f0e8f. [ Links ]
81. Hoppmann R, Cook T, Hunt P, Fowler S, Paulman L, Wells J, et al. Ultrasound in medical education: a vertical curriculum at the University of South Carolina School of Medicine. J S C Med Assoc. 2006; 102: 330–4.
82. Ten Cate OTJ, Kusurkar RA, Williams GC. How self-determination theory can assist our understanding of the teaching and learning processes in medical education. AMEE Guide No. 59. Med Teach. 2011; 33: 961–73.
Correspondência:José Mariz josemariz@med.uminho.pt
Serviço de Urgência do Hospital de Braga; Braga, Portugal
Sete Fontes - São Victor - 4710-243 Braga
Conflitos de Interesse: Os autores declaram a inexistência de conflitos de interesse na realização do presente trabalho.
Fontes de Financiamento: Não existiram fontes externas de financiamento para a realização deste artigo.
Conflicts of interest: The authors have no conflicts of interest to declare.
Financing Support: This work has not received any contribution, grant or scholarship.
Recebido: 16/07/2017
Aceite:09/09/2018














