Introdução
O vírus da hepatite C (VHC) continua a ser uma das principais causas de doença hepática.1 É estimado que 58 milhões de pessoas no mundo estejam infetadas pelo VHC, surgindo 1,5 milhões de novos infetados por ano.2 A história natural da infeção por VHC é variável, podendo manifestar-se desde formas frustes até extensa fibrose, cirrose e surgimento de carcinoma hepatocelular. 1 A Organização Mundial de Saúde (OMS) estima que, em 2019, 290 000 pessoas tenham morrido em consequência da infeção por VHC, seja por cirrose ou carcinoma hepatocelular.2 Para além da doença hepática, a infeção VHC pode também ter manifestações extra-hepáticas.3.4O vírus foi identificado em 1989, tendo-se posteriormente percorrido um rápido caminho, em pouco mais de 20 anos, até à descoberta dos primeiros antivirais de ação direta em 2010,5 que vieram revolucionar o tratamento desta infeção. Os tratamentos baseados em interferão e ribavirina, demorados, mal tolerados e pouco eficazes, deram lugar a tratamentos muito eficazes e com boa tolerância.4•6Fundamentada por estes novos tratamentos, a OMS lançou, em 2016, o objetivo de reduzir em 80% até 2030 a incidência e em 65% a mortalidade por VHC.2
Em 2019, o surgimento da crise pandémica SARS-CoV-2, tornou-se um grande encargo para os sistemas de saúde.7 Houve necessidade de reajustar os serviços de saúde, mobilizando equipas e reestruturando atividades. Estas alterações surgiram num momento fulcral para poder alterar as dinâmicas necessárias para atingir os objetivos da OMS para o tratamento da infeção VHC.2•7Apesar de ainda não existirem dados publicados, a prática clínica sugere uma diminuição do número de tratamentos solicitados, pressupondo uma diminuição do número de doentes tratados. No entanto, importa consolidar estes dados de forma a caraterizar o impacto que a pandemia terá sobre o tratamento da hepatite C e quais as causas para esta aparente diminuição de tratamentos.
O nosso estudo tem por objetivo analisar de forma retrospetiva o tratamento da hepatite C num hospital distrital, bem como avaliar o impacto da pandemia SARS-CoV-2 no tratamento da hepatite C.
Material e Métodos
Neste estudo, foram avaliados, retrospetivamente, os doentes tratados e seguidos no Centro Hospitalar do Médio Tejo, entre o dia 1 de janeiro de 2015 e o dia 31 de dezembro de 2020. A análise descritiva foi realizada a partir de Microsoft Excel®. As variáveis categóricas (sexo, fator de risco, genótipo, presença de cirrose, Classificação Child-Pugh e tratamento prévio) foram expressas em frequência e percentagem e as variáveis contínuas (idade, doentes tratados e tempo de espera) são expressas em média e desvio padrão. A diferença entre variáveis contínuas foi avaliada pelo teste Mann-Whitney para variáveis independentes (amostras sem distribuição normal). Um p <0,05 é considerado estatisticamente significativo. Foi utilizado IBM SPSS Statistics® para Windows®, versão 20.0 para análise estatística.
Resultados
Durante o período estudado foram tratados 267 doentes (n = 267), 78% do sexo masculino e 22% do sexo feminino, com idade de 50,36 ± 10,3 anos (Tabela 1 ). Aquando do diagnóstico de hepatite C, os doentes tinham em média 40,55 ± 12,16 anos.
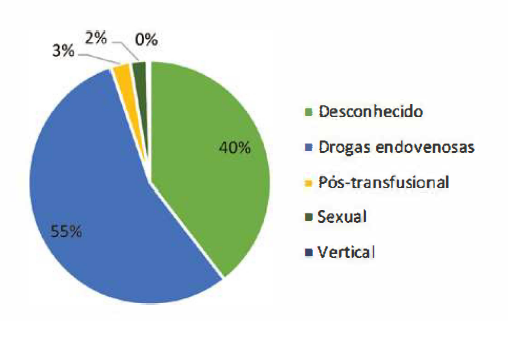
O fator de risco para infeção mais vezes identificado foi o consumo de drogas endovenosas (55, 1 %), seguindo-se a transfusão de componentes sanguíneos (2,6%), o contacto sexual de risco (2,2%) e a transmissão vertical (0,4%). Em 39,7% não se conseguiu identificar o fator de risco para infeção VHC (Fig. 1).
Em relação ao genótipo, o mais comumente identificado foi o genótipo 1 (63,3%), seguindo-se o 3 (27%), o 4 (9,3%) e, em 0,4%, a combinação dos genótipos 1 e 4 (Fig. 2). Dentro do genótipo 1, 70,4% eram 1 a, 29% 1 b e 0,6% 1 c. Dos doentes tratados, 27% apresentava cirrose hepática. Quando se avaliou a Classificação de Child-Pugh, 61 % apresentavamse em Classe A e 14% em Classe B, sendo que em 25% não foi possível apurar.
Em relação ao tratamento prévio, 32% dos doentes já tinha sindo tentada outra abordagem, tendo realizado em média 1 ,30 ± 0,66 tratamentos prévios. Dos tratamentos prévios, o mais comum foi o interferão peguilado com ribavirina (72,5%), seguindo-se interferão (8,3%), o interferão com ribavirina (3,7%), interferão peguilado (1,8%), sofosbuvir com ribavirina (1 ,8%), ledispasvir com sofosbuvir (1,8%), sofosbuvir com interferão peguilhado e ribavirina (1 ,8%), boceprevir com interferão peguilado e ribavirina (0,9%) e ledispasvir com sofosbuvir e ribavirina (0,9%). Em 6,4% dos doentes, não se conseguiu identificar o tratamento prévio.
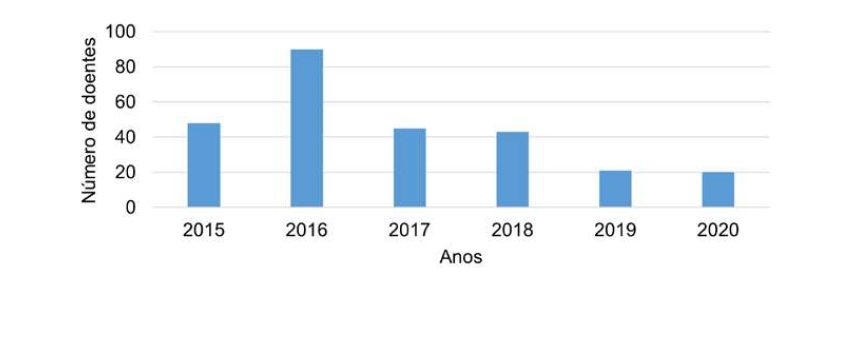
Podemos observar na Fig. 3 que após o grande número de doentes tratados em 2016 (90 doentes), verificou-se uma diminuição paulatina, até se atingir o número mínimo de doente tratados em 2020 (20 doentes).
Os doentes esperaram em média 3, 19 ± 2,05 meses pelo tratamento. O tempo de espera antes da pandemia SARSCoV-2 (período compreendido entre 2015 e 2019), foi de 3, 11 ± 2,01 meses. Por sua vez, o tempo de espera durante a pandemia, em 2020, foi de 4,15 ± 2,36 meses. Quando comparados estes dois grupos, pré-pandemia (2015-2019) e durante a pandemia (2020) foi possível verificar um aumento do tempo de espera estatisticamente significativo (U = 1693; p = 0,017).
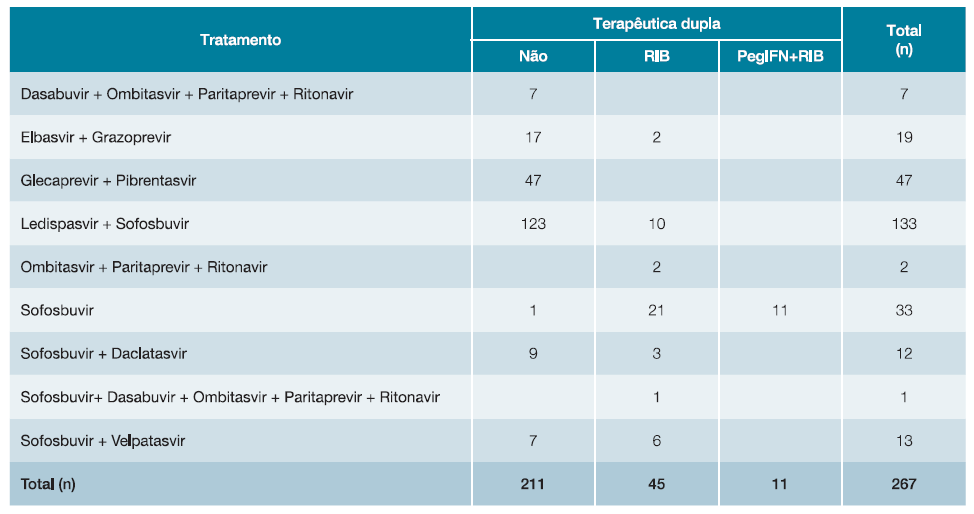
A distribuição dos tratamentos pode ser observada na Tabela 2. O tratamento mais vezes utilizado foi o ledispasvir com sofosbuvir. Durante os anos de 2019 e 2020, foram usados exclusivamente glecaprevir com pibrentasvir e sofosbuvir com velpatasvir.
Dos doentes submetidos a tratamento, 225 terminaram o mesmo. Dos doentes que não terminaram, 8 faleceram e 34 faltaram ao seguimento. Dos doentes que terminaram o tratamento, 99, 11 % atingiu resposta virológica sustentada.
Dentro dos doentes com resposta virológica sustentada, 70% teve alta para o médico assistente, 19% mantém seguimento e 11 % faltou ao seguimento.
Discussão
A OMS recomenda oferecer tratamento a todos os indivíduos com mais de 12 anos de idade com infeção por VHC.3 O objetivo principal do tratamento é alcançar a cura virológica com o intuito de prevenir complicações hepáticas e extrahepáticas, bem como melhorar a qualidade de vida e prevenir a transmissão.1
No nosso estudo retrospetivo, a população era na sua maioria constituída por homens, provenientes de grupos de risco, nomeadamente utilizadores de drogas endovenosas (55%), o que vai ao encontro dos dados nacionais.8 Em consonância com os dados mundiais3 e nacionais,8 o genótipo 1 foi o mais frequentemente identificado, seguindo-se o 3. A percentagem de doentes em estadia de cirrose foi de 28%, conforme o apresentado a nível nacional.8
Durante o período estudado, o número de doentes tratados diminuiu paulatinamente, sendo o seu máximo atingido em 2016, com 90 doentes tratados. Durante o ano de 2020 atingiu-se o número mais baixo de doentes tratados (20 doentes). Esta diminuição poderá ter estado relacionada com a menor afluência aos serviços de saúde durante a pandemia de SARS-CoV-2, com a mobilização dos profissionais de saúde para outras atividades clínicas, o que dificultou a observação de novos doentes, ou ainda com a diminuição do número de diagnósticos, eventualmente pelo menor número de doentes identificados ou mesmo infetados. De forma a garantir a eliminação do vírus é necessário criar parcerias com organizações governamentais e não governamentais, para tentar chegar aos doentes de maior risco, como os presidiários e os utilizadores de drogas endovenosas, permitindo assim eliminar o vírus nestes nichos de doentes.
Em relação ao tempo de espera pelo tratamento, este foi de 3, 19 ± 2,05 meses, não existindo dados a nível nacional que permitam a comparação deste valor. Durante o ano de 2020 observou-se um aumento do tempo médio para 4, 15 ± 2,36 meses, quando comparado com o tempo de espera pré-pandemia (3, 11 ± 2,01 meses). O aumento do tempo de espera do período pré-pandemia para o período durante a pandemia foi estatisticamente significativo. Este aumento do tempo de espera durante o ano 2020 foi muito provavelmente consequência da reorganização dos serviços de saúde durante a pandemia.
O impacto que o aumento do tempo de espera, bem como a diminuição do número de tratamentos terá a longo prazo ainda não é certo. No entanto, um estudo mostrou que um ano de paragem nos programas de luta para a eliminação da hepatite C poderá resultar num aumento de 72 300 mortes relacionadas com doenças do fígado e um aumento de 44 800 cancros do fígado a nível mundial nos próximos 10 anos.7 Mesmo em países onde atingir as metas da OMS era um objetivo real, a pandemia alterou essa realidade, tornando-se agora muito difícil atingi-lo.9
O uso de tratamentos pangenotípicos tem ganho relevo no tratamento destes doentes.1·3Assim, apesar do tratamento mais frequentemente escolhido ter sido o ledispasvir com sofosbuvir, nos últimos dois anos optou-se exclusivamente pelos tratamentos pangenotípicos, o que está em conformidade com as recomendações internacionais.1•3De acordo com evidência científica, os antivirais de ação direta demostram alta eficácia, com taxas de resposta virológica sustentada acima dos 90%,3 o que também ficou demonstrado no nosso estudo.
O seguimento dos doentes é semelhante ao descrito por Anjo et al, que refere que dos doentes tratados, 79,5% deixaram de ser seguidos e 20% mantinham seguimento.8 De acordo com as recomendações europeias, deverão manter seguimento doentes com fibrose avançada ou cirrose, mesmo que apresentem resposta virológica sustentada, uma vez que apresentam risco de carcinoma hepatocelular.1 Acrescentam-se a estes os doentes que mantêm comportamentos de risco, devido à possibilidade de reinfeção,1 permitindo assim uma identificação e tratamentos mais céleres.
É necessária uma estratégia conjunta e sustentada de forma a conseguir identificar e tratar o máximo número de doentes. Apesar de ainda não ser possível observar as consequências da pandemia de SARS-CoV-2, no que diz respeito à infeção por VHC, atrasar os programas de eliminação do VHC irá contribuir para o aumento da morbimortalidade associada ao VHC nos próximos 10 anos.7•9
Apesar do nosso estudo ser retrospetivo, com um número pequeno de doentes, consideramos que possibilita traçar uma amostra da realidade Portuguesa, permitindo observar umas das consequências diretas da pandemia de SARS-CoV-2 que foi o aumento do tempo de espera pelo tratamento. De forma a poder identificar o real impacto da pandemia no tratamento da hepatite C, torna-se necessário continuar a analisar os dados no futuro.
Conclusão
A infeção por VHC continua a representar um encargo grande a nível de saúde pública mundial e também em Portugal. Conseguir diagnosticar e tratar estes doentes de forma eficaz e rápida é fundamental, para conseguirmos interromper as cadeias de transmissão e atingir os objetivos de eliminação das hepatites propostos pela OMS para 2030. A pandemia veio inviabilizar muitos projetos pré-pandémicos que pretendiam chegar, de forma eficaz, aos grupos de risco mais vulneráveis. Torna-se imperativo voltar à ação para que seja possível atingir as metas propostas pela OMS para 2030.