Introdução
As estatinas, que inibem a enzima HMGCR (3-hidroxi-3-methyl-glutaril-CoA redutase), são dos fármacos mais prescritos mundialmente, pelo seu papel no controlo do risco cardiovascular.1 O mecanismo pelo qual induzem miopatia inflamatória e necrotizante ainda não está esclarecido, sendo um efeito adverso raro e potencialmente grave.1,2Caracteriza-se por fraqueza muscular proximal e elevação da creatinaquinase (CK).1,2O diagnóstico requer elevada suspeição, nomeadamente quando a clínica e a elevação de CK se mantêm mesmo após suspensão do fármaco.1,2A confirmação é pela presença de autoanti-corpos anti-HMGCR, embora a biópsia muscular seja o gold-standard.1,3O tratamento consiste na corticoterapia sistémica em alta dose, seguida de outros fármacos imunossupressores como metotrexato, azatioprina, micofenolato de mofetil para além da suspensão da estatina; as imunoglobulinas e o rituximab podem ser usados em casos mais graves.1,3
CASO CLÍNICO 1
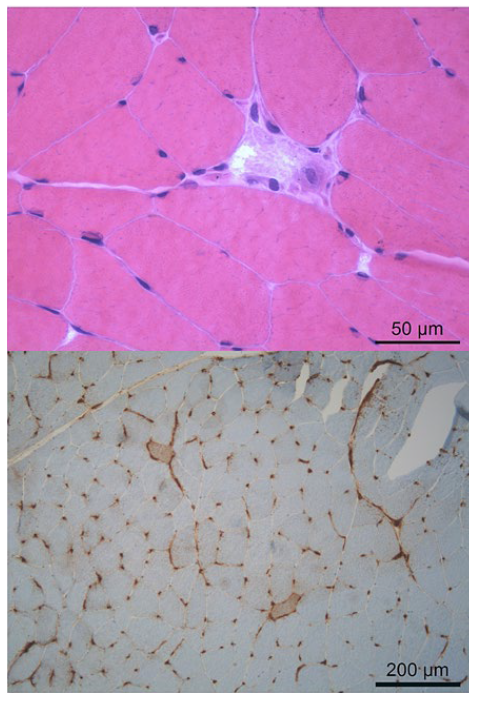
Reportamos o caso de um homem de 60 anos com risco cardiovascular elevado filiado em síndrome metabólico completo, medicado com metformina 850 mg e desde 2019 com atorvastatina 20 mg (LDL 170 mg/dL). Foi internado em janeiro de 2021 por pneumonia por SARS-CoV2 grave. Apresentava rabdomiólise, sem história prévia a este quadro, que se filiou na infeção (Tabela 1); existiam casos descritos na literatura e apesar do mecanismo não ser claramente conhecido, sabe-se, porém, que as infeções víricas se associam a rabdomiólise por invasão dos miócitos pelos vírus ou pela sua destruição mediada por citoquinas. Foi instituída fluidoterapia, dexametasona e, por suspeita de sobreinfeção bacteriana, ceftriaxone. À data da alta apresentava melhoria (Tabela 1). Durante o internamento foi suspensa a estatina, tendo sido retomada à data de alta. Na reavaliação em consulta nos cuidados de saúde primários, três meses depois, verificou-se reagravamento da rabdomiólise, tendo o seu médico de família reduzido a dose de atorvastatina para 10 mg; três meses mais tarde apresentava novamente agravamento. Por este motivo foi referenciado para consulta de medicina interna em outubro de 2021 (Tabela 1). Desde o internamento, que referia mialgias a nível dos quadríceps. Sem outras queixas do foro reumatológico ou história familiar de doença auto-imune. À observação na consulta de medicina não apresentava défice de força muscular, ou quaisquer outras alterações ao exame objetivo. Analiticamente, com elevação da CK e -HMGCR e fibrilharina positivos (Tabela 1). Realizou biópsia de músculo do quadríceps (Fig. 1) que confirmou a suspeita de miopatia inflamatória imunomediada, apresentando algumas fibras atrofiadas e com necrose. A eletromiografia (EMG) dos membros superiores e inferiores revelou algum excesso de polifasia com alguns potenciais de amplitude borderline nos músculos iliopsoas esquerdo e vasto medial esquerdo e recrutamento precoce em músculos proximais do mem-bro inferior esquerdo e proximais e distais ao nível do membro superior esquerdo compatíveis com eventual processo miopático. A ressonância magnética (RM) das coxas não apresentava sinais de inflamação ou necrose muscular. O estudo subsequente para exclusão de síndrome paraneoplásica foi negativo (Tabela 1). Iniciou seguimento em consulta de doenças autoimunes (DAI), e apesar de clinicamente melhorado, mantinha rabdomiolise importante (Tabela 1) tendo realizado bólus de 125 mg de metilprednisolona. Por manter rabdomiólise, iniciou metotrexato 10 mg/semana que suspendeu após 1 mês por hepatotoxicidade, tendo-se iniciado azatioprina 100 mg/dia que, por sua vez, suspendeu após 3 meses, por intolerância gastrointestinal. Iniciou terapêutica com 850 mg de rituximab com melhoria clínica e analítica, com redução das enzimas musculares e dos valores dos auto-anticorpos (Tabela 1- a). Foi reforçada a necessidade de controlo dietético e de atividade física conseguindo-se alcançar os objetivos (LDL-c<100 mg/dL).
CASO CLÍNICO 2
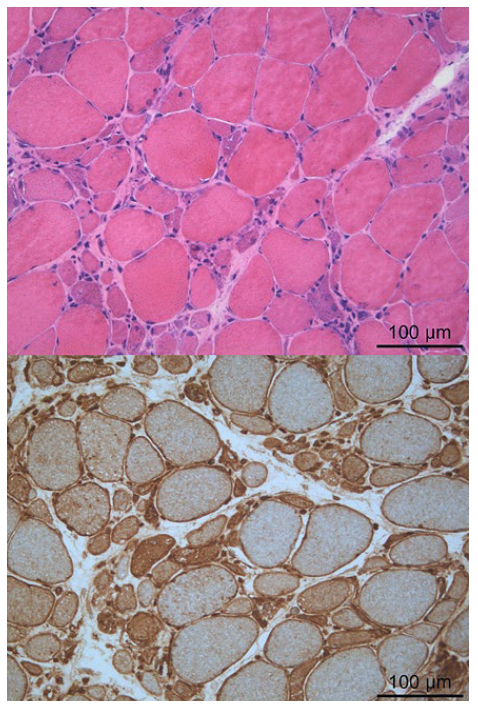
Mulher de 61 anos com risco cardiovascular muito elevado filiado em síndrome metabólico completo com mau controlo metabólico, já com nefropatia diabética que se titulou até rosuvastatina 20 mg (LDL 248 mg/dL); submetida a nefrectomia parcial por carcinoma de células renais em maio de 2021 Um mês após, iniciou fraqueza muscular a nível proximal com dificuldade na marcha, disfonia, disfagia, astenia, anorexia e atrofia muscular, motivo pelo qual recorreu ao serviço de urgência; sem outras queixas do foro reumatológico ou história familiar de doença auto-imune. Objetivamente, apresentava fraqueza muscular sobretudo proximal bilateral grau 3 (membros superiores e inferiores), sem marcha autónoma. Analiticamente, com elevação das enzimas musculares (Tabela 2). Foi internada para estudo, tendo-se suspendido a estatina. Realizou TC toraco-abdomino-pélvica e tomografia por emissão de positrões (PET) sem evidência de recidiva oncológica. Realizou também TC e RM da coluna lombossagrada que não demonstraram compromisso radicular. A EMG apresentava sinais compatíveis com processo miopático, sobretudo em músculos mais proximais dos membros superiores e inferiores, bem como atividade espontânea abundante, sugerindo provável processo de inflamação muscular. Estudo imunológico positivo para anti-HMGCR. Realizou biópsia do músculo deltóide que revelou aspetos sugestivos de miopatia inflamatória auto-imune necrotizante em fase crónica (Fig. 2). Iniciou pulsos de metilpdrenisolona 125 mg durante 3 dias e, dada a gravidade do caso, iniciou terapêutica de indução com imunoglobulinas (Ig) endovenosas (EV) 2 g/kg, seguindo-se manutenção com metotrexato (MTX) 15 mg/semana. Pela lenta evolução de enzimas musculares, decidiu-se iniciar prednisolona 0,5 mg/kg/dia durante uma semana. Foi transferida para unidade de reabilitação após 76 dias de internamento, mantendo tetraparésia de predomínio proximal. Teve alta um mês depois, já havendo terminado o desmame da prednisolona, mantendo apenas metotrexato (15 mg/semana) - ver Tabela 2 (*). Na reavaliação em consulta, por manter incapacidade motora com tetraparésia de predomínio a nível dos membros superiores (grau 2 -3 versus grau 4 nos membros inferiores) decidiu-se associar IgIV 60 g/dia, 2 dias/mês, aumento do metotrexato para 17,5 mg/semana e associação de 50 mg de azatioprina, com melhoria da força muscular para grau 4-5 nos membros superiores e mantendo grau 4 nos membros inferiores (Tabela 2 (**)). Instituiu-se ezetimibe atendendo ao objetivo de LDL-c <70 mg/dL.
Discussão
A miopatia necrotizante induzida por estatinas é uma entidade rara que ocorre em cada 2-3/100 000 doentes medicados.1,3A média de idades é de 65 anos e não há predomínio de género.3 A fisiopatologia não está bem esclarecida mas pensa-se que a estatina induz mecanismos de auto-imunidade contra a enzima envolvida na síntese do colesterol, HMG-CoA redutase (alvo de atuação da estatina), em indivíduos aparentemente já com alguma predisposição auto-imune, dada a maior prevalência do haplótipo DRB1*11:01 em doentes com o auto-anticorpo anti-HMGCR positivo.1-3Apesar da maioria dos quadros descritos estarem associados à atorvastatina, não parece haver uma associação específica com esta estatina.2 Tipicamente o quadro apesenta-se com diminuição da força a nível proximal, bilateral e simétrica, disfagia, mialgias, cãibras e astenia.1,2O início desta patologia não é tempo dependente, podendo ocorrer semanas a anos após o início da terapêutica, havendo descrição de uma mediana de 41 meses.2,3
Em 90% dos casos, a CK atinge níveis> 2000 U/L. A EMG demonstra potenciais de ação de baixa amplitude na placa motora com atividade espontânea aumentada.1,3Na RMN geralmente há edema e tecido muscular substituído por infiltrado lipídico.1,4A biópsia muscular, exame gold-standard para confirmação do diagnóstico, revela necrose das fibras musculares com algumas em regeneração, infiltrado de macrófagos, poucos linfócitos T (CD3+, CD4+ e CD8+) e células dendríticas plasmocitoides CD123+.1-3Todavia o diagnóstico pode ser feito através da positividade para o auto anticorpo anti-HMGCR que, é um método menos invasivo, mais rápido e simples.5,6Os diagnósticos diferenciais são polimiosite, dermatomiosite, síndrome antisintetase, miosite de corpos de inclusão, miosite induzida por outros fármacos e síndrome paraneoplasico.7 Raramente há resolução completa apenas com a suspensão do fármaco.3 A evidência disponível até ao momento é sobretudo baseada em estudos observacionais sugerindo-se iniciar o tratamento com corticosteroides sistémicos (1 mg/kg/dia de prednisolona ou equivalente) associando-se à posteriori imunossupressores poupadores de corticoides, habitualmente o metotrexato.7 No caso particular de anti-HMGCR positivo, está descrita particular eficácia das IgEV em monoterapia ou em associação.7 Em doentes diabéticos ou com elevado risco cardiovascular, é preferível evitar os corticosteroides e ponderar monoterapia com IgEV.6 O prognóstico é geralmente favorável, com descrição na literatura de resolução dos sintomas em 91% dos doentes; porém, pode recidivar. Estão reportados casos com evolução fatal por falência ventilatória por fraqueza muscular respiratória.6 Parece ainda haver uma associação entre o autoanticorpo anti-HMGCR positivo e risco acrescido de neoplasia malignas nestes doentes, com idade superior a 50 anos e após três anos do diagnóstico.3
Os casos reportados correspondem a casos típicos na sua apresentação, dado que se trata de doentes na sétima década de vida, que desenvolveram miopatia meses após o início do tratamento com estatina e que cursaram com miopatia proximal e elevação da CK>2000 U/L.
Já a gestão terapêutica foi desafiante: no caso 1 pelos efeitos adversos associados aos imunossupressores mais comumente usados, com recurso ao rituximab; no caso 2, pela gravidade clínica com compromisso respiratório, com necessidade de introdução de imunoglobulinas e tendo-se optado por tratamento pulsado com metilprednisolona.7
Conclusão
São necessários mais estudos de modo a se definir o tratamento ótimo, desde os fármacos a administrar à posologia ideal.4 Assim, em doentes medicados com estatina, deve ser vigiada a presença de mialgias e doseadas as enzimas musculares - aspectos muitas vezes esquecidos pela frequência de prescrição e segurança habitual destes fármacos - pois pode conduzir a um diagnóstico precoce.6 O relato destes dois casos pretende ilustrar a heterogeneidade clínica desta patologia e os desafios da gestão terapêutica.