Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Jornal Português de Gastrenterologia
versão impressa ISSN 0872-8178
J Port Gastrenterol. v.17 n.6 Lisboa nov. 2010
Hepatite C aguda no profissional de saúde - revisão a propósito de um caso clínico
Cristina Valente*, Cláudia Fernandes**, Luís Trindade*
*Assistente Hospitalar Graduado em Infecciologia, **Interna do Internato Complementar de Infecciologia, Serviço de Doenças Infecciosas – Centro Hospitalar de Coimbra (EPE), Coimbra (Director. Dr. A. Vieira)
Resumo
O vírus da hepatite C (VHC) representa actualmente uma das causas mais importantes de hepatite crónica, cirrose e carcinoma hepatocelular.
A hepatite C aguda sintomática manifesta-se em cerca de 10 a 15% dos indivíduos, podendo ocorrer uma resolução espontânea em quase metade dos casos; por outro lado a grande maioria das formas assintomáticas tende a evoluir para a cronicidade.
A transmissão do VHC, seguindo-se a uma picada acidental, constitui uma importante preocupação para os Profissionais de Saúde. A monitorização destes profissionais constitui a melhor forma de avaliar a necessidade do tratamento da fase aguda, de forma a prevenir a evolução para formas crónicas.
Todos aqueles que mantêm um RNA-VHC positivo à 12ª semana após o acidente são potenciais candidatos ao tratamento. Tem sido claramente demonstrado, em vários estudos, o benefício do tratamento da Hepatite C aguda, atingindo-se taxas de cura de 90 a 95%.
PALAVRAS-CHAVE: Hepatite C aguda, profissional de saúde, tratamento.
Acute viral hepatitis C in the health care worker - review based on a clinical case
Abstract
Hepatitis C virus infection (HCV) is a major cause of chronic hepatitis, cirrhosis and hepatocellular carcinoma.
Symptomatic acute hepatitis C occurs in only about 10 - 15% and in these individuals spontaneous clearance happens in almost half of the patients; on the other hand the majority of asymptomatic cases progress to chronicity.
HCV transmission following a needle stick is an important threat to health care workers. Monitoring these professionals, is the best way to provide the rationale for treating them in the acute phase in order to prevent chronic evolution. Those patients who have detectable HCV-RNA at week 12 after exposure are potential candidates to treatment.
Several studies have shown that treatment of acute HCV hepatitis is beneficial, achieving rates of success of 90 - 95%.
KEYWORDS: Acute hepatitis C, health care workers, treatment.
INTRODUÇÃO
O virus da hepatite C (VHC) é uma das causas mais importantes de doença hepática, responsável nomeadamente por hepatite crónica, cirrose, descompensação hepática e carcinoma hepatocelular1. Estima-se que cerca de 3% da população mundial esteja infectada por este vírus1. A hepatite C aguda é habitualmente assintomática e de difícil diagnóstico, ocorrendo as formas sintomáticas em apenas 10 a 15% das pessoas infectadas2.
Na grande maioria dos casos (55 a 85%), a infecção evolui para formas crónicas2,3. O Profissional de Saúde (P.S.) é infectado por via parentérica e/ou através da exposição mucosa4-5. Neste grupo populacional, a hepatite C, para além das repercussões clínicas descritas, pode ter consequências legais e sociais. O objectivo da vigilância destes profissionais é possibilitar o tratamento adequado no momento certo, evitando a evolução para formas crónicas.
A sua complexidade no que diz respeito aos aspectos epidemiológicos e a cofactores que modificam a evolução tem dificultado, de alguma forma, a sua prevenção e controlo. Os autores descrevem sucintamente um caso clínico ilustrativo deste problema.
CASO CLÍNICO
MJMP, 22 anos, sexo feminino, aluna de enfermagem, sofreu uma picada acidental a nível do 4º dedo da mão esquerda com agulha oca, utilizada em doente com hepatite C crónica. Este último, apesar de ter actividade vírica, não tinha indicações para tratamento.
Para além da retirada imediata das luvas, medidas de desinfecção locais e colheitas para anti-HBs (anticorpo de superfície do vírus da hepatite B) (vacinada), anti-VHC (anticorpo para o vírus da hepatite C) e anti-VIH (anticorpo para o vírus da imunodeficiência humana), a profissional de saúde foi aconselhada e orientada para consulta de Virologia, em Hospital de Dia de Doenças Infecciosas do Centro Hospitalar de Coimbra. Verificou-se imunidade para o VHB e ausência de anticorpos para VHC e VIH. Na avaliação da 4ª semana estava assintomática, tendo realizado colheitas que revelaram: AST 18 UI/ml e ALT 21 UI/ml, anti-VHC negativo e RNA-VHC positivo pela técnica de Polymerase Chain Reaction-Real Time (PCR-RT) – 6 601 126 UI/ml (6,8 log), o que levou a testar a amostra sanguínea basal pela mesma técnica, que revelou RNA-VHC indetectável. Tratava-se de uma hepatite C aguda, demonstrada por técnica virológica. A aluna manteve-se assintomática, pelo que foi aconselhada vigilância clínica e controlo laboratorial, prevendo-se novos testes bioquímicos, serológico (anti-VHC) e virológico (RNA-VHC) 4 semanas depois. Um pouco antes da 8ª semana iniciou um quadro de icterícia, astenia e colúria, apresentando nesta altura os seguintes valores bioquímicos: AST1250 UI/ml, ALT 2534 UI/ml, BT 67 μnol/L. O RNA-VHC da 8ª semana revelou um valor de 338 939 UI/ml (5,5 log). Nesta altura e por ter havido uma descida de 1,3 log em 4 semanas, optou-se mais uma vez por vigilância clínica e laboratorial semanais. O genótipo do VHC não foi determinado por não se ter tomado qualquer decisão terapêutica. Houve uma boa evolução clínica e o controlo da 12ª semana mostrou uma descida nos valores das aminotransferases (ALT 75 UI/L, AST 38 UI/L) e um RNA-VHC de 97 UI/ml.
O controlo realizado 1 mês depois (à 16ª semana) revelou virémia indetectável e bioquímica sem alterações. O surgimento do quadro clínico acompanhado de icterícia e o baixo valor do RNA-VHC à 12ª semana, indiciavam possibilidade de resolução espontânea do VHC, o que aconteceu com esta profissional de saúde. Esta desenvolveu hepatite C aguda, resultante de um procedimento invasivo, isto é picada acidental com agulha proveniente de colheita de sangue a fonte positiva para o VHC, o que ilustra a importância da hepatite C como doença ocupacional.
DISCUSSÃO
Apesar das mudanças epidemiológicas que se têm vindo a assistir, este vírus continua a ser transmitido fundamentalmente por via parentérica, isto é, drogas injectáveis, equipamentos médicos contaminados (ex: unidades de diálise), tatuagens, etc, e mais raramente através de transfusão de sangue, via sexual ou perinatal1,6. Alguns procedimentos cosméticos, religiosos ou culturais continuam a levantar controvérsias7.
O risco de transmissão do VHC é determinado pela infecciosidade do fluido orgânico e pela natureza dos tecidos expostos. Após exposição, a probabilidade de infecção depende fundamentalmente dos seguintes factores: a) via de transmissão, isto é, pele intacta, mucosa ou via percutânea, b) concentração das partículas virais no fluido implicado8, e c) volume de material infectante5. A profundidade da picada, a utilização de agulha oca e a co-infecção pelo VIH, são os três factores mais importantes associados a um maior risco de transmissão1,9.
No caso do Profissional de Saúde a infecção ocorre sobretudo por exposição ao sangue através das vias percutâneaou mucosa. Outros fluidos podem considerar-se potencialmente infecciosos (LCR, líquido sinovial, pleural, peritoneal e amniótico)5, não havendo, no entanto, qualquer registo de infecção após a exposição aos mesmos. Também e apesar de alguns casos relatados de exposição a grandes volumes de sangue a nível de pele intacta, nenhum caso foi identificado através desta via5. A transmissão através de exposição mucosa foi descrita em casos em que grande quantidade de sangue salpicou os olhos de um P.S.8
Segundo o Centers for Disease Control (CDC) o risco de transmissão do VHC após picada com agulha contaminada é cerca de 5 a 6 vezes superior ao do VIH (1,85 versus 0,36%)5,8, apesar de estudos mais recentes registarem taxas mais baixas (0,2 - 0,5%)10-13. Obviamente há que ter em conta vários factores que podem modificar estas percentagens: os viriões penetram através da pele e este inóculo é significativamente mais infeccioso se a exposição resultar de uma picada com agulha oca ou caso se trate de uma fonte com altos níveis de RNA-VHC8. Após a transmissão do VHC a evolução está dependente de factores do hospedeiro e de factores virais. O modo de transmissão e a idade de aquisição também alteram o curso desta infecção1.
Apesar da detecção da hepatite C aguda ser difícil, visto ser na maioria dos casos assintomática, 15 a 20% do total das hepatites agudas diagnosticadas são da responsabilidade do VHC14-16. O quadro de hepatite aguda ocorre em geral, 2 a 12 semanas após a exposição (média 7 semanas) e dura 2 a 12 semanas17, 10 - 15% dos indivíduos com hepatite C aguda têmuma resolução espontânea18, sendo esta probabilidade maior nos casos sintomáticos comparativamente com as formas subclínicas ou assintomáticas1,15,19-22. Nas formas sintomáticas, a clearance viral ocorre em quase metade dos casos, tendo lugar por volta da 10ª - 12ª semana após o início dos sintomas15. Inversamente alguns estudos demonstraram que em nenhum dos indivíduos assintomáticos ocorreu a eliminação espontânea do VHC15. (Fig. 1)
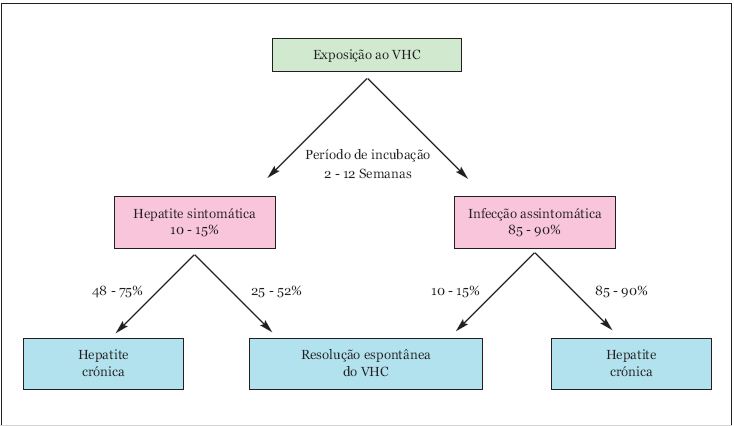
Fig. 1. Exposição ao VHC.
O quadro clínico da hepatite aguda é geralmente precedido de fadiga, mialgias, náuseas, vómitos, dores abdominais ou febre baixa15,23. Este quadro é ligeiro na maioria dos casos, podendo raramente assumir formas mais severas e prolongadas ou evoluir para formas fulminantes1,15. Estas últimas ocorrem sobretudo na presença de alguns cofactores, nomeadamente em utilizadores de drogas endovenosas (UDEV) e na infecção concomitante pelo VIH24. Só em 10 a 20% dos casos ocorre icterícia19, embora alguns estudos revelem percentagens mais elevadas em UDEV e em idosos (69%)1. Parece que os doentes que desenvolvem icterícia tendem a ter taxas maiores de resolução espontânea do VHC, comparativamente com os que têm infecção assintomática1,25. A icterícia, bem como a presença de sintomas de um modo geral, parecem ser bons indicadores de resposta imune do hospedeiro, originando maior probabilidade de clearance viral25.
Outros factores têm sido descritos como estando associados a uma maior taxa de resolução espontânea, tais como sexo feminino15,25, raça branca15,26, genótipo 327, virémia baixa28 e um rápido declínio do valor do RNA-VHC nas primeiras 4 semanas20, facto verificado no caso acima descrito. Pelo contrário a raça negra e a co-infecção pelo VIH estão associadas a uma mais elevada taxa de persistência da infecção1.
No caso descrito, o sexo feminino, a idade e a raça branca constituíram factores favorecedores da resolução espontânea do VHC.
Vários mecanismos parecem contribuir para a persistência do vírus, tais como uma ineficácia da resposta das células T perante a infecção viral, elevada taxa de mutações, desenvolvimento de quasispécies29 e uma possível interacção entre as proteínas virais e variadas proteínas intracelulares do hospedeiro15,25.
A eliminação espontânea do VHC tem sido observada nos primeiros meses desta interacção entre o vírus e o hospedeiro. Uma vez estabelecida a infecção crónica, a resolução espontânea é rara, daí este período inicial ser de crucial importância na evolução da doença15.
Em geral, em todos aqueles em que a infecção resolve espontaneamente, os níveis de RNA-VHC permanecem indetectáveis25.
Apesar de não serem comuns valores das aminotransferases superiores a 10 vezes o valor normal (VN), há casos registados com valores acima de 20 VN15,23, o que se verificou no caso acima relatado.
Não há teste serológico específico para a detecção da hepatite C aguda. A presença de anticorpos isolados não tem valor diagnóstico e muitas vezes aquela só é suspeitada quando os indivíduos já têm anti-VHC positivo. Num Profissional de Saúde torna-se mais fácil a documentação da infecção após a ocorrência de uma exposição acidental. A seroconversão num indivíduo previamente negativo é a forma de estabelecer o diagnóstico correcto.
Assim, é sugestivo de u ma hepatite C aguda, a presença de pelo menos um dos seguintes critérios: a) exposição conhecida ou suspeita ao VHC nos 4 meses precedentes, b) documentação de seroconversão recente (anti-VHC negativo para anti-VHC positivo), c) elevação da ALT (> 20 VN) e d) exclusão de outras causas de doença hepática1, 23.
O IgM anti-VHC não provou ser um bom marcador, visto que as suas concentrações permanecem mais ou menos constantes, quer nas formas agudas, quer crónicas1,30. O IgG anti-VHC é detectável apenas por volta dos 2 a 3 meses após a exposição, embora técnicas mais recentes o detectem mais precocemente. São os testes qualitativos ou quantitativos para detecção do RNA-VHC, que nos permitem estabelecer o diagnóstico, sendo por vezes os únicos testes positivos na infecção aguda (ex: real-time (RT) PCR, branched DNA (bDNA), transcription-mediated amplification (TMA))1. A detecção do RNA-VHC sem a presença do anticorpo, sugere uma hepatite C aguda, especialmente quando seguida de seroconversão.
No momento do acidente o P.S. deve realizar os chamados testes baseline, nomeadamente bioquímica, Anti-VHC e RNAVHC5; a sua realização vai permitir conhecer o status do profissional.
Durante o seguimento, a bioquímica e um teste virológico devem ser repetidos entre as 2 e as 4 semanas; nesta altura, e devido à flutuação do RNA-VHC, recomenda-se também a realização do anti-VHC, para que o teste virológico não seja o único marcador nesta fase. Foi demonstrado no homem, a presença do RNA-VHC entre os 3 e os 14 dias após a exposição ao vírus8,31-32. Um teste virológico positivo entre a 5ª e a 6ª semana (pelo menos sem grande decréscimo em relação ao valor inicial) traduz uma baixa probabilidade de clearance viral23. A importância da repetição do RNA-VHC baseia-se, por um lado, na ocorrência de casos raros de falsos positivos e, por outro lado, nas flutuações que o RNA-VHC sofre no decurso de uma hepatite C aguda, o que reforça a necessidade da sua realização algumas semanas mais tarde em todos os indivíduos com resultado negativo mas com suspeita da infecção aguda8,30.
O controlo clínico e laboratorial depende da evolução, permitindo assim acompanhar a necessidade de tratamento.
Se por um lado pode não ser necessário tratar um Profissional de Saúde que poderá ter hipóteses de resolução espontânea, por outro lado, esta vigilância permite evitar a evolução para a cronicidade (ver Proposta de Controlo Laboratorial). (Quadro 1)
Quadro 1. Proposta de controlo laboratorial.
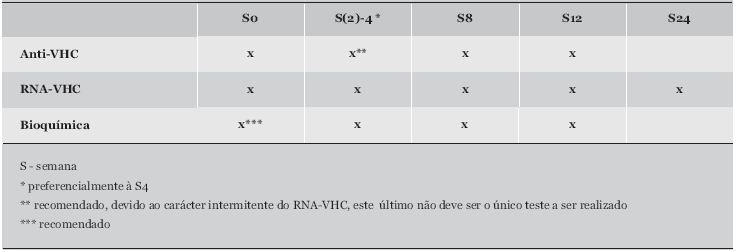
Todos os estudos realizados têm demonstrado que há benefício em tratar a hepatite C aguda, ficando claramente reduzido o risco de evolução para a cronicidade1,23,25,33. Num artigo em que são analisados 17 estudos, envolvendo 369 doentes tratados, foi demonstrada uma Resposta Viral Sustentada (RVS – RNA-VHC indetectável 24 semanas após final do tratamento) em 62% nos doentes tratados, comparativamente com 12% nos não tratados18. A possibilidade de cura pode atingir os 91% nos indivíduos sintomáticos7. Jeackel et al obteve com IFN alfa-2b em monoterapia, durante 24 semanas, uma RVS de 98%, independentemente do genótipo, utilizando uma dose de indução diária de 4 semanas33.
Apesar de não estar bem definido qual a terapêutica ideal, o tratamento com Interferão Peguilado (PEG-IFN) demonstrou melhores resultados comparativamente com o IFN convencional23,25,34-35.
Enquanto Kamal et al em 2004, com a utilização do IFN convencional conseguiu 85% de RVS36, um estudo alemão mais recente, demonstrou em 89 doentes tratados com PEG-IFN alfa-2b durante 24 semanas, uma percentagem global de cura de 71%, que atingiu 89% (70/89), nos doentes com boa adesão ao tratamento23. Tal como em outros estudos, o tratamento foi bem tolerado.
A questão mais importante é conhecer o timing apropriado. Os estudos até agora realizados não são muitos e os tamanhos das amostras nem sempre suficientemente demonstrativos. Não está bem definido se é melhor tratar imediatamente ou aguardar até que haja indícios de que o doente vá ou não desenvolver uma infecção crónica, não havendo infelizmente marcadores que nos façam predizer esta evolução.
O estudo de Kamal25 que envolveu uma amostra importante de doentes (n = 175), verificou uma RVS de 95,3%, 93,2%, 76,6%, respectivamente, consoante início da terapêutica à 8ª, 12ª ou 20ª semana. Quanto à relação RVS/genótipo os resultados foram: G1 - 72%, G2 - 100%, G3 - 93% e G4 - 84%. Nos indivíduos com genótipo 1, a melhor RVS foi conseguida quando o tratamento foi iniciado à 8ª semana, versus 12ª ou 20ª semana. No G4, não se verificaram diferenças entre a 8ª ou 12ª versus semana 20. O estudo sugere que, exceptuando no G1, iniciar o tratamento da fase aguda à 8ª ou 12ª semana, não altera a eficácia do tratamento.
Relativamente ao G4 e pelo facto da população portuguesa estar maioritariamente infectada pelo G4 c/d37 o seu comportamento em termos de sucesso terapêutico assemelha-se muito ao G138, ao invés dos resultados apresentados por Kamal e outros autores39. Nesses países o genótipo predominante é o 4a, que tem uma resposta à terapêutica, que mais se aproxima do G2 e G3. Entre nós seria razoável, que a atitude perante o genótipo 4 fosse semelhante à do genótipo 1.
Independentemente do momento em que deve iniciar o tratamento da hepatite C aguda, parece que um período de 12 semanas permite uma RVS de 88,5%, com boa tolerância e poucas descontinuações terapêuticas ou necessidade de ajuste de dose25.
Segundo os dados de Kamal et al, no follow-up destes doentes tratados, verificou-se que a resposta viral se mantém para além de 48 semanas após o final do tratamento, sugerindo que o tratamento da infecção aguda reduz claramente a evolução para formas crónicas25,40.
Concluindo e esquematizando as questões mais frequentes:
1) Qual o momento certo para iniciar tratamento, considerando a possibilidade de resolução espontânea?
Admitindo que 1) a presença de RNA-VHC à 5ª - 6ª semana, com valores sobreponíveis aos iniciais, traduz uma baixa probabilidade de resolução23 2) o sucesso terapêutico não difere muito, com o início do tratamento à 8ª ou 12ª (salvo no genótipo G1)25, uma estratégia razoável seria uma vigilância apertada e iniciar tratamento à 12ª semana, nos casos sintomáticos, caso a virémia continue detectável18,25, admitindo-se um início mais precoce (8ª semana) nos indivíduos assintomáticos7,35,41 e em indivíduos com G1 e virémias acima de 800 000 IU/mL42.
2) Qual o melhor esquema terapêutico?
O uso do PEG-IFN é indiscutível, pelos melhores resultados obtidos, comparativamente com o Interferão convencional23,25.
A combinação de PEG-IFN + Ribavirina ainda não foi testada extensivamente de forma a que permita concluir que o seu uso combinado seja melhor que o PEG-IFN em monoterapia.
Os estudos já realizados demonstraram que a terapêutica dupla não modifica muito os resultados35,36; no entanto, poder-se-á propor a terapêutica em associação nos casos de coinfecção pelo VIH e genótipo 1, isto é, reservar a Ribavirina para os casos mais difíceis de tratar1. (Quadro 2)
Quadro 2. Proposta de terapêutica.

3) Qual o tempo de tratamento?
Uma estratégia adequada seria tratar durante 12 semanas42 e reservar um tempo mais prolongado de 24 semanas, se não se verificar resposta à 4ª semana e em outras situações: genótipo 1, cargas virais elevadas, co-infecção pelo VIH, Não Respondedor ou Relapser em esquema curto anterior. O tempo apropriado de follow-up destes doentes deve ser de 1 ano após o tratamento, no sentido de vigiar uma possível recaída18.
Como em tudo, a prevenção é a melhor estratégia para reduzir o risco e não havendo vacina nem profilaxia pós-exposição, as medidas devem assentar em princípios, tais como práticas/uso das precauções universais de forma correcta e sistemática.
REFERÊNCIAS
1. Maheshwari A, Ray S, Thuluvath PJ. Acute hepatitis C. Lancet 2008;372:321-332.
2. Thomas DL, Seeff LB. Natural history of hepatitis C. Clin Liver Dis 2005;9:383-398.
3. Seeff LB. Natural history of chronic hepatitis C. Hepatology 2002;36:S35-S46.
4. Williams IT, Perz JF, Bell BP. Viral hepatitis transmission in ambulatory health care settings. Clin Infect Dis 2004;38:1592-1598.
5. Centers for Disease Control and Prevention. Updated US Public Health Service Guidelines for the management of occupational exposures for HBV, HCV and HIV and recommendations for post exposure prophylaxis. MMWR Morb Mortal Wkly Rep 2001;50:1-67.
6. Orland JR, Wright TL, Cooper S. Acute hepatitis C. Hepatology 2001;33: 321-327.
7. Shepard CW, Finelli L, Alter MJ. Global epidemiology of hepatitis C virus infection. Lancet Infect Dis 2005;5:558-567.
8. Sulkowski MS, Ray S, Thomas DL. Needlestick transmission of hepatitis C. JAMA 2002;287:2406-2413.
9. Campbell SR, Srivastava P, Williams I, et al. Hepatitis C virus infection after occupational exposure. Infect Control Hosp Epidemiol 2000;21:107.
10. Chung H, Kudo M, Kumada T, et al. Risk of HCV transmission after needlestick injury and the efficacy of short-duration interferon administration to prevent HCV transmission to medical personnel. J Gastroenterol 2003;38:877-879.
11. De Carli G, Puro V, Ippolito G. Studio italiano rischio occupazionale da HIV Group. Risk of hepatitis C virus transmission following percutaneous exposure in healthcare workers. Infection 2003;31:22-27.
12. Wiegand J, Aslan N, Ciner A, et al. Kinetics of HCV-specific CD4+ and CD8+T cell responses during and after therapy with pegylated interferon-alfa-2B in patients with acute hepatitis C. Hepatology 2004;40:256A.
13. Jagger J, Puro V, De Carli G. Occupational transmission of Hepa titis C virus (Letter). JAMA 2002;288:1469.
14. Armstrong GL, Alter MJ, McQuillanGM, et al. The past incidence of hepatitis C virus infection: implications for the future burden of chronic liver disease in the United States. Hepatology2000;31:777-782.
15. Gerlach JT, Diepolder HM, Zachoval R, et al. Acute hepatitis C: high rate of both spontaneous and treatment-induced viral clearance. Gastroenterology 2003;125:80-88.
16. Williams I. Epidemiology of hepatitis C in the United States. Am J Med 1999;107:2S-9S.
17. Marcellin P. Hepatitis C: the clinical spectrum of the disease. J Hepatology 1999;31:9-16.
18. Albert A, Boccato S, Vario A, et al. Therapy of acute hepatitis C. Hepatology 2002;36:S195-200.
19. Alter MJ, Margolis HS, Krawcznski K, et al. The natural history of community-acquired hepatitis C in the United States. N Engl J Med 1992;327:1899-1905.
20. Hofer H, Watkins-Riedel T, Janata O, et al. Spontaneous viral clearance in patients with acute hepatitis C can be predicted by repetead measurements of serum viral load. Hepatology 2003:37:60-64.
21. Hoofnagle JH. Course and outcome of hepatitis C. Hepatology 2002;36:S21-29.
22. Licata A, Di Bona D, Schepis F, et al. When and how to treat acute hepatitis C? J Hepatol 2003;39:1056-1062.
23. Wiegand J, Buggisch P, Boecher W, et al. Early monotherapy with pegylated Interferon alpha-2b for acute hepatitis C infection: the HEP-NET Acute-HCV-II Study. Hepatology 2006;43:250-256.
24. Deterding K, Wedemeyer H. Update on treatment of acute Hepatitis C. Em: Maria Buti, Rafael Esteban, eds. BC. VH Viral Hepatitis 2006:218-277.
25. Kamal SM, Fouly AE, Kamel RR, et al. Peginterferon alpha-2b therapy in acute hepatitis C: Impact of onset of therapy on sustained virologic response. Gastroenterology 2006;130:632-638.
26. Thomas DL, Asremborki J, Rai RM, et al. The natural history of hepatitis C infection: host, viral and environmental factors. JAMA 2000;284:450-456.
27. Lehmann M, Meyer MF, Monazahian M, et al. High rate of spontaneous clearance of acute hepatitis C virus genotype 3 infection. J Med Virol 2004;73:387-391.
28. Villano SA, Vlahov D, Nelson KE, et al. Persistence of viremia and the importance of long-term follow-up after acute hepatitis C infection. Hepatology 1999;29:908-914.
29. Chang KM, Rehermann B, McHutchison JG, et al. Immunological significance of cytotoxic T lymphocyte epitope variants in patients chronically infected by the hepatitis C virus. J Clin Invest 1997;100:2376-2385.
30. Lange C, Sarrazin. Acute and chronic hepatitis C- diagnostic tests. Em: Mauss, Berg, Rockstroh, Sarrazin, Wedemeyer, eds. Hepatology 2009. Clinical Text Book. 1ª ed. Duesseldorf: Flying Publisher; 2009.p.171-182.
31. Mosley JW, Operskalski EA, Tobler LH, et al. Viral and host factors in early hepatitis C virus infection. Hepatology 2005;42:86-92.
32. Pawlotsky JM. Use and interpretation of virological tests for hepatitis C. Hepatology 2002;36:215-217.
33. Jaeckel E, Cornberg M, Wedemeyer H, et al. Treatment of acute hepatitis C with interferon alfa-2b. N Engl J Med 2001;345:1452-1457.
34. Santantonio T, Fasano M, Sinisi E, et al. Efficacy of a 24-week course of PEG-interferon alpha-2b monotherapy in patients with acute hepatitis C after failure of spontaneous clearance. J Hepatol 2005;42:329-333.
35. Cornberg M, Manns M, Wedemeyer H. Standard of care. Em: Mauss, Berg, Rockstroh, Sarrazin, Wedemeyer, eds. Hepatology 2009. Clinical Text Book. 1ª ed. Duesseldorf: Flying Publisher; 2009.p.183-210.
36. Kamal SM, Ismail A, Graham CS, et al. Pegylated interferon alpha therapy in acute hepatitis C: relation to hepatitis C virus-specific T cell response kinetics. Hepatology 2004;39:1721-1731.
37. Valente C. Co-infecção VIH/VHC. Revista Portuguesa de Doenças Infecciosas 2007;3:78-86. [ Links ]
38. Ramos E, Ribeiro J, Fernandes C, et al. Resposta ao tratamento dos doentes infectados pelo VHC-genótipo 4 – diferenças entre mono e co-infectados VIH/VHC. 4ª Reunião Co-Infecção VIH/hepatites. Livro de Resumos. P7 Óbidos, 21 de Maio de 2009.
39. El-Zayadi A, Attia M, Barakat E, et al. Response of hepatitis C genotype 4 naïve patients to 24 weeks of Peg-Interferon-alpha 2b/Ribavirin or Induction-dose Interferon-alpha 2b/Ribavirin Amantadine: a non-randomized controlled study. Am J Gastroenterol 2005;100:2447-2452.
40. Wiegand J, Jaeckel E, Cornberg M, et al. Long-term follow-up after successful interferon therapy of acute hepatitis C. Hepatology 2004;40:98-107.
41. Strader DB, Wright T, Thomas DL, et al. Diagnosis, Management and Treatment of hepatitis C. AASLD Practice Guideline. Hepatology 2004;39:1147-1171.
42. Ghany MG, Strader DB, Thomas DL, et al. Diagnosis, Management and treatment of hepatitis C: an update (AASLD Practice Guidelines). Hepatology 2009;49:1335-1374.
Cristina Valente;
E-mail: cristinavalente@chc.min-saude.pt
Recebido para Publicação: 16/04/2009 e Aceite para Publicação: 05/07/2010.













