Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Jornal Português de Gastrenterologia
versão impressa ISSN 0872-8178
J Port Gastrenterol. vol.19 no.5 Lisboa set. 2012
Megacólon tóxico como forma de apresentação de colite ulcerosa grave: um desafio clínico
Toxic megacolon as first manifestation of severe ulcerative colitis: A clinical challenge
Pedro Barreiro∗, Cristina Chagas, Gilberto Couto e Leopoldo Matos
Serviço de Gastrenterologia, Centro Hospitalar de Lisboa Ocidental, Lisboa, Portugal
*Autor para correspondência
Resumo
As agudizações da colite ulcerosa apresentam um largo espectro de gravidade clínica, desde quadros ligeiros, subclínicos, até quadros de colite fulminante ou megacólon tóxico ameaçadoras da vida do doente. Nestes últimos, a resposta à corticoterapia é usualmente eficaz, contudo cerca de 30% dos doentes revelam-se resistentes aos corticoides.
Apresentamos o caso clínico de uma mulher de 45 anos que desenvolve quadro de megacólon tóxico como primeira manifestação de colite ulcerosa corticorrefratária. Neste caso, foi realizada terapêutica médica precoce com infliximab, observando-se excelente resposta clínica e endoscópica.
Fazemos uma breve revisão da abordagem clínica da colite ulcerosa grave e corticorefratária.
Palavras-chave Colite ulcerosa corticorefractária; Megacólon tóxico; Infliximab
Abstract
Exacerbations of ulcerative colitis can lead to a wide spectrum of clinical manifestations from mild severity, sub-clinical, to fulminant colitis or toxic megacolon, which can threat the life of the patient. In the latter, the response to steroids is usually effective, yet about 30% of patients fail to respond, being steroids refractory.
Here, we present the case of a 45 years old woman who developed a toxic megacolon as a first manifestation of a steroid refractory ulcerative colitis. The early use of medical therapy with infliximab resulted in an excellent clinical and endoscopic response.
We briefly review the clinical approach to severe ulcerative colitis and steroid-refractory.
Keywords Steroid refractory ulcerative colitis; Toxic megacolon; Infliximab
Introdução
O espectro de atividade da colite ulcerosa (CU) é variável e o seu curso clínico pode ser imprevisível. Embora a maioria destes doentes apresente evolução favorável da doença com episódios de agudização e remissão capazes de serem resolvidos com recurso a salicilatos e corticoesteroides per os, cerca de 15-20% irá apresentar agudizações graves com necessidade de hospitalização1.
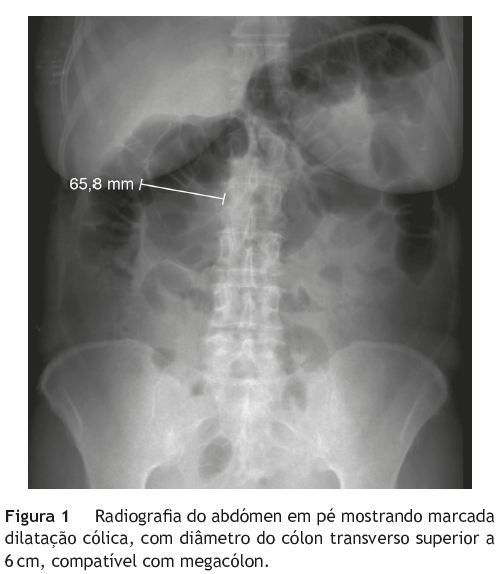
Recentemente o American College of Gastroenterology e o European Crohns and Colitis Organization definiram como agudização grave a presença de 6 ou mais dejeções por dia e evidência de sinais de toxicidade sistémica demonstrados por febre, taquicardia, anemia ou elevação da velocidade de sedimentação2,3. Se existir dilatação cólica não obstrutiva (mais de 6 cm de diâmetro no cólon transverso) associada aos achados tóxicos sistémicos, estamos perante um quadro de megacólon tóxico, uma emergência médica potencialmente fatal que exige rápida e agressiva monitorização e intervenção médica-cirúrgica4.
Ainda que a maioria dos doentes com CU grave responda à corticoterapia, cerca de 30% são refratários, restando a terapêutica médica de 2.a linha com infliximab ou ciclosporina, ou a abordagem cirúrgica5.
Caso clínico
Apresentamos o caso clínico de uma mulher de 45 anos, caucasiana, sem antecedentes pessoais relevantes, que iniciou quadro de diarreia aquosa (3-4 dejeções por dia) com 4 dias de evolução, acompanhada de cólicas abdominais, náuseas, mal-estar geral e períodos subfebris (37,0 ◦C- 37,5 ◦C). No exame objetivo destacou-se pele e mucosas ligeiramente desidratadas, temperatura axilar de 37,2 ◦C e dor abdominal difusa ligeira a moderada. Analiticamente, apresentava hemoglobina (Hb) de 13,2 g/dl, com leucocitose de 14 100 cél/mm3 e elevação da proteína C reativa (PCR) com 5,2 mg/dl. Nesta altura, a doente iniciou em ambulatório ciprofloxacina (500 mg de 12/12H via oral) e terapêutica sintomática com antiemético e antipirético, aconselhando-se reforço hídrico e dieta com restrição de gorduras, resíduos e lactose. Todavia, foi observado um agravamento da sintomatologia ao longo das primeiras 96 horas após o início da antibioterapia com aumento do número de dejeções diárias (6-7) com presença esporádica de sangue, persistência das cólicas abdominais, anorexia e astenia marcada. Nesta ocasião encontrava-se desidratada, pálida, febril (38,0◦-38,5 ◦C), taquicárdica (112 bpm), hipotensa (TA - 95/47 mmHg), apresentando o abdómen distendido e doloroso à palpação sem evidência de irritação peritoneal. Laboratorialmente, destacava-se descida da Hb (11,8 g/dl), agravamento dos parâmetros inflamatórios (leucócitos - 15 400 cél/mm3; PCR - 15,1 mg/dl; velocidade de sedimentação - 40 mm/hora), insuficiência renal ligeira (creatinina - 1,4 mg/dl; ureia - 72 mg/dl) e hipocaliémia (K+ - 3,1 mmol/L). A radiografia do abdómen em pé mostrou distensão do cego e transverso com cerca de 4,5 cm de diâmetro, sem níveis hidroaéreos. A ecografia abdominal e a tomografia computorizada abdominal revelaram espessamento parietal de todo o cólon, mais exuberante no cego, e adenopatias na raiz do mesentério. Neste contexto, a doente foi internada iniciando-se correção hidroeletrolítica, terapêutica sintomática antipirética e analgésica (paracetamol) e antibioterapia com ciprofloxacina e metronidazol.
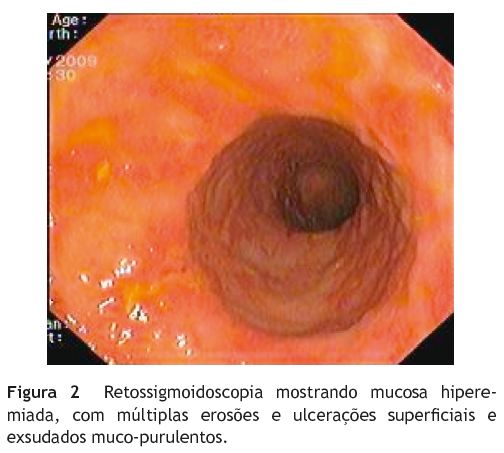
Nas primeiras 48 horas do internamento, a doente manteve quadro clínico com 7 dejeções diárias associadas a quadro de toxicidade sistémica com febre, taquicardia (100-110 bpm) e persistência dos parâmetros inflamatórios elevados. Repetiu radiografia do abdómen, que mostrou aumento da dilatação cólica ao nível do cego e cólon transverso, atingindo este último um diâmetro de 6,5 cm, compatível com quadro de megacólon tóxico (fig. 1). Nesse mesmo dia, realizou retossigmoidoscopia flexível, com insuflação mínima e progressão somente até aos 35 cm, registando-se em toda a mucosa observada a presença de múltiplas erosões e ulcerações superficiais com exsudado mucopurulento, associadas a marcada hiperémia e perda da rede vascular da mucosa (fig. 2). Foi colocada a hipótese diagnóstica de uma primeira manifestação de CU com atividade grave complicada com megacólon tóxico, não sendo possível nesta altura a exclusão de etiologia infecciosa. Desta forma, iniciou-se corticoterapia (prednisolona 60 mg endovenoso por dia) e antibioterapia de largo espectro (piperacilina-tazobactam 4,5 g de 8/8H e metronidazol 500 mg de 8/8H por via endovenosa). Adicionalmente, foram instituídas medidas de descompressão intestinal com colocação de sonda nasogástrica, sonda retal, mobilização periódica da doente da posição de supinação para pronação e dieta zero.
Vinte e quatro horas após a otimização da terapêutica observou-se resolução do megacólon tóxico (cólon transverso com 5 cm nesta altura), contudo sem melhoria clínica satisfatória ao 3.◦ e 7.◦ dias, mantendo-se febril (37,5◦- 38,0 ◦C), com 4-5 dejeções diárias com sangue, cólicas abdominais e parâmetros inflamatórios elevados.
Entretanto, os exames culturais seriados (hemoculturas e coproculturas), a pesquisa da toxina A e B do Clostridium difficile e o estudo parasitológico das fezes foram negativos. O resultado das biopsias da mucosa cólica corroborou a hipótese de CU em fase ativa sem identificação de microrganismos patogénicos ou superinfeção por citomegalovírus.
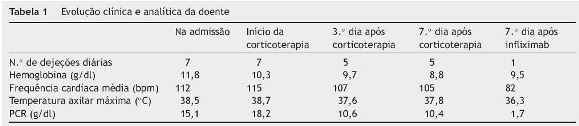
Por persistência da atividade moderada/grave da doença após 7 dias de corticoterapia, optou-se pela instituição de terapêutica biológica com infliximab na dose de 5 mg/kg. Nos primeiros 7 dias após a primeira administração observou-se rápida normalização do trânsito intestinal (1-2 dejeções por dia com consistência mantida e sem evidência de perdas hemáticas), mantendo-se apirética, hemodinamicamente estável e com progressiva normalização dos parâmetros laboratoriais (nomeadamente da Hb e parâmetros inflamatórios) (tabela 1).
A doente apresenta 5 meses de seguimento, encontrando-se em remissão sob dose de manutenção com infliximab (5 mg/kg de 8/8 semanas, após 3 doses de indução às semanas 0, 2 e 6) e já sem corticoterapia concomitante, que se suspendeu ao fim de 3 meses após desmame progressivo. 2 meses depois do início da terapêutica, foi realizada colonoscopia total, que mostrou mucosa cólica com pólipos inflamatórios dispersos, contudo, sem evidência endoscópica de atividade da doença.
Discussão
A maioria dos doentes com CU tem manifestações ligeiras ou moderadas de doença, contudo cerca de 10% tem como apresentação inaugural quadro de colite grave ou, mais raramente, de megacólon tóxico6. O caso clínico apresentado é exemplo de um desses casos: a rápida instalação de um quadro de doença cólica grave, de etiologia inicialmente não esclarecida, com evidente repercussão sistémica e desenvolvimento de megacólon exigiu uma rápida e eficaz intervenção médica. Assim, na forte suspeita de CU grave, ainda que sem confirmação histológica e com os exames culturais em curso, optou-se por iniciar corticoterapia endovenosa (60 mg por dia) associada a antibióticos de largo espectro. Esta opção terapêutica tem-se revelado segura, mesmo quando mais tarde a etiologia revela ser infecciosa3. Na verdade, vários estudos controlados não mostraram benefício da utilização de antibióticos na CU grave; contudo, esta deverá ser ponderada na suspeita de infeção nomeadamente nos episódios inaugurais de colite ulcerosa em que ainda não se excluiu etiologia infecciosa, assim como nos quadros de megacólon tóxico ou previamente à abordagem cirúrgica, quando necessária6-9. Adicionalmente, a dose de corticoterapia utilizada neste caso parece ser a ideal tendo em conta a relação risco/benefício: doses mais elevadas não parecem trazer maior benefício clínico e relacionam-se com mais efeitos adversos7.
Tão importante como o início precoce da terapêutica dirigida é a monitorização apertada da resposta à mesma, com avaliação clínica, analítica e radiológica diária. Doentes sem resolução do megacólon tóxico após 48-72 horas de terapêutica intensiva ou com evidência de complicações como perfuração, hemorragia maciça ou falência multiorgânica têm indicação para colectomia de urgência7,8. No caso clínico apresentado observou-se rápida resolução do megacólon com corticoterapia; contudo, a resposta aos corticoides manteve-se insatisfatória. De facto, um dos maiores desafios nestas situações é a identificação precoce dos doentes com resposta insatisfatória à corticoterapia. A sua identificação permite o início precoce de terapêutica médica de 2.a linha e, desta forma, diminui a necessidade de colectomia e, caso esta seja necessária, reduz o seu atraso inapropriado6,7,9. Várias têm sido as abordagens criadas com este objetivo7,9,10. Um dos algoritmos mais simples e úteis é a avaliação ao 3.a dia após início de terapêutica intensiva, do número de dejeções diárias e do valor da PCR. A persistência de mais de 8 dejeções ou mais de 3 dejeções associadas a um valor de PCR superior a 4,5 mg/dl (índice de Oxford) predizem a necessidade de colectomia em 85% dos casos11. Por outro lado, a ausência de resposta evidente aos corticoides ao fim de 7 dias torna muito improvável uma resposta posterior5. Desta forma, ao 3.◦ dia de corticoterapia deve tentar-se a identificação dos doentes refratários, avaliando-se a eventual necessidade de terapêutica médica de 2.a linha ou colectomia. Esta decisão deve ser tomada até ao 5.◦-7.◦ dia6,8.
Quer os inibidores da calcineurina (ciclosporina e tacrolimus) quer o infliximab têm-se revelado 2 opções válidas nos casos de colite ulcerosa grave corticorefratária2,6,7,12. Porém, a ausência de estudos comparativos dificulta a opção terapêutica6,7,12. A decisão deverá então ser individualizada, tendo em conta eventuais contraindicações, terapêuticas prévias do doente e experiência clínica local6. Apesar de a eficácia da ciclosporina na capacidade de indução da remissão ter sido demonstrada na ordem dos 50-80% dos casos, não parece ser eficaz na manutenção da mesma, reservando-se, na maioria das vezes, como «ponte» para outra terapêutica imunosupressora6,7. Assim, caso o doente apresente uma agudização já sob tratamento imunosupressor (p. ex. azatioprina) ou intolerância a essa medicação, o papel da ciclosporina é reduzido a médio/longo prazo. Neste contexto, o infliximab revela-se uma melhor opção, visto que se encontra indicado tanto para a indução da remissão como para a sua manutenção. A resposta clínica a estes fármacos verifica-se usualmente entre o 4.◦ e o 7.◦ dia, estando recomendada a abordagem cirúrgica se não se obtiver eficácia terapêutica até essa altura8. No caso clínico descrito optou-se por iniciar infliximab, muito devido à experiência do centro no uso deste fármaco e ao facto de ser uma opção válida não só para a remissão, mas também para a manutenção da doença, obtendo-se excelente resposta a curto/médio prazo.
Apesar do desenvolvimento das terapêuticas médicas e otimização dos protocolos de abordagem destes doentes, a colite ulcerosa grave com megacolón tóxico constitui ainda um desafio clínico, pois é potencialmente ameaçadora da vida.
Bibliografia
1. Langholz E, Munkholm P, Davidsen M, Binder V. Course of ulcerative colitis: Analysis of changes in disease activity over years. Gastroenterology. 1994;107:3-11. [ Links ]
2. Kornbluth A, Sachar D. Ulcerative colitis practice guidelines in adults (update): american college of gastroenterology, practice parameters committee. Am J Gastroenterol. 2004;99: 1371-85. [ Links ]
3. Stange EF, Travis SPL, Vermeire S, Reinisch W, Geboes K, Barakauskiene A. European evidence-based consensus on the diagnosis and management of ulcerative colitis: definitions and diagnosis. J Crohns Colitis. 2008;2:1-23. [ Links ]
4. Fazio VW. Toxic megacolon in ulcerative colitis and Crohns colitis. Clin Gastroenterol. 1980;9:389-407. [ Links ]
5. Turner D, Walsh CM, Steinhart AH, Griffiths AM. Response to corticosteroids in severe ulcerative colitis: a systematic review of the literature and a meta-regression. Clin Gastroenterol Hepatol. 2007;5:103-10. [ Links ]
6. Doherty GA, Cheifetz AS. Management of acute severe ulcerative colitis. Expert Rev Gastroenterol Hepatol. 2009;3:395-405. [ Links ]
7. Travis SPL, Stange EF, Lémann M, Oresland T, Bemelman WA, Chowers Y, et al. European evidence-based consensus on the diagnosis and management of ulcerative colitis: current management. J Crohns Colitis. 2008;2:24-62. [ Links ]
8. Caprilli R, Viscido A, Latella G. Current management of severe ulcerative colitis. Nat Clin Pract Gastroenterol Hepatol. 2007;4:92-101. [ Links ]
9. Dunckley P, Jewell D. Management of acute severe colitis. Best Pract Res Clin Gastroenterol. 2003;17:89-103. [ Links ]
10. Hyde GM, Jewell DP. Review article: the management of severe ulcerative colitis. Aliment Pharmacol Ther. 1997;11:419-24. [ Links ]
11. Travis SP, Farrant JM, Ricketts C, Nolan DJ, Mortensen NM, Kettlewell MG, et al. Predicting outcome in severe ulcerative colitis. Gut. 1996;38:905-10. [ Links ]
12. Caprilli R, Clemente V, Frieri G. Historical evolution of the management of severe ulcerative colitis. J Crohns Colitis. 2008;2:263-8. [ Links ]
Conflito de interesses
Os autores declaram não haver conflito de interesses.
*Autor para correspondência
Correio eletrónico: pedrobarreiro@msn.com (P. Barreiro).
Recebido a 14 de agosto de 2010; aceite a 29 de outubro de 2010













