Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Jornal Português de Gastrenterologia
versão impressa ISSN 0872-8178
J Port Gastrenterol. vol.20 no.2 Lisboa mar. 2013
https://doi.org/10.1016/j.jpg.2012.09.008
Infeções bacterianas no doente com cirrose hepática
Bacterial infections in patients with liver cirrhosis
Paulo Carrola ∗, Isabel Militão e José Presa
Unidade de Hepatologia, Centro Hospitalar de Trás-os-Montes e Alto Douro, EPE, Unidade de Vila Real, Vila Real, Portugal
*Autor para correspondência
RESUMO
As infeções bacterianas são uma complicação frequente na cirrose hepática, principalmente nos doentes internados.
Os autores fazem uma revisão da prevalência, fatores de risco e patogénese das infeções bacterianas no doente com cirrose hepática, salientando os mecanismos da translocação bacteriana.
As infeções bacterianas mais comuns na cirrose são as designadas infeções «espontâneas», nomeadamente a peritonite bacteriana espontânea, o empiema pleural bacteriano espontâneo e a bacteriémia espontânea.
No final, faz-se uma breve referência às estratégias de prevenção da infeção na cirrose, nomeadamente a profilaxia da peritonite bacteriana espontânea e a prevenção das infeções virais ou bacterianas específicas através da vacinação.
Palavras-Chave Infeção; Cirrose hepática; Translocação bacteriana
ABSTRACT
Bacterial infections are a frequent complication on hepatic cirrhosis, particularly in hospitalized patients.
In this article we review the prevalence, risk factors and pathogenesis of bacterial infections in cirrhotic patients, focusing on the mechanisms of bacterial translocation.
The most common bacterial infections in cirrhotic patients are the commonly called spontaneous infections, namely spontaneous bacterial peritonitis, spontaneous bacterial pleural empyema and spontaneous bacteraemia.
At the end of this article we make a brief reference to the prevention strategies for infection in cirrhosis, namely prophylaxis of spontaneous bacterial peritonitis and prevention of specific viral or bacterial infections through vaccination.
Keywords Infection; Liver cirrhosis; Bacterial translocation
Introdução
As infeções bacterianas são uma complicação importante na cirrose hepática, principalmente nos doentes internados1.
As infeções bacterianas ocorrem em 32 a 34% dos doentes hospitalizados com cirrose (versus 5 a 7% na população geral) e em cerca de 45% daqueles admitidos por hemorragia gastrointestinal2-4. A hemorragia gastrointestinal e a gravidade da doença hepática, refletida pela albumina sérica e pelo score Child-Turcotte-Pugh (CTP), são fatores preditivos independentes da infeção bacteriana nos doentes com cirrose5-7.
A etiologia alcoólica foi associada com maior frequência a infeções (68,9%), quando comparada com outras causas de cirrose hepática (30,4%), isto nos doentes com score CTP A ou B8,9. Nos doentes cirróticos com score CTP C, não existe diferença relativamente à frequência de infeção ou à mortalidade9.
A mortalidade intra-hospitalar dos doentes cirróticos com infeção é de cerca de 15%, mais do dobro daqueles sem infeção, subindo essa percentagem para valores superiores a 70% em caso de choque séptico1,10.
A infeção é diretamente responsável por cerca de 30% das mortes na cirrose11.
Os doentes com cirrose hepática estão predispostos a infeções devido a um sistema imune alterado e a um aumento quer do crescimento bacteriano intestinal quer da passagem das bactérias do intestino para locais extraintestinais (translocação bacteriana)12,13. A translocação bacteriana contribui para um agravamento do estado hemodinâmico do doente com cirrose hepática avançada, mesmo na ausência de infeção1.
As infeções no doente cirrótico são, em mais de 90% dos casos, bacterianas14. As mais frequentes são a peritonite bacteriana espontânea (PBE) (25%), infeções do trato urinário (20%), pneumonia (15%), bacteriémia (12%) e infeções dermatológicas (2 a 11%)3,15.
Numa meta-análise recentemente publicada por Arvaniti et al., a mortalidade nos doentes cirróticos com infeção foi, antes do ano 2000, de 47,7% e, após esta data, de 32,3% (p = 0,023)16. No que diz respeito à PBE, apenas a mortalidade a 30 dias foi reduzida (49 versus 31,5%; p = 0,005)16. O mesmo estudo conclui ainda que a infeção aumenta em 4 vezes a mortalidade dos doentes cirróticos (30% dos doentes morre dentro de um mês e outros 30% morre no primeiro ano)16.
Patogénese
A maior prevalência de infeções bacterianas nos doentes cirróticos deve-se a uma disfunção multifatorial do sistema imunitário que pode ser parcialmente atribuída a uma diminuição da atividade bactericida das células fagocíticas12,13. Adicionalmente, os níveis de complemento, que são críticos na fagocitose bacteriana, estão diminuídos na cirrose e o sistema reticuloendotelial (SRE), que constitui o principal sistema defensivo contra as bactérias e outras infeções adquiridas pela via hematogénica, está disfuncional17-19. A maior parte da atividade do SRE está localizada no fígado, onde as células de Kupffer (macrófagos teciduais) são os componentes major1. Na cirrose, a atividade do SRE está comprometida devido ao efeito do desvio portossistémico do fluxo sanguíneo e devido à ineficácia da atividade fagocítica das células de Kupffer1. O efeito do desvio portossistémico do fluxo sanguíneo permite ainda que produtos bacterianos como endotoxinas e citocinas entrem diretamente na circulação sistémica1.
As alterações hemodinâmicas da cirrose têm efeitos nefastos na motilidade intestinal, permeabilidade intestinal e microflora15. O sistema nervoso simpático hiperativo destes doentes atrasa a motilidade intestinal e facilita a estase e o crescimento bacteriano15. A presença de hipertensão portal resulta em edema da submucosa intestinal e compromete a integridade protetora da barreira da mucosa15. Todos estes efeitos associados resultam num desequilíbrio da microflora intestinal favorável ao excessivo crescimento das bactérias gram-negativas15.
As infeções nos doentes cirróticos não estão associadas aos microrganismos característicos de doentes imunodeprimidos. As bactérias gram-negativas, na sua maioria Escherichia coli, são isoladas mais frequentemente na PBE e nas infeções do trato urinário, enquanto as bactérias grampositivas são causas mais comuns de pneumonias (Streptococcus) e infeções relacionadas com instrumentação (Staphylococcus)3,15. Nas infeções adquiridas na comunidade, predominam as bactérias gram-negativas (60% dos isolados) enquanto nas infeções associadas a cuidados de saúde predominam as bactérias gram-positivas (60% dos isolados)20. As culturas são positivas em cerca de 50 a 70% dos casos20. As infeções fúngicas (Candida spp.) estão envolvidas em cerca de 15% dos casos de sépsis grave na cirrose10.
Translocação bacteriana
A translocação bacteriana consiste na migração de bactérias ou produtos bacterianos (lipopolissacarídeos-LPS e endotoxinas) do lúmen do intestino para locais extraintestinais como gânglios linfáticos mesentéricos21. A partir daqui, as bactérias entéricas e os seus produtos atingem a circulação sistémica a partir da qual se disseminam para outros locais, nomeadamente para o líquido ascítico14. Embora a passagem de bactérias comensais para os gânglios linfáticos seja um processo normal que resulta na destruição daquelas, a translocação bacteriana torna-se clinicamente significativa na cirrose devido a uma ineficiência dos mecanismos de defesa imune locais e sistémicos22,23.
A translocação bacteriana está significativamente aumentada nos doentes cirróticos com score CPT C (30%) comparativamente aos doentes com score CPT B (8%) e CPT A (3%)4.
Existem 3 fatores principais que contribuem para a translocação bacteriana: excessivo crescimento bacteriano intestinal, aumento da permeabilidade intestinal e disfunção do sistema imunitário1. Os trabalhos existentes até ao momento parecem favorecer a seguinte sequência de eventos: hiperproliferação bacteriana; aumento da permeabilidade intestinal; aumento da translocação de toxinas bacterianas e/ou de outras endotoxinas para o sistema circulatório; aumento dos mediadores pró-inflamatórios, nomeadamente o fator de necrose tumoral _ (TNF-_), interleucina (IL) 1 e 6 e espécies reativas de oxigénio pelas células de Kupffer; lesão celular do fígado e, provavelmente, de outros órgãos24.
A translocação bacteriana foi também implicada na exacerbação do estado de circulação hiperdinâmica nos doentes cirróticos1 (fig. 1). O estado de circulação hiperdinâmico da cirrose é caracterizado por vasodilatação esplâncnica e sistémica, aumento do débito cardíaco e redução da pressão arterial média. É responsável pelo crescimento das varizes, ascite e pela síndrome hepatorrenal. Este estado surge devido ao aumento dos níveis séricos de citocinas pró-inflamatórias como o TNF-_ com ativação subsequente do óxido nítrico (NO) na circulação sistémica e esplâncnica e posterior vasodilatação25,26.
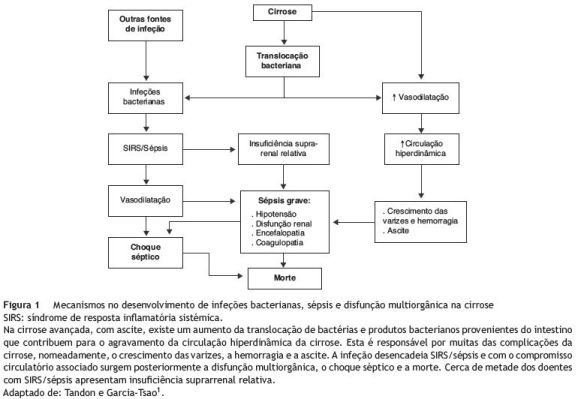
As bactérias que mais facilmente sofrem translocação são as que estão mais frequentemente implicadas nas complicações infecciosas da cirrose, ou seja, Enterobacteriaceae, Enterococci e Streptococci27,28. As bactérias anaeróbicas raramente sofrem translocação e são responsáveis por menos de 1% das infeções bacterianas na cirrose27,29. A sua presença dominante na microflora entérica é protetora contra a colonização e excessivo crescimento das bactérias patogénicas15.
Infeções espontâneas na cirrose
As infeções mais frequentes na cirrose e aquelas que são consideradas características da doença são as chamadas infeções «espontâneas», nomeadamente a PBE, o empiema pleural bacteriano espontâneo e a bacteriémia espontânea1. Estas infeções partilham mecanismos patogénicos e abordagem similares1. São designadas «espontâneas» porque não existe uma fonte óbvia das bactérias que explique a sua passagem para o líquido ascítico, pleural ou sangue1.
Peritonite bacteriana espontânea
A paracentese diagnóstica, com uma análise adequada do líquido ascítico, é fundamental em todos os doentes investigados por ascite para excluir outras causas além da cirrose hepática e despistar nestes a existência de PBE. A ascite devida a hipertensão portal pode ser diferenciada da ascite devida a outras causas através do gradiente de albumina entre o soro e o líquido ascítico (SAAG). Se o SAAG for superior ou igual a 1,1 g/dl (ou 11 g/L), a ascite é devida a hipertensão portal com uma precisão de 97%30,31.
A PBE é definida como a infeção espontânea do líquido ascítico na ausência de uma fonte identificável de infeção ou inflamação intra-abdominal.
A apresentação clínica da PBE pode ir desde uma ausência de sintomas até dor abdominal, febre, sintomas gastrointestinais ou disfunção multiorgânica (insuficiência renal, encefalopatia e instabilidade hemodinâmica)32. Dada a elevada taxa de PBE assintomática (cerca de 50%), em doentes cirróticos com ascite hospitalizados deve ser realizada uma paracentese diagnóstica na admissão e em todos os doentes que apresentem qualquer sintoma, sinal ou valor laboratorial sugestivo de PBE33. A paracentese diagnóstica deve ainda ser realizada nos doentes cirróticos com hemorragia gastrointestinal, choque e em doentes com agravamento da função renal ou hepática e encefalopatia hepática33. O diagnóstico de PBE é efetuado quando a contagem de polimorfonucleares do líquido ascítico é superior a 250/mm3.
Devem ser efetuadas hemoculturas e culturas do líquido ascítico (10 ml num frasco de hemocultura)34. A inoculação do líquido ascítico deverá ser sempre efetuada em meio de hemocultura por este apresentar uma sensibilidade de 93 versus 42% se for efetuada em meios convencionais34. Os frascos devem ser inoculados ao lado da cama do doente35. As hemoculturas são positivas em cerca de 50% dos casos, enquanto as culturas do líquido ascítico o são em aproximadamente 80%, desde que inoculadas em frascos de hemocultura à cabeceira do doente e antes da administração de qualquer antibiótico15,33-35. Os microrganismos mais frequentemente isolados no líquido ascítico são as bactérias gram-negativas (habitualmente Escherichia coli) e cocos gram-positivos (geralmente Estreptococos e Enterococos)33.
É também fundamental distinguir entre peritonite bacteriana primária e secundária, já que esta requer quase sempre abordagem cirúrgica1. A peritonite bacteriana secundária caracteriza-se por uma contagem de polimorfonucleares superior ou igual a 250/mm3 (geralmente na ordem dos milhares), múltiplos microrganismos na cultura do líquido ascítico (que incluem frequentemente fungos, anaeróbios e enterococos) e pelo menos 2 dos seguintes critérios: proteínas totais do líquido ascítico superiores a 1 g/dL, lactato desidrogenase superior ao limite superior do normal no soro e glucose inferior a 50 mg/dL33,36. Estes critérios mostraram uma sensibilidade de 100%, mas apenas 45% de especificidade em diagnosticar perfuração de víscera oca36.
Alguns doentes apresentam «bacteriascite», na qual a cultura é positiva mas o líquido ascítico apresenta uma contagem de neutrófilos inferior a 250/mm3 33. Em alguns casos, resulta de colonização bacteriana secundária da ascite a partir de uma infeção extraperitoneal33. Estes doentes apresentam geralmente sintomas gerais e sinais de infeção. Noutros doentes, a «bacteriascite» é devida à colonização espontânea da ascite e podem ser assintomáticos ou apresentar dor abdominal e febre33. Enquanto, em alguns doentes, particularmente nos assintomáticos, a «bacteriascite» constitui uma colonização reversível espontânea e transitória da ascite, noutros, principalmente nos sintomáticos, a «bacteriascite» pode representar o primeiro passo no desenvolvimento da PBE33. Se o doente exibir sinais de inflamação sistémica, deve ser tratado com antibióticos; caso contrário, deve realizar uma segunda paracentese33. Se a contagem de neutrófilos for superior a 250/mm3, deve ser tratado como PBE33. Se a cultura do líquido ascítico persistir positiva, mesmo que com contagem de neutrófilos inferior a 250/mm3, deve também ser submetido a tratamento com antibióticos32. Os restantes doentes devem manter vigilância33.
As cefalosporinas de terceira geração (cefotaxima, ceftriaxone) são os agentes de escolha no tratamento da PBE e devem ser iniciadas imediatamente após o seu diagnóstico (tabela 1)1,37. Duas alternativas igualmente eficazes são a amoxicilina/ácido clavulânico e a ciprofloxacina. A primeira, além de possuir formulação oral, apresenta custos mais reduzidos33. A segunda possui as vantagens de, em formulação oral, apresentar uma absorção entérica favorável, elevada biodisponibilidade no líquido ascítico e ser menos dispendiosa do que qualquer uma das formulações parentéricas15. No entanto, não deve ser considerada opção no caso de doente já em profilaxia com quinolonas33. A duração de tratamento deverá ser de 5 dias30,33,38. Os antibióticos administrados por via endovenosa podem ser alterados para formulações orais às 48 h se houver melhoria clínica e/ou os polimorfonucleares do líquido ascítico mostrarem uma melhoria significativa (redução de pelo menos 25% do valor pré-tratamento)1,15,33. A ausência de resposta à terapêutica antibiótica é geralmente devida à presença de bactérias resistentes ou peritonite bacteriana secundária33. As infeções nosocomiais estão associadas à emergência de bactérias resistentes39. Neste grupo, predominam claramente os gram-positivos (32% são Estafilococos com uma elevada prevalência dos meticilinorresistentes)39. O uso frequente de antibióticos na população de doentes cirróticos, que sofrem infeções recorrentes, provavelmente leva à seleção de bactérias resistentes39. Outro aspeto importante é que a contagem de polimorfonucleares neutrófilos nos doentes com PBE é habitualmente mais elevada quando a etiologia são os gram-negativos do que com os gram-positivos39. Grande parte dos doentes com PBE a cocos gram-positivos tem contagem de polimorfonucleares neutrófilos inferiores a 250/mm3 39. Se o doente não melhora clinicamente às 48 horas, a vancomicina deve ser adicionada para cobertura empírica do Estafilococos aureus meticilinorresistente (MRSA)15,39. Além da condição imunossupressora da cirrose, existem outros fatores de risco para infeção por MRSA, nomeadamente o cada vez maior número de doentes tratados em unidades de cuidados intensivos, o aumento do número de procedimentos invasivos e o tempo prolongado de internamento40. Nos doentes com infeções a gram-negativos resistentes a cefalosporinas de terceira geração, o imipenem-cilastatina constitui uma opção válida para o tratamento da maioria destas infeções39.
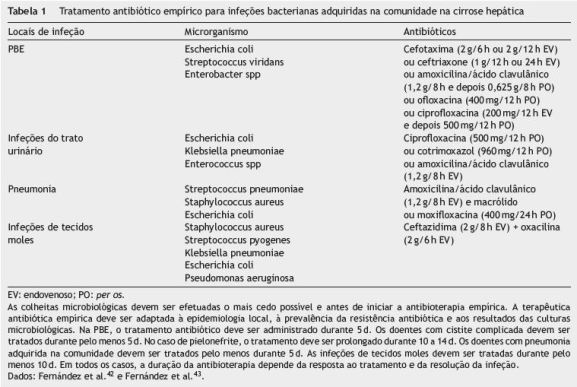
A utilização da albumina nos doentes com PBE deve ser restrita aos doentes de alto risco (bilirrubina sérica superior a 4 mg/dl e creatinina superior a 1 mg/dl)1. Além do efeito de expansão do plasma e um aumento do preload, a albumina liga-se a substâncias vasoativas e citocinas e tem um efeito antioxidante41,42. A dose de albumina recomendada é 1,5 g/kg peso corporal por via endovenosa no dia do diagnóstico e 1 g/kg peso corporal no dia 3 de tratamento1. A utilização de albumina nestes moldes reduziu a incidência de síndrome hepatorrenal tipo 1 de 30 para 10% e a mortalidade de 29 para 10%33. No entanto, são necessários mais estudos para avaliar a eficácia da albumina e de outros expansores plasmáticos no tratamento da PBE, dado que estas recomendações se baseiam em análises secundárias de pequenas séries publicadas43-45.
Empiema pleural bacteriano espontâneo
A infeção de um hidrotórax preexistente é rara, embora a exata prevalência seja desconhecida33. O diagnóstico é baseado na análise do líquido pleural obtido por toracocentese. O empiema pleural bacteriano espontâneo é caracterizado por cultura do líquido pleural positiva e mais de 250 neutrófilos/mm3 ou por cultura negativa do líquido pleural e mais de 500 neutrófilos/mm3, na ausência de infeção do parênquima pulmonar33. As culturas do líquido pleural são positivas em 75% dos casos33.
Esta entidade está associada a PBE em cerca de 50% dos casos e deve ser tratada de forma similar33.
Prevenção
As estratégias preventivas nestes doentes incluem a abstinência do consumo de álcool, a profilaxia da PBE e a prevenção de infeções virais ou bacterianas específicas através de vacinas46.
A profilaxia da PBE consiste na utilização de medidas potenciais que possam diminuir a translocação bacteriana. Um dos mecanismos consiste na administração de antibióticos não absorvíveis ou fracamente absorvíveis de modo a eliminar os organismos gram-negativos do intestino, medida designada de descontaminação intestinal seletiva1. Um segundo mecanismo consiste na modificação da composição da microflora intestinal através da administração de pré/probióticos ou ácidos biliares47,48. No entanto, e apesar de apresentarem base racional de aplicação, a sua utilização não está recomendada na prática clínica por apresentarem estudos com dados contraditórios e inconclusivos47-49. O terceiro mecanismo consiste em acelerar o trânsito intestinal através do uso de pró-cinéticos (por exemplo, cisapride) ou _-bloqueadores (por exemplo propranolol)50. Estes últimos, além do mecanismo referido, apresentam outros capazes de prevenir o desenvolvimento de PBE, nomeadamente, a diminuição da translocação bacteriana e o aumento da eficácia do sistema imunitário51. O efeito protetor dos _-bloqueadores é evidente nos doentes tratados quer em profilaxia primária quer em profilaxia secundária para hemorragia e é independente da resposta hemodinâmica à terapêutica51. Turnes et al. mostraram que uma redução de 11% no gradiente de pressão da veia hepática relativamente ao valor basal constituiu o melhor preditor de prevenção de PBE52. Este valor é nitidamente inferior ao considerado como protetor para a hemorragia de varizes (20%)51.
Assim, e até que as medidas não antibióticas sejam testadas clinicamente, a profilaxia da infeção nos doentes cirróticos é baseada na descontaminação intestinal seletiva, principalmente no uso da norfloxacina por via oral1. Contudo, esta terapêutica está associada a resistência aos antibióticos do grupo das quinolonas e trimetoprimsulfametoxazol4.
A terapêutica profilática deve ser restringida aos doentes com maior risco de PBE33. Existem 3 grupos que poderão beneficiar desta estratégia. O primeiro são os doentes hospitalizados com hemorragia gastrointestinal, nos quais se provou benefício na terapêutica antibiótica de curta duração (5 a 7 dias) na prevenção da infeção bacteriana e na redução da mortalidade, da taxa de ressangramento e na duração do internamento53. Estes benefícios foram observados independentemente do tipo de antibiótico utilizado53. O ceftriaxone é uma opção adequada, principalmente nos doentes com doença hepática mais grave (pelo menos 2 dos seguintes critérios: ascite, malnutrição grave, encefalopatia ou bilirrubina sérica superior a 3 mg/dL)33,54. O segundo grupo são os doentes com conteúdo de proteínas do líquido ascítico reduzido sem história prévia de PBE. Num estudo realizado, provou-se que estes doentes tinham um risco aumentado de PBE (20% ao ano versus 0% ao ano, se as proteínas do líquido ascítico > 10 g/L)55. A administração de norfloxacina por via oral (400 mg/dia) em doentes com proteínas no líquido ascítico inferior a 15 g/L e cirrose avançada (score CPT ≥9 pontos com bilirrubina sérica ≥3 mg/dL ou creatinina ≥1,2 mg/dL/ureia ≥50 mg/dL ou sódio sérico ≤130 mEq/L) sem PBE prévia reduziu a probabilidade de PBE e síndroma hepatorrenal e melhorou a sobrevivência aos 3 meses33,56. O terceiro e último grupo consiste nos doentes que recuperaram de um episódio de PBE. Estes doentes têm uma probabilidade de recorrência de PBE de 70% ao ano e uma taxa de sobrevida anual de 30 a 50%57,58. Um ensaio controlado com placebo demonstrou uma redução significativa da recidiva de PBE (20%) em um ano com a administração de norfloxacina na dose de 400 mg diária57. Todos os doentes que recuperaram de um episódio de PBE devem ser considerados candidatos a transplante hepático33.
A pentoxifilina é um inibidor do TNF-_. Num ensaio clínico com 335 doentes com cirrose hepática avançada (score CPT C), a administração de pentoxifilina oral (1 200 mg/d) reduziu significativamente o risco de complicações, nomeadamente, infeção bacteriana, insuficiência renal, encefalopatia hepática e hemorragia gastrointestinal59. No entanto, a sua administração não reduziu a mortalidade aos 2 meses, o objetivo primário do estudo59.
Algumas infeções na cirrose são prevenidas pela vacinação. A imunização pode reduzir a morbilidade e mortalidade relacionada com a cirrose60. A vacinação contra a hepatite A e B está recomendada nos doentes com doença hepática crónica não imunizados60. As vacinas antigripal (administrada anualmente) e antipneumocócica polisacarídica (administrada a cada 3 a 5 anos) estão recomendadas em todos os doentes cirróticos60. Uma particularidade na imunização destes doentes é a de que deve ser realizada o mais precocemente possível durante o seu acompanhamento de modo a melhorar a resposta imunitária60.
A título final, apenas uma breve referência à crescente utilização dos inibidores da bomba de protões (IBP) nos doentes com cirrose hepática em grande parte dos casos sem fundamentação na evidência científica61. A sua utilização foi associada a um risco aumentado de infeção neste grupo de doentes62. Um estudo mostrou que os IBP estavam associados a um maior risco de PBE em doentes com cirrose avançada63. No entanto, são necessários mais estudos prospetivos que avaliem a potencial associação entre os inibidores da bomba de protões e a infeção nos doentes cirróticos. Provavelmente, a única indicação para utilização dos IBP na cirrose, além das indicações habitualmente definidas na população geral, é a prevenção e tratamento das complicações esofágicas decorrentes do tratamento endoscópico das varizes, principalmente quando se utiliza a técnica de escleroterapia61.
Conclusão
As infeções bacterianas são uma causa importante de morbilidade e mortalidade nos doentes cirróticos devido ao seu estado de imunodeficiência relativa. A translocação bacteriana desempenha um papel fulcral na patogénese das infeções e no estado de circulação hiperdinâmica da cirrose. Estas alterações hemodinâmicas pioram com o desenvolvimento de infeção e podem progredir para sépsis grave e choque séptico. A profilaxia, reconhecimento precoce e o tratamento rápido das infeções bacterianas e suas complicações são essenciais para melhorar as taxas de sobrevida destes doentes.
Tendo em conta a crescente emergência de resistências bacterianas aos antibióticos, torna-se premente a investigação de abordagens «não-antibióticas» para profilaxia primária da PBE.
Responsabilidades éticas
Proteção de pessoas e animais. Os autores declaram que para esta investigação não se realizaram experiências em seres humanos e/ou animais.
Confidencialidade dos dados. Os autores declaram ter seguido os protocolos de seu centro de trabalho acerca da publicação dos dados de pacientes e que todos os pacientes incluídos no estudo receberam informações suficientes e deram o seu consentimento informado por escrito para participar nesse estudo.
Direito à privacidade e consentimento escrito. Os autores declaram que não aparecem dados de pacientes neste artigo.
Bibliografia
1. Tandon P, Garcia-Tsao G. Bacterial infections, sepsis, and multiorgan failure in cirrhosis. Semin Liver Dis. 2008;28:26-42. [ Links ]
2. Borzio M, Salerno F, Piantoni L, Cazzaniga M, Angeli P, Bissoli F, et al. Bacterial infection in patients with advanced cirrhosis: a multicentre prospective study. Dig Liver Dis. 2001;33:41-8. [ Links ]
3. Fernández J, Navasa M, Gómez J, Colmenero J, Vila J, Arroyo V, et al. Bacterial infections in cirrhosis: epidemiological changes with invasive procedures and norfloxacin prophylaxis. Hepatology. 2002;35:140-8. [ Links ]
4. Bernard B, Grangé JD, Khac EN, Amiot X, Opolon P, Poynard T. Antibiotic prophylaxis for the prevention of bacterial infections in cirrhotic patients with gastrointestinal bleeding: a metaanalysis. Hepatology. 1999;29:1655-61. [ Links ]
5. Deschênes M, Villeneuve JP. Risk factors for the development of bacterial infections in hospitalized patients with cirrhosis. Am J Gastroenterol. 1999;94:2193-7. [ Links ]
6. Yoshida H, Hamada T, Inzuka S, Ueno T, Sata M, Tanikawa K. Bacterial infection in cirrhosis, with and without hepatocelular carcinoma. Am J Gastroenterol. 1993;88:2067-71. [ Links ]
7. Caly WR, Strauss E. A prospective study of bacterial infections in patients with cirrhosis. J Hepatol. 1993;18:353-8. [ Links ]
8. De Mattos AA, Coral GP, Menti E, Valiatti F, Kramer C. Infecção bacteriana no paciente cirrótico. Arq Gastroenterol. 2003;40:11-5. [ Links ]
9. Rosa H, Silvério AO, Perini RF, Arruda CB. Bacterial infection in cirrhotic patients and its relationship with alcohol. Am J Gastroenterol. 2000;95:1290-3. [ Links ]
10. Plessier A, Denninger MH, Consigny Y, Pessione F, Francoz C, Durand F, et al. Coagulation disorders in patients with cirrhosis and severe sepsis. Liver Int. 2003;23:440-8. [ Links ]
11. Foreman MG, Mannino DM, Moss M. Cirrhosis as a risk factor for sepsis and death: analysis of the National Hospital Discharge Survey. Chest. 2003;124:1016-20. [ Links ]
12. Garcia-Tsao G, Wiest R. Gut microflora in the pathogenesis of the complications of cirrhosis. Best Pract Res Clin Gastroenterol. 2004;18:353-72. [ Links ]
13. Christou L, Pappas G, Falagas ME. Bacterial infection-related morbidity and mortality in cirrhosis. Am J Gastroenterol. 2007;102:1510-7. [ Links ]
14. Wong F, Bernardi M, Balk R, Christman B, Moreau R, Garcia-Tsao G, et al. Sepsis in cirrhosis: report on the 7th meeting of the International Ascites Club. Gut. 2005;54:718-25. [ Links ]
15. Ghassemi S, Garcia-Tsao G. Prevention and treatment of infections in patients with cirrhosis. Best Pract Res Clin Gastroenterol. 2007;21:77-93. [ Links ]
16. Arvaniti V, DAmico G, Fede G, Manousou P, Tsochatzis E, Pleguezuelo M, et al. Infections in patients with cirrhosis increase mortality four-fold and should be used in determining prognosis. Gastroenterology. 2010;139:1246-56. [ Links ]
17. Finlayson ND, Krohn K, Fauconnet MH, Anderson KE. Significance of serum complement levels in chronic liver disease. Gastroenterology. 1972;63:653-9. [ Links ]
18. Mellencamp MA, Preheim LC. Pneumococcal pneumonia in a rat model of cirrhosis: effects of cirrhosis on pulmonary defense mechanisms against Streptococcus pneumoniae. J Infect Dis. 1991;163:102-8. [ Links ]
19. Homann C, Varming K, Høgåsen K, Mollnes TE, Graudal N, Thomsen AC, et al. Acquired C3 deficiency in patients with alcoholic cirrhosis predisposes to infection and increased mortality. Gut. 1997;40:544-9. [ Links ]
20. Gustot T, Durand F, Lebrec D, Vincent JL, Moreau R. Severe sepsis in cirrhosis. Hepatology. 2009;50:2022-33. [ Links ]
21. Berg RD, Garlington AW. Translocation of certain indigenous bactéria from the gastrointestinal tract to the mesenteric lymph nodes and other organs in a gnotobiotic mouse model. Infect Immun. 1979;23:403-11. [ Links ]
22. Garcia-Tsao G, Albillos A, Barden GE, West AB. Bacterial translocation in acute and chronic portal hypertension. Hepatology. 1993;17:1081-5. [ Links ]
23. Garcia-Tsao G, Lee FY, Barden GE, Cartun R, West AB. Bacterial translocation to mesenteric lymph nodes is increased in cirrhotic rats with ascites. Gastroenterology. 1995;108:1835-41. [ Links ]
24. Mão de Ferro S, Salazar M, Machado M, Ramalho F, Pinto HC. Permeabilidade intestinal em doentes com cirrose hepática: correlação com endotoxemia e níveis circulantes de TNF_, IL-1 e IL-6. J Port Gastrenterol. 2011;18:66-72. [ Links ]
25. Battista S, Bar F, Mengozzi G, Zanon E, Grosso M, Molino G. Hyperdynamic circulation in patients with cirrhosis: direct measurement of nitric oxide levels in hepatic and portal veins. J Hepatol. 1997;26:75-80. [ Links ]
26. Lumsden AB, Henderson JM, Kutner MH. Endotoxin levels measured by a chromogenic assay in portal, hepatic and peripheral venous blood in patients with cirrhosis. Hepatology. 1988;8:232-6. [ Links ]
27. Steffen EK, Berg RD, Deitch EA. Comparison of translocation rates of various indigenous bacteria from the gastrointestinal tract to the mesenteric lymph node. J Infect Dis. 1988;157:1032-8. [ Links ]
28. Wiest R, Garcia-Tsao G. Bacterial translocation (BT) in cirrhosis. Hepatology. 2005;41:422-33. [ Links ]
29. Wells CL, Maddaus MA, Reynolds CM, Jechorek RP, Simmons RL. Role of anaerobic flora in the translocation of aerobic and facultatively anaerobic intestinal bacteria. Infect Immun. 1987;55:2689-94. [ Links ]
30. Runyon BA, Practice Guidelines Committee, American Association for the Study of Liver Diseases (AASLD). Management of adult patients with ascites due to cirrhosis. Hepatology. 2004;39:841-56. [ Links ]
31. Runyon BA, Montano AA, Akriviadis EA, Antillon MR, Irving MA, McHutchison JG. The serum-ascites albumin gradient is superior to the exudate-transudate concept in the differential diagnosis of ascites. Ann Intern Med. 1992;117:215-20. [ Links ]
32. Rimola A, Gracía-Tsao G, Navasa M, Piddock LJ, Planas R, Bernard B, et al. Diagnosis, treatment and prophylaxis of spontaneous bacterial peritonitis: a consensus document. International Ascites Club. J Hepatol. 2000;32:142-53. [ Links ]
33. European Association for the Study of the Liver. EASL clinical practice guidelines on the management of ascites, spontaneous bacterial peritonitis, and hepatorenal syndrome in cirrhosis. J Hepatol. 2010;53:397-417. [ Links ]
34. Runyon BA, Canawati HN, Akriviadis EA. Optimization of ascitic fluid culture technique. Gastroenterology. 1988;95:1351-5. [ Links ]
35. Runyon BA, Antillon MR, Akriviadis EA, McHutchison JG. Bedside inoculation of blood culture bottles is superior to delayed inoculation in the detection of spontaneous bacterial peritonitis. J Clin Microbiol. 1990;28:2811-2. [ Links ]
36. Akriviadis EA, Runyon BA. Utility of an algorithm in differentiating spontaneous from secondary bacterial peritonitis. Gastroenterology. 1990;98:127-33. [ Links ]
37. Rimola A, Salmerón JM, Clemente G, Rodrigo L, Obrador A, Miranda ML, et al. Two different dosages of cefotaxime in the treatment of spontaneous bacterial peritonitis in cirrhosis: results of a prospective, randomized, multicenter study. Hepatology. 1995;21:674-9. [ Links ]
38. Runyon B, McHutchison J, Antillon M, Akriviadis EA, Montano AA. Short-course versus long-course antibiotic treatment of spontaneous bacterial peritonitis. A randomized controlled study of 100 patients. Gastroenterology. 1991;100:1737-42. [ Links ]
39. Campillo B, Richardet JP, Kheo T, Dupeyron C. Nosocomial spontaneous bacterial peritonitis and bacteremia in cirrhotic patients: impact of isolate type on prognosis and characteristics of infection. Clin Infect Dis. 2002;35:1-10. [ Links ]
40. Almeida PR, Camargo NS, Arenz M, Tovo CV, Galperim B, Behar P. Peritonite bacteriana espontânea: impacto das mudanças da microbiologia. Arq Gastroenterol. 2007;44:68-72. [ Links ]
41. Ruiz-del-Arbol L, Urman J, Fernández J, González M, Navasa M, Monescillo A, et al. Systemic, renal, and hepatic hemodynamic derangements in cirrhotic patients with spontaneous bacterial peritonitis. Hepatology. 2003;38:1210-8. [ Links ]
42. Fernández J, Navasa M, Garcia-Pagan JC, Abraldes JG, Jiménez W, Bosch J, et al. Effect of intravenous albumin on systemic and hepatic hemodynamics and vasoactive neurohormonal systems in patients with cirrhosis and spontaneous bacterial peritonitis. J Hepatol. 2004;41:384-90. [ Links ]
43. Fernández J, Monteagudo J, Bargallo X, Jiménez W, Bosch J, Arroyo V, et al. A randomized unblinded pilot study comparing albumin versus hydroxyethyl starch in spontaneous bacterial peritonitis. Hepatology. 2005;42:627-34. [ Links ]
44. Sigal SH, Stanca CM, Fernandez J, Arroyo V, Navasa M. Restricted use of albumin for spontaneous bacterial peritonitis. Gut. 2007;56:597-9. [ Links ]
45. Terg R, Gadano A, Cartier M, Casciato P, Lucero R, Munoz A, et al. Serum creatinine and bilirubin predict renal failure and mortality in patients with spontaneous bacterial peritonitis: a retrospective study. Liver Int. 2009;29:415-9. [ Links ]
46. Fica A. Diagnóstico, manejo y prevención de infeccionas en pacientes con cirrosis hepática. Rev Chilena Infectol. 2005;22:63-74. [ Links ]
47. Levitsky J. Probiotics: application of healthy bacteria to liver transplant recipients. Hepatology. 2006;44:507-10. [ Links ]
48. Lorenzo-Zúniga V, Bartolí R, Planas R, Hofmann AF, Vinado B, Hagey LR, et al. Oral bile acids reduce bacterial overgrowth, bacterial translocation, and endotoxemia in cirrhotic rats. Hepatology. 2003;37:551-7. [ Links ]
49. Bauer TM, Fernández J, Navasa M, Vila J, Rodés J. Failure of Lactobacillus spp. to prevent bacterial translocation in a rat model of experimental cirrhosis. J Hepatol. 2002;36:501-6. [ Links ]
50. Zhang SC, Wang W, Ren WY, He BM, Zhou K, Zhu WN. Effect of cisapride on intestinal bacterial and endotoxin translocation in cirrhosis. World J Gastroenterol. 2003;9:534-8. [ Links ]
51. Senzolo M, Cholongitas E, Burra P, Leandro G, Thalheimer U, Patch D, et al. Beta-Blockers protect against spontaneous bacterial peritonitis in cirrhotic patients: a meta-analysis. Liver Int. 2009;29:1189-93. [ Links ]
52. Turnes J, Garcia-Pagan JC, Abraldes JG, Hernandez-Guerra M, DellEra A, Bosch J. Pharmacological reduction of portal pressure and long-term risk of first variceal bleeding in patients with cirrhosis. Am J Gastroenterol. 2006;101:506-12. [ Links ]
53. Chavez-Tapia NC, Barrientos-Gutierrez T, Tellez-Avila FI, Soares-Weiser K, Uribe M. Antibiotic prophylaxis for cirrhotic patients with upper gastrointestinal bleeding. Cochrane Database Syst Rev. 2010;9:CD002907, http://dx.doi.org/10.1002/14651858.CD002907.pub2. [ Links ]
54. Fernández J, Ruiz del Arbol L, Gómez C, Durandez R, Serradilla R, Guarner C, et al. Norfloxacin vs ceftriaxone in the prophylaxis of infections in patients with advanced cirrosis and hemorrhage. Gastroenterology. 2006;131:1049-56. [ Links ]
55. Llach J, Rimola A, Navasa M, Ginès P, Salmerón JM, Ginès A, et al. Incidence and predictive factors of the first episode of spontaneous bacterial peritonitis in cirrhosis with ascites: relevance of ascitic fluid protein concentration. Hepatology. 1992;16:724-7. [ Links ]
56. Fernández J, Navasa M, Planas R, Montoliu S, Monfort D, Soriano G, et al. Primary prophylaxis of spontaneous bacterial peritonites delays hepatorenal syndrome and improves survival in cirrhosis. Gastroenterology. 2007;133:818-24. [ Links ]
57. Ginés P, Rimola A, Planas R, Vargas V, Marco F, Almela M, et al. Norfloxacin prevents spontaneous bacterial peritonitis recurrence in cirrhosis: results of a double-blind, placebo-controlled trial. Hepatology. 1990;12:716-24. [ Links ]
58. Titó L, Rimola A, Ginès P, Llach J, Arroyo V, Rodés J. Recurrence of spontaneous bacterial peritonitis in cirrhosis: frequency and predictive factors. Hepatology. 1988;8:27-31. [ Links ]
59. Lebrec D, Thabut D, Oberti F, Perarnau JM, Condat B, Barraud H, et al. Pentoxifylline does not decrease short-term mortality but does reduce complications in patients with advanced cirrhosis. Gastroenterology. 2010;138:1755-62. [ Links ]
60. Loulergue P, Pol S, Mallet V, Sogni P, Launay O, GEVACCIM Group. Why actively promote vaccination in patients with cirrhosis? J Clin Virol. 2009;46:206-9. [ Links ]
61. Lodato F, Azzaroli F, di Girolamo M, Sogni P, Launay O. Proton pump inhibitors in cirrhosis: tradition or evidence based practice? World J Gastroenterol. 2008;14:2980-5. [ Links ]
62. Bajaj J, Tannous M, Bootwala Z, Sanyal AJ, Heuman DM. Proton pump inhibitor use is associated with the development of a broad range of infections in cirrhosis. J Hepatol. 2010;52:S66. [ Links ]
63. Bajaj JS, Zadvornova Y, Heuman DM, Hafeezullah M, Hoffmann RG, Sanyal AJ, et al. Association of proton pump inhibitor therapy with spontaneous bacterial peritonitis in cirrhotic patients with ascites. Am J Gastroenterol. 2009;104:1130-4. [ Links ]
Conflito de interesses
Os autores declaram não haver conflito de interesses.
*Autor para correspondência
Correio eletrónico: pcarrola@sapo.pt (P. Carrola).
Recebido a 18 de março de 2011; aceite a 19 de setembro de 2012













