Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Jornal Português de Gastrenterologia
versão impressa ISSN 0872-8178
J Port Gastrenterol. vol.20 no.2 Lisboa mar. 2013
https://doi.org/10.1016/j.jpg.2012.07.003
Neoplasia mucinosa papilar intraductal com fistulização gástrica e duodenal: uma forma rara de apresentação
Intraductal papillary mucinous neoplasm with fistulization into the stomach and duodenum: A rare form of presentation
Rita Pimentel∗, Fernando Castro Poças, José Manuel Castro Ferreira e Jorge Alberto Areias
Serviço de Gastrenterologia, Hospital de Santo António, Porto, Portugal
*Autor para correspondência
RESUMO
A neoplasia mucinosa papilar intraductal (NMPI) constitui uma lesão cística pancreática rara com elevado potencial maligno. Apresentamos o caso de um homem, 64 anos, avaliado em consulta por esteatorreia e emagrecimento (17% do peso corporal). A colonoscopia mostrou gotículas de gordura nas fezes, sem outras alterações. Na endoscopia alta observou-se um orifício fistuloso, com drenagem de muco, no bolbo duodenal e papila de Vater protuberante, possivelmente por compressão extrínseca. TAC abdominal mostrou lesão cística cefalopancreática com 5,8 cm, Wirsung marcadamente dilatado, colédoco ligeiramente dilatado. Ecoendoscopia revelou lesão multicística cefalopancreática, de contornos irregulares, sugestiva de NMPI. Citologia, obtida por punção aspirativa guiada por ecoendoscopia, confirmou NMPI. A RMN demonstrou a NMPI com fistulização para o estômago e para o bolbo duodenal. Realizada duodenopancreatectomia cefálica, obtendo-se um diagnóstico anátomo-patológico de adenocarcinoma mucinoso enxertado em NMPI. Ausência de evidência de recidiva em 14 meses de seguimento. A NMPI é geralmente diagnosticada em fase assintomática, sendo a esteatorreia a manifestação mais rara. Ocorre fistulização para órgãos adjacentes em 7-15% dos casos. Fistulização combinada para duodeno e estômago ocorre em apenas 6%.
Palavras-Chave Neoplasia pancreática; Adenocarcinoma mucinoso; Fístula
ABSTRACT
Intraductal papillary mucinous neoplasm (IPMN) is a rare pancreatic cystic neoplasm with high risk of malignancy. We present the case of a 64-year-old male with steatorrhea and weight loss (17% total body weight). Colonoscopy detected presence of oil droplets in stools. Esophagogastroduodenoscopy revealed a fistulous orifice with mucous drainage in the duodenal bulb and a bulging ampulla of Vater, possibly by external compression; Abdominal CT showed the presence of a cystic lesion in the pancreatic head, 5.8 cm in diameter, significant dilation of wirsung and slight dilation of common bile duct. EUS revealed a multicystic lesion with irregular contours in the pancreatic head, suggestive of IPMN. EUS guided fine needle citologic examination confirmed IPMN. Abdominal MRI detected fistulization to the duodenum and stomach. Pancreatoduodenectomy was performed and a pathological diagnosis of mucinous adenocarcinoma in IPMN was obtained. There has been no evidence of recurrence during 14 months of follow-up. Most patients diagnosed with IPMN are assymptomatic, steatorrhea is the less frequent form of presentation. Fistulization to adjacent organs occurs in 7-15% cases, combined fistula to duodenum and stomach in only 6%.
Keywords Pancreatic neoplasm; Mucinous adenocarcinoma; Fistula
Introdução
A neoplasia mucinosa papilar intraductal (NMPI) constitui uma das neoplasias císticas do pâncreas, diagnosticada com frequência crescente desde a sua descrição inicial em 1982. Atualmente a maioria dos casos são detetados numa fase assintomática, constituindo um achado acidental1. Quando sintomática, a esteatorreia é a forma de apresentação mais rara2. A fistulização para órgãos adjacentes está descrita, inclusivamente para 2 órgãos em simultâneo3,4.
Caso clínico
Homem de 64 anos, referenciado à consulta de Gastrenterologia por diarreia com 5 meses de evolução, acompanhada por emagrecimento com perda de 17% do peso corporal (índice de massa corporal: 19 kg/m2). O doente referia 8 a 10 dejeções diárias, com diarreia noturna, caracterizadas por fezes moles, claras e com restos alimentares. Negava dor abdominal, anorexia ou vómitos. Antecedentes de hipertensão arterial, diabetes mellitus e cardiopatia isquémica, com hábitos tabágicos passados.
Ao exame objetivo apresentava-se emagrecido, anitérico, com dor à palpação profunda do epigastro, sem tumefações palpáveis.
Analiticamente não apresentava alteração do hemograma, das provas hepáticas, nem das enzimas pancreáticas, destacando-se um discreto aumento do antigénio carcinoembrionário (CEA), com um valor de 5,9 ng/ml (normal: < 5 ng/ml), sem elevação do CA 19.9. O exame das fezes revelou numerosos lípidos e fibras musculares mal digeridas.
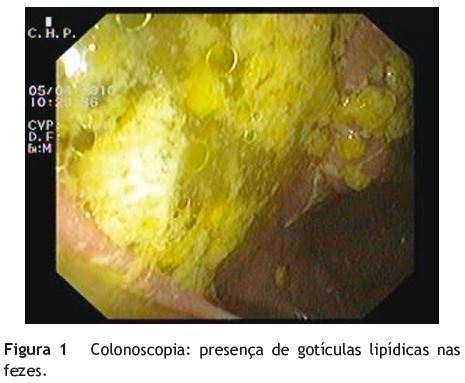
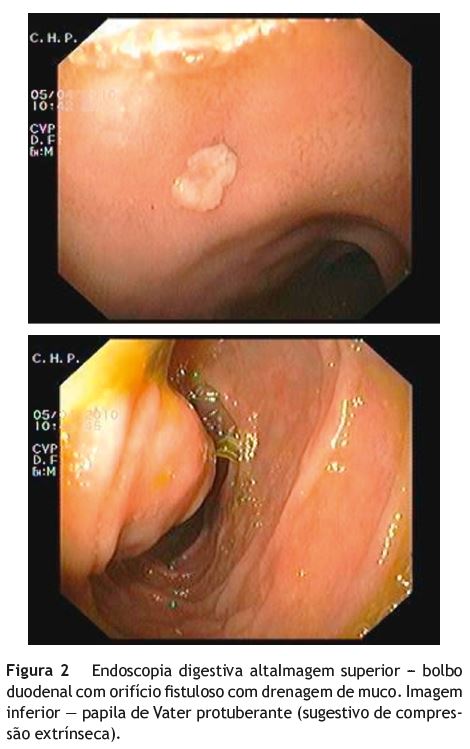
A colonoscopia total mostrou gotículas de gordura nas fezes, sem outras alterações (fig. 1). Na endoscopia digestiva alta observou-se, no bolbo duodenal, um aparente orifício fistuloso com drenagem de muco e uma papila de Vater protuberante, em possível relação com compressão extrínseca (fig. 2).
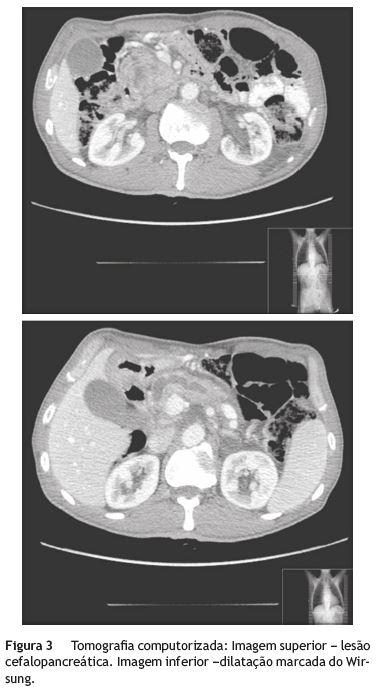
A TAC revelou lesão cefalopancreática com 5,8 cm de diâmetro, associada a marcada dilatação do Wirsung e ligeira dilatação do colédoco (fig. 3).
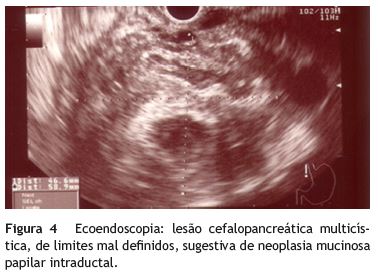
Prosseguiu-se para ecoendoscopia alta, efetuando-se punção aspirativa com agulha fina de uma lesão cefalopancreática heterogénea, de contornos irregulares e limites mal definidos, com múltiplos espaços císticos e 5,9 cm de maior diâmetro, sugestiva de se tratar de NMPI (fig. 4). A citologia confirmou o diagnóstico imagiológico.
Pré-operatoriamente foi realizada RMN abdominal, observando-se lesão compatível com NMPI, com 2 trajetos fistulosos entre o Wirsung e, respetivamente, o corpo gástrico e o bolbo duodenal (fig. 5).
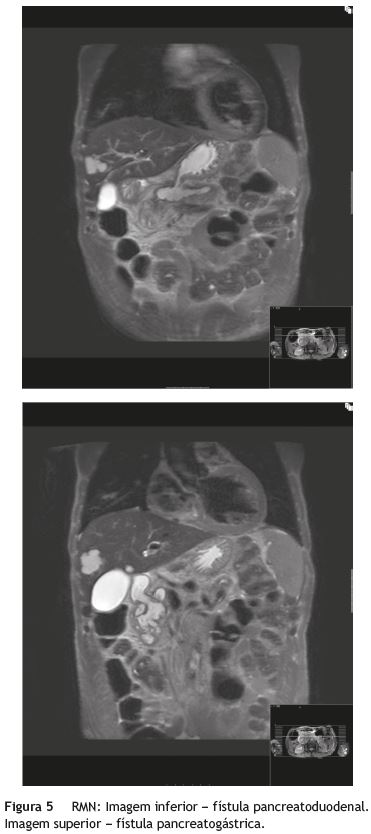
O doente foi submetido a duodenopancreatectomia cefálica. O exame anátomo-patológico da peça cirúrgica revelou um adenocarcinoma mucinoso enxertado numa NMPI, limitado ao pâncreas, sem metastização ganglionar regional. O pós-operatório decorreu sem complicações. Sem evidência de recidiva nos primeiros 14 meses de follow-up.
Discussão
O uso crescente de exames de imagem tem levado a um aumento do número de lesões císticas pancreáticas identificadas, na sua maioria constituindo achados acidentais em indivíduos assintomáticos5.
A NMPI é um dos tipos de lesões císticas do pâncreas, definida pela Organização Mundial de Saúde como uma neoplasia com origem num epitélio secretor de mucina, com ou sem projeções papilares, que envolve o ducto pancreático principal e/ou ramos laterais6. Localiza-se mais frequentemente na cabeça do pâncreas e classifica-se em 2 tipos: a NMPIducto principal (NMPI-DP), em que há dilatação cística do Wirsung superior a 1 cm, e a NMPI-ducto lateral (NMPI-DL), que se origina num dos ramos laterais, este comunicando com um Wirsung não dilatado. Tal como outros tumores do tubo digestivo, histologicamente constitui um amplo espetro de neoplasias, podendo variar desde adenoma a carcinoma invasor, com diferentes graus de agressividade, sendo por isso considerada uma lesão pré-maligna7. Quando comparada com o adenocarcinoma ductal pancreático, a NMPI tem um crescimento mais lento e um prognóstico mais favorável. O prognóstico depende do tipo NMPI, com uma prevalência de malignidade associada à NMPI-DP e à NMPIDL de, respetivamente, 70% (66% de cancros invasores) e 25% (15% de cancros invasores)8.
A hipersecreção mucinosa pode levar ao impactamento de muco nos ductos pancreáticos com consequente obstrução da drenagem pancreática, sendo uma causa frequente de sintomatologia/manifestações clínicas como dor abdominal, pancreatites agudas de repetição, esteatorreia, diabetes mellitus, iterícia. Numa série de 140 doentes com NMPI ressecadas, 73% estavam sintomáticos no diagnóstico, a maioria com dor abdominal e/ou emagrecimento e a esteatorreia constituindo o sintoma mais raro (9%)2. O preenchimento dos ductos pancreáticos com mucina gera aumentos significativos da pressão intraductal, que podem culminar na formação de fístulas para órgãos adjacentes, constituindo um tipo de penetração mecânica como forma de alívio da alta pressão intraductal. O outro mecanismo para o desenvolvimento de fístulas é a invasão direta do cancro para órgãos vizinhos9. A fistulização associada a NMPI está descrita em 7-15% dos casos3,9. Numa série de 18 NMPI fistulizadas, as fístulas foram significativamente mais frequentes nas NMPI-DP, em 39% dos casos ocorreu fistulização para múltiplos órgãos, sendo os mais frequentemente envolvidos o duodeno (67%), o estômago (44%) e o colédoco (33%)9.
A NMPI é com frequência detetada acidentalmente numa TAC ou RMN realizadas por outra indicação. A investigação diagnóstica envolve outras modalidades imagiológicas como a ecoendoscopia, a CPRE ou a colangioRMN, que permitem uma melhor caracterização da lesão, confirmar a comunicação com o sistema ductal pancreático e, no caso da CPRE e da ecoendoscopia, a colheita de material para citologia e doseamento de marcadores tumorais10,11. Na CPRE, a observação de uma papila de Vater protuberante, «em olho de peixe», com exteriorização de muco é patognomónica e faz o diagnóstico11. A ecoendoscopia diagnostica com uma boa acuidade as proliferações papilares intracísticas (nódulos murais)12 que, juntamente com as dimensões da lesão, o diâmetro do Wirsung, a papila de Vater protuberante, a presença de sintomas, são considerados fatores preditivos de malignidade13,14.
De acordo com as recomendações de consenso internacionais, tendo em conta a elevada prevalência de malignidade, todas as NMPI-DP têm indicação para resseção cirúrgica (duodenopancreatectomia cefálica, pancreatectomia distal ou pancreatectomia total), desde que o doente tenha condições para a cirurgia. As NMPI-DL com menos de 30mm, sem nódulos murais, em doentes assintomáticos, poderão ser apenas vigiadas, progredindo-se para cirurgia somente em caso de aparecimento de sintomas ou de alterações imagiológicas preditivas de malignidade. Pelo significativo risco de recorrência, as NMPI malignas tratadas cirurgicamente devem manter um seguimento semestral com TAC ou RMN, não havendo utilidade no doseamento sérico do CEA e CA 19,98.
Como conclusão sublinha-se o facto de a NMPI ser uma neoplasia rara que, no entanto, tem vindo a ser diagnosticada com frequência crescente, muitas vezes constituindo um achado acidental. A elevada prevalência de malignidade associada à NMPI-DP torna fundamental a sua identificação e correto diagnóstico.
A originalidade do caso descrito advém do facto de a neoplasia se ter manifestado por esteatorreia, uma das manifestações de NMPI mais raramente descritas na literatura. Além disso, apesar de a fistulização para órgãos adjacentes estar descrita como uma complicação, sobretudo das NMPI com transformação maligna, esta apenas ocorre numa minoria de casos e ainda mais raramente para 2 orgãos em simultâneo. Foi possível neste caso, com os exames endoscópicos, obter um diagnóstico no pré-operatório e detetar a complicação. O facto de, durante a EDA, não se ter detetado a fistulização para o estômago, poderá ser explicado pela presença de um orifício fistuloso de dimensões reduzidas, sem drenagem ativa de mucina aquando da realização do exame, tendo por estas razões passado desapercebido.
No caso em questão estavam presentes, à data do diagnóstico, vários fatores preditivos de NMPI maligna (presença de sintomas, Wirsung com marcada dilatação, lesão com dimensões superiores a 3 cm, papila protuberante), diagnóstico confirmado pelo exame anátomo-patológico da peça cirúrgica.
Bibliografia
1. Ferrone CR, Correa-Gallego C, Warshaw AL, Brugge WR, Forcione DG, Thayer SP, et al. Current trends in pancreatic cystic neoplasms. Arch Surg. 2009;144:448-54. [ Links ]
2. Salvia R, Fernández-del Castillo C, Bassi C, Thayer SP, Falconi M, Mantovani W, et al. Main-duct intraductal papillary mucinous neoplasms of the pancreas. Clinical predictors of malignancy and long-term survival following resection. Ann Surg. 2004;239:678-87. [ Links ]
3. Shimizu M, Kawaguchi A, Nagao S, Hozumi H, Komoto S, Hokari R, et al. A case of intraductal papillary mucinous neoplasm of the pancreas rupturing both the stomach and duodenum. Gastrointest Endosc. 2010;71:406-12. [ Links ]
4. Jaussét F, Delvaux M, Dumitriu D, Bressenot A, Bruot O, Mathias J, et al. Benign intraductal papillary mucinous neoplasm of the pancreas associated with spontaneous pancreatogastric and pancreatoduodenal fistulas. Digestion. 2010;82: 42-6. [ Links ]
5. Fernández-del Castillo C, Targarona J, Thayer SP, Rattner DW, Brugge WR, Warshaw AL. Incidental pancratic cysts: clinicopathologic characteristics and comparison with syntomatic patients. Arch Surg. 2003;138:427-33. [ Links ]
6. Kloppel G, Solcia E, Longnecker DS, Capella C, Solbin LH. Histological typing of tumors of the exocrine pancreas. Em: WHO international classification of tumours. 2nd ed. Berlin: Springer; 1996. [ Links ]
7. Carpizo DR, Allen PJ, Brennan MF. Current management of cystic neoplasms of the pancreas. Surgeon. 2008;6: 298-307. [ Links ]
8. Tanaka M, Chari S, Adsay V, Fernández-del Castillo C, Falconi M, Shimizu M, et al. International consensus guidelines for management of intraductal papillary mucinous neoplasms and mucinous cystic neoplasms of the pancreas. Pancreatology. 2006;6:17-32. [ Links ]
9. Kobayashi G, Fujita N, Noda Y, Ito K, Horaguchi J, Obana T, et al. Intraductal pappilary mucinous neoplasms of the pâncreas showing fistula formation into other organs. J Gastroenterol. 2010;45:1080-9. [ Links ]
10. Fernández-del Castillo C, Adsay N. Intraductal papillary mucinous neoplasm of the pancreas. Gastroenterology. 2010;139:708-13. [ Links ]
11. Cellier C, Cuiellerier E, Palazzo L, Rickaert F, Flejou JF, Napoleon B, et al. Intraductal papillary and mucinous tumours of the pancreas: accuracy of preoperative computer tomography, endoscopic retrograde pancreatography and endoscopic ultrasonography and long-term outcome in large surgical series. Gastrointest Endosc. 1998;47:42. [ Links ]
12. Sugiyama M, Atomi Y, Saito M. Intraductal papillary tumors of the pancreas: evaluation with endoscopic ultrasonography. Gastrointest Endosc. 1998;48:164-71. [ Links ]
13. Kubo H, Chijiiwa Y, Akahoshi K, Hamada S, Harada N, Sumii T, et al. Intraductal papillary mucinous tumors of the pancreas: differential diagnosis between benign and malignant tumors by endoscopic ultrassonography. Am J Gastroenterol. 2001;96:1429-34. [ Links ]
14. Fujino Y, Matsumoto I, Ueda T, Toyama H, Kuroda Y. Proposed new score predicting malignancy of intraductal papillary mucinous neoplasms of the pâncreas. Am J Surgery. 2007;194:304-7 [ Links ]
Conflito de interesses
Os autores declaram não haver «conflito de interesses.
*Autor para correspondência
Correio eletrónico: pimentelrita80@gmail.com (R. Pimentel).
Recebido a 11 de novembro de 2011; aceite a 11 de maio de 2012













