Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Jornal Português de Gastrenterologia
versão impressa ISSN 0872-8178
J Port Gastrenterol. vol.20 no.2 Lisboa mar. 2013
https://doi.org/10.1016/j.jpg.2012.04.036
Ganglioneuromatose intestinal difusa associada a adenocarcinomas do intestino delgado
Intestinal diffuse ganglioneuromatosis associated with small bowel adenocarcinomas
Pedro Monsantoa,∗, Paulo Soutoa, Juliana Oliveirab, Júlio Leiteb, Maria Augusta Ciprianoc, Frederico Carvalheirod, José Ilharcod, Hermano Gouveiaa e Carlos Sofiaa
a Serviço de Gastrenterologia, Hospitais da Universidade de Coimbra, Coimbra, Portugal
b Serviço de Cirurgia A, Hospitais da Universidade de Coimbra, Coimbra, Portugal
c Serviço de Anatomia Patológica, Hospitais da Universidade de Coimbra, Coimbra, Portugal
d Serviço de Imagiologia, Hospitais da Universidade de Coimbra, Coimbra, Portugal
*Autor para correspondência
RESUMO
A ganglioneuromatose intestinal inclui-se dentro das síndromes não-hereditárias de polipose hamartomatosa. É uma patologia rara do sistema nervoso entérico, caracterizada por uma hiperplasia difusa dos plexos neuronais da parede intestinal. Manifesta-se habitualmente sob a forma de obstipação ou diarreia associada a dor e distensão abdominal, e ocorre frequentemente associada à neurofibromatose tipo 1 ou à síndrome de neoplasias endócrinas múltiplas tipo 2b, podendo ser a sua manifestação inicial. Pode mais raramente apresentar-se sob uma forma esporádica e isolada. Embora seja encarada como uma lesão benigna, poderá estar associada a degeneração neoplásica do epitélio intestinal. O caso aqui descrito relata uma forma de ganglioneuromatose intestinal difusa do intestino delgado associada a carcinomas, muito raramente descrita na literatura.
Palavras-Chave Ganglioneuromatose intestinal; Adenocarcinoma Intestinal; Intestino delgado; Endoscopia
ABSTRACT
Intestinal ganglioneuromatosis is included in the syndrome of non-hereditary hamartomatous polyposis. It is a rare disorder of the enteric nervous system, characterized by a diffuse hyperplasia of the neural plexus of the intestinal wall. Usually it manifests in the form of constipation or diarrhea associated with abdominal distension and pain. It is often associated with neurofibromatosis type 1 and multiple endocrine neoplasia type 2b and may be one of its first manifestations. More rarely it can present in a sporadic and isolated form. Although regarded as a benign lesion, it can be associated with neoplastic degeneration of the intestinal epithelium. In the present case we describe a diffuse intestinal ganglioneuromatosis of small bowel associated with carcinomas, very rarely described in literature.
Keywords Intestinal ganglioneuromatosis; Intestinal Adenocarcinoma; Small Bowel; Endoscopy
Introdução
As lesões neurofibromatosas do trato gastrointestinal compreendem lesões hamartomatosas benignas, caracterizadas por um crescimento excessivo de células ganglionares do sistema nervoso entérico. Podem expressar-se por distintas formas e, por esse motivo, foram-lhes atribuídas diversas designações como neurofibromatose intestinal, ganglioneuromatose, neurofibromatose difusa plexiforme, displasia intestinal neuronal e polipose ganglioneuromatosa difusa. Surgem frequentemente num contexto sindrómico associadas à neurofibromatose tipo 1 (NF1) ou à síndrome de neoplasias endócrinas múltiplas tipo 2b (NEM2b), também se encontrando descrita na ausência destas doenças sistémicas. A ganglioneuromatose intestinal (GNI) pode sobrevir numa forma polipóide, manifestando-se por pólipos isolados compostos por células fusiformes e células ganglionares, numa forma de polipose múltipla, mais comum no íleon terminal e cólon, ou numa forma difusa, caracterizada por hiperplasia do plexo mioentérico e proliferação infiltrativa do tecido ganglioneuromatoso ao longo da parede de várias ansas intestinais1. Embora considerada uma lesão benigna pode muito raramente estar associada a degeneração neoplásica do epitélio intestinal2, com alguns casos de transformação maligna documentados na literatura3-8.
Caso clínico
Apresentamos o caso de uma mulher de 54 anos de idade, com queixas de enfartamento gástrico e distensão abdominal com vários anos de evolução. Sem emagrecimento recente, referia episódios de diarreia com início após colecistectomia por colecistite litiásica 6 anos antes, mencionando também um episódio de pancreatite aguda no passado. Antecedentes de fibromiomas uterinos, sem mais história pessoal ou familiar de patologia oncológica e medicada apenas com omeprazole. Em 2004, para estudo destas queixas tinha realizado um trânsito do intestino delgado que evidenciara uma volumosa dilatação do duodeno na transição da 2.a para a 3.a porção, suspeitando-se de uma síndrome da artéria mesentérica superior. O restante estudo do delgado mostrava ligeiro aumento do calibre das ansas, sem outras zonas dilatadas, também presente em TC abdominal, mas não valorizado. A EDA nessa mesma altura mostrava uma papila de Vater proeminente e irregular e um pólipo pediculado adjacente. Contudo, as biopsias da papila mostraram apenas uma mucosa com lesões inflamatórias sem displasia. Este estudo foi complementado por uma colonoscopia com polipectomia de 5 adenomas tubulovilosos (< 10 mm).
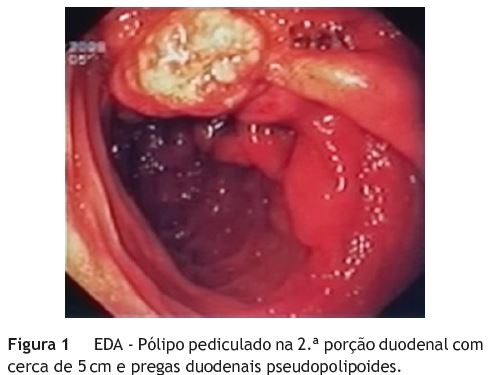
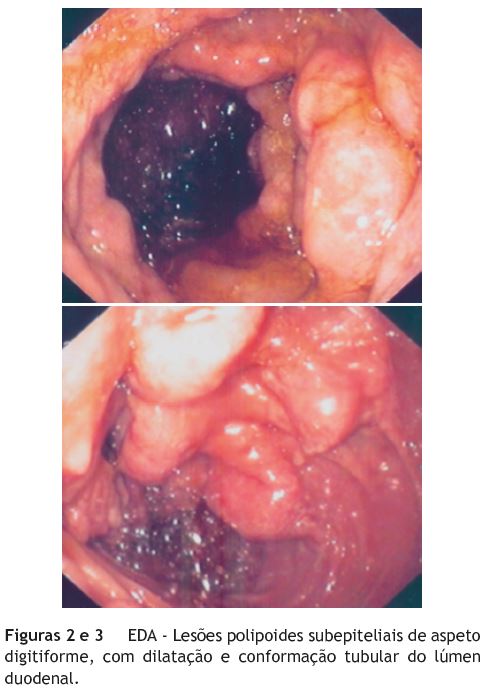
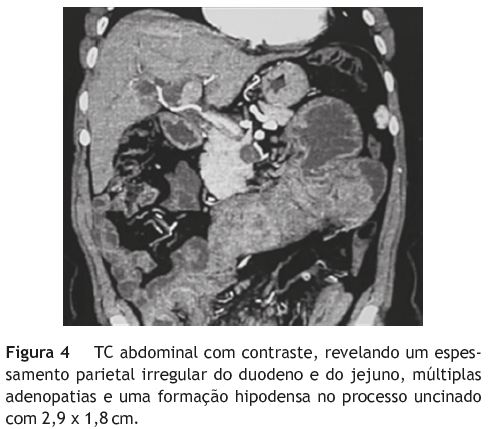
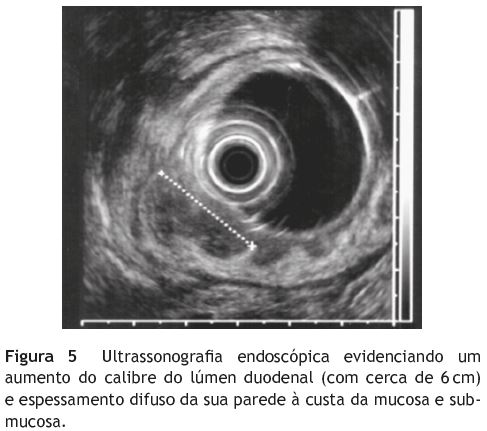
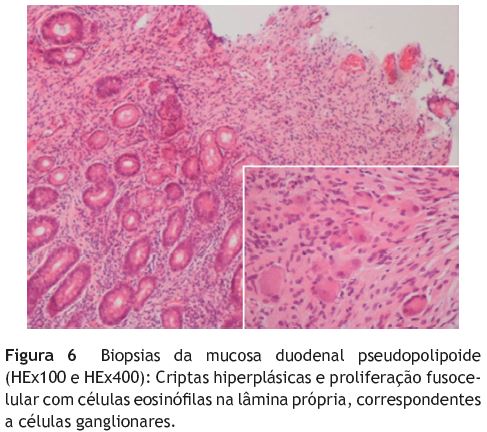
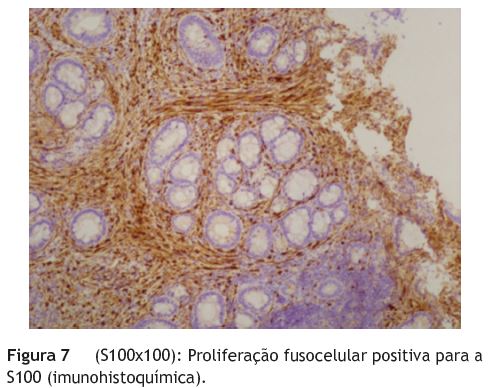
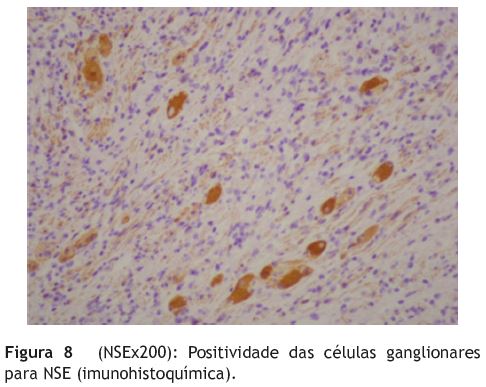
Seguida durante alguns anos pelo médico assistente, foi posteriormente referenciada à nossa consulta por agravamento da sintomatologia. Não apresentava alterações quer ao exame físico quer no estudo laboratorial e, numa nova EDA, identificava-se um pólipo pediculado com 5 cm ao nível da 2a porção duodenal, submetido a ressecção endoscópica (fig. 1), descrito histologicamente como pólipo hiperplásico. As biopsias da papila revelaram novamente um infiltrado inflamatório misto sem alterações epiteliais. Era também visível um aspeto pseudopolipoide das pregas duodenais (figs. 2 e 3). Realizou angioTC abdominal que excluía síndrome da artéria mesentérica superior, mas mostrava dilatação de ansas do delgado e dilatação da via biliar principal (1,1 cm) condicionada por espessamento parietal irregular do duodeno e do jejuno (fig. 4), identificando-se também um nódulo no processo uncinado pancreático (2,9 x 1,8 cm). A ultrassonografia endoscópica (fig. 5) mostrou espessamento difuso da mucosa e submucosa (11mm) e a citologia da punção do nódulo pancreático mostrou apenas grupos de células ductais normais. Foram repetidas biopsias endoscópicas da mucosa duodenal pseudopolipoide, sendo evidentes criptas dismórficas e hiperplásicas, em cuja lâmina própria se observava um infiltrado inflamatório e uma proliferação fusocelular com células de citoplasma eosinófilo sugestivas de células ganglionares (fig. 6). No estudo imunohistoquímico a proliferação fusocelular mostrou positividade para a S100 e as células ganglionares para NSE, confirmando a sua origem nervosa, e compatível com uma polipose ganglioneuromatosa intestinal. (fig. 7 e fig. 8). A panqueratina MNF116 e os marcadores endócrinos cromogranina A e sinaptofisina eram negativos. Estes aspetos estavam já presentes nas amostras do passado, quando revistas as lâminas das peças de polipectomia e biopsias da papila duodenais. O doseamento de vários parâmetros hormonais era normal, os anticorpos para doença celíaca eram negativos, a ecografia da tiroide com punção revelara 2 nódulos coloides e uma cintigrafia para recetores da somatostatina não individualizava lesões. A presença de uma mancha café-au-lait (fig. 9) levantou a suspeita de uma associação com NF1; no entanto, o estudo efetuado, incluindo RMN-CE e radiografia do esqueleto, não revelou outras características necessárias para o seu diagnóstico. Igualmente, o estudo genético com pesquisa de mutações nos genes RET (recetor tyrosine kinase), NF1, Von-Hippal-Lindau, succinato desidrogenase subunidade B e D foi negativo.

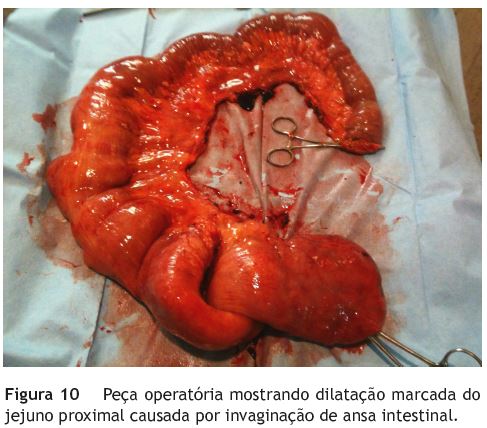
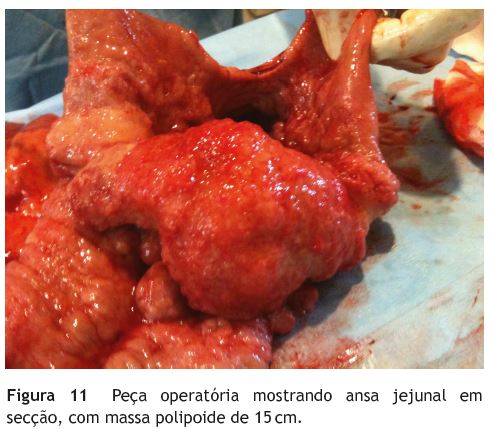
Manteve vigilância endoscópica e imagiológica, continuando a evidenciar-se um espessamento no delgado desde o início da 2.a porção duodenal, sem zona de transição evidente para ansas normais e ansas dilatadas, que atingiam um calibre máximo de 7,5 cm. Dado o caráter difuso, a cirurgia não parecia uma opção válida, pelo que se manteve a mesma atitude expectante. Ocorreu agravamento gradual da sintomatologia, com episódios frequentes de distensão abdominal, sem paragem da emissão de gases ou fezes, mas com hiperperistaltismo, dor abdominal tipo cólica, diarreia e vómitos ocasionais, associados a perda ponderal. Em reavaliação imagiológica por TC, num desses episódios, identificou-se uma formação polipoide com 7,5 cm de diâmetro que se invaginava no interior de outra ansa, condicionando uma dilatação marcada do jejuno proximal. Após resolução do quadro de sub-oclusão realizou-se uma laparotomia exploradora eletiva, identificando-se para além da distensão do jejuno proximal uma massa polipoide de 15 cm, múltiplas lesões polipóides sésseis da mucosa e conglomerados de nódulos mesentéricos (fig. 10 e fig. 11). Optou-se por efetuar uma jejunectomia segmentar com 130 cm de extensão. As lesões polipoides jejunais e mesentéricas correspondiam a uma proliferação de células fusiformes (S100+) e ganglionares (NSE+) da submucosa, traduzindo, respetivamente, um processo de ganglioneurofibromatose difusa do jejuno e neurofibromas plexiformes do mesentério. Contudo, a lesão polipoide com 15 cm correspondia a um adenocarcinoma mucinoso invasor, que infiltrava o tecido adiposo mesentérico. Para além deste, encontraram-se na peça operatória mais 2 adenocarcinomas invasores síncrones com padrão tubular e doença metastática nos gânglios linfáticos regionais. Uma outra lesão polipoide correspondia a um adenoma tubular com morfologia de neoplasia intraepitelial de baixo grau. O estadiamento TNM/AJCC correspondia deste modo a uma lesão T3N2 Mx/estádio IIIB, pelo que foi proposta para realização de quimioterapia em esquema de capecitabina e oxiplatina. Não se verificaram novos episódios suboclusivos ou de distensão abdominal, num período de observação de 5 meses.
Discussão
A GNI inclui-se dentro das síndromes não-hereditárias de polipose hamartomatosa. Compreende uma proliferação benigna das células nervosas ganglionares, fibras nervosas e células da glia9. Embora vários genes de suscetibilidade tenham sido determinados para outras poliposes, nenhum gene individual foi identificado para a GNI, atribuindo-se o seu desenvolvimento a um fator de crescimento solúvel de células nervosas10.
Ocorre frequentemente associada à NF1 ou à síndrome NEM2b, podendo ser a sua manifestação inicial. Aproximadamente 25% dos doentes com NF1, uma doença neurocutânea caracterizada pela presença de tumores benignos das bainhas nervosas, apresenta neurofibromatose que acomete o trato digestivo com múltiplos ganglioneuromas11. Também a síndrome NEM2b, caracterizada pela presença de feocromocitoma, carcinoma medular da tiroide e neuromas mucocutâneos, se associa a ganglioneuromatose gastrointestinal12. Além destas associações, estão ainda descritos casos de ocorrência familiar e em polipose cólica juvenil e adenomatosa13-15. Tal como no caso descrito, pode igualmente ocorrer como achado isolado sem evidência clínica de síndromes polipoides ou neurocutâneas e de neoplasias endócrinas múltiplas16,17.
Os ganglioneuromas gastrointestinais podem incluir-se num de 3 grupos: ganglioneuromas polipoides isolados, polipose ganglioneuromatosa e ganglioneuromatose difusa1. Cada uma delas acomete mais frequentemente o cólon e reto e menos frequentemente o intestino delgado, estando descritos alguns casos localizados ao trato digestivo superior1,18. A apresentação clínica correlaciona-se com a localização e extensão das lesões e seu efeito na motilidade gastrointestinal, podendo manifestar-se como alteração dos hábitos intestinais, dor abdominal, obstrução intestinal, hemorragia ou como massas abdominais17. No caso de associação com a NF1, os achados clínicos incluem manchas café-au-lait, efélides, nódulos de Lisch e displasias ósseas (tabela 1)19. Já no contexto da síndrome NEM2b podem estar presentes o habitus marfanoide, neuromas muco-cutâneos, hipertrofia dos nervos da córnea e múltiplas alterações músculo-esqueléticas. Doentes com NEM2b e ganglioneuromatose apresentam-se tipicamente numa idade jovem e com alterações da motilidade gastrointestinal20. No caso clínico apresentado, uma associação com NF1 ou com a síndrome NEM2b foi afastada, não cumprindo os respetivos critérios de diagnóstico.

Numa forma difusa de GNI como aquele que descrevemos, com proliferação das lesões na submucosa originando dilatações do intestino delgado, pode ocorrer diarreia, síndrome de má absorção, distensão abdominal e, em casos mais graves, oclusão e perfuração intestinal21. O tamanho das lesões é variável, desde lesões milimétricas a massas de 17 cm, que causam estreitamentos luminais semelhantes a uma estenose por carcinoma. A TC pode revelar esse estreitamento e espessamento circunferencial das ansas intestinais afetadas e, em alguns casos de atingimento ileal, pode estar presente o sinal do pente, simulando a doença de Crohn21,22.
Embora não se encontrem alterações endoscópicas características, alguns aspetos podem sugerir o diagnóstico. Por um lado, a proliferação de células nervosas intramucosas eleva o epitélio e origina a formação de lesões subepiteliais de aspeto digitiforme, de tamanho e distribuição variáveis. Enquanto em alguns casos estas lesões são diminutas e atapetam parte de um segmento intestinal, em outros a dimensão das lesões resulta numa estenose. Por outro lado, as alterações da inervação da parede intestinal devido à hiperplasia do plexo mioentérico e de outras estruturas do sistema nervoso autónomo do trato digestivo determinam alterações segmentares de contração intestinal e desenham um aspeto tubular do seu lúmen5. Esta aparência era claramente identificada no caso clínico que descrevemos, quer quanto ao espessamento difuso da parede duodenal visível na ultrassonografia endoscópica, quer no pregueamento pseudopolipoide do duodeno visível na endoscopia. As biopsias endoscópicas são um dos pilares diagnósticos, contudo, as amostras colhidas podem proporcionar apenas fragmentos de mucosa indemne sobrejacente às lesões, dada a sua localização variável na parede digestiva17. É característica a proliferação de fibras nervosas, células ganglionares e células da glia, desde uma expansão hiperplásica fusiforme do plexo mioentérico a uma proliferação ganglioneuromatosa transmural e irregular que distorce o plexo mioentérico e infiltra a parede intestinal adjacente. A imunohistoquímica proporciona uma preciosa ajuda ao diagnóstico. A imunorreatividade das células ganglionares para a proteína S100, proteína ácida fibrilar glial, vimentina, enolase neurónio específica e sinaptofisina confirma a origem nervosa da proliferação celular5. A dificuldade diagnóstica resulta não só do seu aspeto endoscópico e imagiológico inespecífico, mas também da sua baixa incidência, não sendo considerada ab initio no diagnóstico diferencial deste género de lesões. Este terá de ter em conta as várias neoplasias epiteliais e do estroma gastrointestinal, bem como os linfomas do tubo digestivo, nomeadamente numa apresentação sob a forma de polipose linfomatosa.
Neste caso que descrevemos, não se adotou nenhuma atitude diagnóstica invasiva suplementar relativamente ao nódulo pancreático, uma vez que, por um lado, o controlo por TC revelava estabilidade das suas dimensões, e por outro lado, a cintigrafia de recetores de somatostatina, as características imagiológicas e o doseamento de diversos parâmetros laboratoriais não favorecia a hipótese de tumor neuroendócrino. Embora o estudo citológico mostrasse apenas grupos celulares coesivos de células ductais normais, não seria de excluir a hipótese de se tratar de um ganglioneuroma pancreático.
Como se sabe, há uma conhecida associação entre o carcinoma do cólon e a polipose adenomatosa. No entanto, no que concerne às síndromes de polipose hamartomatosa, apenas a polipose de Peutz-Jeghers e a polipose juvenil implicam um acréscimo no risco de malignidade. Já a relação entre GNI e malignidade não está consistentemente estabelecida. Contudo, apesar de numa revisão elaborada por Shekitka e Sobin que incidiu sobre 43 doentes com ganglioneuromas gastrointestinais seguidos entre 3,3 e 24 anos não se ter verificado nenhum caso de carcinoma intestinal23, a coexistência da GNI com o adenocarcinoma do intestino delgado e colorretal foi reportada em algumas ocasiões3-8. Um facto a realçar é que na maioria desses casos, tal como no caso aqui apresentado, a ganglioneuromatose não se encontrava associada à NF1. Esta associação com o adenocarcinoma intestinal legitima alguma incerteza quanto à orientação terapêutica destas situações. No caso de ganglioneuromas polipoides isolados ou numa polipose ganglioneuromatosa circunscrita a um curto segmento digestivo, o tratamento adequado será primariamente cirúrgico no caso de estenose, invaginação ou alterações da motilidade gastrointestinal que ocasionem sintomas suboclusivos que não respondam ao tratamento médico. Tal deverá também ser ponderado sempre que se suspeite de uma lesão neoplásica. Já no caso de um atingimento difuso do intestino delgado, como no caso aqui apresentado, com necessidade de ressecções alargadas e inerente risco síndrome de intestino curto, a decisão sobre uma intervenção cirúrgica é mais delicada. Contudo, embora não se encontrem casos descritos na literatura, tal poderá ser contornado com a realização de um transplante intestinal.
Bibliografia
1. Shekitka KM, Sobin LH. Ganglioneuromas of the gastrointestinal tract: relation to Von Recklinghausen disease and other multiple tumor syndromes. Am J Surg Pathol. 1994;18:250-7. [ Links ]
2. Flanders DJ, Mitros FA. Mucosal ganglioneuromatosis associated with multiple colonic polyps. Am J Surg Pathol. 1984;8:779-86. [ Links ]
3. Macenlle R, Fernandez-Seara J, Pato M, Pereira J, Pascual P, Montero M, et al. Ganglioneuromatous polyposis of the colon associated with adenocarcinoma and primary hyperparathyroidism. Eur J Gastroenterol Hepatol. 1999;11:447-50. [ Links ]
4. Snover DC, Weigent CE, Sumner HW. Diffuse mucosal ganglioneuromatosis of the colon associated with adenocarcinoma. Am J Clin Pathol. 1981;75:225-9. [ Links ]
5. Chambonnière ML, Porcheron J, Scoazec JY, Audigier JC, Mosnier JF. Intestinal ganglioneuromatosis diagnosed in adult patients. Gastroenterol Clin Biol. 2003;27:219-24. [ Links ]
6. Stratopoulos C, Papakonstantinou A, Anagnostopoulos G, Terzis I, Tzimas G, Gourqiotis S, et al. Intestinal neurofibromatosis and small-bowel adenocarcinoma: a single case study. Eur J Cancer Care. 2009;18:466-9. [ Links ]
7. Shousha S, Smith PA. Colonic ganglioneuroma, Report of a case in a patient with neurofibromatosis, multiple colonic adenomas and adenocarcinoma. Virchows Arch A Pathol Anat Histol. 1981;392:105-9. [ Links ]
8. Tomita H, Miya K, Tanaka H, Shimokawa K. Ganglioneuroma and adenocarcinoma associated with neurofibromatosis type 1 in the colorectal region. Int J Colorectal Dis. 2006;21:89-91. [ Links ]
9. Haggitt RC, Reid BJ. Hereditary gastrointestinal polyposis syndromes. Am J Surg Pathol. 1986;10:871-87. [ Links ]
10. DeSchryver-Kecskemeti K, Clouse RE, Goldstein MN, Gersell D, ONeal L. Intestinal ganglioneuromatosis: a manifestation of overproduction of nerve growth factor? N Engl J Med. 1983;308:635-9. [ Links ]
11. Rutgeerts P, Hendricks H, Geboes K, Ponette E, Broeckaert L, Vantrappen G. Involvement of the upper digestive tract by systemic neurofibromatosis. Gastrointest Endosc. 1981;27:22-5. [ Links ]
12. Carney JA, Go VL, Sizemore GW, Hayles AB. Alimentary-tract ganglioneuromatosis. A major component of the syndrome of multiple endocrine neoplasia, type 2b. N Engl J Med. 1976;295:1287-91. [ Links ]
13. Weidner N, Flanders DJ, Mitros FA. Mucosal ganglioneuromatosis associated with multiple colonic polyps. Am J Surg Pathol. 1984;8:779-86. [ Links ]
14. Mendelsohn G, Diamond MP. Familial ganglioneuromatous polyposis of the large bowel, Report of a family with associated juvenile polyposis. Am J Surg Pathol. 1984;8:515-20. [ Links ]
15. Rafiq S, Hameer H, Sitrin MD. Ganglioneuromatous polyposis associated with juvenile polyps and a tubular adenoma. Dig Dis Sci. 2005;50:506-8. [ Links ]
16. Bononi M, De Cesare A, Stella MC, Fiori E, Galati G, Atella F, et al. Isolated intestinal neurofibromatosis of colon, Single case report and review of the literature. Dig Liver Dis. 2000;32:737-42. [ Links ]
17. Carter JE, Laurini JA. Isolated intestinal neurofibromatous proliferations in the absence of associated systemic syndromes. World J Gastroenterol. 2008;14:6569-71. [ Links ]
18. Maunoury V, Fabre S, Wacrenier A, Mariette C, Triboulet JP. Extensive ganglioneuromatosis of the esophagus: uncommon location of Von Recklinghausens disease. Gastroenterol Clin Biol. 2005;29:1181-2. [ Links ]
19. National Institute of Health Consensus Development Conference. Neurofibromatosis. Conference Statement. Arch Neurol. 1988;45:575-8. [ Links ]
20. Demos TC, Blonder J, Schey WL, Braithwaite SS, Goldstein PL. Multiple endocrine neoplasia (MEN) syndrome type IIB: gastrointestinal manifestations. AJR Am J Roentgenol. 1983;140: 73-8. [ Links ]
21. Tobler A, Maurer R, Klaiber C. Stenosing ganglioneuromatosis of the small intestine with ileus and ileal rupture. Schweiz Med Wochenschr. 1981;111:684-8. [ Links ]
22. Charagundla SR, Levine MS, Torigian DA, Campbell MS, Furth EE, Rombeau J. Diffuse intestinal ganglioneuromatosis mimicking Crohns disease. AJR Am J Roentgenol. 2004;182:1166-8. [ Links ]
23. Shekitka KM, Sobin LH. Ganglioneuromas of the gastrointestinal tract, Relation to Von Recklinghausen disease and other multiple tumor syndromes. Am J Surg Pathol. 1994;18:250-7. [ Links ]
Conflito de interesses
Os autores declaram não haver conflito de interesses.
*Autor para correspondência
Correio eletrónico: pedromonsanto@gmail.com (P. Monsanto).
Recebido a 28 de novembro de 2011; aceite a 9 de janeiro de 2012













