Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Jornal Português de Gastrenterologia
versão impressa ISSN 0872-8178
J Port Gastrenterol. vol.20 no.6 Lisboa dez. 2013
https://doi.org/10.1016/j.jpg.2013.01.002
ARTIGO ORIGINAL
Determinação das diferentes estirpes de Clostridium difficile num grupo de doentes com infecção causada por esta bactéria
Clostridium difficile strain stypes determination in patients infected with this bacteria
Cláudia Cardosoa,∗, Ricardo Freirea, Jesuína Duarteb, Mónica Oleastroc, Andrea Santosc, João Carlos Rodriguesc, Isabelle Cremersa e Ana Paula Oliveiraa
a Serviço de Gastrenterologia, Centro Hospitalar de Setúbal, Setúbal, Portugal
b Serviço de Patologia Clínica, Centro Hospitalar de Setúbal, Setúbal, Portugal
c Departamento de Doenças Infecciosas, Instituto Nacional de Saúde Doutor Ricardo Jorge, Lisboa, Portugal
*Autor para correspondência
RESUMO
Introdução: Nos últimos anos tem-se verificado uma incidência crescente da doenc¸a associada a Clostridium difficile (DACD). A caracterização molecular das várias estirpes tem permitido o reconhecimento de determinados ribotipos da bactéria associados a uma maior virulência.
Objetivo: Isolamento e caracterização molecular das estirpes de Clostridium difficile responsáveis por DACD e a sua correlação clínica numa série hospitalar.
Material e métodos: Análise prospetiva de doentes consecutivos com DACD, incluídos durante um período de 18 meses. Foi realizada a colheita de dados epidemiológicos, clínicos e laboratoriais. Após exame cultural das fezes, todas as estirpes da bactéria foram caracterizadas geneticamente, por deteção do gene gluD, específico da espécie, e dos genes codificantes das toxinas A e B. Posteriormente, as estirpes foram genotipadas, com determinação do ribotipo, por amplificação por PCR da região intergénica RNAr16S-23S e separação por eletroforese em gel por capilaridade.
Resultados: Foram incluídos 20 doentes, 65% do sexo feminino, com uma idade média de 73 anos. A maioria dos doentes adquiriu a infeção em contexto nosocomial e apresentava história de antibioterapia prévia. O diagnóstico de DACD ocorreu, em média, ao 7.◦ dia de internamento. Todas as estirpes foram confirmadas como sendo Clostridium difficile, produtoras das toxinas A e/ou B. Foi possível obter um perfil de ribotipo em 17 estirpes, não tendo sido identificada nenhuma dominante. Os ribotipos mais observados foram o R014, o R027, o R126 e o R501, cada um detetado em 2 doentes. Foram ainda isolados 3 novos perfis, sem homologia na base de dados. Não houve correlação entre a gravidade da doença e os ribotipos identificados.
Conclusões: Na nossa casuística não se isolou nenhum ribotipo dominante, observando-se 2 casos causados pela estirpe hipervirulenta R027. Não se verificou associação entre a gravidade da doença e os ribotipos isolados.
Palavras-chave: Clostridium difficile; Ribotipagem; Electroforese em gel por capilaridade
ABSTRACT
Introduction: The incidence of Clostridium difficile- associated disease (CDAD) has increased in the last years. Molecular analysis of the different strains of this bacteria has identified specific ribotypes associated with a more severe disease.
Aim: Molecular characterization of Clostridium difficile strains isolated from consecutive inpatients with CDAD and its correlation with clinical outcome.
Material and methods: A prospective analysis of consecutive patients with CDAD recruited during 18 months. Epidemiological, clinical and laboratory data were collected. After stool culture, the isolates were genetically characterized with primers for gluD, tcdA and tcdB genes. The strains were then typed by PCR ribotyping, with primers for rRNA16S-23S genes, and capillary gel electrophoresis analysis.
Results: 20 patients were included, 65% were female. Their mean age was 73 years. In the majority of cases the infection was nosocomial and there was a history of antibiotic therapy intake. All strains were confirmed as toxins A and/or B producing Clostridium difficile. Ribotypes R014, R027, R126 and R051 were the most common strains. There was no correlation between isolated strains and the severity of the disease.
Conclusions: In our series, there was a lack of association between clinical outcome of Clostridium difficile-associated diarrhea and the several strains identified.
Keywords: Clostridium difficile; Ribotyping; Pulsed field gel electrophoresis
Introdução
O Clostridium difficile (C. difficile) é uma bactéria gram positiva anaeróbia que se encontra presente na flora intestinal de 3% da população adulta saudável.
Existem, no entanto, várias condições que podem afetar a flora intestinal e predispor a doença associada a C. difficile (DACD) no Homem.
O espectro clínico da DACD varia desde o portador assintomático (cuja prevalência atinge os 35% em doentes hospitalizados) até à colite pseudomembranosa grave com megacólon tóxico associado, cuja mortalidade se situa entre 6-30%1-3.
Tradicionalmente, a DACD ocorre em contexto nosocomial, associada à utilização de antibióticos (principal factor de risco para a infeção), idade avançada e estados de imunossupressão. Existem, contudo, na literatura, casos descritos de infeção por esta bactéria em populações da comunidade consideradas de baixo risco4.
A sua virulência é mediada, na maioria dos casos, pela produção em simultâneo de 2 toxinas, A e B, ambas codificadas por genes do locus de patogenicidade, ocorrendo a sua transmissão por via fecal-oral e a sua disseminação através do contacto com doentes infetados, profissionais de saúde ou superfícies contaminadas5,6.
Nos últimos anos, tem-se assistido, a nível mundial, a um aumento do número de casos de infeção por C. difficile associados a doença mais grave, maior resistência aos antibióticos, com mortalidade e taxa de recidivas mais elevadas. São conhecidos atualmente mais de 150 ribotipos e 24 toxinotipos da espécie7. A emergência de uma nova estirpe de C. difficile, designada de NAP1 ou ribotipo 027, tem sido implicada em vários surtos de doença grave na última década quer em contexto hospitalar quer em populações saudáveis da comunidade. A produção de níveis mais elevados de toxinas A e B, para além de uma toxina adicional conhecida como a toxina binária, parecem conferir uma maior virulência8-10.
No Centro Hospitalar de Setúbal assistiu-se, em determinada altura, a um aumento da incidência de DACD com critérios de gravidade e com uma percentagem de recidiva mais elevada, o que motivou o início deste estudo inovador com o intuito de caracterizar as estirpes circulantes na nossa Instituição e melhorar as recomendações diagnósticas, terapêuticas e preventivas na DACD.
Objetivo
Isolamento e caracterização molecular das estirpes de C. difficile responsáveis por DACD e a sua correlação clínica numa série hospitalar.
Material e métodos
Análise prospetiva de doentes consecutivos com DACD, incluídos durante um período de 18 meses (março de 2010-agosto de 2011). O estudo foi aprovado pela Comissão de Ética Hospitalar, tendo sido obtido o consentimento informado em todos os casos.
Foram incluídos doentes seguidos em internamento nos Serviços de Medicina Interna, Gastrenterologia e Nefrologia do Centro Hospitalar de Setúbal.
O diagnóstico de DACD baseou-se no quadro clínico complementado por um dos seguintes achados:
- Presença de toxinas A e/ou B nas fezes detetadas através do método de imunocromatografia (sensibilidade de 87-92%).
- Exames endoscópico e histológico com achados sugestivos de infeção.
Foram considerados critérios de gravidade da doença a presença de febre (≥38◦C), leucocitose > 15.000 células/mL, hipoalbuminémia de novo < 3,5 g/dL, megacólon tóxico, sépsis grave/choque séptico, perfuração intestinal e morte.
Após exame cultural das fezes em meio seletivo Oxoid todas as estirpes da bactéria foram caracterizadas geneticamente, por deteção do gene gluD, específico da espécie, e dos genes codificantes das toxinas A e B. Posteriormente, as estirpes foram genotipadas, com determinação dos ribotipo por amplificação por PCR da região intergénica RNAr16S-23S e separação por eletroforese em gel por capilaridade.
A denominação de cada estirpe foi realizada através da homologia com os padrões de migrac¸ão das estirpes inseridas na base de dados europeia (http://webribo.ages.at), onde se encontram registados todos os ribotipos conhecidos até ao momento.
O estudo decorreu em parceria com o Instituto Nacional de Saúde Doutor Ricardo Jorge.
Resultados
Foram incluídos 20 doentes, 65% do sexo feminino, com uma idade média de 73 anos (32-89).
A infeção foi adquirida em contexto nosocomial em 85% dos casos. Todos os doentes se encontravam sob antibioterapia. As principais doenças infeciosas que motivaram a necessidade de antibioterapia foram a respiratória e a urinária (fig. 1). As classes de antibióticos mais utilizadas foram as penicilinas, carbapenems, quinolonas e cefalosporinas (fig. 2). O número médio de antibióticos por doente foi de 2.

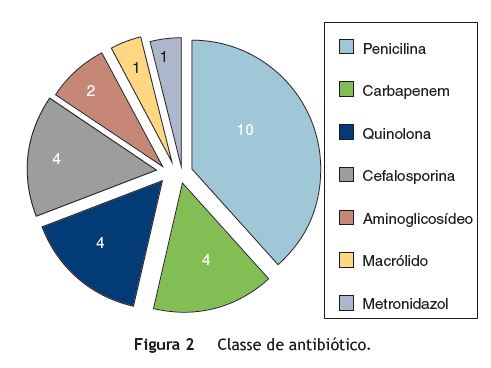
Três doentes adquiriram a doença em ambulatório, sem fatores de risco identificados para infeção.
O diagnóstico de DACD ocorreu em média ao 7.◦dia de internamento. A diarreia aquosa foi a forma de manifestação da doença em todos os casos, com um número médio de 7 dejeções/dia. As principais alterações analíticas foram a leucocitose (55%), com valores inferiores a 15.000 células/mL, e a hipoalbuminémia (85%), com um valor médio de 2,7 g/dL (fig. 3). No entanto, os baixos níveis de albumina já se verificavam previamente ao início da DACD, em relac¸ão provável com as intercorrências infeciosas que motivaram o início de antibioterapia e a baixa ingesta alimentar.

Não se registaram casos de DACD com critérios de gravidade.
Todas as estirpes eram produtoras de toxina A e, na maioria dos casos, de toxina B em simultâneo.
Onze doentes foram submetidos a rectossigmoidoscopia, a qual revelou aspetos sugestivos de colite pseudomembranosa, caracterizada por placas esbranquiçadas a recobrir a mucosa do reto e/ou sigmóide, confirmada histologicamente, em 6 casos, e erosões, em 3 casos, não se verificando alterações da mucosa na extensão observada em 2 doentes.
O metronidazol foi a antibioterapia de primeira linha utilizada em todos os doentes na dose de 500 mg 8/8 h, na maioria dos casos administrada por via oral (n = 16) e, na sua ausência, por via endovenosa (n = 4). Dada a ausência de melhoria nas primeiras 72 h em 3 doentes sob antibioterapia por via endovenosa, o esquema antibiótico foi alterado para vancomicina, com resolução do quadro (fig. 4). A duração do esquema terapêutico foi de 10 dias.
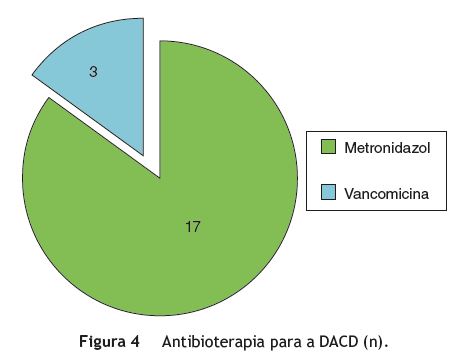
A caracterização genética confirmou que todas as estirpes eram produtoras de toxina A e, em 85% dos casos, de toxina B. A produção de toxina binária documentou-se em 25% dos casos, nomeadamente nos ribotipos 027, 126, 203 e novo ribotipo 3 (fig. 5).

Foi possível obter um perfil de ribotipo em 17 estirpes, tendo sido identificados 13 perfis distintos. Os mais frequentes foram os ribotipos 014, 027, 126 e 501, cada um detetado em 2 doentes (fig. 6).

Foram ainda identificados 3 novos perfis de ribotipos, designados no estudo como novos ribotipos 1, 2 e 3, sem homologia na base de dados europeia e que aguardam denominação.
Discussão
A diarreia associada a C. difficile constituí a causa mais frequente de diarreia infeciosa nosocomial no mundo ocidental. A apresentação clínica e a gravidade da doença são variáveis, com um espectro clínico que vai desde a diarreia ligeira até à colite grave complicada de megacólon tóxico, perfuração intestinal, sépsis e morte.
A virulência da bactéria é mediada pelas enterotoxina A e a citotoxina B, ambas codificadas por genes do locus de patogenicidade e cuja expressão é regulada pelo gene TcdR, estimulador da expressão, e reprimida pelo gene TcdC11,12.
Atualmente são conhecidos mais de 150 ribotipos da bactéria, mas apenas alguns são enteropatogéneos humanos. A amplificação por PCR da região intergénica RNAr16S-23S e separação por eletroforese em gel por capilaridade é o método mais utilizado a nível europeu na identificação dos vários ribotipos, permitindo a homologia da técnica de ribotipagem entre os vários laboratórios13.
Na última década, a estirpe NAP1/027 tem sido associada a surtos de doença em vários países Europeus, Canadá e Estados Unidos, caracterizados por maior gravidade do quadro clínico, com taxas de recidivas e de mortalidade mais elevadas. A presença de mutações em genes que suprimem a produção das toxinas A e B, como é o caso do gene TcdC, levando a uma maior produção de ambas, tem sido implicada na sua maior virulência14,10. Para além disso, esta estirpe produz a toxina binária, que se pensa promover a adesão às células do cólon, embora o seu papel não se encontre ainda totalmente estabelecido15. A maior taxa de esporulação e a consequente promoção da disseminação e persistência no meio hospitalar, bem como a resistência às fluoroquinolonas, têm sido outras das características inerentes a esta estirpe descritas em vários estudos. Contudo, várias séries mais recentes têm sugerido que, em contexto não epidémico, esta estirpe não se associa a doença mais grave16-18.
A epidemiologia molecular do C. difficile na nossa instituição revelou ser diversa, com a identificação de 13 estirpes diferentes.
Na nossa série o ribotipo 027 foi isolado em apenas 2 casos, ambos produtores de toxina binária. Embora seja um número reduzido, os doentes infetados não apresentaram critérios de gravidade da doença, suportando a ausência de uma maior virulência desta e das restantes estirpes isoladas em contexto não epidémico.
Este é o primeiro estudo a nível nacional sobre a epidemiologia molecular da infeção por C. difficile numa instituição hospitalar e que permitiu identificar 3 ribotipos não conhecidos a nível mundial. Como limitações ao estudo temos a amostra reduzida de doentes incluídos. Um estudo prospetivo multicêntrico que permitisse a inclusão de um maior número de doentes seria desejável, com o intuito de se determinar os ribotipos circulantes a nível nacional e o seu impacto clínico.
Concluindo, embora com um número reduzido de doentes incluídos, na nossa casuística não se isolou nenhum ribotipo dominante, observando-se 2 casos causados pela estirpe 027. Não se verificou associação entre a gravidade da doença e os ribotipos isolados. Foram detetados 3 novos perfis de ribotipos sem homologia na base de dados europeia e que aguardam denominação.
Bibliografia
1. Bartlett JG. Clinical practice: Antibiotic-associated diarrhea. N Engl J Med. 2002;31:334-9. [ Links ]
2. Akerlund T, Svenungsson B, Lagergren A, Burman LG. Correlation of disease severety with fecal toxin levels in patients with Clostridium difficile-associated diarrhea and distribution of PCR ribotypes and toxin yields in vitro of corresponding isolates. J Clin Microbiol. 2006;44:353-8. [ Links ]
3. Aslam S, Hamill RJ, Musher DM. Treatment of CDAC: Old therapies and new strategies. Lancet Inft Dis. 2005;5:549-57. [ Links ]
4. Johal SS, Hammond J, Solomon K, James PD, Mahida YR. Clostridium difficile associated diarrhoea in hospitalised patients: Onset in the community and hospital and role of flexible sigmoidoscopy. Gut. 2004;53:673-7. [ Links ]
5. Viscidi R, Willey S, Bartlett JG. Isolation rates and toxigenic potential of Clostridium difficile isolates from various patient populations. Gastroenterology. 1981;81:5-9. [ Links ]
6. Rupnik M, Dupuy B, Fairweaher NF. Revised nomenclature of Clostridium difficile toxins and associated genes. J Med Microbiol. 2005;54:113-7. [ Links ]
7. Kuiper EJ, Coignard B, Tull P. Emergence of Clostridium difficileassociated disease in North America and Europe. Clin Microbiol Infect. 2006;12 Suppl 6:2-18. [ Links ]
8. Spigaglia P, Mastrantonio P. Molecular analysis of the pathogenicity locus and polymorphism in the putative negative regulator of toxin production (TcdC) among Clostridium difficile clinical isolates. J Clin Microbiol. 2002;40:3470-5. [ Links ]
9. Popoff MC, Rubin EJ, Gill DM, Boquet P. Actin-specific ADPribosyltransferase produced by Clostridium difficile strain. Infect Immun. 1988;56:2299-306. [ Links ]
10. Warny M, Pepin J, Fang A, Killgore G, Thompson A, Brazier J, et al. Toxin production by an emerging strain of Clostridium difficile associated with outbreaks of severe disease in North America and Europe. Lancet. 2005;366:1079-84. [ Links ]
11. Mani N, Dupuy B. Regulation of toxin synthesis in Clostridium difficile by an alternative RNA polymerase sigma factor. Proc Natl Acad. 2001;98:5844-9. [ Links ]
12. Matamouros S, England P, Dupuy B. Clostridium difficile toxin expression is inhibited by the novel regulator TcdC. Mol Microbiol. 2007;64:1274-88. [ Links ]
13. Indra A, Huhulescu S, Schneeweis M, Hasenberger P, Kernbichler S, Fiedler A, et al. Characterization of Clostridium difficile isolates using capillary gel electrophoresis-based PCR ribotyping. J Med Microbiol. 2008;57:1377-82. [ Links ]
14. Dupuy B, Govind R, Antunes A, Matamouros S. Clostridium difficile toxin synthesis is negatively regulated by TcdC. J Med Microbiol. 2008;57:685-9. [ Links ]
15. Schwan C, Stecher B, Tzivelekidis T, van Ham M, Rohde M, Hardt WD, et al. Clostridium difficile toxin CDT induces formation of microtubule-based protrusions and increases adherence of bacteria. PLoS Pathog. 2009:e1000626. [ Links ]
16. Cloud J, Noddin L, Pressman A, Hu M, Kelly C. Clostridium difficile strain NAP-1 is not associated with severe disease in a nonepidemic setting. Clin Gastroenterol Hepatol. 2009;7:868-73. [ Links ]
17. Morgan OW, Rodrigues B, Elston T, Verlander NQ, Brown DF, Brazier J, et al. Clinical severity of Clostridium difficile PCR ribotype 027: A case-case study. PLoS One. 2008;3:e1812. [ Links ]
18. Wilson V, Cheek L, Satta G, Walker-Bone K, Cubbon M, Citron D, et al. Predictors of death after Clostridium difficile infection: A report on 128 strain-typed cases from a teaching hospital in the United Kingdom. Clin Infect Dis. 2010;50:e77-81. [ Links ]
Responsabilidades éticas
Proteção de pessoas e animais. Os autores declaram que para esta investigação não se realizaram experiências em seres humanos e/ou animais.
Confidencialidade dos dados. Os autores declaram ter seguido os protocolos do seu centro de trabalho acerca da publicação dos dados de pacientes e que todos os pacientes incluídos no estudo receberam informações suficientes e deram o seu consentimento informado por escrito para participar nesse estudo.
Direito à privacidade e consentimento escrito. Os autores declaram que não aparecem dados de pacientes neste artigo.
Conflito de interesses
Os autores declaram não haver conflito de interesses.
*Autor para correspondência
Correio eletrónico: claudiamarcal@gmail.com (C. Cardoso).
Recebido a 28 de agosto de 2012; aceite a 17 de janeiro de 2013













