Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Revista Portuguesa de Pneumologia
versão impressa ISSN 0873-2159
Rev Port Pneumol v.16 n.1 Lisboa jan. 2010
Síndroma da veia cava superior como apresentação de neoplasia
Nuno Filipe Pires1, António Morais2, Henrique Queiroga3
1 Interno Complementar de Pneumologia/Resident, Pulmonology
2 Assistente Hospitalar de Pneumologia/Consultant, Pulmonology
3 Chefe de Serviço de Pneumologia/Head of Pulmonology
Hospital de S. João, Porto
Resumo
A síndroma da veia cava superior (SVCS) é causada por uma obstrução/compressão gradual e insidiosa da veia cava superior, caracterizando -se por fácies pletórica, edema e ingurgitamento vascular do pescoço e parte superior do tronco. É geralmente tradutora de neoplasia, sendo o cancro do pulmão a sua causa mais comum.
Objectivo: Estudo retrospectivo dos internamentos no Hospital de S. João entre Janeiro de 1995 e Dezembro de 2006 por SVCS de etiologia a esclarecer com a caracterização clínica dos doentes e a avaliação de factores de prognóstico.
Material e métodos: Foram seleccionados 60 doentes que à data de admissão não tinham causa para SVCS. Foram avaliados, entre outros, idade, sexo, exposição e carga tabágica, etiologia do SVCS, tratamento e sobrevivência global.
Resultados: Dos doentes estudados, 87% apresentavam cancro do pulmão, sendo o tipo histológico mais comum o carcinoma pulmonar de pequenas células (CPPC), com 41% dos casos. Em 10% dos doentes foi diagnosticado linfoma não Hodgkin. Em relação aos factores de prognóstico estudados, verificou-se que a ausência de metastização, o diagnóstico histológico de linfoma, o bom estado geral e a ausência de consumo tabágico se correlacionam positivamente de forma significativa com a sobrevivência. Contrariamente, o diagnóstico de CPPC apresentou igualmente de forma significativa uma menor sobrevivência.
Conclusão: Nesta série de doentes com SVCS como apresentação da doença observou -se uma sobrevivência significativamente menor nos casos de CPPC, doentes fumadores (especialmente com ≥ 40 UMA), naqueles com mau estado geral, bem como nos que apresentavam uma maior progressão da doença, com presença de metastização.
Palavras-chave: Síndroma da veia cava superior, tipo histológico, sobrevivência global.
Superior vena cava syndrome as tumour presentation
Abstract
Superior vena cava syndrome (SVCS) is characterised by gradual and insidious compression/obstruction of the superior vena cava (SVC). Upper chest and neck ingurgitation, plethoric face and oedema are the common symptoms/signs. It generally means the presence of neoplasm, namely lung cancer.
Aim: Retrospective analysis of the patients admitted to S. João Hospital, Porto, Portugal, January 1995-December 2006 with SVCS without previous diagnosis. Patients, tumour characteristics and prognostic factors were studied.
Material and methods: Data was collected by consulting the clinical files of 60 SVCS patients without previous diagnosis. Data was gathered on the patients’ demographic characteristics (age, gender, smoking habits), performance status, histology, staging, treatment and overall survival.
Results: Lung cancer was observed in 87% of the patients. Small-cell lung cancer (SCLC) was the most frequent histological type; 41% of the patients. It is noticeable that 10% were diagnosed with non- Hodgkin’s lymphoma. In terms of prognostic factors analysed, the absence of metastasis, the lymphoma’s histological diagnosis, good performance status and non-smoker status were positively correlated with the survival rate. On the contrary SCLC was significantly correlated with a worse survival.
Conclusions: In our analysis we concluded that SCLC, smokers and a poorer performance status as well as metastatic disease were unfavourable prognostic factors to SVCS as tumour presentation.
Key-words: Superior vena cava syndrome, histology, overall survival.
Introdução
A síndroma da veia cava superior (SVCS) resulta da obstrução do fluxo sanguíneo ao longo da veia cava superior (VCS). Tal obstrução pode ser causada por invasão ou compressão extrínseca da VCS por processos patológicos contíguos que envolvem o pulmão direito, gânglios linfáticos e outras estruturas mediastínicas, ou por trombose intraluminal. Ocasionalmente ambos os fenómenos, compressão extrínseca e trombose, coexistem1-2.
Na era pré-antibiótica, as causas mais frequentes de SVCS eram aneurismas sifilíticos da artéria aorta torácica, mediastinite fibrosante e outras complicações devido a infecções não tratadas2,3. Actualmente, a patologia infecciosa tem um papel reduzido na etiologia da doença e as neoplasias são a causa mais comum, sendo responsáveis por 60 a 95% do total de casos4-6. O quadro sintomático clássico é composto por fácies pletórica, edema e ingurgitamento vascular do pescoço e parte superior do tronco, com dificuldade de retorno venoso dos membros superiores em elevação de 90 graus. Estes sintomas são frequentemente acompanhados por sintomas respiratórios, como dispneia ou tosse e, mais raramente, por sintomas neurológicos, como cefaleias, vertigens, alterações da visão e acufenos, que atestam a perturbação da irrigação do sistema nervoso central3,5. Este quadro clínico instala-se em semanas ou meses devido ao rápido crescimento tumoral, o que impede a formação adequada de fluxo colateral venoso1.
O cancro do pulmão é o diagnóstico mais comum no SVCS associado a neoplasia, seguido do linfoma não Hodgkin, sendo estas duas entidades responsáveis por 95-99% dos casos neste contexto5,7. Calcula-se que 2 a 4% dos doentes com neoplasia do pulmão irão apresentar SVCS ao longo da evolução da doença. Em relação ao SVCS como manifestação inicial de neoplasia, estudos revelam uma maior incidência em doentes com carcinoma pulmonar de pequenas células (CPPC), nos quais 10% tem esta forma de apresentação, presumivelmente devido ao rápido crescimento tumoral nas vias aéras centrais. No carcinoma pulmonar de não pequenas células (CPNPC), a incidência de SVCS como apresentação de neoplasia é inferior a 2%8-13, havendo no entanto alguns autores que apontam para valores mais elevados14.
Este estudo pretende analisar a população de doentes internados no Hospital de S. João por SVCS ainda sem diagnóstico etiológico, de modo a caracterizá-los clinicamente, para além da análise da terapêutica instituída e da sobrevivência. Pretendeu-se igualmente avaliar os factores de prognóstico associados aos doentes com SVCS como apresentação da doença.
Material e métodos
Foi feita uma análise retrospectiva dos doentes internados no Hospital de S. João entre Janeiro de 1995 e Dezembro de 2006 por SVCS de etiologia a esclarecer. Foram seleccionados através do departamento de estatística do hospital 167 doentes com diagnóstico de SVCS. Destes, encontravam-se disponíveis para consulta 134 processos clínicos, tendo sido seleccionados 60 doentes que à data de admissão não tinham etiologia estabelecida para o SVCS. Em quatro doentes não foi possível ter acesso ao seguimento posterior ao diagnóstico. Foram avaliados, entre outros, a idade, o sexo, a exposição e carga tabágica, a etiologia do SVCS, o tratamento e a sobrevivência global.
Todos os dados obtidos por consulta dos processos clínicos dos doentes foram organizados numa base de dados informatizada, tendo a análise estatística sido realizada pelo programa SPSS (Statistical Package for Social Sciences) versão 15.0.
Os 60 doentes seleccionados obtiveram em regime de internamento hospitalar o diagnóstico histológico de neoplasia, tendo feito estudo analítico e imagiológico direccionado, de modo a caracterizar a doença e a fazer o estadiamento associado. Foram de seguida sujeitos a regime terapêutico adequado ao tipo histológico do tumor e ao estado geral apresentado, tendo sido seguidos de modo regular em regime de ambulatório.
Resultados
Os doentes incluídos apresentavam uma idade mediana de 56,5 anos e 83,3% pertenciam ao sexo masculino. Quanto aos hábitos tabágicos, 42 (70%) eram fumadores, 5 (8,3%) ex-fumadores e 13 (21,7%) não fumadores – Quadro 1. Os fumadores tinham uma carga tabágica elevada, com 75% a apresentarem uma carga ≥ 40 UMA.
Quadro I – Características dos doentes (n=60)

Os sintomas/sinais mais descritos no processo clínico aquando do diagnóstico foram os seguintes: dispneia (95,5%), edema do pescoço (86,4%), edema da face (72,7%), ingurgitamento venoso (63,8%) e sintomas constitucionais (52,3%) – Fig. 1. Outros sintomas e sinais, como tosse, disfagia, ortopneia, disfonia/estridor, face pletórica, hemoptises, dor torácica, cefaleias, vertigens e sonolência foram menos frequentes (entre 5-40% dos casos).
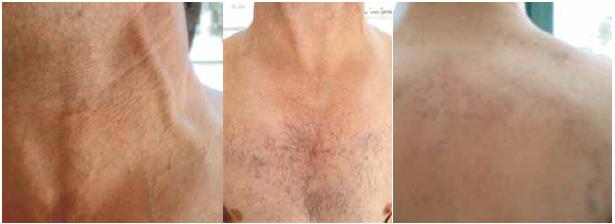
Fig. 1 – Edema e ingurgitamento vascular do pescoço associado a circulação colateral superficial torácica (face anterior e posterior) em doente com SVCS
A maioria dos doentes apresentou sintomas e sinais clínicos referentes ao SVCS com menos de duas semanas de evolução (68,2%), enquanto 27,3% apresentava evolução da sintomatologia entre duas semanas e dois meses e os restantes 4,5% tinham sintomas/sinais há mais de dois meses.
O principal tipo histológico diagnosticado foi o carcinoma pulmonar de pequenas células (CPPC), com 41,7% dos casos (25 doen tes), seguido de carcinoma epidermóide com 28,3% (17 doentes) e adenocarcinoma em 16,7% dos casos (10 doentes). O linfoma não Hodgkin foi observado em 10% dos doentes observados (6 casos), tendo os restantes 2 doentes (3,3%) teratomas do mediastino posterior – Fig. 2. Vinte e três doentes (38,3%) estavam no estádio IV na altura do diagnóstico. Os locais de metastização eram: cérebro (9 doentes), ossos (6), fígado, rim e suprarrenal (2 doentes cada). Dois doentes apresentavam vários órgãos metastizados.
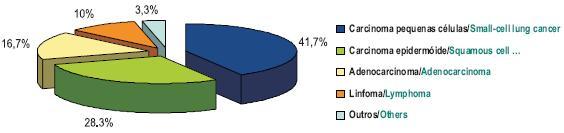
Fig. 2 – Diagnóstico histológico dos doentes com SVCS
O tratamento passou maioritariamente por QT, associada ou não a RT, sendo a associação nongencitabina/carboplatino o esquema mais usado no caso do carcinoma pulmonar de não pequenas células; no CPPC, a associação etoposido/carboplatino teve uma taxa de utilização elevada. Dos doentes que realizaram QT+RT, 52,4% fizeram -no de forma concomitante e 47,6% de forma sequencial – Fig. 3.
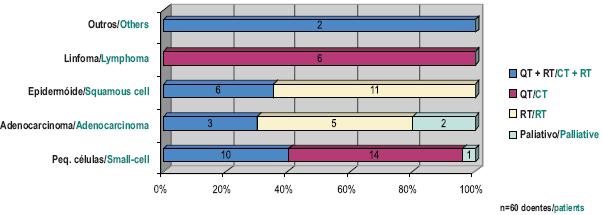
Fig. 3 – Tratamento efectuado aos doentes (por tipo histológico)
A sobrevivência global mediana foi de 8 meses. Considerando apenas os casos com o diagnóstico de cancro do pulmão, obteve–se uma sobrevivência global mediana no carcinoma de não pequenas células de 7 meses [0,5 – 17 meses] e no CPPC uma sobrevivência global mediana de 5 meses [0,4 – 16 meses]. Relativamente aos casos de linfoma não Hodgkin, a sobrevivência global mediana foi de 70 meses [4 -120 meses]. Nos dois casos de teratomas do mediastino posterior, a sobrevivência global mediana foi de 20 meses – Quadro II e Fig. 4.
Quadro II – Sobrevivência global mediana por tipo histológico

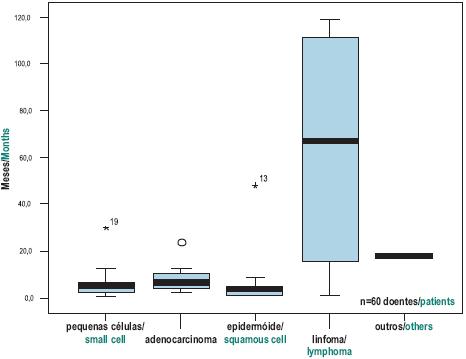
Fig. 4 – Sobrevivência global mediana por histologia
Em relação aos factores de prognóstico estudados, verificou-se que um bom estado geral (performance status 0/1), o diagnóstico histológico de linfoma e a ausência de metastização se correlacionam positivamente com a sobrevivência global, havendo diferenças estatisticamente significativas (p=0,033, p=0,041 e p=0,027, respectivamente).
Também os doentes não fumadores apresentam uma maior sobrevivência global em relação aos doentes fumadores (p=0,038) – Figs. 5-8. De referir que estes factores de prognóstico foram calculados ao fim de 6 meses, pois a partir daí o número de doentes vivos não permite obtenção de valores estatísticos significativos para a análise das variáveis, que são independentes para o prognóstico. Fazendo uma análise de regressão linear para estudo da potência das variáveis, observa-se que estas apresentam de facto potência estatística para a amostra de doentes em estudo.
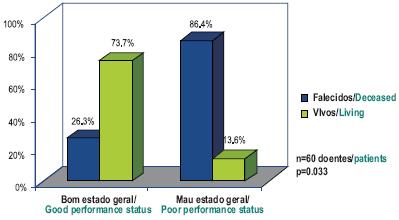
Fig. 5 – Avaliação da sobrevivência global mediana aos 6 meses em função do estado geral (performance status)
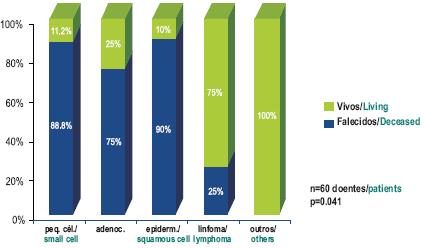
Fig. 6 – Avaliação da sobrevivência global mediana aos 6 meses em função do tipo histológico
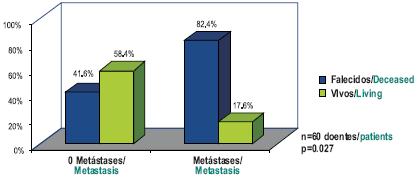
Fig. 7 – Avaliação da sobrevivência global mediana aos 6 meses em função da presença de metástases
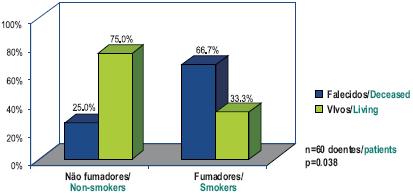
Fig. 8 – Avaliação da sobrevivência global mediana aos 6 meses em função dos hábitos tabágicos
Após quimioterapia de 1.ª linha, 12% dos doentes apresentaram resposta parcial e 68% estabilização do quadro.
Quinze doentes faleceram no internamento (25%), sendo que todos eram fumadores (carga tabágica ≥ 40 UMA) e com mau estado geral (performance status ≥ 2). Doze destes doen tes encontravam-se igualmente em estádio IV. Mais de 90% dos que tiveram alta apresentaram regressão do SVCS que, posteriormente, recidivou em 17% dos casos.
Discussão e considerações finais
A síndroma da veia cava superior (SVCS) resulta de um conjunto de sintomas e sinais causados pela obstrução do fluxo sanguíneo ao longo da veia cava superior (VCS). Os sintomas que rapidamente orientam para esta síndroma incluem o edema da face, pescoço, tórax e membros superiores, associados frequentemente a dispneia e tosse. Menos frequente é o aparecimento de disfonia, dor torácica, disfagia e hemoptises. Ao exame objectivo observa-se frequentemente distensão das veias do pescoço, edema da face e membros superiores, face pletórica e taquipneia. Cianose, síndroma de Horner e paresia das cordas vocais, embora raros, podem igualmente estar presentes3.
Desde que o SVCS foi descrito pela primeira vez, em 1757, por William Hunter, o espectro de condições associadas passou de entidades de etiologia infecciosa, como a tuberculose e aneurismas da aorta ascendente sifilíticos, para patologias malignas3. Actualmente, o SVCS traduz neoplasia em cerca de 95% dos casos descritos, sendo o carcinoma pulmonar de pequenas células (CPPC) a causa mais comum, seguido do carcinoma epidermóide e do adenocarcinoma do pulmão, do linfoma não Hodgkin e do carcinoma de grandes células do pulmão1,3,14.
A causa não maligna de SVCS mais frequente é a trombose associada a cateteres intracava ou a fios de pacemaker 15.
Causas raras adicionais incluem metástases de neoplasias das células germinativas, sarcoma de Kaposi, neoplasia da mama, cólon ou esófago, timoma, linfoma de Hodgkin e sarcoidose16. A gravidade da síndroma depende da rapidez de início da obstrução e da sua localização. Quanto mais rápido se instalar maior será a gravidade dos sintomas devido à ausência de tempo para as veias colaterais se acomodarem ao aumento do fluxo sanguíneo4-6.
O presente estudo mostrou resultados sobreponíveis às várias séries publicadas no que diz respeito à etiologia do SVCS e ao estádio dos doentes na altura do diagnóstico. No entanto, o número de doentes com diagnóstico de adenocarcinoma foi mais elevado do que o habitual, uma vez que este tipo de neoplasia é geralmente periférico e não condiciona obstrução de grandes vasos. Efectivamente, na série descrita, 16,7% dos doentes que apresentaram SVCS como manifestação inaugural tinham adenocarcinoma, número manifestamente elevado, tendo em conta que em algumas séries a percentagem neste tipo de patologia não ultrapassa os 2-4%11-13. Na presença de um doente com SVCS de etiologia desconhecida, a prioridade deverá ser o de estabelecer o diagnóstico da doença subjacente antes da ponderação de qualquer terapêutica, uma vez que 75% dos doentes têm sintomas com mais de uma semana de evolução antes de recorrer a cuidados médicos, 3% a 5% dos doentes diagnosticados com SVCS não apresentam neoplasia e a causa de morte relaciona-se geralmente com a evolução da doença e não com complicações decorrentes do SVCS3. Na ausência de obstrução traqueal, edema laríngeo grave ou sintomas neurológicos tradutores de edema cerebral, o SVCS não deve ser considerado como emergência oncológica e, portanto, o tratamento prévio ao diagnóstico não é indicado.
No passado, o SVCS era considerado uma emergência médica potencialmente fatal, sendo os doentes submetidos com urgência a radioterapia (RT), de modo a aliviar a obstrução.
Para além dos dados referidos, que aconselham a tomada de medidas terapêuticas apenas após o diagnóstico estabelecido, deverá igualmente ser considerado que, no caso de se ponderar a realização de RT como terapêutica inicial e prévia ao diagnóstico esta pode dificultar a análise histológica posterior.
Num estudo de Loeffler et al com 19 doentes com SVCS no contexto de massas mediastínicas e que receberam RT de emergência, o diagnóstico histológico por biopsia só foi estabelecido em 11 (58%)17.
Quanto ao tratamento, no caso dos tumores quimiossensíveis como o CPPC e o linfoma não Hodgkin, este passa predominantemente por QT, geralmente sem RT. Na sua maioria, estes doentes obtêm uma remissão a médio/longo prazo, com melhoria sintomática a surgir ao fim de uma a duas semanas de tratamento9-13,18-20. Nestes tumores, a RT isolada leva a resultados pouco expressivos e pode comprometer o sucesso posterior da QT11-13,20. Numa revisão efectuada em 2002 por Rowell et al em doentes com SVCS inaugural, o tratamento com QT aliviou os sintomas em 77% dos doentes com CPPC, sendo que apenas 17% acabaram por apresentar recidiva8. Em algumas situações, a adição de RT em combinação com QT sistémica pode diminuir as taxas de recidiva local, especialmente em casos de CPPC limitado. Estes resultados, no que respeita ao tratamento, são similares, tendo os doentes com linfoma não Hodgkin sido sujeitos a QT sistémica, com boa resposta, ao passo que nos doentes com CPPC a QT foi efectuada isoladamente em 14 doentes ou associada a RT em 10, apresentando estes últimos lesões de maior dimensão, embora passíveis de irradiação ou doença limitada, com melhor taxa de resposta com terapêutica associada.
Quanto ao carcinoma pulmonar de não pequenas células (CPNPC), a abordagem terapêutica é diferente dos tumores quimiosensíveis referidos, devendo ter a orientação geral aconselhada para cada estádio, nomeadamente a associação de QT e RT nos estádios IIIB e QT no estádio IV. No entanto, a radioterapia é usada mesmo neste último estádio em casos de obstrução grave, com o objectivo de redução mais rápida da compressão e em casos em que o doente não apresente condições para a administração de quimioterapia. Na amostra de doentes relativa a este estudo observa-se que nos doentes com adenocarcinoma apenas três foram sujeitos a terapêutica combinada QT+RT, enquanto a maioria (5) foi sujeita a tratamento com RT isolada para paliação dos sintomas e sinais associados ao SVCS, tendo dois efectuado apenas tratamento de suporte médico.
Os doentes com carcinoma epidermóide tiveram uma abordagem terapêutica similar; seis foram submetidos a QT e RT e 11 apenas a RT isolada pelos mesmos motivos. Estes dados são igualmente sobreponíveis à literatura disponíve13.
Na presença de sintomas tradutores de risco de vida, como os decorrentes de edema cerebral ou obstrução grave da via aérea, deverá ser ponderada a introdução de prótese intravascular, procedimento com baixo risco de complicações e associado a um rápido alívio sintomático3,21. Esta intervenção poderá igualmente ser efectuada em casos de menor gravidade, na presença de tumores com terapêutica de eficácia limitada ou nos casos em que os sintomas se mantêm após a terapêutica preconizada ter sido efectuada3,21.
Embora na quase totalidade dos doentes estudados tenham sido prescritos corticóides e diuréticos, o papel destes fármacos permanece incerto, não havendo evidência clínica do seu benefício3,21 .
Um dado importante a realçar é o de que, apesar de uma boa caracterização dos doentes com neoplasia pulmonar em vários estudos publicados, estes referem-se habitualmente a doentes com SVCS no decurso da doença, sendo escassas as referências na fase de apresentação da doença. Neste estudo, a presença de SVCS não se revelou um factor de mau prognóstico em si mesmo, tendo em conta a sobrevivência global (OS) observada ser em cada um dos tipos histológicos sobreponível à descrita nos casos em que não se encontra SVCS, o que vem de encontro ao que é descrito maioritariamente na literatura9,11,12.
Existem no entanto descrições em sentido contrário, como no estudo de Martins e Pereira, o qual refere o SVCS como factor de mau prognóstico, com OS de 5 meses22.
A avaliação dos factores de prognóstico nesta série de doentes revelou que aqueles com CPPC apresentam de forma significativa uma sobrevivência global menor. Verificou-se o mesmo resultado nos doentes fumadores, nomeadamente naqueles com uma carga tabágica elevada (≥ 40 UMA), o que poderá estar relacionado com a menor resposta à terapêutica descrita nos indivíduos que mantêm o consumo tabágico, para além de um possível aumento das comorbilidades associadas a esta adição, não sendo possível no entanto fundamentar esta informação, dado o registo e análise das comorbilidades não ter sido objecto de estudo. A menor sobrevivência global associada ao estádio IV deverá ser consequência de um estádio mais avançado associado à presença de metástases.
Bibliografia
1. Gomes MJM, Sotto-Mayor R. Tratado de Pneumologia, vol. II. Permanyer Portugal 2003; 1138-1139.
2. Schechter MM. The superior vena cava syndrome. Am J Med Sci 1954; 227:46.
3. Wilson LD, Detterbeck FC, Yahalom J. Clinical practice. Superior vena cava syndrome with malignant causes. N Engl J Med 2007; 356:1862.
4. Yellin A, et al. Superior vena cava syndrome. The myth – the facts. Am Rev Respir Dis 1990; 141:1114.
5. Parish JM, et al. Etiologic considerations in superior vena cava syndrome. Mayo Clinic Proc 1981; 56:407.
6. Rice TW, Rodriguez RM, Light RW. The superior vena cava syndrome: clinical characteristics and evolving etiology. Medicine (Baltimore) 2006; 85:37.
7. Markman M, Diagnosis and management of superior vena cava syndrome. Cleve Clin J Med 1999; 66:59.
8. Rowell NP, Gleeson FV. Steroids, radiotherapy, chemotherapy and stents for superior vena caval obstruction in carcinoma of the bronchus: a systematic review. Clin Oncol (R Coll Radiol) 2002; 14:338.
9. Dombernowsky P, Hansen HH. Combination chemotherapy in the management of superior vena caval obstruction in small-cell anaplastic carcinoma of the lung. Acta Med Scand 1978; 204:513.
10. Spiro SG, et al. Treatment of obstruction of the superior vena cava by combination chemotherapy with and without irradiation in small-cell carcinoma of the bronchus. Thorax 1983; 38:501.
11. Sculier JP, et al. Superior vena caval obstruction syndrome in small cell lung cancer. Cancer 1986; 57:847.
12. Urban T, et al. superior vena cava syndrome in smallcell lung cancer. Arch Intern Med 1993; 153:384. 13. Wurschmidt F, et al. Smalll cell lung cancer with and without superior vena cava syndrome: a multivariate analysis of prognostic factors in 408 cases. Int J Radiat Oncol Biol Phys 1995; 33:77.
13. Wurschmidt F, et al. Smalll cell lung cancer with and without superior vena cava syndrome: a multivariate analysis of prognostic factors in 408 cases. Int J Radiat Oncol Biol Phys 1995; 33:77.
14. Schraufnagel DE, et al. Superior vena caval obstruction. Is it a medical emergency? Am J Med 1981; 70:1169.
15. Gray BH, et al. Safety and efficacy of thrombolytic therapy for superior vena cava syndrome. Chest 99(1): 54-59, 1991.
16. Yahalom J. Oncologic emergencies: superior vena cava syndrome. In: DeVita VT, Hellman S, Rosenberg SA, eds.: Cancer: Principles and Practice of Oncology. Philadelphia: JB Lippincott Company, 4th Edition, 1993; 2111-2118.
17. Loeffler JS, et al. Emergency prebiopsy radiation for mediastinal masses: impact on subsequent pathologic diagnosis and outcome. J Clin Oncol 1986; 4:716.
18. Rodrigues CI, Njo KH, Karim AB. Hypofractionated radiation therapy in the treatment of superior vena cava syndrome. Lung Cancer 10(3,4): 221 -228, 1993.
19. Tanigawa N, Sawada S, Mishima K, et al. Clinical outcome of stenting in superior vena cava syndrome associated with malignant tumors. Comparison with conventional treatment. Acta Radiologica 1998; 39(6):669 -674. [ Links ]
20. Perez -Soler R, et al. Clinical features and results of management of superior vena cava syndrome secondary to lymphoma. J Clin Oncol 1984; 2:260.
21. Yu JB, Wilson LD, Detterbeck FC. Superior vena cava syndrome – a proposed classification system and algorithm for management. J Thorac Oncol 2008; 3 (8):811 -814.
22. Martins SJ, Pereira JR. Clinical factors and prognosis in non-small cell lung cancer. Am J Clin Oncol 1999; 22:453.
Correspondência/Correspondence to:
Serviço de Pneumologia
Hospital S. João
Alameda Prof. Hernâni Monteiro,
4202-451 Porto
Telefone: 225512215
e-mail: nunofxpires@gmail.com
Recebido para publicação/received for publication: 08.12.17
Aceite para publicação/accepted for publication: 09.06.08













