Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Acta Obstétrica e Ginecológica Portuguesa
versão impressa ISSN 1646-5830
Acta Obstet Ginecol Port vol.14 no.3 Coimbra set. 2020
ARTIGO DE REVISÃO/ REVIEW ARTICLE
Preservação da fertilidade no doente oncológico pediátrico
Fertility preservation in pediatric oncological patient
Maria do Pilar Ferreira1, Ana Margarida Póvoa2
Faculdade de Medicina da Universidade do Porto
1 Interna de Formação Geral, Fculdade de Medicina da Universidade do Porto
2 Assistente Hospitalar Graduada de Ginecologia e Obstetrícia na Unidade da Medicina da Reprodução do Serviço de Ginecologia do Centro Hospitalar Universitário de São João, Porto, Portugal; Professora Auxiliar convidada da Faculdade de Medicina da Universidade do Porto
Endereço para correspondência | Dirección para correspondencia | Correspondence
ABSTRACT
The incidence of pediatric cancer has been increasing, but the improvement in survival rates contributed to the growing number of survivors of reproductive age.
Oncological treatments can affect fertility therefore, all patients diagnosed with cancer should be informed about the risks of infertility and advised by a multidisciplinary team on the multiple fertility preservation techniques: before puberty or urgency in starting oncological treatment ovarian or testicular tissue cryopreservation are the ones available, although experimental; after puberty, oocyte and sperm cryopreservation are the techniques recommended.
The authors present a review of the literature on this subject.
Keywords: Fertility; Preservation; Pediatric; Cancer.
Introdução
A incidência de doenças oncológicas pediátricas tem vindo a aumentar nas últimas décadas1,2. Devido aos avanços nos tratamentos, as taxas de sobrevida a 5 anos atualmente são superiores a 80% para vários tipos de tumores, em particular para pacientes com cancro na infância ou na adolescência2-4, contribuindo para o aumento de sobreviventes de doenças oncológicas em idade reprodutiva.
Os tratamentos oncológicos têm efeitos secundários a médio/longo prazo podendo afetar a fertilidade e outras áreas da saúde reprodutiva como o desenvolvimento pubertário, produção hormonal e função sexual3,5.
Surge assim a necessidade de explicar os riscos associados aos tratamentos que variam de acordo com o tipo de cancro, o tratamento implementado e a idade do paciente3, e promover métodos de preservação da fertilidade, sendo este um dos aspetos relacionados com a qualidade de vida na sobrevivência.
Atualmente, no adulto, várias técnicas de preservação da fertilidade estão já implementadas.
Esta revisão bibliográfica tem como objetivo descrever as técnicas de preservação da fertilidade disponíveis em idade pediátrica, tendo em conta a idade e o estádio de maturidade sexual, o tipo de carcinoma e a terapêutica oncológica utilizada, contribuindo para a discussão das opções de preservação da fertilidade na orientação oncológica pediátrica, de modo a não colocar em causa a fertilidade futura destes doentes5,6.
Métodos
Foi realizada uma revisão da literatura na PUBMED/ /MEDLINE , utilizando como palavras-chave: «fertility preservation », «pediatric», «cancer», «oncofertility», e complementada com publicações citadas nos artigos pesquisados.
Risco das terapêuticas oncológicas na fertilidade
As terapêuticas oncológicas, de acordo com a literatura, podem ter um potencial efeito adverso como a esterilidade, infertilidade ou subfertilidade , que varia de acordo com a dose usada, a duração do tratamento e as características dos pacientes, sendo a idade um dos mais relevantes7,8.
O impacto das terapêuticas oncológicas na fertilidade pode ocorrer pelos seguintes mecanismos: gonadotoxicidade direta, quando ocorre lesão direta do ovário ou do epitélio seminífero no testículo; neste mecanismo intervêm os agentes antineoplásicos alquilantes ou a radioterapia pélvica; gonadotoxicidade indireta, quando ocorrem alterações no funcionamento do eixo hipotálamo-hipófise-gónadas, por exemplo após radioterapia craniana; alterações ao nível da função uterina ou das funções erétil ou ejaculatória que podem ser causadas por irradiação pélvica ou por intervenções cirúrgicas sobre o aparelho reprodutor.
No caso do sexo feminino, existe uma estratificação do risco da falência ovárica prematura (FOP) que varia entre o baixo risco (20%) e o risco elevado (80%), tendo em conta a dose terapêutica e a idade (Tabela I )9, 10. No sexo masculino, é mais complicada a estratificação específica de risco, embora apresente associações semelhantes às referidas no sexo feminino e o elevado risco de infertilidade10.
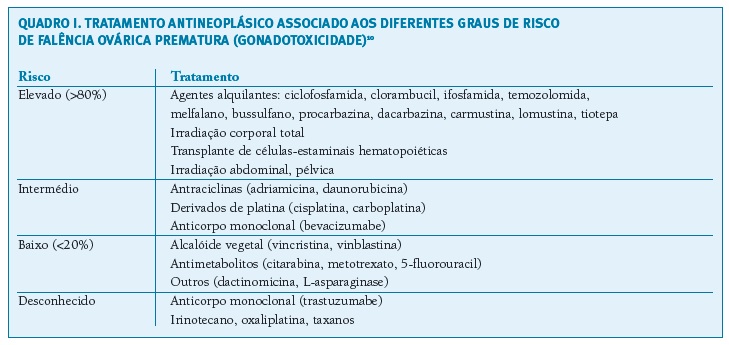
(clique para ampliar ! click to enlarge)
Quimioterapia
Na quimioterapia existem agentes com diferentes riscos de gonadotoxicidade e diferentes probabilidades de FOP11. De uma forma generalizada, todos se relacionam com uma diminuição da fertilidade9.
Os agentes com maior risco de gonadotoxicidade são os da classe alquilante (causam alterações nas cadeias de DNA, impedindo a replicação celular) e os seus principais efeitos secundários são a fibrose ovárica e a depleção folicular e ovocitária prematura, aceleradas pela apoptose dos ovócitos e das células da granulosa12-15. Alguns dos agentes alquilantes têm reconhecida gonadotoxicidade isolada ou em combinação9,16,17.
Existem fatores que podem ter um diferente impacto na fertilidade, tais como a dose terapêutica, a duração da exposição, a idade da doente e a reserva folicular no início da terapêutica, no sexo feminino13,18. A idade mais jovem associada a uma maior reserva ovárica confere maior resistência à gonadotoxicidade, e maior tolerância a doses mais elevadas de quimioterapia7,11,14. Não se efetua uma comparação no sexo masculino por não haver uma reserva, mas uma produção contínua de espermatozoides.
Radioterapia
A radioterapia associa-se a diferentes riscos consoante a dose, o campo de irradiação e o esquema de fracionamento utilizados durante o tratamento19,20.
No sexo feminino, a irradiação abdominal e pélvica aumenta risco de FOP13,14. O ovócito humano é muito sensível à radiação e estima-se que doses inferiores a 2 Gy sejam suficientes para destruir 50% dos folículos primordiais11,15,21. Existe uma maior tolerância nos indivíduos mais jovens, por terem uma maior reserva folicular13,14.
Os efeitos diretos no útero após a irradiação incluem alterações irreversíveis no miométrio (fibrose, atrofia e diminuição do volume e elasticidade), nos vasos sanguíneos (diminuição da vascularização uterina) e no endométrio (atrofia)12,13,19, sendo mais pronunciadas se a exposição for realizada antes da puberdade13. As complicações obstétricas em pacientes que são submetidas a radioterapia, em comparação com a população em geral, incluem abortamentos espontâneos (38% vs. 12%), parto pré-termo (62% vs. 9%) e recém-nascidos com baixo peso ao nascimento (62 % vs. 6%), respetivamente12,21. Após radioterapia é aconselhado adiar a gravidez, pelo menos por um ano12.
Gosden et al22 demonstraram que a depleção de folículos primordiais , em ovários de ratas, estava relacionada com a dose: doses crescentes causam esterilização e doses mais baixas depleção parcial da reserva ovárica, levando a FOP12,22. Existe um maior grau de toxicidade associado à radioterapia realizada numa sessão única em vez de fracionada12,13.
A radioterapia craniana que atinja o hipotálamo ou a hipófise , efetuada antes da puberdade, pode ter como consequência a puberdade precoce, alterações no ciclo hormonal, influenciando a fertilidade futura12,13,21. As crianças que receberam doses elevadas (>30Gy) de irradiação craniana têm um risco acrescido de desenvolver hipogonadismo hipogonadotrófico, com amenorreia hipotalâmica e ausência de desenvolvimento pubertário12,13.
Os pacientes do sexo masculino que receberam doses de radiação testicular superiores a 7,5 Gy foram identificados como tendo menor probabilidade de gerar uma gravidez23. Os testículos na pré-puberdade são menos sensíveis à gonadotoxicidade da radioterapia do que na idade adulta24.
Durante a realização de radioterapia, que não seja direcionada às gónadas, a proteção das mesmas com material blindado reduz a exposição dos órgãos reprodutores à radiação, devendo ser preconizada.
Cirurgia
As cirurgias do aparelho reprodutor feminino como a histerectomia e a ooforectomia bilateral ou do aparelho reprodutor masculino como a orquidectomia bilateral originam esterilidade. A cirurgia oncológica deverá ser o mais conservadora e o menos radical possível, de modo a tentar preservar os órgãos reprodutores.
Técnicas de preservação da fertilidade em crianças e adolescentes
Dada a imaturidade sexual , especialmente em crianças pré-púberes, as técnicas de preservação da fertilidade possíveis são mais limitadas. As mais utilizadas são a criopreservação do tecido ovárico (CTO) ou testicular (CTT) em crianças sexualmente imaturas sendo que, em adolescentes pós-púberes, a estimulação ovárica com a criopreservação de ovócitos ou a criopreservação de esperma são preferíveis13.
Apresentamos cada uma das técnicas usadas, tendo em conta o sexo e a idade pubertária da criança, promovendo uma orientação para cada tipo de técnica.
No sexo feminino
Criopreservação de Ovócitos
A criopreservação de ovócitos é considerada em adolescentes, na idade pós-púbere11,25. Compreende uma fase inicial de estimulação hormonal (10-14 dias), para recrutamento folicular, acompanhada de monitorização ecográfica e analítica (níveis de estradiol)13. O uso de estimulação ovárica não deixa de ser um fator de preocupação nas mulheres com tumores hormono-dependentes, como, por exemplo, o cancro de mama, por acarretar um aumento suprafisiológico dos níveis circulantes de estrogénios. No entanto, a prática atual apoia a estimulação ovárica com gonadotrofinas em simultâneo com a administração de inibidores da aromatase (letrozol) em pacientes com tumores sensíveis ao estrogénio, com o intuito de reduzir os níveis plasmáticos destes5,26. Após a estimulação segue-se a punção folicular ecoguiada por via transvaginal e a criopreservação dos ovócitos12,13. A recuperação é rápida e podem iniciar-se, no mesmo dia, os tratamentos antineoplásicos13.
Em estudos mais antigos, a criopreservação de ovócitos ainda era considerada um procedimento experimental. Atualmente as taxas de fecundação e gravidez após reprodução medicamente assistida com ovócitos frescos ou resultantes de desvitrificação parecem ser semelhantes. O número de nados vivos resultantes de ovócitos criopreservados por vitrificação (congelação rápida) tem aumentado e aparentemente não há diferenças nos resultados perinatais ou na taxa de anomalias congénitas entre crianças nascidas de ovócitos criopreservados em comparação com aquelas nascidas de ciclos de fertilização in vitro a fresco ou até de gravidez espontânea5,27. Os resultados da criopreservação de ovócitos nas pacientes oncológicas parecem ser inferiores aos dos outras pacientes e a doença oncológica poderá ser a causa28.
Atualmente, a criopreservação de ovócitos é uma técnica de preservação da fertilidade com eficácia bem estabelecida21,29.
Criopreservação de tecido ovárico (CTO)
A CTO é, provavelmente, a única opção para preservação da fertilidade em crianças pré-púberes11,30 e nos casos de crianças pós-púberes em que não há tempo para se efetuar a estimulação ovárica necessária para a realização da criopreservação de ovócitos, antes do início da terapêutica oncológica11,13,25,31-33.
A ideia da técnica surgiu após a descoberta da maior resistência às lesões criogénicas dos folículos primordiais, presentes no córtex ovárico, em relação aos ovócitos maduros12,30.
No caso da CTO, deixa de ser necessária a pré-estimulação ovárica para colheita posterior dos ovócitos, uma vez que é colhido diretamente o tecido ovárico por biópsias múltiplas, ou o ovário na sua totalidade, não sendo consensual a opção ideal. A recolha do tecido pode ser realizada por via laparoscópica ou por laparotomia se concomitante com outra intervenção cirúrgica, sem necessidade de qualquer preparação prévia13,31,32.
Após a conclusão do tratamento antineoplásico, o tecido pode ser descongelado e transplantado para a paciente5,32. A viabilidade folicular após criopreservação e descongelamento foi demonstrada em vários estudos12. O pool sobrevivente de folículos primordiais será reativado e os enxertos ováricos poderão restabelecer o ciclo menstrual necessário para a conceção, gestação e parto9. O sucesso do procedimento vai depender da indicação correta para CTO, da idade da paciente, da técnica de preservação e da técnica cirúrgica do transplante31.
Uma possível contraindicação para o processo é o risco de contaminação por células malignas, no autotransplante do tecido32,34, como nos casos de leucemia aguda34. Para tal existem abordagens alternativas experimentais, tais como a maturação in-vitro dos folículos primordiais, ou o desenvolvimento de um ovário artificial11,34.
O primeiro caso relatado de transplante autólogo de tecido ovárico criopreservado data de 200013,35. O primeiro nascimento após transplante de tecido ovárico criopreservado ocorreu em 200411,36,37 e em junho de 2017, o número de nados vivos era superior a 13011. A taxa estimada de gravidez após o transplante de tecido ovárico varia de 11% a 30%7.
Em 2016, foi publicado o caso da primeira gravidez de sucesso, com nado vivo do sexo masculino, resultante de fertilização in vitro (FIV) após transplante de tecido ovário criopreservado, antes da puberdade38.
Esta técnica geralmente é bem tolerada e, apesar de ser invasiva, não está associada a um risco cirúrgico elevado39. Tal não implica que não devam ser avaliados e ponderados os riscos cirúrgicos.
Esta técnica ainda é considerada experimental10,11,39.
Maturação in-vitro (IVM)
Esta técnica tem sido usada principalmente em mulheres com ovário poliquístico de modo a evitar o risco da síndrome de hiperestimulação ovárica. Implica a cultura in vitro (24-48h) de oócitos imaturos obtidos após aspiração ovárica transvaginal (in vivo) de folículos antrais (2-10mm) de pacientes sem, ou com estimulação ovárica ligeira. Segue-se a fertilização (ICSI) dos ovócitos maduros obtidos e a transferência embrionária. Embora as taxas de sucesso com recurso a ovócitos maturados in vitro sejam inferiores às da FIV após estimulação ovárica controlada, estima-se que já tenham ocorrido mais de 5000 nascimentos com recurso a IVM e sem aumento de anomalias congénitas comparativamente aos resultantes de FIV convencional40-42.
A IVM in vivo também pode ser uma estratégia alternativa de preservação da fertilidade na pós-puberdade, nos casos de impossibilidade de criopreservação de ovócitos (tratamento oncológico inadiável ou contraindicação para estimulação ovárica)43.
Estão reportados três nascimentos com recurso a esta técnica para preservação da fertilidade, por motivos oncológicos44,45.
A IVM ex-vivo, em que os ovócitos são recuperados durante o processamento do tecido ovárico antes da sua criopreservação, pode ser considerada como opção adicional aquando da preservação de tecido ovárico, embora com baixa eficácia, especialmente na pré -puberdade46-49.
Ambas as técnicas são consideradas experimentais.
Ooforopexia (Transposição ovárica)
Muitas crianças com doenças oncológicas são tratadas com irradiação abdominal e/ou pélvica total.
A ooforopexia foi descrita, pela primeira vez, em 195812. Consiste na remoção dos ovários do campo direto da radiação, através do seu reposicionamento, variando de acordo com a anatomia da paciente e do tratamento5,13,50. Pode ser efetuada simultaneamente ao tratamento cirúrgico ou, se este não fizer parte do plano terapêutico, a transposição laparoscópica é a melhor escolha e deve ser realizada antes da radioterapia13,30,31.
A transposição ovárica permite preservar a função ovárica, com taxas de sucesso que variam de 60% a 89% e dependem amplamente da idade da paciente, da dose de radiação, do local, do tipo de tratamento e do uso concomitante de quimioterapia5,13,51. Mesmo nos casos em que os ovários estão fora do campo de irradiação, as doses de dispersão podem causar insuficiência ovárica em até 50 -90% dos casos5,50.
Após a conclusão do tratamento, a doente é novamente submetida a cirurgia com reposicionamento dos ovários na sua localização original, permitindo, desse modo, o retorno da função reprodutiva5.
Uso preventivo de agonistas da hormona libertadora de gonadotrofinas (GnRH)
A possibilidade de administrar agonistas da GnRH, de modo a minimizar o dano gonadal causado pelos agentes gonadotóxicos, é atraente contudo, uma meta-análise que envolveu 28 estudos controlados e randomizados52, bem como outro mais recente randomizado53 confirmam que, apesar de haver evidência de potenciais benefícios em termos de recuperação da ovulação e dos ciclos menstruais, as taxas de gravidez não melhoraram e por isso a evidência da eficácia desta medida ainda é insuficiente33. As guidelines da ASCO de 2018 sugerem que em determinadas situações em que os restantes métodos de preservação da fertilidade não sejam viáveis, os análogos da GnRH possam ser oferecidos às pacientes na expectativa da redução do risco da falência ovárica após quimioterapia10.
No sexo masculino
Criopreservação de esperma
A criopreservação de esperma está indicada para idades pediátricas pós-púberes, quando já existem espermatozoides no esperma. É recomendada antes do início do tratamento antineoplásico, uma vez que um único tratamento de quimioterapia pode afetar adversamente a qualidade do esperma5,54. Pacientes com determinadas patologias como tumor testicular de células germinativas ou linfoma de Hodgkin, podem ser oligo ou azoospérmicos, mesmo antes do tratamento5.
A colheita da amostra de esperma é normalmente feita por masturbação5,55. Outros métodos de colheita estão disponíveis, como extração de esperma testicular, aspiração epididimária microcirúrgica de espermatozoides e estimulação vibratória peniana12,55.
Através desses métodos obtemos uma amostra cuja qualidade é avaliada, permitindo determinar a viabilidade da criopreservação54.
Posteriormente, podem ser usadas várias técnicas, tais como inseminação intrauterina, FIV ou microinjeção intracitoplasmática de espermatozoide (ICSI). Mesmo nos casos com qualidade subótima de esperma, a ICSI permite uma fertilização bem-sucedida12,31,56. Assim, perspetivase uma possível capacidade reprodutiva futura.
Criopreservação do tecido testicular (CTT)
Em idades pré-púberes, quando não há a produção de espermatozoides, a CTT pode ser o procedimento usado, sendo semelhante à CTO21,31.
Embora o testículo pré-púbere não produza espermatozoides maduros, ele contém as células estaminais a partir das quais se irão desenvolver os espermatozoides12.
O processo baseia-se na colheita e congelamento do tecido testicular, antes dos tratamentos antineoplásicos. Após cura do paciente, o tecido pode ser descongelado e as células germinativas armazenadas podem ser reimplantadas no próprio testículo do paciente, onde darão origem à espermatogénese completa e normal, nos túbulos seminíferos. Este procedimento é conhecido como transplante de células germinativas12.
Uma das questões centrais no autotransplante de células germinativas é o risco de reintroduzir células malignas. Dada a concentração de células leucémicas no testículo, o risco de reintroduzir células malignas no autotransplante de células germinativas é superior em cancros hematológicos. Neste grupo de pacientes, a técnica de maturação in-vitro de células estaminais permite evitar esse risco12.
O tecido testicular tem uma taxa de viabilidade pós -descongelamento superior (95%) em comparação com a preservação das células-estaminais (66%)31.
Mais tarde, essas técnicas de preservação da fertilidade poderiam ser combinadas com processos de reprodução medicamente assistida permitindo aos doentes em idades pediátricas uma forma alternativa de reprodução, apesar de uma possível infertilidade31.
Esta técnica é ainda considerada experimental21. Ainda não há casos de tentativa de restauração da fertilidade após autotransplante, em humanos, por questões de segurança57.
Em 2019 foi reportado o sucesso desta técnica no macaco rhesus58.
A Tabela II sintetiza os principais métodos de preservação da fertilidade usados em oncologia pediátrica, com requisitos, vantagens e desvantagens.
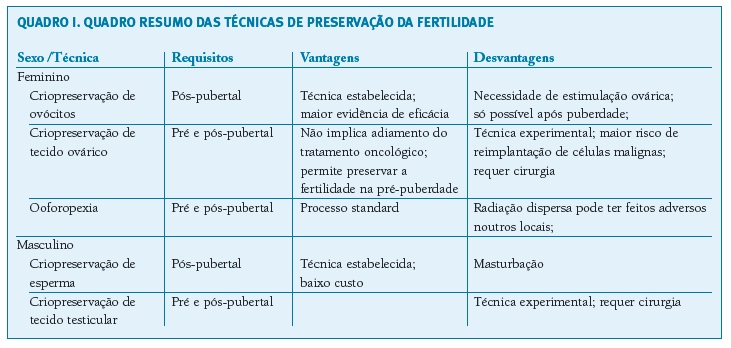
(clique para ampliar ! click to enlarge)
Num estudo efetuado em Portugal, uma das principais barreiras à prática de discussão sobre as técnicas de preservação da fertilidade, pelos oncologistas, foi a falta de tempo com os pacientes59. Esta discussão também pode levantar questões éticas por motivos culturais, religiosos ou conflitos de interesse entre o paciente e a família, podendo ser mediados por um consultor de ética60.
Conclusão
Todas as crianças e adolescentes com o diagnóstico de cancro e seus pais devem ser informados sobre o risco de infertilidade relacionada com os tratamentos propostos e aconselhados acerca de métodos de preservação da fertilidade. Este aconselhamento deve ser efetuado por uma equipa multidisciplinar que deve incluir um oncologista pediátrico, um especialista em medicina da reprodução, um urologista com experiência em fertilidade masculina , bem como um profissional de saúde mental e ainda um consultor de ética. Deste modo são fornecidas opções individualizadas de preservação da fertilidade antes do início da terapêutica, uma vez que a eficácia das técnicas de preservação da fertilidade diminui muito se aplicadas após terapêutica, sendo questionável a sua validade.
Em idades pré-púberes ou com urgência em iniciar as terapêuticas oncológicas, as técnicas atualmente disponíveis são a CTO ou CTT, embora experimentais. Após a puberdade, a criopreservação de ovócitos ou de esperma são as técnicas recomendadas.
A preservação da fertilidade dos pacientes oncológicos pediátricos tem de ser reconhecida como relevante e indispensável na sua qualidade de vida futura pelo que se deseja um maior investimento no estudo das técnicas de preservação da fertilidade bem como sua divulgação.
REFERÊNCIAS BIBLIOGRÁFICAS
1. Lopategui, D.M., R. Yechieli, and R. Ramasamy, Oncofertility in sarcoma patients. Translational andrology and urology, 2017. 6(5): p. 951-958.
2. Miller, K.D., et al., Cancer treatment and survivorship statistics, 2016. CA Cancer J Clin, 2016. 66(4): p. 271-289.
3. Rodriguez-Wallberg, K.A. and K. Oktay, Fertility preservation during cancer treatment: clinical guidelines. Cancer Manag Res, 2014. 6: p. 105-117.
4. Volerman, A., Primary Care of the Childhood Cancer Survivor. Med Clin North Am, 2015. 99(5): p. 1059-1073.
5. Hudson, J.N., et al., New Promising Strategies in Oncofertility. Expert review of quality of life in cancer care, 2017. 2(2): p. 67-78.
6. Quinn, G.P., et al., Quality of life in adolescent and young adult cancer patients: a systematic review of the literature. Patient Relat Outcome Meas, 2015. 6: p. 19-51.
7. Imbert, R., et al., Safety and usefulness of cryopreservation of ovarian tissue to preserve fertility: a 12-year retrospective analysis. Hum Reprod, 2014. 29(9): p. 1931-1940.
8. Kovacs, P., Fertility preservation in reproductive age women with cancer. Journal of obstetrics and gynaecology of India, 2014. 64(6): p. 381-387.
9. Rosendahl, M., et al., Cryopreservation of ovarian tissue for fertility preservation: no evidence of malignant cell contamination in ovarian tissue from patients with breast cancer. Fertility and Sterility, 2011. 95(6): p. 2158-2161.
10. Oktay, K., et al., Fertility Preservation in Patients With Cancer: ASCO Clinical Practice Guideline Update. J Clin Oncol, 2018. 36(19): p. 1994-2001.
11. Donnez, J. and M.M. Dolmans, Fertility Preservation in Women. N Engl J Med, 2017. 377(17): p. 1657-1665.
12. Maltaris, T., et al., Gonadal damage and options for fertility preservation in female and male cancer survivors. Asian J Androl, 2006. 8(5): p. 515-33.
13. Oktay, K. and O. Oktem, Fertility preservation medicine: a new field in the care of young cancer survivors. Pediatr Blood Cancer, 2009. 53(2): p. 267-73.
14. Sklar, C., Maintenance of ovarian function and risk of premature menopause related to cancer treatment. J Natl Cancer Inst Monogr, 2005(34): p. 25-7.
15. Dolmans, M.M. and J. Donnez, Indications for fertility preservation in women from malignant diseases to benign conditions to age-related fertility decline. Minerva Ginecol, 2018. 70(4): p. 402-407.
16. Andres, M.M. and V. Castel, [Preservation of fertility in children and adolescents with cancer: current situation and future perspectives]. An Pediatr (Barc), 2009. 71(5): p. 4406.
17. Dinikina, Y., et al., Ovarian tissue cryopreservation in prepubertal patients with oncological diseases: multidisciplinary approach and outcomes. J Matern Fetal Neonatal Med, 2019: p. 1-8.
18. Roberts, J., et al., Fertility preservation in reproductive-age women facing gonadotoxic treatments. Current oncology (Toronto, Ont.), 2015. 22(4): p. e294-e304.
19. Meirow, D. and D. Nugent, The effects of radiotherapy and chemotherapy on female reproduction. Hum Reprod Update, 2001. 7(6): p. 535-43.
20. Sarafoglou, K., et al., Gonadal function after bone marrow transplantation for acute leukemia during childhood. J Pediatr, 1997. 130(2): p. 210-6.
21. Anderson, R.A., et al., Cancer treatment and gonadal function: experimental and established strategies for fertility preservation in children and young adults. Lancet Diabetes Endocrinol, 2015. 3(7): p. 556-567.
22. Gosden, R.G., et al., Impact of congenital or experimental hypogonadotrophism on the radiation sensitivity of the mouse ovary. Hum Reprod, 1997. 12(11): p. 2483-2488.
23. Reinmuth, S., et al., Impact of chemotherapy and radiotherapy in childhood on fertility in adulthood: the FeCt-survey of childhood cancer survivors in Germany. J Cancer Res Clin Oncol, 2013. 139(12): p. 2071-2078.
24. Rivkees, S.A. and J.D. Crawford, The relationship of gonadal activity and chemotherapyinduced gonadal damage. Jama, 1988. 259(14): p. 2123-2125.
25. Donnez, J. and M.M. Dolmans, Ovarian cortex transplantation: 60 reported live births brings the success and worldwide expansion of the technique towards routine clinical practice. J Assist Reprod Genet, 2015. 32(8): p. 1167-1170.
26. Checa Vizcaino, M.A., et al., The effects of letrozole on ovarian stimulation for fertility preservation in cancer-affected women. Reprod Biomed Online, 2012. 24(6): p. 606-610.
27. Chian, R.C., et al., Obstetric and perinatal outcome in 200 infants conceived from vitrified oocytes. Reprod Biomed Online, 2008. 16(5): p. 608-610.
28. Cobo, A., et al., Elective and Onco-fertility preservation: factors related to IVF outcomes. Hum Reprod, 2018. 33(12): p. 2222-2231.
29. Fertility preservation and reproduction in patients facing gonadotoxic therapies: a committee opinion. Fertil Steril, 2013. 100(5): p. 1224-1231.
30. Sonmezer, M. and K. Oktay, Fertility preservation in female patients. Hum Reprod Update, 2004. 10(3): p. 251-266.
31. Wunder, D., et al., Fertility preservation in cancer patients. Review of the French speaking part of Switzerland and recommendations for different situations. Swiss Med Wkly, 2012. 142: p. w13645.
32. Ovarian tissue cryopreservation: a committee opinion. Fertil Steril, 2014. 101(5): p. 1237-1243.
33. Donnez, J., et al., Ovarian cortex transplantation: time to move on from experimental studies to open clinical application. Fertil Steril, 2015. 104(5): p. 1097-1098.
34. Anderson, R.A., W.H.B. Wallace, and E.E. Telfer, Ovarian tissue cryopreservation for fertility preservation: clinical and research perspectives. Hum Reprod Open, 2017. 2017(1): p. hox001.
35. Oktay, K. and G. Karlikaya, Ovarian function after transplantation of frozen, banked autologous ovarian tissue. N Engl J Med, 2000. 342(25): p. 1919.
36. Donnez, J., et al., Livebirth after orthotopic transplantation of cryopreserved ovarian tissue. Lancet, 2004. 364(9443): p. 1405-1410.
37. Donnez, J., D.D. Manavella, and M.M. Dolmans, Techniques for ovarian tissue transplantation and results. Minerva Ginecol, 2018. 70(4): p. 424-431.
38. Matthews, S.J., et al., Successful pregnancy in a woman previously suffering from betathalassemia following transplantation of ovarian tissue cryopreserved before puberty. Minerva Ginecol, 2018. 70(4): p. 432-435.
39. Oktay, K. and O. Oktem, Ovarian cryopreservation and transplantation for fertility preservation for medical indications: report of an ongoing experience. Fertil Steril, 2010. 93(3): p. 762-8.
40. Sauerbrun-Cutler, M.T., et al., In vitro maturation and its role in clinical assisted reproductive technology. Obstet Gynecol Surv, 2015. 70(1): p. 45-57.
41. Mostinckx, L., et al., Obstetric and neonatal outcome of ART in patients with polycystic ovary syndrome: IVM of oocytes versus controlled ovarian stimulation. Hum Reprod, 2019. 34(8): p. 1595-1607.
42. Belva, F., et al., Growth and other health outcomes of 2-year-old singletons born after IVM versus controlled ovarian stimulation in mothers with polycystic ovary syndrome. Hum Reprod Open, 2020. 2020(1): p. hoz043.
43. Song, X.L., et al., Enhancing the scope of in vitro maturation for fertility preservation: transvaginal retrieval of immature oocytes during endoscopic gynaecological procedures. Hum Reprod, 2020. 35(4): p. 837-846.
44. Grynberg, M., et al., First birth achieved after fertility preservation using vitrification of in vitro matured oocytes in a woman with breast cancer. Ann Oncol, 2020. 31(4): p. 541-542.
45. Creux, H., et al., Thirteen years' experience in fertility preservation for cancer patients after in vitro fertilization and in vitro maturation treatments. J Assist Reprod Genet, 2018. 35(4): p. 583-592.
46. Kedem, A., et al., Outcome of immature oocytes collection of 119 cancer patients during ovarian tissue harvesting for fertility preservation. J Assist Reprod Genet, 2018. 35(5): p. 851-856.
47. Revel, A., et al., At what age can human oocytes be obtained? Fertility and Sterility, 2009. 92(2): p. 458-463.
48. Fasano, G., et al., Outcomes of immature oocytes collected from ovarian tissue for cryopreservation in adult and prepubertal patients. Reproductive BioMedicine Online, 2017. 34(6): p. 575-582.
49. Segers, I., et al., In vitro maturation (IVM) of oocytes recovered from ovariectomy specimens in the laboratory: a promising "ex vivo" method of oocyte cryopreservation resulting in the first report of an ongoing pregnancy in Europe. J Assist Reprod Genet, 2015. 32(8): p. 1221-1231.
50. Zapardiel, I., et al., Assisted reproductive techniques after fertility-sparing treatments in gynaecological cancers. Hum Reprod Update, 2016. 22(3): p. 281-305.
51. Terenziani, M., et al., Oophoropexy: a relevant role in preservation of ovarian function after pelvic irradiation. Fertil Steril, 2009. 91(3): p. 935.e15-16.
52. Bedaiwy, M.A., et al., Gonadotropin-releasing hormone analog cotreatment for preservation of ovarian function during gonadotoxic chemotherapy: a systematic review and meta-analysis. Fertil Steril, 2011. 95(3): p. 906-14.e1-4.
53. Demeestere, I., et al., No Evidence for the Benefit of Gonadotropin-Releasing Hormone Agonist in Preserving Ovarian Function and Fertility in Lymphoma Survivors Treated With Chemotherapy: Final Long-Term Report of a Prospective Randomized Trial. J Clin Oncol, 2016. 34(22): p. 2568-2574.
54. Bizet, P., et al., Sperm cryopreservation before cancer treatment: a 15-year monocentric experience. Reprod Biomed Online, 2012. 24(3): p. 321-330.
55. Moss, J.L., et al., Male adolescent fertility preservation. Fertil Steril, 2016. 105(2): p. 267273.
56. Hsiao, W., et al., Successful treatment of postchemotherapy azoospermia with microsurgical testicular sperm extraction: the Weill Cornell experience. J Clin Oncol, 2011. 29(12): p. 1607-1611.
57. Martinez, F., Update on fertility preservation from the Barcelona International Society for Fertility Preservation-ESHRE-ASRM 2015 expert meeting: indications, results and future perspectives. Fertil Steril, 2017. 108(3): p. 407-415.e11.
58. Fayomi, A.P., et al., Autologous grafting of cryopreserved prepubertal rhesus testis produces sperm and offspring. Science, 2019. 363(6433): p. 1314-1319.
59. Melo, C., et al., Portuguese oncologists' practices regarding female fertility preservation: Which barriers most relate to these practices? Eur J Cancer Care (Engl), 2018. 27(2): p. e12812.
60. Klipstein, S., M.E. Fallat, and S. Savelli, Fertility Preservation for Pediatric and Adolescent Patients With Cancer: Medical and Ethical Considerations. Pediatrics, 2020. 145(3).
Endereço para correspondência | Dirección para correspondencia | Correspondence
Maria do Pilar Ferreira
Rua do Henriquinho 4A 2º drt, Fajã de baixo. 9500-460 Ponta Delgada
E-Mail: pilarpimentelferreira@hotmail.com
Recebido em: 08/04/2020. Aceite para publicação: 09/06/2020.














