Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Angiologia e Cirurgia Vascular
versão impressa ISSN 1646-706X
Angiol Cir Vasc vol.14 no.3 Lisboa set. 2018
ARTIGO ORIGINAL
Síndrome pós-implante no EVAR
Post-implantation syndrome after EVAR
Rita Soares Ferreira1,2; Frederico Bastos Gonçalves1,2; Rodolfo Abreu1; Nelson Camacho1, Joana Catarino1, Ricardo Correia1, Maria Emília Ferreira1
1Department of Angiology and Vascular Surgery, Hospital de Santa Marta, CHLC, Lisbon, Portugal
2NOVA Medical School, Lisbon, Portugal
Endereço para correspondência | Dirección para correspondencia | Correspondence
RESUMO
lntrodução/Objectivos: O Síndrome pós-implante (SPI) caracteriza-se por febre, sintomas semelhantes aos gripais, leucocitose e elevação da PCR no pós-operatório de EVAR. Os autores têm como objectivo estimar a incidência de SPI pós-EVAR na sua instituição, identificar factores de risco e determinar a associação a eventos clínicos.
Materiais/Métodos: Foi desenhado um estudo retrospectivo num centro terciário. Todos os doentes submetidos a EVAR entre Julho de 2014 e Dezembro de 2016 foram incluídos. Os dados foram colhidos através da consulta dos processos electrónicos hospitalares, nomeadamente leucograma, PCR e temperatura corporal. O endpoint primário avaliado foi a incidência de SPI, definido como febre >38º e doseamento de PCR >75mg/L. Foi avaliada a associação com características demográficas e do procedimento, tempo de internamento e eventos clínicos (morte ou complicações major) perioperatórias.
Resultados: Foram identificados 205 doentes neste período. Após análise dos processos, foram excluídos 25 doentes por terem sido utilizadas endopróteses ramificadas ou fenestradas, 11 doentes por terem sido submetidos a EVAS, 17 doentes pela indicação para o EVAR não ser um aneurisma primário e 46 doentes pela cirurgia ser realizada em contexto de urgência. Nos 106 doentes restantes, a incidência de SPI foi de 19% (n=20). Foi encontrada uma relação estatística significativa em relação ao tabagismo (p=0,005), DPOC (p=0,005) e terapêutica com estatina (p=0,031). Após construção de um modelo de regressão logística multivariável, corrigindo para tabagismo e terapêutica com estatina, verificou-se que o primeiro é um importante factor de risco (OR 7,26; p=0,03) e a terapêutica com estatina um factor protector (OR=0,341; p=0,049). Relativamente a características do procedimento, abordagem percutânea, quantidade de contraste, complicações intra-operatórias e necessidade de procedimentos acessórios, não se verificaram diferenças. Foi encontrada uma diferença significativa entre grupos no que respeita ao tempo de internamento, sendo a mediana de 5 dias no grupo sem SPI e 7 dias no grupo com SPI (p=0,034). Não foram encontradas diferenças relativamente a eventos cardiovasculares, complicações ou morte nos 30 dias pós-operatório.
Conclusão: A incidência de SPI foi de 19 % e está de acordo com o descrito na literatura. Os resultados sugerem que o tabagismo constitui um factor de risco. Verificou-se ainda um aumento de tempo de internamento em 2 dias nos casos de SPI. A terapêutica com estatina na altura da operação é um factor modificável e que se revelou protector em relação à incidência de SPI, reforçando o benefício desta terapêutica no período perioperatório de doentes com AAA.
Palavras-chave: Inflamação; Aneurisma da Aorta Abdominal; Procedimentos endovasculares; Síndrome Pós-Implante
ABSTRACT
lntroduction: Post-implantation syndrome (PIS) is characterized by fever, flu-like symptoms, leukocytosis and elevation of reactive C protein in the postoperative period of EVAR. The authors aim to estimate the incidence of PIS after EVAR in their institution, identify risk factors and determine the association with clinical events. Materials and Methods: A retrospective study was designed at a tertiary center. All patients undergoing EVAR between July 2014 and December 2016 were included. Data were collected through electronic clinical records, as leukogram, reactive C protein and body temperature. The primary endpoint evaluated was the incidence of PIS, defined as fever> 38 ° and reactive C protein > 75mg / L. The association with demographic and procedural characteristics, length of hospitalization and perioperative clinical events (death or major complications) was assessed.
Results:205 patients were identified in this period. After analysis of the clinical records, 25 patients were excluded due to the use of branched or fenestrated endografts; 11 patients were excluded due to EVAS; in 17 patients, the indication wasnt a primary aneurysm or it was a mycotic aneurysm and; in 46 patients the time of surgery wasnt elective. In the remaining 106 patients, the incidence of PIS was 19% (n = 20). A statistically significant association was found between PIS and smoking (p = 0.005), COPD (p = 0.005) and statin therapy (p = 0.031). The multivariate logistic regression analysis, correcting for smoking and statin therapy, revealed that smoking is an important risk factor (OR 7.26, p = 0.03) and statin therapy a protective factor (OR = 0.341, p = 0.049). Regarding for the characteristics of the procedure, percutaneous approach, amount of contrast, intraoperative complications and need for complementary procedures, no differences were observed. A significant difference was found between groups in hospitalization length, with a median of 5 days in the group without PIS and 7 days in the PIS group (p = 0.034). No significant differences were found in cardiovascular events, complications or death within 30 days postoperatively between the groups.
Conclusion:The incidence of PIS was 19%, which is concordant with literature. The results suggest that smoking is a risk factor. There was also an increase in hospitalization length in 2 days in PIS group. Statin therapy at the time of surgery is a modifiable factor that has been shown to be protective with respect to PIS, reinforcing the benefit of this therapy in the perioperative period of AAA patients.
Keywords:Inflammation; Aortic Aneurysm, Abdominal; Endovascular Procedures; Postimplantation syndrome
Introdução
Apesar da exclusão endovascular de aneurismas da aorta abdominal (EVAR) ser um procedimento minimamente invasivo, verifica-se numa proporção de doentes uma reacção inflamatória no pós-operatório, caracterizada por febre, sintomas semelhantes aos gripais, leucocitose e elevação da Proteína C reactiva (PCR), denominada Síndrome Pós-Implante (SPI).(1-7)
O SPI pode definir-se pela presença de dois critérios de Síndrome de Resposta Inflamatória Sistémica (SRIS), leucócitos >12000/ml e febre (>38ºC)(1-7) ou pelos critérios de febre (temperatura>38ºC) e elevação da PCR(8,9).
Os autores têm como objectivo estimar a incidência de SPI pós-EVAR na sua instituição, identificar factores de risco e determinar a associação a eventos clínicos.
Materiais/métodos
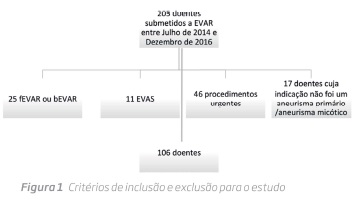
Foi desenhado um estudo retrospectivo num centro terciário. Todos os doentes submetidos a EVAR entre Julho de 2014 e Dezembro de 2016 no Hospital de Santa Marta, Centro Hospitalar Lisboa Central, foram incluídos. Os procedimentos realizados em urgência (aneurismas sintomáticas ou rotos), procedimentos cuja indicação não foi um aneurisma primário ou foi um aneurisma de etiologia micótica foram excluídos, bem como os procedimentos em que foram utilizadas endopróteses ramificadas ou fenestradas e Nellix® (Esquema 1).
Os dados foram colhidos através da consulta dos processos electrónicos hospitalares, nomeadamente características demográficas, protocolo operatório e dados intra-operatórios, bem como evolução clínica e analítica no pós-operatório. Os registos da temperatura auricular de 8 em 8h durante o internamento foram consultados, bem como as análises solicitadas, tendo todos os doentes uma avaliação analítica nas primeiras 24h de pós-operatório e daí em diante conforme evolução clínica.
O endpoint primário avaliado foi a incidência de SPI, definido como febre >38º e doseamento de PCR >75mg/L, sendo excluídos os doentes em que se constatou um foco infeccioso no pós-operatório, nomeadamente urinário, pulmonar, no sangue ou na ferida operatória.
Foi avaliada a associação com características demográficas e do procedimento, tempo de internamento e eventos clínicos (morte ou complicações major) nos 30 dias pós-operatórios.
A análise estatística foi realizada através do SPSS versão 21, sendo as variáveis continuas apresentadas sob a forma de média+-desvio padrão ou mediana e intervalo interquartil, conforme o padrão de normalidade ou não de distribuição destas. Para verificar as associações foi realizado o Teste de Qui quadrado e após este foi construído um modelo de regressão logística multivariável.
Resultados
Foram identificados 205 doentes neste período. Após análise dos processos, foram excluídos: 25 doentes por terem sido utilizadas endopróteses ramificadas ou fenestradas; 11 doentes por terem sido submetidos a EVAS; 17 doentes pela indicação para o EVAR não ser um aneurisma primário ou ser um aneurisma micótico; e 46 doentes pela cirurgia ser realizada em contexto de urgência. (Figura 1)
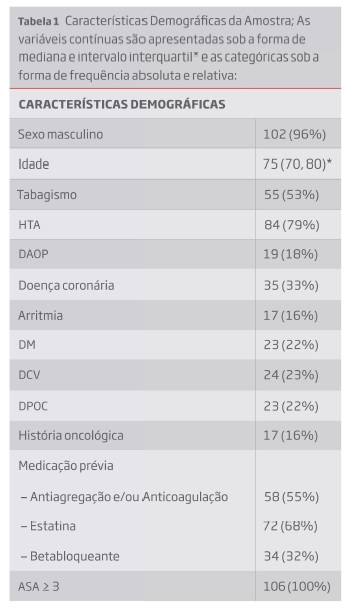
Relativamente às características demográficas nos 106 doentes restantes, 102 eram do sexo masculino com uma mediana de idade de 75 anos (intervalo interquartil 70-80), 55 doentes tinham hábitos tabágicos e 23 Doença Pulmonar Obstrutiva Crónica (DPOC), 84 eram hipertensos, 19 tinham Doença Arterial Obstrutiva Periférica (DAOP) conhecida, 35 doença coronária, 23 Diabetes Mellitus, 24 Doença Cerebrovascular (DCV) e 17 doentes tinham história oncológica (tabela 1). Todos os doentes tinham uma classificação ASA (ASA physical status classification system) igual ou superior a 3.
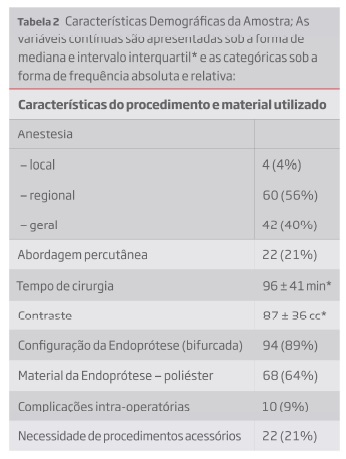
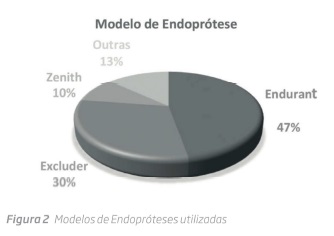
Relativamente às características do procedimento, 4 doentes foram submetidos a anestesia local, 60 a anestesia regional e 42 a anestesia geral. Em 22 doentes o procedimento foi percutâneo. O tempo de cirurgia médio foi de 96 ± 41 minutos (min) e a quantidade de contraste média utilizada foi de 87 ± 36 centímetros cúbicos (cc). (Tabela 2). Relativamente às endopróteses utilizadas, 89% foram bifurcadas. 32 foram Excluder®, 10 Zenith®, 50 Endurant® e 14 de outros modelos (Gráfico 1), sendo que 89% do total de endopróteses foram de poliéster.
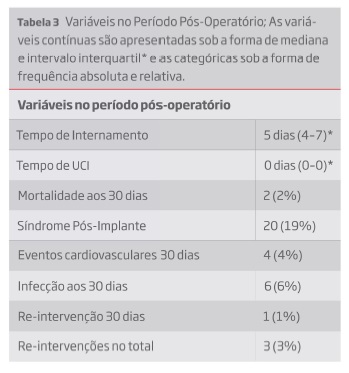
A mediana de duração de internamento foi de 5 dias (intervalo interquartil 4-7) e a de internamento em Unidade de Cuidados Intensivos (UCI) foi 0. Relativamente a complicações no pós-operatório, verificaram-se eventos cardiovasculares em 4 doentes e foram documentadas infecções (foco urinário, respiratório ou ferida operatória) em 6 doentes. A mortalidade aos 30 dias foi de 2% (n=2) e a incidência de SPI foi de 19% (n=20), excluindo as infecções documentadas (Tabela 3). O doseamento da PCR foi realizada na maiora dos doentes no 1º e 3º dias pós-operatório (a mediano do 1º doseamento foi 1 dia e do 2º doseamento foi 3 dias).
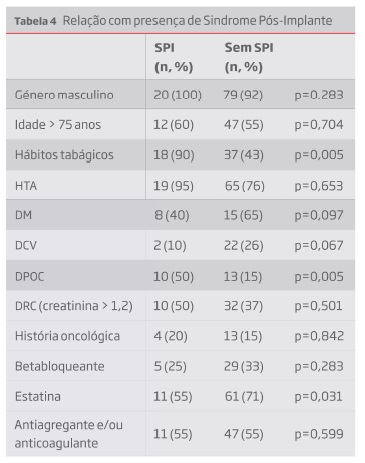
Foi encontrada uma relação estatística significativa em relação ao tabagismo (p=0,005), DPOC (p=0,005) e terapêutica com estatina (p=0,031) (Tabela 4). A incidência de SPI foi igualmente testada em relação à idade dos doentes, não se encontrando qualquer diferença estatisticamente significativa entre os doentes mais jovens e mais idosos (foi testado para os 70 (p=0,704) e 75 anos (p=0,251)). Após construção de um modelo de regressão logística multivariável, corrigindo para tabagismo e terapêutica com estatina, verificou-se que o primeiro é um importante factor de risco (OR 7,26; p=0,03) e a terapêutica com estatina um factor protector (OR=0,341; p=0,049) (Tabela 5).
Relativamente a características do procedimento, abordagem percutânea, quantidade de contraste, complicações intra-operatórias e necessidade de procedimentos acessórios, não se verificaram diferenças. A incidência de SPI foi de 15% no grupo de doentes em que a prótese implantada foi de PTFE e de 25% no grupo da prótese de poliéster (p=0,412).
Foi encontrada uma diferença significativa entre os grupos no que respeita ao tempo de internamento, sendo a mediana de 5 dias no grupo sem SPI e 7 dias no grupo com SPI (p=0,034).
Não foram encontradas diferenças relativamente a eventos cardiovasculares, complicações ou morte nos 30 dias pós-operatório.
Discussão
Neste estudo retrospectivo num centro terciário com 106 doentes, a indicidência de SPI pós-EVAR foi de 19%. Entre os factores demográficos, o tabagismo foi identificado como um factor de risco e a terapêutica com estatina como um factor protector. Não foi identificada uma relação estatisticamente significativa entre a ocorrência de SPI e características inerentes ao procedimento, bem como eventos clínicos no período pós-operatório de 30 dias, para além de um prolongamento do tempo de internamento de 2 dias.
A incidência de SPI varia entre os 14 e 60%(10), estando a incidência de 19% encontrada neste estudo enquadrada na descrita na literatura.
Voûte et al. encontraram uma incidência maior nas endopróteses com poliéster relativamente às de ePTFE (56.1% vs 17.9%; p <0 .001)(8), bem como Sartipy et al. (28,1% vs. 7,7% p=0,24). Neste estudo, foi encontrada uma diferença mas sem significado estatístico, provavelmente pela pequena dimensão da amostra.(7)
Relacionando as características demográficas com a incidência de SPI, foi encontrada uma relação com tabagismo, sendo um factor de risco (OR=7,26, p=0,003) e com a terapêutica com a estatina, sendo esta um factor protector (OR=0,341, p=0,049). A terapêutica com estatina é referenciada na literatura como eventual tratamento do Síndrome Pós-Implante, pelos seus efeitos anti-inflamatórios(10). No entanto, a terapêutica pré-operatória constituir um factor protector para a incidência deste Síndrome e o tabagismo, um factor de risco, não têm sido verificados(5,8,11).
Pelo contrário, não foram encontradas diferenças estatisticamente significativas em relação a características do procedimento, como abordagem percutânea, quantidade de contraste, complicações intra-operatórias e necessidade de procedimentos acessórios; o que está de acordo com o descrito por outros autores(5,8,11).
Relativamente ao tempo de internamento, verificou-se, tal como já conhecido um prolongamento deste(6,7), com uma mediana de 5 dias no grupo sem SPI e de 7 dias no grupo em que ocorreu SPI.
As eventuais consequências a longo prazo deste síndrome foram analisadas em 2 ensaios. Num dos ensaios (44 meses de follow-up) não foram encontradas diferenças estatisticamente significativas relativamente à sobrevida (p=0,761) e outros eventos adversos (p=0,562); foi encontrada, contudo, uma diminuição no número de endoleaks tipo II(2). No outro ensaio (1 ano de follow-up), foram encontradas diferenças estatisticamente significativas nos eventos adversos cardiovasculares major bem como noutros eventos adversos, como insuficiência renal aguda, reinternamentos e morte por qualquer causa (p=0,007 e p=0,005)(3). No nosso estudo, não foram encontradas diferenças estatisticamente significativas relativamente a eventos cardiovasculares, complicações ou morte nos 30 dias pós-operatório. A relação com endoleaks tipo II não foi avaliada.
Relativamente a profilaxia e terapêutica deste síndrome, a administração pré-operatória de corticosteróide parece reduzir a sua incidência, conforme foi concluído por Motte et al. (9). Neste estudo, os doentes não foram submetidos a anti-inflamatórios não esteróides nem esteróides no período peri-operatório e nos doentes em que foi diagnosticado SPI, pela manifestação benigna que os 20 casos apresentaram, não foi efectuada qualquer tipo de terapêutica específica e mantiveram-se apenas sob vigilância.
A irregularidade temporal e menor frequência de doseamentos analíticos dos parâmetros inflamatórios inerente ao desenho retrospectivo, constituem, na opinião dos autores, a principal limitação deste estudo. Os autores acreditam que a incidência deste síndrome poderá por esta razão estar subestimada.
Conclusão
A incidência de Síndrome Pós-Implante no EVAR foi de 19%. Os resultados sugerem que o tabagismo constitui um factor de risco. Verificou-se ainda um aumento de tempo de internamento em 2 dias nos casos de SPI. A terapêutica com estatina na altura da operação é um factor modificável e que se revelou protector em relação à incidência de SPI, reforçando o benef ício desta terapêutica no período perioperatório de doentes com AAA.
REFERÊNCIAS BIBLIOGRÁFICAS
1. Ferreira V, Machado R, Martins J et al. Síndrome inflamatório pós-EVAR - análise retrospectiva de 52 doentes tratados. Angiol Cir Vasc 2015;11:193-8. [ Links ]
2. Nano G, Occhiuto M, Stegher S et al. Postimplantation Syndrome after Endovascular Aortic Repair Using the Anaconda Endograft. Ann Vasc Surg 2014; 28 (6): 1409-15. [ Links ]
3. Arnaoutoglou E, Kouvelos G, Papa N et al. Prospective evaluation of postimplantation syndrome evolution on patient outcomes after endovascular aneurysm repair for abdominal aortic aneurysm. J Vasc Surg. 2016 May;63(5):1248-55. [ Links ]
4. Sartipy F, Lindstrom D, Gillgren P et al. THe Role of Procalcitonin in Postimplantation Syndrome after EVAR: A Pilot Study. Ann Vasc Surg. 2014; 28(4):866-73. [ Links ]
5. Kakisis JD,Moulakakis KG, Antonopoulos CN et al. Volume of new-onset thrombus is associated with the development of postimplantation syndrome after endovascular aneurysm repair. J Vasc Surg 2014;60:1140-45. [ Links ]
6. Kwon H, Ko GY, Kim MJ et al. Effects of postimplantation systemic inflammatory response on long-term clinical outcomes after endovascular aneurysm repair of an abdominal aortic aneurysm. Medicine (Baltimore). 2016 Aug;95(32): 4532. [ Links ]
7. Sartipy F, Lindstrom D, Gillgren P et al. The Impact of Stent Graft Material on the Inflammatory Response After EVAR. Vasc Endovascular Surg. 2015 Apr-May;49(3-4):79-83. [ Links ]
8. Voûte M, Gonçalves FB, Luijtgaarden KM et al. Stent graft composition plays a material role in the postimplantation syndrome. J Vasc Surg. 2012; 56(6):1503-9. [ Links ]
9. Motte L, Kehlet H, Vogt K et al. Preoperative Methylprednisolone Enhances Recovery After Endovascular Aortic Repair - A Randomized, Double-Blind, Placebo-Controlled Clinical Trial. Ann Surg. 2014;260(3):540-8. [ Links ]
10. Arnaoutoglou E, Kouvelos G, koutsoumpelis A et al. An Update on the Inflammatory Response after Endovascular Repair for Abdominal Aortic Aneurysm. . Mediators of Inflammation. 2015. [ Links ]
11. Moulakasis K, Alepaki M, Sfyroeras G et al. The impact of endograft type on inflammatory response after endovascular treatment of abdominal aortic aneurysm. Journal of Vascular Surgery 2013; 57: 668-77. [ Links ]
Endereço para correspondência | Dirección para correspondencia | Correspondence
Correio eletrónico: ana.ferreira2@chlc.min-saude.pt (R. Ferreira).
Responsabilidades éticas
Proteção de pessoas e animais: Os autores declaram que para esta investigação não se realizaram experiências em seres humanos e/ou animais.
Confidencialidade dos dados: Os autores declaram ter seguido os protocolos do seu centro de trabalho acerca da publicação dos dados dos doentes.
Direitoà privacidade e consentimento informado: Osautores declaram que não aparecem dados de doentes neste artigo.
Conflitos de interesses: Os autores declaram não haver conflito deinteresses.
Recebido a 31 de agosto de 2017
Aceite a 24 de maio de 2018