Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Angiologia e Cirurgia Vascular
versão impressa ISSN 1646-706X
Angiol Cir Vasc vol.14 no.4 Lisboa dez. 2018
ARTIGO DE REVISÃO
Rastreio do Aneurisma da Aorta Abdominal, estado atual da arte
Screening of abdominal aortic aneurysm, current state of the art
Susana Costa1; Rui Machado1,2; Rui de Almeida1,2
1Instituto de Ciências Biomédicas Abel Salazar (ICBAS) - Universidade do Porto
2Serviço de Angiologia e Cirurgia Vascular, Centro Hospitalar Universitário do Porto
Endereço para correspondência | Dirección para correspondencia | Correspondence
RESUMO
O aneurisma da aorta abdominal (AAA) ocorre mais frequentemente em homens de idade avançada, raça caucasiana, com historial tabágico ou história familiar de AAA. Os AAA parecem ter indicação para rastreio populacional pela sua prevalência (4-8%) e mortalidade (80-90%); existência de período de latência até à rotura do aneurisma; uso de técnica eficaz, económica e segura para rastrear; e, tratamento com baixa taxa de mortalidade. O objetivo deste trabalho foi efetuar uma análise crítica dos resultados de programas de rastreio populacional de AAA e seu impacto na mortalidade. Na revisão bibliográfica analisou-se ainda se o decréscimo na prevalência na última década poderá ter implicações na viabilidade destes programas. Os estudos randomizados MASS, Chichester e Viborg demonstraram que o rastreio de AAA é viável, mesmo 13 a 15 anos após o início do programa. Dois dos estudos comprovaram o custo-eficácia de rastrear AAA. O estudo realizado na Austrália revelou-se não efetivo, provavelmente por um diagnóstico incidental elevado. A meta-análise destes estudos demonstrou que o rastreio populacional de AAA reduz a mortalidade relacionada com AAA em 4 por 1000 homens com mais de 65 anos e reduz a mortalidade por todas as causas a longo termo, em 5 por 1000. Um estudo de coorte com 61.982 participantes reportou uma redução no número de aneurismas rotos e na média do diâmetro aórtico ao longo de 20 anos. Estudos recentes sugerem que o rastreio de AAA é economicamente viável até uma prevalência de 0,5% nos homens e 1,1% nas mulheres. Modelos estatísticos demonstraram que o rastreio de AAA importa benefícios comparáveis com outros programas de rastreio. A implementação de programas populacionais de rastreio de AAA na população masculina com mais de 65 anos é viável e clinicamente relevante, contribuindo para uma redução na mortalidade associada aos AAA. O rastreio de mulheres, pelo menos com historial tabágico, parece ter legitimidade, mas é necessária maior evidência para determinar a sua viabilidade. Segundo dados dos programas “Aorta não avisa” e “Aorta é vida” a prevalência de AAA em Portugal é de cerca de 4%, o que parece justificar a implantação de programa de rastreio populacional no país.
Palavras-chave: Aneurisma da aorta abdominal; Rastreio; Ultrassonografia; Viabilidade económica; Vigilância
ABSTRACT
Abdominal aortic aneurysm (AAA) occurs most often in older men, Caucasian, with history of smoking or family history of AAA. AAA seems to have indication for population screening for its prevalence (4-8%) and mortality (80-90%); existence of a latency period until aneurysm rupture; use of an efficient, economic and safe screening technique; and treatment with a low mortality rate. The objective of this work was to perform a critic analysis of the results of AAA population screening programs and their impact on mortality. It was also analyzed if the decrease in the prevalence in the last decade will have implications in the viability of these programs. The randomized trials MASS, Chichester and Viborg showed that the screening of AAA is feasible, even 13 to 15 years after the begging of the program. Two of the trials have proven that screening AAA is cost-effective. The trial performed in Australia revealed to be ineffective, probably due to a high incidental diagnosis. The meta-analysis of these studies has shown that population-based screening for AAA reduces the AAA-related mortality by 4 per 1000 men with 65 years or more and reduces all-cause mortality in the long-term, by 5 per 1000. A cohort study with 61,982 participants reported a reduction in the number of ruptured aneurysms and reduction of mean aortic diameter over 20 years. Recent studies suggest that screening of AAA is economically viable up to a prevalence of 0.5% in men and 1.1% in women. Statistical models have shown that screening of AAA has benefits comparable to other screening programs. The implementation of AAA population screening programs in the male population over 65 years-old is viable and clinically relevant, contributing to a reduction in mortality related to AAA. The screening in women, at least with history of smoking, appears to have legitimacy, but more evidence is needed to determine its viability. According to data of “Aorta não avisa” and “Aorta é Vida” programs the prevalence of AAA in Portugal is around 4%, which seems to justify the implementation of a population screening program in the country.
Keywords: Abdominal aortic aneurysm; Screening; Ultrasonography; Economic viability; Surveillance
Introdução
O aneurisma da aorta abdominal (AAA) é definido como uma dilatação da aorta abdominal com um diâmetro igual ou superior a 3 cm nos planos ântero-posterior ou transverso, que corresponde a mais de 2 desvios padrões acima do diâmetro médio da aorta(1,2). Os AAA ocorrem maioritariamente na aorta infrarrenal, próximo da bifurcação das artérias ilíacas comuns(3). A sua prevalência varia com a idade, o género e a raça, sendo mais prevalente em homens caucasianos de idade avançada(4,5). O AAA é responsável por 1-2% das causas de morte nos homens com mais de 65 anos(6,7). Estudos iniciais sugerem uma prevalência de 4-8% em homens com mais de 65 anos e 0,5-1,5% nas mulheres(8-11). Publicações recentes mencionam que a prevalência da doença tem diminuído na última década, possivelmente por diminuição do consumo de tabaco, prevenção de fatores de risco cardiovasculares, diminuição da mortalidade e morbilidade perioperatória na cirurgia eletiva e melhoria dos resultados pós-cirúrgicos de aneurismas rotos(12-14).
Os AAA com 3 a 4,9 cm de diâmetro aórtico têm baixo risco de rotura, pelo que não está recomendada intervenção cirúrgica nestes pacientes, realizando-se apenas vigilância imagiológica regular e tratamento médico. A ecografia é o exame de imagem de escolha para a deteção e vigilância dos AAA em pacientes assintomáticos pelo seu baixo custo e acessibilidade. Ademais, a ecografia é um exame não invasivo e tem uma sensibilidade e especificidade próximas dos 100%(15, 16).A principal desvantagem da ecografia abdominal é a dificuldade em visualizar a aorta em pacientes obesos e/ou com excesso de ar no trato intestinal. Os pacientes com AAA com um diâmetro aórtico =5,5 cm, sintomáticos ou com um ritmo de crescimento superior a 1 cm por ano têm indicação para referenciação para a especialidade de Cirurgia Vascular e intervenção cirúrgica pelo risco acrescido de rotura do aneurisma e consequente elevado risco de morte (80-90%). Os pacientes com risco acrescido de rotura devem ser considerados para cirurgia eletiva quando apresentam um AAA com um diâmetro aórtico de 5 cm. Nas mulheres está indicada a referenciação para a Cirurgia Vascular em AAA com um diâmetro aórtico de 5 cm e intervenção cirúrgica com 5,2 cm(17), porque estas têm um risco de rotura do aneurisma comparativamente aos homens 3 a 4 vezes superior e uma taxa de mortalidade intra-hospitalar superior. Além disso, existe um risco acrescido de rotura de pequenos aneurismas no sexo feminino(18, 19). A correção cirúrgica, quando indicada, deve ser realizada em centros especializados auditados, com uma taxa de mortalidade inferior a 5% e 2% por cirurgia eletiva via aberta e via endovascular (EVAR), respetivamente. Ademais, estes centros devem realizar pelo menos 50 cirurgias eletivas por ano(17).
O AAA tem uma história natural que favorece o seu rastreio, nomeadamente a sua prevalência, a existência de um período de latência de anos até à rotura, a existência de uma técnica eficaz, económica e segura para rastrear, o tratamento cirúrgico eletivo associado a baixa taxa de mortalidade e a mortalidade elevada da doença quando não tratada, que sugerem que a realização de rastreio populacional poderá trazer benefícios(20, 21). Neste contexto, efetuamos uma análise dos programas de rastreio de AAA publicados para avaliar a população a rastrear, a viabilidade da sua implementação, e seu impacto na mortalidade. Neste trabalho analisou-se ainda se o decréscimo na prevalência na última década poderá ter implicações na viabilidade destes programas.
Outros temas também serão abordados nesta revisão bibliográfica, como por exemplo, o impacto na qualidade de vida do diagnóstico da doença, a medição do diâmetro aórtico, o intervalo de vigilância de pequenos aneurismas e as ectasias aórticas.
Material e Métodos
Uma pesquisa de artigos científicos publicados em inglês, nas bases de dados eletrónicas: MEDLINE/PubMed, Web of Science e Cochrane foi realizada utilizando as palavras-chave “abdominal aortic aneurysm” e “screening”. A pesquisa foi limitada aos artigos publicados entre janeiro de 2007 e dezembro de 2017. Da pesquisa realizada resultaram 1225 referências. Após eliminação dos artigos em duplicado foram analisados o título e resumo dos artigos encontrados e excluídos os artigos fora do âmbito deste trabalho, nomeadamente, os artigos de revisão, os artigos de opinião, os artigos de rastreio oportunista de AAA e os artigos documentando apenas a prevalência dos AAA no grupo em estudo. No final, foram selecionados 61 artigos para a elaboração deste artigo.
Adicionalmente foi conduzida uma pesquisa em português relativa a programas de rastreio de AAA realizados em Portugal.
Rastreio do Aneurisma da Aorta Abdominal
O AAA é assintomático numa fase inicial e apenas quando atinge um diâmetro aórtico considerável é que complica e se manifesta. A sua rotura é uma emergência médica e está associada a uma taxa de mortalidade elevada (80-90%). A maioria dos doentes morre ainda antes de chegar no hospital, e aqueles que chegam vivos são submetidos a cirurgia de urgência, com um risco de morte de 50%(20, 21). De acordo com os critérios da Organização Mundial de Saúde (OMS)(22) há potencial para realizar-se o rastreio populacional de AAA.
Estudos randomizados
O primeiro estudo de rastreio de AAA foi implementado por Collins, em 1988, em Oxford(23). No final dos anos 80s, início da década de 90 surgiram os primeiros estudos de larga escala para determinar a viabilidade e benefício da implementação de programas de rastreio de AAA. Estes decorreram no Reino Unido (Chichester, MASS), na Dinamarca (Viborg) e na Austrália (Western Australia) para rastrear homens com 65 anos ou mais.
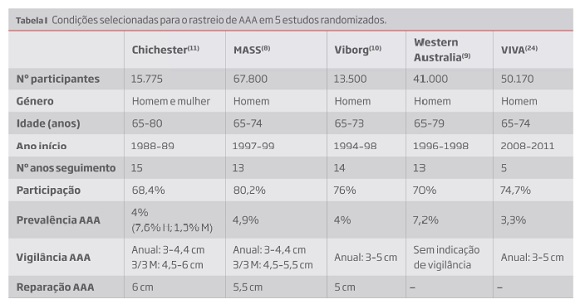
Em todos os estudos o rastreio foi realizado através de uma ecografia abdominal. Na tabela I estão descritas as condições de implementação de cada estudo.
O estudo decorrido em Chichester incluiu 15.775 pessoas entre os 65 e os 80 anos de idade, com uma prevalência de AAA de 7,6% em homens e 1,3% em mulheres. No sexo masculino, o grupo convidado evidenciou uma redução de 55% na incidência de rotura do aneurisma e uma redução na morte por rotura ao quinto ano de estudo de 42%(11). A longo termo verificou-se uma diminuição nos benefícios do programa, com uma redução na mortalidade por AAA a 10 anos de 21%(25) e apenas 11% a 15 anos(26). O número considerável de cirurgias eletivas na população não rastreada e o aumento da incidência de rotura e do número mortes relacionados com AAA após 10 anos de estudo no grupo controlo poderá ter contribuído para o esmorecimento dos benefícios do programa de rastreio com o passar do tempo(25).
Para o estudo MASS foram selecionados 67.800 homens com idades compreendidas entre os 65 e os 74 anos(8), dos quais 1333 tinham um diâmetro aórtico =3 cm, o que correspondeu a uma prevalência de AAA de 4,9%. A redução no número de mortes relacionadas com AAA rondou os 42-48% nos 13 anos de estudo(8,27-29). O decréscimo no risco relativo observado após 10 anos de rastreio deveu-se à ocorrência de rotura de AAA em participantes inicialmente rastreados com um diâmetro aórtico inferior a 3 cm. O número de homens necessário rastrear para evitar 1 morte foi estimado em 216(29). Embora inicialmente não tenham observado impacto na mortalidade global(8), no final do estudo os autores advogaram uma redução de 3% na mortalidade por todas as causas(29).
Para o estudo randomizado realizado na Dinamarca foram selecionados 13.500 homens com 65 a 73 anos de idade, com uma prevalência de AAA no grupo rastreado de 4,2%(10). Os resultados do estudo demonstraram igualmente uma redução significativa na mortalidade por AAA, com uma redução superior a 65% ao longo dos 14 anos de estudo(30-32). Conformemente ao estudo MASS, o programa de rastreio realizado em Viborg originou uma redução na mortalidade global de 2%. O grupo de trabalho avaliou ainda se o rastreio de AAA poderia ser restringido a grupos de alto risco. Os dados demonstraram uma redução drástica no número de rastreios (73%), no entanto, seriam prevenidas menos de metade das mortes relacionadas com AAA(33).
No estudo implementado na Austrália Ocidental observaram uma prevalência de 4,8% nos homens entre os 65 e os 69 anos e 10,8% para idade superior(9, 34). Ao longo do estudo verificaram uma menor diferença na mortalidade por AAA entre os grupos controlo e rastreado comparativamente aos outros estudos randomizados. Os resultados demonstraram que o programa foi mais benéfico nos participantes com idades entre os 65 e os 75 anos, com uma redução na mortalidade por AAA de apenas 8% nos participantes dessa faixa etária. Vários fatores poderão ter contribuído para a baixa eficácia na redução da mortalidade neste estudo, nomeadamente:
- Faixa etária dos participantes, com participantes até aos 83 anos de idade;
- Taxa de comparência inferior a outros estudos randomizados;
- Reduzido número de aneurismas com indicação cirúrgica, embora apresente uma elevada prevalência da doença;
- Inclusão de participantes no programa não elegíveis para rastreio e/ou tratamento;
- Grupo convidado para rastreio incluiu um elevado número indivíduos que não compareceram e que durante o estudo morreram por complicações associadas ao AAA;
- Elevada percentagem de diagnósticos incidentais e tratamento eletivo de sucesso no grupo de controlo, contribuindo para uma baixa taxa de mortalidade por AAA nesse grupo(9, 34).
O número de rastreios necessários para prevenir uma morte por AAA a 5 anos foi estimado em 4784 para homens com idades compreendidas entre os 64 e os 83 anos; e, 3290 para homens com 65 a 74 anos de idade(34). Os resultados deste estudo randomizado foram os menos promissores dentre os 4, com uma redução na mortalidade por AAA inferior à observada nos outros estudos, bem como a necessidade de um número muito superior de rastreios para prevenir uma morte por AAA.
Em continuação do estudo inicialmente desenvolvido para o rastreio de AAA, o departamento de Cirurgia Vascular do Hospital de Viborg prosseguiu com um estudo randomizado (VIVA) para o rastreio combinado de AAA, tensão arterial e doença arterial periférica(35). Dos 18.749 homens que participaram no estudo, 3,3% tinham AAA, 10,9% doença arterial periférica e 10,5% hipertensão arterial(36). Após 5 anos de estudo, os resultados demonstraram uma redução na mortalidade global de 7% no grupo rastreado(24). Os autores estimaram que seria necessário convidar 169 homens para o programa de rastreio para salvar 1 vida. Os resultados obtidos sugerem que a implementação de programa de rastreio vascular poderá providenciar ganhos em saúde semelhantes, talvez até superiores, ao dos programas de rastreio de cancro.
Meta-análise dos 4 estudos randomizados
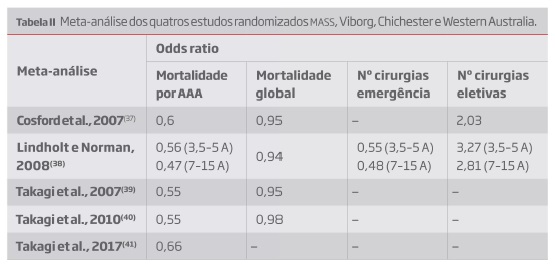
A análise estatística dos 4 estudos randomizados foi realizada por 3 grupos de trabalho e os resultados estão resumidos na tabela II.
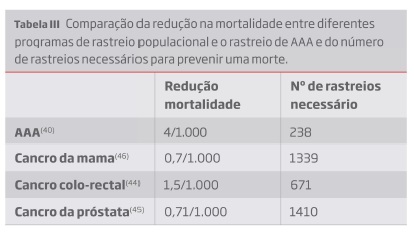
As meta-análises de Cosford et al.(37) e Lindholt et al.(42) evidenciaram uma redução estatisticamente significativa na morte por AAA, com odds ratio de 0,6 e 0,56, respetivamente. No que refere à mortalidade global a análise estatística demostrou uma redução não significativa (odds ratio 0,95/0,94). As meta-análises elaboradas por Takagi e colaboradores(39-41) também demonstraram uma redução significativa na mortalidade relacionada com AAA, designadamente de 4 por 1.000 homens com mais de 65 anos. Assim sendo, seria necessário rastrear 238 homens com mais de 65 anos para salvar uma vida(40). Os resultados das meta-análises indicam que o rastreio de AAA poderá ter um benefício superior ao de programas de rastreio implementados, como o cancro da mama(43), o cancro colo-rectal(44) ou o cancro da próstata(45) (tabela III). A análise estatística dos resultados mais recentes dos estudos randomizados sugere uma redução na mortalidade por todas as causas a longo termo, de 5 por 1000, embora este não atinga estritamente uma significância estatística(39).
Estudos não randomizados
No Reino Unido foram efetuados alguns programas de rastreio de AAA para além dos estudos randomizados Chichester e MASS. Em Gloucestershire foram rastreados 52.690 homens com 65 anos de idade no início da década de 90(47). Dos participantes no programa, 2412 tinham um diâmetro aórtico entre 2,6 e 5,4 cm (4,57%) e 148 um diâmetro superior a 5,4 cm (0,28%). Ao longo dos 20 anos de programa ocorreu um decréscimo na média do diâmetro aórtico nos homens rastreados.
Na Escócia, entre 2001 e 2004, foram rastreados 8146 homens com idades compreendidas entre os 65 e os 74 anos, pertencentes à região de Highland e de Western Isles(48). A prevalência de aneurismas foi de 5,1% e as ectasias aórticas (diâmetro aórtico 2,5-2,9 cm) foram detetadas em 8,2% dos rastreados. A mortalidade ao longo do programa foi inferior ao observado noutros estudos, com apenas 11 mortes por AAA em 7 anos de estudo, representando 0,14% da coorte e 1,7% de todas as causas de morte.
Em Dublin o risco cardiovascular de 481 homens com mais de 60 anos foi avaliado, com uma prevalência de AAA de 4,8%(49). Ao contrário do expectável o risco cardiovascular a 10 anos foi semelhante entre a população sem AAA e os participantes com AAA. O programa demonstrou-se custo-eficaz, sugerindo benefício na incorporação da avaliação do risco cardiovascular nos programas de rastreio de AAA, tal como observado no estudo randomizado VIVA.
Orientações europeias, americanas e canadianas relativamente ao rastreio de AAA
Com base no conhecimento atual sobre AAA e dos potenciais benefícios do seu rastreio entidades especializadas em Cirurgia Vascular têm redigido diretrizes neste âmbito.
A Sociedade Europeia de Cirurgia Vascular (ESVS) publicou em 2011 orientações sobre a prática clínica de AAA, nomeadamente recomendações quanto ao rastreio de indivíduos do sexo masculino aos 65 anos(17). O rastreio poderá ser realizado numa idade mais jovem se houver um risco elevado de desenvolver AAA e a reavaliação imagiológica deve limitar-se aos indivíduos rastreados em idade jovem ou com alto risco de desenvolver AAA. O rastreio de homens e mulheres com história familiar de AAA parece recomendável. No que refere às mulheres de baixo risco não está indicado o rastreio. Por sua vez, não é explícito relativamente às mulheres com historial tabágico. O rastreio de asiáticos não está indicado, pois não parece ser custo-eficaz. O rastreio oportunístico de AAA deve ser considerado em indivíduos com doença arterial periférica, uma vez que a incidência de AAA é elevada neste grupo.
A US Preventive Service Task Force (USPSTF)(50) publicou as mais recentes orientações sobre o rastreio de AAA em 2014. A USPSTF recomenda um rastreio único por ultrassonografia de homens com 65 a 75 anos com historial de tabaco, isto é, consumo de pelo menos 100 cigarros. Esta, recomenda ainda o rastreio de casos selecionados de homens não fumadores. O rastreio de mulheres não está recomendado, nem mesmo naquelas com historial tabágico. A American College of Preventive Medicine fez recomendações similares, sugerindo o rastreio único de homens com 65 a 75 anos com historial tabágico(51).
A Canadian Society for Vascular Surgery recomenda a implementação de um programa populacional de rastreio de AAA a todos os homens com 65 a 75 anos de idade e ainda pessoas com alto risco de desenvolver AAA, incluindo mulheres com 65 anos de alto risco, por consumo tabágico, doença cardiovascular ou história familiar de AAA; e, homens com menos de 65 anos com história familiar de AAA(52). Recentemente, a Canadian Task Force on Preventive Health Care reforçou a indicação para o rastreio único de homens entre os 65 e os 80 anos(53).
Programas nacionais de rastreio de AAA
Decorrente dos resultados promissores obtidos nos estudos randomizados e das orientações internacionais foram implementados programas de rastreio de AAA no Reino Unido, na Suécia e nos EUA.
No Reino Unido a implementação de programa de rastreio populacional de AAA em homens com 65 anos de idade iniciou-se em 2009. Um ano após o início do National Health Service Abdominal Aortic Aneurysm Screening Program (NAAASP) já tinham sido realizados 4216 rastreios(54) e 15.000 em 3 anos(55). O programa revelou uma prevalência de AAA de apenas 1,7%. Este decréscimo na prevalência comparativamente a estudos anteriores realizados no Reino Unido poderá estar relacionado com alterações na dieta e no estilo de vida, diminuição dos hábitos tabágicos e prevenção do risco cardiovascular(55). Em 2016, a linha dos 700.000 rastreios foi ultrapassada e a prevalência diminuiu ligeiramente para os 1,09%(56). O número de rastreios necessários para a identificação de um aneurisma foi de 78 na raça caucasiana, 154 na raça negra e 431 na raça asiática, respetivamente(57).
Na Suécia o programa de rastreio foi introduzido gradualmente em 2006 e atingiu a cobertura nacional em 2015(58). Ao longo de 8 anos de programa mais de 250 mil homens com 65 anos ou mais foram rastreados, com uma prevalência de AAA de 1,5%. O programa nacional demonstrou uma redução significativa na mortalidade por AAA, designadamente uma redução de 4% por ano de rastreio. O número necessário rastrear para prevenir uma morte foi de 667, que corresponde para uma população de 9,5 milhões à prevenção de 90 mortes prematuras por AAA por ano, e um ganho de 577 anos ajustado à qualidade de vida.
Nos EUA, a Veterans Affairs iniciou em 2007 um programa de rastreio de AAA em veteranos do sexo masculino entre os 65 e os 75 anos, que fumaram pelo menos 100 cigarros ao longo da vida e em mulheres com 50 anos ou mais com história familiar de AAA. Dos 9751 pacientes rastreados, 698 foram diagnosticados com AAA, o que corresponde a uma prevalência de 7,1%. Em simultâneo a Medicare começou a rastrear utentes do sexo masculino com historial tabágico, e homens e mulheres com história familiar de AAA(59). O programa teve um baixo rendimento, com rastreio de apenas 1-3% dos utentes elegíveis(59, 60). Segundo dados do Screening Abdominal Aortic Aneurysms Very Efficiently Act (SAAAVE) o impacto do programa foi modesto, sem alterações significativas na taxa de reparação de AAA, sua rotura ou na mortalidade global(60).
Realidade portuguesa
Em Portugal, em 2012, foi realizado um programa de rastreio de AAA, não sistemático, designado “Aorta não avisa”. O projeto promovido pela Sociedade Portuguesa de Angiologia e Cirurgia Vascular (SPACV) percorreu todas as capitais de distrito do país. No decorrer do projeto foram realizadas 1822 ecografias abdominais, com uma prevalência de AAA estimada em 2,2% na população com mais de 60 anos. Este valor ascendeu para 3,94% em homens com mais de 65 anos(61). Os dados do estudo insinuam uma prevalência semelhante à observada em alguns estudos europeus. Segundo dados de Sousa, P. e Fernandes e Fernandes, J.(61, 62) o diagnóstico incidental de AAA em Portugal é baixo, por exemplo, em 2014, menos de 500 AAA não rotos foram diagnosticados, o que estará a contribuir para a reduzida taxa de tratamento da doença no país. Dados não publicados de outro projeto, “Aorta é Vida”, revelaram uma prevalência de AAA de 4,2% entre as mais de mil pessoas rastreadas.
Em 2016, Castro-Ferreira et al.(63, 64) realizou um programa de rastreio sistemático de AAA e de avaliação do risco cardiovascular na USF Valongo. A prevalência de AAA foi de 2,1% em homens com mais de 65 anos, valor inferior ao observado nos outros projetos.
Rastreio de AAA no sexo feminino
O AAA tem uma menor prevalência no sexo feminino, mas um maior risco de complicações, especialmente um risco superior de rotura, incluindo dos pequenos aneurismas. Estudos sugerem que existe diferenças nas características clínicas e anatómicas dos AAA na população feminina, nomeadamente apresentação de AAA numa idade mais avançada e características anatómicas desfavoráveis, como uma anatomia mais complexa e maior ângulo do colo do aneurisma que contribuem para o acrescido risco de complicações(65).
Chichester foi o único estudo randomizado a incluir mulheres na amostragem. A baixa prevalência de aneurismas, a rotura dos aneurismas numa idade mais avançada e uma incidência de rotura dos aneurismas semelhante entre os grupos ao longo do estudo traduziu-se num benefício limitado de rastreio nas mulheres no estudo Chichester(66).
O programa de rastreio vascular patrocinado pela Stroke and Aneurysm Vascular Evaluation (SAVE)(67) que decorreu entre 2004 e 2006 em alguns estados dos EUA revelou uma prevalência de AAA de 0,6% na população feminina. A prevalência aumentou para 1% em fumadoras. A prevalência também aumentou com a idade, de 1,4% em mulheres com 75 anos para 2,7% em mulheres com mais de 85 anos. Um estudo realizado na Suécia apresentou resultados parecidos, com uma prevalência de 0,4% em mulheres com 70 anos(68).
Uma meta-análise de 8 estudos, englobando mais de 1,5 milhões de mulheres, refere heterogeneidade na prevalência dos AAA. Segundo a meta-análise a prevalência é geralmente superior a 1% em mulheres com mais de 70 anos ou com historial tabágico(69).
A análise estatística realizada por Wanhainen et al.(70) estimou que o rastreio de AAA em mulheres com 65 anos de idade deverá ser custo-eficaz para uma prevalência superior a 1,1%. Assim sendo, o rastreio de mulheres, pelo menos as com historial tabágico, parece viável economicamente. No entanto, são necessários estudos adicionais para corroborar os benefícios em saúde do rastreio de AAA desta população em específico.
Intervalo de vigilância de aneurismas da aorta abdominal
Os AAA com diâmetro aórtico de 3 a 5,5 cm têm um risco de rotura baixo, pelo que está indicado apenas vigilância regular por ecografia abdominal. Ainda não existe consenso sobre o intervalo de vigilância a implementar no seguimento desses pacientes.
Uma meta-análise sobre o ritmo de crescimento dos AAA estimou que o acréscimo de 1 cm no diâmetro aórtico está associado a um aumento no ritmo de crescimento de 1,62 mm/ano(71). Assim sendo, um aneurisma com 3,5 cm de diâmetro levará em média 6,2 anos a atingir 5,5 cm de diâmetro, enquanto um aneurisma com 4,5 cm de diâmetro atingirá essa dimensão em apenas 2 a 3 anos. Neste sentido, segundo os autores um intervalo de vigilância de vários anos para aneurismas entre os 3 e os 4 cm é clinicamente aceitável. Para os aneurismas com 4 a 4,9 cm de diâmetro a vigilância anual é custo-eficaz, enquanto uma vigilância semestral de aneurismas com 5 a 5,5 cm é aceitável.
Viabilidade da vigilância de ectasias aórticas
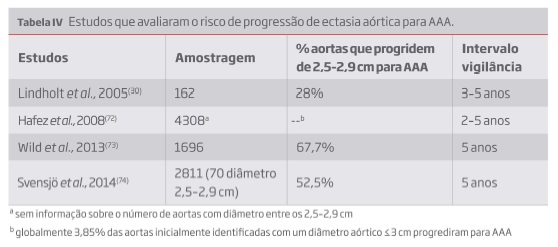
Os estudos randomizados Viborg e Chichester foram dos primeiros a avaliar o risco de progressão de ectasia aórtica (2,5-2,9 cm de diâmetro aórtico) para AAA. No estudo Viborg dos 162 participantes com um diâmetro aórtico inicial de 2,5-2,9 cm, 28% progrediram para AAA em 3 a 5 anos(30). No estudo Chichester foram detetados 166 casos com AAA durante o estudo, os quais tinham um diâmetro aórtico médio inicial de 2,5 cm, sugerindo que aortas abdominais com um diâmetro aórtico entre os 2,5 e os 2,9 cm têm um risco acrescido de progredir para aneurisma(72). Neste contexto, foram realizados alguns estudos para determinar a viabilidade económica e os benefícios da vigilância de pacientes rastreados com ectasia aórtica, os quais estão resumidos na tabela IV.
Um estudo observacional multicentro verificou a progressão de 67,7% das ectasias aórticas para AAA em 5 anos. A análise a longo-termo da mortalidade de pacientes com ectasias aórticas demonstrou um efeito significativo na mortalidade global(73). Os dados obtidos com um modelo estatístico demonstraram viabilidade económica na vigilância das ectasias aórticas uma vez 5 anos após o rastreio inicial(75).
Estes estudos apoiam a inclusão das ectasias aórticas no programa de vigilância, pelo menos uma vez, fomentando uma redução na incidência de AAA não diagnosticados e uma redução na morte por AAA.
Medição do diâmetro aórtico
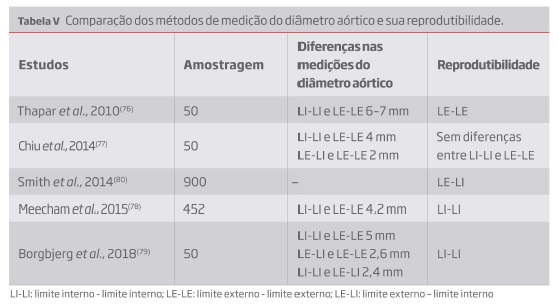
No que refere à medição do diâmetro aórtico não há consenso, com os estudos a selecionarem diferentes pontos da parede aórtica como referência. Na maioria dos estudos são usadas uma das três opções: limite interno - limite interno (LI-LI), limite externo - limite externo (LE-LE) ou limite externo - limite interno (LE-LI) da parede aórtica para a medição do diâmetro aórtico. Alguns estudos avaliaram se havia diferença nas dimensões do diâmetro aórtico para estes 3 métodos de medição e a sua reprodutibilidade. Os resultados obtidos nesses estudos estão sumariados na tabela V. O diâmetro aórtico quando medido pelo método LE-LE é cerca de 4 a 6 mm superior à medição pelo método LI-LI(76-79). Essa diferença é menor quando comparados os métodos LE-LI e LE-LE, com uma diferença de 2 a 2,6 mm no diâmetro aórtico(77, 79). Borgbjerg et al.(79) observou uma quase duplicação na prevalência de AAA quando usado o método LE-LE em vez do LI-LI. Pelas diferenças observadas entre os métodos de medição do diâmetro aórtico alguns autores recomendam a vigilância de pacientes com diâmetro aórtico entre os 2,5 e os 2,9 cm quando utilizada a metodologia LI-LI no rastreio inicial(78). No que refere à reprodutibilidade do método de medição do diâmetro aórtico existe inconsistência entre os estudos, sendo necessários estudos adicionais para uma análise mais fidedigna da reprodutibilidade destes métodos.
Custo-eficácia do programa de rastreio de AAA
Os estudos randomizados MASS e Viborg foram os primeiros a demonstrar viabilidade económica na implementação de programas de rastreio populacional de AAA. O estudo MASS verificou uma melhoria no custo-eficácia com o progredir do tempo, com um custo por ano de vida ganho estimado em £41.000 no 4º ano de estudo, £14.000 no 7º ano e £7.600 após 10 anos de estudo(27, 28). Ao 7º ano do estudo já apresentava um custo inferior ao valor referenciado como aceitável para a realização de intervenções em saúde no Reino Unido (£25.000)(81). O estudo Viborg foi igualmente custo-efetivo com um custo estimado em 157 por ano de vida ganho e 179 por ano ajustado à qualidade de vida(32).
O programa nacional de rastreio de AAA implementado no Reino Unido demonstrou ser custo-eficaz, mesmo apesar dos custos do programa e da baixa prevalência de AAA. O programa NAAASP continua a ser custo-eficaz a longo-termo, com um custo estimado em £5758 por ano de vida ganho e £7370 por ano ajustado à qualidade de vida a 30 anos, valor bem abaixo do limite recomendado pelo NICE (The National Institute for Health and Care Excellence)(82).
A viabilidade de implementar programas de rastreio de AAA em outros países também tem vindo a ser avaliada. O custo de rastreio de homens de 65 a 75 anos italianos(83) foi estimado em 290 e 350, para as coortes de “não rastreio” e “rastreio”, respetivamente. Para uma comparência de 62% no grupo rastreado, o estudo estimou um incremento do rácio custo-eficácia de 5673 por ano ajustado à qualidade de vida. Com base neste valor os autores consideram ser custo-eficaz a implementação de um programa de rastreio no serviço nacional de saúde italiano. O modelo de Markov também foi aplicado na determinação do custo-eficácia de um programa de rastreio de AAA na Holanda e na Noruega(84), demonstrando que o rastreio de AAA em homens de 65 anos poderá ser eficaz nestes países, mesmo para uma prevalência de AAA de 1%. No caso da Dinamarca os custos foram estimados em £43.485 por ano ajustado à qualidade de vida, valor esse superior ao estimado como custo-eficaz (£30.000) para a implementação de um programa no país(85).
Estudos recentes demonstraram um decréscimo na prevalência de AAA, e neste contexto, alguns estudos foram realizados para avaliar a implicação na viabilidade dos programas de rastreio. Svensjö et al.(86) verificou que o rastreio único em homens com 65 anos de idade continua a ser custo-eficaz até uma prevalência de 0,5% e clinicamente revelante como medida de saúde preventiva. O programa deixaria de ser custo-eficaz se o diagnóstico incidental de AAA fosse superior a 65% e a prevalência da patologia inferior a 0,8%. Um outro estudo baseado nos dados do programa nacional de rastreio sueco demonstrou igualmente que é ainda custo-eficaz rastrear AAA(87). Segundo Svensjö(86), para além de viável economicamente, o rastreio de AAA continua a ser benéfico em termos de saúde, com redução do risco relativo de morte por AAA em 42% e redução do risco absoluto de morte por AAA de 15,1 por 10.000 convidados para rastreio. Ademais, o rastreio de AAA continua a ter impacto clínico comparável com outros programas de rastreio, como por exemplo, o cancro da próstata e o cancro da mama que conferem uma redução do risco relativo de 20%(45) e de 15%(43), respetivamente.
Considerando os dados obtidos nos programas de rastreios realizados em Portugal, os quais sugerem uma prevalência de AAA superior a 2%, associado a uma reduzida taxa de tratamento da doença, apoiam a implementação de programa de rastreio populacional de AAA no país.
Impacto do rastreio de AAA na qualidade de vida
O estudo MASS foi dos primeiros a avaliar o impacto psicossocial do diagnóstico de AAA, com ausência de efeitos adversos quanto à ansiedade e à depressão nos participantes diagnosticados com aneurisma. No entanto, a curto prazo estes pacientes tiveram uma pontuação inferior nos questionários disponibilizados no que refere ao estado de saúde mental e físico e na autoavaliação da sua saúde(8). No estudo VIVA, de entre os 460 pacientes com AAA que preencheram um questionário de qualidade de vida, apenas 28 (6%) referiram um aumento da ansiedade durante o período de vigilância(24).
Um estudo prospetivo decorrido na Austrália avaliou o bem-estar psicológico e a qualidade de vida de pacientes previamente rastreados para AAA(88). Os questionários preenchidos antes do rastreio não apresentavam diferenças entre o grupo controlo e o grupo rastreado com AAA. Por sua vez, os questionários de seguimento a 6 meses evidenciaram uma diminuição significativa no estado geral de saúde, mas sem diferenças em termos de ansiedade e depressão.
No estudo realizado no Skane University Hospital, Suécia, os 52 participantes com AAA reportaram mais problemas de funcionamento físico, dor, stress e afeção da saúde em geral comparativamente aos participantes sem AAA. No que refere à ansiedade e à depressão não verificaram diferenças entre os grupos(89).
Berterö et al.(90) entrevistou 10 homens com AAA, os quais referiram ter pensamentos depressivos sobre o diagnóstico de AAA e a incerteza do que poderia vir a acontecer, nomeadamente os riscos associados ao crescimento do aneurisma e à cirurgia. Num outro estudo realizado na Suécia os participantes experienciaram ansiedade ao longo do primeiro ano após o diagnóstico da doença, insegurança sobre como o estilo de vida poderia influenciar a doença e relativamente ao que poderiam fazer para melhorar a sua saúde(91).
No geral os pacientes com AAA parecem apresentar um pior estado geral, apreensão e insegurança sobre a doença e nalguns dos estudos observou-se também ansiedade, dor e stress. Alguns destes estudos empregaram um número muito reduzido de participantes limitando a extrapolação de conclusões gerais sobre o impacto psicológico do diagnóstico de AAA, pelo que persiste a necessidade de realizar mais estudos, e com uma amostra mais representativa para obter evidência científica quanto ao impacto emocional e psicossocial do diagnóstico de AAA.
Conclusões
O AAA é uma doença potencialmente fatal se não for diagnosticada e tratada atempadamente. A sua rotura é uma emergência médica e está associada a uma taxa de mortalidade elevada. Neste sentido, a comunidade médica tem desenvolvido vários estudos para avaliar a viabilidade económica e benefícios de saúde do rastreio populacional de AAA. Os estudos randomizados MASS, Chichester e Viborg comprovaram que o rastreio populacional de AAA é viável. Além disso, o rastreio de AAA demonstrou ser benéfico como medida de saúde preventiva, com uma redução no número de mortes por AAA em mais de 40%. A longo-termo em dois dos estudos verificou-se uma diminuição nos benefícios em termos de mortalidade, mas continuando a evidenciar-se custo-efetividade após 13-15 anos de estudo. Um quarto estudo randomizado realizado na Austrália Ocidental, pelo contrário, revelou-se não efetivo. Alguns fatores poderão ter contribuído para esta desconformidade de resultados, como a faixa etária dos participantes, reduzido número de aneurismas com indicação cirúrgica, elevada taxa de diagnóstico incidental e tratamento eletivo no grupo de controlo. O rastreio de AAA poderá reduzir a mortalidade por AAA em 4 por 1.000 homens com mais de 65 anos, indicando um benefício de saúde comparável ao estabelecido para outros programas de rastreio, como o cancro da mama, da próstata e colo-rectal.
Na última década a prevalência de AAA baixou para menos de 2% no Reino Unido e Suécia, segundo os dados dos respetivos programas de rastreio nacionais. Mesmo perante este novo paradigma, os programas de rastreio de AAA continuam a ser custo-efetivos e clinicamente relevantes até uma prevalência de 0,5% em homens com idade igual ou superior a 65 anos de idade.
Os dados de tratamento de AAA (baixo diagnóstico incidental) e de programas de rastreio realizados em Portugal (prevalência semelhante aos estudos internacionais) apoiam a implementação de programa de rastreio populacional de AAA no país.
Um programa de rastreio vascular populacional combinado, nomeadamente fatores de risco cardiovascular, doença arterial periférica e aneurisma, parece ser efetivo, com resultados promissores na redução da mortalidade global. A implementação de programas de rastreio cardiovascular mais completos poderá ser especialmente benéfico em regiões com uma baixa prevalência de AAA, mas são necessários mais estudos para evidenciar esses benefícios.
O rastreio de AAA em mulheres com 65 anos de idade parece ser custo-eficaz até uma prevalência de 1,1%, pelo que o rastreio de mulheres, pelo menos as com historial tabágico, parece viável economicamente. No entanto, são necessários estudos adicionais para avaliar a viabilidade do rastreio de AAA nesta população em específico.
Um intervalo de vigilância de vários anos para AAA com um diâmetro aórtico entre os 3 e os 4 cm, vigilância anual de aneurismas entre os 4 e os 4,9 cm e semestral de aneurismas entre os 5 e os 5,5 cm parece aceitável. As ectasias aórticas têm um risco acrescido de progressão para AAA pelo que vários autores recomendam a inclusão deste subgrupo nos programas de vigilância, com viabilidade económica para a sua reavaliação pelo menos uma vez 5 anos após o rastreio inicial.
A metodologia a aplicar na medição do diâmetro aórtico não é consensual, mas é fundamental a sua uniformização futuramente, porque existem diferenças na medição do diâmetro aórtico até 4-6 mm entre métodos.
Os estudos de avaliação psicossocial demonstraram um pior estado geral, apreensão e insegurança nos pacientes com AAA e em alguns casos ansiedade, dor e stress.
A implementação de programas populacionais de rastreio de AAA na população masculina com mais de 65 anos é viável e clinicamente relevante, contribuindo para uma redução na mortalidade na população alvo. O rastreio de mulheres, pelo menos naquelas com historial tabágico, parece ter legitimidade, mas é necessária maior evidência para determinar a sua viabilidade. Os dados existentes apoiam a sua implementação em Portugal.
REFERÊNCIAS BIBLIOGRÁFICAS
1. Steinberg I. Arteriosclerotic abdominal aortic aneurysms - Report of 200 consecutive cases diagnosis by intravenous aortography. JAMA. 1966;195(12):149-53. [ Links ]
2. Wanhainen A, Thermudo R, Ahlstrom H, Lind L, Johausson L. Thoracic and abdominal aortic dimension in 70-year-old men and women - A population-based whole-body magnetic resonance imaging (MRI) study. J Vasc Surg. 2008;47(3):504-12. [ Links ]
3. Johnston KW, Rutherford RB, Tilson MD, Shah DM, Hollier L, Stanley JC. Suggested standards for reporting on arterial aneurysms. J Vasc Surg. 1991;13(3):452-8. [ Links ]
4. Gillum RF. Epidemiology of aortic-aneurysm in the United-States. J Clin Epidemiol. 1995;48(11):1289-98. [ Links ]
5. Forsdahl SH, Singh K, Solberg S, Jacobsen BK. Risk factors for abdominal aortic aneurysms: a 7-year prospective study: the Tromso Study, 1994-2001. Circulation. 2009;119(16):2202-8. [ Links ]
6. Budd JS, Finch DR, Carter PG. A study of the mortality from ruptured abdominal aortic aneurysms in a district community. Eur J Vasc Surg. 1989;3(4):351-4. [ Links ]
7. Ehlers L, Sorensen J, Jensen LG, Bech M, Kjolby M. Is population screening for abdominal aortic aneurysm cost-effective? BMC Cardiovasc Disord. 2008;8(32). [ Links ]
8. Ashton HA, Buxton MJ, Day NE, Kim LG, Marteau TM, Scott RAP, et al. The Multicentre Aneurysm Screening Study (MASS) into the effect of abdominal aortic aneurysm screening on mortality in men: a randomised controlled trial. Lancet. 2002;360(9345):1531-9. [ Links ]
9. Norman PE, Jamrozik K, Lawrence-Brown MM, Le MTQ, Spencer CA, Tuohy RJ, et al. Population based randomised controlled trial on impact of screening on mortality from abdominal aortic aneurysm. Brit Med J. 2004;329(7477):1259-62. [ Links ]
10. Lindholt JS, Henneberg EW, Fasting H, Juul S. Hospital based screening of 65-73 year old men for abdominal aortic aneurysms in the county of Viborg, Denmark. J Med Screen. 1996;3(1):43-6. [ Links ]
11. Scott RA, Wilson NM, Ashton HA, Kay DN. Influence of screening on the incidence of ruptured abdominal aortic aneurysm: 5-year results of a randomized controlled study. Brit J Surg. 1995;82(8):1066-70. [ Links ]
12. Svensjö S, Björck M, Gurtelschmid M, Gidlund KD, Hellberg A, Wanhainen A. Low prevalence of abdominal aortic aneurysm among 65-year-old Swedish men indicates a change in the epidemiology of the disease. Circulation. 2011;124(10):1118-23. [ Links ]
13. Mani K, Bjorck M, Wanhainen A. Changes in the management of infrarenal abdominal aortic aneurysm disease in Sweden. Brit J Surg. 2013;100(5):638-44. [ Links ]
14. Mani K, Lees T, Beiles B, Jensen LP, Venermo M, Simo G, et al. Treatment of abdominal aortic aneurysm in nine countries 2005-2009: A Vascunet Report. Eur J Vasc Endovasc. 2011;42(5):598-607. [ Links ]
15. Lederle FA, Walker JM, Reinke DB. Selective screening for abdominal aortic aneurysms with physical examination and ultrasound. Arch Intern Med. 1988;148(8):1753-6. [ Links ]
16. Lindholt JS, Vammen S, Juul S, Henneberg EW, Fasting H. The validity of ultrasonographic scanning as screening method for abdominal aortic aneurysm. Eur J Vasc Endovasc Surg. 1999;17(6):472-5. [ Links ]
17. Moll FL, Powell JT, Fraedrich G, Verzini F, Haulon S, Waltham M, et al. Management of abdominal aortic aneurysms clinical practice guidelines of the european society for vascular surgery. Eur J Vasc Endovasc. 2011;41:S1-S58. [ Links ]
18. Powell JT, Brady AR, Brown LC, Forbes JF, Fowkes FGR, Greenhalgh RM, et al. Mortality results for randomised controlled trial of early elective surgery or ultrasonographic surveillance for small abdominal aortic aneurysms. Lancet. 1998;352(9141):1649-55. [ Links ]
19. McPhee JT, Hill JS, Eslami MH. The impact of gender on presentation, therapy, and mortality of abdominal aortic aneurysm in the United States, 2001-2004. J Vasc Surg. 2007;45(5):891-9. [ Links ]
20. Basnyat PS, Biffin AHB, Moseley LG, Hedges AR, Lewis MH. Mortality from ruptured abdominal aortic aneurysm in Wales. Brit J Surg. 1999;86(6):765-70. [ Links ]
21. Johnston KW. Ruptured abdominal aortic aneurysm: six-year follow-up results of a multicenter prospective study. Canadian Society for Vascular Surgery Aneurysm Study Group. J Vasc Surg. 1994;19(5):888-900. [ Links ]
22. Wilson JMG, Jungner G, World Health Organization. Principles and Practice of Screening for Disease. Geneva: Who; 1968;22(11):28-41. Disponível em: http://apps.who.int/iris/bitstream/handle/10665/37650/WHO_PHP_34.pdf?sequence=17&isAllowed=y [ Links ]
23. Ellis M, Powell JT, Greenhalgh RM. Limitations of ultrasonography in surveillance of small abdominal aortic aneurysms. Br J Surg. 1991;78(5):614-6. [ Links ]
24. Lindholt JS, Sogaard R. Population screening and intervention for vascular disease in Danish men (VIVA): a randomised controlled trial. Lancet. 2017;390(10109):2256-65. [ Links ]
25. Vardulaki KA, Walker NM, Couto E, Day NE, Thompson SG, Ashton HA, et al. Late results concerning feasibility and compliance from a randomized trial of ultrasonographic screening for abdominal aortic aneurysm. Brit J Surg. 2002;89(7):861-4. [ Links ]
26. Ashton HA, Gao L, Kim LG, Druce PS, Thompson SG, Scott RAP. Fifteen-year follow-up of a randomized clinical trial of ultrasonographic screening for abdominal aortic aneurysms. Brit J Surg. 2007;94(11):696-701. [ Links ]
27. Kim LG, Scott RAP, Ashton HA, Thompson SG. A sustained mortality benefit from screening for abdominal aortic aneurysm. Ann Intern Med. 2007;146(10):699-706. [ Links ]
28. Thompson SG, Ashton HA, Gao L, Scott RAP. Screening men for abdominal aortic aneurysm: 10 year mortality and cost effectiveness results from the randomised Multicentre Aneurysm Screening Study. BMJ. 2009;338:b2307. [ Links ]
29. Thompson SG, Ashton HA, Gao L, Buxton MJ, Scott RA. Final follow-up of the Multicentre Aneurysm Screening Study (MASS) randomized trial of abdominal aortic aneurysm screening. Br J Surg. 2012;99(12):1649-56. [ Links ]
30. Lindholt JS, Juul S, Fasting H, Henneberg EW. Screening for abdominal aortic aneurysms: single centre randomised controlled trial. Brit Med J. 2005;330(7494):750-5. [ Links ]
31. Lindholt JS, Juul S, Fasting H, Henneberg EW. Preliminary ten year results from a randomised single centre mass screening trial for abdominal aortic aneurysm. Eur J Vasc Endovasc. 2006;32(6):608-14. [ Links ]
32. Lindholt JS, Sorensen J, Sogaard R, Henneberg EW. Long-term benefit and cost-effectiveness analysis of screening for abdominal aortic aneurysms from a randomized controlled trial. Br J Surg. 2010;97(6):826-34. [ Links ]
33. Lindholt JS, Juul S, Henneberg EW. High-risk and low-risk screening for abdominal aortic aneurysm both reduce aneurysm-related mortality. A stratified analysis from a single-centre randomised screening trial. Eur J Vasc Endovasc. 2007;34(1):53-8. [ Links ]
34. McCaul KA, Lawrence-Brown M, Dickinson JA, Norman PE. Long-term outcomes of the Western Australian Trial of screening for abdominal aortic aneurysms secondary analysis of a randomized clinical trial. JAMA Intern Med. 2016;176(12):1761-7. [ Links ]
35. Grondal N, Sogaard R, Henneberg EW, Lindholt JS. The Viborg vascular (VIVA) screening trial of 65-74 year old men in the central region of Denmark: study protocol. Trials. 2010;11(67):1-6. [ Links ]
36. Grondal N, Sogaard R, Lindholt JS. Baseline prevalence of abdominal aortic aneurysm, peripheral arterial disease and hypertension in men aged 65-74 years from a population screening study (VIVA trial). Brit J Surg. 2015;102(8):902-6. [ Links ]
37. Cosford PA, Leng GC. Screening for abdominal aortic aneurysm (Review). Cochrane Database Syst Rev. 2007(2):1-18. [ Links ]
38. Lindholt JS, Fasting U. Screening for abdominal aortic aneurysm among patients referred to vascular laboratory. Indeed feasible - But acceptable? Eur J Vasc Endovasc. 2008;35(6):675-6. [ Links ]
39. Takagi H, Tanabashi T, Kawai N, Kato T, Umemoto T. Abdominal aortic aneurysm screening reduces mortality: Meta-analyses of randomized, controlled trials. Eur J Vasc Endovasc. 2007;33(1):132-3. [ Links ]
40. Takagi H, Goto S, Matsui M, Manabe H, Umemoto T. A further meta-analysis of population-based screening for abdominal aortic aneurysm. J Vasc Surg. 2010;52(4):1103-8. [ Links ]
41. Takagi H, Ando T, Umemoto T. Abdominal aortic aneurysm screening reduces all-cause mortality: make screening great again. Angiology. 2018;69(3):205-11. [ Links ]
42. Lindholt JS, Norman P. Screening for abdominal aortic aneurysm reduces overall mortality in men. A meta-analysis of the mid- and long-term effects of screening for abdominal aortic aneurysms. Eur J Vasc Endovasc. 2008;36(2):167-71. [ Links ]
43. Gotzsche PC, Nielsen M. Screening for breast cancer with mammography. Cochrane Database Syst Rev. 2006(4):1-61. [ Links ]
44. Hewitson P, Glasziou P, Watson E, Towler B, Irwig L. Cochrane systematic review of colorectal cancer screening using the fecal occult blood test (hemoccult): an update. Am J Gastroenterol. 2008;103(6):1541-9. [ Links ]
45. Schroder FH, Hugosson J, Roobol MJ, Tammela TL, Ciatto S, Nelen V, et al. Screening and prostate-cancer mortality in a randomized European study. N Engl J Med. 2009;360(13):1320-8. [ Links ]
46. Gotzsche PC. Relation between breast cancer mortality and screening effectiveness: systematic review of the mammography trials. Dan Med Bull. 2011;58(3):A4246. [ Links ]
47. Darwood R, Earnshaw JJ, Turton G, Shaw E, Whyman M, Poskitt K, et al. Twenty-year review of abdominal aortic aneurysm screening in men in the county of Gloucestershire, United Kingdom. J Vasc Surg. 2012;56(1):8-14. [ Links ]
48. Duncan J, Harrild K, Iversen L, Lee A, Godden D. Long-term outcomes in men screened for Abdominal Aortic Aneurysm: a prospective cohort study. Brit J Surg. 2012;344(e2958):1-9. [ Links ]
49. Waterhouse DF, Cahill RA. Simple adaptation of current abdominal aortic aneurysm screening programs may address all-cause cardiovascular mortality: Prospective observational cohort study. Am Heart J. 2008;155(5):938-45. [ Links ]
50. LeFevre ML. Screening for Abdominal Aortic Aneurysm: U.S. Preventive Services Task Force Recommendation Statement. Ann Intern Med. 2014;161(4):281-91. [ Links ]
51. Lim LS, Haq N, Mahmood S, Hoeksema L, Comm APP. Atherosclerotic cardiovascular disease screening in adults american college of preventive medicine position statement on preventive practice. Am J Prev Med. 2011;40(3):e1-10. [ Links ]
52. Surgery TCSfV. Canadian Society Surgery (CSVS) Statement on AAA Screening 2008. Disponível em: https://canadianvascular.ca/Resources/Documents/AAA_statement08.pdf. [ Links ]
53. Singh H, Bell N, Dickinson JA, Lewin G, Tonelli M, Thombs B, et al. Recommendations on screening for abdominal aortic aneurysm in primary care. Can Med Assoc J. 2017;189(36):E1137-E45. [ Links ]
54. Conway AM, Malkawi AH, Hinchliffe RJ, Holt PJ, Murray S, Thompson MM, et al. First-year results of a national abdominal aortic aneurysm screening programme in a single centre. Brit J Surg. 2012;99(1):73-7. [ Links ]
55. Davis M, Harris M, Earnshaw JJ. Implementation of the National Health Service Abdominal Aortic Aneurysm Screening Program in England. J Vasc Surg. 2013;57(5):1440-5. [ Links ]
56. Jacomelli J, Summers L, Stevenson A, Lees T, Earnshaw JJ. Impact of the first 5 years of a national abdominal aortic aneurysm screening programme. Br J Surg. 2016;103(9):1125-31. [ Links ]
57. Benson RA, Poole R, Murray S, Moxey P, Loftus IM. Screening results from a large United Kingdom abdominal aortic aneurysm screening center in the context of optimizing United Kingdom National Abdominal Aortic Aneurysm Screening Programme protocols. J Vasc Surg. 2016;63(2):301-4. [ Links ]
58. Wanhainen A, Hultgren R, Linne A, Holst J, Gottsater A, Langenskiold M, et al. Outcome of the Swedish Nationwide Abdominal Aortic Aneurysm Screening Program. Circulation. 2016;134(16):1141-8. [ Links ]
59. Olchanski N, Winn A, Cohen JT, Neumann PJ. Abdominal aortic aneurysm screening: how many life years lost from underuse of the medicare screening benefit? J Gen Intern Med. 2014;29(8):1155-61. [ Links ]
60. Shreibati JB, Baker LC, Hlatky MA, Mell MW. Impact of the Screening Abdominal Aortic Aneurysms Very Efficiently (SAAAVE) Act on abdominal ultrasonography use among Medicare beneficiaries. Arch Intern Med. 2012;172(19):1456-62. [ Links ]
61. Fernandes e Fernandes J. Rede de Referenciação Hospitalar Angiologia e Cirurgia Vascular. 2017. [ Links ]
62. Sousa P, Fernandes e Fernandes J. A cirurgia vascular em Portugal de 2005 a 2025: conhecer para melhorar. Faculdade de Medicina da Universidade de Lisboa, 2016. [ Links ]
63. Castro-Ferreira R, Mendes P, Couto P, Barreira R, Peixoto F, Aguiar M, et al. Rastreio populacional de aneurisma da aorta abdominal em Portugal - o imperativo da sua realização. Angiologia e Cirurgia Vascular. 2016;12(4):267-70. [ Links ]
64. Porto NU. FMUP desenvolve rastreio inédito de Aneurisma da Aorta Abdominal, 2016. Disponível em: https://noticias.up.pt/fmup-desenvolve-rastreio-inedito-de-aneurisma-da-aorta-abdominal/. [ Links ]
65. Machado R, Teixeira G, Oliveira P, Loureiro L, Pereira C, Almeida R. Endovascular Abdominal Aneurysm Repair in Women: What are the Differences Between the Genders? Braz J Cardiova Surg. 2016;31(3):232-8. [ Links ]
66. Scott RAP, Bridgewater SG, Ashton HA. Randomized clinical trial of screening for abdominal aortic aneurysm in women. Brit J Surg. 2002;89(3):283-5. [ Links ]
67. Derubertis BG, Trocciola SM, Ryer EJ, Pieracci FM, McKinsey JF, Faries PL, et al. Abdominal aortic aneurysm in women: prevalence, risk factors, and implications for screening. J Vasc Surg. 2007;46(4):630-5. [ Links ]
68. Svensjö S, Björck M, Wanhainen A. Current prevalence of abdominal aortic aneurysm in 70-year-old women. Br J Surg. 2013;100(3):367-72. [ Links ]
69. Ulug P, Powell JT, Sweeting MJ, Bown MJ, Thompson SG, Group SC. Meta-analysis of the current prevalence of screen-detected abdominal aortic aneurysm in women. Br J Surg. 2016;103(9):1097-104. [ Links ]
70. Wanhainen A, Lundkvist J, Bergqvist D, Bjorck M. Cost-effectiveness of screening women for abdominal aortic aneurysm. J Vasc Surg. 2006;43(5):908-14. [ Links ]
71. Thompson SG, Brown LC, Sweeting MJ, Bown MJ, Kim LG, Glover MJ, et al. Systematic review and meta-analysis of the growth and rupture rates of small abdominal aortic aneurysms: implications for surveillance intervals and their cost-effectiveness. Health Technol Assess. 2013;17(41):1-118. [ Links ]
72. Hafez H, Druce PS, Ashton HA. Abdominal aortic aneurysm development in men following a "normal" aortic ultrasound scan. Eur J Vasc Endovasc Surg. 2008;36(5):553-8. [ Links ]
73. Wild JB, Stather PW, Biancari F, Choke EC, Earnshaw JJ, Grant SW, et al. A multicentre observational study of the outcomes of screening detected sub-aneurysmal aortic dilatation. Eur J Vasc Endovasc Surg. 2013;45(2):128-34. [ Links ]
74. Svensjö S, Björck M, Wanhainen A. Editor's choice: five-year outcomes in men screened for abdominal aortic aneurysm at 65 years of age: a population-based cohort study. Eur J Vasc Endovasc Surg. 2014;47(1):37-44.
75. Sogaard R, Laustsen J, Lindholt JS. Cost effectiveness of abdominal aortic aneurysm screening and rescreening in men in a modern context: evaluation of a hypothetical cohort using a decision analytical model. BMJ. 2012;345(e4276):1-13. [ Links ]
76. Thapar A, Cheal D, Hopkins T, Ward S, Shalhoub J, Yusuf SW. Internal or external wall diameter for abdominal aortic aneurysm screening? Ann R Coll Surg Engl. 2010;92(6):503-5. [ Links ]
77. Chiu KW, Ling L, Tripathi V, Ahmed M, Shrivastava V. Ultrasound measurement for abdominal aortic aneurysm screening: a direct comparison of the three leading methods. Eur J Vasc Endovasc Surg. 2014;47(4):367-73. [ Links ]
78. Meecham L, Evans R, Buxton P, Allingham K, Hughes M, Rajagopalan S, et al. Abdominal aortic aneurysm diameters: A study on the discrepancy between inner to inner and outer to outer measurements. Eur J Vasc Endovasc Surg. 2015;49(1):28-32. [ Links ]
79. Borgbjerg J, Bogsted M, Lindholt JS, Behr-Rasmussen C, Horlyck A, Frokjaer JB. Superior reproducibility of the leading to leading edge and inner to inner edge methods in the ultrasound assessment of maximum abdominal aortic diameter. Eur J Vasc Endovasc Surg. 2018;55(2):206-13.
80. Smith RW, Evans T, Wolstenhulme S. Reliability of aortic aneurysm screening measurements. Ultrasound. 2014;22(2):80-90. [ Links ]
81. Rawlins MD, Culyer AJ. National Institute for Clinical Excellence and its value judgments. Brit Med J. 2004;329(7459):224-7. [ Links ]
82. Glover MJ, Kim LG, Sweeting MJ, Thompson SG, Buxton MJ. Cost-effectiveness of the National Health Service Abdominal Aortic Aneurysm Screening Programme in England. Br J Surg. 2014;101(8):976-82. [ Links ]
83. Giardina S, Pane B, Spinella G, Cafueri G, Corbo M, Brasseur P, et al. An economic evaluation of an abdominal aortic aneurysm screening program in Italy. J Vasc Surg. 2011;54(4):938-46. [ Links ]
84. Spronk S, van Kempen BJ, Boll AP, Jorgensen JJ, Hunink MG, Kristiansen IS. Cost-effectiveness of screening for abdominal aortic aneurysm in the Netherlands and Norway. Br J Surg. 2011;98(11):1546-55. [ Links ]
85. Ehlers L, Overvad K, Sorensen J, Christensen S, Bech M, Kjolby M. Analysis of cost effectiveness of screening Danish men aged 65 for abdominal aortic aneurysm. BMJ. 2009;338:1-7. [ Links ]
86. Svensjö S, Mani K, Björck M, Lundkvist J, Wanhainen A. Screening for abdominal aortic aneurysm in 65-year-old men remains cost-effective with contemporary epidemiology and management. Eur J Vasc Endovasc. 2014;47(4):357-65. [ Links ]
87. Zarrouk M, Lundqvist A, Holst J, Troeng T, Gottsater A. Cost-effectiveness of screening for abdominal aortic aneurysm in combination with medical intervention in patients with small aneurysms. Eur J Vasc Endovasc Surg. 2016;51(6):766-73. [ Links ]
88. Lesjak M, Boreland F, Lyle D, Sidford J, Flecknoe-Brown S, Fletcher J. Screening for abdominal aortic aneurysm: does it affect men's quality of life? Aust J Prim Health. 2012;18(4):284-8.
89. Ericsson A, Holst J, Gottsater A, Zarrouk M, Kumlien C. Psychosocial consequences in men taking part in a national screening program for abdominal aortic aneurysm. J Vasc Nurs. 2017;35(4):211-20. [ Links ]
90. Bertero C, Carlsson P, Lundgren F. Screening for abdominal aortic aneurysm, a one-year follow up: an interview study. J Vasc Nurs. 2010;28(3):97-101. [ Links ]
91. Pettersson M, Hansson A, Brodersen J, Kumlien C. Experiences of the screening process and the diagnosis abdominal aortic aneurysm among 65-year-old men from invitation to a 1-year surveillance. J Vasc Nurs. 2017;35(2):70-7. [ Links ]
Endereço para correspondência | Dirección para correspondencia | Correspondence
Correio eletrónico: susanpatricia88@hotmail.com (S. Costa).
Responsabilidades éticas
Os autores declaram que para este trabalho não se realizaram experiências em seres humanos e/ou animais.
Os autores declaram terem seguido os protocolos do seu centro de trabalho acerca da publicação dos dados dos doentes.
Conflitos de interesses: Os autores declaram não haver conflito de interesses.
Recebido a 29 de fevereiro de 2018
Aceite a 03 de fevereiro de 2019