Introdução
A fístula aorto-cava primária (FAC) no contexto de aneurisma da aorta abdominal é uma entidade clínica rara, associada a menos de 1% dos AAA. Está classicamente associada à “tríade” de dor abdominal, massa abdominal pulsátil e sopro abdominal, sendo que as principais manifestações clínicas são dependentes do débito da fístula e muitas vezes inespecíficas1.Pode manifestar-se com insuficiência cardíaca aguda (ICA), edema dos membros inferiores, lesão renal aguda (LRA) e insuficiência hepática aguda (IHA)2,3. A cirurgia convencional associa-se a elevada mortalidade (16-66%)1. Apesar da limitada evidência acerca da abordagem desta patologia, o tratamento endovascular, quando exequível, aparenta ser eficaz e associado a menor morbimortalidade.
Os autores têm como objetivo descrever a apresentação clínica, terapêutica e resultados dos AAA complicados de FAC num hospital terciário e comparar com os resultados reportados na literatura.
Materiais e métodos
O estudo está de acordo com a política institucional para investigação clínica observacional e respeita recomendações da Declaração de Helsínquia. Foi desenhado um estudo retrospetivo que incluiu todos os doentes com AAA complicado de FAC tratados entre Janeiro de 2014 e Maio de 2020 num hospital terciário universitário. Os dados foram obtidos através da consulta do processo clínico eletrónico. Esses dados incluíram características demográficas, apresentação clínica, protocolo operatório e complicações intraoperatórias, evolução clínica e laboratorial relevante, bem como exames de imagem pós-operatórios. Os doentes foram divididos em grupo endovascular e cirurgia convencional e foi comparada a apresentação clínica, complicações e mortalidade pós-operatória.
Resultados
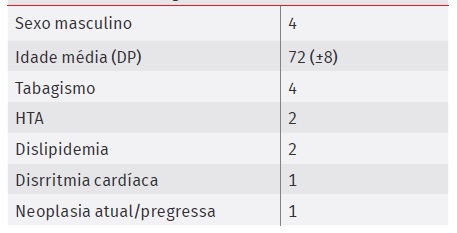
Durante o período compreendido entre Janeiro de 2014 e Maio de 2020, foram identificados quatro doentes com AAA complicado de FAC, todos submetidos a cirurgia emergente. (Tabela 1)
Os quatro doentes eram do sexo masculino, com idade média de 70(±8) anos e tinham como antecedentes tabagismo ativo ou pregresso (n=4), HTA (n=2), dislipidémia (n=2) e disritmia cardíaca (n=1).
Na admissão, todos os doentes apresentavam dor lombar (n=4) e hipotensão/taquicardia (n=4). Outros sinais/sintomas frequentemente associados foram massa abdominal pulsátil (n=3) e LRA com hematúria (n=2). Apenas um doente apresentava edema dos membros inferiores exuberante. (Tabela 2)
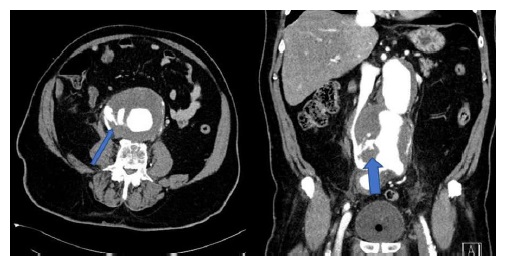
Os quatro doentes realizaram angiotomografia computorizada (AngioTC) com contraste endovenoso na admissão. Em dois doentes o exame revelou AAA com FAC, com extravasamento de contraste para a VCI e veias ilíacas na fase arterial. Nos restantes, a AngioTC revelou ruptura de AAA com hematoma retroperitoneal sem evidência de FAC, que apenas se diagnosticou intraoperatoriamente.
Relativamente à classificação American Society of Anesthesia, todos os doentes foram categorizados como ASA ≥ 4.
Quanto à técnica cirúrgica, três doentes foram submetidos a cirurgia convencional e um doente a exclusão endovascular. (Tabela 3) No grupo submetido a cirurgia convencional, dois doentes foram submetidos a interposição aorto-biilíaca e um a pontagem aorto-bi-femoral. Neste grupo de doentes, todos foram submetidos concomitantemente a rafia endoaneurismática da fístula. No grupo endovascular, o doente foi submetido a exclusão com endoprótese aorto-biilíaca Gore Excluder C3® em posição infra-renal, com selagem na artéria ilíaca externa esquerda e na artéria ilíaca comum direita.
Relativamente às perdas hemáticas, na cirurgia convencional a média das perdas foi de 2750ml e na cirurgia endovascular de 100ml. Não estão descritas outras complicações intra-operatórias, nomeadamente endoleaks.
Quanto às complicações pós-operatórias aos 30 dias, estas ocorreram apenas no grupo da cirurgia convencional. As complicações observadas foram LRA (n=3), insuficiência respiratória (n=2) e insuficiência hepática aguda (IHA) (n=2), isquémia aguda de membro (n=1) e colite isquémica (n=1) tendo-se verificado o óbito em dois destes doentes por falência multiorgânica ao 2º e 3ºdia de pós-operatório. O doente submetido a EVAR aorto-bi-ilíaco não apresentou qualquer complicação pós-operatória, tendo alta ao 7º dia pós-operatório.
Tabela 2 Apresentação clínica e achados imagiológicos
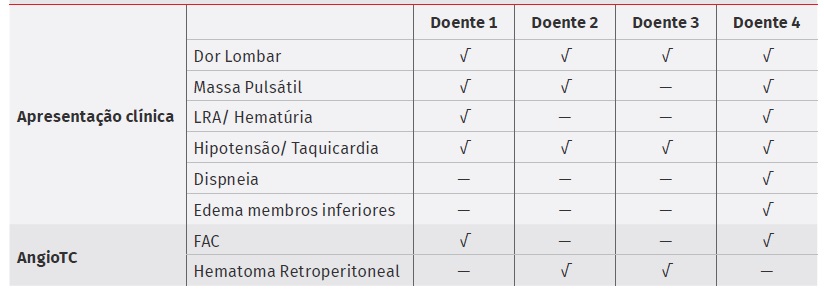
AngioTC: Angiotomografia Computorizada; FAC: Fístula Aorto-Cava; LRA: Lesão Renal Aguda
Durante os primeiros 30 dias pós-operatório verificou-se uma reintervenção: hemicolectomia esquerda, por colite isquémica, ao 1º dia pós-operatório. O mesmo apresentou posteriormente isquemia aguda de membro inferior que não foi submetida a intervenção por não reunir condições anestésico-cirúrgicas, verificando-se o óbito ao 2º dia de pós-operatório.
Após os 30 dias, observou-se uma intervenção secundária no doente submetido a EVAR aorto-bi-ilíaco; aos 3 meses de follow-up, foi submetido a implantação de endoprótese ramificada ilíaca, por aneurisma ilíaco direito não excluído na cirurgia inicial para preservação de uma artéria hipogástrica.
Os doentes apresentam um follow-up de 29 e 66 meses. (Tabela 3)
Discussão
A apresentação clínica desta entidade clínica é variável, podendo mesmo ser assintomática4. As manifestações provavelmente dependem do débito da fístula e da reserva fisiológica do doente, estando descrito na literatura um caso com meses de evolução5. Apesar da variabilidade, a apresentação aguda é claramente a mais frequente, compreendendo a maioria dos casos reportados3,6,7.
Os sintomas são, na sua maioria, inespecíficos, e vão desde sintomas de congestão venosa aguda com disfunção renal, insuficiência cardíaca aguda a, numa fase mais tardia, insuficiência hepática, associada a massa abdominal pulsátil e sopro abdominal.
A nossa experiência institucional é concordante com a literatura, sendo que todos os doentes se manifestaram de forma aguda com dor lombar e/ou abdominal de novo, hipotensão/taquicardia e massa abdominal pulsátil. A lesão renal aguda também foi frequente associada a hematúria.
A técnica cirúrgica mais frequentemente descrita na literatura é a cirurgia convencional (61%), tendo sido observado um aumento do número de casos de cirurgia endovascular reportados, particularmente a partir de 20101. No caso da cirurgia convencional, além da interposição protésica, a técnica descrita mais utilizada para o controlo da hemorragia pela FAC foi a compressão digital e posterior rafia endoaneurismática da fístula. Num número elevado de casos, foi obtido ainda controlo através da colocação de balão intra-cava, nalguns destes após tentativa falhada de controlo com compressão digital. Ambas as técnicas estão descritas como eficazes e a sua escolha refletirá um padrão de preferência institucional e do cirurgião. No caso da cirurgia endovascular, as abordagens reportadas apresentam grande variabilidade. Em muitos casos, a fístula foi excluída apenas através da implantação de endoprótese aórtica e posteriores intervenções guiadas pela angiografia final ou AngioTC de follow-up 8-18. Certos autores, pelo contrário, optaram pela exclusão da FAC com stenting da VCI previamente à implantação da endoprótese aórtica, para estabilização hemodinâmica19-23. Dois grupos optaram pela colocação prévia de filtro na VCI para prevenção de eventual embolização de trombo aneurismático para o sistema venoso21,24.
Tabela 3 Apresentação clínica e achados imagiológicos
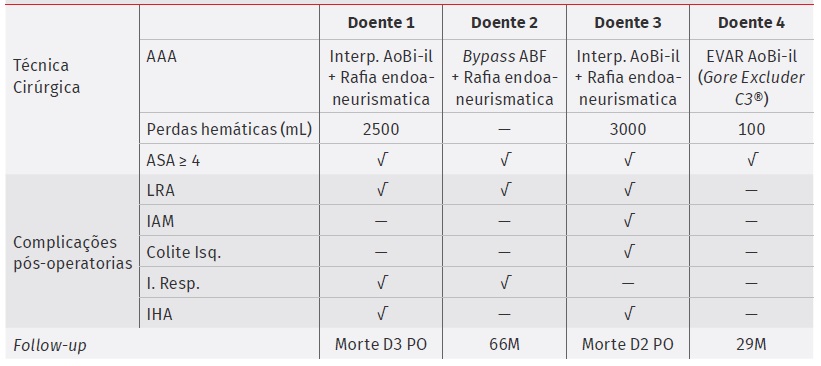
ASA: Classificação de estado físico da American Society of Anesthesiology AAA: aneurisma da aorta abdominal; IAM: isquémia aguda de membro; Bypass ABF: bypass aorto-bifemoral; Colite Isq.: colite isquémica; IHA: insuficiência hepática aguda; Interp. AoBi-il: interposição aorto-bi-iliaca; I.Resp.: insuficiência respiratória; LRA: lesão renal aguda; PO: pós-operatório
Na nossa experiência institucional, optou-se em todos os casos por compressão digital e rafia endoaneurismática da fístula apesar de as perdas hemáticas serem significativas nos casos descritos. Não existe comparação na literatura entre as perdas hemáticas nos doentes com controlo por compressão digital da FAC vs balão intra-cava, mas os autores estão cientes que esta técnica pode associar-se a redução das perdas hemáticas e poderia ter sido útil nos nossos casos descritos. No único caso reportado no nosso centro de exclusão endovascular, optou-se por exclusão da FAC com EVAR aorto-bi-ilíaco, não se verificando endoleaks na angiografia final nem na TC pós-operatória.
Relativamente às complicações e intervenções secundárias no período pós-operatório, na literatura, a cirurgia convencional e endovascular associam-se a um número semelhante de complicações, aproximadamente 35%1,25. No grupo submetido a cirurgia convencional, houve uma menor taxa de reintervenção global pós-operatória quando comparado com o grupo endovascular26.
Na literatura, nos casos reportados de cirurgia endovascular, as complicações médicas verificaram-se num número inferior de doentes. Nos casos reportados de cirurgia endovascular, as complicações técnicas são mais frequentes, sendo o endoleak tipo II pela artéria mesentérica inferior ou artéria lombar com extravasamento por FAC permeável a mais frequente8,9,24,27-29. A abordagem terapêutica nesta situação clínica foi muito variável, sendo que alguns autores optaram pelo tratamento do EL tipo II no tempo cirúrgico inicial19-23, outros num segundo momento cirúrgico, mesmo na ausência de sintomatologia associada8,10,28,30. Outros autores optaram pela vigilância, na ausência de sintomatologia e evolução favorável do saco aneurismático9,24,29, sem necessidade de intervenção secundária ao longo do follow-up disponibilizado. Lee et al e Sfyroeras et al, por manutenção de sintomatologia, optaram pelo tratamento, com melhoria sintomática27,31.
No grupo de doentes descrito pelos autores, as complicações e reintervenções aos 30 dias ocorreram apenas no grupo da cirurgia convencional, sendo as mais frequentes lesão renal aguda, insuficiência respiratória e insuficiência hepática aguda. No doente submetido a cirurgia endovascular, não se verificaram complicações aos 30 dias, nem endoleaks na AngioTC de follow-up. Contudo, foi re-intervencionado aos 3 meses de seguimento, tendo sido submetido a exclusão de aneurisma ilíaco, que se tinha optado por não tratar na cirurgia primária para preservar uma das artérias hipogástricas. Há que salientar que esta reintervenção não está associada a uma complicação direta do tratamento prévio da FAC.
A taxa de mortalidade nos casos reportados no nosso centro é elevada (50%), mas mesmo assim dentro do intervalo descrito na literatura (16-66%)1. Porém, devido à nossa pequena casuística, este valor deve ser interpretado com cautela. Brightwell et al reportam uma morbimortalidade associada à cirurgia endovascular inferior à cirurgia convencional, sendo esta maioritariamente associada ao volume de perdas hemáticas no ato cirúrgico25. Na nossa casuística, os doentes que faleceram, todos submetidos a cirurgia convencional, apresentam perdas muito significativas (média 2750ml), o que está de acordo com o defendido por Brightwell et al.
Por fim, a referir as limitações deste estudo, relacionadas naturalmente com a sua natureza retrospetiva e o reduzido número de doentes. Relativamente à revisão efectuada da literatura, a salientar que a maioria dos artigos referidos correspondem a descrição de casos clínicos.
Conclusões
A FAC pode ocorrer em associação ou não a rotura de AAA com hematoma retroperitoneal. Na presença de hematoma retroperitoneal, esta pode não ser evidente na AngioTC e apenas detetada intra-operatoriamente. Assim, deve existir um elevado índice de suspeição para esta complicação dos AAA na presença de LRA com hematúria e insuficiência cardíaca aguda com edema dos membros inferiores. Tendo em conta a nossa experiência e o descrito na literatura, a congestão venosa aguda com disfunção orgânica de novo é frequente nestes doentes, mesmo na presença de hematoma retroperitoneal. A cirurgia convencional com interposição protésica e rafia endoaneurismática da fístula foi a técnica de eleição, no entanto o tratamento endovascular, se exequível, aparenta ser eficaz e com menor morbilidade e mortalidade nestes doentes, apesar de se associar a uma maior taxa de reintervenção a curto e médio prazo. O não encerramento da comunicação aorto-cava por via endovascular não parece resultar em morbilidade significativa e na presença de endoleak tipo II com preenchimento da FAC, a vigilância, desde que haja uma evolução favorável do saco aneurismático e ausência de sintomas, apresenta-se como uma opção segura.