Introdução
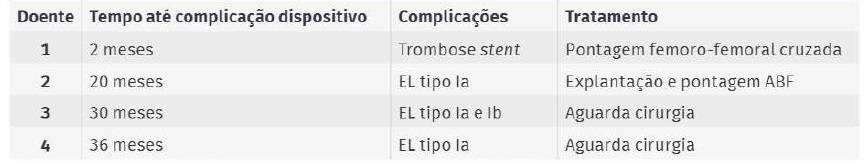
A endoprótese Nellix® (Endologix Inc., Irvine, CA) foi introduzida na Europa em 2013, com indicação no tratamento de aneurismas da aorta abdominal e ilíacos (AAA). É composta por dois stents cobertos (ePTFE) expansíveis por balão (10mm de diâmetro) e dois endobags de poliuretano, que são preenchidos por um polímero de polietilenoglicol, obliterando assim o saco aneurismático e excluindo-o da circulação - Endovascular Aneurysm Sealing (EVAS)(1).Inicialmente, foi introduzida com instruções para uso (IFU) alargadas, possibilitando a utilização em AAA de anatomia mais complexa e associava-se supostamente a uma redução da incidência de endoleak (EL) tipo 1, 2 e 3, bem como de migração protésica(2).Porém, durante a experiência a médio prazo com esta endoprótese, foi descrito um elevado número de complicações, levando à restrição progressiva das IFU (Tabela 1). Atualmente, o seu uso livre foi descontinuado e apenas está disponível em centros aprovados e no contexto de investigação clínica.
O nosso objetivo é rever os resultados institucionais da utilização da endoprótese Nellix® no tratamento de AAA.
Materiais e métodos
O estudo está de acordo com a política institucional para investigação clínica observacional e respeita as recomendações da Declaração de Helsínquia. Trata-se de um estudo retrospectivo referente a doentes tratados a AAA numa instituição terciária universitária, através da utilização da endoprótese Nellix®. Foram incluídos todos os casos eletivos e urgentes, identificados através da consulta de registos clínicos da instituição. Houve inclusão de aneurismas justa-renais e para-renais, assim como casos de re-intervenção após complicação de tratamento endovascular prévio de AAA. Foram excluídos casos de aneurisma toraco-abdominal.
Os dados referentes às características de base, procedimento realizado, curso do internamento e seguimento pós hospitalar foram obtidos por consulta dos processos clínicos. Foram recolhidos dados referentes a características demográficas, apresentação clínica, protocolo operatório e complicações intraoperatórias, evolução clínica e laboratorial relevante, bem como exames de imagem pós-operatórios.
Os endpoints estudados foram sucesso técnico e clínico aos 30 dias, assim como presença de EL, oclusão de endoprótese ou outras complicações pós-operatórias após os 30 dias.
Os dados são apresentados usando estatística descritiva simples, recorrendo a análise de sobrevivência através do método de Kaplan-Meier. Os dados foram tratados usando software estatístico dedicado (SPSS, versão 24.0)
Resultados
Entre os anos de Outubro de 2015 e Novembro de 2017 foram tratados 12 doentes, 9 (75%) do sexo masculino e 3 (25%) do sexo feminino, submetidos a 12 intervenções cirúrgicas. Os doentes apresentam uma idade média de 71(±8) anos. Na admissão, todos os doentes tinham hipertensão arterial (n=12), 58% doença arterial coronária (n=7), 58% tabagismo atual ou pregresso (n=7), 50% DAOP (n=6), 50% doença renal crónica (n=6), 33% diabetes mellitus (n=4), 25% disritmia cardíaca e/ou história de neoplasia pregressa (n=3). Dois doentes tinham como antecedente ainda doença cerebrovascular (17%). (Tabela 2) Não foi objetivada história familiar de patologia aneurismática.
Do total da amostra, 85% (n=10) dos doentes encontravam-se sob terapêutica hipolipemiante com estatina, 9 (75%) com anticoagulação e/ou antiagregação e 7 (58%) com β-bloqueante.
Segundo o sistema de classificação da Sociedade Americana de Anestesiologia, 100% da amostra apresentava ASA ≥3.
Tabela 2 Características Demográficas da Amostra
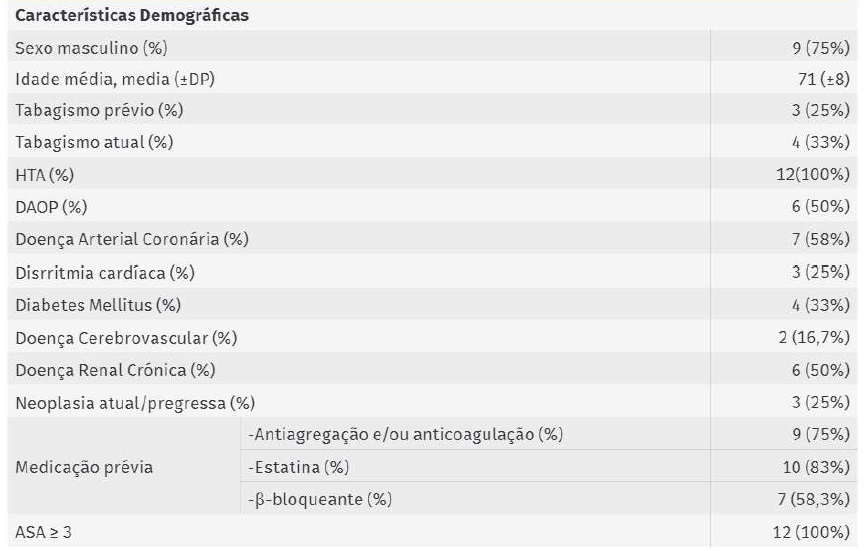
ASA: American Society of Anesthesiology DAOP: doença arterial obstrutiva periférica HTA: hipertensão arterial DP: desvio-padrão
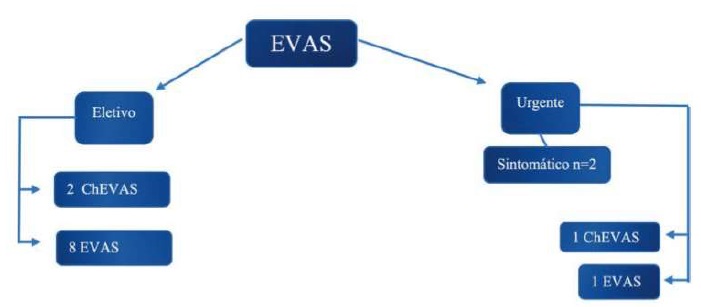
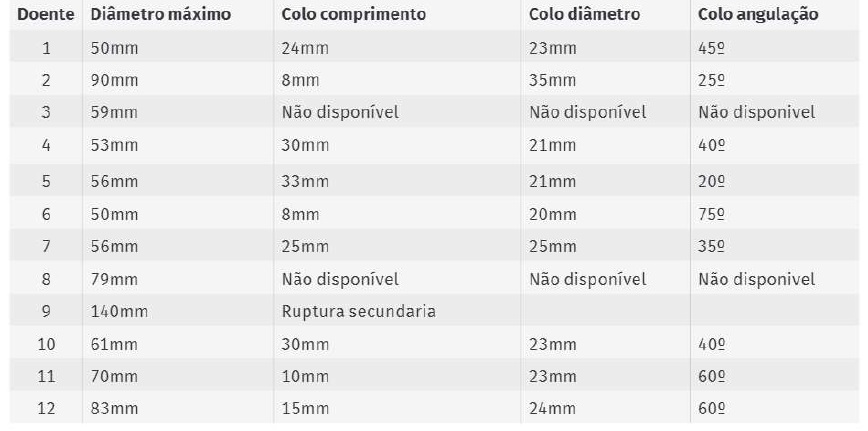
Em dois doentes a indicação terapêutica foi aneurisma sintomático, e o tratamento cirúrgico foi realizado em contexto de urgência. Nos restantes (n=10), o tratamento cirúrgico foi eletivo. (Figura 1) Um dos doentes urgentes apresentava EL tipo 1a secundário a EVAR prévio. Nesta amostra, três aneurismas eram aorto-ilíacos e os restantes aórticos, sendo que em três destes, havia envolvimento de pelo menos uma artéria renal. O diâmetro médio pré-operatório do aneurisma era de 57(±6,5) mm (Tabela 3).
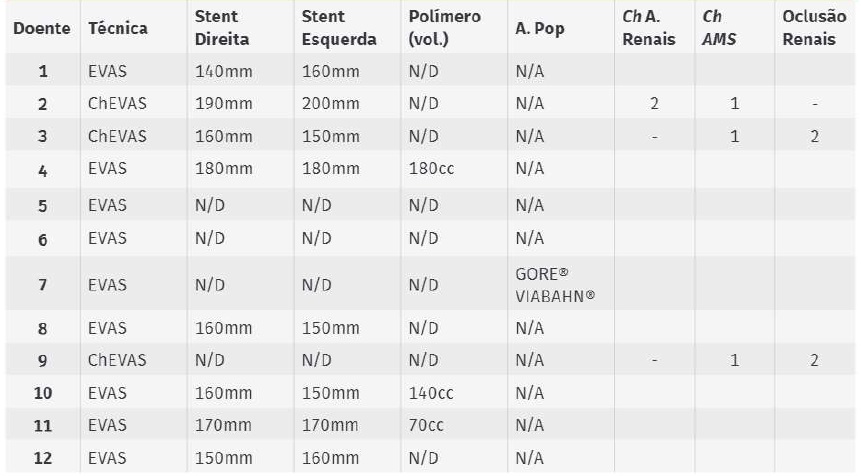
A Tabela 4 resume a técnica cirúrgica utilizada.
Realizaram-se 3 ChEVAS e 9 EVAS sem procedimentos aórticos complementares. Dos ChEVAS, dois foram realizados em contexto eletivo e 1 em contexto urgente (por EL tipo 1a sintomático pós-EVAR). Em dois destes, foi realizada uma chimney para a AMS, com oclusão intencional das artérias renais, por razões anatómicas e por serem doentes com DRC pré-hemodiálise. No terceiro caso, foram colocadas chimneys para as artérias renais e artéria mesentérica superior.
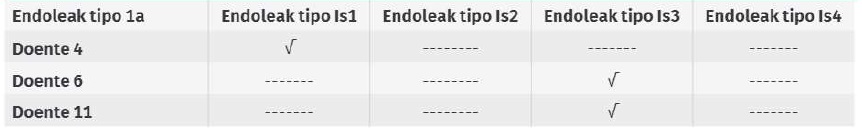
Tabela 6 Classificação dos endoleaks proximais (1a) segundo a classificação de Van Den Ham et al(10)
Os restantes doentes foram submetidos a EVAS em posição infrarrenal, um em contexto urgente. Um dos doentes eletivos foi submetido a exclusão com stent coberto de aneurisma popliteu no mesmo tempo operatório. O comprimento médio dos stents aórticos utilizados foi 160mm. Não foi possível aceder ao volume de polímero utilizado na maioria dos doentes, no entanto, a média dos volumes utilizados disponível foi de 130cc.
A modalidade anestésica mais utilizada foi a anestesia geral 75% (n=9) e nos restantes foi anestesia raquidiana com sedação (n=3).
A taxa de sucesso técnico (definido como correto implante da endoprótese e preenchimento dos endobags, sem endoleaks na angiografia final) foi de 100%. Foram observadas, contudo, duas complicações relacionadas com o acesso femoral percutâneo, por falência do dispositivo de encerramento percutâneo, sendo necessária rafia direta do local de punção, após exposição vascular. Não se verificaram outras complicações imediatas.
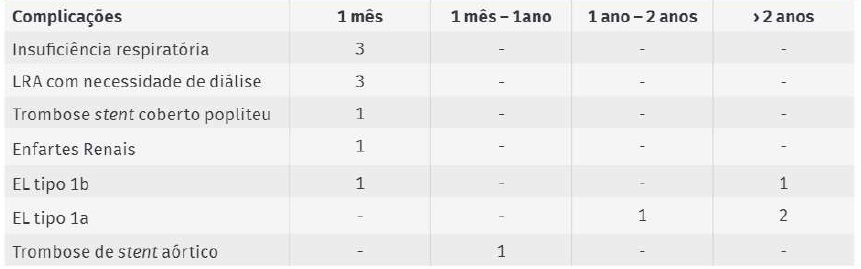
Durante os primeiros 30 dias verificaram-se complicações em 6 doentes. (Tabela 5) Destas, as mais frequentes foram insuficiência respiratória e LRA com necessidade de diálise em 25% (n=3). Salienta-se, que em dois dos casos de LRA, houve oclusão intencional das artérias renais (doentes com doença renal crónica terminal pré-diálise). Observou-se ainda trombose do stent coberto popliteu implantado (n=1), um EL tipo 1b (n=1), detetado em AngioTC pós-operatória e um caso de enfartes renais por embolização (n=1), com chimney renal permeável.
Verificou-se uma reintervenção aos 30 dias, no doente com trombose de stent popliteu e isquémia aguda de membro, sendo submetido a trombólise dirigida por cateter.
Aos 30 dias, verificaram-se dois óbitos. Um, por falência multiorgânica no doente submetido a ChEVAS, em que se detectou endoleak tipo Ib e enfartes renais por embolização na AngioTC, os últimos clinicamente significativos. O endoleak tipo Ib não foi tratado porque o doente manteve-se instável, não estando o endoleak relacionado com a instabilidade clínica. Verificou-se ainda outro óbito neste período, por infecção respiratória, num doente submetido a ChEVAS.
Após os 30 dias, observaram-se complicações relacionadas com a endoprótese em 4 doentes. Aos 2 meses de follow-up, verificou-se trombose de um stent aórtico num doente, tendo sido submetido a pontagem femoral cruzada. Em três doentes, no follow-up imagiológico, foi detetado EL tipo 1a aos 20, 30 e 36 meses, respetivamente. Um destes doentes apresentava concomitantemente endoleak tipo 1b. Segundo a classificação de van den Ham et al. para os endoleaks proximais, dois doentes apresentavam EL tipo Is3 (presença de contraste ou trombo fresco entre os endobags ou dentro do saco aneurismático) e um EL tipo Is1 (presença de contraste entre os endobags e a parede do colo proximal, porém sem contraste no saco aneurismático) (Tabela 6). Um dos doentes com EL tipo 1a foi submetido a explantação protésica e reconstrução em pontagem aorto-bi-femoral, com morte no período peri-operatório precoce por insuficiência respiratória secundária a pneumonia e ARDS (acute respiratory distress syndrome).
Dois doentes estão a aguardar intervenção cirúrgica por EL tipo 1a e 1b (Tabelas 7 e 8).
O diâmetro médio do aneurisma no último exame de imagem ou pré-reintervenção é 59±10mm.
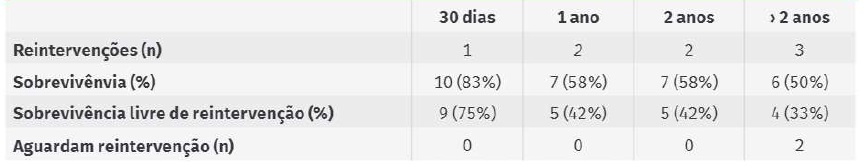
A mediana de follow-up é 2,3(±1.6) anos. Durante o follow-up, verificou-se o óbito em 6 doentes, com uma sobrevivência aos 2 anos de 60% (SE=.154). Como anteriormente referido, dois destes óbitos ocorreram nos primeiros 30 dias pós-operatórios. Após os 30 dias verificaram-se 4 óbitos, 3 destes durante o primeiro ano após cirurgia e outro, como anteriormente referido, após reintervenção por EL tipo 1a, quatro anos após a cirurgia inicial. Um dos óbitos deveu-se a múltiplas complicações médicas após a primeira intervenção, tendo um internamento prolongado com óbito ao 51º dia pós cirurgia. Em dois doentes, pelo facto do óbito se ter verificado noutra instituição de saúde, não foi possível avaliar a sua causa.
Exceptuando a trombose de stent aórtico, o diagnóstico de complicações relacionadas com o aneurisma após os 30 dias deu-se predominantemente a partir do segundo ano de cirurgia, tendo sido observados endoleaks tipo 1a e/ou 1b em 3 doentes.
Discussão
Nesta análise retrospetiva dos casos de EVAS realizados na nossa instituição, apesar do sucesso técnico de 100%, verificou-se um elevado número de complicações e mortalidade a curto prazo com mortalidade aos 30 dias de 16% (n=2) e intra-hospitalar de 25% (n=3), sendo que em um dos óbitos se verificaram complicações precoces da endoprótese e relacionadas com o procedimento (El tipo 1b e enfartes renais por embolização). A médio e longo prazo, particularmente a partir do 2º ano pós-operatório, verificou-se uma taxa elevada de complicações da endoprótese, sendo o EL tipo 1a (n=3) a mais frequente.
Um dos fatores limitantes do EVAR é a durabilidade a longo prazo e a necessidade de intervenções secundárias(3), e a endoprótese Nellix® foi concebida com o intuito da redução do risco de EL decorrentes do tratamento endovascular de aneurismas da aorta abdominal. Os resultados iniciais dos registos globais desta endoprótese apresentaram resultados promissores, com taxas de EL na ordem dos 3-5% no final do primeiro ano após implantação(2,4). O estudo ASCEND, que reporta os resultados da utilização off-label de ChEVAS no tratamento de AAA para- e juxta-renais, reporta uma sobrevivência livre de endoleaks de 94.2% no primeiro ano(5). Reijnen et al, numa série de 58 doentes, reportam taxas de mortalidade e de reintervenção a 30 dias não inferiores ao EVAR, mesmo com elevada taxa de utilização fora das IFU (em cerca de 50% casos)(6). Por estes resultados promissores, verificou-se uma generalização rápida na utilização desta prótese, com elevada taxa de utilização fora das IFU.
No entanto, a experiência demonstrou que as complicações relacionadas com o aneurisma são mais comuns do que o inicialmente previsto, e com abordagens terapêuticas mais complexas do que no caso do EVAR convencional. Harrison et al reportam complicações frequentes, particularmente após os dois anos pós-implantação, referindo que metade dos pacientes que sobrevivem mais do que 3 anos apresentam complicações relacionadas com a endoprótese(7).
Os nossos resultados são sobreponíveis ao reportado por diversos autores e refletem uma evolução desfavorável a médio e longo prazo da endoprótese Nellix®, apesar de uma baixa taxa de complicações técnicas precoces(7,8). Apesar de não ter sido avaliada na nossa amostra, estão descritos na literatura vários mecanismos de falência a médio/longo prazo, sendo o mais frequente a migração protésica caudal com consequente EL tipo 1a(8). Não existem abordagens standardizadas no tratamento desta complicação. As abordagens descritas incluem embolização com coils e/ou Onyx®, extensão proximal Nellix-in-Nellix com/sem chimneys ou cirurgia convencional com explantação protésica e reconstrução in situ ou extra-anatómica(9). Apesar de atualmente não estar disponível o seu uso livre, seria potencialmente benéfica a disponibilidade desta endoprótese em casos selecionados, particularmente naqueles doentes com complicações de um EVAS previamente implantado e com comorbilidades proibitivas para cirurgia convencional, e nos quais uma eventual extensão Nellix-in-Nellix, apesar dos riscos conhecidos, seja a única solução fisiologicamente comportável pelo doente.
Quanto à vigilância pós-operatória, não existe nenhum esquema específico para esta endoprótese reportado na literatura. Face à nossa experiência e a de outros autores, e associado aos mecanismos de endoleak específicos desta endoprótese, em particular os proximais, a vigilância através da utilização de eco-doppler isoladamente parece ineficaz. Assim, a ausência de endoleak objetivável em eco-doppler não exclui a presença de falência proximal da endoprótese, visto a presença de novo e/ou aumento do volume de trombo entre a parede aórtica e os endobags e/ou entre os endobags (associado a separação dos mesmos) serem o reflexo de um endoleak proximal. A partir dos dois anos de pós-operatório, intervalo a partir do qual se verifica o maior número de complicações tardias relacionadas com a endoprótese, o follow-up semestral utilizando eco-doppler associado a radiografia abdominal (para detecção de migração protésica caudal, mecanismo mais frequente) pode ser uma hipótese razoável, em particular nos doentes com doença renal crónica e/ou alergia ao contraste. No entanto, a angiotomografia computorizada é o exame de eleição para vigilância destes doentes.
Por fim, a referir como principais fatores limitantes deste estudo a sua natureza retrospetiva, bem como o baixo número de doentes incluídos e inclusão de aneurismas com características anatómicas diferentes.
Conclusões
Na nossa instituição, a utilização da endoprótese Nellix® está associada a elevada taxa de complicações peri-operatórias e médio prazo, com elevada taxa de complicações relacionadas com o aneurisma, sendo o endoleak tipo 1A a mais frequente. Assim, deve promover-se um plano de vigilância intensiva a este subgrupo de doentes para deteção precoce de complicações, e deve ser oferecido a estes doentes medidas terapêuticas quer endovasculares, quer convencionais, adequadas às suas expectativas e comorbilidades.