INTRODUÇÃO
A pele sensível é uma queixa dermatológica frequente na população geral. Embora inicialmente considerada uma condição puramente cosmética ou psicossomática, a pele sensível tem sido objeto de estudo nos últimos anos e, atualmente, a designação de síndrome de pele sensível (SPS) está amplamente difundida na literatura. Esta síndrome é atualmente considerada uma entidade clínica específica, com sintomas e fatores desencadeantes característicos. A SPS merece ser identificada e tratada, pois tem um elevado impacto na qualidade de vida dos doentes. O objetivo deste artigo é efetuar uma revisão da literatura sobre esta síndrome muitas vezes esquecida, negligenciada ou desconhecida, e fornecer um algoritmo prático para o diagnóstico e tratamento.
Definição e Classificação
A definição mais recente de SPS, e a primeira a receber um con-senso internacional, foi apresentada em 2017, no Fórum Internacional do Estudo do Prurido.1 O grupo de estudo propôs a seguinte definição: síndrome definida pela ocorrência de sensações desagradáveis (de picada, ardor, dor, prurido ou dormência) após a exposição da pele a estímulos físicos, químicos ou térmicos que normalmente não causariam estes sintomas. Estas sensações desagradáveis não podem ser explicadas por outra doença cutânea. A pele pode parecer objetivamente normal ou acompanhar-se de eritema, e pode ocorrer em qualquer local, sendo mais frequente na face.1
Mais recentemente houve necessidade de distinguir a SPS da sensibilidade seletiva a produtos específicos. Nesse sentido, Misery propôs o termo “pele reativa” para substituir “pele sensível”. Embora este novo termo seja mais preciso no que diz respeito à etiologia e fisiopatologia da doença, a expressão “pele sensível” continua a ser mais difundida e utilizada.1
Epidemiologia
A SPS é muito frequente. A prevalência estimada no Japão, Europa e Estados Unidos da América é de 50% das mulheres e 30% dos homens, com uma distribuição semelhante entre os vários países (Tabela 1).2-5A maior parte destes estudos baseia-se em entrevistas telefónicas e na avaliação subjetiva dos doentes e não numa observação objetiva por um dermatologista. A prevalência de pele sensível em doentes com dermatoses pré-existentes poderá ser ainda superior. Por exemplo, 83,6% das mulheres com dermatite atópica refere ter pele sensível e a prevalência em doentes com rosácea pode ser até 100%.6
Tabela 1 Frequência de pele sensível em diferentes países.
| País | Pele Sensível (%) |
|---|---|
| Japão | 54,47 |
| Itália | 53,8 |
| França | 51,9 |
| EUA | 44,6 |
| Rússia | 39,72 |
| Alemanha | 35,6 |
| Brasil | 34,22 |
| Espanha | 31,6 |
| Suiça | 30,8 |
| Grécia | 29,8 |
| Portugal | 27,4 |
| Bélgica | 25,8 |
Adaptado de Taieb C, et al. Sensitive skin in Brazil and Russia: an epidemiologi-cal and comparative approach. Eur J Dermatol. 2014;24:372-6.5
A SPS é mais frequente em idades mais jovens2,4e as mulheres parecem ser mais afetadas do que os homens.1,4,7A síndrome é mais comum nos fotótipos mais baixos,2,7,8e a prevalência é mais alta no verão.9 Não parece existir correlação com o ambiente rural, urbano ou classe sócio-económica.1 A SPS é também mais frequente em doentes com diabetes mellitus, insulinorresistência e obesidade, provavelmente pela disfunção epidérmica e do sistema nervoso autónomo a que estas condições estão associadas.6 A associação entre SPS e síndrome do intestino irritável também já foi descrita.10
Fisiopatologia
A fisiopatologia da SPS ainda é pouco compreendida. A evidência atual sugere que indivíduos com pele sensível têm uma ou mais das seguintes alterações cutâneas: diminuição da função de barreira epidérmica, disfunção neurossensorial e disfunção imunológica.1,11,12Estas alterações contribuem para o desenvolvimento dos sintomas habituais da SPS quando a pele entra em contacto com estímulos agressores. Estes estímulos podem ser exógenos - físicos (luz ultravioleta, vento, humidade e poluição), térmicos (frio e calor) e químicos (cosméticos) - ou endógenos, relacionados com a alimentação, stress ou fatores hormonais.13Num estudo realizado na China, as mulheres foram mais sensíveis a estímulos ambientais, como o sol e humidade, e os homens foram mais sensíveis a estímulos emocionais.11
Diminuição da função de barreira epidérmica
A integridade da barreira epidérmica é essencial à manutenção da estrutura e funções da pele. Para muitos autores, a disfunção desta barreira, resultando numa camada córnea mais fina e permeável, está na origem da SPS.14,15Esta barreira epidérmica incompetente facilita a permeabilidade cutânea de irritantes e alergénios, torna as fibras nervosas intraepidérmicas desprotegidas e aumenta a perda transepidérmica de água.1,9,13,16Todos estes fatores poderiam explicar os sintomas da SPS.
A causa desta disfunção da epiderme não está estabelecida. Uma das hipóteses é existir uma alteração da composição lipídica da epiderme. De facto, alguns estudos demonstraram que a pele sensível tem menos lípidos neutros, esfingolípidos e ceramidas do que a pele normal.1 Num estudo com espetrometria de massa e cromatografia, indivíduos com SPS a nível do couro cabeludo revelaram um aumento do pH, da produção de sebo e da concentração de porfirinas, bem como uma disrupção do microbioma com aumento da proliferação de Cutibacterium e menor diversidade bacteriana, em comparação com indivíduos saudáveis.17Em contrapartida, outros estudos mostraram características biofísicas e composição química semelhantes entre indivíduos com pele sensível e indivíduos com pele normal.8,11Por exemplo, um estudo que utilizou a microespetroscopia confocal para avaliar a espessura da camada córnea e a quantidade de ácidos gordos e ceramidas não revelou diferenças significativas entre os dois grupos.8,11Estes autores argumentam que a SPS se deve sobretudo a uma disfunção neurossensorial na pele.
Disfunção neurossensorial
O papel da disfunção neurossensorial na fisiopatologia da SPS tem sido cada vez mais salientado. Para muitos autores, trata-se de uma neuropatia de pequenas fibras.18As neuropatias de pequenas fibras são um grupo de doenças que afeta pequenas fibras Aδ mielinizadas e fibras-C não-mielinizadas.18 Alguns estu-dos demonstraram que a diminuição da função da barreira epidérmica resulta num dano às fibras nervosas intraepidérmicas, especialmente das fibras-C peptidérgicas, em doentes com SPS.8,11,18As fibras-C estão envolvidas na transmissão da dor, prurido e temperatura.8 Esta diminuição da densidade de fibras nervosas causaria uma hiperreatividade das fibras nervosas remanescentes, explicando, assim, os sintomas da SPS.11
Um dos focos de maior interesse no estudo da fisiopatologia da SPS está nos chamados canais de potenciais recetores transitórios (TRP). Os canais TRP são expressos em vários tipos de tecidos e estão envolvidos na homeostasia e proliferação celular, função secretória endócrina e exócrina e mecanismos imunológicos e inflamatórios.10O papel do TRP vanilóide 1 (TRPV1) na inflamação neurogénica e na patogénese da pele sensível tem sido extensamente estudado.4 Este recetor, expresso principalmente nos queratinócitos, é estimulado por químicos, calor, frio, forças mecânicas e pela capsaicina, e atua como sensor celular, com papel na perceção da dor e do prurido e na inflamação cutânea.4,13A expressão de TRPV1 parece estar aumentada em doentes com SPS e parece correlacionar-se diretamente com a intensidade dos sintomas.16 Outros TRP menos estudados, mas que também podem ser relevantes na patogénese da SPS, incluem: TRP melastatina 8 (TRPM8) e o TRP anquirina 1 (TRPA1), expressos essencialmente nos neurónios sensitivos e estimulados pelo frio e por substâncias como o mentol4,13; o TRPV3, estimulado pelo calor e pela cânfora; e o TRPV4, estimulado pelo calor, por forças mecânicas e por stress hipoosmótico.10
Disfunção imunológica
A ativação dos canais TRPV1 na pele reativa despoleta a libertação de substância P e de outros neuropéptidos e, consequentemente, de citocinas pró-inflamatórias, tais como a interleucina(IL)-2, fator de necrose tumor alfa, interferão gama, IL-23 e IL-31.19Estas citocinas estimulam a resposta imunológica ao recrutar células do sistema imunitário para a pele. Todos estes fatores podem ser responsáveis pela sensação de ardor e prurido características da SPS.1
Diagnóstico
O diagnóstico de SPS é clínico e baseia-se sobretudo nas queixas relatadas pelo doente. Um diagnóstico formal mais objetivo é dificultado pela falta de consenso relativamente aos testes de diagnóstico.11
História clínica e exame físico
Os sintomas incluem prurido, dor ou sensação de picada, ardor, calor, queimadura ou dormência.4,7Estes sintomas ocorrem minutos a horas após a exposição a um fator desencadeante, como radiação ultravioleta, vento, humidade, poluição, diferenças térmicas ou cosméticos.13 Importa salientar que um cosmético pode desencadear os sintomas mesmo após uso prolongado, por efeito cumulativo.4 Com frequência, os doentes referem sentir a pele seca ou espessada.4 A face é a região mais afetada, especialmente a região nasogeniana, provavelmente porque é local frequente de aplicação de cosméticos e porque a pele é menos espessa e tem maior densidade de fibras nervosas nesta localização.4 Outras regiões frequentemente afetadas são a superfície flexora dos antebraços, mãos, região genital e couro cabeludo.4,17,19,20
Os sintomas podem ser ou não acompanhados de alterações no exame objetivo, como eritema, telangiectasias, xerose ou descamação.2 Na presença de sinais ao exame objetivo, é necessário excluir a presença de uma dermatose primária.4 A presença de sensações desagradáveis na pele, de natureza transitória, após exposição a um estímulo agressor, e um exame objetivo praticamente normal favorecem o diagnóstico de SPS.4
A Tabela 2 mostra o “questionário dos 13-itens”, com as questões que se devem colocar na entrevista ao doente e que permitirão o diagnóstico de SPS. As questões do bloco I avaliam a perceção do doente relativamente à sua pele quanto à sensibilidade, irritação e reatividade, as questões do bloco II avaliam a reação da pele a cosméticos e as questões do bloco III avaliam a reação da pele a fatores ambientais. O diagnóstico de SPS pode ser feito se o doente der uma resposta afirmativa em ≥2 questões do bloco I, nas 3 questões do bloco II ou ≥3 questões do bloco III.1 Este questionário também pode ser utilizado ao longo das consultas para avaliar a eficácia das medidas terapêuticas.11
Existem outros questionários além do “questionário dos 13-itens”. Misery desenvolveu e validou o Sensitive Scale-10 (SS-10) - um questionário de 10 itens, no qual um score a partir dos 20 pontos (numa escala de 0-100) identifica indivíduos com SPS.21
O SS-10 é uma readaptação do SS-14, que foi a primeira escala de quantificação da gravidade da sensibilidade cutânea.11
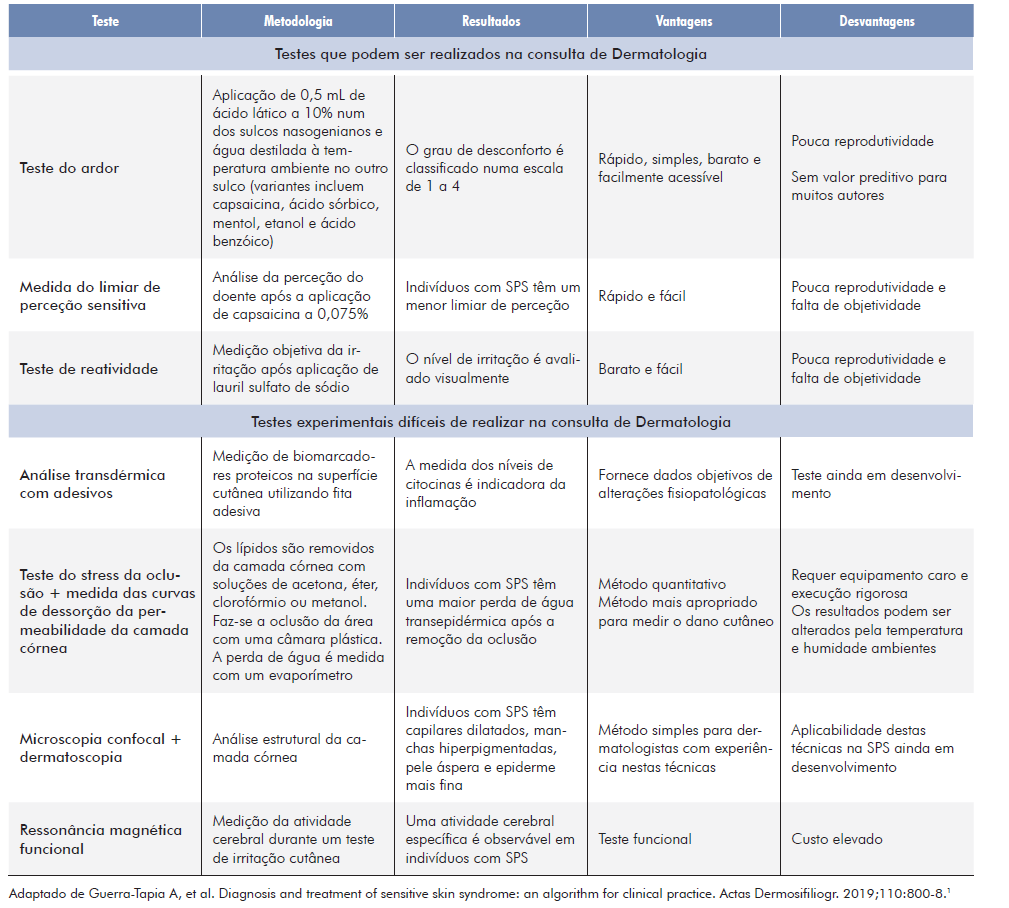
Testes de diagnóstico
Os questionários são o método mais fiável para fazer o diagnóstico de SPS.12 No entanto, existem testes de diagnóstico que podem servir de complemento.1 A Tabela 3 lista estes testes com as suas vantagens e desvantagens. Existem outros testes descritos além dos referidos, sendo que a maioria consiste em aplicar substâncias pouco concentradas relativamente inertes e inócuas (p.e. dimetilsulfóxido, nicotina ou histamina) numa pele normal mas que desencadeiam os sintomas típicos da SPS numa pele de um indivíduo com este diagnóstico.11
Algoritmo de diagnóstico
De seguida, apresenta-se uma sugestão de algoritmo prático para o diagnóstico de SPS (Fig. 1). A falta de estandardização dos exames complementares dificulta o diagnóstico formal da SPS. Por esse motivo, consideramos um resultado positivo para o “questionário dos 13-itens” como suficiente para o diagnóstico.
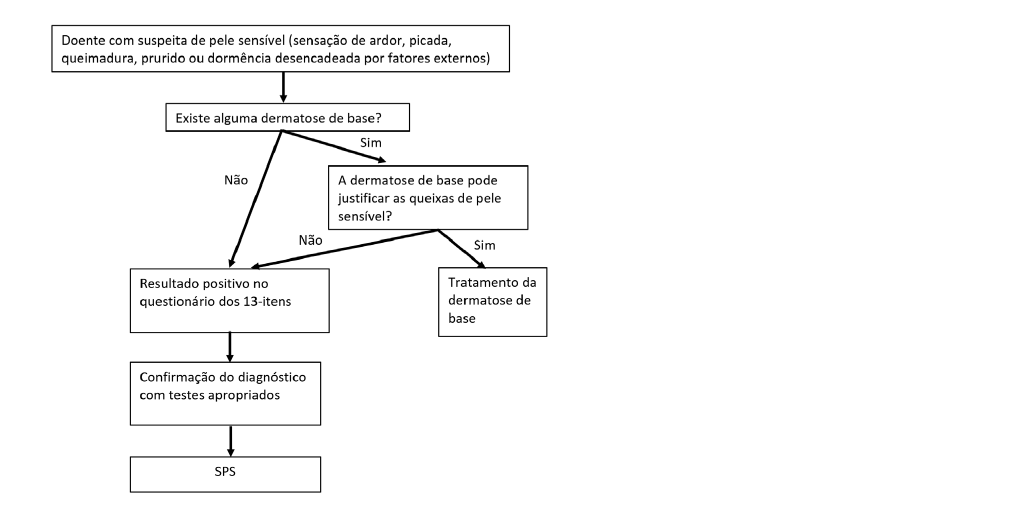
Adaptado de Guerra-Tapia A, et al. Diagnosis and treatment of sensitive skin syndrome: an algorithm for clinical practice. Actas Dermosifiliogr. 2019;110:800-8.1
Figura 1 Algoritmo de diagnóstico de Síndrome da Pele Sensível
Diagnóstico diferencial
A SPS é um diagnóstico de exclusão. Por isso, é necessário excluir outras dermatoses que possam cursar com sinais e sintomas semelhantes. De seguida, apresentam-se as principais dermatoses a excluir.
A rosácea deve ser sempre considerada.11 Esta dermatose caracteriza-se por eritema facial e pode acompanhar-se de sensação de picada ou calor, tal como na SPS. No entanto, na SPS, estas queixas são habitualmente transitórias e despoletadas por um fator desencadeante. As lesões primárias típicas da rosácea (pápulas, pústulas e alterações tróficas) estão ausentes na SPS.
A dermatite de contacto alérgica ou irritativa também é um diagnóstico diferencial importante, mas distingue-se facilmente pela história de contacto recente com uma substância causadora e pelas lesões ao exame objetivo.11 As provas epicutâneas permitem o diagnóstico de dermatite de contacto alérgica e devem ser consideradas na investigação de doentes com suspeita de SPS. Doentes com SPS terão provas negativas.4
A fototoxicidade causada por medicamentos também deve ser incluída no diagnóstico diferencial.11 Esta ocorre quando químicos fotoreativos são ativados pela luz ultravioleta e dão origem a espécies reativas de oxigénio, com consequente irritação cutânea. Existem vários medicamentos fotossensibilizantes, tais como antibióticos (quinolonas, tetraciclinas ou sulfonamidas), agentes antitumorais (5-fluorouracil, vimblastina ou vemurafenib), antidiabéticos (sulfonilureia), antimaláricos (quinina ou cloroquina) e psicofármacos (fenotiazinas, antidepressivos tricíclicos ou imipramina).11Não existem exames complementares facilmente disponíveis em ambiente clínico para confirmar esta fototoxicidade. A substituição por medicamentos de outra classe está recomendada para alívio sintomático e confirmação diagnóstica.
Tratamento
Medidas gerais
Os doentes devem compreender a natureza da SPS de forma a evitar os fatores desencadeantes e a cumprirem as recomendações terapêuticas. Recomenda-se suspender a aplicação de todos os cosméticos, durante pelo menos 2 semanas, e reintroduzir cada um deles de modo faseado para detetar reações adversas e identificar o causador. De um modo geral, o número de cosméticos a utilizar deverá ser reduzido ao mínimo essencial.22 Os doentes devem utilizar roupas largas e confortáveis, evitar alterações súbitas de temperatura, exposição solar excessiva, exposição a fontes de calor e ao vento22 e moderar o consumo de álcool.
Numa fase aguda, os corticóides tópicos de potência baixa e média podem ser aplicados por um período curto, até 5 dias, para alívio sintomático, e os inibidores da calcineurina tópicos podem ser mantidos como tratamento de manutenção, se necessário.11
Tratamento da função de barreira alterada
Os doentes com pele sensível devem utilizar hidratantes adequados, que restaurem a função da barreira epidérmica, reduzindo assim a suscetibilidade à irritação e melhorando os sintomas da SPS.2 A limpeza diária da pele deve ser suave, sem fricção mecânica e sem recurso a exfoliantes.
Os produtos que os doentes aplicam devem:
1. Conter elementos hidratantes com biocompatibilidade, tais como glicerina, ácido hialurónico e elementos relipidantes, como óleos vegetais e ceramidas.1 Um dos ingredientes ativos com interesse no tratamento da SPS é a nicotinamida. Esta molécula promove a síntese de lípidos e de ceramidas pela epiderme, reduz a libertação de mediadores pró-inflamatórios, regula a libertação de histamina e tem propriedades pró-bióticas1;
2. Ter um pH fisiológico (5,5-6)1;
3. Ser formulações minimalistas, isto é, conter apenas os ingredientes essenciais;
4. Conter conservantes com baixo potencial de sensibilização, como parabenos com um comprimento de cadeia lateral de até 3 átomos de carbono (parabenos metil-, etil-, propil- e isopropil parabenos)11;
5. Conter baixa concentração de alergénios e irritantes comuns, como a lanolina, álcoois de lã, cera de lã, veículos voláteis como substâncias derivadas do álcool, perfumes, ácido benzóico, ácido cinâmico, ácido lático, propilenoglicol, ureia ou ácido sórbico.1,11
6. Conter alcanodióis com baixo potencial irritativo, tais como o 1,2-hexanodiol e alquil poliglicosídeos C8, C10, C14 e C1611;
7. Conter surfactantes não irritativos. Os surfactantes anfotéricos e não-iónicos são menos irritativos, mas menos apelativos cosmeticamente porque são pegajosos. De entre os surfactantes mais comuns, o lauril sulfato de sódio tem o maior potencial irritativo, e o cocoil isetionato de sódio é o mais suave. O sabão sintético (syndet) é preferível ao sabão detergente convencional.11
Tratamento da disfunção neurossensorial
O tratamento da hiperatividade neurossensitiva deverá incluir a evicção de tópicos (cosméticos ou medicamentos) que desencadeiem os sintomas de SPS. Atualmente ainda não existem trata-mentos dirigidos às vias de sinalização afetadas na doença, mas estes estão a ser investigados. Os inibidores da TRPV1, como o trans-4-tertbutilciclohexanol e a furocoumarina, mostraram ser eficazes no alívio dos sintomas de SPS.1,4O pimecrolimus também parece agir sobre o TRPV1 e mostrou eficácia num estudo real investigada no tratamento da SPS e mostrou eficácia em estudos clínicos ao inibir a inflamação neurogénica.1 Esta molécula es-timula a produção de endorfinas e encefalinas nos queratinócitos e contribui para a função de barreira epidérmica, protegendo as fibras-C nervosas.1
CONCLUSÃO
A SPS é atualmente considerada uma entidade específica e o seu diagnóstico pode ser realizado com recurso a questionários. Os testes de diagnóstico atuais podem ser usados como complemento, mas aguardam validação. Os dermatologistas devem estar consciencializados para esta condição altamente prevalente e estar familiarizados com as recomendações terapêuticas.
O que acrescenta ao conhecimento atual esta revisão
A SPS é uma condição clínica muito prevalente à escala global, mas difícil de objetivar. O diagnóstico pode ser realizado com recurso a questionários. Os testes de diagnóstico atuais aguardam validação. Tratamentos dirigidos estão a ser desenvolvidos.