Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Revista Portuguesa de Medicina Geral e Familiar
versão impressa ISSN 2182-5173
Rev Port Med Geral Fam vol.28 no.4 Lisboa jul. 2012
ESTUDOS ORIGINAIS
Efetividade da vacina antigripal na época 2010-2011 em Portugal: resultados do projeto EuroEVA
Effectiveness of the influenza vaccine in 2010-2011 in Portugal: results from the EuroEVA project
Baltazar Nunes,1 Ausenda Machado,2 Pedro Pechirra,3 Isabel Falcão,4 Paulo Gonçalves,5 Patrícia Conde,6 Raquel Guiomar,6 Inês Batista,8 José Marinho Falcão9
1 Doutor em Probabilidades e Estatística, Instituto Nacional de Saúde Dr Ricardo Jorge (INSA)
2 Engenheira Química, INSA
3 Licenciatura em Biologia, INSA
4 Chefe de Serviço de Medicina Geral e Familiar, Direção-Geral da Saúde
5 Licenciatura em Biologia Aplicada (Biotecnologia), INSA
6 Licenciatura em Engª Biotecnológica, Mestrado em Saúde Pública, INSA
7 Licenciatura em Biologia, INSA
8 Assistente operacional, INSA
9 Chefe de Serviço de Saúde Pública, Epidemiologista, INSA
Endereço para correspondência | Dirección para correspondencia | Correspondence
RESUMO
Objetivos: O estudo EuroEVA (Efetividade da vacina antrigripal na Europa) teve como objetivos estimar a efetividade da vacina antigripal sazonal 2010-2011 na população geral e nos indivíduos com 65 ou mais anos de idade.
Tipo de estudo: Estudo observacional do tipo caso-controlo e método screening
Local: Portugal Continental
População: População portuguesa residente e não institucionalizada sem contra-indicação para a toma da vacina antigripal
Métodos: Foram utilizados dois delineamentos de estudo para estimar a efetividade da vacina (EV): caso-controlo e o método screening. No delineamento caso-controlo, os casos de síndroma gripal (SG) com confirmação laboratorial para o vírus da gripe foram comparados com os casos de SG negativos para o vírus da gripe. A EV foi estimada por 1-odds ratio de estar vacinado nos casos versus controlos, ajustada para efeitos de confundimento por regressão logística. No método screening, a cobertura da vacina antigripal nos casos SG positivo foi comparada com a cobertura estimada na população geral. A EV foi estimada por intermédio da fórmula de Orenstein e ajustada para confundimento pelo método de Farrington.
Resultados: Os resultados indicam que a EV da vacina contra a gripe na época 2010-11 foi de 79% (IC95%, 43% a 94%) no delineamento caso-controlo e de 70% (IC95%, 32% a 87%) pelo método screening. Após ajustamento, a EV decresceu, respetivamente, para 58% (IC95%, -61% a 89%) e 64% (IC95%, 17% a 84%).
Conclusões: As estimativas da EV antigripal obtidas pelos dois métodos foram muito semelhantes e encontram-se entre os valores da EV publicados para a época 2010-11. Os dados recolhidos neste estudo não permitiram obter estimativas da EV específicas para os indivíduos dos grupos alvo da vacinação antigripal. Este facto vem reforçar a necessidade da realização de estudos multicêntricos com protocolo comum, como é o caso do I-MOVE “Monitoring influenza vaccine efectiveness during influenza seasons and pandemics in the European Union”.
Palavras-chave: Investigação Comparativa da Efetividade; Gripe Humana; Vacina Contra a Gripe.
ABSTRACT
Objective: The objectives the EuroEVA study (Influenza vaccine effectiveness in Europe) were to estimate the effectiveness of the seasonal influenza vaccine (VE) in 2010-2011 in the general population and among individuals 65 years of age and older.
Study type: An observational study using the case-control and screening methods
Local: Continental Portugal
Population: The Portuguese population with no contraindications for influenza vaccination
Methods: Two study designs were used to estimate Vaccine Effectiveness (VE): the case-control test-negative design and the screening method. In the test-negative design, influenza-like illness cases (ILI) with laboratory confirmation of infection by the influenza virus were compared with the influenza-like illness cases negative for infection by the influenza virus. The influenza VE was estimated as 1 minus the odds ratio of being vaccinated among the cases versus the controls and adjusted for confounding by logistic regression. In the screening method, the influenza vaccine coverage of the ILI positive cases was compared with coverage estimated in the general population. The influenza VE was estimated using the Orenstein formula and adjusted for confounding by the Farrington method.
Results: The results show that the effectiveness of the influenza vaccine in 2010-2011 was 79% (CI95% 43-94) using the test-negative design and 70% (95%CI 32%-87%) using the screening method. After adjusting for confounders, the VE decreased respectively to 58% (95%CI -61%-89%) and 64% (95%CI 17%-84%).
Conclusions: The estimates of the influenza vaccine effectiveness obtained by the two methods were similar and are within the values published in other studies conducted during the 2010-2011 season. The present study was unable to estimate the VE in the target groups for influenza vaccination. These results strengthen the need for international multicentre studies with a common protocol such as I-MOVE (Monitoring influenza vaccine efectiveness during influenza seasons and pandemics in the European Union).
Key-words: Comparative Effectiveness Research; Human Influenza; Influenza Vaccines.
Introdução
Anualmente o vírus da gripe é responsável por epidemias que afetam as populações humanas, originando infeções respiratórias normalmente benignas mas que podem ter repercussões elevadas na saúde dos indivíduos. Em termos de impacto, estima-se que as epidemias de gripe sejam responsáveis por excessos de consultas em cuidados primários, que podem variar entre 0,4% (Portugal)1 e 1,4%2 (Holanda) da população geral. Igualmente de referir são os efeitos da gripe no funcionamento dos serviços de saúde, no tratamento de complicações da gripe, bem como o impacto económico decorrente de um grande número de casos com diagnóstico leve a moderado que resulta em absentismo laboral e escolar e consequente perda de produção.3
Em Portugal, o Instituto Nacional de Saúde Dr. Ricardo Jorge (INSA) calculou, com base na rede Médicos--Sentinela, que a percentagem de indivíduos da população idosa que desenvolvem síndroma gripal por época variou entre 1,8% e 6,0%, no período de 1998-99 a 2006-07.4 Adicionalmente estima-se que as epidemias de gripe sazonal estejam associadas a um excesso médio de anual de 24,7 óbitos por 100.000 habitantes, dos quais 90% correspondem a indivíduos com 65 ou mais anos de idade.5
Grupos específicos da população têm um risco elevado de complicações devidas à infeção pelo vírus influenza. Pertencem ao grupo de alto risco os indivíduos com 65 e mais anos de idade, bem como aqueles que sofrem de doenças crónicas, nomeadamente de diabetes, doença cardiovascular, doença hepática crónica, doença renal crónica, doença respiratória crónica e os imunocomprometidos. A vacinação antigripal anual no Outono é recomendada para estes grupos na maioria dos países da União Europeia, pois corresponde a uma das principais medidas de mitigação da gripe, sendo reconhecido o seu papel na redução do risco de contágio da doença e de ocorrência das respetivas complicações.6-8
A constante evolução dos vírus influenza obriga à reformulação da composição da vacina em cada ano.9 A efetividade da vacina antigripal deve, assim, ser estimada anualmente no início da época de vigilância da gripe e monitorizada ao longo do período epidémico (ou eventual período pandémico).
A estimativa da efetividade da vacina antigripal reveste-se de grande importância, pois pode influenciar decisões na recomendação da vacina, identificar segmentos da população onde a efetividade é menor, identificar e responder a casos de falha da vacina e ainda contribuir para a avaliação dos efeitos adversos após vacinação.10
Neste contexto, o INSA tem participado desde 2008 no projecto europeu multicêntrico (I-MOVE – “Monitoring influenza vaccine efectiveness during influenza seasons and pandemics in the European Union”).11,12 Este projecto, coordenado pela EpiConcept SARL e financiado pelo European Centre for Disease Prevention and Control, tem como objetivo estimar a efectividade da vacina antigripal sazonal e pandémica durante e após cada época de gripe. O projecto I-MOVE é formado por um consórcio de 20 institutos de saúde pública europeus, 11 dos quais se encontram a desenvolver estudos de efetividade da vacina antigripal.
No âmbito deste projeto europeu, foram implementados estudos com diferentes delineamentos (coorte, caso-controlo e método screening).13 No que respeita aos estudos caso-controlo, os países participantes desenvolveram e aplicaram anualmente um protocolo de investigação comum14 permitindo, assim, no contexto de um estudo multicêntrico, o cálculo de uma estimativa comum da efectividade da vacina.
A componente portuguesa do estudo I-MOVE tomou a designação de “EuroEVA” e iniciou-se na época 2008-09 com um estudo piloto que visava avaliar a adequabilidade do desenho caso-controlo, com diferentes grupos de controlo, no estudo da efetividade da vacina antigripal sazonal em individos com 65 e mais anos.15 Os resultados obtidos demonstraram a exequibilidade do delineamento utilizado embora a dimensão da amostra recrutada no âmbito do projecto EuroEVA fosse reduzida e só permitisse obter estimativas da efetividade da vacina com intervalos de confiança muito amplos.16,17 No entanto, a conjugação dos resultados obtidos no contexto do estudo caso-controlo multicêntrico (Portugal, Espanha, Dinamarca, Hungria e Roménia) permitiu estimar a EV antigripal nos indivíduos com 65 ou mais anos de idade em 59% (IC95%, 15% a 80%), ajustada para efeitos de confundimento.18
Durante a época de gripe de 2009-2010, o protocolo comum foi melhorado e implementado em Portugal através do EuroEVA. O objetivo foi estimar não só a efetividade da vacina contra a gripe sazonal mas também contra a gripe pandémica, respetivamente, para os idosos (65 e mais anos) e para todas as idades. Naquela época, no âmbito do projecto EuroEVA, não foi possível estimar a EV pandémica ou sazonal em Portugal uma vez que no estudo não ocorreram falhas da vacina.19 No entanto, no âmbito do estudo caso-controlo multicêntrico (Portugal, Espanha, Irlanda, França, Itália, Hungria e Roménia) obteve-se uma estimativa da EV pandémica de 72% (IC95%, 46% a 86%) contra a gripe confirmada laboratorialmente.20
Para a época 2010-11, o projecto I-MOVE voltou a lançar o estudo caso-controlo multicêntrico, contando com a participação de Portugal, Espanha, Itália, França, Polónia, Hungria, Irlanda e Roménia. Pretendia-se, à semelhança dos anos anteriores, estimar a efectividade da vacina sazonal.
No presente artigo descreve-se a componente portuguesa (EuroEVA) do estudo I-MOVE na época 2010-11, que teve como objectivo estimar a efectividade da vacina antigripal sazonal 2010-11 contra a gripe, na população geral e nos individuos com 65 e mais anos.
Métodos
No estudo EuroEVA 2010-2011 foram utilizadas duas abordagens: caso-controlo, onde casos de síndroma gripal confirmados laboratorialmente (SG+) para a presença de vírus da gripe foram comparados com os casos de síndroma gripal com resultado laboratorial negativo para o vírus da gripe e o método screening, onde a cobertura da vacina antigripal nos casos SG+ foi comparada com a cobertura da vacina na população geral. O estudo EuroEVA decorreu entre a 45.a semana de 2010 e a 11.a semana de 2011.
Método caso-controlo teste negativo
A população em estudo correspondeu ao conjunto de indivíduos não institucionalizados residentes em Portugal sem contra indicação para a toma da vacina da gripe.
A dimensão total da amostra foi estabelecida tendo em conta o objetivo principal do estudo, ou seja, estimar a EV antigripal. O número total de casos de SG a selecionar era de 320, dos quais 130 seriam casos e 190 controlos negativos. Estes valores foram calculados de forma a estimar uma EV antigripal de 70% com um limite inferior do intervalo de confiança a 95% igual a 35%, assumindo que a cobertura da vacina antigripal nos controlos seria de 20% e que a proporção de casos de SG positivos para o vírus da gripe seria 40%. Para este efeito utilizou-se uma adaptação da fórmula de Lemeshow, Hosmer and Klar (1988).21
A seleção da amostra teve como base de amostragem inicial a Rede Médicos-Sentinela (MS),22 que consiste numa rede de médicos de família (MF), cuja atividade profissional se desenvolve em Centros de Saúde do Serviço Nacional de Saúde (SNS) e que, voluntariamente, notificam casos ou episódios de doença e de outras situações relacionadas com saúde dos indivíduos inscritos nas respetivas listas de utentes. No ano de 2010 estavam inscritos nesta rede 152 MF, colocados nos 18 distritos do Continente e nas Regiões Autónomas dos Açores e da Madeira. A Rede MS foi escolhida para a base de amostragem devido à sua longa experiência (desde 1989) na vigilância epidemiológica da gripe.
A amostra de casos de síndroma gripal foi selecionada em duas etapas:
1. Foram selecionados e contactados MF inscritos na base de dados da Rede MS (participantes atuais e ex-participantes) e na base de dados de participantes dos estudos EuroEVA anteriores. Aos médicos que aceitaram participar foi-lhes pedido, também, que indicassem outros colegas interessados;
2. Cada médico participante selecionou, por semana, os primeiros dois casos de síndroma gripal, com menos de 65 anos e ainda todos os casos de SG com 65 ou mais anos de idade. A definição de caso de SG utilizada foi a da União Europeia,23 que consiste na apresentação obrigatória de início súbito dos sintomas (em menos de 24 horas) e pelo menos um sintoma sistémico (febre ou febrícula, mal estar, debilidade ou prostração, cefaleias, mialgias ou dores generalizadas) e pelo menos um sintoma respiratório (tosse, dor de garganta ou inflamação da mucosa nasofaríngea sem outros sinais respiratórios relevantes ou dificuldade respiratória);
3. Os MF participantes recebiam um sms semanal para efeito de recordatória para a recolha de casos.
A cada utente com SG que aceitou participar no estudo e após obtenção do consentimento informado, foi colhido um exsudado nasofaríngeo, enviado num prazo de 24 horas para o Laboratório Nacional de Referência para o Vírus da Gripe no INSA, para deteção do vírus da gripe através de métodos moleculares (real-time reverse transcription-polymerase chain reaction, RT-rtPCR).
Adicionalmente, o MF recolheu, através de um breve questionário, informação sobre a idade, sexo, características clínicas do SG, o estado vacinal na época 2010-11 e 2009-10 e potenciais fatores de confundimento (história tabágica, presença de doenças crónicas, estado funcional, nível educacional, número de consultas de MF nos últimos 12 meses). Esta informação era recolhida perguntando diretamente ao doente ou por consulta do ficheiro clínico pelo MF. Foram considerados como vacinados os indivíduos que receberam uma dose da vacina trivalente 2010-11 pelo menos 14 dias antes do início de sintomas.
Os casos de SG com confirmação laboratorial de infeção pelo vírus da gripe (casos) foram comparados com os casos de SG com resultado negativo para o vírus da gripe (controlos). Para além desta comparação, foi ainda realizada comparação entre os casos positivos para vírus do tipo B (Casos B), vírus do tipo A(H1N1)pdm09 (Casos A(H1N1)pdm09) e os controlos negativos.
As características gerais foram comparadas entre casos e controlos utilizando os testes de Qui-quadrado e Exato de Fisher (variáveis categóricas) e o teste não paramétrico de Mann-Whitney (variáveis numéricas). A efetividade da vacina foi estimada como 1-odds ratio (OR) de estar vacinado nos casos vs controlos.
Calcularam-se estimativas brutas e ajustadas para os fatores de confundimento estudados através de regressão logística não condicional. No modelo de regressão logística foram incluídos todos os fatores de confundimento que alteraram o OR bruto em pelo menos 10% após ajustamento pelo método de Mantel Haenszel.
Método screening
Nesta componente do estudo a efetividade da vacina antigripal sazonal foi determinada através da comparação da cobertura da vacina nos casos de SG e SG+ com a cobertura da vacina na população geral, através da fórmula de Orenstein.24 De referir que nesta componente também foi calculada a EV antigripal contra o síndroma gripal, ou seja apenas com diagnóstico clínico.
A amostra de casos de SG e SG+ foi obtida através do estudo caso-controlo teste negativo (descrito atrás). A cobertura da vacina na população geral foi estimada com base na amostra ECOS (“Em Casa Observamos Saúde”), uma amostra aleatória de unidades de alojamento do continente estratificada por região NUTS II com alocação homogénea. Uma descrição mais detalhada da metodologia pode ser encontrada em Nunes et al. (2004).25
A EV ajustada para fatores de confundimento foi determinada através do método de Farrington.24 Para todos os testes estatísticos aplicados e intervalos de confiança calculados foi estabelecido o nível de significância de 5%. Quando necessário, o nível de significância foi corrigido para as comparações múltiplas pelo método de Bonferroni. Todos os resultados apresentados foram obtidos com o pacote de programas estatísticos STATA SE 11.26
O protocolo de investigação do estudo EuroEVA 2010-2011 foi submetido e aprovado pela Comissão de Ética do INSA e pela Comissão Nacional de Proteção de Dados.
Resultados
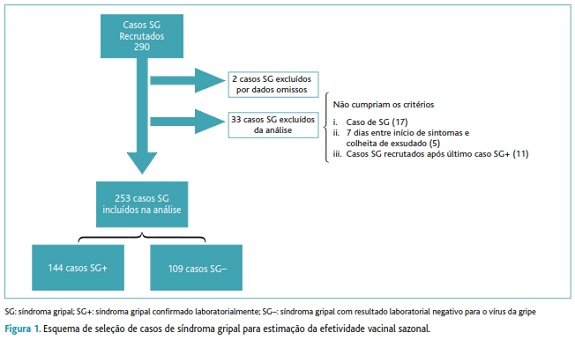
Nesta época 2010-2011, aceitaram participar no projeto EuroEVA 58 MF, dos quais 35 reportaram casos de SG, correspondendo a uma taxa de participação de 60%. Durante o período de estudo, da semana 45/2010 à semana 11/2011, foram recrutados 290 casos de SG. Na figura 1 encontra-se representado o esquema de seleção.
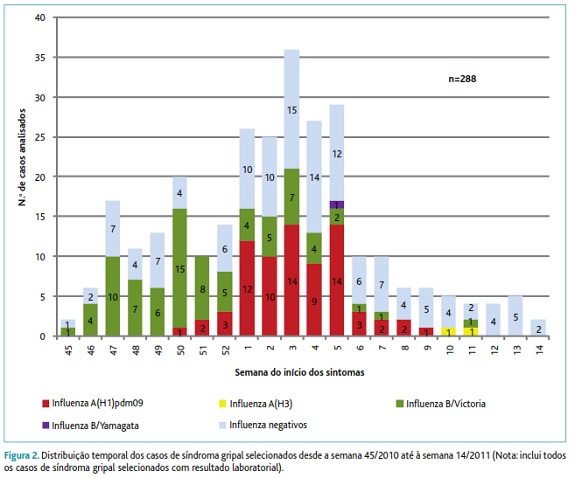
A percentagem de SG positivos para o vírus da gripe foi de 57%. De entre os casos positivos, 73 foram positivos para o vírus do tipo B, 69 para vírus do tipo A(H1N1)pdm09 e 2 para o tipo A(H3N1). A distribuição temporal dos casos de SG recrutados, de acordo com o respetivo resultado laboratorial, encontra-se detalhada na figura 2.
Caso-controlo teste negativo
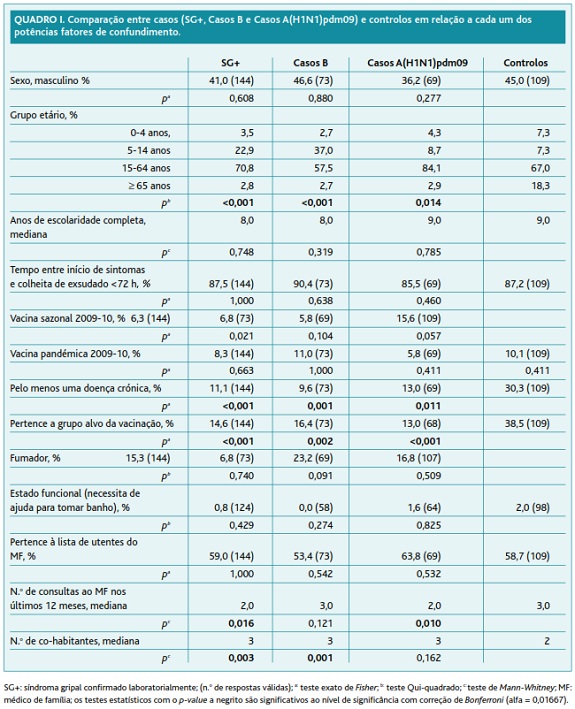
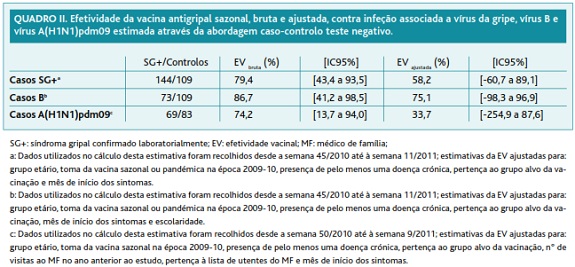
No quadro I encontra-se a comparação das características gerais dos casos e controlos, onde se observam algumas diferenças estatisticamente significativas, nomeadamente: os casos SG+ e os Casos B são mais novos que os controlos em análise; a cobertura da vacina sazonal 2009-10, a prevalência de doença crónica, a percentagem de doentes pertencentes ao grupo alvo da vacinação e a mediana do número de visitas ao MF nos últimos 12 meses foram inferiores nos casos em comparação com os controlos; por outro lado, a mediana do número de co-habitantes foi mais elevada nos casos do que nos controlos.
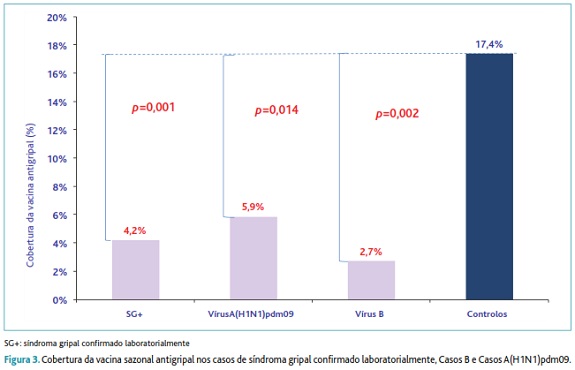
Em relação à exposição em estudo (toma da vacina sazonal 14 dias antes do início dos sintomas de SG), verifica-se que a cobertura da vacina nos controlos era significativamente mais elevada (17,4%) do que nos casos SG+ (4,2%), Casos B (2,7%) e Casos A (H1N1)pdm09 (5,9%) (figura 3).
Relativamente ao objetivo principal deste estudo, foram calculadas as estimativas brutas da EV antigripal, considerando como variável dependente os casos SG+, e por tipo de vírus: Casos B e Casos A(H1N1)pdm09. Os resultados obtidos situam a estimativa pontual da EV bruta entre os 74,2% (contra a infeção por vírus A(H1N1)pdm09) e 86,7% (contra a infeção por vírus B), valores estatisticamente significativos (quadro II).
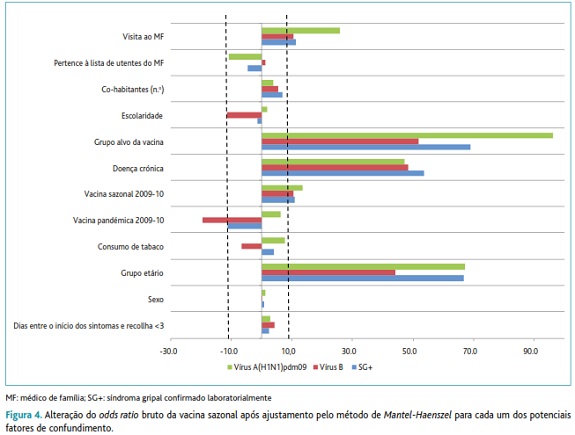
Para obter estimativas da EV ajustadas, procedeu-se à análise dos potenciais fatores de confundimento que, após ajustamento pelo método de Mantel-Haenszel, alteravam em pelo menos 10% o OR bruto da vacina sazonal antigripal 2010-11. O resultado desta análise encontra-se na figura 4, verificando-se que o efeito de confundimento dos fatores estudados varia de acordo com o tipo de vírus da gripe associado à infeção. De uma forma geral, os factores que mais contribuíram para alterar o OR bruto foram o grupo etário, ter pelo menos uma doença crónica e pertencer ao grupo alvo da vacinação. O não ajustamento para estes três fatores de confundimento levaria a uma sobre-estimação da EV antigripal, podendo estes ser considerados como fatores de confundimento positivos. Este resultado é transversal a todos os tipos de caso de gripe em análise, i.e., caso SG+, Casos B e Casos A(H1N1)pdm09. Adicionalmente, outros fatores, como a escolaridade e toma da vacina pandémica em 2009-10, surgiram como potenciais fatores de confundimento para a associação com a infeção pelo vírus da gripe do tipo B.
No quadro II apresentam-se as estimativas da EV antigripal sazonal ajustadas por regressão logística e respetivos intervalos de confiança a 95%. Nenhumas das EV ajustadas podem ser consideradas estatisticamente significativas.
Método screening
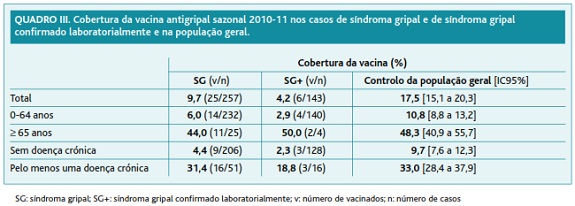
Na amostra ECOS da época 2010-11 (na qual foram inquiridas 903 unidades de alojamento, correspondendo a 2684 indivíduos), a cobertura da vacina foi de 17,5% (IC95%, 15,1% a 20,3%).27 Tendo em conta esta abordagem e para todos os indivíduos, mais uma vez se verificou que a cobertura da vacina nos controlos (na população geral) foi superior à cobertura nos casos SG e SG+ (quadro III).
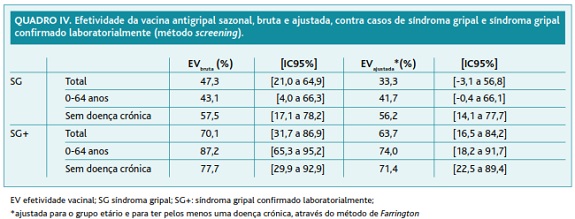
Tendo em conta os resultados anteriores, foram determinadas estimativas da EV (valores brutos e ajustados) para casos de SG e casos SG+. Os resultados (quadro IV) indicam que, após ajustamento para fatores de confundimento (idade e ter pelo menos uma doença crónica), as estimativas da EV decresceram de forma considerável. Dada a reduzida dimensão da amostra de SG e SG+, não foi possível calcular as EV para os indivíduos do grupo alvo da vacinação, os idosos e os que tinham, pelo menos, uma doença crónica.
Discussão
Após ajustamento para potenciais fatores de confundimento, a estimativa da efetividade da vacina trivalente 2010-2011 contra a gripe, determinada pelo método caso-controlo teste negativo, foi de 58,2% (IC95%, -61,7% a 89,1%). Ainda considerando este método, a estimativa ajustada da EV contra a infeção pelo vírus da gripe do tipo B foi de 75,1% (IC95%, -98,3% a 96,9%) e para o vírus do tipo A(H1N1)pdm09 foi de 33,7% (IC95%, -254,9% a 87,6%). Estas estimativas não tiveram significado estatístico, como revelado pela análise dos intervalos de confiança.
Considerando o método screening, a estimativa ajustada da EV contra casos SG com confirmação laboratorial para gripe foi de 63,7% (IC95%, 16,5% a 84,2%), com significado estatístico.
Para que haja consistência nas estimativas da EV sazonal 2010-11 entre os dois métodos utilizados, é importante que a cobertura da vacina seja similar nos dois grupos de controlo em estudo. No presente estudo, esta premissa foi alcançada, tendo-se observado valores de cobertura da vacina muito próximos nos dois grupos: 17,4% nos controlos do método caso-controlo teste negativo e 17,5% nos controlos da população geral. Esta aproximação dos valores de cobertura vacinal teve, como consequência, valores pontuais da estimativa da EV igualmente similares (58% e 64%).
Comparando os resultados obtidos neste estudo com as estimativas da EV sazonal 2010-11 obtidas por Kissling et al. (2011),28 Savulescu et al. (2011)29 e Pebody et al. (2011),30 verifica-se que o valor estimado se encontra na gama dos valores publicados (42% a 65%), evidenciando igualmente alguma uniformidade das estimativas da EV para esta época em diferentes populações.
A estimativa da EV trivalente contra o SG foi obtida apenas através do método screening, sendo o valor calculado (33,3%; IC95%, -3,1% a 56,8%) inferior à estimativa da EV contra casos de gripe confirmados laboratorialmente. Este resultado era de alguma forma expectável, uma vez que o SG é uma medida menos específica de infeção pelo vírus da gripe do que o resultado laboratorial.
Comparativamente aos resultados publicados até ao momento, a única estimativa disponível da EV sazonal 2010-11 contra casos SG foi obtida através de uma coorte de indivíduos com doenças crónicas,31 que estimou uma EV de 31% (IC95%, 20% a 40%). Apesar do desenho e da população sob observação nesse estudo serem diferentes (apenas indivíduos com doença crónica), a estimativa para toda população (que inclui os indivíduos com doença crónica) obtida no presente trabalho é muito similar (33% vs 31%).
No projeto EuroEVA optou-se por um estudo observacional caso-controlo para medir a efetividade da vacina antigripal. É importante referir que o desenho mais indicado para estimar a eficácia de uma vacina seria um ensaio clínico controlado e aleatorizado (ECA). No entanto dado que a vacina antigripal se encontra disponível e é recomendada para determinados grupos da população, a execução de um ECA para medir a capacidade protetora da vacina levantaria problemas éticos, optando-se, desta forma, por estudos de caráter observacional.32-34
No contexto dos estudos observacionais, o delineamento caso-controlo teste negativo, apesar não se encontrar validado, tem sido recorrentemente utilizado no estudo da efetividade de vacinas.35-38 Algumas das razões para esta preferência estão relacionadas com a facilidade de obtenção do estado vacinal de casos e controlos na ausência de registos oficiais,39 o que corresponde à realidade portuguesa, e com custos inferiores e menor logística do que outros delineamentos observacionais, tais como os estudos de coorte. De igual forma, o método screening é considerado como sendo simples, de rápida aplicação e com necessidade de poucos recursos.40
Em particular, a seleção dos controlos no método caso-controlo teste negativo é interessante, uma vez que podem ser obtidos diretamente através do sistema de vigilância da sindroma gripal, apenas acrescentando algumas variáveis que permitem uma análise estratificada, análise do efeito modificador e de confundimento. Igualmente interessante é a seleção dos controlos da população geral no método screening, uma vez que são selecionados através de um sistema nacional independente deste estudo, que produz, de forma anual e contínua, dados da estimativa da cobertura da vacina antigripal.
No entanto, é amplamente conhecido que os estudos observacionais, e em particular os estudos caso-controlos utilizados no estudo da efetividade de vacinas, estão sujeitos a potenciais vieses de seleção, informação e confundimento.41
Neste estudo os casos e controlos foram selecionados de forma não aleatória no contexto dos cuidados de saúde primários do SNS e, como tal, todos os indivíduos da população-alvo que não se dirigiram a um MF participante durante o período de estudo não tiveram possibilidade de ser selecionados. Assim, se esta subpopulação tiver comportamentos preventivos, tais como a toma da vacina, diferentes dos participantes no estudo, a cobertura vacina antigripal nos casos e controlos da amostra selecionada poderá encontrar-se sobrestimada. Tendo em conta que o MF no momento da seleção desconhece a que grupo (caso ou controlo) o doente recrutado irá pertencer, uma vez essa classificação será dada pelo resultado laboratorial, considera-se que este viés é minimizado.
Outro potencial viés está relacionado com o critério clínico de SG utilizado. Tal como referido, os casos SG foram selecionados de acordo com o critério clínico proposto pela União Europeia, que consiste num conjunto muito estrito de sintomas. Do total de casos selecionados, apenas 17 não cumpriam o critério clínico para SG (i.e., 94% dos casos enviados foram corretamente selecionados). Ao utilizar este critério poderão não estar a ser selecionados casos de SG com sintomatologia mais moderada, facto que poderá introduzir viés nas estimativas da EV. Nomeadamente, se os verdadeiros casos de gripe vacinados (falhas da vacina) apresentarem uma doença menos severa, com um menor número de sinais e sintomas clínicos, estes casos terão uma maior probabilidade de não ser selecionados para confirmação laboratorial por não corresponderem à definição de SG. Ou seja, o que corresponderia a ter um critério de seleção menos sensível. Este facto teria como consequência a subestimação da cobertura da vacina nos casos e por consequência a sobrestimação da EV. Embora se reconheça a possibilidade da existência deste viés, não foi possível estimar a sua verdadeira dimensão no âmbito do projeto EuroEVA.
O viés de seleção poderá também estar presente no método screening, uma vez que a população utilizada neste método é uma amostra nacional de unidades de alojamento com telefone fixo e móvel e não a população da área de influência dos MF. Este facto poderá introduzir um viés nas estimativas da EV uma vez que os controlos foram selecionados de uma população mais ampla (e eventualmente diferente) de que os casos. No entanto, o facto dos MF participantes no EuroEVA trabalharem no SNS e deste ser o maior prestador de cuidados de Medicina Geral e Familiar, pode indicar que o viés não tenha grande efeito.
No estudo caso-controlo teste negativo, a confirmação do estado vacinal do indivíduo foi igual para casos e controlos. Para além dos dados que se encontram no processo clínico do doente, a inoculação da vacina foi ainda confirmada pelo MF por pergunta direta ao doente, tendo sido registada quando possível a marca da vacina. De forma a validar a informação dada pelo doente, foi ainda confirmado se a vacinação teria sido através de injeção, excluindo-se assim outras formas de administração de medicamentos que podem ser erroneamente identificadas pelos doentes como vacinação antigripal.
Adicionalmente todas as variáveis que caraterizam casos e controlos foram recolhidas pelo MF por entrevista direta por aplicação de um mesmo questionário. Uma vez que à data da obtenção da informação o MF não tem conhecimento se o doente se trata de um caso ou de um controlo, não é à partida plausível que os MF utilizem medidas de inquirição diferenciadas entre casos e controlos.
Contudo, no método screening a obtenção da informação relativa à toma da vacina e doença crónica foi auto-reportada pelo respondente ou dada por proxy pelo respondente relativamente aos restantes elementos da unidade de alojamento. Este fato poderá introduzir viés na medida em que o estado vacinal dos casos de gripe (recolhida e validada pelo MF) difere da dos controlos (auto-reportada). De forma a reduzir este viés, só foram considerados como vacinados os controlos que referiram ter tomado a vacina por injeção.
As estimativas pontuais após ajustamento decresceram entre 10 a 20%, comparativamente com as estimativas brutas. Tal como referido, as variáveis de confundimento só foram incluídas no modelo se, após ajustamento pelo método de Mantel-Haenszel, alteravam em pelo menos 10% o OR bruto da vacina sazonal antigripal 2010-11.
A utilização desta metodologia permitiu a identificação de fatores de confundimento positivos, i.e., fatores que produzem uma sobrestimação da EV, bem como fatores de confundimento negativos. Assim, verificou-se que a idade, ter pelo menos uma doença crónica e pertencer ao grupo alvo da vacina constituíam os principais fatores de confundimento positivos. Por outro lado, como fatores de confundimento negativo, apenas a variável vacina pandémica, em 2009-2010, produziu efeitos relevantes na EV após ajustamento.
É ainda importante salientar o impacto do ajustamento na precisão das estimativas da EV antigripal. Com efeito, no estudo caso-controlo teste negativo, após ajustamento para confundimentos, todas as estimativas da EV deixaram de ser estatisticamente significativas. Este fato é resultado da elevada heterogeneidade dos fatores de confundimento entre casos e controlos e da reduzida dimensão da amostra. Na realidade a dimensão da amostra obtida ficou aquém do planeado (253 para 320). Os motivos para este facto estão relacionados com a taxa de participação efetiva dos MF (60%) e com a exclusão de 35 doentes por incumprimento dos critérios de inclusão e análise. De qualquer forma, considera-se que a dimensão da amostra inicialmente planeada não seria suficiente para obter uma estimativa precisa da EV após ajustamento para todos os fatores de confundimento encontrados. Neste contexto o aumento da dimensão da amostra em futuros estudos deve ser alvo de um esforço adicional.
Em conclusão, os resultados obtidos pelo projeto EuroEVA 2010-2011 indicam que as estimativas brutas da efetividade da vacina (EV) antigripal sazonal na época 2010-11, contra os casos de gripe, foram de 79,4% (caso-controlo teste negativo) e de 70,1% (método screening).
Após ajustamento, estes valores decresceram para 58,2% e 63,7%, respetivamente, mas sem significância estatística. Em termos pontuais, estes resultados estão de acordo com outros resultados publicados em revistas científicas com revisão por pares.
No estudo caso-controlo foi ainda possível estimar a EV contra a infeção pelo vírus da gripe do tipo B (EVbruta = 87% e EVajustada = 75%) e contra o vírus pandémico A(H1N1)pdm09 (EVbruta = 74% e EVajustada = 34%). Estes resultados sugerem que a EV sazonal 2010-11 foi inferior à EV monovalente da época 2009-10 estimada pelo estudo multicêntrico I-MOVE: 72% (IC95%, 46% a 86%).
Os dados recolhidos no estudo EuroEVA não permitiram obter estimativas da EV específicas para os indivíduos dos grupos alvo da vacinação antigripal nem obter estimativas ajustadas com significância estatística, o que reforça a necessidade de realizar estudos internacionais multicêntricos, desenvolvidos com um protocolo comum, como é o caso do projeto I-MOVE.
REFERÊNCIAS BIBLIOGRÁFICAS
1. Rebelo-de-Andrade H. Vigilância epidemiológica da gripe em Portugal. Revista Portuguesa de Clinica Geral 2005 Jul-Ago; 21 (4): 379-88.
2. Fleming DM, Zambon M, Bartelds AI, de Jong JC. The duration and magnitude of influenza epidemics: a study of surveillance data from sentinel general practices in England, Wales and the Netherlands. Eur J Epidemiol 1999 May;15 (5): 467-73. [ Links ]
3. ECDC. Disponível em: http://ecdc.europa.eu/en/healthtopics/seasonal_influenza/basic_facts/Pages/factsheet_general_public.aspx [ac edido em 28/08/2012]. [ Links ]
4. Nunes B, Falcão I, Machado A, Rodrigues E, Falcão JM. Influenza vaccine coverage and the attack rate of influenza-like illness among the elderly in Portugal: is there a correlation? Euro Surveill 2007 May 17; 12 (5): E070517.2. [ Links ]
5. Nunes B, Viboud C, Machado A, Ringholz C, Rebelo-de-Andrade H, Nogueira P, et al. Excess mortality associated with influenza epidemics in portugal, 1980 to 2004. PLoS One 2011; 6 (6): e20661. [ Links ]
6. Oropesa S, Acosta B, Pinon A, Andreus H, Hernandez B, Borrego I, et al. The impact of influenza vaccination in the reduction of morbidity and in the exacerbation in asthmatic patients. Options for the Control of Influenza 2004; 1263: 355-9. [ Links ]
7. Francisco PM, Donalisio MR, Lattorre MR. Impacto da vacinação contra influenza na mortalidade por doenças respiratórias em idosos. Rev Saude Publica 2005 Fev; 39 (1): 75-81. [ Links ]
8. Nichol KL, Nordin J, Mullooly J, Lask R, Fillbrandt K, Iwane M. Influenza vaccination and reduction in hospitalizations for cardiac disease and stroke among the elderly. N Engl J Med 2003 Apr 3; 348 (14): 1322-32. [ Links ]
9. Tosh PK, Jacobson RM, Poland GA. Influenza vaccines: from surveillance through production to protection. Mayo Clin Proc 2010 Mar; 85 (3): 257-73. [ Links ]
10. Nichol KL. Challenges in evaluating influenza vaccine effectiveness and the mortality benefits controversy. Vaccine 2009 Oct 23; 27 (45): 6305-11. [ Links ]
11. I-MOVE. Influenza - Monitoring Vaccine Effectiveness. Disponível me: http://sites.google.com/site/epiflu/ [acedido em 28/08/2012]. [ Links ]
12. Valenciano M, Ciancio B, Moren A, Influenza Vaccine Effectiveness Working Group. First steps in the design of a system to monitor vaccine effectiveness during seasonal and pandemic influenza in EU/EEA Member States. Euro Surveill 2008 Oct 23; 13 (43). pii: 19015. [ Links ]
13. Valenciano M, Kissling E, Ciancio BC, Moren A. Study designs for timely estimation of influenza vaccine effectiveness using European sentinel practitioner networks. Vaccine 2010 Oct 28; 28 (46): 7381-8. [ Links ]
14. Kissling E, Moren A, Valenciano M. Protocol for case control studies to measure pandemic and seasonal influenza vaccine effectiveness in the European Union and European Economic Area member States. Paris: EpiConcept; 2009. [ Links ]
15. Falcão J, Nunes B, Rebelo de Andrade,H, Barreto M, Gonçalves P, Santos L, Batista I. Pilot Pilot case-control study measuring influenza vaccine effectiveness, in Portugal, 2008-2009. Lisbon: Instituto Nacional de Saúde Dr Ricardo Jorge (INSA), 2009. p. 55. [ Links ]
16. Falcão J, Nunes B, Rebelo de Andrade H, Barreto M, Gonçalves P, Santos L, Batista I. Efectividade da vacina antigripal: um estudo piloto na época 2008/2009. Disponível em: http://www.insa.pt/sites/INSA/Portugues/Publicacoes/Outros/Paginas/Obs43Jun2009.aspx [acedido em 28/08/20112]. [ Links ]
17. Falcão J, Nunes B, Rebelo de Andrade,H, Barreto M, Gonçalves P, Santos L, Batista I. Pilot Pilot case-control study measuring influenza vaccine effectiveness, in Portugal, 2008-2009. Lisbon: Instituto Nacional de Saúde Dr Ricardo Jorge (INSA), 2009. p. 55.
18. Kissling E, Valenciano M, Falcão J, Larrauri A, Widgren K, Pitigoi D, et al. “I-MOVE” towards monitoring seasonal and pandemic influenza vaccine effectiveness: lessons learnt from a pilot multi-centric case-control study in Europe, 2008-9. Euro Surveill 2009 Nov 5; 14 (44). pii: 19388.
19. Nunes B, Guiomar R, Machado A, Falcão I, Gonçalves P, Conde P, et al. Final report - Case control study for measuring influenza vaccine effectiveness in Portugal - Season 2009-10. Disponível em: http://www.insa.pt/sites/INSA/Portugues/Publicacoes/Outros/Documents/Epidemiologia/Relatorio_Euroeva_Case_control_final_report_2009-10_PT_corrigido.pdf [accedido em 28/08/2012].
20. Valenciano M, Kissling E, Cohen JM, Oroszi B, Barret AS, Rizzo C, et al. Estimates of pandemic influenza vaccine effectiveness in Europe, 2009-2010: results of Influenza Monitoring Vaccine Effectiveness in Europe (I-MOVE) multicentre case-control study. PLoS Med 2011 Jan; 8 (1) :e1000388.
21. Lemeshow S, Hosmer DW Jr, Klar J. Sample size requirements for studies estimating odds ratios or relative risks. Stat Med 1988 Jul; 7 (7): 759-64.
22. Médicos–Sentinela. O que se fez em 2007. Lisboa: Instituto Nacional de Saúde Dr. Ricardo Jorge; 2009.
23. European Centre for Disease Prevention and Control. Influenza case definitions. Stockholm: ECDC; 2010.
24. Farrington CP. Estimation of vaccine effectiveness using the screening method. Int J Epidemiol 1993 Aug; 22 (4): 742-6.
25. Nunes B, Contreiras T, Falcão J. Vacinação anti-gripal: cobertura da população portuguesa entre 1998/1999 e 2002/2003. Rev Port Pneumol 2004 Mar-Abr; 10 (2): 115-23.
26. StataCorp. Statistical Software: Release 11.0. College Station, TX: Stata Corporation; 2009.
27. Branco M, Nunes B. Vacinação antigripal da população portuguesa em 2010-2011: cobertura e algumas características do acto vacinal. Departamento de Epidemiologia. Instituto Nacional de Saúde Dr Ricardo Jorge; 2011. Disponível em: http://www.insa.pt/sites/INSA/Portugues/Publicacoes/Outros/Documents/Epidemiologia/RelatorioVacinacaoAntiGripal_2010-2011.pdf [acedido em 28/08/2912].
28. Kissling E, Valenciano M, I-MOVE Case-Control Studies Team. Early estimates of seasonal influenza vaccine effectiveness in Europe, 2010/11: I-MOVE, a multicentre case-control study. Euro Surveill 2011 Mar 17; 16 (11). pii: 19818.
29. Savulescu C, Jiménez-Jorge S, de Mateo S, Ledesma J, Pozo F, Casas I, et al. Effectiveness of the 2010/11 seasonal trivalent influenza vaccine in Spain: preliminary results of a case-control study. Euro Surveill 2011;16(11). pii: 19820.
30. Pebody R, Hardelid P, Fleming D, McMenamin J, Andrews N, Robertson C, et al. Effectiveness of seasonal 2010/11 and pandemic influenza A(H1N1)2009 vaccines in preventing influenza infection in the United Kingdom: mid-season analysis 2010/11. Euro Surveill 2011 Feb 10; 16 (6). piii: 19791.
31. Castilla J, Moran J, Martinez-Artola V, Reina G, Martinez-Baz I, Garcia Cenoz M, et al. Effectiveness of trivalent seasonal and monovalent influenza A(H1N1)2009 vaccines in population with major chronic conditions of Navarre, Spain: 2010/11 mid-season analysis. Euro Surveill 2011 Feb 17; 16 (7). piii: 19799.
32. Torvaldsen S, McIntyre PB. Observational methods in epidemiologic assessment of vaccine effectiveness. Commun Dis Intell 2002; 26 (3): 451-7.
33. Chen RT, Orenstein WA. Epidemiologic methods in immunization programs. Epidemiol Rev 1996; 18 (2): 99-117.
34. Baxter R, Lee J, Fireman B. Evidence of bias in studies of influenza vaccine effectiveness in elderly patients. J Infect Dis 2010 Jan 5; 201 (2): 186-9.
35. Fleming DM, Andrews NJ, Ellis JS, Bermingham A, Sebastianpillai P, Elliot AJ, et al. Estimating influenza vaccine effectiveness using routinely collected laboratory data. J Epidemiol Community Health 2010 Dec; 64 (12): 1062-7.
36. Skowronski DM, Masaro C, Kwindt TL, Mak A, Petric M, Li Y, et al. Estimating vaccine effectiveness against laboratory-confirmed influenza using a sentinel physician network: Results from the 2005-2006 season of dual A and B vaccine mismatch in Canada. Vaccine 2007 Apr 12; 25 (15): 2842-51.
37. Skowronski DM, De Serres G, Crowcroft NS, Janjua NZ, Boulianne N, Hottes TS, et al. Association between the 2008-09 seasonal influenza vaccine and pandemic H1N1 illness during Spring-Summer 2009: four observational studies from Canada. PLoS Med 2010 Apr 6; 7 (4): e1000258.
38. Belongia EA, Kieke BA, Donahue JG, Greenlee RT, Balish A, Foust A, et al. Effectiveness of inactivated influenza vaccines varied substantially with antigenic match from the 2004-2005 season to the 2006-2007 season. J Infect Dis 2009 Jan 15; 199 (2): 159-67.
39. Orenstein WA, Bernier RH, Dondero TJ, Hinman AR, Marks JS, Bart KJ, et al. Field evaluation of vaccine efficacy. Bull World Health Organ 1985; 63 (6): 1055-68.
40. Orenstein WA, Bernier RH, Hinman AR. Assessing vaccine efficacy in the field. Further observations. Epidemiol Rev 1988;10:212-41.
41. Ferdinands JM, Shay DK. Magnitude of potential biases in a simulated case-control study of the effectiveness of influenza vaccination. Clin Infect Dis 2012 Jan 1; 54 (1): 25-32.
Endereço para correspondência | Dirección para correspondencia | Correspondence
Baltazar Nunes
Departamento de Epidemiologia
Instituto Nacional de Saúde Dr. Ricardo Jorge
Av. Padre Cruz
1649-016 Lisboa
Portugal
baltazar.nunes@insa.min-saude.pt
Artigo redigido usando o novo acordo.
Agradecimentos
Os autores gostariam de agradecer a todos os médicos de família que participaram neste estudo.
Gostariam ainda de agradecer:
• À Associação Portuguesa de Medicina Geral e Familiar (APMGF), parceira do INSA no desenvolvimento do EuroEVA;
• Ao Dr. Carlos Matias Dias, coordenador do Departamento de Epidemiologia, por todo o apoio no decorrer do estudo e pela revisão final deste artigo.
Conflitos de interesses dos autores e financiamento do estudo
Os autores declaram a ausência de conflitos de interesse.
O estudo EuroEVA é financiado pelo Centro Europeu de Prevenção e Controlo de Doenças (ECDC) no contexto do projeto I-MOVE (Influenza Monitoring Vaccine Efectiveness in Europe), que é coordenado pela empresa EpiConcept SARL, contratada pelo European Centre of Disease Prevention and Control para os devidos efeitos. A transferência das verbas para o INSA é feita através da empresa EpiConcept SARL no contexto de um “Protocol agreement” assinado entre as duas instituições.
Recebido em 15/04/2012
Aceite para publicação em 19/08/2012