Introdução
A albumina sérica humana (ASH) pertence à superfamília das albuminas e constitui a proteína sérica mais abundante no plasma, representando cerca de 60-65% das proteínas totais. Desempenha uma importante função como proteína de transporte, essencial tanto para a distribuição de componentes endógenos como exógenos, nomeadamente fármacos. São atualmente conhecidos diversos polimorfismos na expressão da ASH, resultando em fenótipos que variam entre a presença de variantes genéticas funcionais (como a aloalbuminemia ou bisalbuminemia) até à ausência completa da sua expressão (analbuminemia congénita).1
A bisalbuminemia caracteriza-se por uma variação qualitativa da ASH, traduzindo a co-expressão de dois tipos de ASH, com mobilidade eletroforética diferente, apresentando-se como uma dupla banda. Esta apresentação pode surgir de forma inata nos indivíduos heterozigóticos, uma patologia genética relativamente rara (1:1.000-1:10.000), ou de forma transitória (adquirida) como alteração secundária a várias patologias. 2
Descrição do caso
Apresenta-se o caso de uma criança de quatro anos de idade, do sexo masculino, raça negra, natural de Portugal. Inserido numa família reconstruída, de ascendência cabo-verdiana, pertencente a uma classe socioeconómica média-baixa (classe IV), segundo classificação de Graffar. Reside com os pais, três irmãos maternos e um irmão paterno, sendo de destacar como antecedentes familiares um irmão de 18 anos de idade, com diagnóstico de arterite de Takayasu, sob imunossupressão.
Mantém um seguimento médico adequado, cumprindo o Programa de Vigilância de Saúde Infantil e Juvenil, bem como o Programa Nacional de Vacinação. Em consulta de vigilância com a médica de família, a mãe refere um quadro com cerca de um ano de evolução de seletividade alimentar excessiva, com receio de repercussões no desenvolvimento estaturo-ponderal da criança. Este padrão alimentar era mantido desde há vários anos em casa e de forma idêntica em ambiente escolar, sendo também descrito pelos educadores. Descrita preferência por alimentos de textura mole, com recusa de alimentos inteiros como carne. À data tinha como antecedentes pessoais síndroma de apneia obstrutiva do sono, a aguardar tratamento cirúrgico, sem terapêutica habitual.
Ao exame objetivo não foram detetadas alterações, com pele e mucosas coradas, progressão estaturo-ponderal dentro dos percentis habituais (estatura P50-85 e peso P15-50), sem sinais sugestivos de défices vitamínicos específicos. Não apresentava alterações do desenvolvimento psicomotor, cumprindo todos os itens de avaliação do desenvolvimento na escala de Mary Sheridan.
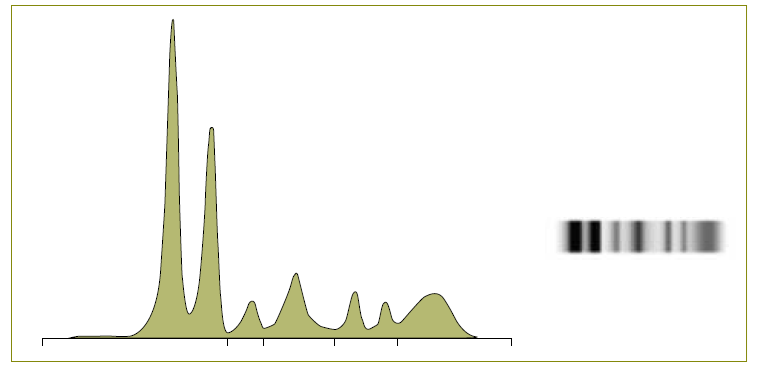
De forma a excluir défices nutricionais foram solicitados exames complementares de diagnóstico, que a criança realizou no mês de maio em contexto de ambulatório. A avaliação analítica (Tabela 1) revelou anemia ferropénica, ligeira elevação dos parâmetros inflamatórios e na eletroforese de proteínas um padrão de bisalbuminemia com distribuição em dois picos (Figura 1), sem alteração dos valores absolutos ou da distribuição das restantes proteínas.
Perante o diagnóstico de bisalbuminemia foi complementada a avaliação de forma a excluir que esta fosse uma apresentação secundária a outra causa. Não foram encontradas outras comorbilidades, com função renal normal, sem marcadores de lesão hepática e função tiroideia sem alterações. Foram pesquisadas ainda outras causas como iatrogenia medicamentosa, associada à toma recente de antibioterapia com betalactâmicos, que também não se verificou.
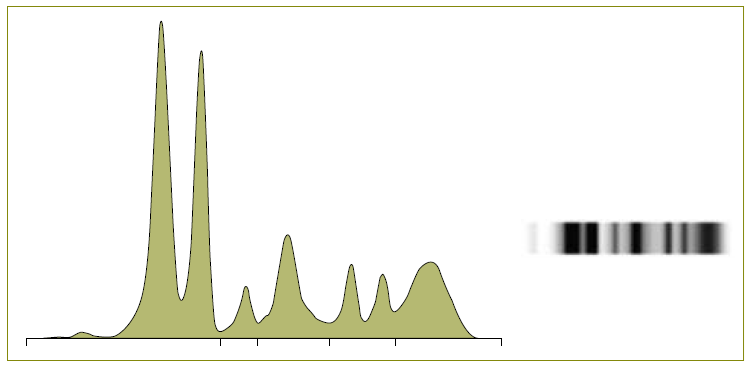
Não existindo indícios de que se tratasse de uma causa secundária foi presumida a forma inata, com causa genética. Para corroborar esta hipótese foi solicitada avaliação com eletroforese de proteínas à mãe, que mostrou a presença de um padrão idêntico (Figura 2), sem outras comorbilidades identificadas.
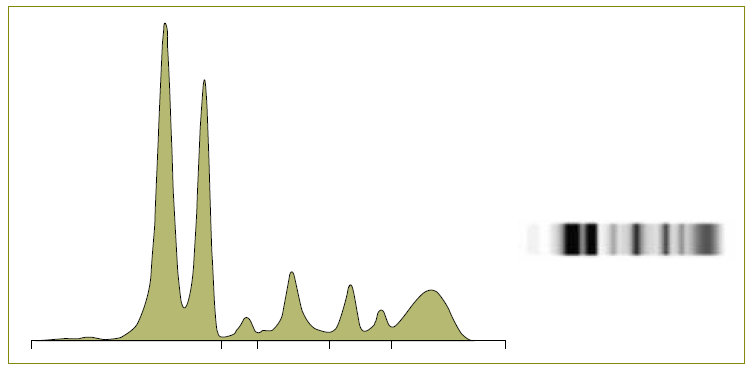
De forma dirigida à seletividade alimentar e anemia ferropénica foi iniciada suplementação com ferro 4-5 mg/kg/dia durante dois meses, pelo défice nutricional identificado, e foram adotadas estratégias comportamentais. Após três meses foi realizada reavaliação analítica (Tabela 1), onde se confirmou correção da anemia ferropénica, resolução dos parâmetros inflamatórios e manutenção do padrão de bisalbuminemia (Figura 3).
A criança mantém o seguimento com a sua médica de família, sem intercorrências e sem necessidade de referenciação a outras especialidades médicas.
Comentário
A expressão genética dos genes codificantes da ASH, bem como de outras proteínas desta superfamília, como a α-fetoproteína e a proteína ligante da vitamina D, é determinada de forma codominante, estando localizados no cromossoma 4. A sua grande variabilidade genética associa-se à presença de variantes funcionais, tendo sido identificadas até à data 73 variantes circulantes da albumina. 3
A bisalbuminemia é um achado raro e geralmente o seu diagnóstico é incidental. O padrão apresentado na eletroforese de proteínas resulta da mobilidade eletroforética diferente de dois tipos de albumina ou de porções alteradas de parte desta proteína. 2 Perante este resultado torna-se imperativo diferenciar as formas inatas - de causa genética - das formas adquiridas, que são habitualmente transitórias e secundárias a outras patologias.
A bisalbuminemia hereditária é geralmente benigna, assintomática e não está associada a patologias clínicas. No entanto, algumas variantes da ASH podem ter uma afinidade diferente para hormonas, iões metálicos, ácidos gordos ou fármacos. 4
A forma adquirida é habitualmente transitória e frequentemente associa-se a quadros de gamapatia, como o mieloma múltiplo ou a macroglobulinemia de Waldenstrom. Pode ainda cursar com síndroma nefrótico, doença renal crónica ou doença pancreática quística. Por fim, está descrita em contextos de exposição a elevadas doses de beta-lactâmicos. 5
O caso apresentado relata o achado incidental de um padrão de bisalbuminemia, sem comorbidades identificadas, cujo padrão de transmissão heredofamiliar se verifica com a confirmação de um padrão idêntico na mãe da criança. A manutenção do padrão de forma idêntica na reavaliação analítica permite também reforçar a hipótese diagnóstica da forma genética, uma vez que o padrão se mantém inalterado. 6
O conhecimento deste padrão pelos médicos no âmbito dos cuidados de saúde primários (CSP) torna-se relevante, de forma que possa ser realizada uma investigação adequada das possíveis causas associadas à forma adquirida, uma vez que o estudo analítico é de fácil acesso e interpretação, sem a necessidade de referenciação aos cuidados de saúde secundários na ausência de outras alterações. Perante a necessidade de confirmação do padrão hereditário será relevante complementar o estudo com outros membros familiares, um estudo também facilmente realizado pelo médico de família. Nos casos em que este achado seja confirmado noutro membro familiar, também ele sem comorbidades identificadas, a causa genética é assim corroborada, dispensando outras intervenções.
Embora a bisalbuminemia hereditária tenha uma prevalência reduzida na população, o seu reconhecimento é de particular relevância na prática clínica, sobretudo no contexto dos CSP. A identificação precoce desta variante benigna permite ao médico de família orientar o utente de forma adequada, esclarecendo a natureza genética e não patológica da condição. Esta clarificação é essencial para evitar exames complementares e intervenções desnecessárias, promovendo uma gestão clínica eficiente e alinhada com o princípio da não-maleficência. Assim, o papel do médico de família centra-se na educação e tranquilização do utente, assegurando um acompanhamento informado e evitando preocupações infundadas, dada a ausência de repercussões clínicas significativas.