Introdução
A isquemia mesentérica aguda (IMA) é uma causa relativamente rara de ventre agudo perfazendo cerca de 1-2% das emergências abdominais agudas1 e menos de 1 em cada 1000 (0,1%) de todas as hospitalizações.2 Esta entidade resulta de uma hipoperfusão intestinal súbita o que frequentemente leva a enfarte da parede intestinal com consequente necrose intestinal. Os mecanismos patogénicos nesta entidade nosológica são distintos pelo que se pode classificar a isquemia intestinal aguda em quatro subtipos principais de acordo com a etiologia: embolia arterial (EAMI); trombose arterial (TAMI); trombose venosa (VAMI); não oclusiva (NOMI). Ao contrário das primeiras três etiologias a isquemia mesentérica não oclusiva é uma entidade que ocorre com a vasculatura mesentérica arterial e venosa patente sendo frequente em doentes que apresentam hipovolemia, hipotensão, insuficiência cardíaca e/ou espasmo mesentérico por definição. Tem uma maior preponderância em indivíduos hospitalizados em estado crítico com patologia cardíaca grave, sepsis, terapia de suporte com inotrópicos ou hemodialisados.2,3
A IMA é uma patologia que atinge mais doentes idosos, pelo que a clínica é numa grande parte dos casos muito inespecífica incluindo dor abdominal intensa frequentemente referida como desproporcional ao exame objetivo do abdómen. Outros sinais e sintomas mais frequentemente relatados são náuseas e vómitos, diarreia, hematoquézias, melenas, febre, distensão abdominal, taquicardia ou hipotensão arterial.4,5 A clínica inespecífica leva a que o diagnóstico seja realizado em fases mais avançadas ou que este seja impreciso e apesar dos novos avanços nas terapêuticas endovasculares e cirúrgicas, pode resultar em taxas de mortalidade muito elevadas, com valores aproximados de 40-80%.6
Em termos laboratoriais não há nenhum marcador plasmático específico para a deteção precoce de isquemia do mesentério, no entanto, é frequente documentar leucocitose, desvio esquerdo no rácio de neutrófilos imaturos para maduros,2 acidose metabólica com anion gap aumentado, hemoconcentração e elevação dos níveis plasmáticos de proteína C reativa, amílase, aspartato aminotransferase (AST) e creatina cinase (CK).1 Níveis de D-dímeros elevados têm elevada sensibilidade na deteção de isquemia mesentérica em estádios iniciais (96-100%), no entanto são pouco específicos.7 A elevação dos níveis de L-lactato sérico reflete um estadio mais avançado com enfarte transmural da parede intestinal, metabolismo anaeróbio e necrose da parede intestinal pelo que não tem interesse na deteção precoce de isquemia, tendo apenas valor prognóstico na medida em que a sua clearance progressiva com o sucesso da terapêutica é um bom preditor independente de melhoria clínica.8
O exame complementar de diagnóstico de primeira linha atualmente mais aceite para diagnóstico precoce de IMA é a tomografia computorizada (TC) multidetetor com contraste com uma sensibilidade e especificidade estimadas de 93,3% e 95,9% respetivamente.9 A angiografia convencional é considerada o gold standard para o diagnóstico, no entanto a sua principal importância atualmente prende-se com o seu uso no tratamento.2,10) A TC multidetetor com contraste é também um exame muito útil para excluir eventuais diagnósticos diferenciais e para estratificar a gravidade da isquemia intestinal de acordo com os achados radiológicos como pneumatose intestinal, presença de gás portomesentérico, densificação do tecido adiposo mesentérico e ascite que indiciam isquemia severa e enfarte transmural.11
O tratamento da isquemia mesentérica aguda inclui o uso de técnicas endovasculares, cirúrgicas (revascularização e ou resseção intestinal), híbridas (retrograde open mesenteric stenting - ROMS) ou apenas tratamento médico dependendo da etiologia em questão e das características específicas clínicas e imagiológicas de cada paciente. As recomendações e guidelines existentes atualmente são baseadas essencialmente em estudos retrospetivos com pequenas amostras e estudos de caso, não estando publicados ensaios randomizados e controlados de forma a orientar o tratamento nesta patologia em específico.12,13 As técnicas endovasculares disponíveis incluem trombectomia percutânea mecânica ou por aspiração do trombo, angioplastia percutânea transluminal (PTA) por balão/stenting, infusão de fibrinolíticos e/ou vasodilatadores.
O objetivo deste estudo é realizar uma revisão da literatura das modalidades de tratamento endovascular da isquemia mesentérica aguda, avaliando a sua eficácia em termos técnicos e clínicos, incidência de complicações, taxa de recorrência e taxa de mortalidade precoce e a longo prazo.
Materiais e Métodos
A pesquisa foi realizada em agosto de 2020 com recurso às bases de dados PubMed e EMBASE com recurso às palavras-chave "Mesenteric Ischemia [MeSH]", "Acute Disease [MeSH]", "Endovascular Procedures [MAJR]”, "Thrombectomy [MeSH]” e “Thrombolysis”. Os algoritmos de pesquisa utilizados em cada base de dados estão incluídos no Anexo 1 (fig. 2). Os critérios de inclusão adotados relacionam-se com a língua (Inglês, Português e Castelhano), espécie (humana) e data de publicação nos últimos 15 anos (desde 2006 a 2020). Foram excluídos artigos de revisão, revisões sistemáticas e meta-análises, guidelines, estudos de caso e artigos de opinião. Foram excluídos os estudos que não apresentassem pelo menos um dos outcomes pretendidos (sucesso técnico, sucesso clínico, taxa de recorrência, complicações e taxas de mortalidade). Dos artigos referentes a isquemia mesentérica de etiologia arterial foram excluídos os estudos com amostra inferior a 10 (n < 10), enquanto nos artigos referentes a isquemia mesentérica de etiologia venosa não foi aplicado qualquer limite inferior de amostra.
A extração de dados dos artigos selecionados foi realizada inicialmente com a divisão dos estudos no grupo dos pacientes com isquemia mesentérica aguda de etiologia arterial e dos pacientes com isquemia mesentérica aguda de etiologia venosa. Os dados extraídos são referentes às seguintes variáveis: tipo de estudo, data de publicação, tamanho da amostra, idade média da amostra, etiologia da oclusão, vasos atingidos, tipo(s) de tratamento(s) endovascular(es) instituído(s), sucesso técnico, sucesso clínico, taxa de recorrência, complicações, taxas de mortalidade precoce e tardia e intervenções pós tratamento endovascular (laparotomia, laparoscopia e resseção intestinal). Dados adicionais de pacientes submetidos exclusivamente a tratamentos não endovasculares (sistémicos e/ou cirúrgicos) ou com isquemia mesentérica crónica (IMC) foram excluídos, sendo apenas recolhidos dados das amostras de pacientes com isquemia mesentérica aguda submetidos a pelo menos uma técnica endovascular.
Sucesso técnico é definido como o restabelecimento do fluxo arterial/venoso sem necessidade de reintervenção cirúrgica ou endovascular. Sucesso clínico é definido como a resolução do quadro clínico após o tratamento em cada estudo. As complicações relatadas por estudo concernem preferencialmente às imputadas apenas aos tratamentos endovasculares, salvo se estas forem indissociáveis das complicações de outros tratamentos precedentes ou subsequentes. Mortalidade precoce é definida como morte em 30 dias e/ou durante internamento hospitalar por falha terapêutica, complicações relacionadas com o tratamento (isquémicas, hemorrágicas, inflamatórias, infeciosas e outras) ou pela presença de outras comorbilidades. Mortalidade a longo prazo adiciona à mortalidade precoce as mortes documentadas após alta do internamento hospitalar por follow-up.
Resultados
Na pesquisa inicial foram encontrados 521 resultados, 325 na base de dados PubMed e 196 na base de dados EMBASE, dos quais foram excluídos 39 duplicados. Com a aplicação dos critérios de inclusão acima descritos, foram posteriormente selecionados os artigos relevantes, recorrendo à análise dos títulos e abstracts, perfazendo um total de 49 artigos potencialmente elegíveis para a presente revisão.
Após uma análise mais detalhada foram selecionados para ser incluídos neste trabalho de revisão 19 estudos, 14 referentes a isquemia mesentérica aguda de etiologia arterial e 5 referentes a isquemia mesentérica aguda de etiologia venosa. Dos 30 estudos excluídos: 8 apresentavam uma amostra inferior ao limite (n < 10), 7 apresentavam apenas resultados de técnica híbrida, 3 apresentavam apenas resultados de tratamento cirúrgico, 3 apresentavam resultados conjuntos de abordagem multidisciplinar, 2 apresentavam resultados conjuntos de tratamento de IMA e IMC, 2 abordavam o risco do uso de contraste na tomografia computorizada (TC), 1 avaliava apenas fatores de prognóstico, 1 avaliava os resultados do timing de laparotomia, 1 apresentava uma avaliação relacionada apenas com hospitalizações e custos, 1 avaliava prevalência do uso de diferentes modalidades terapêuticas e 1 apresentava resultados de tratamento com fibrinólise sistémica. A figura 1 ilustra o diagrama de seleção dos artigos. As tabelas 1, 2, 3 e 4 resumem os dados extraídos dos artigos referentes a isquemia mesentérica de etiologia arterial e a isquemia mesentérica de etiologia venosa respetivamente.

Figura 1: Diagrama ilustrativo de seleção dos estudos. Adaptado de Moher D, Liberati A, Tetzlaff J, Altman DG, The PRISMA Group (2009). Preferred Reporting Items for Systematic Reviews and Meta-Analyses: The PRISMA Statement. PLoS Med 6(7): e1000097. doi:10.1371/journal.pmed1000097
Isquemia mesentérica aguda de etiologia arterial
Dos 14 estudos analisados foram recolhidos dados referentes a um total de 1551 participantes. A idade média dos pacientes em cada estudo variou entre 60,2 anos e 79 anos.
A etiologia embólica foi mais prevalente em 3 publicações,14,15,16 enquanto que a etiologia trombótica foi mais prevalente em 6 publicações.17,18,19,20,21,22 A prevalência de cada etiologia não foi escrutinada em 5 publicações.23,24,25,26,27 Block et al.21 reportam ainda um caso de IMA por disseção arterial e outro por trombose de stent já previamente colocado.
A artéria mais vezes envolvida foi a artéria mesentérica superior (AMS) e os seus ramos periféricos, sendo que em 6 estudos15,16,21,22,23,27 foi a única artéria envolvida em todos os pacientes da amostra. Outras artérias envolvidas incluíram a artéria mesentérica inferior (AMInf) e o tronco celíaco (TrC) em menor preponderância.
Tabela 1: Dados dos estudos referentes a isquemia mesentérica aguda de etiologia arterial
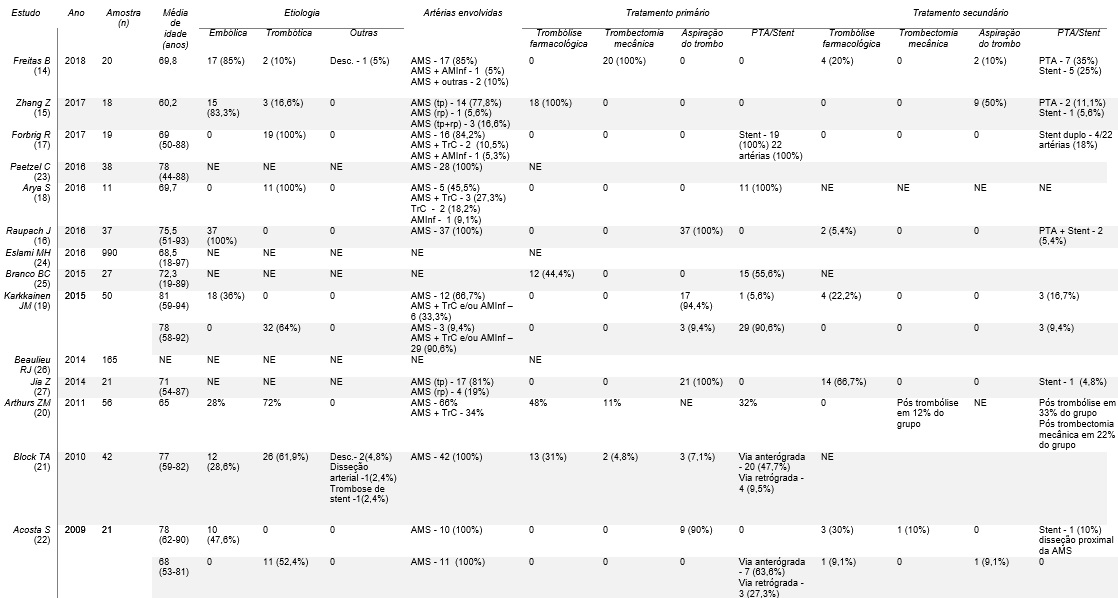
Legenda: AMS - artéria mesentérica superior; AMInf - artéria mesentérica inferior; TrC - tronco celíaco; tp - tronco principal; rp - ramo periférico; ROMS - retrograde open mesenteric stenting; Desc. - desconhecida; NE - não especificado
Tabela 2: (continuação tabela 1) Dados dos estudos referentes a isquemia mesentérica aguda de etiologia arterial
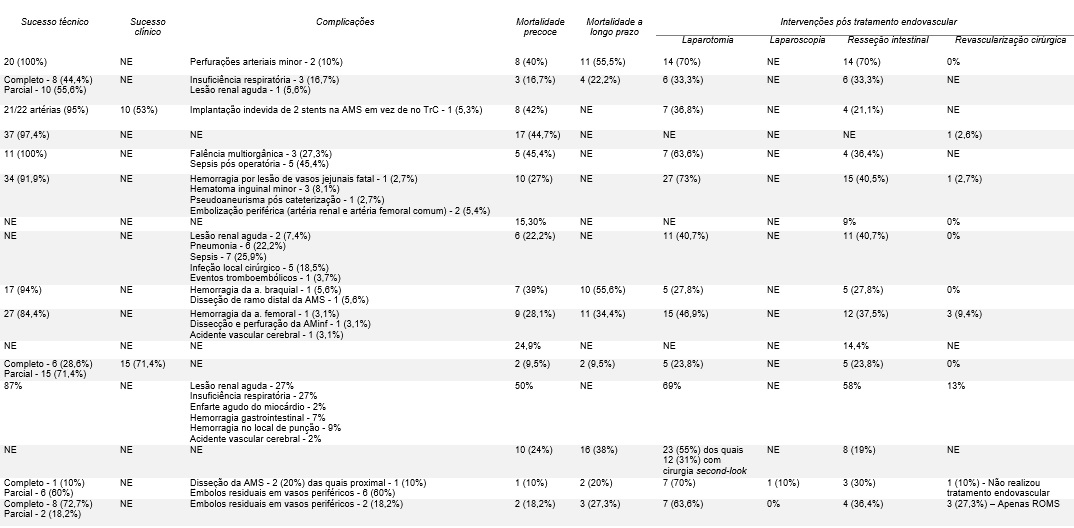
Tabela 3: Dados dos estudos referentes a isquemia mesentérica aguda de etiologia venosa
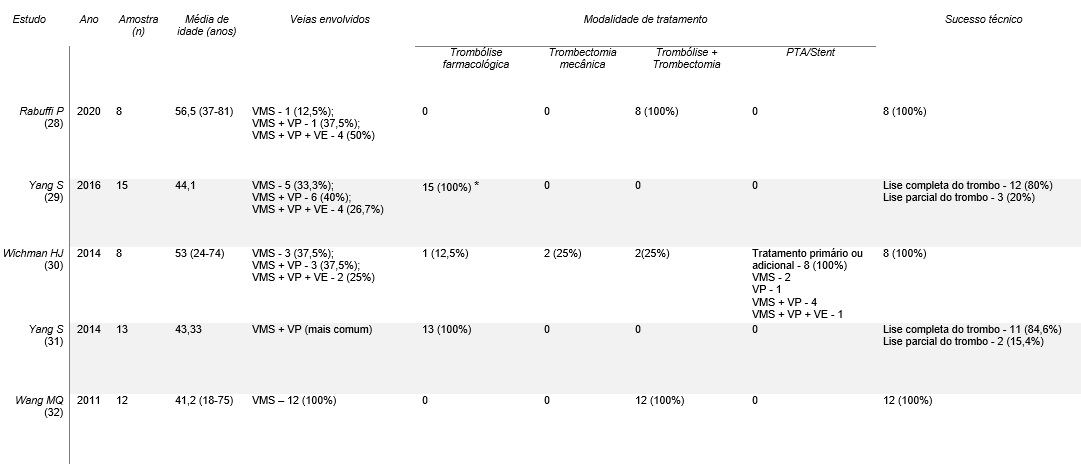
Legenda: VMS - veia mesentérica superior; VP - veia porta; VE - veia esplénica; VJI - veia jugular interna; * - Tratamento realizado após resseção intestinal por laparotomia em todos os pacientes; SDRA - síndrome de dificuldade respiratória aguda; NE - não especificado
Tabela 4: (continuação tabela 3) Dados dos estudos referentes a isquemia mesentérica aguda de etiologia venosa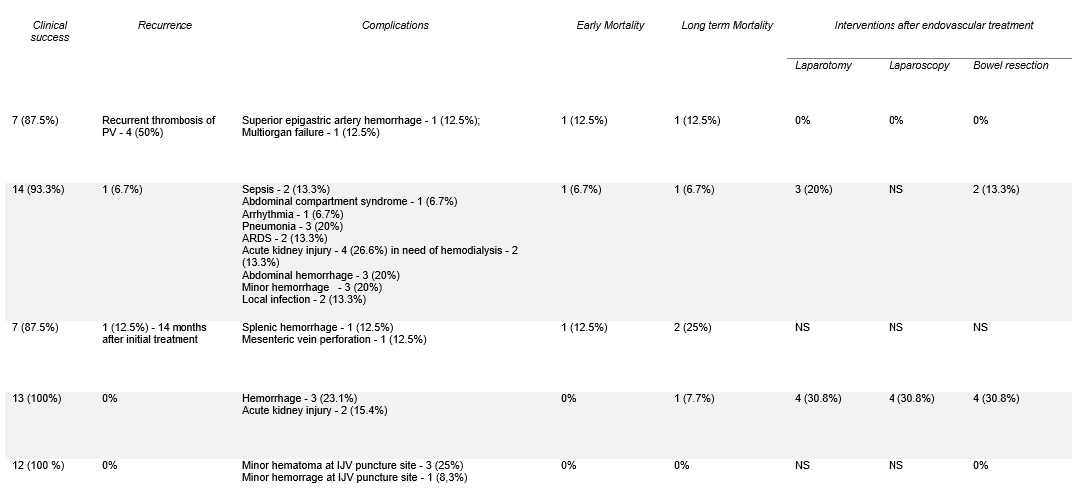
No estudo de Zhang Z et al.15 foi instituído como tratamento primário em todos os pacientes a trombólise farmacológica guiada por cateter, no estudo de Freitas B et al.14 recorreu-se à trombectomia mecânica percutânea com dispositivo rotatório - 6F Rotarex® S Debulking Device (Straub Medical, Wangs, Switzerland), nos estudos de Raupach J et al.16 e de Jia Z et al.27 recorreu-se à trombectomia por aspiração do trombo por cateter e no estudo de Forbrig R et al.17 a angioplastia percutânea transluminal (PTA)/Stent. Nas restantes publicações foram utilizadas combinações das várias técnicas endovasculares excluindo 323,24,26) em que não são reportadas quais as técnicas instituídas.
Sucesso técnico de 100% foi atingido em 4 estudos.14,15,18,27 Nos restantes foi atingido sucesso técnico de 97,4%,23 95%,17 91,9%,16 88%,19 87%20 e 81%.22 Sucesso clínico foi reportado em duas publicações com valores de 71,4%27 53%.17
As complicações relatadas mais frequentemente associadas diretamente aos tratamentos endovasculares foram perfuração arterial minor 10%;14 hemorragia no local de punção 4%19 e 9%;20 hematoma no local de punção 8,1%;16 formação de êmbolos residuais periféricos 38,1%;22 implantação indevida de stents 5,3%;17 formação de pseudoaneurisma pós cateterização 2,7%;16 hemorragia de vasos jejunais fatal 2,7%;16 disseção da AMS proximal 4,8%22 e de ramos distais 2%19 e 4,8%;22 disseção e perfuração da AMInf 2%19 e formação de êmbolos periféricos em artérias de grande calibre (artéria femoral comum e artéria renal) 5,4%.16 Outras complicações relatadas concernem não só aos tratamentos endovasculares realizados, mas também aos subsequentes tratamentos cirúrgicos como insuficiência respiratória 16,7%15 e 27%;20 lesão renal aguda 5,6%,15 7,4%25 e 27%;20 infeção do local cirúrgico 18,5%;25 pneumonia 22,2%;25 sepsis 45,4%18 e 25,9%;25 enfarte agudo do miocárdio 2%;20 acidente vascular cerebral 2%;9,20 outros eventos tromboembólicos não especificados 3,7%;25 hemorragia gastrointestinal 7%20 e falência multiorgânica 27,3%.18
As taxas de mortalidade precoce foram muito variáveis de estudo para estudo, sendo que o seu valor mínimo foi de 9,5%27 e máximo de 44,7%.18 A mortalidade a longo prazo variou entre 9,5%27 e 55,5%.14
Em relação a intervenções pós tratamento endovascular relatadas, a necessidade de laparotomia variou entre 23,8%27 e 73%,16 apenas o estudo de Acosta S et al.22 reporta o uso de laparoscopia em 1 caso (10%) no subgrupo de pacientes com IMA de etiologia embólica. A necessidade de resseção intestinal após tratamento endovascular variou entre 9%24 e 70%14 e em relação à necessidade de revascularização cirúrgica pós tratamento endovascular (excluindo os dados de Acosta S et al.22 em que nem todos os pacientes foram submetidos a tratamento percutâneo não-híbrido) variou entre 0%14,24,25,27 e 13%.20
Isquemia mesentérica aguda de etiologia venosa
De 5 publicações analisadas foram recolhidos dados de 56 pacientes com uma idade média entre cada estudo de 41,2 a 56,5 anos.
A veia mais frequentemente envolvida foi a veia mesentérica superior, sendo afetada de forma isolada em todos os casos no estudo de Wang MQ et al..3 Nas restantes publicações registaram-se casos em que foram afetadas de forma concomitante a veia porta e/ou veia esplénica.
A trombólise farmacológica guiada por cateter por via direta (transhepática percutânea/transjugular intrahepática) ou indireta (através da artéria mesentérica superior) foi a técnica utilizada em todos os pacientes nas publicações de Yang S et al.,29,31 sendo que no estudo de 201629 a via indireta foi a única a ser utilizada. Nos estudos de Rabuffi P et al.28 e Wang MQ et al.32 foi utilizada a trombólise farmacológica guiada por cateter apenas por via direta em combinação com a trombectomia mecânica percutânea com aspiração do trombo. No estudo de Wichman HJ et al.30 todos os pacientes foram submetidos a stenting de pelo menos um vaso, adicionalmente em parte dos pacientes recorreu-se também a trombólise farmacológica guiada por cateter e/ou trombólise mecânica percutânea com aspiração do trombo.
Foi atingido em todos os estudos sucesso técnico de 100%, no entanto de forma parcial nos estudos de Yang S et al. em 20%29 e 15,4%31 dos pacientes. Duas publicações reportaram sucesso clínico de 100%,31,32 uma 93,3%29 e duas 87,5%.28,30 As taxas de recorrência reportadas foram de 0%,31,32 6,7%,29 12,5%30 e 50%.28
Foram relatadas complicações associadas aos tratamentos endovasculares como hemorragia no local de punção da veia jugular interna 8,3%;32 hematoma no local de punção da veia jugular interna 25%;32 perfuração de veia mesentérica 12,5%;30 hemorragia da artéria epigástrica superior 12,5%;28 hemorragia da veia esplénica 12,5%30 e outras hemorragias não especificadas 20%29 e 23,1%.31 Outras complicações relatadas concernem não só aos tratamentos endovasculares realizados, mas também aos subsequentes tratamentos cirúrgicos entre as quais sepsis 13,3%;29 arritmia 6,7%;29 síndrome de dificuldade respiratória aguda 13,3%;29 pneumonia 20%;29 síndrome do compartimento abdominal 6,7%;29 lesão renal aguda 26,6%29 e 15,4%31 com necessidade de hemodiálise 13,3%;29 hemorragia abdominal 20%;29 infeção do local cirúrgico 13,3%29 e falência multiorgânica 12,5%.28
As taxas de mortalidade precoce foram de 0%,31,32 6,7%29 e 12,5%.28,30 A longo prazo a mortalidade relatada foi de 0%,32 6,7%,29 7,7%,31 12,5%,28 25%.30
Após tratamento endovascular foi reportada necessidade de laparotomia em 0%,28 20%29 e 38%31 dos casos, laparoscopia em 0%28 e 30,8%31 e resseção intestinal em 0%,28,32 13,3%29 e 30,8%.31
Discussão
Isquemia mesentérica aguda de etiologia arterial
A isquémia mesentérica aguda de origem arterial pode ser classificada de acordo com a sua etiologia em embólica e trombótica. A causa embólica é a mais frequente com prevalência de 30-50% dos casos de AMI e a fonte embólica mais frequente é cardíaca, estando associada a doença cardíaca isquémica ou estrutural, doença valvular cardíaca, endocardite infeciosa e fibrilhação auricular.1,10 A causa trombótica é a implicada em aproximadamente 15-35% dos casos de AMI,2,10 esta também está mais frequentemente associada a oclusões da artéria mesentérica superior proximais junto ao ostium arterial comparando com a embolia, devido à sua relação íntima com fenómenos de aterosclerose mais frequentes a este nível.1,10 No tratamento de AMI embólica a embolectomia cirúrgica aberta é o procedimento habitualmente indicado, no entanto se não houver evidência de necrose intestinal com necessidade de resseção intestinal podem ser tentadas técnicas endovasculares de forma primária, enquanto que na AMI trombótica devem ser empregues inicialmente técnicas endovasculares (mais comummente PTA/Stent, com possibilidade de recurso a outras técnicas como trombectomia mecânica por aspiração do trombo e fibrinólise guiada por cateter) em todos os pacientes que não apresentem evidência de necrose intestinal.12
O uso primário de angioplastia percutânea por balão (PTA)/stent foi o método de escolha em pacientes com IMA de etiologia trombótica, sendo a principal modalidade de tratamento no estudo de Forbrig et al.17 e nos subgrupos de IMA de etiologia trombótica dos estudos de Kärkkäinen JM et al.19 e Acosta S et al..22 Nestes casos as taxas de sucesso técnico foram elevadas [95%,17 84%19 e 100%22], a mortalidade precoce foi mais elevada no estudo de Forbrig et al.17 comparada com as restantes [42%,17 28,1%19 e 18,2%22], com taxas de mortalidade a longo prazo relatadas sobreponíveis entre estudos [34,4%19 e 27,3%22]. O uso de laparotomia foi mais predominante no estudo de Acosta S et al.22 [36,8%17 vs 46,9%19 vs 63,6%22], com taxas de resseção intestinal mais elevadas nas publicações de Kärkkäinen JM et al.19 e Acosta S et al.22 [21,1%,17 37,5%19 e 36,4%22].
Comparando as modalidades de tratamento endovascular nos pacientes com IMA de etiologia embólica destacam-se: a) trombectomia por aspiração do trombo guiada por cateter nos estudos de Raupach J et al.,16 de Jia Z et al.27 e nos subgrupos de IMA de etiologia embólica dos estudos de Kärkkäinen JM et al.19 e de Acosta S et al.;22 b) a trombectomia mecânica no estudo de Freitas B et al.;14 e c) trombólise farmacológica guiada por cateter no estudo de Zhang Z et al..15
O sucesso técnico reportado nos estudos com trombectomia mecânica e trombólise guiada por cateter foi superior [100%14,15] que nos estudos com trombectomia por aspiração [100%,27 91,9%,16 94%19 e 70%22]. A mortalidade precoce foi mais elevada no estudo com recurso à trombectomia mecânica 40%14 e inferior em dois estudos com uso de trombectomia por aspiração 9,5%27 e 10%,22 no entanto nos restantes dois estudos com uso de trombectomia por aspiração relataram-se taxas de mortalidade precoce mais elevadas 27%16 e 39%19. No estudo com recurso à trombólise guiada por cateter a mortalidade precoce situou-se nos 16,7%.15 A taxa de mortalidade a longo prazo foi mais elevada no estudo com recurso à trombectomia mecânica e num dos estudos com uso da trombectomia por aspiração [55,5%14 e 55,6%19], nos restantes e no estudo com recurso a trombólise guiada por cateter as taxas de mortalidade a longo prazo reportadas foram mais favoráveis [9,5%,27 20%22 e 22,2%15].
A taxa de laparotomia foi mais elevada no estudo com recurso à trombectomia mecânica e em 2 com uso da trombectomia por aspiração [70%,14 73%16 e 70%22], os restantes estudos com uso de trombectomia por aspiração e o estudo de trombólise guiada por cateter apresentaram taxas de laparotomia mais baixas [27,8%,19 23,8%27 e 33,3%15]. A taxa de resseção intestinal foi significativamente mais elevada no estudo com uso de trombectomia mecânica 70%14 quando comparada com as dos restantes [33,3%,15 40,5%,16 27,8%,19 23,8%27 e 30%22].
Os resultados dos tratamentos endovasculares primários foram comparados a resultados de tratamento cirúrgico (revascularização cirúrgica) em sete estudos.
Zhang Z et al.15 comparam resultados entre 12 doentes submetidos a terapias endovasculares e 18 doentes submetidos a terapêutica cirúrgica, as terapias endovasculares mostraram necessidade de menor extensão de resseção intestinal em média (88±44 vs 253±103 cm, p=0,01), sendo que não foram encontradas diferenças significativas de mortalidade a 30 dias nem de necessidade de laparotomia secundária.
No estudo de Arya S et al.18 não foram observadas diferenças significativas entre ambos os grupos (11 doentes com tratamento endovascular e 23 com tratamento cirúrgico) em termos de complicações, morbilidade e mortalidade.
Eslami MH et al.24 num estudo multicêntrico com dados de 2003 a 2011 da base de dados norte-americana NIS (National Inpatient Sample) que envolveu 990 pacientes submetidos a tratamento endovascular e 573 submetidos a tratamento cirúrgico, concluiu que apesar do aumento de frequência do uso de terapias endovasculares na IMA, não se demonstraram alterações estatisticamente significativas na mortalidade a longo prazo por IMA. No entanto a mortalidade intrahospitalar (15,3% vs 21,9%, p=0,01), necessidade de resseção intestinal (9% vs 14,9%, p<0,001), duração de internamento hospitalar (p<0,001) e custos medianos de internamento ($73317 vs $101762, p<0,001) foram significativamente inferiores no grupo de tratamento endovascular, apesar de maiores índices de comorbilidades - Elixhauser comorbidities index (3±0,1 vs. 2.7±0,1 p=0,008).
Outro estudo multicêntrico de Branco BC et al.25 com recurso à base de dados norte-americana NSQIP (National Surgical Quality Improvement Program) com dados de pacientes compreendidos entre 2005 e 2010 comparou 3 grupos [27 doentes com tratamento endovascular, 23 com tratamento híbrido (retrograde open mesenteric stenting - ROMS) e 389 com tratamento cirúrgico] e concluiu que o grupo submetido a terapêuticas endovasculares apresentou uma mortalidade a 30 dias inferior (22,2% vs 34,8% vs 40,4% p=0,049). Houve tendência para menor ocorrência de complicações como pneumonia e sepsis, bem como menor necessidade de transfusões de concentrados eritrócitos, no entanto não de forma estatisticamente significativa. Não foram encontradas diferenças significativas em termos de necessidade de resseção intestinal, laparotomia secundária e duração de internamento hospitalar.
Beaulieu RJ et al.26 usando dados da base de dados norte-americana NIS (National Inpatient Sample) compreendidos entre 2005 e 2009, realizaram uma comparação entre 2 grupos (165 pacientes submetidos a tratamento endovascular e 514 submetidos a tratamento cirúrgico). A mortalidade 24,9% vs 39,3% (p=0,01), duração média de internamento hospitalar 12,9 vs 17,1 dias (p=0,006), necessidade de resseção intestinal 14,4% vs 33,3% (p<0,001) e necessidade de nutrição parenteral total 24,4% vs 13.7% (p=0,025) foram inferiores no grupo endovascular.
Na publicação de Arthurs ZM et al.20 foram comparados outcomes de 56 pacientes submetidos a técnicas endovasculares e 14 submetidos a terapêutica cirúrgica, com o grupo submetido a técnicas endovasculares com menores taxas de laparotomia (69% vs 100% p<0,05), menor extensão de resseção de intestino necrótico [mediana e intervalo interquartil (IIQ): 52 cm (11-140 cm) vs 160 cm (90-250 cm), p<0,05], menor incidência de lesão renal aguda (27% vs 50%, p<0,05) e de insuficiência respiratória (27% vs 64%, p<0,05). Na mortalidade geral não foram observadas diferenças significativas, no entanto no subgrupo de IMA de etiologia trombótica a mortalidade foi inferior no grupo submetido a terapêutica endovascular [odds ratio (OR): 0,1, IC a 95% de 0,1-0,76, p<0,05].
Um estudo multicêntrico de Block TA et al.21 com recurso à base de dados sueca Swedish Vascular Registry (Swedvasc) analisou e comparou dados de 121 pacientes submetidos a revascularização cirúrgica e 42 pacientes submetidos a procedimentos endovasculares entre 1999 e 2006. O grupo endovascular apresentou menores taxas de laparotomia (55% vs 100%, p<0,001), menor taxa de resseção intestinal (19% vs 63%, p<0,001), menor incidência de síndrome do intestino curto (27% vs 55%, p=0,009) e menor necessidade de laparotomia de second-look (31% vs 67%, p<0,001). A mortalidade a 30 dias (24% vs 42%, p=0,03) e a 1 ano (38% vs 59%, p=0,02) foi significativamente inferior no grupo endovascular, bem como a mortalidade estimada a longo prazo (p=0,02).
Isquemia mesentérica aguda de etiologia venosa
A isquémia mesentérica aguda de etiologia venosa/trombose venosa mesentérica representa 5-15% dos casos de isquémia mesentérica.2,10 Esta pode ser idiopática ou secundária na maioria dos casos (90%) a estados de hipercoagulabilidade como trombofilias e neoplasias, cirrose e hipertensão portal, patologia inflamatória abdominal como pancreatite, diverticulite e patologia infeciosa/inflamatória do trato biliar.2,10 O tratamento passa por anticoagulação sistémica com heparina não fracionada; nos doentes em que não há melhoria clínica pode ser necessário o uso de tratamentos mais invasivos como trombectomia cirúrgica ou endovascular, trombólise farmacológica sistémica ou guiada por cateter.12,13
Realizando uma comparação dos outcomes dos estudos incluídos nesta revisão, Rabuffi P et al.28 e Wang MQ et al.32 reportam em toda a amostra o uso combinado de trombectomia mecânica com aspiração do trombo e trombólise farmacológica guiada por cateter, Yang S et al.29 e Yang S. et al.31 reportam o uso isolado de trombólise farmacológica guiada por cateter, sendo de realçar que no estudo de 2016 de Yang S. et al.29 todos os pacientes foram submetidos a resseção intestinal emergente primariamente, portanto não é possível comparar os dados de forma fiel com os restantes. No estudo de Wichman HJ et al.30 o tratamento ao qual todos os pacientes foram submetidos foi stenting ± angioplastia primária por balão, com recurso às restantes técnicas em 62,5% dos doentes.
O sucesso técnico nos quatro estudos foi de 100% e o sucesso clínico foi máximo (100%) no estudo de Yang S et al.31 e na publicação de Wang MQ et al.,32 nos restantes foi de 87,5%.28,30 Rabuffi P et al.28 apresentou a taxa de recorrência mais elevada, esta foi inferior no estudo de Wichman HJ et al.30 (12,5%) e nos restantes foi de 0%.31,32 Nestes últimos a mortalidade precoce foi mais favorável [0%31,32] comparando com as publicações de Wichman HJ et al.30 e Rabuffi P et al.28 (12,5%). A mortalidade a longo prazo foi superior no estudo com recurso a stenting [25%30] e inferior num dos estudos com recuso a trombectomia mecânica + trombólise [0%32]. Nos restantes foi de 12,5%28 e 7,7%.31
Apenas o estudo com uso isolado de trombólise farmacológica reporta a necessidade do uso de intervenções pós tratamento endovascular, sendo que 30,8% dos pacientes foram submetidos a laparotomia e consequente resseção intestinal e outros 30,8% a laparoscopia.31
No estudo de 2016 de Yang S. et al.29 são avaliados os outcomes de um grupo de 15 pacientes em que é realizado tratamento com trombólise farmacológica guiada por cateter colocado na artéria mesentérica superior (urokinase 100.000 UI bolus + 600.000UI/dia + papaverina 120 mg/dia até 72h após a cirurgia, posteriormente heparina de baixo peso molecular (HBPM) 80UI/kg/dose, dose bidiária), desta feita após trombectomia aberta e resseção intestinal emergente, comparando com outro grupo de 17 doentes em que é realizada no pós operatório apenas anticoagulação sistémica (heparina de baixo peso molecular (HBPM) 80UI/kg/dose, dose bidiária 12h após a cirurgia). Concluiu-se que o grupo da trombólise guiada por cateter apresentou maiores taxa de remoção completa do trombo (80% vs 29,4% vs p = 0,001), menor necessidade de laparotomia de second-look (20% vs 70,6%, p=0,001) e de nova resseção intestinal posterior (13,3% vs 58,8% p=0,002), bem como consequentemente de menor incidência de síndrome do intestino curto (6,7% vs 41,2%, p=0001). A mortalidade a 30 dias (6,7% vs 41,2%, p=0,001) e a 1 ano (52,9% vs 93,3%, p=0,014) foram significativamente inferiores no grupo de trombólise guiada por cateter. A diferença nas taxas de incidência de hemorragia abdominal com necessidade de intervenção cirúrgica e transfusão de concentrados de eritrócitos não foi estatisticamente significativa entre os dois grupos.
O estudo de 2014 de Yang S. et al.31 teve por objetivo avaliar qual o tratamento inicial com melhores resultados em doentes com IMA por trombose da veia mesentérica superior com peritonite circunscrita e suspeita de necrose intestinal. Foram comparados outcomes de um grupo de 12 pacientes que são submetidos primariamente a exploração cirúrgica emergente (trombectomia aberta e/ou resseção intestinal) a outro grupo de 13 pacientes que são submetidos a trombólise farmacológica guiada por cateter por via transhepática percutânea/ transjugular intrahepática ou via artéria mesentérica superior (urokinase 100.000 UI bolus + 200.000/300.000 UI/dia ± papaverina 120 mg/dia). Em ambos os grupos os doentes foram anticoagulados com fondaparinux sódico 5 mg/dia oral e argatroban 80 mL/dia endovenoso. O grupo submetido a trombólise guiada por cateter apresentou menor duração média de internamento hospitalar (20,46 ± 6,59 dias vs 43 ± 13,77 dias, p<0,001), menor período para a remissão de sintomas desde a admissão (7,23 ± 2,42 dias vs 18,25 ± 7,69 dias, p<0,001), reposição de nutrição oral/entérica mais precoce (8,92 ± 1,89 dias vs 20,5 ± 5,13 dias, p<0,001), menores extensões intestinais ressecadas (29,23 ± 50,24 cm vs 170,83 ± 61,27 cm, p<0,001) e menores custos totais associados ao internamento (72785,6 ± 21828,16¥ vs 2000020,4 ± 91505,62¥, p=0,001). Não foram observadas diferenças estatisticamente significativas nos dois grupos em termos de taxas de morbilidade, mortalidade a 30 dias e mortalidade a 1 ano.
Limitações
Uma das limitações desta revisão prende-se com o facto de os estudos analisados serem na sua totalidade retrospetivos (baseados num único centro ou multicêntricos) e com amostras pouco significativas em que se objetivou uma grande heterogeneidade entre técnicas endovasculares utilizadas, a sua utilização de forma isolada ou combinada dependendo da sua disponibilidade/estado clínico de cada doente e fármacos administrados [exemplo: alteplase (rtPA)/urokinase (uPA)] e em algumas publicações ausência de dados relativos às modalidades terapêuticas utilizadas. Portanto, com os dados dos estudos disponíveis, não é possível comparar de forma altamente fidedigna os outcomes associados a cada técnica endovascular individualmente, por inexistência de estudos a larga escala, comparando as diferentes técnicas individualmente.
Outra das limitações relaciona-se com a comparação de resultados de revascularização cirúrgica com técnicas endovasculares na medida em que os protocolos de gestão intrahospitalar de doentes com IMA apresentam alguma heterogeneidade. Em alguns casos é possível a existência de viés de seleção com uso das técnicas endovasculares em detrimento de revascularização cirúrgica em pacientes com maiores comorbilidades não candidatos a cirurgia. De outro ponto de vista também se pode verificar que no caso de pacientes em estado mais grave com maior tempo de duração de isquemia e maior probabilidade de necrose intestinal, estes serem mais provavelmente propostos para tratamento cirúrgico em detrimento do uso de técnicas mais conservadoras.
Conclusão
Tendo em conta a evidência disponível é possível concluir que o uso crescente de técnicas endovasculares no tratamento da isquémia mesentérica aguda de etiologia arterial e venosa contribui para a melhoria dos outcomes associados a esta patologia que continua a estar associada a um prognóstico sombrio.
Estas modalidades de tratamento mais conservadoras são especialmente relevantes em doentes com diagnóstico mais atempado. Nestas situações há uma maior probabilidade de sucesso das terapêuticas endovasculares, obviando tratamentos cirúrgicos nomeadamente em contexto emergente, com altas taxas de morbimortalidade.
















