INTRODUÇÃO
A celulose é obtida diretamente de material vegetal fibroso e o facto de se acrescentarem a este polissacarídeo grupos etil-, metil- e carboximetil-, pode aumentar a resistência da celulose à degradação (1, 2).
A carboximetilcelulose de sódio (CMC) é um tipo de éter de celulose linear, onde os grupos -OH são substituídos por grupos carboximetil (−CH2-COOH), o que a torna um polissacarídeo aniónico linear, hidrossolúvel e de cadeia longa (3-5).
Este composto apresenta uma vasta gama de aplicações na indústria alimentar, e na saúde, sendo também utilizado em combinação com outros compostos para a melhoria das suas caraterísticas e consequentemente do produto desenvolvido (2, 3, 6, 7).
Quando os alimentos são armazenados por um período prolongado, o uso de aditivos é essencial para manter a sua qualidade e consistência, conferindo atividade antimicrobiana e antioxidante (8). A CMC é um aditivo alimentar, ou seja, uma substância natural ou artificial que é intencionalmente adicionada para alterar as propriedades químicas e físicas dos alimentos, com interesse crescente no mundo científico devido às características provenientes da celulose e ao seu carácter polieletrólito (9). Esta pode ser adicionada aos alimentos como revestimento, estabilizante, emulsionante sintético, espessante, ligante, humidificante, antiaglomerante e gelificante (8-10).
Em resposta a preocupações crescentes deste aditivo, a European Food Safety Authority (EFSA) realizou um pedido de dados técnicos e toxicológicos sobre a CMC para utilizações como aditivo alimentar em alimentos para todos os grupos populacionais, incluindo bebés com menos de 16 semanas (1, 9, 11).
A CMC, classificada na Europa como E466 ou E469, quando hidrolisada enzimaticamente, está atualmente autorizada como aditivo alimentar para todas as espécies animais, sem um conteúdo mínimo e máximo, em conformidade com o anexo II do Regulamento (CE) n.º 1333/2008, com critérios de pureza específicos definidos no Regulamento (UE) n.º 231/20124 da Commission Regulation (8, 11). O objetivo deste artigo de revisão é estudar a CMC, as suas aplicações, a sua toxicidade e a extensão do seu impacto na saúde humana.
METODOLOGIA
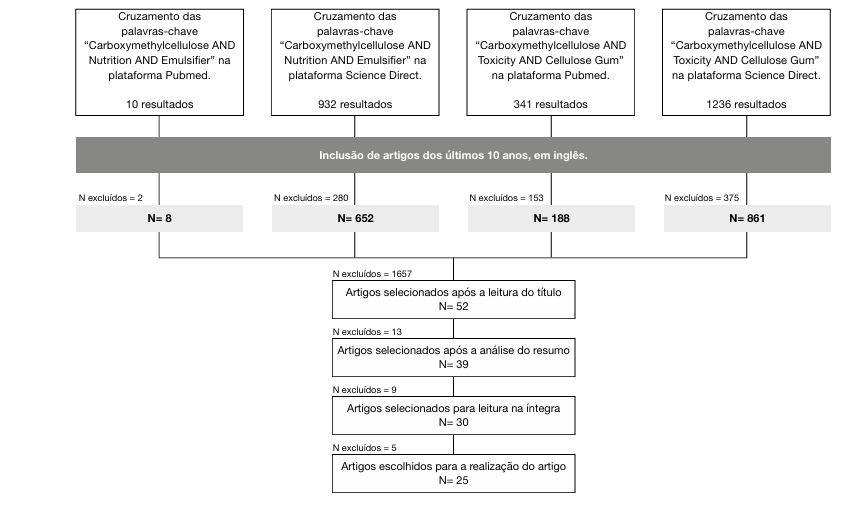
Esta revisão bibliográfica foi elaborada por cinco investigadoras, com base na pesquisa de literatura de carácter científico nas bases de dados Pubmed e Sciencedirect, utilizando as palavras-chave "Carboxymethylcellulose’’ AND ‘’Cellulose Gum’’ AND ‘Nutrition’’ AND ‘Toxicity’’ AND ‘Emulsifier" e verificou-se que as mesmas estavam presentes na lista dos DeCS (Descritores em Ciências da Saúde), num intervalo de tempo de 10 anos. Para diminuir a dimensão da pesquisa e de forma a atingir o objetivo do trabalho, foram aplicados filtros, tais como intervalo de tempo entre 2012 e 2022 e na língua inglesa. Por fim, na gestão das referências bibliográficas foi utilizado o software Mendeley. Não foi possível colocar todas as palavras-chave numa só pesquisa, uma vez que, desse modo, não foram obtidos resultados, portanto foi necessário dividi-las por duas pesquisas. Nas bases de dados Pubmed e Science Direct, após o cruzamento das palavras-chave ‘’Carboxymethylcellulose AND Nutrition AND Emulsifier’’ e a aplicação dos filtros, foram obtidos 8 e 652 resultados, respetivamente. Nas bases de dados Pubmed e Science Direct, após o cruzamento das palavras-chave ‘’Carboxymethylcellulose AND Toxicity AND Cellulose Gum’’ e a aplicação dos filtros, foram obtidos 188 e 1859 resultados, respetivamente.
Dos resultados provenientes dos dois cruzamentos de palavras-chave, foram primeiro selecionados 52 artigos pelo título, 39 após análise do resumo e, de seguida, 30 para leitura na íntegra, sendo posteriormente selecionados 25 artigos científicos para a elaboração do artigo de revisão, como é possível observar no fluxograma da Figura 1.
No que diz respeito aos critérios de exclusão, foram excluídos todos os artigos publicados anteriormente a 2012, assim como aqueles que não se enquadravam na temática.
Aplicações
A CMC possui uma vasta gama de aplicações devido às suas propriedades e à sua versatilidade, sendo que ainda estão a ser investigadas as áreas de utilização e aprimoradas as suas propriedades juntamente com outros compostos. Na Tabela 1consta um resumo dos artigos com os principais tópicos abordados acerca das aplicações da CMC em alimentos e os seus efeitos.
Tabela 1 Descrição dos estudos acerca das aplicações da carboximetilcelulose de sódio nos alimentos
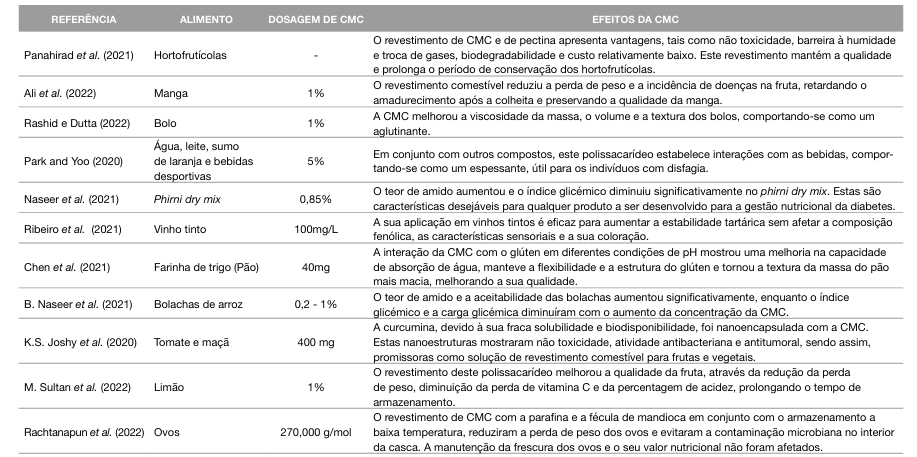
CMC: Carboximetilcelulose de sódio
A solubilidade dos alimentos pode ser modificada pela adição de CMC, o que foi comprovado por Naseer B et al., que mostraram que o aumento da concentração de CMC diminuiu o índice de insolubilidade num produto em pó utilizado para fabricar Phirni, uma sobremesa láctea tradicional na Índia. As partículas de CMC são adsorvidas nas partículas de leite em pó, aumentando a sua hidrofilicidade (12).
A CMC é habitualmente utilizada também como aditivo enológico na estabilização tartárica do vinho branco, dado que a formação de cristais no vinho engarrafado é causada pela instabilidade do tartarato, um fenómeno que se desenvolve naturalmente no vinho. Num estudo desenvolvido por Filipe-Ribeiro L et al., a CMC não diminuiu a estabilidade da cor dos vinhos tintos, nem afetou a quantidade e natureza do material em suspensão, quando comparado com o vinho de controlo. A utilização de CMC em vinho tinto, embora ainda não autorizada pela Organização Internacional da Vinha e do Vinho, seria benéfica devido às suas propriedades (13).
Este composto também tem sido amplamente utilizado na massa do pão com glúten, por exemplo. No estudo de Chen Y et al. foi sugerido que a CMC melhorou a capacidade de retenção de água, formou uma textura mais suave e manteve a elasticidade e a estrutura do glúten tanto num estado neutro como alcalino (14).
Além de ser utilizada na formulação de produtos com glúten, a CMC é igualmente utilizada para combater os desafios tecnológicos da cozedura sem glúten em produtos de padaria e pastelaria. Num estudo de Naseer B et al., realizado em bolachas, as condições de cozedura e concentração de CMC afetaram significativamente a qualidade destas. Com o aumento da concentração de CMC, o teor de amido e a capacidade de aceitação global das bolachas aumentaram, enquanto que o índice e a carga glicémica e a dureza diminuíram. Observou-se que este composto compete pela água e restringe a gelatinização e hidrólise do amido durante a cozedura, resistindo assim ao ataque das enzimas digestivas. Assim sendo, o desenvolvimento de produtos de panificação de baixa carga glicémica, incorporando uma percentagem de CMC, deve ser testado no futuro em produtos destinados a celíacos e diabéticos (15). Noutro estudo de Rashid S et al., concluiu-se também que a incorporação da CMC melhorou as propriedades sensoriais e funcionais do bolo analisado (5).
O estudo de Karakus S et al. teve como objetivo obter um novo nanomaterial conservante antimicrobiano e antifúngico, a partir do biopolímero CMC, como agente estabilizador, e estromatólito de hidromagnesite (HS), como aditivo natural fossilizado. Provou-se que a junção dos bionanocompostos CMC e HS tinham efeitos não tóxicos e de citocompatibilidade, excelentes atividades antibacterianas e antifúngicas, e assim, poderiam ser adequados como nanoaditivos conservantes alternativos contra microrganismos patogénicos (16).
O desenvolvimento de embalagens inovadoras, seguras e sustentáveis é uma grande preocupação para a indústria alimentar, que visa conservar os alimentos e minimizar o desperdício em toda a cadeia de distribuição, garantindo produtos de alta qualidade com maior vida útil. Portanto, uma boa opção seria substituir polímeros não renováveis por biopolímeros, biodegradáveis e de fácil acesso e produção, como as películas de CMC (9, 11, 17).
A espessura é um dos fatores importantes das películas biodegradáveis, uma vez que pode afetar as suas propriedades de barreira bem como as propriedades mecânicas. Num estudo realizado por Mirzaei Mohkam A et al., a adição de Vitamina E nanoencapsulada às películas biodegradáveis de CMC aumentou o valor da espessura, diminuiu significativamente a permeabilidade e levou a algumas alterações nas estruturas poliméricas, afetando as propriedades mecânicas das peliculas. Além disso, diminuiu a transferência de radiações UV e visíveis, resultando não só num papel mais eficaz na eliminação de radicais livres, mas também na melhoria do desempenho funcional das películas (18).
As películas de CMC atuam ainda como um revestimento comestível na fruta, funcionando como uma barreira eficaz entre o produto tratado e a atmosfera circundante, conduzindo subsequentemente à troca de gases e ao desenvolvimento de uma atmosfera interna modificada, geralmente constituída por um baixo teor de oxigénio e um elevado teor de dióxido de carbono, o que atrasa a atividade metabólica e o rápido amadurecimento da fruta (3, 19, 20).
O revestimento de CMC é ainda conhecido pela sua hidrofobicidade, o que limita a dessecação devido à formação de uma camada semi permeável resistente à água em redor da superfície da fruta (3). Este tem sido amplamente aplicado nos últimos anos, particularmente devido à sua disponibilidade e baixo preço, transparência, não apresentando sabor nem odor (2, 21, 22).
Ali S et al. concluíram que o tratamento com CMC antes do armaze namento reduziu a perda de peso em mangas, pêssegos e mirtilos e inibiu a ocorrência de doenças, pois este atua como uma barreira contra diferentes agentes patogénicos. Para além disso, suprimiu a acumulação total de carotenóides na casca da manga, atrasando as mudanças de cor (2, 3).
Além disso, a CMC tem sido utilizada como revestimento de casca de ovo, sendo que Rachtanapun P et al. concluíram que este revestimento aumenta o prazo de validade, dado que ao revestir a superfície do ovo preserva a qualidade do conteúdo interno, aumenta a resistência e diminui a carga microbiana na superfície da casca do ovo (21).
Potenciais Efeitos na Saúde e Toxicidade
Embora a CMC seja passível de ser amplamente utilizada em diversas áreas, é crucial compreender cuidadosamente os potenciais efeitos na saúde associados ao seu uso. Na Tabela 2 consta um breve resumo da literatura analisada, destacando os principais tópicos abordados sobre os efeitos da CMC na saúde.
Tabela 2 Descrição dos estudos acerca dos efeitos da carboximetilcelulose de sódio na saúde
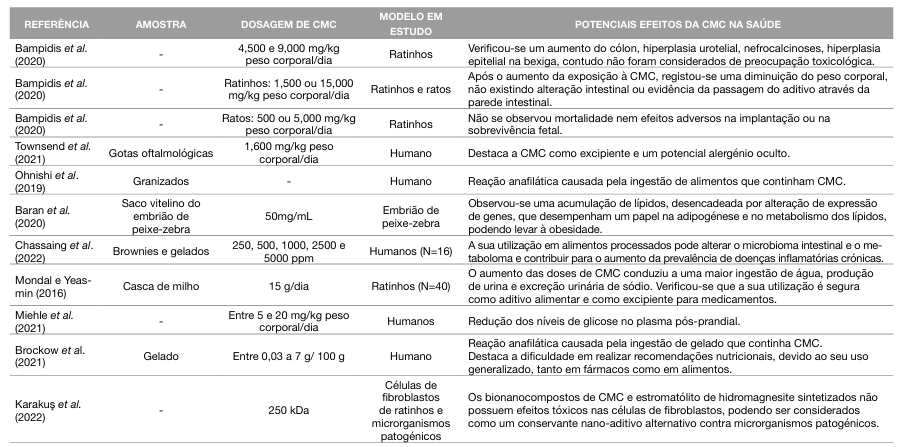
CMC: Carboximetilcelulose de sódio
Hamid et al. relataram que para determinar a segurança de um produto químico ou fármaco para o ser humano, a avaliação toxicológica é realizada em animais experimentais, de forma a prever a toxicidade e, consequentemente, fornecer orientações para a seleção de uma dose segura em humanos (8).
Os embriões de peixe-zebra foram estudados por Baran A et al. e foi demonstrado que a exposição à CMC não causa qualquer efeito tóxico nas doses aplicadas, nem afetou a eclosão da espécie. Porém, ocorreu, pela primeira vez, uma acumulação de lípidos nos embriões expostos de forma dose-dependente, podendo conduzir a efeitos no metabolismo lipídico, ao causar alterações na expressão de alguns genes que poderão levar à obesidade (9).
Já Mondal MIH et al. tiveram como objetivo determinar a toxicidade da CMC, após administração oral em ratinhos. As enzimas hepáticas não apresentaram aumento ou diminuição apreciável, o que demonstra que o composto não tem efeito hepatotóxico. Como não teve efeito tóxico para as hemácias dos animais nem interferiu na sua produção, os autores afirmaram que a CMC também não é hematotóxica. Na análise bioquímica realizada, a CMC aumentou significativamente os valores de glicose e colesterol séricos em comparação com o grupo de controlo e diminuiu significativamente os valores de triglicerídeos séricos. No entanto, esses valores permaneceram dentro da faixa de normalidade durante todo o período experimental, sendo mais um parâmetro que indica que não se verifica toxicidade da CMC (8). Um artigo publicado pela EFSA refere que estudos também realizados em ratinhos, com valores entre 4,500 e 9,000 mg de CMC/ kg de peso corporal/ dia, observaram alguns efeitos (aumento do cólon, hiperplasia urotelial, nefrocalcinoses, hiperplasia epitelial difusa na bexiga urinária), no entanto, não foram considerados de preocupação toxicológica. Ainda neste artigo, mas com base num conjunto limitado de dados, estudos de toxicidade de exposição crónica realizados em ratinhos revelaram um atraso no crescimento, principalmente num nível de dosagem mais elevado, contudo, a CMC não revelou efeitos carcinogénicos (1).
Ainda segundo a EFSA, a utilização da CMC como aditivo alimentar é considerada segura para o ambiente, o que foi comprovado pela observação da degradação microbiana e, para além disso, a adição do composto na alimentação animal não é motivo de preocupação para a segurança dos mesmos (1).
O Panel on Additives and Products or Substances used in Animal Feed (FEEDAP) da EFSA afirmou, em 2018, que considera desnecessário estabelecer uma dose diária aceite para a CMC, com base numa baixa toxicidade e numa absorção negligenciável no trato gastrointestinal humano. Embora existam alguns estudos que afirmam que este aditivo tem alguns efeitos negativos em ratinhos, foi relatado na maioria dos estudos que a CMC não é tóxica (1, 9).
Impacto na Microbiota Intestinal
Alguns tipos de fibras dietéticas solúveis, como a CMC, reduzem a absorção de açúcar através da alteração da viscosidade do conteúdo intestinal. Um dos muitos benefícios para a saúde deste tipo de fibras inclui a redução do nível de glicemia pós-prandial, o que é significativo para indivíduos com tolerância à glicose reduzida ou com Diabetes Mellitus tipo 2 (23).
Um estudo realizado em ratos por Mondal e Yeasmin, demonstrou que a CMC poderia alterar a microbiota intestinal, promover a inflamação da gota, a obesidade e prejudicar o controlo glicémico (9).
Apesar da falta de testes de segurança extensivos, a CMC foi aprovada nos anos 60 para utilização em alimentos em concentrações até 2% (p/p) por agências reguladoras, incluindo a US Food and Drug Administration e a Comissão Europeia, com base na designação GRAS (geralmente considerada segura) desenvolvida por estas agências. Presume-se que a CMC e outros emulsionantes são seguros devido ao facto de não serem facilmente absorvidos pelo organismo e, portanto, na sua maioria, eliminados nas fezes. Contudo, tal passagem através do intestino permite que estes produtos interajam diretamente com a microbiota intestinal (10).
Chassaing B et al. centraram-se nos impactos a curto prazo da CMC, sendo que a adição de 15 g por pessoa deste composto a uma dieta saudável aumentou o desconforto abdominal pós-prandial, alterou a composição da microbiota intestinal de uma forma aparentemente prejudicial e teve um forte impacto no metaboloma fecal, o que sustenta a noção de que a ampla utilização deste composto em alimentos pode ter contribuído para o aumento da incidência de doenças inflamatórias crónicas (10).
As concentrações deste composto em alimentos preparados não são amplamente relatadas, tornando extremamente difícil estimar quantitativamente o consumo de aditivos alimentares em humanos. A dose de CMC utilizada no estudo relatado anteriormente excede provavelmente a ingestão de CMC da maioria dos indivíduos. Contudo, esta dose pode aproximar-se da quantidade total de consumo de emulsionantes por pessoas cujas dietas são em grande parte constituídas por alimentos altamente processados, que contêm numerosos emulsionantes, muitos dos quais parecem afetar negativamente a microbiota humana in vitro (10).
Anafilaxia
A anafilaxia à CMC é rara e tem sido associada a produtos farmacêuticos que contenham este composto, contudo pode estar subdiagnosticada, uma vez que a CMC é cada vez mais utilizada no quotidiano em diferentes alimentos e por isso, têm sido reportados casos de anafilaxia à CMC associada a estes (11, 24). Em Ohnishi A. et al., foi relatado o primeiro caso de anafilaxia causada por produtos alimentares numa criança com 14 anos que consumiu um gelado que continha CMC (24).
Em Townsend K et al., foi reportado outro caso em que foi consumido um gelado que continha CMC, cujos sintomas alérgicos sofreram um atraso de três a quatro horas. Os autores do artigo atribuíram este atraso nos sintomas, ao facto dos seres humanos carecerem da enzima celulase para digerir a CMC e, portanto, os metabolitos só são absorvidos em pequenas quantidades, dependendo da digestão microbiana gastrointestinal. Nomeadamente, como o paciente em questão tinha ingerido uma refeição com elevado volume juntamente com o gelado, pode ter contribuído para um atraso na absorção intestinal e, por conseguinte, para um atraso na reação alérgica. Os autores afirmam que é importante identificar excipientes como a CMC, como causas de alergia, para reduzir a carga de outras reações de hipersensibilidade, não só a medicamentos, mas também a outros alimentos. Além disso, este caso chama também à atenção para a nomenclatura variável de excipientes como a CMC, também conhecida E469 quando hidrolisada enzimaticamente, que pode representar uma dificuldade na evicção da exposição ao alergénio, para doentes afetados (11).
As recomendações nutricionais para estes indivíduos são difíceis de estabelecer, devido à utilização generalizada da CMC. Embora exista a obrigação pela US Food and Drug Administration de declarar a CMC nos rótulos das embalagens alimentares, não é obrigatória nos alimentos não embalados, sendo necessário ter um cuidado acrescido (25).
ANÁLISE CRÍTICA
A CMC é um composto que apresenta diversas características, tornando possível a sua aplicação em vários campos da indústria alimentar.
Globalmente, a informação disponível permite concluir que a CMC, como aditivo alimentar, é de baixa preocupação a nível toxicológico, sendo considerada segura para a maior parte das espécies animais, não existindo estipulação de uma dose diária máxima para humanos. Apesar de cada vez mais existirem estudos sobre estes derivados de celulose, a maioria são realizados em animais e os efeitos secundários e tóxicos deste composto ainda não foram totalmente elucidados em humanos. Assim, torna-se necessário analisar os efeitos toxicológicos da CMC mais minuciosamente, avaliar com precisão os seus riscos para a saúde humana para uma utilização mais segura e perceber se as vantagens do uso desta superam os possíveis riscos que esta possa acarretar (1).