Introdução
A fibromialgia é uma síndrome de dor musculoesquelética generalizada, crónica e de etiologia desconhecida, com elevado impacto na qualidade de vida e funcionalidade dos doentes, acarretando custos pessoais, sociais e de saúde significativos.1 De acordo com a definição mais recente (2010) do Colégio Americano de Reumatologia, a fibromialgia carateriza-se pela presença de dor generalizada com duração superior a 3 meses, associada à sensibilidade dolorosa aumentada em 11 ou mais dos 18 pontos de pressão específicos, na ausência de doenças somáticas que possam explicar os sintomas, sendo por isso considerada um diagnóstico de exclusão.2 As pessoas com fibromialgia frequentemente reportam pobre qualidade do sono, fadiga, depressão, alterações cognitivas e altos níveis de incapacidade, que culminam numa baixa qualidade de vida e um grande consumo de serviços de saúde e opioides.2
A fibromialgia é uma doença comum, com uma prevalência global de 2,5%-9,3%, 3,1% no continente americano e 2,5% na Europa.2 A sua prevalência na população geral portuguesa é de 2% a 4%, estimando-se que represente de 5% a 10% das consultas de Medicina Geral e Familiar e até 15% das consultas de Reumatologia.1 A fibromialgia é mais comum em mulheres do que homens (3:1) e em trabalhadores da indústria têxtil e metalúrgica, podendo atingir uma prevalência superior a 50% em grupos expostos a lesões de estiramento repetitivas.2
A etiopatogenia da fibromialgia é desconhecida, aceitando-se atualmente que seja o resultado de uma interação entre fatores biológicos e psicológicos.2 Várias condições que se associam a maior probabilidade de ter fibromialgia já foram identificadas: depressão, obesidade, sedentarismo, abuso físico, sexual ou psicológico na infância, insónia, stress psicológico de longa duração, stress físico (acidentes, cirurgias, infeções podem atuar como fatores despoletantes).2 As alterações fisiológicas associadas à fibromialgia são alterações no processamento central da dor, aumento das citocinas pró-inflamatórias e diminuição das anti-inflamatórias, distúrbios dos neurotransmissores dopamina e serotonina e patologia da fibra nervosa.2
O tratamento da dor da fibromialgia é um desafio para a prática clínica, com apenas uma minoria dos pacientes a reportar benefícios terapêuticos relevantes com as terapêuticas convencionais.2 Apesar de os opioides não apresentarem uma eficácia clinicamente relevante no tratamento da dor da fibromialgia, estes são largamente utilizados. O consumo epidémico de opioides levanta a necessidade de alternativas farmacológicas para o tratamento da dor crónica. Uma possível alternativa que tem vindo a ser estudada são os canabinoides provenientes da planta de canábis (Cannabis sativa L.).3 A utilização medicinal da planta de canábis para o tratamento de diferentes patologias está amplamente documentada em inúmeras civilizações desde 2700 anos a.C.4 A planta de canábis contém mais de 500 fitoquímicos, dos quais mais de 100 são fitocanabinoides, sendo que dois têm particular interesse para a Medicina: o delta 9-tetrahidrocanabinol (THC) e o canabidiol (CBD).3
O sistema endocanabinoide (SEC) é um sistema biológico modulador presente em todos os mamíferos composto pelos recetores canabinoides e pelos canabinoides endógenos, nomeadamente a anandamida (ANA) e o 2-araquidonoil glicerol (2-AG).3 Este sistema tem três principais funções nos mamíferos: 1) promoção da homeostasia em resposta ao stress, através da regulação dos sistemas nervoso, endócrino e comportamental; 2) regulação energética, através da regulação do apetite, armazenamento e utilização da energia; 3) modulação do sistema imune e da resposta inflamatória.2,3 O SEC participa ainda em múltiplas funções fisiológicas, como a antinociceção, cognição, humor, memória, função endócrina, ação sobre náuseas e vómitos e modulação imune e inflamatória.2,3
Os canabinoides endógenos (ANA e 2-AG) e exógenos (THC e CBD) exercem os seus efeitos farmacológicos através dos recetores canabinoides tipo 1 (CB1) e tipo 2 (CB2): o recetor CB1 é expresso maioritariamente no sistema nervoso central, enquanto o CB2 é expresso maioritariamente nas células do sistema imunitário.2,3
O THC é um agonista parcial do recetor CB1, com efeitos psicotrópicos, analgésicos e que interfere com a cognição e a função motora.3 O CBD é antagonista do recetor CB2 e agonista do recetor 5-HT e do recetor vaniloide tipo 1 com igual potência que a capsaicina.3 O CBD não possui efeitos psicotrópicos, mas afeta o humor e a cognição, participa na modulação da dor, tem efeitos anti-inflamatório, antioxidante e imunomodulador. É também um antagonista farmacodinâmico do THC, que contrabalança os efeitos negativos do THC na memória, humor e cognição.3
A distribuição dos recetores canabinoides no cérebro, com maior densidade na região límbica e frontal, sugere que os canabinoides atuam preferencialmente na dimensão afetiva da dor, a componente responsável pela sensação de sofrimento associada à dor.3 Assim, o sistema endocanabinoide parece funcionar como um sistema tampão, que “amortece” os efeitos do stress através da modulação da emoção e das funções cognitivas.3
Metodologia
Para responder ao objetivo deste trabalho foi elaborada uma revisão baseada na evidência (RBE). Foi colocada a questão PICO: “Nos doentes com fibromialgia (População), o uso de canabinoides (Intervenção), em comparação com a terapêutica convencional (Controlo), tem algum benefício no tratamento da doença (Outcome)?”.
Foi realizada a pesquisa de artigos científicos, na língua portuguesa, espanhola e inglesa, publicados nos últimos 5 anos, nas categorias de ensaio clínico randomizado, guidelines, meta-análise (MA) e revisão sistemática (RS) nas bases de dados PubMed, Cochrane e do National Institute for Health and Care Excellence - NICE, no dia 16 de maio de 2022, utilizando as palavras-chave: (fibromyalgia [MeSH] AND cannabinoids [MeSH]) OR (cannabis).
Foram excluídos os estudos que não se enquadram no objetivo desta RBE ou duplicados. Para atribuição do nível de evidência (NE) e da força de recomendação (FR), foi utilizada a escala Strength of Recommendation Taxonomy (SORT), da American Academy of Family Physician.5
A seleção dos artigos foi feita em duplicado por 5 autores, com uma taxa de concordância final de 100%. A leitura integral, a avaliação do NE e da FR e a supervisão final do artigo foram realizadas por todos os autores.
Esta revisão foi elaborada com base nas recomendações de PRISMA for systematic review protocols (PRISMA-P).6
Resultados
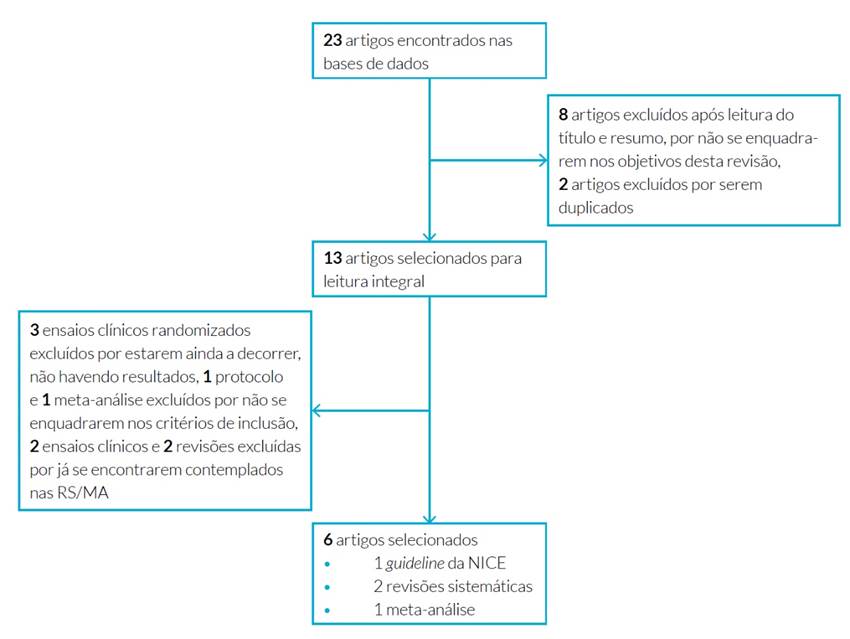
Da pesquisa na PubMed foram encontrados 9 artigos, tendo sido excluídos três por não responderem à PICO, 2 por já se encontrarem contemplados nas revisões sistemáticas/MAs incluídas e 1 por não se enquadrar nos critérios de inclusão. Da base de dados Cochrane foram encontrados 13 artigos, tendo sido excluídos cinco por não responderem à PICO, dois duplicados, três ensaios clínicos por ainda estarem a decorrer e um ensaio e uma revisão por já se encontrarem contemplados numa RS. Da NICE foi encontrada uma guideline acerca do uso de canabinoides que foi incluída neste artigo. Na Fig. 1 está representado o fluxograma de seleção de artigos. Na Tabela 1 encontram-se descritos os estudos incluídos nesta RBE.
Na RS realizada por Khurshid H et al7 foram incluídos 22 estudos. Destes fazem parte 12 revisões clássicas, 3 revisões sistemáticas, 2 ensaios clínicos e 5 estudos observacionais. O objetivo desta RS é averiguar os benefícios terapêuticos dos canabinoides, assim como as suas características e os seus efeitos no tratamento da fibromialgia. As revisões mais antigas concluíam que o uso de nabilona e dronabinol estavam associados a mais efeitos adversos e baixa tolerância. Por outro lado, as revisões mais recentes mostraram que o uso de canabinoides no tratamento da fibromialgia era seguro, eficaz, tinha uma eficácia superior ao placebo e estava associado a uma maior redução da escala visual da dor (EVD). Os restantes estudos demonstraram que o tratamento da fibromialgia com canabinoides era vantajoso, com poucos efeitos adversos. Khurshid H et al,7 reconhecem que os canabinoides são uma opção terapêutica, quando as restantes já foram utilizadas, contudo, como a patogénese da fibromialgia e os mecanismos pelos quais os canabinoides atuam na dor ainda não estão totalmente esclarecidos, os autores da revisão concluíram que são precisos mais estudos para melhor caracterizar o papel dos canabinoides no tratamento da fibromialgia.
Kurlyandchik I et al8 realizaram uma RS onde se incluíram 10 ensaios em humanos submetidos a tratamento com canábis medicinal. Três eram ensaios randomizados, seis eram estudos observacionais e um comparava a dor crónica de doentes com fibromialgia submetidos a diferentes terapêuticas farmacológicas. O objetivo desta revisão era avaliar o impacto do tratamento com canabinoides na redução da dor, qualidade de vida e presença de efeitos adversos, em doentes com fibromialgia tratados com formulações orais de dronabinol e nabilona ou produtos derivados da planta cannabis. Nestes ensaios participaram 1136 pacientes e como outcomes foram avaliados efeitos na saúde reportados pelos pacientes, os efeitos secundários e qualidade de vida. Os efeitos secundários mais comuns foram a sonolência, tonturas, desorientação, cansaço, náuseas e diminuição da coordenação e concentração. Estes efeitos devem-se principalmente ao THC e são amplificados quando o método de absorção é a inalação versus ingestão. Esta revisão sustenta o uso de canabinoides por serem seguros e bem tolerados, no entanto, o método de administração e a dose administrada deverá ser mais bem estudada.
Stockings et al9 efetuaram uma MA e uma RS de 47 ECA e 57 estudos observacionais, dos quais 48 incidiam sobre o uso dos canabinoides na doença neuropática. O objetivo deste trabalho foi avaliar a intensidade da dor, funcionalidade física e emocional dos pacientes, impressão geral de mudança, efeitos adversos e desistências em doentes tratados com diversos canabinoides. Verificou-se uma redução de 30% na dor em 29% dos pacientes tratados com canabinoides versus 25,9% no grupo controlo (placebo), verificando-se uma diferença estatisticamente significativa. O number needed to benefit (NNTB) para diminuição de 30% da dor foi de 24, valor superior aos dos outros analgésicos. O number needed to harm (NNTH) foi de apenas 6. À semelhança de outros estudos, os participantes recorreram à medicação habitual para a dor, pelo que as conclusões tiradas podem estar enviesadas. A maioria dos estudos incluídos foram realizados em amostras pequenas e houve alguns lapsos na recolha e interpretação dos dados. Deste modo, os autores desta RS consideraram que o nível de evidência do uso de canabinoides no tratamento da dor neuropática é escasso.
Tabela 1. Síntese dos resultados obtidos e nível de evidência atribuído.
| Autores | Tipo de estudo | População | Métodos | Resultados | Nível de evidência |
| Stockings E et al, 2018 | RS e meta-análise | 176 pacientes | Avaliar redução da dor em 30% e 50%, em pacientes tratados com vários tipos de canabinoides (nabilona, cannabis sativa e dronabinol), como terapêutica principal ou como adjuvante | Dos 6 estudos abordados nesta revisão, 4 demonstraram um efeito positivo na diminuição da dor (n=114). Contudo, os autores consideram que o nível de evidência era escasso e de baixo nível | B |
| Kurlyandchik I et al, 2020 | RS | 1136 pacientes | Avaliar impacto do tratamento com canabinoides na redução da dor, qualidade de vida e presença de efeitos adversos, em pacientes tratados com formulações orais de dronabinol e nabilona ou produtos derivados da planta cannabis sativa | Os ensaios demonstraram que o canábis medicinal é seguro e bem tolerado, mas que o meio de administração e a dose administrada precisam de ser mais bem estudados | A |
| Khurshid H et al, 2021 | RS | Inclui 12 revisões e 3 revisões sistemáticas (NR ao número de pacientes); Inclui 2 ensaios clínicos (n=37) e 5 estudos observacionais (n=1289) | Extração das conclusões dos estudos incluídos no estudo; As substâncias utilizadas foram a nabilona, o dronabinol, o bedrocan (22,4 mg THC, <1 mg CBD), o bediol (13,4 mg THC, 17,8 mg CBD) e bedrolite (18,4 mg CBD, <1 mh THC) | A revisão refere que o uso de canabinoides no tratamento da fibromialgia era seguro, eficaz, tinha uma eficácia superior ao placebo e estava associado a uma maior redução da escala visual da dor (EVD); Concluem assim que os canabinoides são uma opção terapêutica a ter em conta, quando as restantes já foram utilizadas | A |
Discussão
A dor da fibromialgia é difícil de tratar, sendo um desafio para a prática clínica, com apenas uma minoria dos pacientes a reportar benefícios terapêuticos relevantes com os tratamentos farmacológicos convencionais.2 Ao contrário do que se possa pensar, a dor da fibromialgia não é particularmente diferente de outras condições associadas à dor crónica.2 Na dor crónica de diferentes etiologias, apenas uma pequena proporção dos pacientes tem boa resposta ao tratamento farmacológico.2
Apesar de não existirem recomendações que suportem a utilização de opioides na fibromialgia, nem evidência de benefícios na dor, funcionalidade e qualidade de vida, estes são frequentemente prescritos.1,2,7,10 Os moduladores da dor, nomeadamente SNRIs, amitriptilina, gabapentina e pregabalina evidenciaram apenas benefício modesto.1,2 Atualmente, menos de 25% dos pacientes com fibromialgia que receberam terapia farmacológica reportam um alívio significativo da dor (redução de pelo menos 50% da intensidade da dor).2 Assim, o tratamento farmacológico disponível para a fibromialgia tem um perfil de risco-benefício desfavorável para a maioria dos pacientes e com frequência os efeitos adversos superam os benefícios da terapêutica.1,2,10 As guidelines internacionais recomendam uma abordagem multidisciplinar, com recurso a intervenções farmacológicas baseadas em evidência, associadas a intervenções não farmacológicas, nomeadamente prescrição de exercício físico adaptado e intervenções cognitivas.1,2
Numa era marcada pela prescrição epidémica de opioides, há necessidade de encontrar alternativas farmacológicas para o tratamento da dor crónica. Os canabinoides têm sido alvo de extensa investigação nos últimos anos, tendo vindo a revelar o seu potencial terapêutico em várias patologias, mas têm tido particular interesse devido aos seus efeitos analgésicos. Muitos dos problemas associados à prescrição de canabinoides são semelhantes aos problemas associados a outras classes farmacológicas usadas no tratamento da fibromialgia, nomeadamente os opioides e as benzodiazepinas. Exemplos destes problemas são o potencial de dependência, o uso recreativo, o enquadramento legal, a relação risco-benefício desfavorável a longo prazo, os efeitos psicotrópicos e a deterioração cognitiva.2,3,10-12
As normas de boas práticas de apoio à prescrição de canabinoides do National Institute for Health and Care Excellence (NICE) do Reino Unido são semelhantes às recomendações do Center for Disease Control and Prevention (CDC) para a prescrição adequada de opioides.10,11 Estas normas recomendam que, previamente à prescrição de canabinoides ou opioides, seja feita uma avaliação inicial que inclui uma anamnese cuidada, com levantamento dos antecedentes pessoais de uso, abuso e dependência de substâncias psicoativas (canabinoides, opioides, benzodiazepinas, álcool, etc.), bem como os antecedentes pessoais e familiares de doenças psiquiátricas (dependências de substâncias nocivas, esquizofrenia, psicoses).10,11 Além disso, é recomendada a realização de um estudo analítico para avaliação da função hepática e renal, bem como a avaliação do risco cardiovascular e o rastreio de arritmias.10,11 No que respeita às interações medicamentosas, o principal risco prende-se com a interação dos canabinoides com outros depressores do sistema nervoso central, como os opioides, benzodiazepinas e anti-epiléticos.11 A relação risco-benefício a curto e a longo prazo deverá sempre ser discutida com o paciente e, se se optar pela prescrição de canabinoides ou opioides, esta deverá ser imediatamente suspensa sempre que não seja documentado um benefício clínico significativo (redução igual ou superior a 50% da intensidade da dor) ou que os efeitos adversos sejam intoleráveis para o paciente ou ponham em risco a sua segurança.10,11
São ainda necessários mais estudos para que os canabinoides possam começar a ser utilizados como terapêutica na fibromialgia. Uma das limitações mais notórias dos estudos já existentes é as amostras serem reduzidas. Por outro lado, muitas vezes os participantes recorrem à medicação habitual para a dor em associação com os canabinoides, não se conseguindo assim avaliar o efeito individual desta substância, mas sim o seu efeito sinérgico. Também há uma taxa significativa de indivíduos que acabam por desistir do tratamento com canabinoides antes do prazo estipulado, por não tolerarem ou não desejarem os efeitos psicotrópicos desta substância.2,3 Persistem ainda muitas dúvidas acerca da dosagem e do método mais eficaz de administração dos canabinoides para uma melhor gestão da dor.
Conclusão
Os canabinoides parecem ter potencial terapêutico na área da dor crónica. No entanto, são necessários mais estudos, com seguimento de longa duração, sobre o papel dos canabinoides no tratamento da dor crónica, em particular na fibromialgia. Os próximos estudos deverão ter em conta o interesse nos resultados relacionados com a duração da terapêutica de longa duração (8-12 semanas) e o número de pacientes que abandonam a terapêutica devido a efeitos adversos. Resta realçar a importância da avaliação da eficácia analgésica de acordo com uma redução significativa da dor e impacto positivo na funcionalidade e na qualidade de vida.