Introdução
A anemia é causada em 50% dos casos por défice de ferro (50%),1 sendo que a anemia ferropénica afeta cerca de 30% da população mundial.2 As principais causas de défice de ferro são o aumento da necessidade, a ingestão inadequada na dieta, a má absorção e a perda por hemorragia crónica.1
Cerca de 50% das hemorragias gastrointestinais têm origem no trato superior, sendo as causas mais comuns: úlcera péptica, varizes gastroesofágicas, esofagite e angioectasias.3,4
As lesões de Cameron (LC) foram descritas pela primeira vez em 1986, por Cameron e Higgins, para identificar lesões da mucosa gástrica como causa de anemia crónica, em doentes com grandes hérnias diafragmáticas.5
As alterações caracterizam-se por erosões ou úlceras com conformação e localização típica.5,6 O diagnóstico é feito através da observação das lesões na endoscopia, no entanto, estas podem ser de difícil visualização ou já não estarem presentes no momento do exame, uma vez que podem cicatrizar espontaneamente, subestimando o seu diagnóstico.6 De seguida, é apresentado um caso de anemia grave ferropénica por perdas hemáticas crónicas, numa doente com lesões de Cameron.
Caso clínico
Apresenta-se uma mulher de 77 anos, seguida na consulta de Medicina Interna, por astenia de evolução prolongada, com diagnóstico de anemia ferropénica, sem suplementação e obesidade, dislipidemia e síndrome depressivo. A endoscopia digestiva alta e baixa prévias não revelaram hemorragia ativa ou lesões potencialmente hemorrágicas. A doente negou: perdas hemáticas macroscópicas, como epistáxis, hematemeses, hematoquézias, melenas, hematúria ou perdas vaginais; lesões da pele como petéquias, equimoses ou hematomas; história de febre, icterícia, hipersudorese, anorexia ou perda ponderal; restrições alimentares e consumo excessivo de álcool; alterações da medicação habitual. Ao exame objetivo, apresentou palidez cutânea, aumento da frequência respiratória; auscultação pulmonar normal e cardíaca com taquicardia; abdómen sem organomegalias palpáveis; sem lesões cutâneas ou adenopatias palpáveis; com perfil tensional estável, frequência cardíaca aumentada (105-110 batimentos por minuto), saturação periférica de 96%, sem suplementação de oxigénio e apirética. Do estudo analítico realizado: hemoglobina 3,7 g/dL, com volume globular médio baixo (67,1 fL), índice reticulocitário inferior a 2, ferro (4,2 ug/dL), ferritina (2,8 ng/mL) e saturação de transferrina (1,1%) reduzidos e capacidade total de fixação do ferro (390,8 ug/dL) elevada, isto é, anemia microcítica ferropénica grave. Não se observaram alterações da função renal e hepática, com teste de Coombs direto e indireto negativos.
Realizou-se transfusão sanguínea com 2 unidades de concentrado eritrocitário e iniciou-se suplementação endovenosa de ferro, associada a inibidor da bomba de protões (IBP).
A pesquisa de sangue oculto nas fezes revelou-se positiva.
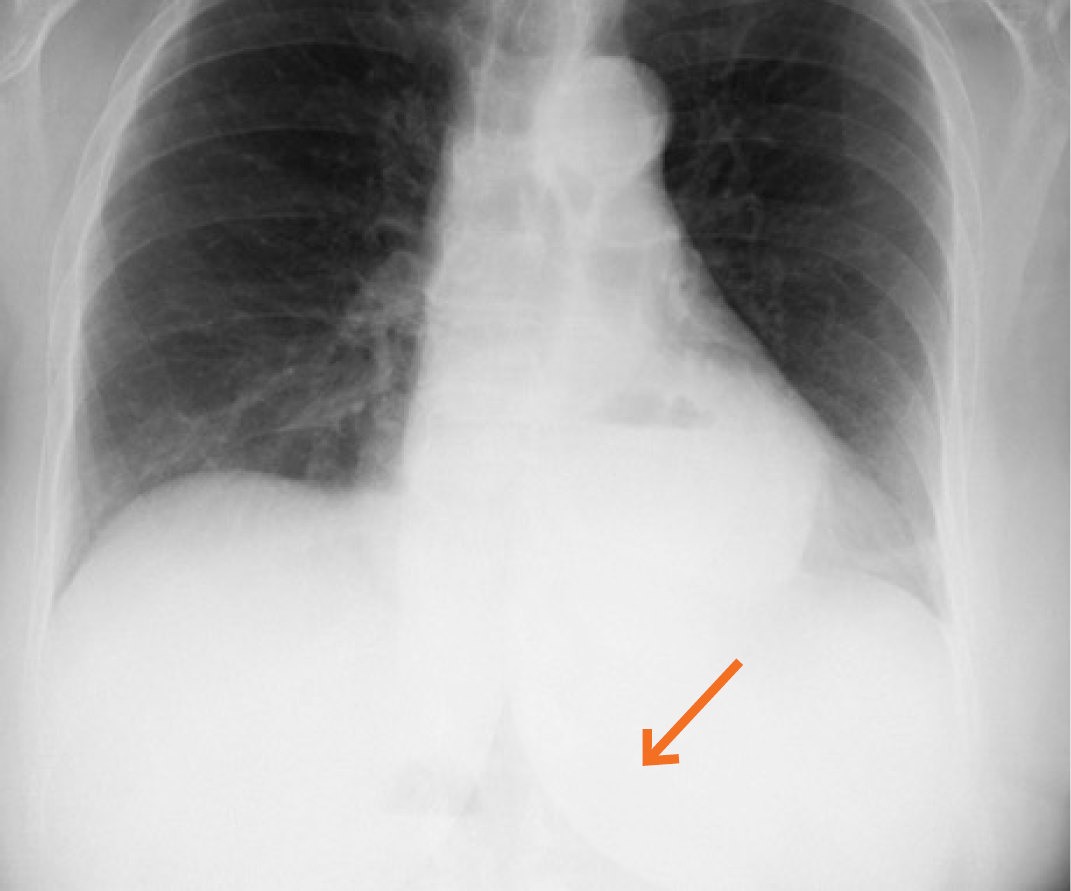
Figura 1 Radiografia de tórax: silhueta cardíaca com interposição da silhueta gástrica e evidência da câmara gasosa no tórax (seta).
A radiografia torácica mostrou hipotransparência sobreposta à silhueta cardíaca na base direita, com nível aéreo, sugestivo de hérnia do hiato, com câmara gástrica no hemitórax esquerdo (Fig. 1).
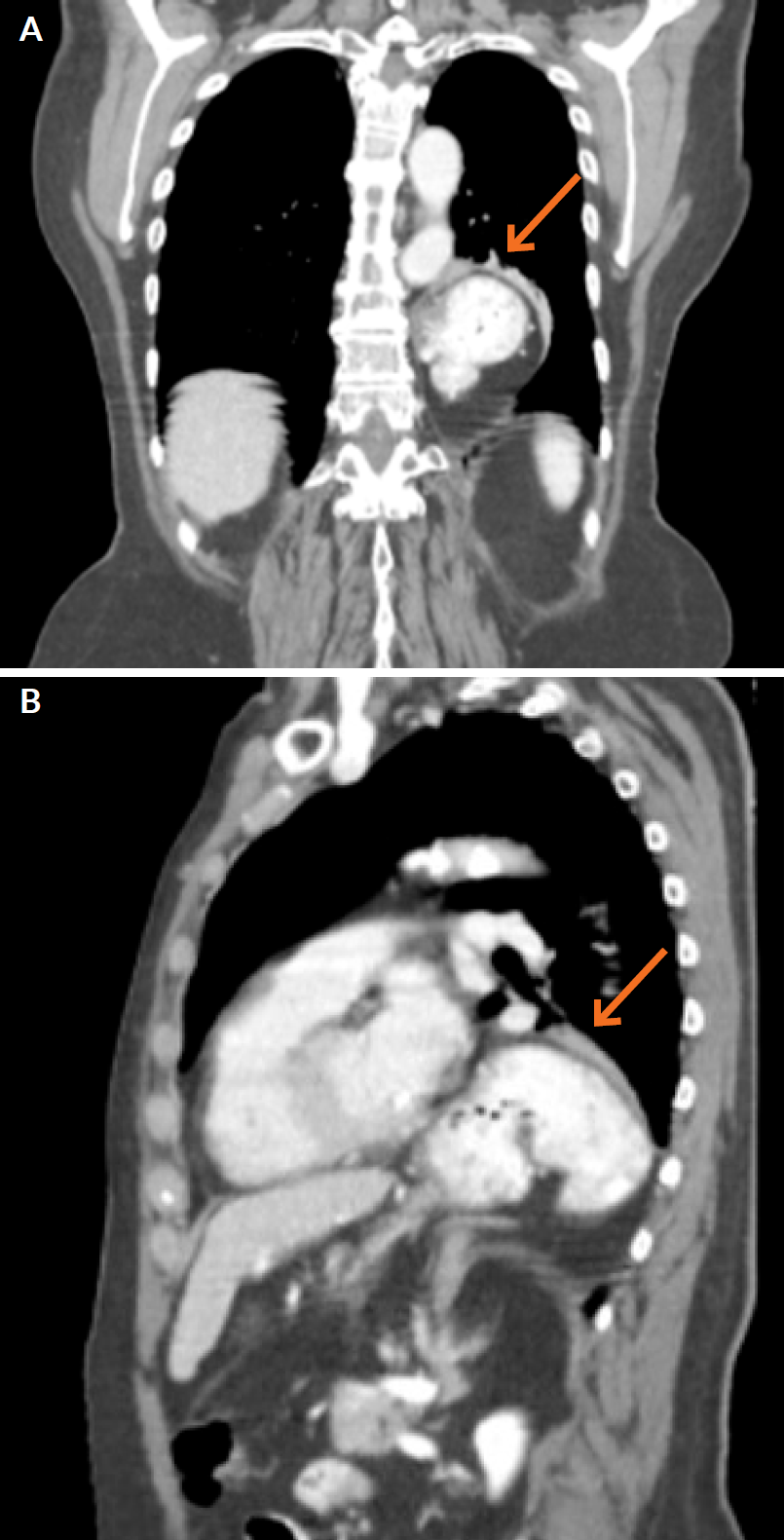
Figura 2 Tomografia computorizada do tórax: estômago (setas) na cavidade torácica, em corte coronal (A) e sagital (B).
A tomografia computorizada mostrou volumosa hérnia do hiato esofágico com migração quase integral do estômago para a cavidade torácica (Fig. 2). A colonoscopia não evidenciou lesões potencialmente hemorrágicas.
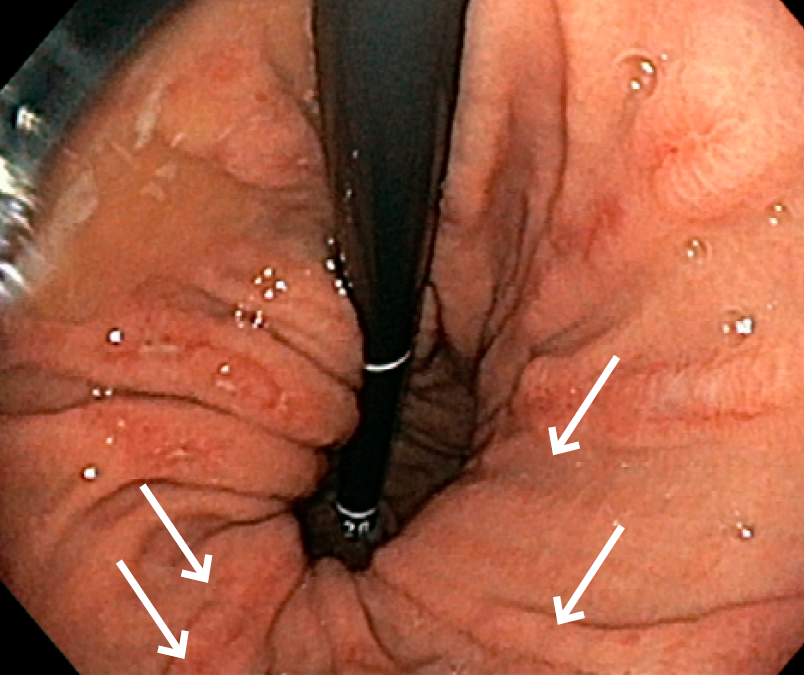
Figura 3 Imagem obtida através da endoscopia digestiva alta: lesões ulcerosas longitudinais (setas), compatíveis com as lesões de Cameron.
A endoscopia digestiva alta revelou hérnia do hiato com cerca de 5 cm, estomago com fundo com erosões ulcerosas longitudinais, localizadas na transição corpo/antro, sem estigmas de hemorragia recente (Fig. 3).
Foram realizadas biópsias que evidenciaram gastrite crónica ligeira do corpo gástrico, com erosão e alterações reativas do epitélio. Estes aspetos endoscópicos e histopatológicos corroboram o diagnóstico de lesões de Cameron como causa de perda hemorrágica crónica e consequente anemia por défice de ferro.
Após 2 semanas de tratamento com IBP e suplementação de ferro, a hemoglobina melhorou para 8,1 g/dL. A doente manteve seguimento em consulta, com controlo analítico e estabilização da hemoglobina nas 11 g/dL.
Discussão
A anemia é uma complicação comum em doentes com´hérnia do hiato esofágico (HHE), com uma prevalência que chega aos 33%.7 Este pode ser o primeiro sinal que leva à procura de ajuda médica, sendo que dentro dos exames complementares, as hérnias paraesofágicas extensas são muitas vezes observadas nas radiografias de tórax e nas tomografias computorizadas torácicas.3,8
Neste caso, foi através destes exames que se fez o diagnóstico de HHE.
As hemorragias gastrointestinais altas de causa não varicosa têm elevada prevalência e alta taxa de mortalidade,3,9 sendo endoscopia digestiva alta considerada gold standard para o seu diagnóstico e tratamento.10
As LC são uma causa rara deste tipo de hemorragia3 de perdas agudas ou crónicas,10,11 podendo causar anemia.12 Segundo a literatura, as LC resultam do trauma mecânico provocado pelo diafragma nas pregas gástricas, dando origem a erosões e úlceras da mucosa, no local ligeiramente acima ou abaixo do nível do diafragma, pelo movimento deste músculo a cada ciclo respiratório.6 A isquemia da mucosa e a lesão devido à exposição ao ácido gástrico, são também etiologias adicionais importantes.6,10,11 Vários estudos comprovam que as HHE estão envolvidas no processo fisiopatológico da anemia ferropénica crónica.8 Os sintomas de HHE são limitados,11 apresentando maior frequência à medida que aumenta o tamanho da mesma. Os doentes recorrem ao médico pelos sintomas decorrentes da anemia.3,6
Endoscopicamente, as LC são lineares e apresentam uma faixa exsudativa central, com um halo eritematoso, raramente com hemorragia ativa ou coágulo aderente.6,10 A prevalência das LC é difícil de estimar, porque são frequentemente subdiagnosticadas, dado que as lesões podem ser subtis e difíceis de identificar,6,8,11 podendo estar presentes de forma intermitente6 na endoscopia. De acordo com diferentes estudos, estas lesões estão presentes pelo menos em 5% dos doentes com HHE,11 mas podem ir até 20% - 50%,8,10 dependendo do tamanho da HHE.12 Existe uma correlação entre hemorragia ativa das LC e anemia, no entanto, a ausência de sinais hemorrágicos recente, não exclui o diagnóstico etiológico do défice de ferro.8
A biópsia não está recomendada para este tipo de diagnóstico, mas à observação microscópica encontram-se oclusões vasculares características de gastropatia isquémica; o exame histopatológico revela atrofia gástrica, fibrose, necrose e infiltração por células imunológicas.3
Mais de 80% dos doentes com LC apresenta HHE iguais ou superiores a 5 cm, que corrobora as hipóteses de que estas lesões são mais frequentes em grandes hérnias do hiato13,14 do que em hérnias pequenas (inferiores a 3 cm).7 As grandes HHE são o principal fator de risco identificável para as LC.15
A doente referida apresenta uma HHE com cerca de 5 cm, que lhe confere um maior risco para LC. A HHE é mais frequente na população idosa, pelo que as LC também se encontram maioritariamente nesta faixa etária,3 sendo a sua prevalência maior em mulheres do que em homens.3,11
O tratamento primário das HHE passa pela abordagem médica conservadora,11,12 com elevada taxa de sucesso.
Dado que a produção de ácido gástrico desempenha um papel importante na anemia ferropénica,8 parte do tratamento passa pelo uso de inibidores da bomba de protões (IBP).14 Outro pilar terapêutico, passa pela suplementação de ferro (oral ou endovenoso), dependendo da necessidade fisiológica do doente.1
Com esta terapêutica, os doentes podem manter-se estáveis e com níveis de hemoglobina razoáveis.8,13 A taxa de melhoria após terapêutica médica dirigida é excelente,3 variando entre 83% a 100%.13 Porém, tendo em conta que o principal mecanismo das LC é o trauma mecânico, a reparação cirúrgica da hérnia pode ser necessária, principalmente quando refratários à terapêutica médica,13,14 mas ainda não há consenso sobre o tratamento ideal desta patologia.6
Os doentes submetidos a cirurgia de reparação da HHE têm grande redução da necessidade de suplementação de ferro e do uso de IBP.8 Para o tratamento cirúrgico é necessário ter indicação e condições operatórias, pelo que a decisão deve ser tomada pelo doente informado, médico assistente e cirurgião,8 baseada na necessidade de transfusão sanguínea frequente versus o risco de mortalidade/morbidade inerentes à cirurgia.6 A decisão cirúrgica baseia-se frequentemente nos sintomas associados como disfagia e dor torácica pós-prandial.8 A anemia ferropénica, em doentes com HHE de grande tamanho (com ou sem LC) ou em doentes refratários ao tratamento médico (com terapêutica com IBP e suplementação de ferro mantêm baixo valor de hemoglobina), tem indicação cirúrgica.6,10 Doentes com hemorragia incontrolável e hérnias complicadas com encarceramento, volvo ou perfuração também têm indicação cirúrgica.3,11,12
A taxa média de sucesso, após cirurgia, é de 92%, com uma recorrência inferior a 10% e um benefício terapêutico entre 76% e 100%.13 Através desta intervenção é possível reverter o mecanismo fisiopatológico traumático e isquémico das LC, com cicatrização das mesmas, reduzindo a probabilidade de hemorragia e, consequentemente, a anemia,13 com melhoria da qualidade de vida.7
Em doentes com anemia persistente e HHE (iguais ou superiores a 5 cm), mesmo sem achados endoscópicos, deve considerar-se que a anemia ferropénica se enquadra em prováveis perdas sanguíneas intermitentes por LC.7,8,13 Ou seja, devem considerar-se as LC com etiologia em casos de hemorragia digestiva alta oculta.11,15 Com a maior incidência de obesidade na população mundial, há maior frequência de HHE,11 o que pode levar a que as LC se tornem causa mais frequente de hemorragia gastrointestinal,13 daí a importância do seu reconhecimento para um tratamento dirigido e eficaz da anemia de causa potencialmente reversível.















