INTRODUÇÃO
A imobilidade prolongada no leito está muitas vezes relacionada com a doença critica e com o internamento numa Unidade de Cuidados Intensivos (UCI). Se numa pessoa sem doença critica a imobilidade a imobilidade tem consequências nefastas a vários níveis(1), nos doentes críticos, estes efeitos são potenciados por fatores como: falência multiorgânica, ventilação mecânica, fármacos (corticoides e bloqueadores musculares), citoquinas inflamatórias e catabolismo elevado, contribuindo para o desenvolvimento de fraqueza muscular generalizada, que condiciona a recuperação do doente e a sua alta(2). Para além debilidade física, o internamento prolongado em UCI associa-se também a estados de debilidade psicossocial, comprometendo a qualidade de vida futura e dificultando a reintegração social e profissional destes doentes, constituindo a designada síndrome pós-cuidados intensivos(3-5). Por definição, esta síndrome diz respeito ao comprometimento, de novo ou agravamento, da condição física, cognitiva ou mental, que ocorre após a doença crítica e que persiste após a alta da unidade de cuidados intensivos(6).
Nesse sentido, foi desenvolvida a Bundle ABCDEF, que inclui os seguintes feixes de intervenção: avaliação, prevenção e tratamento da dor (A); coordenação do despertar com o treino de ventilação espontânea (B); escolha de sedação e analgesia (C); avaliação, prevenção e tratamento do delírio (D); mobilização e reabilitação precoce (E); e envolvimento e empoderamento da família (F) (7,8).
Apesar de todos feixes serem importantes, no contexto da enfermagem de reabilitação, a mobilização e reabilitação precoce tem particular interesse. A esse respeito, a European Respiratory Society e a European Society of Intensive Care Medicine dizem-nos que a mobilização ativa ou passiva e o treino muscular devem ser instituídos precocemente e que técnicas como posicionamento, mobilização passiva e alongamento muscular devem ser usados para preservar a mobilidade articular e o comprimento do músculo-esquelético em doentes incapazes de se mover espontaneamente(9). A German Society of Anaesthesiology and Intensive Care complementa que por princípio, a mobilização precoce deve ser realizada em todos os doentes tratados em cuidados intensivos, a que não se aplicam critérios de exclusão e que, o tratamento deve começar o mais tardar 72 h após a admissão em cuidados intensivos e ser realizado duas vezes por dia com uma duração de pelo menos 20 minutos. Recomenda ainda que a mobilização seja gradual e sugere o desenvolvimento de um algoritmo específico para uma unidade ou hospital(10).
Apesar dos aparentes benefícios da mobilização precoce, uma meta-analise realizada em 2015(11), concluiu que a reabilitação precoce, ainda que permita a mais doentes ter alta hospitalar a deambular de forma autónoma, não apresenta benefícios comprovados na duração da ventilação mecânica, no tempo de permanência em UCI ou no tempo de hospitalização, na melhoria da funcionalidade, da força muscular ou da qualidade de vida. De igual forma, uma outra revisão sistemática, publicada em 2018(12), refere não existir evidência suficiente do efeito da mobilização precoce na funcionalidade, força muscular, qualidade de vida ou ocorrência de eventos adversos. Em oposição, uma outra revisão sistemática reforçava os benefícios de um programa de mobilização precoce na força muscular respiratória e periférica, na diminuição do tempo de ventilação mecânica e do tempo de internamento nos doentes mobilizados precocemente(13).
Outras duas revisões sistemáticas com meta-análise, publicadas em 2019, observaram que os doentes mobilizados precocemente evidenciavam redução do tempo de internamento hospitalar, aumento da força muscular(14), aumento o número de dias livres de ventilação, aumento da distância de marcha independente à alta hospitalar e aumento da probabilidade de alta para o domicílio(15). Apesar de não se verificarem diferenças significativas na mortalidade hospitalar, mortalidade e efeitos adversos aumentam ligeiramente nos casos de mobilização precoce(14,15). Não se verificaram igualmente diferenças a nível da qualidade de vida(14).
Como se confirma, este é ainda um tema em aberto com resultados inconsistentes para a maioria dos desfechos. As revisões citadas incluíram diferentes formas de mobilização (cicloergómetro, neuroestimulação elétrica transcutânea e levante precoce, por exemplo) o que poderá ter influência nos seus resultados. Apesar dos protocolos ou programas de mobilização progressiva precoce serem cada vez mais uma realidade (16,17), e numa pesquisa prévia a esta revisão, não encontramos na literatura uma síntese dos seus eventuais benefícios. Em adição, as revisões existentes centram-se sobretudo em estudos randomizados, mais robustos, mas em menor número, excluindo um número significativo de estudos de menor relevância científica, como a analise programas de melhoria de qualidade, mas que reúnem um conjunto de informação que não pode ser desprezada.
Assim surge a necessidade desta revisão, que tem por objetivo: conhecer o efeito dos programas de mobilização progressiva precoce nos resultados do doente crítico. A questão de partida para esta investigação foi: Qual o efeito de um programa de mobilização progressiva precoce, nos resultados do doente crítico, face ao tratamento habitual. Estes programas ou protocolos de mobilização deverão ter várias fases, ajustadas à condição do doente, e devem ter como objetivo progredir para a mobilização fora do leito e deambulação ativa. Os resultados foram comparados com grupos sem intervenção ou sob os cuidados habituais, incluindo o regime habitual de fisioterapia.
Esta revisão é a primeira a debruçar-se em concreto sobre este tipo de programas. Em adição, ao incluir vários desenhos de investigação, nomeadamente resultados da implementação de projetos de melhoria de qualidade, permite reunir muitos estudos que não integram as anteriores revisões sobre o tema. Ao englobar um importante número de variáveis, ou resultados em saúde, constitui uma importante síntese do conhecimento atual sobre o tema.
Esta revisão sistemática da literatura seguiu os pelos princípios da Cochrane(18), em conformidade com o Preferred Reporting Items for Systematic reviews and Meta-Analyses (PRISMA)(19) e encontra-se registada no international prospective register of systematic reviews (www.crd.york.ac.uk/prospero) com o número CRD42020162101.
METODOLOGIA
Estratégia de pesquisa e seleção dos estudos
A estratégia de pesquisa obedeceu aos conceitos chave definidos pelo seguinte modelo PICO(18):
População - Doentes adultos, com 18 anos ou mais, internados em UCI, independentemente de doença ou gravidade;
Intervenção - Programas (ou protocolos) de mobilização progressiva precoce que visem a mobilização fora do leito e deambulação ativa, independentemente do prestador. Estes programas devem ter várias fases ajustadas à condição do doente;
Comparador - Sem intervenção ou cuidados habituais (inclui o regime habitual de fisioterapia);
Outcomes /Resultados - Mortalidade, tempo de ventilação mecânica, tempo de internamento em UCI, número de readmissões, tempo de internamento hospitalar (outcomes primários), funcionalidade na alta da UCI, força muscular na alta da UCI, proporção de altas para o domicílio, incidência de infeções na UCI, incidência de úlceras de pressão na UCI, incidência de fenómenos tromboembólicos na UCI (outcomes secundários).
A pesquisa foi realizada, no dia 20 de janeiro de 2022, nas bases de dados PubMed (MEDLINE), Cumulative Index of Nursing and Allied Health (CINAHL), Cochrane Central Register of Controlled Trials (CENTRAL), Physiotherapy Evidence Database (PEDro), Clinical Trials.gov, WHO International Clinical Trials Registry Platform e EU Clinical Trials Register.
Tabela 1 Estratégia de pesquisa
| Base de dados | Expressão | Resultados | |
|---|---|---|---|
| MEDLINE | #1 | (“Early Ambulation”[Mesh]) OR (“walking”[Mesh]) OR (“mobili*”[Title/Abstract]) | 270 997 |
| #2 | ("Intensive Care Units"[Mesh]) OR ("Critical Care"[Mesh]) OR ("Critical Illness"[Mesh]) | 140 507 | |
| #3 | #1 AND #2 | 1 139 | |
| CINAHL (via EbscoHost) | #1 | MW Early Ambulation OR MW walking OR AB mobili* | 51 182 |
| #2 | MW Intensive Care Units OR MW Critical Care OR MW Critical Illness | 88 816 | |
| #3 | #1 AND #2 | 863 | |
| CENTRAL (via EbscoHost) | #1 | MW Early Ambulation OR MW walking OR AB mobili* | 18 266 |
| #2 | MW Intensive Care Units OR MW Critical Care OR MW Critical Illness | 5 243 | |
| #3 | #1 AND #2 | 84 | |
| PEDro | Critical care AND mobility | 14 | |
| Clinical Trials.gov | #1 | Early Ambulation OR walking OR mobility | 18 135 |
| #2 | Intensive Care Units OR Critical Care OR Critical Illness | 7 775 | |
| #3 | #1 AND #2 | 411 | |
| WHO International Clinical Trials Registry Platform | #1 | (Early Ambulation) OR (walking) OR (mobili*) | 7 349 |
| #2 | (Intensive Care Units) OR (Critical Care) OR (Critical Illness) | 7 076 | |
| #3 | #1 AND #2 | 129 | |
| EU Clinical Trials Register | #1 | (Early Ambulation) OR (walking) OR (mobili*) | 757 |
| #2 | (Intensive Care Units) OR (Critical Care) OR (Critical Illness) | 222 | |
| #3 | #1 AND #2 | 8 | |
Foram pesquisados os termos “early ambulation”, “walking” ou “mobility” combinados com “intensive care units”, “critical care” ou “critical illness”, de acordo com a estratégia apresentada na tabela 1.
Para reunir o máximo de informação disponível, esta revisão, para além de incluir estudos randomizados incluiu também estudos quase-experimentais, casos-controlo e estudos de coorte (incluindo programas de melhoria de qualidade com desenho antes e após) publicados em inglês, espanhol e português. Foi definido um período de análise de 15 anos anterior à realização da pesquisa, incluindo estudos publicados entre 2004 e 2019, para desta forma incluir artigos que possam ter sido base das atuais recomendações para mobilização precoce.
Excluíram-se casos clínicos, revisões sistemáticas, artigos de revisão e quaisquer estudos que analisassem o efeito de programas de mobilização em conjunto com outras intervenções (ex: bundle ABCDE). Após eliminação dos artigos duplicados através do programa Mendeley, dois revisores independentes utilizaram a aplicação Rayyan para analisar o título e resumo dos artigos. Os mesmos revisores analisaram posteriormente o texto completo dos artigos que passaram a primeira fase de revisão para decidir se cumpriam os critérios definidos. Os dados relativos aos estudos a incluir na revisão foram extraídos para um Excel que serviu, também, de base à análise de risco de viés de cada um deles. As discordâncias foram resolvidas por discussão entre os revisores.
RESULTADOS
Da estratégia de pesquisa resultaram 813 publicações, tendo sido selecionadas 49 para análise de texto completo, das quais 18 foram incluídas nesta revisão (Figura 1).
Características dos estudos
Dos 18 estudos incluídos na revisão (20-37) (Tabela 1), 3 são estudos randomizados controlados (ERC) e 15 estudos observacionais. Muitos destes estudos observacionais estão relacionados com programas de melhoria de qualidade e utilizam um desenho que avalia os doentes antes e após a implementação do programa de mobilização precoce. De ressalvar que 15 dos 18 estudos incluídos na revisão resultam de dados colhidos nos Estados Unidos da América (EUA) e que apenas um inclui dados colhidos na Europa.
Tabela 1 Caracteristicas dos estudos incluídos na revisão
| Autor (ano) | País | Tipo de estudo | Tipo de UCI | Tamanho da amostra |
|---|---|---|---|---|
| Azuh et al (2016) (20) |
EUA | Coorte prospetivo com controlo histórico |
UCI médica | |
| Bahouth et al (2018) (21) |
EUA | Estudo quase experimental | UCI neurotrauma | Pré: 27 Pós: 29 |
| Booth et al (2016)(22) |
Coorte prospetivo com controlo histórico |
UCI neurocríticos | Pré:184 Pós:159 |
|
| Clark et al (2013) (23) |
EUA | Coorte retrospetivo | UCI de trauma e queimados | Pré: 1044 Pós:1132 |
| Crane (2017) (24) |
EUA | Estudo quase experimental | UCI médico-cirúrgica | Pré: 115 Pós: 29 |
| Dickinson et al (2013) (25) | EUA | Coorte retrospetivo | UCI cirúrgica | Pré: 555 Pós: 557 |
| Floyd et al (2016) (26) |
EUA | Coorte retrospetivo | UCI cardiotorácica | Pré: 30 Pós: 30 |
| Fraser et al (2015) (27) |
EUA | Coorte retrospetivo | 3 UCI (médica, cirúrgica e coronária) | Pré: 66 Pós: 66 |
| Hodgson et al (2016) (28) | Austrália e Nova Zelândia | ECR | 5 UCI (médica cirúrgica e de trauma) | Int: 29 Ctrl: 21 |
| Klein et al (2015) (29) |
EUA | Estudo quase experimental | UCI neurocríticos | Pré: 260 Pós: 337 |
| Lai et al (2017) (30) |
Taiwan | Coorte retrospetivo | UCI médica | Pré: 63 Pós: 90 |
| Liu et al (2019) (31) |
Japão | Coorte retrospetivo | UCI médico-cirúrgica | Pré: 204 Pós: 187 |
| Mah et al (2013) (32) |
EUA | Coorte prospetivo com controlo histórico | UCI cirúrgica | Pré: 31 Pós: 28 |
| Morris et al (2008) (33) | EUA | Coorte prospetivo | 7 UCI médicas de um mesmo serviço de CI | Int: 165 Ctrl: 165 |
| Ronnebaum et al (2012) (34) |
EUA | Coorte retrospetivo | UCI médico-cirúrgica | Pré: 15 Pós: 13 |
| Schaller et al (2016) (35) | Austria, Alemanha e EUA | ECR | UCI cirúrgica | Int: 104 Ctrl: 96 |
| Schweickert et al (2009) (36) | EUA | ECR | UCI médica | Int: 49 Ctrl: 55 |
| Winkelman et al (2012)(37) | EUA | Estudo quase experimental | UCI médica e UCI cirúrgica | Pré: 20 Pós: 55 |
EUA - Estados Unidos da América; ECR - Estudo clínico randomizado; Int - Grupo de intervenção; Ctrl - Grupo controlo; Pré - Grupo pré intervenção (controlo); Pós - Grupo pós intervenção (intervenção); UCI - Unidade de Cuidados Intensivos
Qualidade e risco de viés
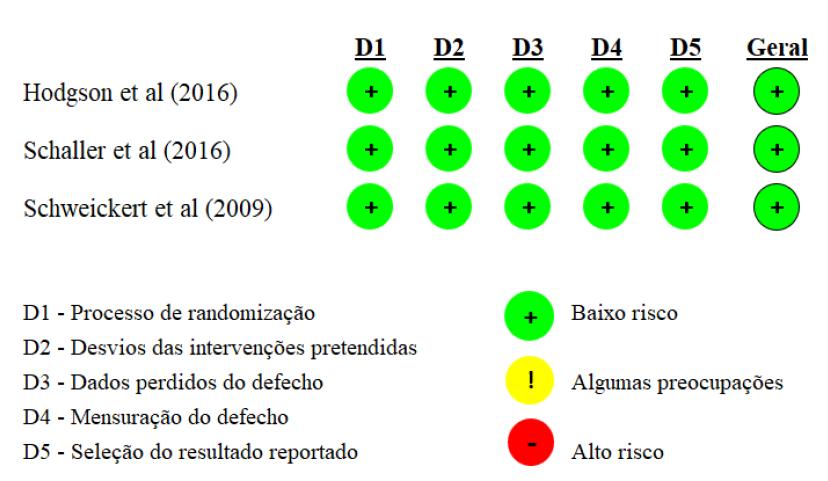
A avaliação da qualidade metodológica e do risco de viés dos estudos incluídos na revisão foi realizada por dois pesquisadores de forma independente, utilizando os critérios da Escala de Newcastle-Ottawa (NOS - Newcastle-Ottawa Scale)(38 ) para estudos de coorte (Tabela 3) e da Risk of Bias 2 (RoB 2) (39) para estudos randomizados (Figura 2). Os casos de discordância foram resolvidos por discussão entre os dois avaliadores.
Tabela 2 Avaliação da Escala de Newcastle-Ottawa para estudos de coorte
| Autor (ano) | Seleção | Comparabilidade | Resultados | TOTAL |
|---|---|---|---|---|
| Azuh et al (2016) (20) | * | ** | ** | 5 |
| Bahouth et al (2018) (21) | ** | ** | ** | 6 |
| Booth et al (2016)(22) | * | ** | ** | 5 |
| Clark et al (2012) (23) | *** | ** | *** | 8 |
| Crane et al (2017) (24) | ** | *** | 5 | |
| Dickinson et al (2013) (25) | *** | ** | *** | 8 |
| Floyd et al (2016) (26) | *** | ** | *** | 8 |
| Fraser et al (2015) (27) | *** | ** | *** | 8 |
| Klein et al (2015) (29) | *** | ** | *** | 8 |
| Lai et al (2017) (30) | ** | ** | ** | 6 |
| Liu et al (2019) (31) | *** | ** | ** | 7 |
| Mah et al (2013) (32) | *** | ** | ** | 7 |
| Morris et al (2008) (33) | ** | ** | ** | 6 |
| Ronnebaum et al (2012) (34) | ** | ** | 4 | |
| Winkelman et al (2012)(37) | ** | ** | ** | 6 |
Mortalidade
Dos estudos incluídos nesta revisão, 12 analisam a mortalidade. Destes, cinco referem-se à mortalidade em UCI(22-24,28,37), seis à mortalidade hospitalar(20,27,31,33,35,36) e um apresenta resultados da mortalidade a 30 dias(29).
Pela análise da tabela 4, pode constatar-se que a mortalidade em UCI variou entre 0 e 17,2%, não se verificando diferenças significativas entre o grupo de doentes submetidos ao programa de mobilização e o grupo de controlo. Ainda assim, dos cinco estudos que analisaram a mortalidade em UCI, quatro reportaram taxas de mortalidade ligeiramente superiores no grupo de mobilização.
No que respeita à mortalidade hospitalar, variou entre 0 e 25%. Apenas numa análise dos resultados de um projeto de melhoria de qualidade através da implementação de um protocolo de mobilização progressiva (31), é identificada uma redução significativa da mortalidade hospitalar nos doentes submetidos ao programa de mobilização precoce (11 vs 24%, p < 0,01). Em três estudos(21,27,35) a mortalidade hospitalar foi maior no grupo de mobilização e em outros 3 foi maior no grupo controlo(31,33,36).
Relativamente à mortalidade a 30 dias(29), no grupo de mobilização ficou 4,5% abaixo do grupo de controlo, ainda que esta diferença não possa ser considerada significativa (p = 0,12).
Em nenhum dos três ERC em análise (28,35,36) se verificam diferenças significativas da mortalidade entre grupos.
Tempo de ventilação
São 12 os artigos que comparam os tempos médios de ventilação entre doentes em programa de mobilização precoce e tratamento habitual (Tabela 4). Os tempos médios de ventilação reportados variaram entre 3(31) e 30,9(34) dias, não se verificando em nenhum dos trabalhos analisados um aumento significativo do tempo de ventilação associado ao desenvolvimento de programas de mobilização progressiva precoce. Por outro lado, em 10 dos estudos analisados verificou-se uma redução do tempo de ventilação no grupo de mobilização progressiva precoce, em relação ao controlo, sendo essa diferença estatisticamente significativa em quatro deles(30,31,34,36).
Os dois estudos randomizados que analisaram este desfecho(28,36) mostram ambos uma redução do tempo de ventilação no grupo de mobilização precoce, mas apenas num(36) essa diferença tem significado estatístico.
Tempo de internamento em UCI
O tempo de internamento em UCI apresentado pelos diferentes estudos é bastante heterogéneo variando entre 3,97(24) e 24.9(34)dias.
Em 15(20,22,23,26-37), dos 18 estudos analisados (Tabela 4) verificou-se uma redução do tempo de internamento no grupo de doentes incluídos no programa de mobilização, em relação ao grupo de controlo. Destes, em sete estudos essa diferença é estatisticamente significativa(29-31,34-37). Em oposição, em três estudos(21,24,25) o grupo de doentes incluídos no programa de mobilização apresentou maior tempo de internamento que o seu grupo controlo, ainda que apenas num(25) essas diferenças tenham significado estatístico.
Em todos os três ERCs em análise(28,35,36) se verifica uma redução no tempo de internamento do grupo de mobilização precoce, em comparação ao controlo, senda essa diferença estatisticamente significativa num dos estudos(35).
Readmissão em UCI
A definição de readmissão varia nos diferentes estudos analisados, um deles refere-se à readmissão hospitalar de doentes críticos(20), enquanto os outros dois se referem à readmissão em UCI no período de 30 dias após a alta dessa unidade(26,27). Pese embora esta diferença de conceitos, nos três estudos analisados verifica-se uma redução do número de readmissões no grupo de mobilização precoce, com diferenças significativas relatadas por dois deles(20,27).
Tempo de internamento hospitalar
O tempo médio de internamento hospitalar foi bastante heterogéneo nos diferentes estudos em análise, variando entre 6,5(26) e 46,5 dias(32).
Observando as diferenças entre grupos verifica-se que os resultados são também heterogéneos. Por um lado, em nove estudos é descrita uma redução do tempo de internamento hospitalar no grupo de mobilização precoce(22,23,26,28-31,33,35) e destes, quatro mostram diferenças significativas em relação ao grupo de controlo(23,29,33,35). Por outro lado, em seis estudos(21,24,25,27,36) é reportado um aumento do tempo de internamento hospitalar no grupo de mobilização precoce, ainda que apenas um(25) reporte diferenças estatisticamente significativas.
Centrando a análise nos estudos randomizados(28,35,36), a evidência mantém-se pouco consistente. Apenas um dos estudos(35) reporta uma redução significativa do tempo de hospitalização nos doentes mobilizados precocemente.
Funcionalidade à alta da UCI
A funcionalidade à alta da UCI, para além de não ser um desfecho analisado com frequência, foi mensurada de formas diferentes nas várias investigações que a incluíram.
Avaliando a funcionalidade através do índice de Barthel(27), verificaram-se resultados significativamente melhores no grupo de doentes mobilizados precocemente (85 vs 63 pontos, com p<0,001). Verificou-se também que mais doentes do grupo de mobilização precoce melhoraram o equilíbrio sentado, desde uma primeira avaliação até à alta (75% vs 36,7%, com p=0,008)(32).
No estudo que avaliou a funcionalidade através do índice de Katz(37), verificou-se igualmente uma melhor funcionalidade na alta no grupo de mobilização precoce, contudo as diferenças não foram estatisticamente significativas.
Em relação ao único ECR que avaliou este desfecho(35), verificou-se que significativamente mais doentes do grupo de intervenção atingiram a capacidade de deambulação, que corresponde a uma pontuação na escala SOMS (surgical intensive care unit optimal mobilisation score) igual ou superior a 4 (52% vs 25%, com p<0,001) e que, em média, os níveis de funcionalidade à alta, avaliados pela escala mmFIM (mini-modified functional independence measure score) eram significativamente superiores nos doentes incluídos no grupo de mobilização precoce, diferença também verificada pelos autores à data da alta hospitalar.
Em comum, todos os estudos identificam melhorias funcionais no grupo de mobilização precoce, em relação ao controlo.
Força muscular à alta da UCI
Apenas um dos estudos incluídos nesta revisão(37) avaliou a força muscular à alta da UCI. Para o efeito utilizou-se o Índice MRC a partir da avaliação bilateral de quatro grupos musculares, em que a força foi pontuada de 0 a 5, com uma pontuação final variável ente 0 e 40. A pontuação média não mostrou diferenças significativas entre o grupo de mobilização precoce (22,4 pontos) e o controlo (26 pontos), com p=0,643.
Alta para o domicílio
Dos 11 estudos incluídos na análise, apenas um(37) analisou o destino à alta da UCI e não o destino à alta hospitalar como as restantes investigações. Comparando os grupos de intervenção com os respetivos controlos, verificamos que na maior parte dos estudos o número de doentes com alta para o domicílio é maior no grupo de mobilização precoce, com dois estudos(29,35) a reportarem diferenças significativas.
Incidência de infeções adquiridas na UCI
Os artigos incluídos nesta revisão, todos eles utilizando grupos não randomizados, analisam possíveis efeitos da mobilização precoce na incidência das seguintes infeções: pneumonia(22,23,33), pneumonia a associada à ventilação(29,37), infeção associada ao cateter vesical(27), infeção da corrente sanguínea(29) e sépsis(23). Em todas as áreas analisadas o grupo de mobilização precoce apresentou menor taxa de infeção em relação ao grupo controlo, com diferenças significativas para a incidência de pneumonia(23), infeção associada ao cateter vesical(27) e infeções da corrente sanguínea(29).
Incidência de úlceras por pressão
A incidência de úlceras por pressão (UPP) foi um desfecho avaliado em sete dos trabalhos de investigação incluídos nesta revisão, todos eles não randomizados. Destes, quatro(20,27,29,37) reportam uma redução da incidência de UPP no grupo de mobilização precoce, com dois deles(20,29) a identificarem diferenças significativas em relação ao grupo de controlo. Acresce ainda um artigo(27) que refere significativa redução dos “quality outcomes” (que incluem: quedas, eventos associados ao ventilador, UPP e infeções associadas ao cateter vesical).
Ao invés, três estudos(23,25,26) referem um aumento da incidência de UPP no grupo de doentes mobilizados precocemente e um deles(25) identifica um aumento significativo em relação aos doentes do grupo de controlo.
Incidência de fenómenos tromboembólicos
Dos estudos incluídos nesta revisão, seis analisaram a incidência de fenómenos tromboembólicos, todos eles não randomizados. Alguns estudos analisaram os fenómenos tromboembólicos no seu conjunto(22,37), outros analisaram separadamente a incidência de trombose venosa profunda e embolia pulmonar(26,33) e outros ainda, analisaram apenas a incidência de trombose venosa profunda(23,29). Da análise dos resultados, três estudos que reportam aumento não significativo dos fenómenos tromboembólicos(29,33,37) e três que reportam uma redução(22,23,26). Em dois casos(22,23) verificaram-se diferenças com significado estatístico, ambas favorecendo o grupo de mobilização precoce.
DISCUSSÃO
Se à partida para esta revisão os benefícios dos programas de mobilização precoce do doente crítico não eram claros, verificamos neste artigo que programas isoladamente podem contribuir para: redução do tempo de ventilação; redução do tempo de internamento em UCI; maior funcionalidade à alta da UCI, independentemente do instrumento de avaliação utilizado. Embora careça de maior investigação, parece haver também uma tendência para: aumento da probabilidade de alta para o domicílio, redução das readmissões e redução das infeções adquiridas na UCI, nomeadamente infeções associadas ao cateter vesical e infeções da corrente sanguínea. Não foram encontrados desfechos negativos, o que suporta a ideia de que se trata de uma prática segura, desde que adequada à condição de cada doente e às recomendações existentes(40).
Relativamente ao tempo de ventilação, os resultados desta revisão estão em linha com outras revisões, que embora incluindo diferentes formas de mobilização e apenas ECRs, chegaram a conclusões idênticas(11,41). Também uma meta-analise conduzida por Wang, em 2020(42), incluindo diferentes estratégias de mobilização e apenas ECR, mostra uma redução significativa do tempo de ventilação nos doentes mobilizados precocemente.
O tempo de internamento em UCI é também um desfecho incluído noutras revisões, que tendem a identificar reduções sem significado estatístico(11,15,41,43,44). Uma vez mais Wang(42), incluindo um maior número de estudos na sua meta-analise, consegue mostrar uma redução importante do tempo de internamento em UCI nos doentes mobilizados precocemente.
No que respeita à funcionalidade, duas revisões consultadas (11,12) citam um único estudo(36) a demostrar melhorias significativas no grupo de mobilização precoce, mas à alta hospitalar e não à alta da UCI, como preconizado nesta revisão. Apenas a meta-análise de Wang(42) analisou este desfecho, reportando um aumento significativo do índice de Barthel no grupo de mobilização precoce.
Duas revisões de ECR, ambas com meta-analise, suportam o aumento das altas para o domicílio nos doentes mobilizados precocemente(41,45). Já a readmissão não foi considerada em nenhuma outra revisão consultada.
Relativamente às infeções adquiridas na UCI, a meta-análise de Wang(42) suporta, uma vez mais, os resultados desta revisão, mostrando uma redução significativa do risco de pneumonia associada à ventilação no grupo de doentes submetidos a mobilização precoce.
Nesta revisão detetaram-se alguns resultados contraditórios entre os estudos incluídos, nomeadamente no que respeita ao efeito dos programas de mobilização progressiva precoce na incidência de fenómenos tromboembólicos, UPP e também os seus efeitos a nível da mortalidade e tempo de internamento hospitalar. Em comparação, a revisão com meta-analise de Wang(42) mostra uma redução significativa do risco de trombose venosa profunda, de incidência de UPP e do tempo de hospitalização, nos doentes mobilizados precocemente. Já no que respeita à mortalidade também não identifica diferenças significativas entre os grupos. Ainda relativamente ao tempo de hospitalização, apesar de numa meta-analise envolvendo doentes pós cirurgia cardíaca(44) não serem detetadas diferenças significativas entre o grupo de mobilização precoce e o tratamento habitual, outra meta-analise(14) reporta redução significativa deste desfecho nos doentes que iniciam mobilização na primeira semana de internamento em UCI, reforçando a importância da precocidade da mobilização.
Apesar de o efeito dos programas de mobilização progressiva precoce na força muscular dos doentes à alta da UCI não ficar claro nesta revisão, dado apenas um dos estudos incluídos reportar esse desfecho, na literatura disponível, relativa à mobilização precoce é claro o seu benefício na redução da fraqueza muscular generalizada adquirida na UCI, principalmente nos doentes com internamentos mais prolongados, por norma associados a uma importante incidência deste problema(41,42).
Um outro desfecho, não tido em conta nesta revisão e estritamente relacionado com a mobilização precoce à a incidência de delírio, sendo a mobilização considerada um fator que contribuiu para a prevenção da ocorrência deste fenómeno(46).
Face a estes resultados, fica clara a necessidade de mudança de mentalidade e assumir a mobilização como uma prioridade nos cuidados ao doente crítico. Existirão, certamente, mais ou menos barreiras em cada serviço (47-49), mas os enfermeiros e em particular os especialistas em enfermagem de reabilitação, enquanto peritos nesta área, devem desenvolver ou dinamizar protocolos de mobilização precoce. Na literatura internacional fala-se no molility champion como alguém que desempenha essas funções(50,51). Olhando para a realidade nacional, para a disponibilidade e competência dos enfermeiros de reabilitação nas UCIs(52,53), estes deverão assumir-se como campeões da mobilidade nas suas unidades.
Limitações do estudo
Este estudo teve várias limitações. Em primeiro lugar a baixa proporção de estudos randomizados incluídos na análise em comparação com os estudos observacionais. Incluiu-se um número significativo de estudos com controlo histórico, podendo os resultados dever-se a outros fatores que não apenas o programa de mobilização. Verificamos ainda discrepâncias ao nível dos cuidados prestados aos doentes nos diferentes grupos de controlo, que poderão dar maior ou menor enfase aos benefícios do programa em análise.
Contribuições para a área
Comparada com outras revisões anteriores, este trabalho, para além de apresentar uma atualização do conhecimento, é inovador na medida em que analisa em concreto o efeito dos programas de mobilização progressiva precoce. Revisões anteriores referem-se à mobilização precoce de modo mais abrangente, incluindo diferentes formas de mobilização ou reabilitação precoce.
Como fica evidente neste artigo, os programas de mobilização progressiva precoce são seguros para os doentes, não se verificando nenhum desfecho negativo decorrente da sua aplicação.
Os benefícios encontrados reforçam a importância de investir neste tipo de programas e mudar de vez o paradigma da mobilização vs imobilização do doente crítico, onde o enfermeiro de reabilitação tem papel importante. É recomendável associá-los a um leque mais variado de intervenções, como a conhecida bundle ABCDEF.
CONCLUSÃO
Esta revisão demonstra benefícios dos programas isolados de mobilização progressiva precoce a nível da redução do tempo de ventilação e do tempo de internamento em cuidados intensivos. Os doentes incluídos nestes programas têm também maior funcionalidade à alta e menor probabilidade de serem readmitidos. Aliado a estes benefícios não foram encontrados desfechos negativos, reforçando que esta é uma prática segura e benéfica.
No complexo plano de cuidados ao doente critico deve contar a mobilização precoce, preferencialmente através de um programa ou protocolo multidisciplinar, constituído por várias etapas adequadas à sua condição.
É igualmente importante fundamentar esta prática com resultados, que para além de darem a conhecer o que se faz em cada serviço, contribuam para melhorar o conhecimento sobre esta importante temática.











 texto em
texto em