Introdução
De acordo com o EPOS2020 - European Position Paper on Rhinosinusitis and Nasal Polyps 20201, a rinossinusite crónica (com ou sem pólipos nasais) consiste na inflamação do nariz e dos seios perinasais e define-se clinicamente, no adulto, pela existência de 2 ou mais sintomas, um dos quais deverá ser a obstrução/congestão nasal ou a rinorreia anterior/posterior, sendo os outros sintomas a dor/pressão na face e a hiposmia ou anosmia. Para estabelecer o diagnóstico clínico deverão existir ainda sinais endoscópicos de doença (pólipos nasais e/ou rinorreia mucopurulenta a drenar do meato médio e/ou edema/obstrução mucosa primariamente no meato médio); e/ou alterações na tomografia computorizada (alterações na mucosa do complexo ostiomeatal e/ou dos seios perinasais). Para que seja válido o diagnóstico de rinossinusite crónica os sintomas devem estar presentes por um período mínimo de 12 semanas. A rinossinusite crónica com pólipos nasais (RSCcPN), caracteriza-se pela presença de pólipos nasais bilaterais identificados na endoscopia nasal em adjuvante aos critérios acima descritos 1,2.
A rinossinusite crónica é uma doença com elevado impacto em termos de morbilidade da população afetada, como também nos gastos em saúde associados a esta patologia e aos períodos de inatividade laboral 3. No que concerne à epidemiologia, foram realizados dois estudos baseados na endoscopia nasal em Portugal. No primeiro, feito no norte de Portugal foi analisado um grupo de 200 cadáveres caucasianos, tendo-se verificado uma prevalência de pólipos nasais de 5,5% 4. O segundo, realizado em 2018, identificou uma prevalência de RSCcPN de 8,8% em 215 trabalhadores da indústria têxtil, significativamente superior à prevalência encontrada em 101 trabalhadores de venda a retalho (que foi de 0%), sugerindo assim que possa haver uma correlação entre a exposição ocupacional a poeiras e a ocorrência da polipose nasal 5.
Num outro estudo da mesma equipa de investigadores, identificou-se uma taxa de recidiva de 31% em 85 doentes submetidos a cirurgia, acompanhados durante um período de seguimento mínimo de 9 meses e com uso concomitante de glicocorticoides intranasais 6. Nestes doentes, aspetos como a exposição ocupacional a poeiras e a presença concomitante de asma não mediada por IgE foram identificados como fatores preditivos de recidiva da doença. Uma revisão sistemática acerca do papel da cirurgia designada como Functional Endoscopic Sinus Surgery (FESS) no tratamento da RSCcPN, verificou que a recorrência da doença após FESS variou de 4 a 60% com uma mediana de 20% em todos os estudos e, no caso da cirurgia de revisão, o intervalo foi de 3 a 42% com uma mediana de 6% 7. Isto demonstra que existe uma percentagem considerável de doentes que apresentam doença recidivante mesmo após esgotadas todas as medidas médicas convencionais e intervenção cirúrgica 6. É neste espectro de doentes que sê prevê benefício de uma eventual terapia biológica.
A rinossinusite crónica tem-se classificado em dois diferentes fenótipos clínicos, a rinossinusite crónica com pólipos nasais e a rinossinusite sem pólipos nasais. Apesar do conhecimento de que a inflamação crónica está na base destas patologias, a elucidação dos mecanismos subjacentes à doença permanece em níveis insatisfatórios, mantendo-se a perspetiva de que a RSC será uma síndrome clínica que corresponde à manifestação final comum de múltiplas vias fisiopatológicas que atingem as cavidades nasais e os seios peri-nasais. O que se sabe é que parece haver uma associação entre a rinossinusite crónica sem pólipos nasais e uma inflamação tipo 1 e, no caso da RSCcPN, uma maior associação com uma inflamação do tipo 2. Esta inflamação do tipo 2 está mais frequentemente associada a um aumento dos fatores inflamatórios IL-4, IL-5, IL-13 e IgE e vão ser estes mediadores que vão estar na origem dos alvos terapêuticos definidos para as novas terapias biológicas para a RSCcPN 3.
Uma das primeiras terapias biológicas a surgir foi o omalizumab. Este funciona como um anticorpo monoclonal anti-IgE humano que se liga às moléculas de IgE livres reduzindo os seus níveis circulantes. Estes níveis reduzidos por sua vez vão diminuir a taxa de ligação de IgE ao seu recetor nos basófilos e mastócitos inibindo assim a sua desgranulação e consequente libertação de citocinas e mediadores inflamatórios 8.
No que diz respeito à IL-5, esta desempenha funções na diferenciação, quimiotaxia e sobrevivência dos eosinófilos, células que desempenham um papel importante na inflamação tipo 2. Anticorpos monoclonais como o mepolizumab atuam como terapêuticas anti-IL-5, possuindo elevada afinidade para a IL-5. Já o benralizumab tem como alvo terapêutico o recetor IL-5, o qual está expresso na superfície tanto dos eosinófilos como dos basófilos. Este consegue inibir a ação da IL-5 nos seus recetores e assim causar citotoxicidade mediada por células dependentes de anticorpos (8).
Já a IL-4 e IL-13 ativam respostas inflamatórias do tipo 2 através da síntese de IgE e tipos celulares relacionados, partilhando como recetor comum o IL-4Rα e atuando como dois mediadores fundamentais na diferenciação Th2. O dupilumab aparece como um anticorpo monoclonal contra o IL-4Rα, com grandes expectativas quanto à sua influência no controlo do processo inflamatório subjacente à RSCcPN (8).
Material e Métodos
A pesquisa referente à literatura publicada sobre o tema desta revisão sistemática com meta-análise foi realizada em 2022 (última data de pesquisa a 02 de fevereiro), utilizando a checklist PRISMA 2020 (Preferred Reporting Items for Systematic Reviews and Meta-Analysis) e a base de dados PubMed. Os ensaios clínicos randomizados (ECRs) incluídos foram também investigados no website www.clinicaltrials.gov. Apenas foram incluídos artigos portugueses e ingleses. Dado tratar-se de uma revisão sistemática, não foi requerida aprovação pela comissão de ética. Foi elaborado um protocolo, submetido e aprovado na PROSPERO (CRD42022308005).
Nesta revisão, foram considerados os artigos publicados entre os anos 2011 e 2021. A pesquisa bibliográfica foi executada por três investigadores independentes, utilizando a sequência de caracteres (rhinosinusitis OR "chronic rhinosinusitis" OR "nasal polyps" OR "nasal polyposis") AND ("monoclonal antibodies" OR biologics OR humanized) AND (treatment OR therapy OR management). A seleção de estudos foi realizada por três investigadores, inicialmente através da leitura rápida do título e resumo do estudo em que numa primeira fase foram excluídos artigos que não se enquadrassem no tema das terapias biológicas na RSCcPN, e numa segunda fase foram excluídos todos os artigos que não fossem ECRs. Posteriormente, os ECRs foram revistos a texto inteiro e foi verificado se cumpriam os critérios de inclusão seguintes:
População com idade superior a 18 anos;
Presença de rinossinusite crónica com pólipos nasais;
Refratariedade ao tratamento com glicocorticoides, e/ou cirurgia prévia a pólipos nasais (mais de três meses de intervalo) com recidiva;
Nasal Polyp Score bilateral ≥5, com uma pontuação ≥ 2 para cada narina.
Paralelamente, foram também estabelecidos critérios de exclusão, nomeadamente:
Doentes com fibrose cística, rinossinusite fúngica alérgica, discinesia ciliar, pólipos antro-coanais e pólipos nasais associados a condições malignas nasossinusais.
Para avaliar o risco de viés, foi utilizada a ferramenta Cochrane risk-of-bias9.
A extração e revisão de dados foi conduzida por três investigadores e qualquer diferença encontrada foi ultrapassada através de desempate. Nesta fase foram extraídos dados relativamente à população de cada estudo e de cada grupo (controlo vs placebo), duração, terapêutica envolvida e respetivo protocolo assim como média e desvio padrão de ambos os grupos relativamente aos parâmetros utilizados na meta-análise.
Os parâmetros avaliados na meta-análise consistiram na análise da qualidade de vida associada à saúde, mensurada através do teste SNOT-22 10(Sino Nasal Outcome Test-22, escala 0-110, diferença clinicamente significativa mínima de 9 (11), em que “maior significa pior”), e na extensão da doença, medida através do NPS 12 (Nasal Polyp Score, escala visual endoscópica que pontua de 0 a 8, em que para cada narina 0 = sem pólipos e 4 = pólipos grandes) e do Lund Mackay Score13 (pontuação 0-24, em que “maior significa pior”, que utiliza a tomografia computadorizada dos seios perinasais para avaliar a extensão da rinossinusite crónica). Estes resultados foram analisados usando o Review Manager 5.4.1 sobre a forma de tabelas comparativas dos diferentes parâmetros utilizando dados contínuos. A variância inversa foi utilizada como método estatístico, os efeitos aleatórios como modelo de análise e a diferença média como medida de efeito. O intervalo de confiança (IC) do estudo aplicado foi de 95% e a heterogeneidade foi medida para todas as comparações. Os resultados foram considerados significativos quando P<0,05.
A segurança dos ensaios foi declarada de acordo com os eventos adversos reportados, a sua severidade e associação com a intervenção comparada com placebo.
Para avaliar o custo-benefício dos medicamentos biológicos, foi efetuada uma revisão da literatura pertinente com pesquisa na PubMed dos termos “biologics”, “cost-efficacy”, “dupilumab”, “monoclonal antibodies”, “chronic rhinosinusitis” e “nasal polyps”. Foram identificados ainda artigos adicionais, a partir da revisão das listas de referências bibliográficas.
Resultados
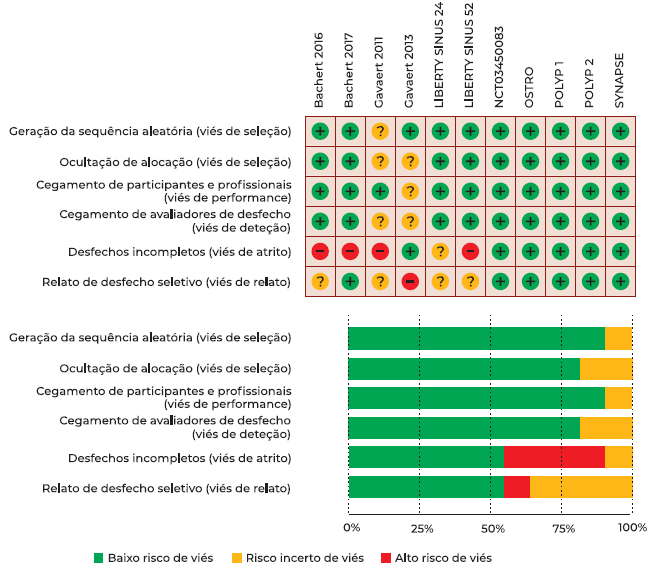
Nesta revisão sistemática, foram incluídos dez estudos, sendo que o risco de viés foi considerado “baixo” ou “pouco claro” na maioria dos parâmetros. No gráfico de risco de viés, presente na Figura 1, é possível observar a avaliação dos autores da revisão relativamente a cada parâmetro de risco de viés, sendo que a percentagem apresentada diz respeito à totalidade de estudos incluídos. Na Figura 1 está também ilustrado um resumo do risco de viés, sendo apresentada a avaliação dos autores em cada parâmetro de risco de viés para cada estudo incluído, individualmente.
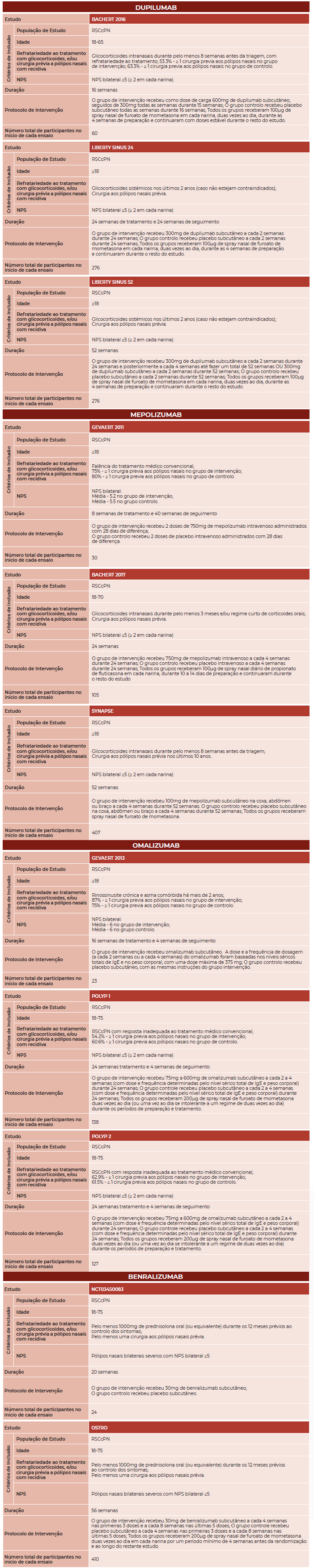
Na Figura 2 pode-se observar o fluxograma do estudo. Foram identificados 1330 artigos através do meio de pesquisa PubMed e, para além destes, 2 outros artigos foram adicionados através de outras fontes. Dos 1332 artigos encontrados, constatou-se que 4 encontravam-se duplicados e, após uma leitura rápida do título e resumo, 1118 foram excluídos numa primeira fase e 189 excluídos na segunda fase. Dos 21 artigos resultantes lidos em texto integral 12 foram excluídos, ou porque não cumpriam os critérios de inclusão/exclusão ou porque eram artigos que abordavam o mesmo estudo. No total contabiliza-se 9 artigos em que 7 desses artigos abordam um estudo por artigo e 2 abordam dois estudos por artigo (LIBERTY SINUS 24 e LIBERTY SINUS 52 são dois ensaios diferentes abordados no mesmo artigo (14) assim como POLYP 1 e POLYP 2 (15)) o que totaliza no final 11 estudos usados na meta-análise. Os critérios de inclusão dos estudos envolvidos na meta-análise estão expostos na Tabela 1.
Tabela 1 Critérios de inclusão e principais características dos ensaios clínicos randomizados incluídos na revisão sistemática com meta-análise.
Foram testados diferentes anticorpos monoclonais através destes 11 ECRs, nomeadamente: dupilumab, abordado em 3 ECRs 14,16 omalizumab, abordado em 3 ECRs 15,17; mepolizumab, abordado em 3 ECRs 18-20 e benralizumab, abordado em 2 ECRs 21,22. A eficácia destes anticorpos monoclonais foi avaliada através do SNOT-22, do NPS e do Lund Mackay Score. Os resultados encontram-se sumarizados na Tabela 2.
Tabela 2 Resultados da meta-análise em que se comparam os grupos intervenção e placebo dentro dos parâmetros avaliados como resposta á terapêutica com anticorpos monoclonais na rinossinusite crónica com pólipos nasais.
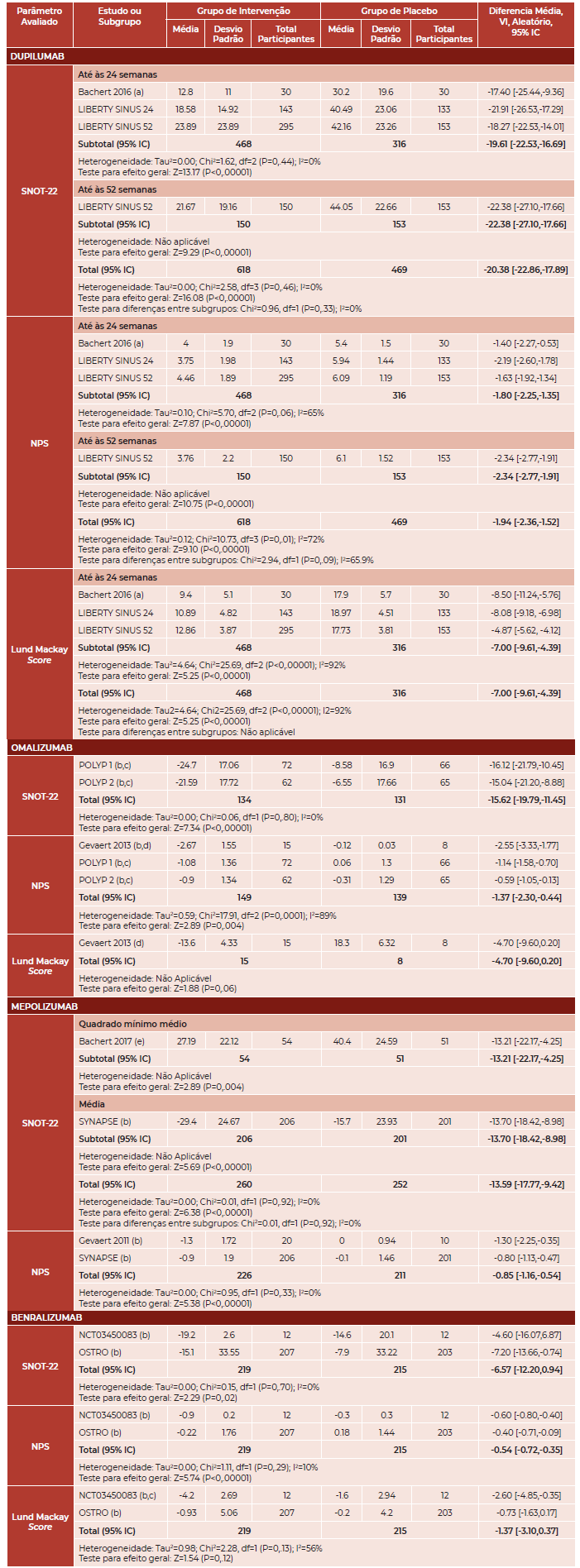
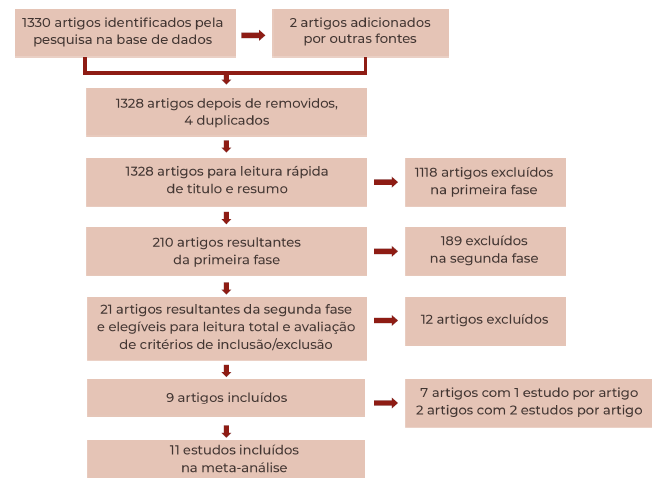
Figura 2 Diagrama de fluxo de estudos PRISMA - Preferred Reporting Items for Systematic Reviews and Meta-Analysis.
Dupilumab
Os efeitos do dupilumab foram avaliados nos estudos Bachert 2016, LIBERTY SINUS 24 e LIBERTY SINUS 52 (14,16), sendo que os parâmetros SNOT-22, NPS e Lund Mackay Score foram avaliados às 24 semanas pelos 3 estudos e o SNOT-22 e NPS foram adicionalmente avaliados às 52 semanas pelo LIBERTY SINUS 52.
Relativamente ao de impacto na qualidade de vida, com o uso de dupilumab verificou-se uma diferença média de -19.61 [(95% CI, -22.53, -16.69), (P<0,00001)] pontos no SNOT-22 às 24 semanas nos 3 estudos e uma diferença média de -22.38 [(95% CI, -27.10, -17.66), (P<0,00001)] pontos às 52 semanas no LIBERTY SINUS 52 em comparação com o uso de placebo.
Relativamente à extensão da doença, com o uso de dupilumab verificou-se uma diferença média de -1.80 [(95% CI, (-2.25, -1.35), (P<0,00001)] pontos no NPS e de -7.00 [(95% CI, -9.61, -4.39), (P<0,00001)] pontos no Lund Mackay Score às 24 semanas nos 3 estudos e uma diferença média de -2.34 [(95% CI, -2.77, -1.91),(P<0,00001] pontos no NPS às 52 semanas no LIBERTY SINUS 52 em comparação com o uso de placebo.
Omalizumab
Os efeitos do omalizumab foram avaliados nos estudos Geavert 2013, POLYP 1 e POLYP 2 (15,17), sendo que o parâmetro SNOT-22 foi avaliado pelos estudos POLYP 1 e POLYP 2, o NPS pelos estudos Geavert 2013, POLYP 1 e POLYP 2 e o Lund Mackay Score pelo estudo Geavert 2013.
Em relação ao impacto na qualidade de vida, com o uso de omalizumab verificou-se uma diferença média de -15.62 [(95% CI, -19.79, -11.45), (P<0,00001)] pontos no SNOT-22 nos estudos POLYP1 e POLYP2 em comparação com o uso de placebo.
No que diz respeito à extensão da doença, com o uso de omalizumab verificou-se uma diferença média de -1.37 [(95% CI, -2.30, -0.44), (P=0,004)] pontos no NPS nos estudos Geavert 2013, POLYP 1 e POLYP 2 em comparação com o uso de placebo. Em relação ao Lund Mackay Score este foi apenas analisado pelo estudo Gevaert 2013, tendo verificado uma diferença média de -4,7 pontos embora sem resultado estatisticamente significativo (P=0,06).
Mepolizumab
Os efeitos do mepolizumab foram avaliados nos estudos Gevaert 2011, Bachert 2017 e SYNAPSE (18-20), sendo que o parâmetro SNOT-22 foi avaliado pelos estudos Bachert 2017 e SYNAPSE e o NPS pelos estudos Gevaert 2011 e SYNAPSE. Nenhum estudo reportou dados válidos para análise em relação ao Lund Mackay Score.
Relativamente ao impacto na qualidade de vida, com o uso de mepolizumab verificou-se uma diferença média de -13.59 [(95% CI, -17.77, -9.42), (P<0,00001)] pontos no SNOT-22 nos estudos Bachert 2017 e SYNAPSE em comparação com o uso de placebo.
No que concerne à extensão da doença, com o uso de mepolizumab verificou-se uma diferença média de -0.85 [(95% CI, -1.16, -0.54), (P<0,00001)] pontos no NPS nos estudos Gevaert 2011 e SYNAPSE em comparação com o uso de placebo.
Benralizumab
Os efeitos do benralizumab foram avaliados nos estudos NCT03450083 e OSTRO (21,22), sendo que os três parâmetros (SNOT-22, NPS e Lund Mackay Score) foram todos avaliados pelos mesmos dois estudos.
Em termos de impacto na qualidade de vida, com o uso de benralizumab verificou-se uma diferença média de -6.57 [(95% CI, -12.20, 0.94), (P=0,02)] pontos no SNOT-22 nos estudos NCT03450083 e OSTRO em comparação com o uso de placebo.
Nos parâmetros da extensão da doença, com o uso de benralizumab verificou-se uma diferença média de -0.54 [(95% CI, -0.72, -0.35), (P<0,00001)] pontos no NPS e de -1.37 [(95% CI, -3.10, -0.37), (P=0,12)] pontos no Lund Mackay Score nos estudos NCT03450083 e OSTRO em comparação com o uso de placebo, embora o resultado do parâmetro Lund Mackay Score não seja estatisticamente significativo.
Efeitos Adversos
Na generalidade dos estudos a percentagem de efeitos adversos foi sobreponível tanto no grupo de tratamento como no grupo placebo. Em nenhum estudo foram reportados efeitos adversos graves associados ao tratamento.
Os efeitos adversos mais comuns foram nasofaringite, dor de cabeça e reações no local da injeção.
Em alguns estudos foram reportadas mortes durante o tratamento, mas nenhuma foi relacionada com o mesmo.
Custo-Benefício dos Medicamentos Biológicos
Luke Rudmik et al. realizaram um estudo em que a FESS seguida de tratamento médico pós operatório foi comparada com o tratamento médico continuado (“convencional”) para a RSCcPN, sendo que foi concluído que a FESS era uma estratégia de tratamento mais custo-efetiva que a terapia médica continuada sozinha, tendo a FESS um custo total de 48,838.38$ acoplado à produção de um total de 20.50 QALYs (Quality Adjusted Life Year) e a terapêutica médica sozinha um custo total de 28,948.98$ associado a uma produção de 17.13 QALYs32. O custo acrescido da FESS comparado com a terapêutica médica continuada sozinha foi de 5,901.90$ por QALY, sendo este um valor considerado aceitável num limite orçamental de 25.000$ por QALY adicionado ao doente32. Num estudo diferente chegou-se à mesma conclusão, ficando provado com 95% de certeza que a FESS era uma hipótese mais custo efetiva num limite orçamental de 20.000$ 33.
Num estudo mais recente, George A. Scangas et al. realizaram uma análise custo-eficácia em que confrontaram a FESS com o uso do dupilumab usando o modelo económico de 10 estados de Markov. Nessa análise, um cohort com 197 doentes com RSCcPN que foram submetidos a FESS foram comparados com 293 doentes com RSCcPN dos ECRs LIBERTY SINUS 24 e LIBERTY SINUS 5214 submetidos a tratamento com dupilumab 34. Usando uma perspetiva temporal de 36 anos, George A. Scangas et al. verificaram que a intervenção cirúrgica conseguiu um total de 9.80 QALYs com um custo de 50,436.99$ ao passo que o tratamento com dupilumab obteve um total de 8.95 QALYs mas com um custo de 536,420.22$ 34. Isto levou os autores a concluírem que a terapêutica com dupilumab era não só extremamente mais cara, como tinha uma eficácia inferior em comparação com a FESS. George A. Scangas et al., através de análises de sensibilidade unidirecionais, mostraram que, para qualquer custo anual do dupilumab acima de 855$, a FESS é mais custo efetiva independentemente do número de cirurgias de revisão necessárias 34.
Discussão
A RSCcPN é uma doença crónica, que está presente em um número significativo de doentes com alta comorbilidade associada e características heterogéneas entre eles. Existe um grande número de doentes que permanecem com doença não controlada, apesar do uso de glicocorticoides tópicos e/ou orais, bem como após cirurgia. Nesta meta-análise, foi comparada a eficácia dos diferentes anticorpos monoclonais no controlo da doença refratária às terapêuticas convencionais.
O anticorpo que mais eficácia demonstrou foi o dupilumab. Quanto ao impacto na qualidade de vida, este anticorpo conseguiu reduzir às 24 semanas um total de -19.61 (P<0,00001) pontos no SNOT-22 em comparação com o uso de placebo. Considerando que a escala SNOT-22 tem como diferença clinicamente significativa mínima um valor de 9 pontos 11, podemos concluir que este anticorpo monoclonal teve um impacto considerável na melhoria dos sintomas e qualidade de vida dos doentes. Com o prolongamento do estudo LIBERTY SINUS 52 14 até às 52 semanas foi atingida uma diferença média -22.38 (P<0,00001) pontos no SNOT-22, ou seja um resultado ainda melhor no longo prazo. No caso da extensão da doença, esta diferença entre o grupo em que foi descontinuado o tratamento às 24 semanas (-1.80 (P<0,00001) pontos no NPS e -7.00 (P<0,00001) pontos no Lund Mackay Score) e o grupo em que foi continuado o tratamento até às 52 semanas (-2.34 (P<0,00001) pontos no NPS) também foi observada, o que pode indicar que ainda não foi atingido o potencial máximo da terapia monoclonal. Apesar de se verificar uma redução da extensão da doença, esta é ainda limitada, com persistência dos pólipos, não oferecendo por isso uma remissão completa dos mesmos. Além disso, nos doentes que descontinuaram o tratamento no LIBERTY SINUS 24 (14) após as 24 semanas, houve um ressurgimento/agravamento progressivo dos sintomas. Isto reflete uma necessidade de tratamento crónico, de forma contínua ou intermitente, com anticorpos monoclonais para que sejam mantidos os resultados.
Em relação aos restantes anticorpos monoclonais, também foram encontradas melhorias apesar de menos expressivas. Para isto pode contribuir o facto de que a quantidade, extensão populacional e tempo de intervenção dos estudos referentes ao omalizumab, mepolizumab e benralizumab ter sido consideravelmente mais baixa do que com o dupilumab. São por isso necessários mais estudos com maiores amostras populacionais e mais prolongados no tempo para caracterizar melhor o impacto destas novas terapias na RSCcPN.
No caso do impacto na qualidade de vida tanto o omalizumab, o mepolizumab como o benralizumab tiveram reduções no SNOT-22 significativas em comparação com o uso de placebo, ainda que inferiores relativamente ao dupilumab. No entanto, no caso do benralizumab o parâmetro SNOT-22 ficou abaixo da diferença clinicamente significativa mínima e mesmo no que concerne à extensão da doença os resultados apesar de significativos foram modestos, tendo se verificado apenas uma diferença média de -0.60 (P<0,00001) pontos no NPS em comparação com o uso de placebo. Com o omalizumab verificou-se uma diferença média de -1.37 (P=0,004) pontos no NPS e com o mepolizumab uma diferença média de -0.85 (P<0,00001) pontos no NPS em comparação com o uso de placebo. Apesar de terem tido mais eficácia do que o benralizumab, o impacto permanece pouco considerável face ao score mínimo de entrada para inclusão no estudo (NPS bilateral ≥5, com uma pontuação ≥ 2 para cada narina). Os resultados da análise referente ao parâmetro Lund Mackay Score não foram avaliados nos estudos referentes ao mepolizumab. Os resultados no caso do omalizumab e do benralizumab, embora não tenham sido estatisticamente significativos revelaram uma tendência para a redução do Lund Mackay Score, com uma diferença média de -4,7 pontos (P=0,06) no caso do omalizumab, e uma diferença média de -1.37 (P=0,12) pontos no caso do benralizumab, em comparação com o uso de placebo.
Um estudo publicado recentemente sobre esta temática, chegou às mesmas conclusões no que concerne ao Dupilumab como melhor escolha no controlo da RSCcPN. Neste estudo realçam ainda o Omalizumab como segundo melhor agente no controlo da doença e apontam o Mepolizumab como o anticorpo monoclonal com maior perfil de efeitos adversos. 36
O nosso estudo possui algumas limitações. Uma delas deve-se ao facto de que parece ainda não ter sido atingido um potencial máximo da terapia monoclonal o que reflete uma necessidade de estudos futuros mais alargados no tempo, para ter dados acerca de um eventual pico terapêutico, bem como de eventuais efeitos adversos de aparecimento mais tardio. Não sabemos também até que ponto uma mudança do tipo de padrão inflamatório basal poderá ter impacto na pessoa e nos seus multissistemas, e que possíveis efeitos adversos possam daí advir.
Indicações dos Biológicos e análise custo eficácia do Dupilumab
Dos anticorpos estudados nos ECRs aqui referidos, apenas o benralizumab não tem indicação formal por parte da Food and Drug Administration23 e European Medicines Agency24 como possível arma terapêutica para o controlo da RSCcPN. Todos os outros anticorpos monoclonais nomeadamente o dupilumab, omalizumab e mepolizumab têm neste momento indicação por parte da Food and Drug Administration25-27 e European Medicines Agency28-30 para o tratamento da RSCcPN severa não controlada apesar do uso de glicocorticoides sistémicos e/ou cirurgia.
Num mundo ideal, a saúde não teria um valor idealizado, no entanto, não podemos deixar de ter em consideração o preço dos tratamentos. Assim, cada terapia tem um valor associado em que o mesmo é definido como a sua qualidade dividida pelo seu custo3. Através do termo Quality Adjusted Life Year (QALY), em que um QALY representa um ano de boa saúde ganho por um determinado indivíduo com a implementação da nova terapia a ser estudada, é possível quantificar o benefício de uma determinada intervenção através do número de QALY’s adicionados por esta e, além disso, podemos estimar o valor da terapêutica usando o custo inerente a cada QALY adicionado à vida do doente 3,31. Os resultados obtidos pela revisão efetuada levantam o problema das implicações económicas associadas ao uso destes novos medicamentos. Se ninguém duvida do elevado impacto económico associado à RSCcPN, não se poderá deixar de questionar também qual o custo que estaremos disponíveis a suportar, enquanto sociedade, com os novos medicamentos biológicos, para conseguir efeitos terapêuticos ainda bastante limitados, nomeadamente em comparação com os tratamentos “convencionais” médicos e cirúrgicos.
Critérios para uso de anticorpos monoclonais na RSCcPN
Com esta noção do custo envolvido nas terapêuticas biológicas associado ao seu potencial inovador para o controlo da RSCcPN, é imperioso que sejam bem classificados os doentes que poderiam beneficiar mais com esta terapêutica.
O European Forum for Research and Education in Allergy and Airway Diseases (EUFOREA) 35 organizou em 2019 uma reunião do conselho de especialistas multidisciplinar para discutir o posicionamento dos biológicos na RSCcPN. Nesta reunião chegaram ao consenso de que para um doente ter indicação terapêutica com biológicos seria necessário a presença de pólipos nasais bilaterais e, 3 ou 4 dos critérios apresentados na Tabela 3, consoante a presença ou ausência de cirurgia prévia respetivamente 35.
Tabela 3 Critérios para uso de terapia biológica em doentes com rinossinusite crónica com pólipos nasais.

No entanto, quando um biológico é usado para tratamento, é fulcral avaliar a resposta do doente na tentativa de evitar tratamentos inapropriados e custos desnecessários. Assim, nesta mesma reunião, foi proposto que para ser considerada uma resposta aceitável à terapia biológica seria preciso avaliar a resposta a 5 critérios que se encontram apresentados na Tabela 4, após 1 ano de tratamento. Consoante o número de critérios satisfeitos, esta resposta seria classificada (ver Tabela 4) e caso não se verificasse resposta ao tratamento, este deveria ser descontinuado 35.
Conclusão
Nesta revisão sistemática conseguimos verificar que o dupilumab foi o anticorpo monoclonal com mais impacto, tanto na qualidade de vida como na extensão da doença, sendo necessários mais estudos no futuro para avaliar melhor o efeito a longo prazo destas novas terapêuticas. No entanto, dado o impacto económico que implica a sua aplicação é imperioso que se avalie de forma eficaz e eficiente quais os potenciais doentes que mais podem beneficiar com elas.