Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Arquivos de Medicina
versão On-line ISSN 2183-2447
Arq Med vol.25 no.5-6 Porto dez. 2011
ARTIGO DE REVISÃO
O Papel da Via Serreada na Carcinogénese Colo-rectal
The role of the serrated pathway in the colorectal carcinogenesis
Sérgio Agostinho Xavier Azevedo1
1 Faculdade de Medicina da Universidade do Porto
RESUMO
O carcinoma colo-rectal é uma das neoplasias malignas mais comuns em termos de incidência e mortalidade, em Portugal e no Mundo Ocidental. São reconhecidos vários mecanismos moleculares associados à carcinogénese colo-rectal esporádica, nomeadamente a instabilidade cromossómica, a instabilidade de microssatélites e, mais recentemente, a instabilidade epigenética (também designada por fenótipo CIMP). Do ponto de vista morfológico reconhecem-se duas vias principais, a adenomatosa e a serreada, associadas, respectivamente, a instabilidade cromossómica e instabilidade de microssatélites (com ou sem fenótipo CIMP). Neste trabalho apresentase uma revisão das características morfológicas e moleculares das lesões precursoras da via serreada (pólipos hiperplásicos, pólipos/ adenomas serreados sésseis, pólipos/ adenomas serreados tradicionais, pólipos mistos), da relação entre estas e o carcinoma colo-rectal e das implicações práticas para o rastreio e tratamento dos doentes.
Palavras-chave: adenoma/pólipo adenomatoso; via serreada; pólipo hiperplásico; pólipo/adenoma serreado séssil; pólipo/adenoma serreado tradicional; carcinoma colo-rectal
ABSTRACT
Colorectal carcinoma is one of the most common malignant neoplasms in terms of incidence and mortality in Portugal and the Western World. Multiple molecular mechanisms are associated with sporadic colorectal carcinogenesis, including chromosomal instability, microsatellite instability and, more recently, epigenetic instability (also called ciMP phenotype). From the morphological point of view are considered two main pathways, adenomatous and serrated, respectively associated with chromosomal instability and microsatellite instability (with or without ciMP phenotype). This paper reviews the morphological and molecular characteristics of the precursor lesions of serrated pathway (hyperplastic polyps, sessile serrated adenomas/ polyps, traditional serrated adenomas/ polyps, mixed polyps), the relationship between these lesions and colorectal carcinoma and practical implications for screening and treatment of patients.
Key-words: adenoma/adenomatous polyp; serrated pathway; hyperplastic polyp; sessile serrated adenoma/polyp; traditional serrated adenoma/polyp; colorectal neoplasms
Introdução
O carcinoma colo-rectal (CCR) constitui um importante problema de Saúde Pública no Ocidente, onde a incidência tem vindo a aumentar progressivamente.1 Mundialmente, o CCR constitui a terceira neoplasia maligna mais frequente e a quarta causa de morte por cancro, contribuindo para cerca de 1,2 milhões de novos casos diagnosticados e 600 000 mortes por ano.1
Entre 60%2 a 80%3 dos casos de CCR desenvolvem-se através da designada via adenomatosa que se caracteriza pela acumulação de alterações moleculares ao longo do processo de transformação maligna com expressão morfológica sequencial de lesões que compreendem focos de criptas aberrantes, adenomas com displasia de baixo grau, adenomas com displasia de alto grau e, finalmente, adenocarcinomas.2,3 a alteração molecular mais precoce consiste na mutação somática do gene APC (adenomatous polyposis coli), um elemento da via de sinalização Wnt, à qual se sucedem mutações nos genes KraS e P53, entre muitos outros.4
Esta via de cancerização (mucosa normal – adenoma -carcinoma) verifica-se predominantemente em carcinomas colo-rectais esporádicos, mas também é característica da Polipose adenomatosa Familiar (PAF), uma doença hereditária, de transmissão autossómica dominante, causada na maior parte dos casos por uma mutação germinativa no gene APC, caracterizada pelo desenvolvimento de centenas a milhares de pólipos adenomatosos no cólon com risco de transformação maligna de 100%.5
Na via de cancerização designada como adenomatosa, as lesões precursoras (adenomas) são susceptíveis de identificação endoscópica, permitindo o estabelecimento de programas de prevenção secundária do CCR através do rastreio endoscópico para identificação e exérese dos adenomas/ pólipos adenomatosos6.
Mais recentemente tem sido desenvolvido o conceito de cancerização colo-rectal pela via serreada e de acordo com os dados disponíveis contribui para 15% a 35% dos CCRs.2,3,7,8
Importa também referir a existência de outra forma hereditária de CCR (além da PAF) que corresponde à Síndrome de lynch causada por mutações germinativas em genes do sistema MMR (mismatch repair genes), de que se destacam os genes hMLH1, hMSH2, hMSH6, entre outros.9,10
Este trabalho tem como objectivo principal compreender o papel da via serreada na carcinogénese colo-rectal. Especificamente, pretende analisar as características morfológicas e moleculares das lesões serreadas do cólon, avaliar a relação entre essas lesões e o CCR e avaliar as implicações práticas do conhecimento nesta área para o rastreio do CCR e tratamento dos doentes.
Lesões serreadas do cólon
As lesões serreadas do cólon foram inicialmente descritas por torlakovic e Snover em 1996 e definidas como um conjunto de lesões com configuração das criptas em dente de serra originalmente diagnosticados como pólipos hiperplásicos.11
A nomenclatura das lesões serreadas do cólon tem sido alvo de uma grande controvérsia na literatura, com várias propostas de classificação. Esta panóplia de classificações deve-se em parte à falta de critérios uniformes para a classificação destas lesões, assim como à baixa reprodutibilidade inter e intraobservador(es).12,13 O facto de algumas destas lesões serem sésseis, torna-as facilmente imperceptíveis na endoscopia devido à presença de muco ou má preparação intestinal.14
A arquitectura serreada (em parte ou na totalidade) é um elemento comum a todas as lesões.8,15,16
Seguidamente são apresentadas as principais lesões serreadas e as diferentes propostas de classificação, dando-se destaque à classificação da Organização Mundial de Saúde (OMS), publicada em 2010.5
Pólipos hiperplásicos
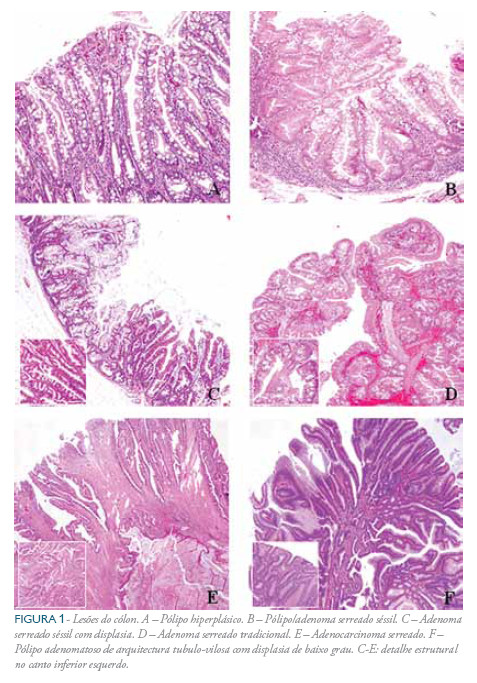
Os pólipos hiperplásicos são considerados, de entre todas as lesões serreadas do cólon, as mais inócuas.2 correspondem a 80-90% das lesões serreadas.3,15,17 Ocorrem em todo o cólon mas são mais comuns no cólondistalenorecto.8,16,18,19 Macroscopicamente são lesões sésseis ou ligeiramente elevadas com um diâmetro geralmente inferior a 5 mm.15 Microscopicamente são caracterizados por criptas alongadas com arquitectura serreada na metade superior das mesmas (Figura 1A).16 A zona proliferativa permanece na porção inferior da cripta, estendendo-se no entanto mais do que o habitual, ocupando mais de metade da altura da cripta.8,16 Contudo, as células continuam a sua maturação em direcção à superfície.18 O aumento da proliferação, bem como a inibição da morte celular programada (apoptose) são responsáveis pelo aspecto serreado destas lesões.2,8,17 Os pólipos hiperplásicos são subdivididos em três subtipos com base no seu padrão de crescimento e nas características celulares (padrão morfológico e padrão de expressão de mucinas).5,20 Foram descritos três subtipos:
- Pólipos hiperplásicos do tipo microvesicular: apresentam arquitectura serreada proeminente e as células têm citoplasma claro e microvesicular. São o subtipo mais frequente e representam os pólipos hiperplásicos típicos do cólon distal.2,5,18
- Pólipos ricos em células caliciformes: são compostos predominantemente por células caliciformes e a serreação é mais subtil do que nos pólipos do tipo microvesicular.2,3,5
- Pólipos pobres em mucina: são os mais raros, têm uma arquitectura micropapilar, o núcleo pode ser hipercromático e têm caracteristicamente infiltrado inflamatório na lámina própria.2,5,21
Na prática, dada a dificuldade em distinguir os diferentes subtipos e uma vez que a relevância clínica desta subclassificação não está demonstrada, a OMS não recomenda a sua aplicação na rotina de diagnóstico.5
A maioria dos pólipos hiperplásicos não apresenta potencial de malignidade.16 contudo, existe evidência de que os do subtipo microvesicular, particularmente os localizados no cólon proximal e os de grandes dimensões, podem corresponder a lesões que precedem a formação de pólipos/ adenomas serreados sésseis (descritos adiante), tendo por isso um risco decancerização que deve ser valorizado.16,19,20
Pólipos/ adenomas serreados sésseis (P/ASS)
Contrariamente às restantes lesões serreadas, os pólipos/ adenomas serreados sésseis são mais frequentes no cólon proximal e têm geralmente mais de 5mm.15 Correspondem a cerca de 18-22% das lesões serreadas do cólon.21 Representam entre 3% a 9% de todos os pólipos do cólon.14,22
Endoscopicamente são sésseis, macios e amarelados. Frequentemente não são identificados devido à presença de muco sobreposto.23 As novas técnicas endoscópicas, como a vídeo-endoscopia de alta resolução e a cromoendoscopia têm vindo a permitir uma melhor visualização destas lesões.12,14,24,25 No cólondistal tendem a ser polipóides.16 O diagnóstico histológico é essencialmente baseado nas características morfológicas da lesão (Figura 1B): criptas ramificadas, dilatação da base das criptas e formação decriptas com morfologia especial (loutinvertido).8,15,21 Estas criptas podem ultrapassar a muscularis mucosae.2,16,18 [aspecto designado por alguns autores como pseudo invasão15]. Estas características são acompanhadas pela presença de células maduras com fenótipo de células caliciformes ou de células foveolares gástricas na base das criptas.26 Assim, é essencial para o diagnóstico destas lesões que a zona basal da mucosa seja avaliada cuidadosamente.15
Os P/ASS não possuem displasia no estadio inicial de desenvolvimento, mas podem adquirir essa característica ao longo da progressão neoplásica (Figura 1C).19,23
O risco de malignização destas lesões ainda não foi quantificado, mas existe evidência de que a sua presença está associada a um aumento de risco de adenocarcinoma serreado (Figura 1E), particularmente no caso de indivíduos do género feminino, de lesões com grandes dimensões e em localização proximal.8,17,20,23,25
Esta lesão satisfaz os critérios de lesão pré-cancerosa definida pela National Cancer Institute-sponsored Conference on Precancer (Tabela 1)27

Pólipos/ adenomas serreados tradicionais (P/AST)
Os pólipos/ adenomas serreados tradicionais ocorrem em todo o cólon, predominam à esquerda, possuem normalmente uma forma pediculada mas também podem ser planos ou ligeiramente elevados.2,13 Geralmente têm mais de 10 mm de diâmetro e apresentam 15,23 aspecto endoscópico cerebriforme ou em pétala. Correspondem a 0,6 a 1,3% das lesões serreadas.18 Microscopicamente (Figura 1D) apresentam lesões de displasia/ neoplasia intraepitelial, o padrão de crescimento ocorre da base da cripta em direcção à superfície, têm morfologia serreada e não apresentam dilatação, horizontalização ou ramificação das criptas.2,21 Tipicamente apresentam criptas ectópicas, o que cria um padrão de crescimento complexo, o citoplasma é hipereosinofílico e há estratificação nuclear.2,16 estas lesões podem desenvolver-se a partir de pólipos hiperplásicos ou pólipos/ adenomas serreados sésseis, ou podem desenvolver-se de novo16
Pólipos mistos
Os pólipos mistos são combinações de adenomas convencionais (tubulares, tubulovilosos (Figura 1F), vilosos) com diferentes graus de displasia/ neoplasia intraepitelial e lesões serreadas.15,16 existem diferentes formas de pólipos mistos de acordo com os seus componentes: P/ASS e adenoma convencional, P/ AST e adenoma convencional ou pólipo hiperplásico e adenoma.15,16 Estas lesões tendem a ocorrer no cólon proximal, têm normalmente mais de 5 mm e apresentam displasia.15 Não está esclarecido se estas lesões se desenvolvem a partir de pólipos hiperplásicos pré-existentes ou se os componentes hiperplásico e displásico resultam de processos independentes.3 é frequente encontrarem-se nos P/ASS áreas com características típicas de pólipo hiperplásico.8 À designação de pólipo misto deve ser acrescentada a descrição dos componentes da lesão entre parêntesis.16,17,20 Uma perspectiva ligeiramente diferente é apresentada na nova classificação da OMS que propõe que os designados pólipos mistos sejam considerados como P/ASS com displasia.5
Alterações moleculares
As lesões serreadas do cólon apresentam características que as distinguem dos adenomas convencionais, e que as relacionam com o adenocarcinoma serreado.18,20,28
No plano molecular, as principais alterações que caracterizam a via serreada de carcinogénese colo-rectal são as mutações dos genes BRAF e KRAS, a metilação de múltiplos promotores de genes por fenómenos epigenéticos e a instabilidade de microssatélites.3,5,19-21
Mutação dos genes BRAF e KRAS
Estes genes representam componentes da via de sinalização RAS/RAF/MAPK, envolvida na regulação da proliferação celular do tubo digestivo.8 As mutações resultam na activação contínua do gene, conduzindo a um estado de proliferação celular autónoma, sem controlo.8
A mutação BRAF V600E é encontrada em focos de criptas aberrantes, pólipos hiperplásicos do tipo microvesicular e P/ASS, tendo sido demonstrado que existe um forte associação entre o diagnóstico histológico de P/ASS e a presença da mutação BRAF29-31. Quando a mutação BRAF está presente num CCR, a sua presença está fortemente associada a instabilidade de microssatélites e ao fenótipo CIMP.19,32 A presença da mutação BRAF V600E suporta também a interpretaçãodequesetratadeumcasoesporádico.31 Apesar de a via serreada com mutação BRAF ser predominante (cerca de 70% dos adenocarcinomas serreados esporádicos), uma segunda via está associada à mutação do gene KRAS.19 a mutação KRAS é encontrada em 37% dos casos de pólipos hiperplásicos, particularmente os do subtipo rico em células caliciformes,8,15 bem como em P/aSt.8,16 Os CCRs que se desenvolvem por esta via, usualmente designada como via serreada tradicional, parecem ter um pior prognóstico que aqueles que se desenvolvem pela via serreada séssil.19,21
As mutações BRAF e KRAS nas lesões serreadas do cólon são mutuamente exclusivas.2,3,8,19,23
Fenótipo CIMP (CpG island methylation phenotype)
A metilação anormal dos promotores de genes supressores tumorais, por um mecanismo epigenético, representa um mecanismo associado à carcinogénese colo-rectal. 30 a 50% dos CCRs apresentam evidência deste fenótipo molecular.8,23
Na via serreada, a metilação das ilhas CpG ocorre numa fase precoce da carcinogénese, com a presença desta alteração em focos de criptas aberrantes, pólipos hiperplásicos e na mucosa cólica normal adjacente às lesões serreadas.8,21,33 consideram-se duas formas deste fenótipo: CIMP-H (CpG island methylation phenotype – high) e CIMP-L (CpG island methylation phenotype –low).8,21,23 Os carcinomas CIMP-H localizam-se mais frequentemente no cólon direito, apresentam características histológicas de carcinoma mucinoso ou pouco diferenciado e, frequentemente, apresentam instabilidade de microssatélites e mutação BRAF.2
Os genes frequentemente alterados por este mecanismo incluem o hMLH1, MGMT, p16/CDKN2A e EPHB2.8
Instabilidade de microssatélites
A instabilidade de microssatélites foi inicialmente descrita em indivíduos com Síndrome de Lynch.
Nestes doentes verifica-se a ocorrência de mutações germinativas em genes envolvidos na reparação do DNA (MMR, mismatch repair genes), mais frequentemente os genes hMLH1 e hMSH2. A perda destes genes conduz a um estado hipermutável no qual ocorrem erros na reparação de defeitos da replicação de sequências de DNA simples e repetitivas, os microssatélites.4
A maioria das sequências de microssatélites estão em regiões não codificantes do genoma.8 Contudo, algumas sequências localizam-se em regiões codificantes ou regiões promotoras de genes envolvidos na regulação da proliferação celular, como por exemplo no BCL2 e no gene que codifica o receptor tipo II do TGF-ß. 19,23
A instabilidade de microssatélites que ocorre nos casos esporádicos resulta da perda funcional do gene hMLH1 por um fenómeno epigenético, em que se verifica metilação do seu promotor, sendo extremamente rara a ocorrência de alterações em outros genes MMR. 9,28,34
Os adenocarcinomas que se desenvolvem pela via serreada apresentam, na sua maioria, níveis elevados de instabilidade de microssatélites (MSI-H, microsatellite instability high).8,17,28
Estes adenocarcinomas localizam-se geralmente no lado direito do cólon e, quando esporádicos, estão associados a idade avançada e ao género feminino.3 Há evidência que suporta a relação dos P/ASS com este tipo de carcinoma.21,28 Por outro lado, os CCRs que não apresentam níveis elevados de instabilidade de microssatélites – são MSS (microsatellite stable) ou MSI-L (microsatellite instability – low) – localizamse predominantemente no cólon distal e recto.3,23,35 Estes adenocarcinomas têm origem em P/aSt com mutação KRAS e estão frequentemente associados a metilação do promotor do gene MGMT.2,36 Estes tumores parecem ter pior prognóstico, comparativamente aos que apresentam MSI-H. 19,21
Comparação via serreada/ via adenomatosa
As vias adenomatosa e serreada de carcinogénese colo-rectal são geralmente descritas separadamente na literatura. Na Figura 2 apresentam-se as características (morfológicas e moleculares) das principais vias de carcinogénese colo-rectal: via clássica adenomatosa, via serreada séssil e via serreada tradicional.
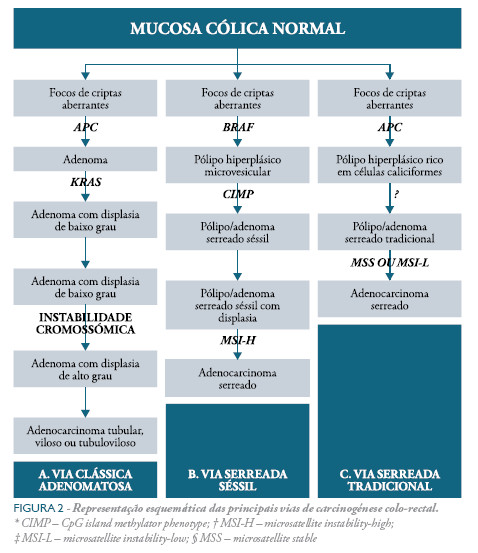
O silenciamento epigenético (fenótipo CIMP) dos genes envolvidos na via serreada foi demonstrado nas lesões precursoras e nos adenocarcinomas resultantes.8,17,19,23 Este mecanismo difere do processo mutagénico da via clássica em que adenomas convencionais progridem para adenocarcinoma através de delecções e perda de heterozigotia de genes supressores tumorais devido à instabilidade cromossómica induzida pela mutação APC e mutações de oncogenes (KRAS).5 O fenótipo CIMP também foi demonstrado na progressão de adenomas convencionais para adenocarcinoma.17
A via de sinalização Wnt parece desempenhar um papel diminuto na via serreada.37 Ao contrário do que acontece nos adenomas convencionais em que há mutação do gene APC com acumulação intracelular de ß catenina, na via serreada ocorre a metilação do promotor do gene APC.37 Este mecanismo ocorre, contudo, numa minoria dos casos.37
A mutação KRAS, característica da via serreada tradicional também está presente em alguns casos de adenocarcinoma não-serreado.21 A mutação BRAF, presente em 75% das lesões serreadas do cólon (via serreada séssil), não é frequente em adenomas convencionais, esporádicos ou no contexto da PAF.31,33
As alterações moleculares características da via serreada e da via adenomatosa podem ocorrer em simultâneo numa minoria (<2%) de lesões adenomatosas do cólon e recto que apresentam características morfológicas e moleculares de ambas as vias. Este fenótipo está associado a uma maior agressividade do adenocarcinomaresultante.17,38,39
Polipose hiperplásica/ polipose serreada (OMS)
A síndrome de polipose hiperplásica (SPH) é uma condição pré-neoplásica, na qual se encontram múltiplas lesões serreadas, particularmente pólipos hiperplásicos, com distribuição pancólica.21 adenomas convencionais sem arquitectura serreada podem ocorrer juntamente com as lesões serreadas nos indivíduos com SPH.40 A maioria das lesões é diminuta (cerca de 2-3mm), o que as torna difíceis de diagnosticar na maioria dos exames endoscópicos de rotina, a menos que haja um alto índice de suspeição que conduz à utilização de técnicas especiais de endoscopia.41
A idade de apresentação e a multiplicidade das lesões sugere uma predisposição genética para a polipose hiperplásica, mas a sua causa genética continua por identificar.42
O subtipo mais frequente de adenocarcinoma na SPH é aquele que, do ponto de vista molecular, se caracteriza por ausência ou baixo grau de instabilidade de microssatélites (MSS ou MSI-L).29 Curiosamente este é também o subtipo com maior associação a história familiar.8
O risco de CCR é superior a 50% e podem ocorrer múltiplos carcinomas síncronos ou metácronos.12,21 Num estudo em que 77 pacientes com SPH foram seguidos através de estudo endoscópico, a prevalência de CCR foi de 35%.43
Os critérios de diagnóstico de SPH propostos pela OMS incluem: i) pelo menos cinco pólipos serreados com localização proximal ao cólon sigmóide ou dois ou mais destes com dimensões maiores de10mm; ii) qual quer número de pólipos serreados proximalmente ao cólon sigmóide num indivíduo com um familiar em primeiro grau com diagnóstico de polipose hiperplásica; iii) mais de 20 pólipos serreados de qualquer tamanho, distribuídos por todo o cólon.5 No estudo de Carvajal-Carmona et al.42 São apresentados critérios moleculares que, na opinião dos autores, podem complementar os critérios morfológicos da OMS na definição de SPH de modo a tornar mais evidente a distinção entre os casos esporádicos de lesões serreadas do cólon e os casos em que estas lesões surgem no contexto de SPH. Assim, é demonstrado que as mutações dos genes BRAF e KRAS quase nunca ocorrem em simultâneo no mesmo paciente; as mutações BRAF ocorrem com maior frequência nos casos de SPH do que nos casos esporádicos; nos pólipos dos pacientes com SPH, as mutações dos genes BRAF ou KRAS (quase nunca ambas) estão geralmente presentes em frequência mais elevada do que nos casos esporádicos.
Foram descritas duas formas de SPH: uma é formada por pólipos hiperplásicos típicos, de pe-quenas dimensões, múltiplos e com baixo risco de CCR; a segunda forma é caracterizada por múltiplos P/ASS de grandes dimensões e/ou P/AST, pólipos mistos e adenomas convencionais, com um risco elevado de CCR.29,40 As alterações genéticas moleculares podem definir estas duas formas e possivelmente outras variantes.5
Actualmente não existe um protocolo de vigilância endoscópica universalmente aceite para os doentes com SPH.20 contudo, são apresentadas as opiniões de autores que se dedicaram ao estudo desta síndrome.
East et al.44 recomendam intervalos de vigilância que variam de 1 a 3 anos com o objectivo de remover todos os pólipos com mais de 5 mm. Na impossibilidade de o fazer, devido ao tamanho ou número de pólipos ou porque o doente não deseja ser submetido regularmente a colonoscopia, deve ser considerada a colectomia com anastomose íleorectal. Caso o doente recuse a cirurgia ou tenha outras co-morbilidades que contra-indiquem o procedimento, todos os pólipos com mais de 5 mm devem ser removidos por endoscopia, informando o doente de que existe o risco de vir a desenvolver um CCR, que pode não ser detectado precocemente. Deve ser proposta colonoscopia aos familiares de 1º grau, a realizar 10 anos antes da idade em que foi feito o diagnóstico no caso índex.
A OMS5 recomenda a vigilância endoscópica anual no caso de lesões com menos de 3-4 mm e a remoção de pólipos de maiores dimensões. Preconiza também a realização de colectomia com anastomose íleo-rectal, com vigilância posterior para identificação de lesões serreadas no recto. Para os familiares de 1º grau,emparticularaquelesquetêmmaisde40anos, é recomendada a realização de colonoscopia. É de salientar o estudo realizado no IPO Francisco Gentil em 200441 onde foram caracterizados do ponto de vista clínico-patológico 14 doentes com SPH e os familiares de 1º grau. Apesar da pequena dimensão da amostra, foi possível identificar lesões hiperplásicas, serreadas e adenomatosas distribuídas pelo cólon nos familiares dos doentes quando submetidos a colonoscopia (lesões observadas em 59% destes casos).
A SPH foi observada nos doentes com doença inflamatória intestinal (DII). Na primeira série de casos que descreveu a doença neste contexto todos os doentes padeciam de pancolite moderada a grave com mais de 10 anos de evolução e tinham mais de 20 pólipos. a possibilidade da ocorrência da via serreada na carcionogénese colo-rectal no contexto de DII é sugerida pelo silenciamento do gene MGMT, por metilação do promotor, e mutação KRAS resultando eventualmentenaprogressãoparaadenocarcinoma.45 As mutações KRAS também são encontradas na mucosa inflamatória sem displasia. Por sua vez, Bossard et al.46 Estudaram retrospectivamente lesões neoplásicas de 36 doentes com DII e conclui que a mutação activante V600E BRAF tem sensibilidade elevada como biomarcador da via serreada na DII.
Manejo dos doentes
A existência de duas ou mais vias independentes de carcinogénese colo-rectal tem implicações na prevenção desta neoplasia.32 Uma parte dos CCR localizados no cólon proximal podem desenvolver-se rapidamente e/ ou surgir a partir de lesões planas e difíceis de reconhecer, mesmo quando é realizada colonoscopiatotal.32
No momento actual, não existem recomendações para o rastreio específico de adenocarcinomas serreados.3,8,15 a principal limitação reside no facto de existirem poucos estudos prospectivos de grande dimensão que caracterizem a história natural das lesões precursoras da via serreada.19 Assim, o seguimento destas lesões é feito de acordo com as recomendações utilizadas para o seguimento dos adenomas convencionais.6 Não obstante, alguns autores sugerem protocolos de vigilância específicos para estas lesões como descrito de seguida.
Bauer et al.13 sugerem que os P/ASS localizados no cólon direito sem evidência de displasia devem ser removidos por endoscopia. A vigilância apertada (2 a 6 meses) deve ser considerada para verificar a remoção completa ou a progressão para displasia.13 uma vez feita a remoção completa, a vigilância deve ser individualizada com base na opinião do endoscopista e nos factores de risco do doente, como o tamanho das lesões, o número de pólipos, a história pessoal ou familiar de CCR.13 Oka et al.25 Concluíram, através da análise de 327 P/ASS, que as lesões com diâmetro maior que 10 mm, em particular aquelas com aspecto endoscópico plano, devem ser removidas. Cerca de 25% destas lesões apresentam displasia de alto grau no momento do diagnóstico.
As recomendações actuais para a vigilância após a detecção de P/ASS de pequenas dimensões são semelhantes às aplicadas aos adenomas de pequenas dimensões (5 anos).14 A vigilância de P/ASS de grandes dimensões ou múltiplos (mais de 3) é idêntica à aplicada aos adenomas de grandes dimensões (3 anos).14 É essencial a vigilância dos doentes após a remoção dos P/ASS ou lesões serreadas com displasia.5
Os factores de risco sugeridos que justificam a necessidade de repetir a endoscopia incluem: o tamanho das lesões (lesões com mais de 10 mm), localização das lesões (lado direito do cólon) e idade (doentes idosos estão em maior risco de desenvolvimento de pólipos/ adenomas serreados sésseis).2 As características sugestivas de SPH devem orientar a prevenção nesse sentido, como descrito anteriormente.
A OMS5 recomenda que os intervalos de vigilância sejam definidos com base no número e tamanho dos pólipos – endoscopias com intervalos de 5 anos para uma ou duas lesões serreadas de pequenas dimensões ( < 10 mm), ou intervalos de 3 anos para lesões com mais de 10 mm ou em número superior a 3 de qualquer dimensão. A OMS recomenda também, ainda que esta abordagem não esteja testada, que os P/ASS com displasia devem ser encarados como lesões com elevada probabilidade de terem instabilidade de microssatélites e que, por isso, devem avaliados um anos após a sua excisão completa e com intervalos de 3 anos daí em diante.
Tem sido postulado que os P/ASS têm um comportamento mais agressivo que os adenomas convencionais, com o argumento de que a alteração nos genes de reparação do DNA pode ser responsável por uma progressãoneoplásicaacelerada.3,8,16 Foi recentemente reportado um caso de um doente de 65 anos com um pólipo hiperplásico de 15 mm, séssil, localizado no cólon ascendente, revelado numa colonoscopia de rotina, no qual passados 8 meses, a mesma lesão apresentava características endoscópicas suspeitas, cujo exame histológico revelou um adenocarcinoma com extensão até à submucosa, sem invasão vascular ou linfática. Curiosamente, na periferia do carcinoma identificava-se uma lesão com características de P/ ASS, com uma área de transição de adenomatubular sugerindo evolução do P/ASS para carcinoma.47
A maioria dos estudos sugere que o tempo de progressão para carcinoma é menor para as lesões serreadas do cólon em relação aos adenomas convencionais.2 Pelo contrário, Ensari et al.17 Concluem que a observação transversal da ocorrência dos vários pólipos através das diferentes faixas etárias sugere que o tempo de progressão dos P/ASS para CCR é maior do que o observado para a sequência adenoma-carcinoma. Do mesmo modo, OBrienet al.19 Estimam que são necessários pelo menos 22,8 anos para sedes envolver um CCR pela via serreada, em comparação com os 10 anos que são geralmente aceites como tempo de malignização de um adenoma convencional.
A uniformização dos critérios diagnósticos das lesões serreadas do cólon, a estandardização da nomenclatura, o treino dos patologistas e o possível desenvolvimento de técnicas diagnósticas com maior acuidade são de extrema importância para o seguimento dos doentes.7,24,32 Com a utilização de novas técnicas diagnósticas de alta definição, como a cromoendoscopia ou a vídeo endoscopia de ampliação, foi demonstrado que a superfície das lesões serreadas têm abertura das criptas mais largas que a mucosa normal, permitindo assim a detecção de lesões de menores dimensões, particularmente P/ASS planos que predominam no cólon proximal e apresentam com maior frequência displasia de alto grau e carcinoma in situ. 20,24,25
Agradecimentos
O autor agradece a disponibilidade e as críticas oportunas da Professora Fátima Carneiro na elaboração deste texto, assim como o contributo da Dra. Helena Baldaia na selecção das fotografias.
Referências
1. Karsa LV , Lignini TA , Patnick J, Lambert R, Sauvaget C. The dimensions of the CRC problem. Best Pract Res Clin Gastroenterol 2010;24:381-96. [ Links ]
2. Snover DC. Update on the serrated pathway to colorectal carcinoma. Hum Pathol 2010. [ Links ]
3. Orlowska J. Serrated polyps of the colorectum: histological classification and clinical significance. Pol J Pathol 2010;61:8-22. [ Links ]
4. Markowitz SD, Bertagnolli MM. Molecular origins of cancer: Molecular basis of colorectal cancer. N Engl J Med 2009;361:2449-60. [ Links ]
5. Bosman FT, Carneiro F, Hruban RH and Theise ND. WHO Classification of Tumours of the Digestive System, Fouth Edition. In. fourth ed. Lyon: IARC Press; 2010. [ Links ]
6. Winawer SJ, Zauber AG, Fletcher RH , et al. Guidelines for colonoscopy surveillance after polypectomy: a consensus update by the US Multi-Society Task Force on Colorectal Cancer and the American Cancer Society. Gastroenterology 2006;130:1872-85. [ Links ]
7. Jass JR, Whitehall VL , Young J, Leggett BA. Emerging concepts in colorectal neoplasia. Gastroenterology 2002;123:862-76. [ Links ]
8. Noffsinger AE . Serrated polyps and colorectal cancer: new pathway to malignancy. Annu Rev Pathol 2009;4:343-64. [ Links ]
9. Bellizzi AM, Frankel WL. Colorectal cancer due to deficiency in DNA mismatch repair function: a review. Adv Anat Pathol 2009;16:405-17. [ Links ]
10. Lynch HT , Boland CR , Gong G, et al. Phenotypic and genotypic heterogeneity in the Lynch syndrome: diagnostic, surveillance and management implications. Eur J Hum Genet 2006;14:390-402. [ Links ]
11. Torlakovic E, Snover DC. Serrated adenomatous polyposis in humans. Gastroenterology 1996;110:748-55. [ Links ]
12. Freeman HJ. Heterogeneity of colorectal adenomas, the serrated adenoma, and implications for screening and surveillance. World J Gastroenterol 2008;14:3461-3. [ Links ]
13. Bauer VP, Papaconstantinou HT . Management of serrated adenomas and hyperplastic polyps. Clin Colon Rectal Surg 2008;21:273-9. [ Links ]
14. Gurudu SR, Heigh RI , De Petris G, et al. Sessile serrated adenomas: demographic, endoscopic and pathological characteristics. World J Gastroenterol 2010;16:3402-5. [ Links ]
15. Aust DE, Baretton GB. Serrated polyps of the colon and rectum (hyperplastic polyps, sessile serrated adenomas, traditional serrated adenomas, and mixed polyps)-proposal for diagnostic criteria. Virchows Arch 2010;457:291-7. [ Links ]
16. Liang JJ, Alrawi S, Tan D. Nomenclature, molecular genetics and clinical significance of the precursor lesions in the serrated polyp pathway of colorectal carcinoma. Int J Clin Exp Pathol 2008;1:317-24. [ Links ]
17. Ensari A, Bosman FT, Offerhaus GJ. The serrated polyp: getting it right! J Clin Pathol 2010;63:665-8. [ Links ]
18. Li SC, Burgart L. Histopathology of serrated adenoma, its variants, and differentiation from conventional adenomatous and hyperplastic polyps. Arch Pathol Lab Med 2007;131:440-5. [ Links ]
19. OBrien MJ, Yang S, Mack C, et al. Comparison of microsatellite instability, CpG island methylation phenotype, BRA F and KRA S status in serrated polyps and traditional adenomas indicates separate pathways to distinct colorectal carcinoma end points. Am J Surg Pathol 2006;30:1491-501. [ Links ]
20. Leggett B, Whitehall V. Role of the serrated pathway in colorectal cancer pathogenesis. Gastroenterology 2010;138:2088-100. [ Links ]
21. Makinen MJ. Colorectal serrated adenocarcinoma. Histopathology 2007;50:131-50. [ Links ]
22. Spring KJ, Zhao ZZ, Karamatic R, et al. High prevalence of sessile serrated adenomas with BRA F mutations: a prospective study of patients undergoing colonoscopy. Gastroenterology 2006;131:1400-7. [ Links ]
23. OBrien MJ, Yang S, Huang CS, Shepherd C, Cerda S, Farraye FA. The serrated polyp pathway to colorectal carcinoma. Diagnostic Histopathology 2008;14:78-93. [ Links ]
24. Glatz K, Pritt B, Glatz D, Hartmann A, OBrien MJ, Blaszyk H. A multinational, internet-based assessment of observer variability in the diagnosis of serrated colorectal polyps. Am J Clin Pathol 2007;127:938-45. [ Links ]
25. Oka S, Tanaka S, Hiyama T, et al. Clinicopathologic and endoscopic features of colorectal serrated adenoma: differences between polypoid and superficial types. Gastrointest Endosc 2004;59:213-9. [ Links ]
26. Mochizuka A, Uehara T, Nakamura T, Kobayashi Y, Ota H. Hyperplastic polyps and sessile serrated adenomas of the colon and rectum display gastric pyloric differentiation. Histochem Cell Biol 2007;128:445-55. [ Links ]
27. Berman JJ, Albores-Saavedra J, Bostwick D, et al. Precancer: a conceptual working definition -- results of a Consensus Conference. Cancer Detect Prev 2006;30:387-94. [ Links ]
28. Goldstein NS. Serrated pathway and APC (conventional)-type colorectal polyps: molecular-morphologic correlations, genetic pathways, and implications for classification. Am J Clin Pathol 2006;125:146-53. [ Links ]
29. Young J, Jenkins M, Parry S, et al. Serrated pathway colorectal cancer in the population: genetic consideration. Gut 2007;56:1453-9. [ Links ]
30. Carr NJ, Mahajan H, Tan KL, Hawkins NJ, Ward RL . Serrated and non-serrated polyps of the colorectum: Their prevalence in an unselected case series and correlation of BRA F mutation analysis with the diagnosis of sessile serrated adenoma. Journal of Clinical Pathology 2009;62:516-8. [ Links ]
31. Minoo P, Moyer MP, Jass JR. Role of BRA F-V600E in the serrated pathway of colorectal tumourigenesis. J Pathol 2007;212:124-33. [ Links ]
32. Jass JR. Molecular heterogeneity of colorectal cancer: Implications for cancer control. Surg Oncol 2007;16 Suppl 1:S7-9. [ Links ]
33. Beach R, Chan AOO, Wu TT , et al. BRA F mutations in aberrant crypt foci and hyperplastic polyposis. American Journal of Pathology 2005;166:1069-75. [ Links ]
34. Sawyer EJ, Cerar A, Hanby AM, et al. Molecular characteristics of serrated adenomas of the colorectum. Gut 2002;51:200-6. [ Links ]
35. Chirieac LR , Shen L, Catalano PJ, Issa JP, Hamilton SR. Phenotype of microsatellite-stable colorectal carcinomas with CpG island methylation. Am J Surg Pathol 2005;29:429-36. [ Links ]
36. Harada K, Hiraoka S, Kato J, et al. Genetic and epigenetic alterations of Ras signalling pathway in colorectal neoplasia: analysis based on tumour clinicopathological features. Br J Cancer 2007;97:1425-31. [ Links ]
37. Fu X, Li J, Li K, Tian X, Zhang Y. Hypermethylation of APC promoter 1A is associated with moderate activation of Wnt signalling pathway in a subset of colorectal serrated adenomas. Histopathology 2009;55:554-63. [ Links ]
38. Jass JR, Baker K, Zlobec I, et al. Advanced colorectal polyps with the molecular and morphological features of serrated polyps and adenomas: concept of a fusion pathway to colorectal cancer. Histopathology 2006;49:121-31. [ Links ]
39. Fu X, Li J, Li K, Tian X, Zhang Y. Hypermethylation of APC promoter 1A is associated with moderate activation of Wnt signalling pathway in a subset of colorectal serrated adenomas. Histopathology 2009;55:554-63. [ Links ]
40. Jass JR. Colorectal polyposes: from phenotype to diagnosis. Pathol Res Pract 2008;204:431-47. [ Links ]
41. Lage P, Cravo M, Sousa R, et al. Management of Portuguese patients with hyperplastic polyposis and screening of at-risk first-degree relatives: a contribution for future guidelines based on a clinical study. Am J Gastroenterol 2004;99:1779-84. [ Links ]
42. Carvajal-Carmona LG, Howarth KM, Lockett M, et al. Molecular classification and genetic pathways in hyperplastic polyposis syndrome. J Pathol 2007;212:378-85. [ Links ]
43. Boparai KS, Mathus-Vliegen EM, Koornstra JJ, et al. Increased colorectal cancer risk during follow-up in patients with hyperplastic polyposis syndrome: a multicentre cohort study. Gut 2010;59:1094-100. [ Links ]
44. East JE, Saunders BP, Jass JR. Sporadic and syndromic hyperplastic polyps and serrated adenomas of the colon: classification, molecular genetics, natural history, and clinical management. Gastroenterol Clin North Am 2008;37:25-46, v. [ Links ]
45. Srivastava A, Redston M, Farraye FA, Yantiss RK, Odze RD. Hyperplastic/serrated polyposis in inflammatory bowel disease: a case series of a previously undescribed entity. Am J Surg Pathol 2008;32:296-303. [ Links ]
46. Bossard C, Denis MG, Bezieau S, et al. Involvement of the serrated neoplasia pathway in inflammatory bowel disease-related colorectal oncogenesis. Oncol Rep 2007;18:1093-7. [ Links ]
47. Oono Y, Fu K, Nakamura H, et al. Progression of a sessile serrated adenoma to an early invasive cancer within 8 months. Dig Dis Sci 2009;54:906-9. [ Links ]
Agostinho Xavier Azevedo
Faculdade de Medicina da Universidade do Porto. Al. Prof. Hernâni Monteiro 4200-319 Porto. Email: sxazevedo@gmail.com














